Stem_Cells.pptx
- Количество слайдов: 37
 СТВОЛОВЫЕ КЛЕТКИ
СТВОЛОВЫЕ КЛЕТКИ
 История изучения стволовых клеток 1868 - Эрнст Геккель вводит понятие “стволовая клетка” (СК) 1876 – Оскар Гертвиг открыл оплодотворение у животных 1878 – Первая попытка оплодотворения яйцеклетки in vitro 1886 – Уильям Сэдвик использует термин СК для растений 1909 – Унитарная теория кроветворения А. А. Максимова 1953 – Лерой Стевенс начал исследования тератом у мышей 1957 – Е. Д. Томас провел первую трансплантацию костного мозга 1959 – Первое применение искусственного оплодотворения у КРС 1963 – Д. Тил и Э. Мак. Калох доказывают существование СК крови 1968 – Первое оплодотворение яйцеклетки человека in vitro 1978 – В Англии родился первый ребенок, зачатый in vitro 1989 - М. Капеччи, М. Эванс, О. Смититс получают нокаутных мышей 1998 – Эмбриональные СК человека научились культивировать 2005 – С. Яманака и К. Такахаши получили СК из обычных клеток
История изучения стволовых клеток 1868 - Эрнст Геккель вводит понятие “стволовая клетка” (СК) 1876 – Оскар Гертвиг открыл оплодотворение у животных 1878 – Первая попытка оплодотворения яйцеклетки in vitro 1886 – Уильям Сэдвик использует термин СК для растений 1909 – Унитарная теория кроветворения А. А. Максимова 1953 – Лерой Стевенс начал исследования тератом у мышей 1957 – Е. Д. Томас провел первую трансплантацию костного мозга 1959 – Первое применение искусственного оплодотворения у КРС 1963 – Д. Тил и Э. Мак. Калох доказывают существование СК крови 1968 – Первое оплодотворение яйцеклетки человека in vitro 1978 – В Англии родился первый ребенок, зачатый in vitro 1989 - М. Капеччи, М. Эванс, О. Смититс получают нокаутных мышей 1998 – Эмбриональные СК человека научились культивировать 2005 – С. Яманака и К. Такахаши получили СК из обычных клеток
 Стволовая клетка – это • клетка, обладающая способностью постоянно делиться и давать потомство, которое созревает в зрелые функционирующие клетки различных органов и тканей
Стволовая клетка – это • клетка, обладающая способностью постоянно делиться и давать потомство, которое созревает в зрелые функционирующие клетки различных органов и тканей
 Свойства стволовых клеток Ø Отсутствие специализации Ø Способность к самообновлению Ø Способность порождать специализированные типы клеток
Свойства стволовых клеток Ø Отсутствие специализации Ø Способность к самообновлению Ø Способность порождать специализированные типы клеток
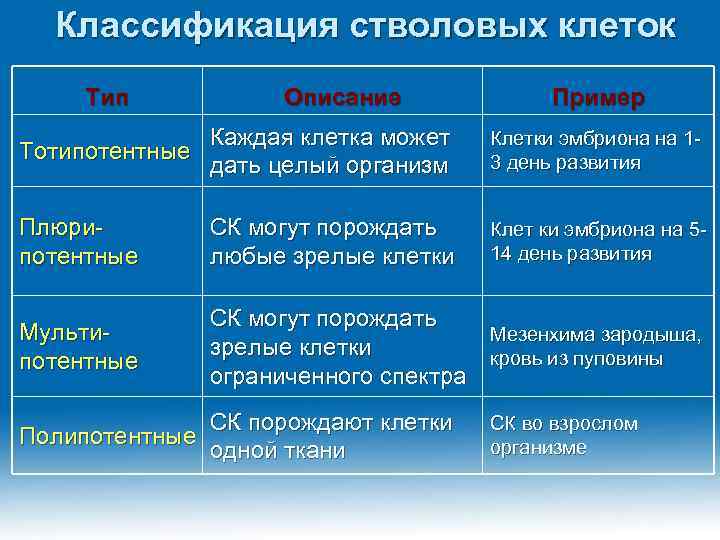 Классификация стволовых клеток Тип Описание Пример Тотипотентные Каждая клетка может дать целый организм Клетки эмбриона на 13 день развития Плюрипотентные СК могут порождать любые зрелые клетки Клет ки эмбриона на 514 день развития Мультипотентные СК могут порождать Мезенхима зародыша, зрелые клетки кровь из пуповины ограниченного спектра Полипотентные СК порождают клетки одной ткани СК во взрослом организме
Классификация стволовых клеток Тип Описание Пример Тотипотентные Каждая клетка может дать целый организм Клетки эмбриона на 13 день развития Плюрипотентные СК могут порождать любые зрелые клетки Клет ки эмбриона на 514 день развития Мультипотентные СК могут порождать Мезенхима зародыша, зрелые клетки кровь из пуповины ограниченного спектра Полипотентные СК порождают клетки одной ткани СК во взрослом организме
 Разновидности СК Эмбриональные стволовые клетки извлекают из 5 -6 дневного эмбриона. Они обладают способностью формировать любые типы клеток организма человека. Эмбриональные зародышевые клетки происходят из той части зародыша, которая формирует во взрослом организме гаметы. Стволовые клетки взрослого организма сохраняются во взрослом организме, порождая ограниченное количество дифференцированных клеточных типов в течении его жизни
Разновидности СК Эмбриональные стволовые клетки извлекают из 5 -6 дневного эмбриона. Они обладают способностью формировать любые типы клеток организма человека. Эмбриональные зародышевые клетки происходят из той части зародыша, которая формирует во взрослом организме гаметы. Стволовые клетки взрослого организма сохраняются во взрослом организме, порождая ограниченное количество дифференцированных клеточных типов в течении его жизни
 ESC vs ASC • Мульти- или плюрипотентные: l дифференцируются в любые типы клеток • Полипотентные: l дифференцируются в ограниченный ряд клеточных типов • Источники разные Источник один • Трудно выделять, • Можно получать из количество ограничено эмбрионов в большом количестве • Не подвергаются иммунному • В принципе могут отторжению, если отторгаться, хотя это аутологичны еще не наблюдалось •
ESC vs ASC • Мульти- или плюрипотентные: l дифференцируются в любые типы клеток • Полипотентные: l дифференцируются в ограниченный ряд клеточных типов • Источники разные Источник один • Трудно выделять, • Можно получать из количество ограничено эмбрионов в большом количестве • Не подвергаются иммунному • В принципе могут отторжению, если отторгаться, хотя это аутологичны еще не наблюдалось •
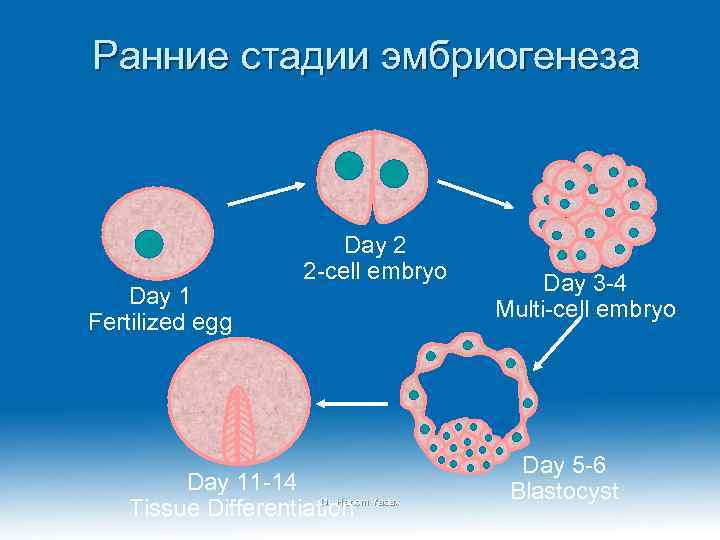 Ранние стадии эмбриогенеза Day 1 Fertilized egg Day 2 2 -cell embryo Day 11 -14 Dr. Hariom Tissue Differentiation Yadav Day 3 -4 Multi-cell embryo Day 5 -6 Blastocyst
Ранние стадии эмбриогенеза Day 1 Fertilized egg Day 2 2 -cell embryo Day 11 -14 Dr. Hariom Tissue Differentiation Yadav Day 3 -4 Multi-cell embryo Day 5 -6 Blastocyst
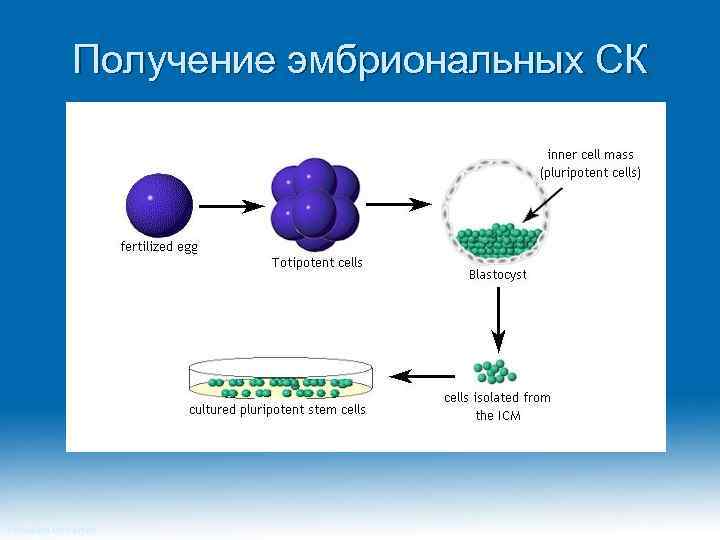 Получение эмбриональных СК Princeton University
Получение эмбриональных СК Princeton University
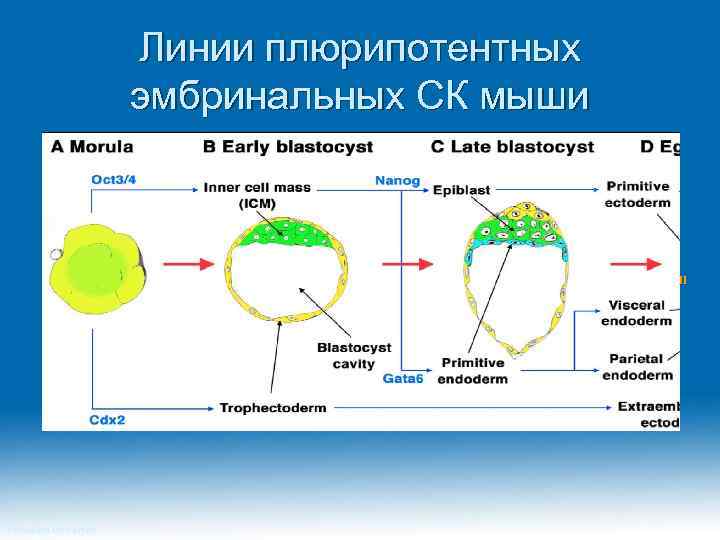 Линии плюрипотентных эмбринальных СК мыши ll Princeton University
Линии плюрипотентных эмбринальных СК мыши ll Princeton University
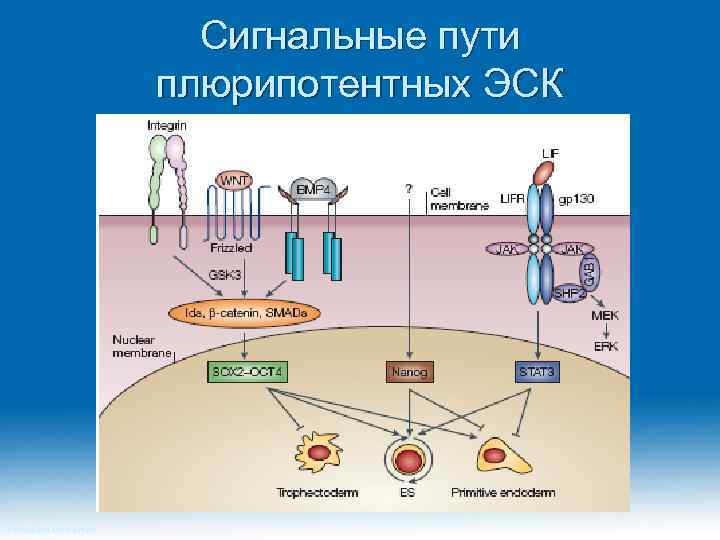 Сигнальные пути плюрипотентных ЭСК Princeton University
Сигнальные пути плюрипотентных ЭСК Princeton University
 Транскрипционный фактор SOX 2 Ø Относится к HMG-белкам семейства DNA-BP Ø Предотвращает дифференцировку ЭСК Ø Является хабом для многих генов, активных у ЭСК Ø Функционирует в составе комплекса с Oct 4 или Oct 1 на энхансерной последовательности Fgf 4 Ø При активации маркеров плюрипотентности кооперирует с другими транскрипционными факторами (например, с Nanog). Princeton University
Транскрипционный фактор SOX 2 Ø Относится к HMG-белкам семейства DNA-BP Ø Предотвращает дифференцировку ЭСК Ø Является хабом для многих генов, активных у ЭСК Ø Функционирует в составе комплекса с Oct 4 или Oct 1 на энхансерной последовательности Fgf 4 Ø При активации маркеров плюрипотентности кооперирует с другими транскрипционными факторами (например, с Nanog). Princeton University
 Транскрипционный фактор OCT 3/4 Поддерживает плюрипотентность ЭСК всех линий Тесно связан с рядом целевых генов, вовлеченных в поддержание стволовости Регуляторные элементы целевых генов расположены рядом с точками связыванияf Sox 2 Рассматривается как ключевой фактор системы самоподдержания стволовости клеток Princeton University
Транскрипционный фактор OCT 3/4 Поддерживает плюрипотентность ЭСК всех линий Тесно связан с рядом целевых генов, вовлеченных в поддержание стволовости Регуляторные элементы целевых генов расположены рядом с точками связыванияf Sox 2 Рассматривается как ключевой фактор системы самоподдержания стволовости клеток Princeton University
 Транскрипционный фактор Nanog Ø Содержит домен гомеобокса Ø Подавляет сигналлинг LIF и BMP Ø Повышенный уровень предотвращает включение LIF и фидерного слоя Ø Функционирует совместно с Oct 4 , Sox 2 и другими транскрипционными факторами Princeton University
Транскрипционный фактор Nanog Ø Содержит домен гомеобокса Ø Подавляет сигналлинг LIF и BMP Ø Повышенный уровень предотвращает включение LIF и фидерного слоя Ø Функционирует совместно с Oct 4 , Sox 2 и другими транскрипционными факторами Princeton University
 Транскрипционный фактор LIF Ø Относится к семейству цитокинов Ø Необходим для поддержания плюрипотенотности in vitro в присутствии сыворотки Ø Связывается на плазмалемме с гетеродимерным рецептором, состоящим из LIFR и gp 130 Ø При его связывании активируется сигнальный путь Jak/Stat Ø Активированный Stat 3 поддерживает плюрипотентность Princeton University
Транскрипционный фактор LIF Ø Относится к семейству цитокинов Ø Необходим для поддержания плюрипотенотности in vitro в присутствии сыворотки Ø Связывается на плазмалемме с гетеродимерным рецептором, состоящим из LIFR и gp 130 Ø При его связывании активируется сигнальный путь Jak/Stat Ø Активированный Stat 3 поддерживает плюрипотентность Princeton University
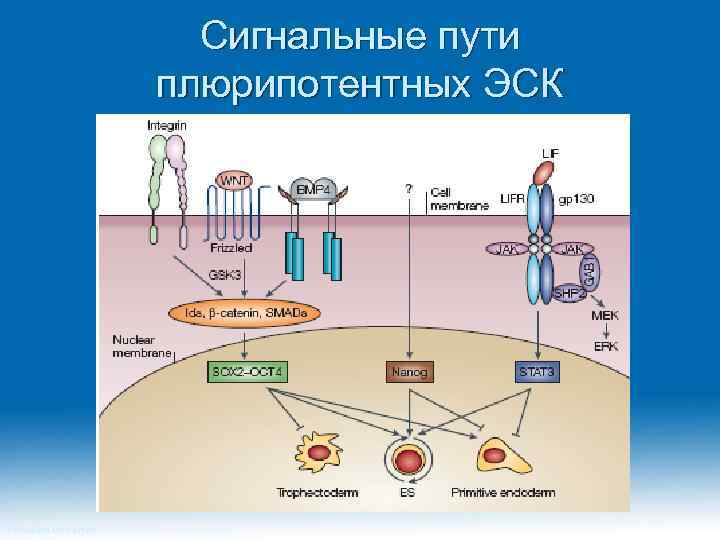 Сигнальные пути плюрипотентных ЭСК Princeton University
Сигнальные пути плюрипотентных ЭСК Princeton University
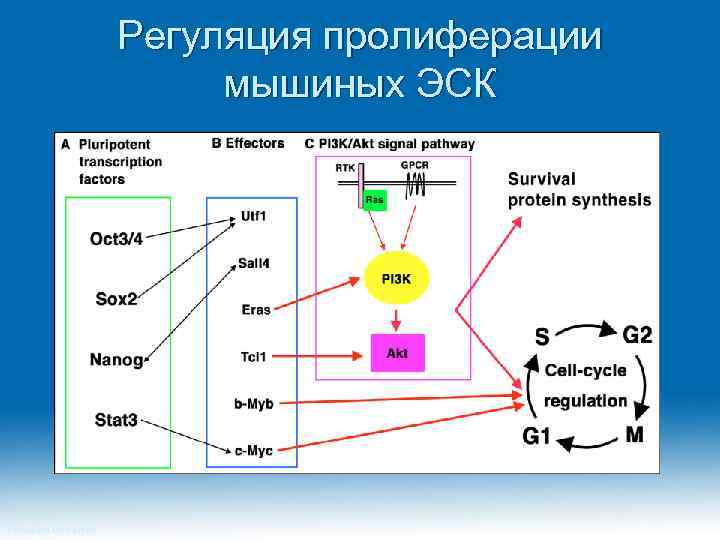 Регуляция пролиферации мышиных ЭСК Princeton University
Регуляция пролиферации мышиных ЭСК Princeton University
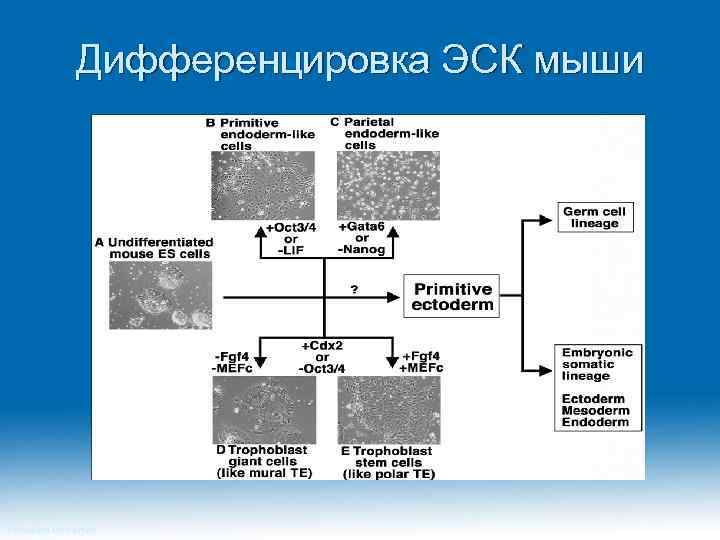 Дифференцировка ЭСК мыши Princeton University
Дифференцировка ЭСК мыши Princeton University
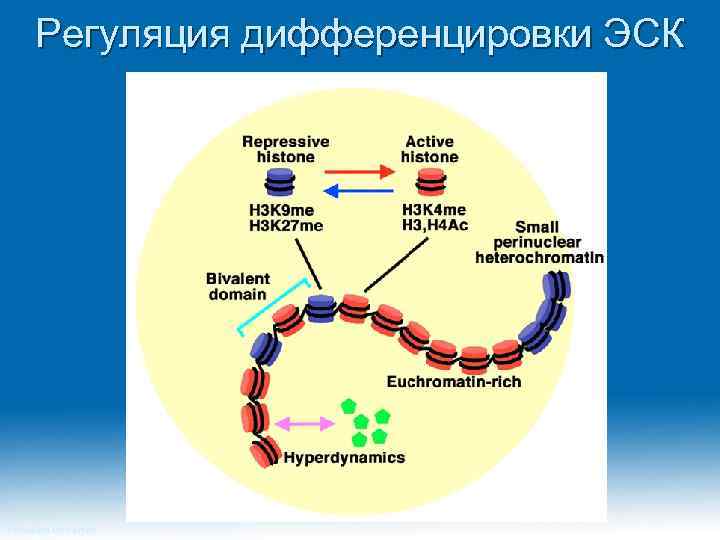 Регуляция дифференцировки ЭСК Princeton University
Регуляция дифференцировки ЭСК Princeton University
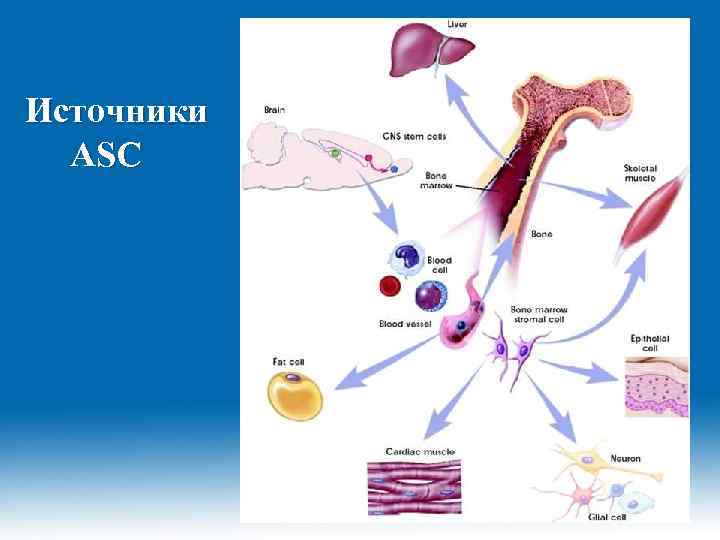 Источники ASC
Источники ASC
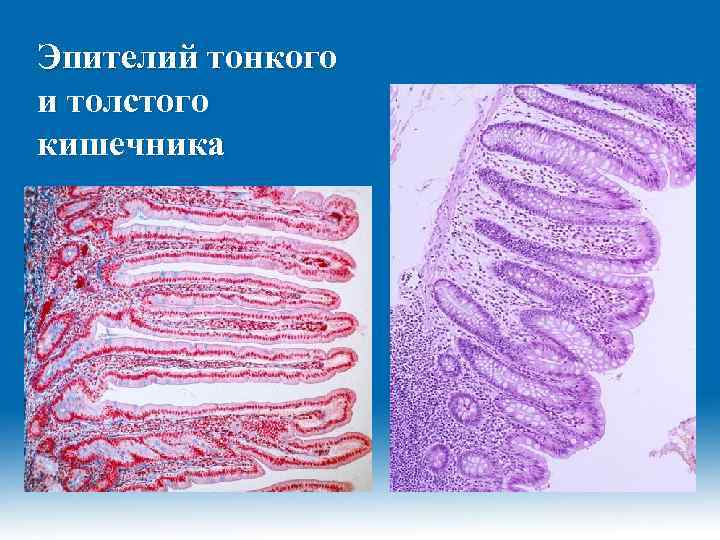 Эпителий тонкого и толстого кишечника
Эпителий тонкого и толстого кишечника
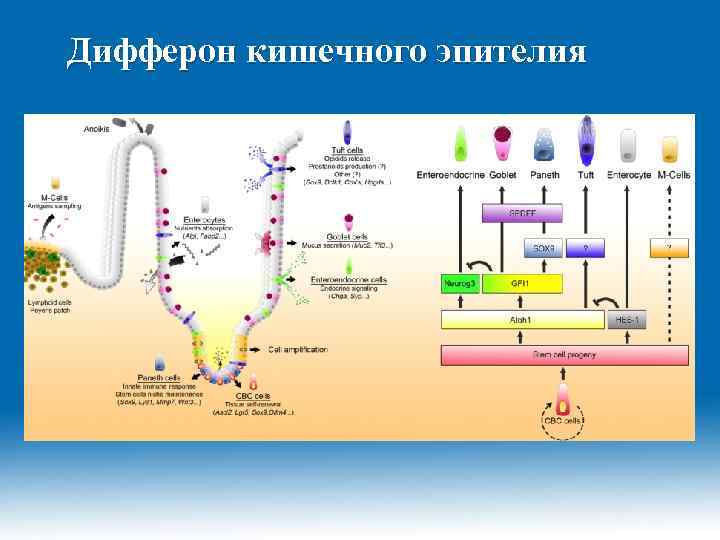 Дифферон кишечного эпителия
Дифферон кишечного эпителия
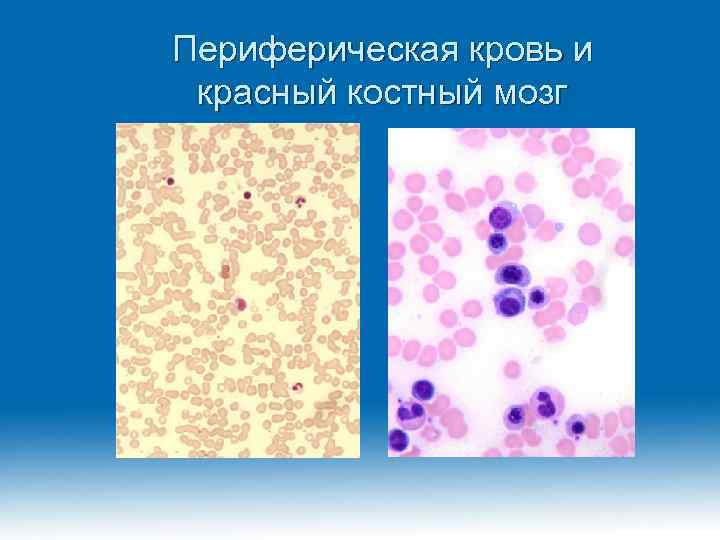 Периферическая кровь и красный костный мозг
Периферическая кровь и красный костный мозг
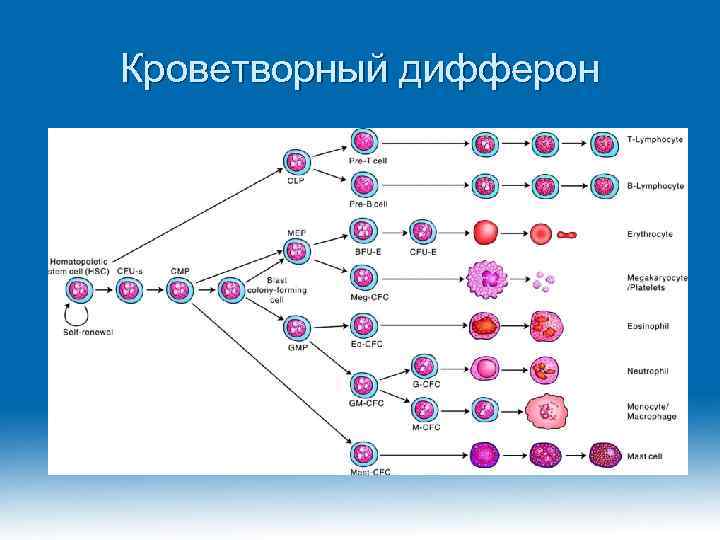 Кроветворный дифферон
Кроветворный дифферон
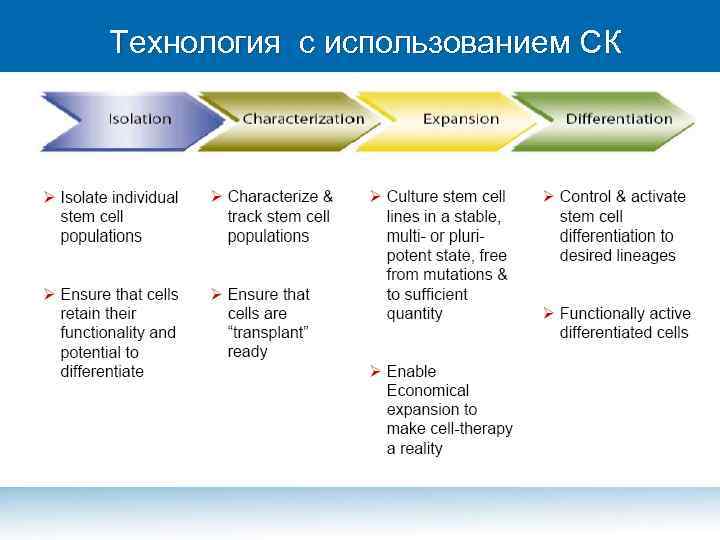 Технология с использованием СК
Технология с использованием СК
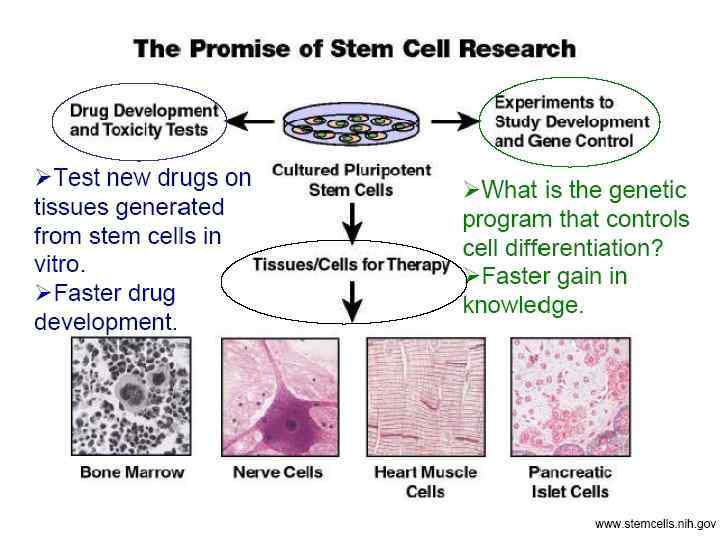 2/9/2018 Dr. Hariom Yadav
2/9/2018 Dr. Hariom Yadav
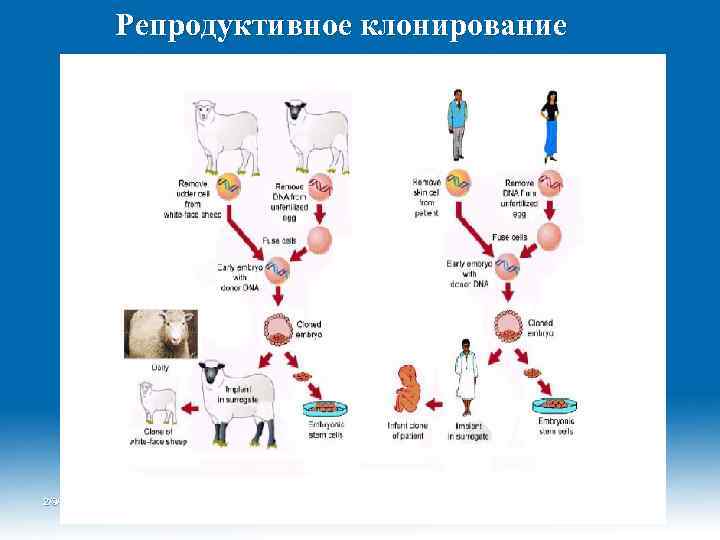 Репродуктивное клонирование 2/9/2018 Dr. Hariom Yadav
Репродуктивное клонирование 2/9/2018 Dr. Hariom Yadav
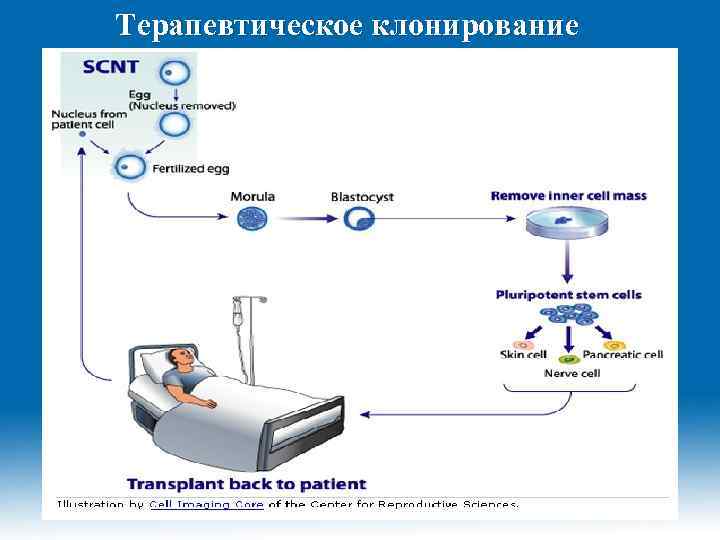 Терапевтическое клонирование 2/9/2018 Dr. Hariom Yadav
Терапевтическое клонирование 2/9/2018 Dr. Hariom Yadav
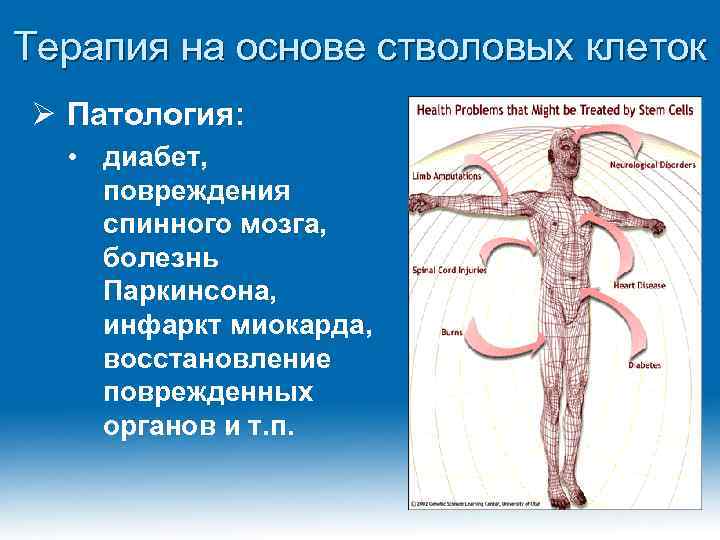 Терапия на основе стволовых клеток Ø Патология: • диабет, повреждения спинного мозга, болезнь Паркинсона, инфаркт миокарда, восстановление поврежденных органов и т. п.
Терапия на основе стволовых клеток Ø Патология: • диабет, повреждения спинного мозга, болезнь Паркинсона, инфаркт миокарда, восстановление поврежденных органов и т. п.
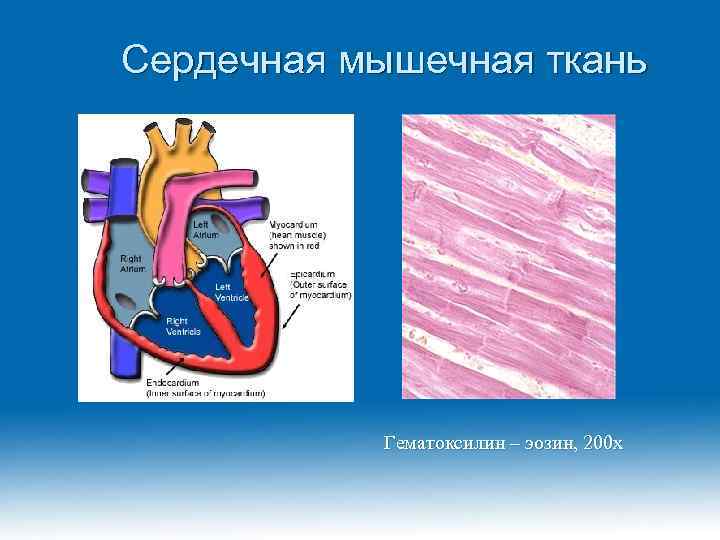 Сердечная мышечная ткань Гематоксилин – эозин, 200 х
Сердечная мышечная ткань Гематоксилин – эозин, 200 х
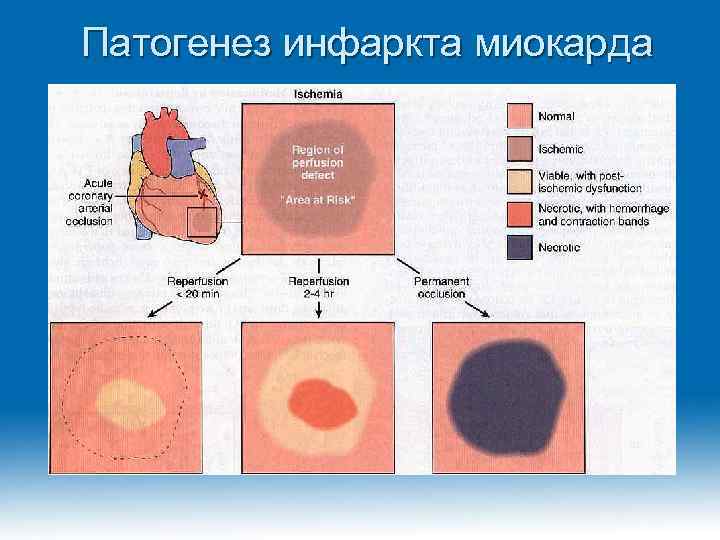 Патогенез инфаркта миокарда
Патогенез инфаркта миокарда
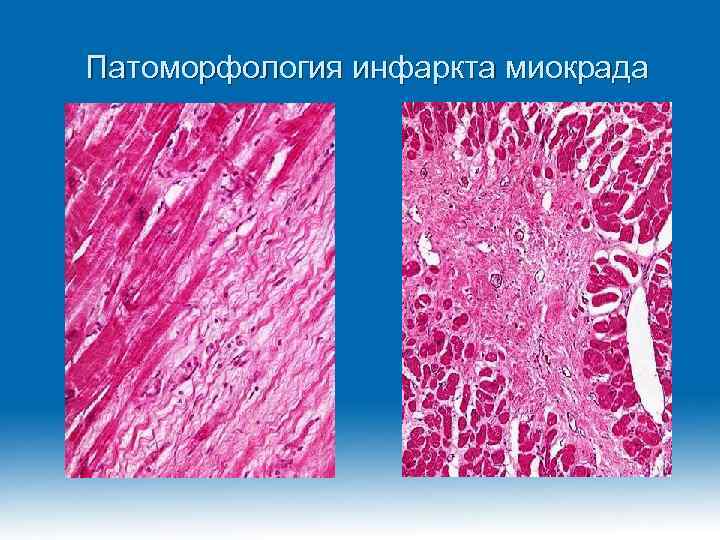 Патоморфология инфаркта миокрада
Патоморфология инфаркта миокрада
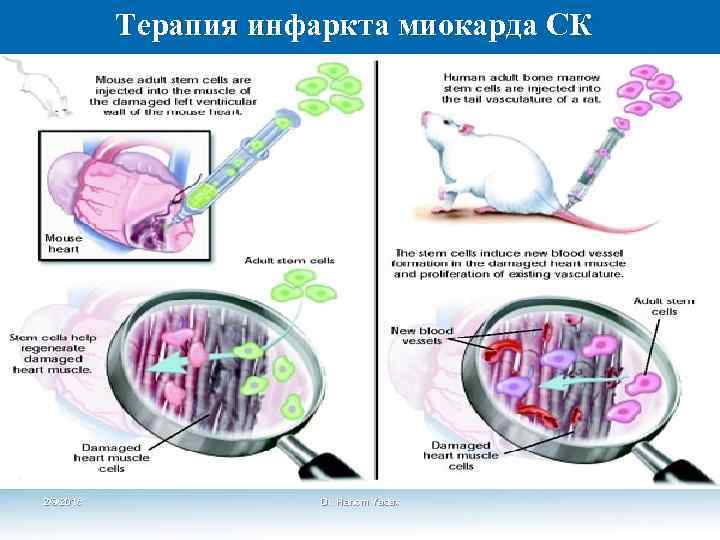 Терапия инфаркта миокарда СК 2/9/2018 Dr. Hariom Yadav
Терапия инфаркта миокарда СК 2/9/2018 Dr. Hariom Yadav
 Проблемы технологии СК СК надо индуцировать к развитию их потомства в определенный тип зрелых клеток перед использованием в клинике. • Найдены аномалии числа и структуры хромосом в некоторых линиях ЭСК. •
Проблемы технологии СК СК надо индуцировать к развитию их потомства в определенный тип зрелых клеток перед использованием в клинике. • Найдены аномалии числа и структуры хромосом в некоторых линиях ЭСК. •
 Проблемы технологии СК В организме пациента необходимо контролировать дифференцировку и пролиферацию СК. • Вероятность отторжения полученных из СК тканевых трансплантов достаточно высока. •
Проблемы технологии СК В организме пациента необходимо контролировать дифференцировку и пролиферацию СК. • Вероятность отторжения полученных из СК тканевых трансплантов достаточно высока. •
 Проблемы технологии СК Существует опасность загрязнения СК вирусами, бакктериями, грибками и микоплазмами. • Использование фидерных клеток мыши как подложки для роста ЭСК потенциально создает проблему ксенотрансплантации. •
Проблемы технологии СК Существует опасность загрязнения СК вирусами, бакктериями, грибками и микоплазмами. • Использование фидерных клеток мыши как подложки для роста ЭСК потенциально создает проблему ксенотрансплантации. •
 Состояние технологии СК • Великобритания l l l • Франция l l l • Либеральная политика в отношении исследований Разрешено терапевтическое клонирование, а также опыты на эмбрионах Разрешена разработка технологий СК Менее либеральная политика Разрешено использовать остаток эмбрионов от ЭКО Репродуктивное и терапевтическое клонирование запрещено Германия l l l Очень большие ограничения Запрещено использовать отходы от ЭКО Эмбрионы для исследований импортируются
Состояние технологии СК • Великобритания l l l • Франция l l l • Либеральная политика в отношении исследований Разрешено терапевтическое клонирование, а также опыты на эмбрионах Разрешена разработка технологий СК Менее либеральная политика Разрешено использовать остаток эмбрионов от ЭКО Репродуктивное и терапевтическое клонирование запрещено Германия l l l Очень большие ограничения Запрещено использовать отходы от ЭКО Эмбрионы для исследований импортируются


