Стволовые клетки октябрь 2014.ppt
- Количество слайдов: 38
 Стволовые клетки и их использование для клеточной терапии Профессор, д. б. н. Е. Ю. Москалева
Стволовые клетки и их использование для клеточной терапии Профессор, д. б. н. Е. Ю. Москалева
 Стволовые клетки (СК) - это клоногенные клетки, способные к самообновлению и дифференцировке в другие типы клеток. СК характеризуются наличием трех главных свойств: 1. СК асимметрично делятся, то есть при делении СК вместо образования 2 -х одинаковых дочерних клеток одна дочерняя клетка становится коммитированной (commit – поручать, вверять), способной стать более специализированной, а другая – остается неспециализированной СК; 2. СК способны к самообновлению, т. е. репопулируют (пролиферируют без дифференцировки) на протяжении неопределенно длительного периода времени или даже в течение всей жизни организма (long-term subset); 3. СК могут дифференцироваться в специализированные типы клеток (по крайней мере, в клетки 2 -х различных фенотипов), проходя стадию прогениторных клеток (progenitor - предшественник) из так называемого краткосрочно существующего пула неспециализированных коммитированных СК (short-term subset).
Стволовые клетки (СК) - это клоногенные клетки, способные к самообновлению и дифференцировке в другие типы клеток. СК характеризуются наличием трех главных свойств: 1. СК асимметрично делятся, то есть при делении СК вместо образования 2 -х одинаковых дочерних клеток одна дочерняя клетка становится коммитированной (commit – поручать, вверять), способной стать более специализированной, а другая – остается неспециализированной СК; 2. СК способны к самообновлению, т. е. репопулируют (пролиферируют без дифференцировки) на протяжении неопределенно длительного периода времени или даже в течение всей жизни организма (long-term subset); 3. СК могут дифференцироваться в специализированные типы клеток (по крайней мере, в клетки 2 -х различных фенотипов), проходя стадию прогениторных клеток (progenitor - предшественник) из так называемого краткосрочно существующего пула неспециализированных коммитированных СК (short-term subset).
 Схема получения эмбриональных стволовых клеток 5 -дневный эмбрион состоит из 200 -250 клеток трофоэктодермы ВКМ содержит 30 -34 клетки. Фидерный слой – митотически инактивированные мышиные фибробласты. Маркеры ЭСК SSEA-3 и SSEA-4 Oct-4 GSTM-2, TRA-1 -60, TRA-1 -81 Теломераза Щелочная фосфатаза Перспективы – биомедицинская инженерия
Схема получения эмбриональных стволовых клеток 5 -дневный эмбрион состоит из 200 -250 клеток трофоэктодермы ВКМ содержит 30 -34 клетки. Фидерный слой – митотически инактивированные мышиные фибробласты. Маркеры ЭСК SSEA-3 и SSEA-4 Oct-4 GSTM-2, TRA-1 -60, TRA-1 -81 Теломераза Щелочная фосфатаза Перспективы – биомедицинская инженерия
 Некоторые маркеры стволовых клеток и их функции Маркер CD 34, CD 133, интегрины Известная или предполагаемая функция Прикрепление клеток к субстрату Bcl-2, теломераза, АВС Выживаемость и повышение устойчивости -транспортеры, клеток альдегидрогеназа c-kit Рецептор фактора СК (SCF) Musashi 1 Ассимметричное деление, обновление СК Нестин Промежуточные эмбриональные филаменты р27 Kip 1 Ингибирование циклин-зависимых киназ р63 Гомолог р53 В СК действуют специфические сигнальные системы, регулирующие их функции Hedgehog (Hh), Wnt, Notch
Некоторые маркеры стволовых клеток и их функции Маркер CD 34, CD 133, интегрины Известная или предполагаемая функция Прикрепление клеток к субстрату Bcl-2, теломераза, АВС Выживаемость и повышение устойчивости -транспортеры, клеток альдегидрогеназа c-kit Рецептор фактора СК (SCF) Musashi 1 Ассимметричное деление, обновление СК Нестин Промежуточные эмбриональные филаменты р27 Kip 1 Ингибирование циклин-зависимых киназ р63 Гомолог р53 В СК действуют специфические сигнальные системы, регулирующие их функции Hedgehog (Hh), Wnt, Notch
 АВС-транспортеры и их роль в стволовых клетках Высокое содержание разных АВС-транспортеров (ABCB 1 - Pgp 170, АВСG 2 - BCRP, ABCB 5) в СК обеспечивает: • удаление цитотоксических препаратов и токсинов из СК, что определяет их устойчивость к повреждающим агентам • секрецию регуляторных факторов, поддерживающих состояние покоя (Gо) СК • СК не включают флуоресцентные красители Hoechst 33342 и родамин-123, что позволяет выделять популяцию СК с помощью проточной цитофлуориметрии при использовании флуориметров-сортировщиков клеток
АВС-транспортеры и их роль в стволовых клетках Высокое содержание разных АВС-транспортеров (ABCB 1 - Pgp 170, АВСG 2 - BCRP, ABCB 5) в СК обеспечивает: • удаление цитотоксических препаратов и токсинов из СК, что определяет их устойчивость к повреждающим агентам • секрецию регуляторных факторов, поддерживающих состояние покоя (Gо) СК • СК не включают флуоресцентные красители Hoechst 33342 и родамин-123, что позволяет выделять популяцию СК с помощью проточной цитофлуориметрии при использовании флуориметров-сортировщиков клеток
 АВС-транспортеры (ATP-Binding Cassete transporters) Семейство трансмембранных белков, которые осуществляют транспорт различных молекул через клеточные мембраны с использованием энергии, выделяющейся при гидролизе АТФ. Верапамил – инггибитор АВС транпортеров.
АВС-транспортеры (ATP-Binding Cassete transporters) Семейство трансмембранных белков, которые осуществляют транспорт различных молекул через клеточные мембраны с использованием энергии, выделяющейся при гидролизе АТФ. Верапамил – инггибитор АВС транпортеров.
 АВС-транспортеры, определяющие устойчивость клеток к различным препаратам Ген Белок Химиотерапевтические препараты и другие вещества, удаляемые из клеток АВС-транспортерами ABCA 2 Эстрамустин ABCB 1 PGP/MDR 1 Колхицин, доксорубицин, этопозид, винбластин, паклитаксель, дигоксин ABCC 1 MRP 1 Доксорубицин, даунорубицин, винкристин, этопозид, колхицин, камппотецин, метотрексат, родамин ABCC 2 MRP 2 Винбластин, цисплатин, доксорубицин, метотрекат, сульфинпиразон ABCC 3 MRP 3 Метотрексат, этопозид ABCC 4 MRP 4 6 -Меркаптопурин, 6 -тиогуанин и его метаболиты, метотрексат, ц. АМФ, ц. ГМФ ABCC 5 MRP 5 6 -Меркаптопурин, 6 -тиогуанин и его метаболиты, ц. АМФ, ц. ГМФ ABCC 6 MRP 6 Этопозид ABCC 11 MRP 11 5 -Фторурацил, ц. АМФ, ц. ГМФ ABCG 2 MXP/BCRP* Митоксантрон, топотекан, доксорубицин, даунорубицин, иринотекан, иматинит, метотрексат
АВС-транспортеры, определяющие устойчивость клеток к различным препаратам Ген Белок Химиотерапевтические препараты и другие вещества, удаляемые из клеток АВС-транспортерами ABCA 2 Эстрамустин ABCB 1 PGP/MDR 1 Колхицин, доксорубицин, этопозид, винбластин, паклитаксель, дигоксин ABCC 1 MRP 1 Доксорубицин, даунорубицин, винкристин, этопозид, колхицин, камппотецин, метотрексат, родамин ABCC 2 MRP 2 Винбластин, цисплатин, доксорубицин, метотрекат, сульфинпиразон ABCC 3 MRP 3 Метотрексат, этопозид ABCC 4 MRP 4 6 -Меркаптопурин, 6 -тиогуанин и его метаболиты, метотрексат, ц. АМФ, ц. ГМФ ABCC 5 MRP 5 6 -Меркаптопурин, 6 -тиогуанин и его метаболиты, ц. АМФ, ц. ГМФ ABCC 6 MRP 6 Этопозид ABCC 11 MRP 11 5 -Фторурацил, ц. АМФ, ц. ГМФ ABCG 2 MXP/BCRP* Митоксантрон, топотекан, доксорубицин, даунорубицин, иринотекан, иматинит, метотрексат
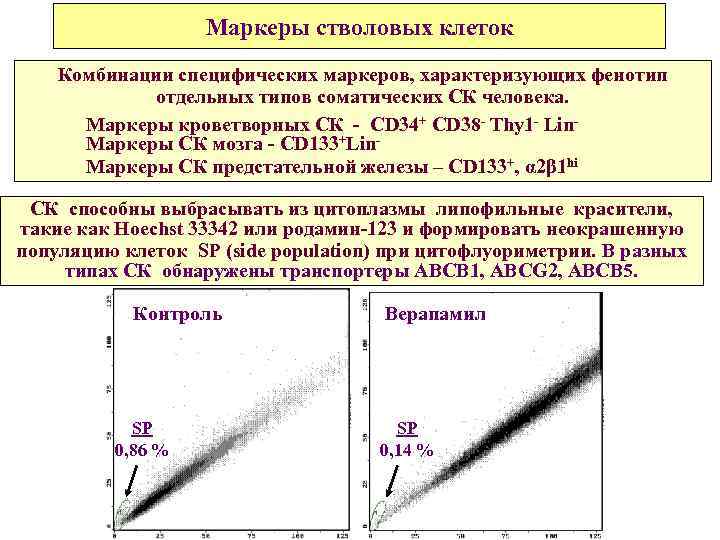 Маркеры стволовых клеток Комбинации специфических маркеров, характеризующих фенотип отдельных типов соматических СК человека. Маркеры кроветворных СК - CD 34+ CD 38 - Thy 1 - Lin. Маркеры СК мозга - CD 133+Lin. Маркеры СК предстательной железы – CD 133+, α 2β 1 hi СК способны выбрасывать из цитоплазмы липофильные красители, такие как Hoechst 33342 или родамин-123 и формировать неокрашенную популяцию клеток SP (side population) при цитофлуориметрии. В разных типах СК обнаружены транспортеры ABCB 1, ABCG 2, ABCB 5. Контроль SP 0, 86 % Верапамил SP 0, 14 %
Маркеры стволовых клеток Комбинации специфических маркеров, характеризующих фенотип отдельных типов соматических СК человека. Маркеры кроветворных СК - CD 34+ CD 38 - Thy 1 - Lin. Маркеры СК мозга - CD 133+Lin. Маркеры СК предстательной железы – CD 133+, α 2β 1 hi СК способны выбрасывать из цитоплазмы липофильные красители, такие как Hoechst 33342 или родамин-123 и формировать неокрашенную популяцию клеток SP (side population) при цитофлуориметрии. В разных типах СК обнаружены транспортеры ABCB 1, ABCG 2, ABCB 5. Контроль SP 0, 86 % Верапамил SP 0, 14 %
 Ниши стволовых клеток • Ниша СК – физиологическое клеточное микроокружение, поддерживающее и обеспечивающее существование СК (R. Schofield, 1978 г. ). • Ниши СК взрослых охарактеризованы в костном мозге, волосяном фолликуле, кишечнике, нервной системе и в семенниках.
Ниши стволовых клеток • Ниша СК – физиологическое клеточное микроокружение, поддерживающее и обеспечивающее существование СК (R. Schofield, 1978 г. ). • Ниши СК взрослых охарактеризованы в костном мозге, волосяном фолликуле, кишечнике, нервной системе и в семенниках.
 Костный мозг - источник стволовых клеток в организме Печень Головной мозг Стволовые клетки ЦНС Скелетная мышца Костный мозг Клетки крови Эндотелиальные клетки Жировые клетки Сердечная мышца Кость Стромальные клетки костного мозга Эпителиальные клетки Нейрон Глиальные клетки
Костный мозг - источник стволовых клеток в организме Печень Головной мозг Стволовые клетки ЦНС Скелетная мышца Костный мозг Клетки крови Эндотелиальные клетки Жировые клетки Сердечная мышца Кость Стромальные клетки костного мозга Эпителиальные клетки Нейрон Глиальные клетки
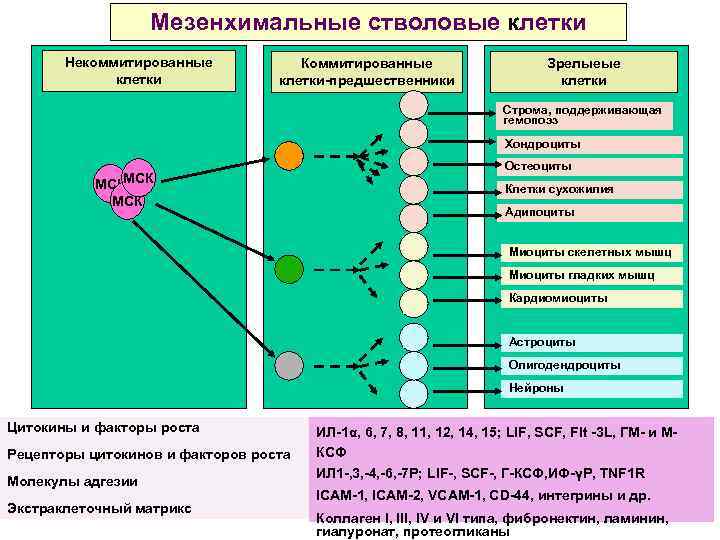 Мезенхимальные стволовые клетки Некоммитированные клетки Коммитированные клетки-предшественники Зрелыеые клетки Строма, поддерживающая гемопоэз Хондроциты МСКМСК Остеоциты Клетки сухожилия Адипоциты Миоциты скелетных мышц Миоциты гладких мышц Кардиомиоциты Астроциты Олигодендроциты Нейроны Цитокины и факторы роста Рецепторы цитокинов и факторов роста Молекулы адгезии Экстраклеточный матрикс ИЛ-1α, 6, 7, 8, 11, 12, 14, 15; LIF, SCF, Flt -3 L, ГМ- и МКСФ ИЛ 1 -, 3, -4, -6, -7 Р; LIF-, SCF-, Г-КСФ, ИФ-γР, TNF 1 R ICAM-1, ICAM-2, VCAM-1, CD-44, интегрины и др. Коллаген I, III, IV и VI типа, фибронектин, ламинин, гиалуронат, протеогликаны
Мезенхимальные стволовые клетки Некоммитированные клетки Коммитированные клетки-предшественники Зрелыеые клетки Строма, поддерживающая гемопоэз Хондроциты МСКМСК Остеоциты Клетки сухожилия Адипоциты Миоциты скелетных мышц Миоциты гладких мышц Кардиомиоциты Астроциты Олигодендроциты Нейроны Цитокины и факторы роста Рецепторы цитокинов и факторов роста Молекулы адгезии Экстраклеточный матрикс ИЛ-1α, 6, 7, 8, 11, 12, 14, 15; LIF, SCF, Flt -3 L, ГМ- и МКСФ ИЛ 1 -, 3, -4, -6, -7 Р; LIF-, SCF-, Г-КСФ, ИФ-γР, TNF 1 R ICAM-1, ICAM-2, VCAM-1, CD-44, интегрины и др. Коллаген I, III, IV и VI типа, фибронектин, ламинин, гиалуронат, протеогликаны
 Приготовлеие мезенхимальных стволовых клеток из жировой ткани 1. Получение жировой ткани с помощью липосакции или в виде фрагмента ткани. 2. Промывание образца фосфатным буфером для удаления крови. 3. Измельчение фрагментов жировой ткани и разрушение соединительной ткани при обработке коллагеназой (2 раза). 4. Нейтрализация коллагеназы средой с сывороткой и фильтрование суспензии через нейлоновую сеточку. 5. Сбор клеток с помощью центрифугирования. 6. Разрушение и удаление примеси эритроцитов с помощью лизирующего буфера. 7. Суспендирование клеток в культуральной среде и перенос в культуральные флаконы или чашки Петри для прикрепления к пластику на 12 -20 часов. 8. Интенсивное промывание клеток фосфатно-солевым буфером для удаления неприкрепившихся клеток. Прикрепившие клетки – фракция, обогащенная МСК. 8 а. Дополнительное наращивание МСК. 9. Замораживание МСК для хранения и хранение в банке МСК. 10. Типирование МСК по системе HLA, проведение необходимых анализов и введение в регистр.
Приготовлеие мезенхимальных стволовых клеток из жировой ткани 1. Получение жировой ткани с помощью липосакции или в виде фрагмента ткани. 2. Промывание образца фосфатным буфером для удаления крови. 3. Измельчение фрагментов жировой ткани и разрушение соединительной ткани при обработке коллагеназой (2 раза). 4. Нейтрализация коллагеназы средой с сывороткой и фильтрование суспензии через нейлоновую сеточку. 5. Сбор клеток с помощью центрифугирования. 6. Разрушение и удаление примеси эритроцитов с помощью лизирующего буфера. 7. Суспендирование клеток в культуральной среде и перенос в культуральные флаконы или чашки Петри для прикрепления к пластику на 12 -20 часов. 8. Интенсивное промывание клеток фосфатно-солевым буфером для удаления неприкрепившихся клеток. Прикрепившие клетки – фракция, обогащенная МСК. 8 а. Дополнительное наращивание МСК. 9. Замораживание МСК для хранения и хранение в банке МСК. 10. Типирование МСК по системе HLA, проведение необходимых анализов и введение в регистр.
 Культуры мышиных MSCBR, MSCBM и NSC и адипогенная (A), хондрогенная (B) и остеогенная (C) дифференцировка MSCBR A MSCBM B NSC C
Культуры мышиных MSCBR, MSCBM и NSC и адипогенная (A), хондрогенная (B) и остеогенная (C) дифференцировка MSCBR A MSCBM B NSC C
 Индукция дифференцировки МСК в разном направлении компонентами среды Направление дифференцировки Индукторы дифференцировки Контроль Без добавок Адипогенная (2 недели) 0, 5 м. М изобутил-метилксантин, 1 мк. М дексаметазон, 10 мк. М инсулин, 200 мк. М индометацин Остеогенная (> 2 недели) 0, 1 мк. М дексаметазон, 50 мк. М аскорбат-2 -фосфат, 10 м. М β-глицерофосфат Хондрогеная (2 недели) 0, 5 мк. М инсулин, 10 нг/мл. TGF- β, 50 н. М аскорбат-2 фосфат Миогенная (6 недель) 0, 1 мк. М дексаметазон, 50 мк. М гидрокортизон, 5% лошадиная сыворотка Культуральная среда – ДМЕМ, 10% фетальная сыворотка, индукторы дифференцировки, 1% антибиотики/антимикотики
Индукция дифференцировки МСК в разном направлении компонентами среды Направление дифференцировки Индукторы дифференцировки Контроль Без добавок Адипогенная (2 недели) 0, 5 м. М изобутил-метилксантин, 1 мк. М дексаметазон, 10 мк. М инсулин, 200 мк. М индометацин Остеогенная (> 2 недели) 0, 1 мк. М дексаметазон, 50 мк. М аскорбат-2 -фосфат, 10 м. М β-глицерофосфат Хондрогеная (2 недели) 0, 5 мк. М инсулин, 10 нг/мл. TGF- β, 50 н. М аскорбат-2 фосфат Миогенная (6 недель) 0, 1 мк. М дексаметазон, 50 мк. М гидрокортизон, 5% лошадиная сыворотка Культуральная среда – ДМЕМ, 10% фетальная сыворотка, индукторы дифференцировки, 1% антибиотики/антимикотики
 Индукция дифференцировки МСК в разном направлении компонентами среды Направление дифференцировки Индукторы дифференцировки Контроль Без добавок Адипогенная (2 недели) 0, 5 м. М изобутил-метилксантин, 1 мк. М дексаметазон, 10 мк. М инсулин, 200 мк. М индометацин Остеогенная (> 2 недели) 0, 1 мк. М дексаметазон, 50 мк. М аскорбат-2 -фосфат, 10 м. М β-глицерофосфат Хондрогеная (2 недели) 0, 5 мк. М инсулин, 10 нг/мл. TGF- β, 50 н. М аскорбат-2 фосфат Миогенная (6 недель) 0, 1 мк. М дексаметазон, 50 мк. М гидрокортизон, 5% лошадиная сыворотка Культуральная среда – ДМЕМ, 10% фетальная сыворотка, индукторы дифференцировки, 1% антибиотики/антимикотики
Индукция дифференцировки МСК в разном направлении компонентами среды Направление дифференцировки Индукторы дифференцировки Контроль Без добавок Адипогенная (2 недели) 0, 5 м. М изобутил-метилксантин, 1 мк. М дексаметазон, 10 мк. М инсулин, 200 мк. М индометацин Остеогенная (> 2 недели) 0, 1 мк. М дексаметазон, 50 мк. М аскорбат-2 -фосфат, 10 м. М β-глицерофосфат Хондрогеная (2 недели) 0, 5 мк. М инсулин, 10 нг/мл. TGF- β, 50 н. М аскорбат-2 фосфат Миогенная (6 недель) 0, 1 мк. М дексаметазон, 50 мк. М гидрокортизон, 5% лошадиная сыворотка Культуральная среда – ДМЕМ, 10% фетальная сыворотка, индукторы дифференцировки, 1% антибиотики/антимикотики
 Две гипотезы регенерации тканей и органов с помощью стволовых клеток костного мозга Костный мозг Тканеспецифические СК-предшественники Оседание в поврежденных тканях Кроветворные СК Трансдифференцировка в поврежденных тканях Поврежденные ткани секретируют не только SDF-1, но и HGF и LIF и др. цитокины, которые «привлекают» СК из периферической крови в зону повреждения. Введение Г-КСФ может быть методом неинвазивной терапии для регенерации миокарда при ОИМ и др. тканей
Две гипотезы регенерации тканей и органов с помощью стволовых клеток костного мозга Костный мозг Тканеспецифические СК-предшественники Оседание в поврежденных тканях Кроветворные СК Трансдифференцировка в поврежденных тканях Поврежденные ткани секретируют не только SDF-1, но и HGF и LIF и др. цитокины, которые «привлекают» СК из периферической крови в зону повреждения. Введение Г-КСФ может быть методом неинвазивной терапии для регенерации миокарда при ОИМ и др. тканей
 Использование Г-КСФ для регенерации миокарда и деструктивных изменений др. тканей. Введение Г-КСФ Стимуляция выхода СК в периферическую кровь. Выделение мононуклеарных лейкоцитов и введение в зону повреждения. Спонтанное оседание СК в зоне повреждения.
Использование Г-КСФ для регенерации миокарда и деструктивных изменений др. тканей. Введение Г-КСФ Стимуляция выхода СК в периферическую кровь. Выделение мононуклеарных лейкоцитов и введение в зону повреждения. Спонтанное оседание СК в зоне повреждения.
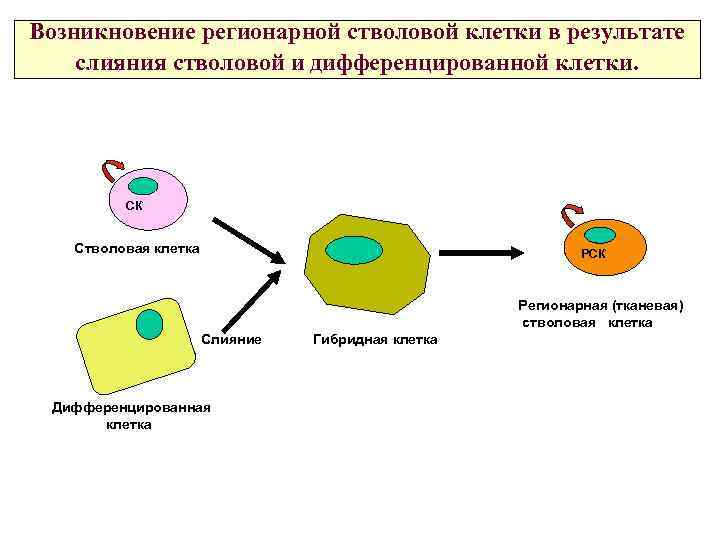 Возникновение регионарной стволовой клетки в результате слияния стволовой и дифференцированной клетки. СК Стволовая клетка РСК Регионарная (тканевая) стволовая клетка Слияние Дифференцированная клетка Гибридная клетка
Возникновение регионарной стволовой клетки в результате слияния стволовой и дифференцированной клетки. СК Стволовая клетка РСК Регионарная (тканевая) стволовая клетка Слияние Дифференцированная клетка Гибридная клетка
 Использование мезенхимальных стволовых клеток в медицине В косметологии – МСК из жировой ткани для снижения старения кожи При лечении переломов – МСК из костного мозга для ускорения образования кости При лечении сердечно-сосудистых заболеваний – МСК из костного мозга для ускорения развития новых сосудов в зоне ишемии при ОИМ Использование СК для лечения различных проявлений старения – проблема ближайшего будущего
Использование мезенхимальных стволовых клеток в медицине В косметологии – МСК из жировой ткани для снижения старения кожи При лечении переломов – МСК из костного мозга для ускорения образования кости При лечении сердечно-сосудистых заболеваний – МСК из костного мозга для ускорения развития новых сосудов в зоне ишемии при ОИМ Использование СК для лечения различных проявлений старения – проблема ближайшего будущего
 МСК, адгезированные на матриксе после 10 суток остеогенной предифференцировки . Стрелками указаны МСК. Фазовый контраст. А – ув. х100, Б – ув. х400. Препарат М. Е. Крашенинникова
МСК, адгезированные на матриксе после 10 суток остеогенной предифференцировки . Стрелками указаны МСК. Фазовый контраст. А – ув. х100, Б – ув. х400. Препарат М. Е. Крашенинникова
 Создание i. PS клеток – индуцированных полипотентных клеток с помощью трансфекции четырех генов
Создание i. PS клеток – индуцированных полипотентных клеток с помощью трансфекции четырех генов
 Sir John B. Gurdon Shinya Yamanaka Нобелевская премия 2012 г по медицине и физиологии за открытие возможности перепрограммироваия зрелых клеток в полипотентные
Sir John B. Gurdon Shinya Yamanaka Нобелевская премия 2012 г по медицине и физиологии за открытие возможности перепрограммироваия зрелых клеток в полипотентные
 Соматические клетки больного i. PS клетки Коррекция генетических дефектов Направленная дифференцировка Внедрение потенциальных лекарств в клинику Проверка на животных Поиск потенциальных лекарств Моделирование заболевания Скрининг потенциальных лекарств Фенотипирование Выявление маркеров Изучение молекулярных механизмов
Соматические клетки больного i. PS клетки Коррекция генетических дефектов Направленная дифференцировка Внедрение потенциальных лекарств в клинику Проверка на животных Поиск потенциальных лекарств Моделирование заболевания Скрининг потенциальных лекарств Фенотипирование Выявление маркеров Изучение молекулярных механизмов
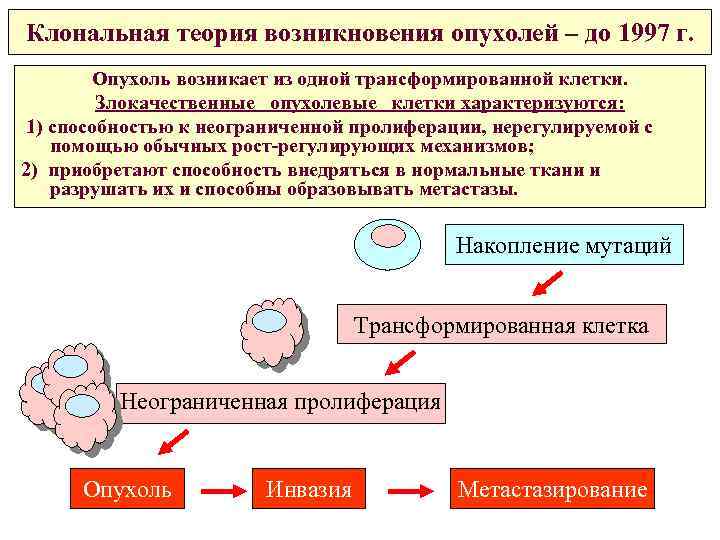 Клональная теория возникновения опухолей – до 1997 г. Опухоль возникает из одной трансформированной клетки. Злокачественные опухолевые клетки характеризуются: 1) способностью к неограниченной пролиферации, нерегулируемой с помощью обычных рост-регулирующих механизмов; 2) приобретают способность внедряться в нормальные ткани и разрушать их и способны образовывать метастазы. Накопление мутаций Трансформированная клетка Неограниченная пролиферация Опухоль Инвазия Метастазирование
Клональная теория возникновения опухолей – до 1997 г. Опухоль возникает из одной трансформированной клетки. Злокачественные опухолевые клетки характеризуются: 1) способностью к неограниченной пролиферации, нерегулируемой с помощью обычных рост-регулирующих механизмов; 2) приобретают способность внедряться в нормальные ткани и разрушать их и способны образовывать метастазы. Накопление мутаций Трансформированная клетка Неограниченная пролиферация Опухоль Инвазия Метастазирование
 Основные постулаты теории опухолевых стволовых клеток ·В каждой опухоли присутствует фракция ОСК, способных индуцировать опухоли при введении иммунодефицитным мышам. ·ОСК имеют определенные поверхностные маркеры, что позволяет успешно и воспроизводимо выделять их из общей массы опухолевых клеток с помощью проточной цитофлуориметрии или различных вариантов иммуноселекции. • Опухоли, развивающиеся из ОСК, содержат смешанную популяцию туморогенных и не туморогенных клеток, соответствующую гетерогенному клеточному составу исходной опухоли.
Основные постулаты теории опухолевых стволовых клеток ·В каждой опухоли присутствует фракция ОСК, способных индуцировать опухоли при введении иммунодефицитным мышам. ·ОСК имеют определенные поверхностные маркеры, что позволяет успешно и воспроизводимо выделять их из общей массы опухолевых клеток с помощью проточной цитофлуориметрии или различных вариантов иммуноселекции. • Опухоли, развивающиеся из ОСК, содержат смешанную популяцию туморогенных и не туморогенных клеток, соответствующую гетерогенному клеточному составу исходной опухоли.
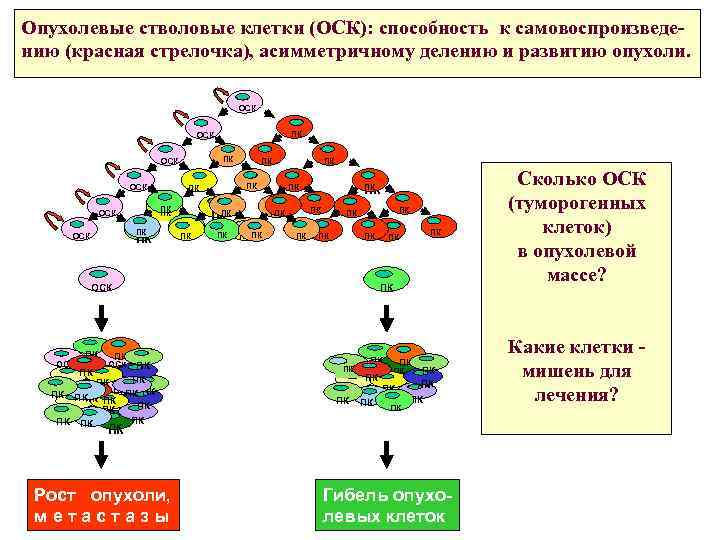 Опухолевые стволовые клетки (ОСК): способность к самовоспроизведению (красная стрелочка), асимметричному делению и развитию опухоли. ОСК ПК ОСК ПК ПК ПК ПК ПК ПК ОСК ПК ПК ПКПК ОСК ПК ПК ПК ПК ПК ПК ПК Рост опухоли, метастазы Гибель опухолевых клеток Сколько ОСК (туморогенных клеток) в опухолевой массе? Какие клетки мишень для лечения?
Опухолевые стволовые клетки (ОСК): способность к самовоспроизведению (красная стрелочка), асимметричному делению и развитию опухоли. ОСК ПК ОСК ПК ПК ПК ПК ПК ПК ОСК ПК ПК ПКПК ОСК ПК ПК ПК ПК ПК ПК ПК Рост опухоли, метастазы Гибель опухолевых клеток Сколько ОСК (туморогенных клеток) в опухолевой массе? Какие клетки мишень для лечения?
 Механизмы высокой устойчивости опухолевых стволовых клеток к действию противоопухолевой терапии Системы репарации ДНК Противоопухолевые препараты Системы антиоксидантов ЦТЛ Опухолевая клетка Hsp 70 и др. Hsp Ионизирующее излучение АВС-транспортеры Ингибиторы апоптоза АПОПТОЗ
Механизмы высокой устойчивости опухолевых стволовых клеток к действию противоопухолевой терапии Системы репарации ДНК Противоопухолевые препараты Системы антиоксидантов ЦТЛ Опухолевая клетка Hsp 70 и др. Hsp Ионизирующее излучение АВС-транспортеры Ингибиторы апоптоза АПОПТОЗ
 Модели исследования туморогенности ОСК человека Иммунодефицитные мыши SCID (severe combined immunodeficiency mouse) – отсутствуют Т- и В- лимфоциты NOD-SCID (Nonobese Diabetic SCID) – отсутствуют T-, B- и NK-лимфоциты Dick J. E. et al, Stem. Cells. , 1997 Al-Hajj M. et al, PNAS, 2003
Модели исследования туморогенности ОСК человека Иммунодефицитные мыши SCID (severe combined immunodeficiency mouse) – отсутствуют Т- и В- лимфоциты NOD-SCID (Nonobese Diabetic SCID) – отсутствуют T-, B- и NK-лимфоциты Dick J. E. et al, Stem. Cells. , 1997 Al-Hajj M. et al, PNAS, 2003
 Количественная оценка размера фракции туморогенных клеток опухолей человека в моделях с использованием ксенотрансплантации • Модель NOD-SCID – эффективность развития опухолей зависит от времени исследования: (вводили менее 10 000 клеток) 8 недель – 1/837000 клеток формируют опухоль 32 недели – 1/111000 клеток формируют опухоль • Модель NOD-SCID-IL 2 rg-/- - пальпируемые опухоли обнаруживались через 8 – 12 недель (вводили 8 клеток) в среднем – 1/9 клеток (1/5 – 1/21) Quintana E. et al. , 2008
Количественная оценка размера фракции туморогенных клеток опухолей человека в моделях с использованием ксенотрансплантации • Модель NOD-SCID – эффективность развития опухолей зависит от времени исследования: (вводили менее 10 000 клеток) 8 недель – 1/837000 клеток формируют опухоль 32 недели – 1/111000 клеток формируют опухоль • Модель NOD-SCID-IL 2 rg-/- - пальпируемые опухоли обнаруживались через 8 – 12 недель (вводили 8 клеток) в среднем – 1/9 клеток (1/5 – 1/21) Quintana E. et al. , 2008
 Количественная оценка размера фракции туморогенных клеток опухолей человека при аутологической трансплантации 59 больных раком на терминальной стадии Выход опухолей - 16/59 • • • 36 случаев аденокарциномы яичника – 12/36 19 случаев плоскоклеточной карциномы – 4/10 4 случая саркомы - 0/4 Опухолевые клетки вводили подкожно во фронтальную поверхность бедра в количестве от 104 до 108 Латентный период - менее 8 недель; TD 50 - 106 - 107 опухолевых клеток по Baumannm. , 2009.
Количественная оценка размера фракции туморогенных клеток опухолей человека при аутологической трансплантации 59 больных раком на терминальной стадии Выход опухолей - 16/59 • • • 36 случаев аденокарциномы яичника – 12/36 19 случаев плоскоклеточной карциномы – 4/10 4 случая саркомы - 0/4 Опухолевые клетки вводили подкожно во фронтальную поверхность бедра в количестве от 104 до 108 Латентный период - менее 8 недель; TD 50 - 106 - 107 опухолевых клеток по Baumannm. , 2009.
 Маркеры опухолевых стволовых клеток в различных солидных опухолях человека. Опухоль Маркер ОСК Ссылки Рак молочной железы CD 44+ CD 24 -/low Lin- [Al-Hajj M. , 2003 ] Опухоли головного мозга CD 133+ [Singh S. K. , 2003, 2004; Hemmati H. D. , 2003; Galli R. , 2004] Опухоли головы и шеи (плоскоклеточная карцинома) CD 44+ [Prince M. E. , et al, 2007] Рак поджелудочной железы CD 44+ CD 24+ ESA+ [Li C. et al, 2007 ] Меланома - суспензионная культура - прикрепляющаяся культура CD 20 CD 133+, ABCG 2+ CD 133+, ABCB 5+ [Fang D. , 2005 ] [Monzani E. , 2007 ] [Frank N. Y. , 2005] Рак предстательной железы CD 44+/α 2β 1 high/CD 133+ [Collins A. T. , 2005, 2006; Lawson 1 D. A. , 2007; Miki J. , 2007] Рак толстой кишки CD 133+ [Dalerba P. , 2007; O'Brien C. A. , 2007] Рак печени CD 133+ [Ma S. , 2007]
Маркеры опухолевых стволовых клеток в различных солидных опухолях человека. Опухоль Маркер ОСК Ссылки Рак молочной железы CD 44+ CD 24 -/low Lin- [Al-Hajj M. , 2003 ] Опухоли головного мозга CD 133+ [Singh S. K. , 2003, 2004; Hemmati H. D. , 2003; Galli R. , 2004] Опухоли головы и шеи (плоскоклеточная карцинома) CD 44+ [Prince M. E. , et al, 2007] Рак поджелудочной железы CD 44+ CD 24+ ESA+ [Li C. et al, 2007 ] Меланома - суспензионная культура - прикрепляющаяся культура CD 20 CD 133+, ABCG 2+ CD 133+, ABCB 5+ [Fang D. , 2005 ] [Monzani E. , 2007 ] [Frank N. Y. , 2005] Рак предстательной железы CD 44+/α 2β 1 high/CD 133+ [Collins A. T. , 2005, 2006; Lawson 1 D. A. , 2007; Miki J. , 2007] Рак толстой кишки CD 133+ [Dalerba P. , 2007; O'Brien C. A. , 2007] Рак печени CD 133+ [Ma S. , 2007]
 История развития представлений об опухолевых стволовых клетках • - изучение срезов тканей с помощью микроскопии – J. Muller, 1840 г. • - постулат о происхождении опухолевой клетки из нормальной – R. Virchov – 19 век. • - постулат о происхождении опухолевых клеток из сохранившихся в организме эмбриональных клеток – J. Cohnheim, 1867 г. • - сформулирована концепция кроветворной стволовой клетки – А. А. Максимов, 1908 г. • - ее подтверждение в радиобиологических исследованиях с трансплантацией клеток костного мозга - 50 - 60 -е гг. , 20 в. • - экспериментально доказано существование мезенхимальных стволовых клеток и описаны их свойства – А. Я. Фриденштейн, 1976 г. • - экспериментально доказано существование эмбриональных стволовых клеток и описаны методы их получения из внутренней клеточной массы - R. Edwards et al, 1968 -1998 гг. • - теория многостадийного канцерогенеза: злокачественная трансформация клетки – результат многих независимых событий – 20 в. • - экспериментально доказано существование в опухолевой массе небольшой фракции клеток, способных индуцировать опухоль и способных к самообновлению J. Dick et al, 1997 г.
История развития представлений об опухолевых стволовых клетках • - изучение срезов тканей с помощью микроскопии – J. Muller, 1840 г. • - постулат о происхождении опухолевой клетки из нормальной – R. Virchov – 19 век. • - постулат о происхождении опухолевых клеток из сохранившихся в организме эмбриональных клеток – J. Cohnheim, 1867 г. • - сформулирована концепция кроветворной стволовой клетки – А. А. Максимов, 1908 г. • - ее подтверждение в радиобиологических исследованиях с трансплантацией клеток костного мозга - 50 - 60 -е гг. , 20 в. • - экспериментально доказано существование мезенхимальных стволовых клеток и описаны их свойства – А. Я. Фриденштейн, 1976 г. • - экспериментально доказано существование эмбриональных стволовых клеток и описаны методы их получения из внутренней клеточной массы - R. Edwards et al, 1968 -1998 гг. • - теория многостадийного канцерогенеза: злокачественная трансформация клетки – результат многих независимых событий – 20 в. • - экспериментально доказано существование в опухолевой массе небольшой фракции клеток, способных индуцировать опухоль и способных к самообновлению J. Dick et al, 1997 г.
 Роль нарушений в белках сигнальных путей, регулирующих активность СК, в происхождении опухолей и ОСК. Активация сигнальных путей Hedgehog (Hh), Notch и Wnt в опухолях Сигнальная система Notch Опухоль Острый Т-лимфобластный лимфолейкоз Эпидермоидная карцинома Нейроболастома Медулобластома Wnt Аденокарцинома толстой кишки Гепатоцеллюлярная карцинома Карцинома щитовидной железы Hh Базально-клеточная карцинома Медулобластома Мелкоклеточный рак легкого Рак поджелудочной железы Опухоли ЖКТ Рак предстательной железы Рак молочной железы Рак толстой кишки Рак печени Рабдомиосаркома Гепатоклеточная карцинома Множественная миелома
Роль нарушений в белках сигнальных путей, регулирующих активность СК, в происхождении опухолей и ОСК. Активация сигнальных путей Hedgehog (Hh), Notch и Wnt в опухолях Сигнальная система Notch Опухоль Острый Т-лимфобластный лимфолейкоз Эпидермоидная карцинома Нейроболастома Медулобластома Wnt Аденокарцинома толстой кишки Гепатоцеллюлярная карцинома Карцинома щитовидной железы Hh Базально-клеточная карцинома Медулобластома Мелкоклеточный рак легкого Рак поджелудочной железы Опухоли ЖКТ Рак предстательной железы Рак молочной железы Рак толстой кишки Рак печени Рабдомиосаркома Гепатоклеточная карцинома Множественная миелома
 Ингибиторы сигнальной системы Hedgehog Структурная формула циклопамина
Ингибиторы сигнальной системы Hedgehog Структурная формула циклопамина
 Ингибиторы сигнальной системы Wnt Структурная формула салиномицина
Ингибиторы сигнальной системы Wnt Структурная формула салиномицина
 Салиномицин снижает фракцию SP в опухолевых клетках Меланома человека линия Mel-8 Контроль MFI, усл. ед. 266, 7 SP 0, 86 % Салиномицин MFI, усл. ед. 771, 3 SP 0, 14 % Верапамил MFI, усл. ед. 821, 0 А SP 0, 19 % Меланома человека линия Mel-10 Контроль MFI, усл. ед. 872, 7 SP 0, 08 % Салиномицин MFI, усл. ед. 999, 8 SP 0, 02% Верапамил MFI, усл. ед. 882, 2 SP 0, 04 % Б
Салиномицин снижает фракцию SP в опухолевых клетках Меланома человека линия Mel-8 Контроль MFI, усл. ед. 266, 7 SP 0, 86 % Салиномицин MFI, усл. ед. 771, 3 SP 0, 14 % Верапамил MFI, усл. ед. 821, 0 А SP 0, 19 % Меланома человека линия Mel-10 Контроль MFI, усл. ед. 872, 7 SP 0, 08 % Салиномицин MFI, усл. ед. 999, 8 SP 0, 02% Верапамил MFI, усл. ед. 882, 2 SP 0, 04 % Б
 Основные мишени создания новых средств противоопухолевой терапии • Ингибиторы альдегидрогеназы • Ингибиторы АВС-транспортеров • Ингибиторы сигнальных путей ОСК (Hedgehog, Wnt, Notch и др. ) • Ниша ОСК блокаторы VEGF, ERB 2 и др. блокаторы хоминга ОСК - CXCR 4 и др. • Индукторы дифферецировки ОСК.
Основные мишени создания новых средств противоопухолевой терапии • Ингибиторы альдегидрогеназы • Ингибиторы АВС-транспортеров • Ингибиторы сигнальных путей ОСК (Hedgehog, Wnt, Notch и др. ) • Ниша ОСК блокаторы VEGF, ERB 2 и др. блокаторы хоминга ОСК - CXCR 4 и др. • Индукторы дифферецировки ОСК.
 Благодарю за внимание !
Благодарю за внимание !


