Spin-Coating.ppt
- Количество слайдов: 54
 Студенческий научный отряд 2012 ПОЛУЧЕНИЕ ТОНКИХ ПЛЕНОК МЕТОДОМ ЦЕНТРИФУГИРОВАНИЯ 1
Студенческий научный отряд 2012 ПОЛУЧЕНИЕ ТОНКИХ ПЛЕНОК МЕТОДОМ ЦЕНТРИФУГИРОВАНИЯ 1
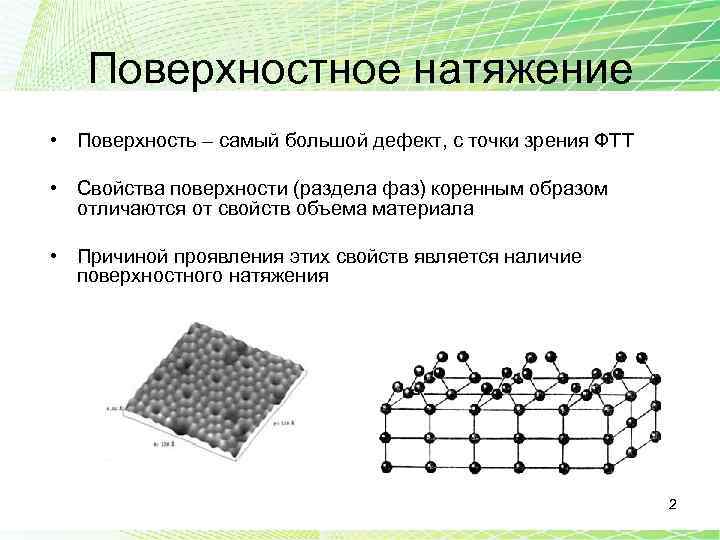 Поверхностное натяжение • Поверхность – самый большой дефект, с точки зрения ФТТ • Свойства поверхности (раздела фаз) коренным образом отличаются от свойств объема материала • Причиной проявления этих свойств является наличие поверхностного натяжения 2
Поверхностное натяжение • Поверхность – самый большой дефект, с точки зрения ФТТ • Свойства поверхности (раздела фаз) коренным образом отличаются от свойств объема материала • Причиной проявления этих свойств является наличие поверхностного натяжения 2
 • • • Молекулы поверхностного слоя оказывают молекулярное давление, стягивая ее поверхность к минимуму. Этот эффект называют поверхностным натяжением. Поверхность, соприкасающаяся с другой средой, например с собственным паром, с какой-либо другой жидкостью или с твердым телом находится в особых условиях по сравнению с остальной массой жидкости. Возникают эти особые условия потому, что молекулы пограничного слоя, в отличие от молекул в ее глубине, окружены молекулами не со всех сторон. Часть “соседей” поверхностных молекул- это частицы второй среды, с которой жидкость граничит. Имея же разных соседей, молекулы поверхностного слоя и взаимодействуют с ними различным способом. Поэтому силы, действующие на каждую молекулу в этом слое, оказываются неуравновешенными: существует некоторая равнодействующая сила, направленная либо в сторону объема жидкости, либо в сторону граничащей с ней среды. 3
• • • Молекулы поверхностного слоя оказывают молекулярное давление, стягивая ее поверхность к минимуму. Этот эффект называют поверхностным натяжением. Поверхность, соприкасающаяся с другой средой, например с собственным паром, с какой-либо другой жидкостью или с твердым телом находится в особых условиях по сравнению с остальной массой жидкости. Возникают эти особые условия потому, что молекулы пограничного слоя, в отличие от молекул в ее глубине, окружены молекулами не со всех сторон. Часть “соседей” поверхностных молекул- это частицы второй среды, с которой жидкость граничит. Имея же разных соседей, молекулы поверхностного слоя и взаимодействуют с ними различным способом. Поэтому силы, действующие на каждую молекулу в этом слое, оказываются неуравновешенными: существует некоторая равнодействующая сила, направленная либо в сторону объема жидкости, либо в сторону граничащей с ней среды. 3
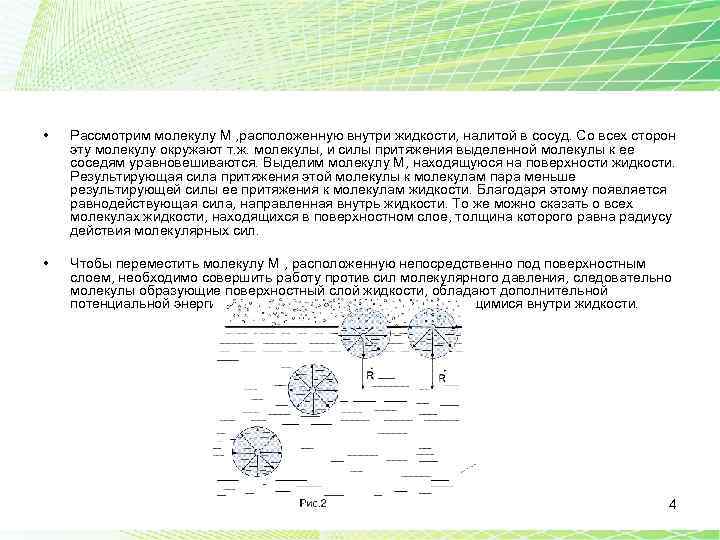 • Рассмотрим молекулу М , расположенную внутри жидкости, налитой в сосуд. Со всех сторон эту молекулу окружают т. ж. молекулы, и силы притяжения выделенной молекулы к ее соседям уравновешиваются. Выделим молекулу М, находящуюся на поверхности жидкости. Результирующая сила притяжения этой молекулы к молекулам пара меньше результирующей силы ее притяжения к молекулам жидкости. Благодаря этому появляется равнодействующая сила, направленная внутрь жидкости. То же можно сказать о всех молекулах жидкости, находящихся в поверхностном слое, толщина которого равна радиусу действия молекулярных сил. • Чтобы переместить молекулу М , расположенную непосредственно под поверхностным слоем, необходимо совершить работу против сил молекулярного давления, следовательно молекулы образующие поверхностный слой жидкости, обладают дополнительной потенциальной энергией по сравнению с молекулами находящимися внутри жидкости. 4
• Рассмотрим молекулу М , расположенную внутри жидкости, налитой в сосуд. Со всех сторон эту молекулу окружают т. ж. молекулы, и силы притяжения выделенной молекулы к ее соседям уравновешиваются. Выделим молекулу М, находящуюся на поверхности жидкости. Результирующая сила притяжения этой молекулы к молекулам пара меньше результирующей силы ее притяжения к молекулам жидкости. Благодаря этому появляется равнодействующая сила, направленная внутрь жидкости. То же можно сказать о всех молекулах жидкости, находящихся в поверхностном слое, толщина которого равна радиусу действия молекулярных сил. • Чтобы переместить молекулу М , расположенную непосредственно под поверхностным слоем, необходимо совершить работу против сил молекулярного давления, следовательно молекулы образующие поверхностный слой жидкости, обладают дополнительной потенциальной энергией по сравнению с молекулами находящимися внутри жидкости. 4
 • Эту энергию называют поверхностной энергией. • Очевидно, что величина поверхностной энергии тем больше, чем больше площадь свободной поверхности. • Пусть площадь свободной поверхности изменилась на ΔS, при этом поверхностная энергия изменилась на где α — коэффициент поверхностного натяжения. Так как для этого изменения необходимо совершить работу Отсюда то 5
• Эту энергию называют поверхностной энергией. • Очевидно, что величина поверхностной энергии тем больше, чем больше площадь свободной поверхности. • Пусть площадь свободной поверхности изменилась на ΔS, при этом поверхностная энергия изменилась на где α — коэффициент поверхностного натяжения. Так как для этого изменения необходимо совершить работу Отсюда то 5
 • Единицей коэффициента поверхностного натяжения в СИ является джоуль на квадратный метр (Дж/м 2). • Коэффициент поверхностного натяжения — величина, численно равная работе, совершенной молекулярными силами при изменении площади свободной поверхности жидкости на единицу при изотермическом процессе. • Так как любая система, предоставленная сама себе, стремится занять такое положение, в котором ее потенциальная энергия наименьшая, то жидкость 6 обнаруживает стремление к сокращению
• Единицей коэффициента поверхностного натяжения в СИ является джоуль на квадратный метр (Дж/м 2). • Коэффициент поверхностного натяжения — величина, численно равная работе, совершенной молекулярными силами при изменении площади свободной поверхности жидкости на единицу при изотермическом процессе. • Так как любая система, предоставленная сама себе, стремится занять такое положение, в котором ее потенциальная энергия наименьшая, то жидкость 6 обнаруживает стремление к сокращению
 Различные модели • Поверхностное натяжение есть величина, измеряемая энергией Гиббса, приходящейся на единицу площади поверхностного слоя. Оно численно равно работе, которую необходимо совершить против сил межмолекулярного взаимодействия для образования единицы поверхности раздела фаз при постоянной температуре. • Из модели Дюпре, поверхностное натяжение равно силе, стремящейся уменьшить поверхность раздела и отнесенной к единице длины контура, ограничивающего поверхность 7
Различные модели • Поверхностное натяжение есть величина, измеряемая энергией Гиббса, приходящейся на единицу площади поверхностного слоя. Оно численно равно работе, которую необходимо совершить против сил межмолекулярного взаимодействия для образования единицы поверхности раздела фаз при постоянной температуре. • Из модели Дюпре, поверхностное натяжение равно силе, стремящейся уменьшить поверхность раздела и отнесенной к единице длины контура, ограничивающего поверхность 7
 Изменение поверхностного натяжения • Способность растворенных веществ изменять поверхностное натяжение растворителя называется поверхностной активностью g: • • Классификация веществ по влиянию на поверхностное натяжение растворителя 1. Поверхностно-активные вещества (ПАВ) – понижают поверхностное натяжение растворителя g > 0 (по отношению к воде – органические соединения дифильного строения). 2. Поверхностно-инактивные вещества (ПИВ) – незначительно повышают поверхностное натяжение растворителя g < 0 (неорганические кислоты, основания, соли, глицерин, ? -аминокислоты и др). 3. Поверхностно-неактивные вещества (ПНВ) – практически не изменяют поверхностного натяжения растворителя g = 0 (по отношению к воде веществами являются сахароза и ряд других). 8
Изменение поверхностного натяжения • Способность растворенных веществ изменять поверхностное натяжение растворителя называется поверхностной активностью g: • • Классификация веществ по влиянию на поверхностное натяжение растворителя 1. Поверхностно-активные вещества (ПАВ) – понижают поверхностное натяжение растворителя g > 0 (по отношению к воде – органические соединения дифильного строения). 2. Поверхностно-инактивные вещества (ПИВ) – незначительно повышают поверхностное натяжение растворителя g < 0 (неорганические кислоты, основания, соли, глицерин, ? -аминокислоты и др). 3. Поверхностно-неактивные вещества (ПНВ) – практически не изменяют поверхностного натяжения растворителя g = 0 (по отношению к воде веществами являются сахароза и ряд других). 8
 • Межфазное натяжение — это поверхностное натяжение или свободная поверхностная энергия на границе двух несмешивающихся или частично смешивающихся веществ. Причина несмешиваемости обычно заключается в большой разнице сил когезии, действующих между молекулами каждого вещества. Поэтому на межфазной поверхности возникает нескомпенсированная сила. Чем больше разница сил когезии, тем выше межфазное натяжение. При достаточно небольшой разнице сил когезии вещества смешиваются друг с другом. Когезия - это силы межмолекулярного взаимодействия, водородной связи и (или) иной химической связи. Они определяют совокупность физических и физико-химических свойств вещества: агрегатное состояние, летучесть, растворимость, механические свойства и т. д. 9
• Межфазное натяжение — это поверхностное натяжение или свободная поверхностная энергия на границе двух несмешивающихся или частично смешивающихся веществ. Причина несмешиваемости обычно заключается в большой разнице сил когезии, действующих между молекулами каждого вещества. Поэтому на межфазной поверхности возникает нескомпенсированная сила. Чем больше разница сил когезии, тем выше межфазное натяжение. При достаточно небольшой разнице сил когезии вещества смешиваются друг с другом. Когезия - это силы межмолекулярного взаимодействия, водородной связи и (или) иной химической связи. Они определяют совокупность физических и физико-химических свойств вещества: агрегатное состояние, летучесть, растворимость, механические свойства и т. д. 9
 Адгезия • Адгезия (от лат. adhaesio — прилипание) в физике — сцепление поверхностей разнородных твёрдых и/или жидких тел. Адгезия обусловлена межмолекулярным взаимодействием (вандерваальсовым, полярным, иногда — образованием химических связей или взаимной диффузией) в поверхностном слое и характеризуется удельной работой, необходимой для разделения поверхностей. В некоторых случаях адгезия может оказаться сильнее, чем когезия, т. е. сцепление внутри однородного материала, в таких случаях приложении разрывающего усилия происходит когезионный разрыв, т. е. разрыв в объёме менее прочного из соприкасающихся материалов. 10
Адгезия • Адгезия (от лат. adhaesio — прилипание) в физике — сцепление поверхностей разнородных твёрдых и/или жидких тел. Адгезия обусловлена межмолекулярным взаимодействием (вандерваальсовым, полярным, иногда — образованием химических связей или взаимной диффузией) в поверхностном слое и характеризуется удельной работой, необходимой для разделения поверхностей. В некоторых случаях адгезия может оказаться сильнее, чем когезия, т. е. сцепление внутри однородного материала, в таких случаях приложении разрывающего усилия происходит когезионный разрыв, т. е. разрыв в объёме менее прочного из соприкасающихся материалов. 10
 Абсорбция • • • АБСОРБЦИЯ газов (лат. absorptio, от absorbeo-поглощаю), объемное поглощение газов и паров жидкостью (абсорбентом) с образованием р-ра. Применение абсорбции в технике для разделения и очистки газов, выделения паров из паро-газовых смесей основано на разл. р-римости газов и паров в жидкостях. Процесс, обратный абсорбции. , наз. десорбцией; его используют для выделения из р-ра поглощенного газа и регенерации абсорбента. Поглощение газов металлами (напр. , водорода палладием) наз. окклюзией. Абсорбция - частный случай сорбции. • Различают физ. и хим. абсорбцию. При физической абсорбции энергия взаимод. молекул газа и абсорбента в р-ре не превышает 20 к. Дж/моль. При химической абсорбции (или абсорбция с хим. р-цией, часто наз. хемосорбцией) молекулы растворенного газа реагируют с активным компонентом абсорбента-хемосорбентом (энергия взаимод. молекул более 25 к. Дж/моль) либо в р-ре происходитдиссоциация или ассоциация молекул газа. Промежут. варианты абсорбции характеризуются энергией взаимод. молекул 20 -30 к. Дж/моль. 11 К таким процессам относится растворение с образованием •
Абсорбция • • • АБСОРБЦИЯ газов (лат. absorptio, от absorbeo-поглощаю), объемное поглощение газов и паров жидкостью (абсорбентом) с образованием р-ра. Применение абсорбции в технике для разделения и очистки газов, выделения паров из паро-газовых смесей основано на разл. р-римости газов и паров в жидкостях. Процесс, обратный абсорбции. , наз. десорбцией; его используют для выделения из р-ра поглощенного газа и регенерации абсорбента. Поглощение газов металлами (напр. , водорода палладием) наз. окклюзией. Абсорбция - частный случай сорбции. • Различают физ. и хим. абсорбцию. При физической абсорбции энергия взаимод. молекул газа и абсорбента в р-ре не превышает 20 к. Дж/моль. При химической абсорбции (или абсорбция с хим. р-цией, часто наз. хемосорбцией) молекулы растворенного газа реагируют с активным компонентом абсорбента-хемосорбентом (энергия взаимод. молекул более 25 к. Дж/моль) либо в р-ре происходитдиссоциация или ассоциация молекул газа. Промежут. варианты абсорбции характеризуются энергией взаимод. молекул 20 -30 к. Дж/моль. 11 К таким процессам относится растворение с образованием •
 Адсорбция • АДСОРБЦИЯ (от лат. ad-на, при и sorbeo-поглощаю), изменение (обычно-повышение) концентрации в-ва вблизи пов-сти раздела фаз ("поглощение на повсти"). В общем случае причина адсорбции - нескомпенсированность межмол. сил вблизи этой пов-сти, т. е. наличие адсорбц. силового поля. Тело, создающее такое поле, наз. адсорбентом, в-во, молекулы к-рого могут адсорбироваться, -а д с о р б т и в о м, уже адсорбиров. в-во-адсорбатом. Процесс, обратный адсорбции, наз. десорбцией. 12
Адсорбция • АДСОРБЦИЯ (от лат. ad-на, при и sorbeo-поглощаю), изменение (обычно-повышение) концентрации в-ва вблизи пов-сти раздела фаз ("поглощение на повсти"). В общем случае причина адсорбции - нескомпенсированность межмол. сил вблизи этой пов-сти, т. е. наличие адсорбц. силового поля. Тело, создающее такое поле, наз. адсорбентом, в-во, молекулы к-рого могут адсорбироваться, -а д с о р б т и в о м, уже адсорбиров. в-во-адсорбатом. Процесс, обратный адсорбции, наз. десорбцией. 12
 • Природа адсорбц. сил м. б. весьма различной. • Если это ван-дер-ваальсовы силы, то адсорбция наз. физической, если валентные (т. е. адсорбция сопровождается образованием поверхностных хим. соединений), - химической, или хемосорбцией. • Отличит. черты хемосорбции - необратимость, высокие тепловые эффекты (сотни к. Дж/моль), активированный характер. • Между физ. и хим. адсорбцией существует множество промежут. случаев (напр. , адсорбция, обусловленная образованием водородных связей). • Возможны также разл. типы физ. адсорбции наиб. универсально проявление дисперсионных межмол. сил притяжения, т. к. они приблизительно постоянны для адсорбентов с пов-стью любой хим. природы (т. наз. неспецифич. адсорбция). • Физ. адсорбция может быть вызвана электростатич. силами (взаимод. между ионами, диполями или квадруполями); при этом адсорбция определяется хим. природой молекул адсорбтива (т. наз. специфич. адсорбция). • Значит. роль при адсорбции играет также геометрия пов-сти 13 раздела: в случае плоской пов-сти говорят об адсорбции на
• Природа адсорбц. сил м. б. весьма различной. • Если это ван-дер-ваальсовы силы, то адсорбция наз. физической, если валентные (т. е. адсорбция сопровождается образованием поверхностных хим. соединений), - химической, или хемосорбцией. • Отличит. черты хемосорбции - необратимость, высокие тепловые эффекты (сотни к. Дж/моль), активированный характер. • Между физ. и хим. адсорбцией существует множество промежут. случаев (напр. , адсорбция, обусловленная образованием водородных связей). • Возможны также разл. типы физ. адсорбции наиб. универсально проявление дисперсионных межмол. сил притяжения, т. к. они приблизительно постоянны для адсорбентов с пов-стью любой хим. природы (т. наз. неспецифич. адсорбция). • Физ. адсорбция может быть вызвана электростатич. силами (взаимод. между ионами, диполями или квадруполями); при этом адсорбция определяется хим. природой молекул адсорбтива (т. наз. специфич. адсорбция). • Значит. роль при адсорбции играет также геометрия пов-сти 13 раздела: в случае плоской пов-сти говорят об адсорбции на
 • Физическая адсорбция проявляется на поверхности раздела: • водный раствор – газ (воздух, собственный пар), пример – снижение поверхностного натяжения путем введения ПАВ; • водный раствор – жидкость (устойчивые эмульсии); • водный раствор – твердое тело (смачивание, капиллярный подсос, флотация, гидрофобизация); • твердое тело – газ (воздух), (адсорбция газов, водяных паров, конденсация. • На поверхности раздела между твердым телом и газом, твердым телом и жидкостью происходит адсорбция тех веществ, которые снижают поверхностное натяжение твердого тела. Адсорбция веществ из газовой среды и растворенных веществ на поверхности твердого тела значительно сложнее, чем адсорбция растворенных веществ на жидкой 14
• Физическая адсорбция проявляется на поверхности раздела: • водный раствор – газ (воздух, собственный пар), пример – снижение поверхностного натяжения путем введения ПАВ; • водный раствор – жидкость (устойчивые эмульсии); • водный раствор – твердое тело (смачивание, капиллярный подсос, флотация, гидрофобизация); • твердое тело – газ (воздух), (адсорбция газов, водяных паров, конденсация. • На поверхности раздела между твердым телом и газом, твердым телом и жидкостью происходит адсорбция тех веществ, которые снижают поверхностное натяжение твердого тела. Адсорбция веществ из газовой среды и растворенных веществ на поверхности твердого тела значительно сложнее, чем адсорбция растворенных веществ на жидкой 14
 Абсорбция (лат. absorptio - поглощение, от absorbeo - поглощаю), поглощение веществ из газовой смеси жидкостями. Адсорбция (от лат. ad - на, при и sorbeo - поглощаю), поглощение вещества из газообразной среды или раствора поверхностным 15 слоем жидкости или твёрдого тела.
Абсорбция (лат. absorptio - поглощение, от absorbeo - поглощаю), поглощение веществ из газовой смеси жидкостями. Адсорбция (от лат. ad - на, при и sorbeo - поглощаю), поглощение вещества из газообразной среды или раствора поверхностным 15 слоем жидкости или твёрдого тела.
 Адгезия • • АДГЕЗИЯ (от лат. adhaesio-притяжение, сцепление) (прилипание), явление соединения приведенных в контакт поветей конденсиров. фаз. Эти фазы составляют основу образующегося в результате молекулярного (т. е. по всей межфазной площади) контакта адгезионного соед. и наз. субстратами, а в-ва, обеспечивающие соединение субстратов, - адгезивами. Обычно субстраты-твердые тела (металлы, полимеры, реже-стекла, керамика), адгезивы — жидкости (рры или расплавы полимеров, реже-низкомол. продукты). Частный случай адгезии - аутогезия, реализуемая при молекулярном контакте двух одинаковых по составу и строению объектов. Закономерности образования и разрушения адгезионных соед. описывают на основе двух независимых подходов-термодинамического и молекулярно-кинетического. В рамках первого из них рассматривают энергетич. характеристики (поверхностные энергии адгезива субстрата и межфазной границы в рамках второго рассматривают когезионные св-ва адгезивов и субстратов (прочность и обусловливающие ее параметры, вязкость адгезива а также условия их контакта (т-ру t, давление р и продолжительность наиб. изучена адгезия полимеров, определяющая закономерности склеивания, сварки, совмещения, получения композитов. Адгезия проявляется в процессах трения, смазки, порошковой металлургии, флотации и др. , а также при 16 взаимод. биол. объектов (целостностьтканей и т. п. ).
Адгезия • • АДГЕЗИЯ (от лат. adhaesio-притяжение, сцепление) (прилипание), явление соединения приведенных в контакт поветей конденсиров. фаз. Эти фазы составляют основу образующегося в результате молекулярного (т. е. по всей межфазной площади) контакта адгезионного соед. и наз. субстратами, а в-ва, обеспечивающие соединение субстратов, - адгезивами. Обычно субстраты-твердые тела (металлы, полимеры, реже-стекла, керамика), адгезивы — жидкости (рры или расплавы полимеров, реже-низкомол. продукты). Частный случай адгезии - аутогезия, реализуемая при молекулярном контакте двух одинаковых по составу и строению объектов. Закономерности образования и разрушения адгезионных соед. описывают на основе двух независимых подходов-термодинамического и молекулярно-кинетического. В рамках первого из них рассматривают энергетич. характеристики (поверхностные энергии адгезива субстрата и межфазной границы в рамках второго рассматривают когезионные св-ва адгезивов и субстратов (прочность и обусловливающие ее параметры, вязкость адгезива а также условия их контакта (т-ру t, давление р и продолжительность наиб. изучена адгезия полимеров, определяющая закономерности склеивания, сварки, совмещения, получения композитов. Адгезия проявляется в процессах трения, смазки, порошковой металлургии, флотации и др. , а также при 16 взаимод. биол. объектов (целостностьтканей и т. п. ).
 17
17
 Смачиваемость • СМАЧИВАНИЕ - процессы, происходящие при взаимодействии жидкости с поверхностью тв. тела или др. жидкости и проявляющиеся в растекании жидкости и формировании площади т. н. адгезионного контакта, возникновении менисков в капиллярных каналах, вытеснении одной жидкости другой, образовании капель жидкости на поверхности или пузырьков в жидкости, в проникновении жидкости в капиллярнопористые тела. С. - следствие адгезии жидкости к определённой поверхности. 18
Смачиваемость • СМАЧИВАНИЕ - процессы, происходящие при взаимодействии жидкости с поверхностью тв. тела или др. жидкости и проявляющиеся в растекании жидкости и формировании площади т. н. адгезионного контакта, возникновении менисков в капиллярных каналах, вытеснении одной жидкости другой, образовании капель жидкости на поверхности или пузырьков в жидкости, в проникновении жидкости в капиллярнопористые тела. С. - следствие адгезии жидкости к определённой поверхности. 18
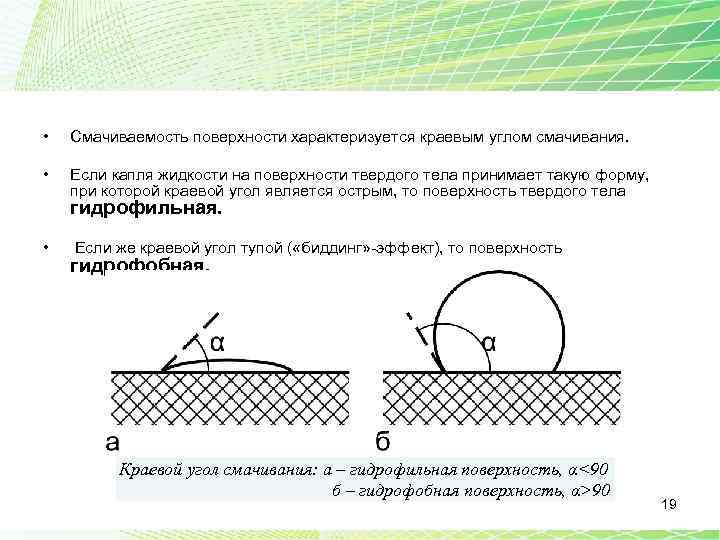 • Смачиваемость поверхности характеризуется краевым углом смачивания. • Если капля жидкости на поверхности твердого тела принимает такую форму, при которой краевой угол является острым, то поверхность твердого тела гидрофильная. • Если же краевой угол тупой ( «биддинг» -эффект), то поверхность гидрофобная. Краевой угол смачивания: а – гидрофильная поверхность, α<90 б – гидрофобная поверхность, α>90 19
• Смачиваемость поверхности характеризуется краевым углом смачивания. • Если капля жидкости на поверхности твердого тела принимает такую форму, при которой краевой угол является острым, то поверхность твердого тела гидрофильная. • Если же краевой угол тупой ( «биддинг» -эффект), то поверхность гидрофобная. Краевой угол смачивания: а – гидрофильная поверхность, α<90 б – гидрофобная поверхность, α>90 19
 • где σтг - поверхностное натяжение на границе раздела фаз твёрдое тело - газ; σтж - поверхностное натяжение на границе раздела фаз твёрдое тело - жидкость; σжг - поверхностное натяжение на границе раздела фаз жидкость - газ. C. твёрдой поверхности жидкостью увеличивается по мере уменьшения угла Q. При рассмотрении угла C. учитывается гистерезис C, зависящий от состояния твердой поверхности - её шероховатости, хим. неоднородности, препятствующих перемещению границы раздела фаз (уменьшение угла C. при оттекании жидкости и увеличение угла Q при натекании жидкости). Краевой угол является мерой С. , его величина зависит от соотношения между энергиями адгезии и когезии жидкости 20
• где σтг - поверхностное натяжение на границе раздела фаз твёрдое тело - газ; σтж - поверхностное натяжение на границе раздела фаз твёрдое тело - жидкость; σжг - поверхностное натяжение на границе раздела фаз жидкость - газ. C. твёрдой поверхности жидкостью увеличивается по мере уменьшения угла Q. При рассмотрении угла C. учитывается гистерезис C, зависящий от состояния твердой поверхности - её шероховатости, хим. неоднородности, препятствующих перемещению границы раздела фаз (уменьшение угла C. при оттекании жидкости и увеличение угла Q при натекании жидкости). Краевой угол является мерой С. , его величина зависит от соотношения между энергиями адгезии и когезии жидкости 20
 Методы получения тонких органических пленок • • • 1. Распыление 2. Полив 3. Окунание 4. Сушка в насыщ. парах растворителя 5. Метод Ленгмюра-Блоджетт …. • Spin-Coating (Центрифугирование) 21
Методы получения тонких органических пленок • • • 1. Распыление 2. Полив 3. Окунание 4. Сушка в насыщ. парах растворителя 5. Метод Ленгмюра-Блоджетт …. • Spin-Coating (Центрифугирование) 21
 • В большинстве случаев жидкость на поверхности твердого тела остается в виде капли, большей или меньшей толщины, контактирующей с твердым телом под определенным углом, который называется краевым углом смачивания и обозначается буквой Q (рис. 1. 24). Растекание капли по поверхности прекратится при достижении равновесия, которое без учета сил тяжести может быть описано уравнением Юнга: 22
• В большинстве случаев жидкость на поверхности твердого тела остается в виде капли, большей или меньшей толщины, контактирующей с твердым телом под определенным углом, который называется краевым углом смачивания и обозначается буквой Q (рис. 1. 24). Растекание капли по поверхности прекратится при достижении равновесия, которое без учета сил тяжести может быть описано уравнением Юнга: 22
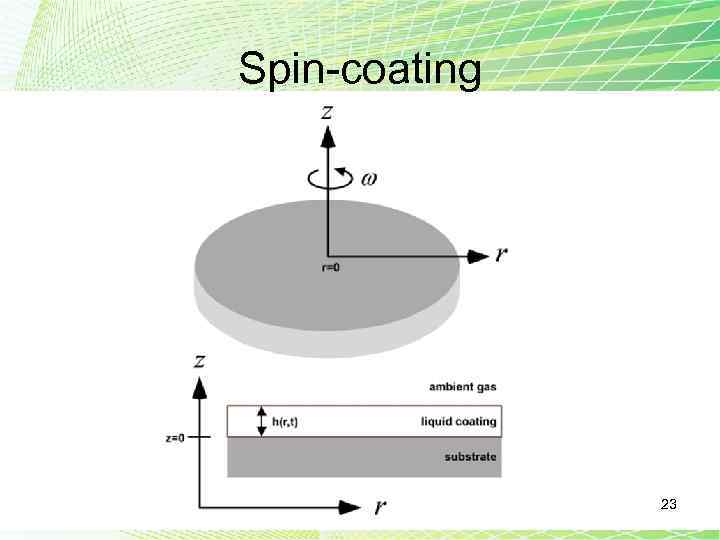 Spin-coating 23
Spin-coating 23
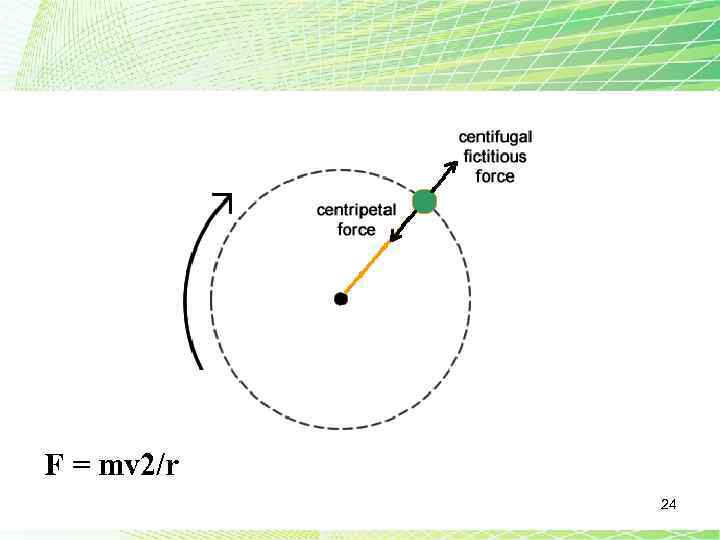 F = mv 2/r 24
F = mv 2/r 24
 Методом центрифугирования наносят слои полимера, толщины которых колеблются в пределах от нескольких нанометров до десятков микрон. При вращении центрифуги с большой частотой происходит испарение растворителя, и вязкость полимера быстро возрастает. Толщина нанесенного слоя hсл зависит от вязкости ν полимера и частоты вращения ω столика центрифуги, т. е. где А – коэффициент пропорциональности, определяемый опытным путем. Используя метод центрифугирования, необходимо учитывать адсорбцию и смачивание при выборе подложки. 25
Методом центрифугирования наносят слои полимера, толщины которых колеблются в пределах от нескольких нанометров до десятков микрон. При вращении центрифуги с большой частотой происходит испарение растворителя, и вязкость полимера быстро возрастает. Толщина нанесенного слоя hсл зависит от вязкости ν полимера и частоты вращения ω столика центрифуги, т. е. где А – коэффициент пропорциональности, определяемый опытным путем. Используя метод центрифугирования, необходимо учитывать адсорбцию и смачивание при выборе подложки. 25
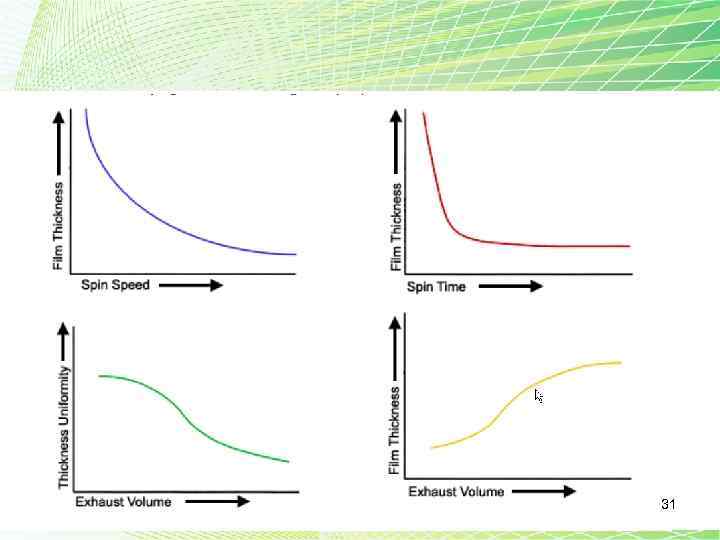
 • Центрифугирование используется уже несколько десятилетий для получения тонких пленок в интевале 10 нм (0. 5 нм) – 10 мкм. • Типичный процесс включает следующее: в центр подложки наносится раствор, Затем подложка вращается с высокой скоростью (500 -6000 оборотов в минуту). В течении от 10 с до нескольких минут • Центробежное ускорение приведет к тому, что капля растечется тонким слоем по поверхности подложки, часть раствора достигнет края подложки и удалится из нее под действием центробежных сил • Толщина пленки зависит от природы различных факторов (вязкость, скорость высыхания, процентное содержание в растворе, поверхностное натяжение и т. д. ) • Структура и толщина пленки, также будет определятся скоростью вращения, ускорением, и среды, присутствующей над раствором 26
• Центрифугирование используется уже несколько десятилетий для получения тонких пленок в интевале 10 нм (0. 5 нм) – 10 мкм. • Типичный процесс включает следующее: в центр подложки наносится раствор, Затем подложка вращается с высокой скоростью (500 -6000 оборотов в минуту). В течении от 10 с до нескольких минут • Центробежное ускорение приведет к тому, что капля растечется тонким слоем по поверхности подложки, часть раствора достигнет края подложки и удалится из нее под действием центробежных сил • Толщина пленки зависит от природы различных факторов (вязкость, скорость высыхания, процентное содержание в растворе, поверхностное натяжение и т. д. ) • Структура и толщина пленки, также будет определятся скоростью вращения, ускорением, и среды, присутствующей над раствором 26
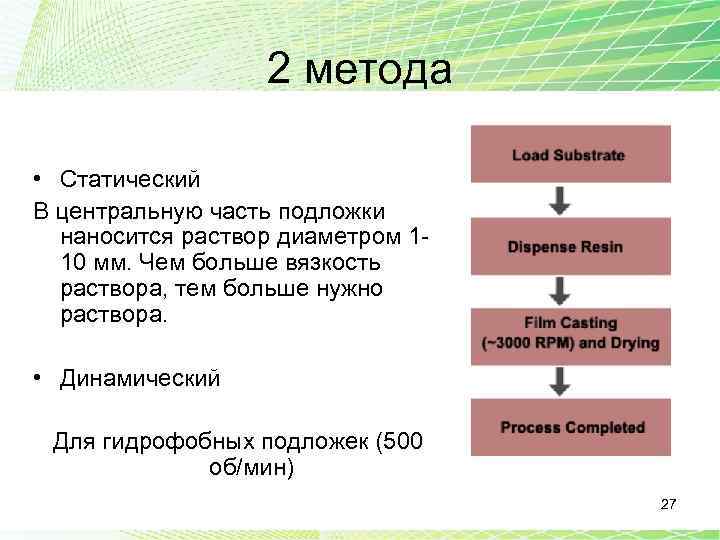 2 метода • Статический В центральную часть подложки наносится раствор диаметром 110 мм. Чем больше вязкость раствора, тем больше нужно раствора. • Динамический Для гидрофобных подложек (500 об/мин) 27
2 метода • Статический В центральную часть подложки наносится раствор диаметром 110 мм. Чем больше вязкость раствора, тем больше нужно раствора. • Динамический Для гидрофобных подложек (500 об/мин) 27
 • Скорость вращения является одним из наиболее важных факторов при формировании пленок. • От скорости вращения зависит величина центробежных сил, действующих на раствор а также скорость и характеристика вихрей, возникающих в воздушном пространстве непосредственно над подложкой. • Относительно незначительные изменения 28 • ± 50 об/мин на этом этапе может
• Скорость вращения является одним из наиболее важных факторов при формировании пленок. • От скорости вращения зависит величина центробежных сил, действующих на раствор а также скорость и характеристика вихрей, возникающих в воздушном пространстве непосредственно над подложкой. • Относительно незначительные изменения 28 • ± 50 об/мин на этом этапе может
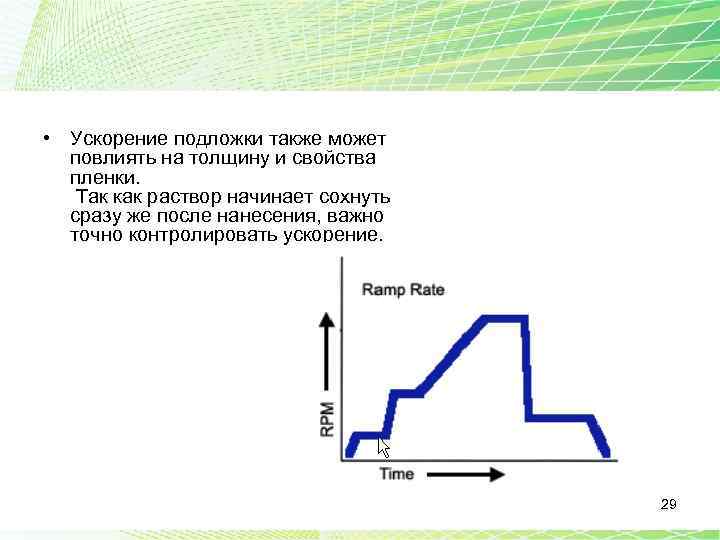 • Ускорение подложки также может повлиять на толщину и свойства пленки. Так как раствор начинает сохнуть сразу же после нанесения, важно точно контролировать ускорение. 29
• Ускорение подложки также может повлиять на толщину и свойства пленки. Так как раствор начинает сохнуть сразу же после нанесения, важно точно контролировать ускорение. 29
 • Испарение 30
• Испарение 30
 31
31
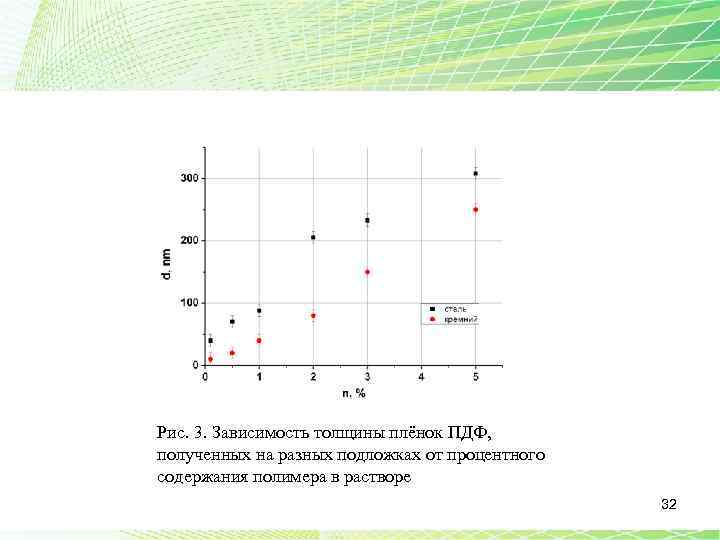 Рис. 3. Зависимость толщины плёнок ПДФ, полученных на разных подложках от процентного содержания полимера в растворе 32
Рис. 3. Зависимость толщины плёнок ПДФ, полученных на разных подложках от процентного содержания полимера в растворе 32
 33
33
 34
34
 35
35
 36
36
 Приготовление раствора с заданным содержанием растворенного вещества 37
Приготовление раствора с заданным содержанием растворенного вещества 37
 38
38
 39
39
 Основные характеристики • 1. Скорость вращения : 500 -6000 об/мин (rpm) • 2. Скорость набора номинальной частоты вращения (ускорение) • 3. Отвод/контроль окружающей атмосферы • 4. Статичность/динамичность 40
Основные характеристики • 1. Скорость вращения : 500 -6000 об/мин (rpm) • 2. Скорость набора номинальной частоты вращения (ускорение) • 3. Отвод/контроль окружающей атмосферы • 4. Статичность/динамичность 40
 Д. материалы 41
Д. материалы 41
 • Вя зкость (вну треннее тре ние) — одно из явлений переноса, свойство текучих тел (жидкостей и газов) оказывать сопротивление перемещению одной их части относительно другой. Механизм внутреннего трения в жидкостях и газах заключается в том, что хаотически движущиеся молекулы переносят импульс из одного слоя в другой, что приводит к выравниванию скоростей — это описывается введением силы 42 трения.
• Вя зкость (вну треннее тре ние) — одно из явлений переноса, свойство текучих тел (жидкостей и газов) оказывать сопротивление перемещению одной их части относительно другой. Механизм внутреннего трения в жидкостях и газах заключается в том, что хаотически движущиеся молекулы переносят импульс из одного слоя в другой, что приводит к выравниванию скоростей — это описывается введением силы 42 трения.
 Конформации макромолекул Конформация – форма расположения макромолекулы в пространстве, 43
Конформации макромолекул Конформация – форма расположения макромолекулы в пространстве, 43
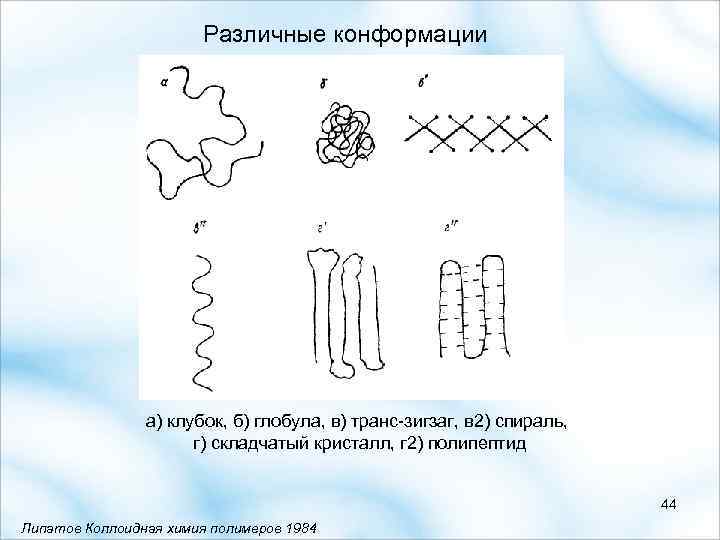 Различные конформации а) клубок, б) глобула, в) транс-зигзаг, в 2) спираль, г) складчатый кристалл, г 2) полипептид 44 Липатов Коллоидная химия полимеров 1984
Различные конформации а) клубок, б) глобула, в) транс-зигзаг, в 2) спираль, г) складчатый кристалл, г 2) полипептид 44 Липатов Коллоидная химия полимеров 1984
 Формирование тонких пленок зависит от величины сил: • адсорбции, (раствор-подложка) • когезии, (между макромолекулами и молекулами растворителя) • поверхностного натяжения (раствор-подложка, раствор-воздух) … 45
Формирование тонких пленок зависит от величины сил: • адсорбции, (раствор-подложка) • когезии, (между макромолекулами и молекулами растворителя) • поверхностного натяжения (раствор-подложка, раствор-воздух) … 45
 Механизмы адсорбции Адсорбция — процесс сгущения растворенного вещества на поверхности раздела фаз Разбавленные растворы а) адсорбированная петлями цепь б) адсорбированный клубок Умеренные растворы в) взаимодействующие клубки г) агрегат клубков 46 Липатов Ю. С. Коллоидная химия полимеров 1984
Механизмы адсорбции Адсорбция — процесс сгущения растворенного вещества на поверхности раздела фаз Разбавленные растворы а) адсорбированная петлями цепь б) адсорбированный клубок Умеренные растворы в) взаимодействующие клубки г) агрегат клубков 46 Липатов Ю. С. Коллоидная химия полимеров 1984
 Когезия – взаимодействие макромолекул полимера между собой и молекулами растворителя. Сильно проявляется для умеренно концентрированных и концентрированных растворов. При агрегативном механизме адсорбции проявляется в поперечном сжатии агрегатов и клубков Поверхностное натяжение – связано со стремлением тела принять форму с минимальной площадью поверхности На границе «раствор-воздух» приводит к разворачиванию клубков На границе «раствор-подложка» приводит к адсорбции цепей петлями для разбавленных растворов 47 Липатов Коллоидная химия полимеров 1984
Когезия – взаимодействие макромолекул полимера между собой и молекулами растворителя. Сильно проявляется для умеренно концентрированных и концентрированных растворов. При агрегативном механизме адсорбции проявляется в поперечном сжатии агрегатов и клубков Поверхностное натяжение – связано со стремлением тела принять форму с минимальной площадью поверхности На границе «раствор-воздух» приводит к разворачиванию клубков На границе «раствор-подложка» приводит к адсорбции цепей петлями для разбавленных растворов 47 Липатов Коллоидная химия полимеров 1984
 Граница раствор-подложка Пленка Гидрофильная С малой шероховатостью Малое поверхностное натяжение Качественные, однородные пленки Гидрофобная С большой шероховатостью Большое поверхностное натяжение Неоднородные, островковые пленки 48
Граница раствор-подложка Пленка Гидрофильная С малой шероховатостью Малое поверхностное натяжение Качественные, однородные пленки Гидрофобная С большой шероховатостью Большое поверхностное натяжение Неоднородные, островковые пленки 48
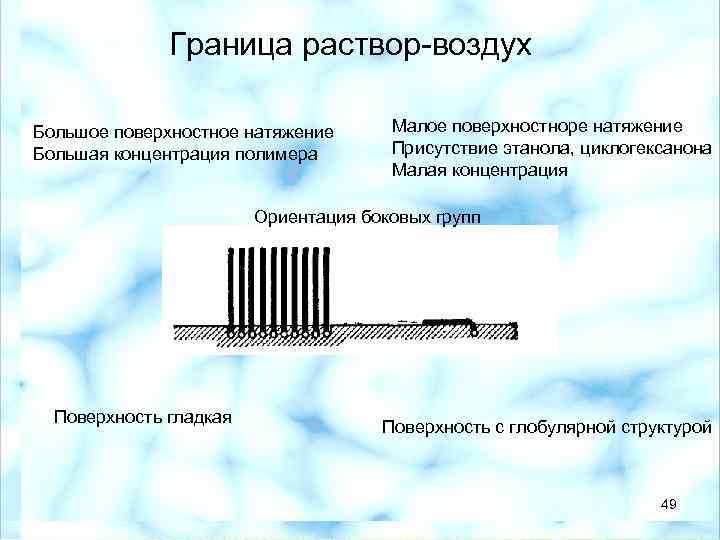 Граница раствор-воздух Большое поверхностное натяжение Большая концентрация полимера Малое поверхностноре натяжение Присутствие этанола, циклогексанона Малая концентрация Ориентация боковых групп Поверхность гладкая Поверхность с глобулярной структурой 49
Граница раствор-воздух Большое поверхностное натяжение Большая концентрация полимера Малое поверхностноре натяжение Присутствие этанола, циклогексанона Малая концентрация Ориентация боковых групп Поверхность гладкая Поверхность с глобулярной структурой 49
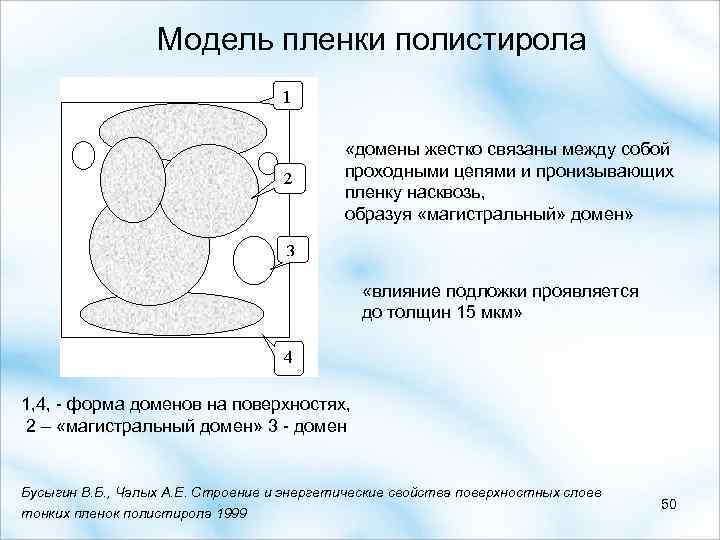 Модель пленки полистирола «домены жестко связаны между собой проходными цепями и пронизывающих пленку насквозь, образуя «магистральный» домен» «влияние подложки проявляется до толщин 15 мкм» 1, 4, - форма доменов на поверхностях, 2 – «магистральный домен» 3 - домен Бусыгин В. Б. , Чалых А. Е. Строение и энергетические свойства поверхностных слоев тонких пленок полистирола 1999 50
Модель пленки полистирола «домены жестко связаны между собой проходными цепями и пронизывающих пленку насквозь, образуя «магистральный» домен» «влияние подложки проявляется до толщин 15 мкм» 1, 4, - форма доменов на поверхностях, 2 – «магистральный домен» 3 - домен Бусыгин В. Б. , Чалых А. Е. Строение и энергетические свойства поверхностных слоев тонких пленок полистирола 1999 50
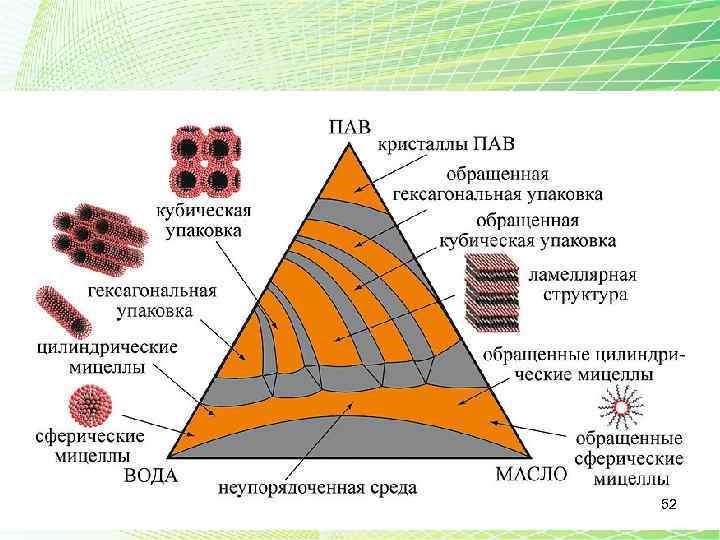
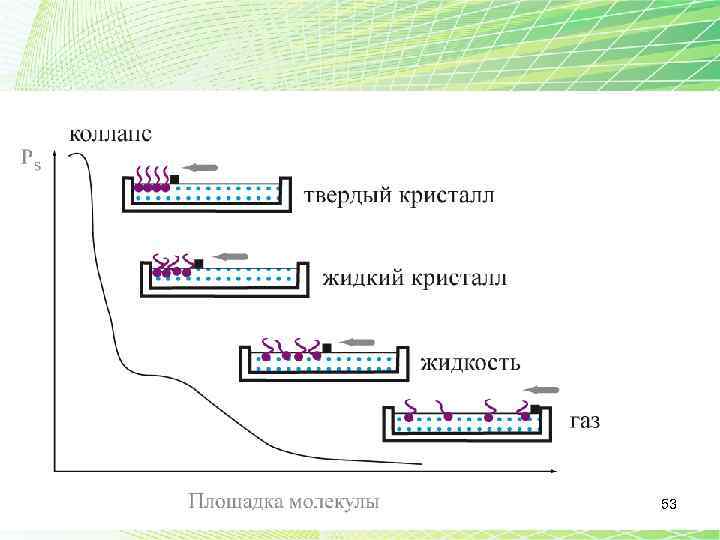
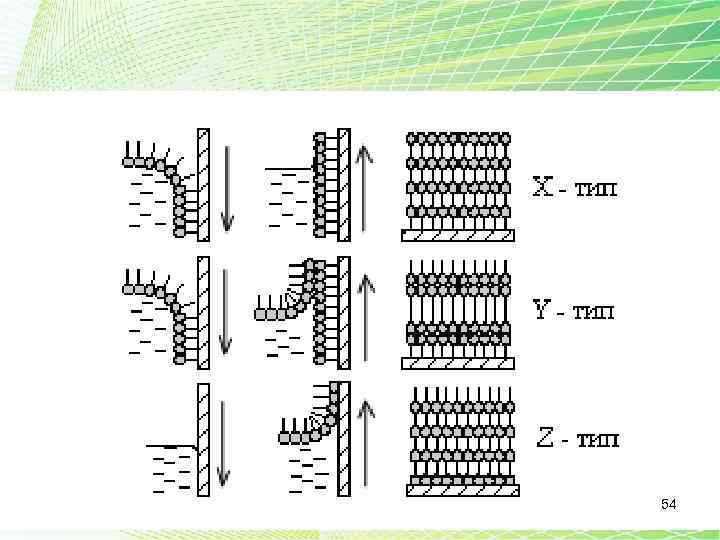
 ЛБП • Ленгмюра–Блоджетт, технология иначе пленки Ленгмюра– Блоджетт; метод Ленгмюра–Блоджетт (англ. Langmuir–Blodgett method сокр. , LB) —технология получения моно- и мультимолекулярных пленок путем переноса наповерхность твердой подложки пленок Ленгмюра (монослоев амфифильныхсоединений, образующихся на поверхности жидкости). Амфифильность (иначе дифильность) — свойство молекул веществ (как правило, органических), обладающих одновременно лиофильными (в частности, гидрофильными) и лиофобными (гидрофобными) свойствами. 51
ЛБП • Ленгмюра–Блоджетт, технология иначе пленки Ленгмюра– Блоджетт; метод Ленгмюра–Блоджетт (англ. Langmuir–Blodgett method сокр. , LB) —технология получения моно- и мультимолекулярных пленок путем переноса наповерхность твердой подложки пленок Ленгмюра (монослоев амфифильныхсоединений, образующихся на поверхности жидкости). Амфифильность (иначе дифильность) — свойство молекул веществ (как правило, органических), обладающих одновременно лиофильными (в частности, гидрофильными) и лиофобными (гидрофобными) свойствами. 51
 52
52
 53
53
 54
54


