Структурообразование в дисперсных системах Рахимбердинова Асель ХТОВ-202


Структурообразование в дисперсных системах Рахимбердинова Асель ХТОВ-202 1

Коллоидная химия – наука о поверхностных явлениях и дисперсных системах. Поверхностные явления – совокупность явлений, связанных с физическими особенностями границ раздела между соприкасающимися фазами. Дисперсные системы – гетерогенные системы, в которых одна из фаз находится в дисперсном (раздробленном состоянии). Дисперсная система Дисперсная фаза Дисперсионная среда (раздробленная часть (непрерывная часть дисперсной системы) 2

Особенности коллоидных систем 1. Избыточная поверхностная энергия GS При увеличении дисперсности увеличивается удельная поверхность частиц дисперсной фазы, большая часть всех молекул или атомов находится на поверхности раздела фаз в несимметричном силовом поле, что приводит к возникновению избыточной поверхностной энергии. 2. Невоспроизводимость (индивидуальность) 3. Термодинамическая неустойчивость 4. Способность к структурообразованию 3

СТРУКТУРООБРАЗОВАНИЕ в дисперсных системах , самопроизвольное соединение частиц дисперсной фазы и их агрегатов в пространственные структуры. Наблюдается в системах с твердой дисперсной фазой и жидкой или газовой дисперсионной средой (суспензии, золи, латексы, биологические системы, порошки и т. п. ) Оно приводит к образованию пространственного структурного каркаса и возникновению структурной вязкости или отверждению системы. 4

Дисперсная система Свободнодисперсная Связнодисперсные (неструктурированная) (структурированные) бесструктурные системы, в обладают определенной которых частицы дисперсной структурой; частицы связаны фазы почти не связаны друг с между собой, не способны к другом и способны независимо взаимному перемещению и могут перемещаться под влиянием совершать лишь колебательные теплового движения или силы движения. тяжести. 5
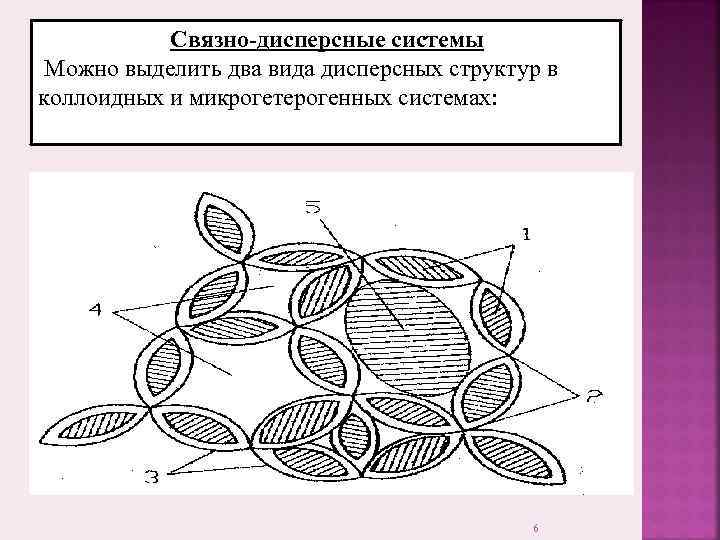
Связно-дисперсные системы Можно выделить два вида дисперсных структур в коллоидных и микрогетерогенных системах: 6

7

Коагуляционные структуры К ним относятся структуры, обычно возникающие в результате понижения агрегативной устойчивости дисперсных систем. Частицы, слипаясь, образуют пространственную сетку, в петлях которой находится дисперсионная среда (рис. 7. 1). Строение пространственных структур, образующихся в лиозоле при астабилизации: 1 -частицы дисперсной фазы; 2 -участки поверхности частиц, лишившиеся фактора устойчивости после астабилизации; 3 -участки поверхности частиц, сохранившие фактор устойчивости; 4 -петли структуры, заполненные дисперсионной средой 8

Коагуляция – явление слипания коллоидных частиц и выпадения их в осадок – наблюдается при нейтрализации зарядов этих частиц, когда в коллоидный раствор добавляют электролит. При этом раствор превращается в суспензию или гель. Некоторые органические коллоиды коагулируют при нагревании (клей, яичный белок) или при изменении кислотно - щелочной среды раствора.

Коагуляция коллоидных растворов может быть вызвана различными факторами: 1) прибавлением электролитов; 2) нагреванием или замораживанием; 3) механическим воздействием; 4) высокочастотными колебаниями; 5) ультрацентрифугированием. 10

Строение коллоидных мицелл Мицелла – частица дисперсной фазы вместе с ДЭС. Внутренняя часть мицеллы - агрегат , состоящий из большого числа молекул или атомов м. р. с. Агрегат электронейтрален, но адсорбирует на своей поверхности ионы из раствора – ПОИ. Правило Фаянса-Пескова: «На твердой поверхности агрегата в первую очередь адсорбируются ионы, которые: • входят в состав агрегата; • способны достраивать кристаллическую решетку агрегата; • образуют малорастворимое соединение с ионами агрегата; • изоморфны с ионами агрегата. » 11

Агрегат вместе с ПОИ составляет ядро мицеллы. Заряженное ядро мицеллы, притягивает ПИ из раствора. Часть ПИ образует адсорбционный слой. Ядро с ПИ плотной части ДЭС образуют гранулу или коллоидную частицу. Знак заряда коллоидной частицы определяется знаком заряда ПОИ. Коллоидную частицу окружают ПИ диффузной слоя – остальная часть ПИ, подвергающихся броуновскому движению и менее прочно связанная с ядром. В целом образуется мицелла. Мицелла в отличие от коллоидной частицы электронейтральна. 12

Коагуляция золей электролитами Правила электролитной коагуляции • Все электролиты при определенной концентрации могут вызвать коагуляцию золя. • Правило знака заряда: коагуляцию золя вызывает тот ион электролита, знак заряда которого противоположен заряду коллоидной частицы. Этот ион называют ионом-коагулятором • Каждый электролит по отношению к коллоидному раствору обладает порогом коагуляции (коагулирующей способностью). 13

Порог коагуляции (γ, Скр) – наименьшая концентрация электролита, достаточная для того, чтобы вызвать коагуляцию золя Коагулирующая способность (Р) – величина, обратная порогу коагуляции • Влияние заряда иона-коагулятора (правило Шульце-Гарди): коагулирующая способность электролита возрастает с увеличением заряда иона – коагулятора n = 2 ÷ 6 14

ь Гели. В определенных условиях коагуляция (явление слипания коллоидных частиц и выпадения их в осадок) золей приводит к образованию студенистой массы, называемой гелем. В этом случае вся масса коллоидных частиц, связывая растворитель, переходит в своеобразное полужидкое-полутвердое состояние. - желатин, желе, мармелад. 15
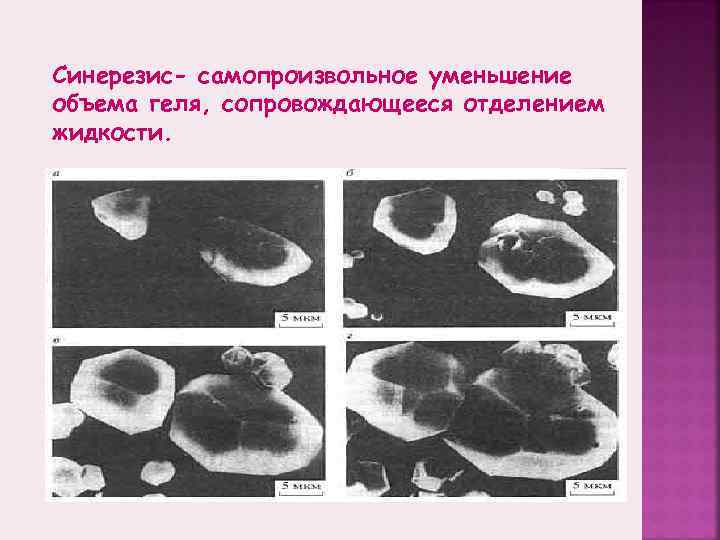
Синерезис- самопроизвольное уменьшение объема геля, сопровождающееся отделением жидкости.
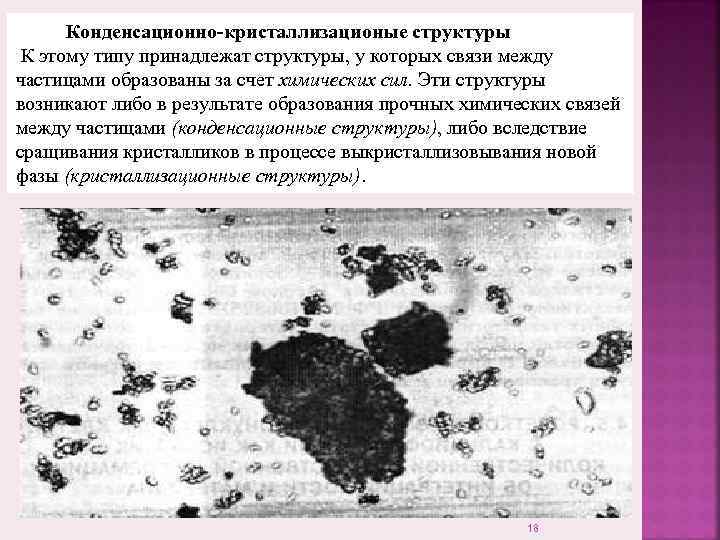
Конденсационно-кристаллизационые структуры К этому типу принадлежат структуры, у которых связи между частицами образованы за счет химических сил. Эти структуры возникают либо в результате образования прочных химических связей между частицами (конденсационные структуры), либо вследствие сращивания кристалликов в процессе выкристаллизовывания новой фазы (кристаллизационные структуры). 18
Конденсационно-кристаллизационные структуры присущи натуральным продуктам, однако они могут образовываться из коагуляционных при удалении дисперсионной среды или срастания частиц дисперсной фазы в расплавах или растворах 19

Основные отличительные признаки структур такого типа: 1. большая прочность по сравнению с прочностью коагуляционных структур, что обусловлено высокой прочностью контактов между частицами; 2. отсутствие тиксотропии и необратимый характер разрушения; 3. Большая хрупкость и упругость из-за жесткости скелета структуры; 4. наличие внутренних напряжений, возникающих в процессе образования фазовых контактов и вызывающих в дальнейшем перекристаллизацию и самопроизвольное понижение прочности вплоть до нарушения сплошности (например растрескивание при сушке) 20

Конденсация — это процесс, противоположный испарению. При испарении жидкость превращается в газ или пар, а при конденсации — наоборот: газ или пар переходят в жидкое или твердое состояние. Конденсация протекает, когда объем газа или пара сжимается или охлаждается. Кристаллиза ция — процесс фазового перехода вещества из жидкого состояния в твёрдое кристаллическое с образованием криссталлов. Фазой называется однородная часть термодинамической системы отделённая от других частей системы(других фаз) поверхностью раздела, при переходе через которую химический состав, структура и свойства вещества изменяются скачками. 21

Конденсационные методы: • основаны на ассоциации молекул в агрегаты из истинных растворов; • используют для получения высокодисперсных систем; • не требуют затраты внешней работы; • появление новой фазы происходит при пересыщении среды. 22

ь Золи получают дисперсионными и конденсационными методами. Диспергирование чаще всего производят при помощи особых “коллоидных мельниц”. При конденсационном методе коллоидные частицы образуются за счет объединения атомов или молекул в агрегаты. При протекании многих химических реакций также происходит конденсация и образуются высокодисперсные системы (выпадение осадков, протекание гидролиза, окислительно- восстановительные реакции и т. д. ) - кровь, лимфа… 23

Золи.

Стадии конденсации 1. Зародышеобразование - возникновение центров кристаллизации в пересыщенном растворе; зародыши образуются тем легче, чем больше чужеродных частиц. 2. Рост зародышей. 3. Формирование слоя стабилизатора (ДЭС). 25

Физические конденсационные методы 1. Метод замены растворителя – раствор вещества приливают к жидкости, в которой это вещество практически не растворимо. Получение гидрозолей серы, холестерина 2. Метод конденсации из паров – образование тумана в газовой фазе при понижении температуры. Образование облаков, тумана, производство H 2 SO 4 26

Химические конденсационные методы Методы основаны на образовании м. р. с. в результате протекания химических реакций. 1. Реакции восстановления (получение золей Au, Ag, Pt). Восстановление аурата натрия формальдегидом. 2 Na. Au. O 2 + 3 HCOH + Na 2 CO 3 = 2 Au + 3 HCOONa +Na. HCO 3 + H 2 O Строение мицеллы : 27

2. Реакции окисления Образование золя серы. 2 H 2 Sр-р + O 2 = 2 S ↓+ 2 H 2 O Строение мицеллы: 28

3. Реакции обмена. Получение золя иодида серебра. Ag. NO 3 + KJ(изб. ) = Ag. J↓ + KNO 3 Строение мицеллы: 29

4. Реакции гидролиза Получение золя гидроксида железа. Fe. Cl 3 + 3 H 2 O = Fe(OH)3 ↓ + 3 HCl Cтроение мицеллы: 30
Коллоидные системы.ppt
- Количество слайдов: 29

