белки и инженерия 2003.ppt
- Количество слайдов: 20

Структурный анализ белков, принципы кристаллографии и наномагнитного резонанса. Рекомбинантные белки и белковая инженерия растений. Подготовили: Маковицкая Мария, Притько Ольга
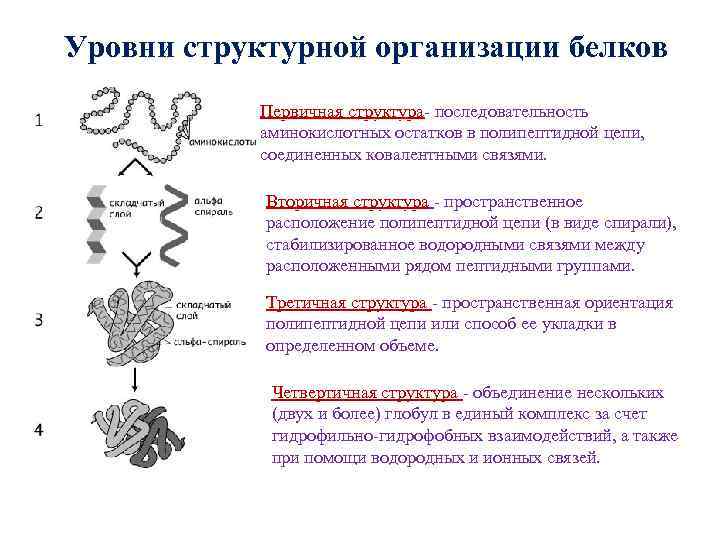
Уровни структурной организации белков Первичная структура- последовательность структура аминокислотных остатков в полипептидной цепи, соединенных ковалентными связями. Вторичная структура - пространственное расположение полипептидной цепи (в виде спирали), стабилизированное водородными связями между расположенными рядом пептидными группами. Третичная структура - пространственная ориентация полипептидной цепи или способ ее укладки в определенном объеме. Четвертичная структура - объединение нескольких (двух и более) глобул в единый комплекс за счет гидрофильно-гидрофобных взаимодействий, а также при помощи водородных и ионных связей.
Методы структурного анализа белков Физические методы позволяющие изучать структуру молекул с разным пространственным разрешением Рентгеновская кристаллография ПЭМ - просвечивающая электронная микроскопия ЯМР - ядерномагнитный резонанс ПМР - парамагнитный резонанс
Наиболее часто используемым методом для установления пространственной структуры белковых молекул является Рентгеновская кристаллография Ядерный магнитный резонанс

Метод рентгеноструктурного анализа кристаллов Он основан на том, что всякое вещество обладает способностью рассеивать падающее на него излучение, в том числе рентгеновское. При этом рассеяние рентгеновских лучей кристаллами находится в определенном соответствии с расположением атомов в кристалле. Особенность метода: выяснить не только очередность связи атомов друг с другом, но и их пространственное расположение, а также некоторые тонкости строения, трудно устанавливаемые иными путями. Рентгеновский метод позволяет надежно определять молекулярные веса белков; для этого необходимы хорошо образованные кристаллы белков, дающие возможность получать хорошие снимки. Рентгеноструктурный анализ применим только для хорошо кристаллизующихся белков.
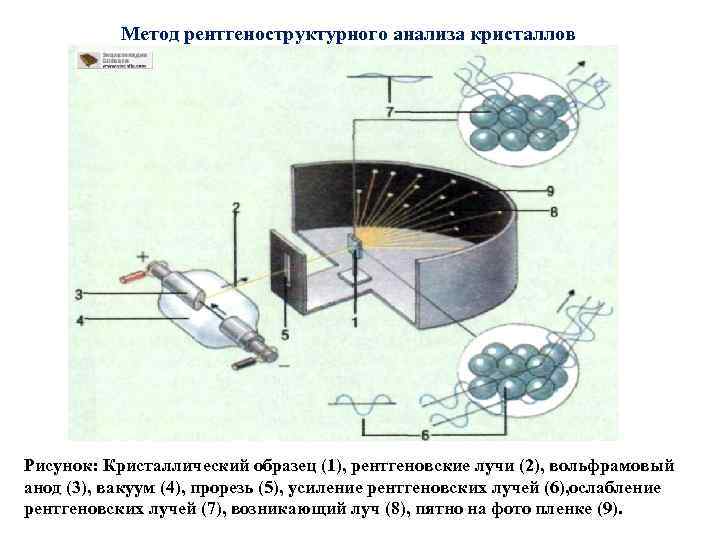
Метод рентгеноструктурного анализа кристаллов Рисунок: Кристаллический образец (1), рентгеновские лучи (2), вольфрамовый анод (3), вакуум (4), прорезь (5), усиление рентгеновских лучей (6), ослабление рентгеновских лучей (7), возникающий луч (8), пятно на фото пленке (9).

Кристаллы белка встречаются в ядрах, пластидах, в хромопластах (кристаллы каротина). Много кристаллов скапливается в отмерших клетках листьев и коры. Форма и расположение кристаллов специфичны для ряда растений, что может иметь значение для их систематики. Кристаллы в клетках растений: а - простой кристалл; б и в - друзы (сростки кристаллов).
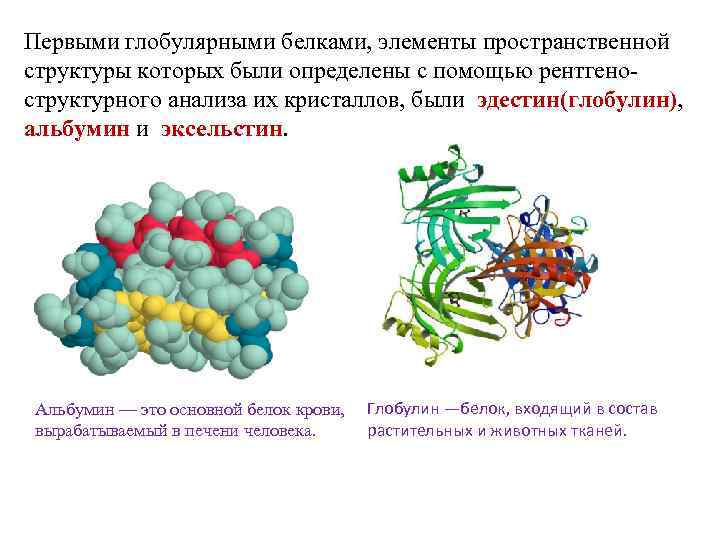
Первыми глобулярными белками, элементы пространственной структуры которых были определены с помощью рентгеноструктурного анализа их кристаллов, были эдестин(глобулин), альбумин и эксельстин. Альбумин — это основной белок крови, вырабатываемый в печени человека. Глобулин —белок, входящий в состав растительных и животных тканей.

Ядерный магнитный резонанс (ЯМР) - резонансное поглощение или излучение электромагнитной энергии веществом, содержащим ядра с ненулевым спином во внешнем магнитном поле, на частоте ν (называемой частотой ЯМР), обусловленное переориентацией магнитных моментов ядер. ЯМР основано: на изучении магнитных явлений, возникающих при поглощении электромагнитной энергии атомными ядрами с ненулевым спином. Преимущества ЯМР: • Работает на белках для которых невозможно получить кристаллы, в отличии от метода рентгено-кристаллографии. • Может изучать естественную динамику белка. Общая задача ЯМР: является получение 3 -мерной структуры белка в высоком разрешении, подобно изображениям получаемым в рентгеновской кристаллографии.

Работает ЯМР так: • На раствор молекул действуют магнитным полем. • Ядра атомов при этом работают (особенно ядра атомов водорода) как гироскопы. • Параметры, при которых ядра вращаются, зависят от магнитного поля в данной позиции, а это зависит от позиции и химических особенностей других атомов-соседей. • Исследователи могут понять по анализу получаемых данных, как разные ядра атомов располагаются друг относительно друга. Как правило, анализируют три типа данных: • химические сдвиги (они зависят от атомов в ближайшем окружении); • остаточное дипольное взаимодействие (на которое влияют химические связи); • эффект Оверхаузера (интерпретирует некоторые химические сдвиги).

Возможности метода ЯМР • С помощью современных методов ЯМР удается установить структуру высокого разрешения биомолекул. • Позволяет определять строение биомолекул в водном растворе – естественной среде их функционирования. • Является единственным экспериментальным методом, позволяющим определять динамические свойства биомолекул с атомным разрешением в шкале времени от пикосекунд до часов. • Позволяют изучать взаимодействия белков с другими белками, ДНК, ионами металлов и низкомолекулярными лигандами. • Применяется для установления строения липидных мембран и их проницаемости.

Рекомбинантные белки и белковая инженерия растений.

• Белковая инженерия — совокупность генноинженерных и биохимических методов, с помощью которых создают рекомбинантные белки и осуществляют модификацию физико-химических или биологических свойств природных белков с целью улучшения их качества. Примером методов, используемых в Б. и. , является мутагенез in vitro, позволяющий изменять кодирующую способность гена в определенном месте. • Рекомбинантный белок - белок, состоящий из аминокислотных последовательностей различных природных белков, полученный с помощью технологии рекомбинантных ДНК.

Что же может белковая инженерия и какие свойства белков изменяют белковые инженеры? 1. улучшать термостабильность 2. улучшать стабильность к органическим растворителям 3. изменять лиганд-связывающие свойства 4. получать химерные и полифункциональные белки, белки с «тагами» • 5. решать сложные задачи по улучшению эффективности белковых лекарственных препаратов • 6. создавать совершенно новые искусственные белки с заданной структурой и свойствами. • •

Общий метод получения рекомбинантного белка
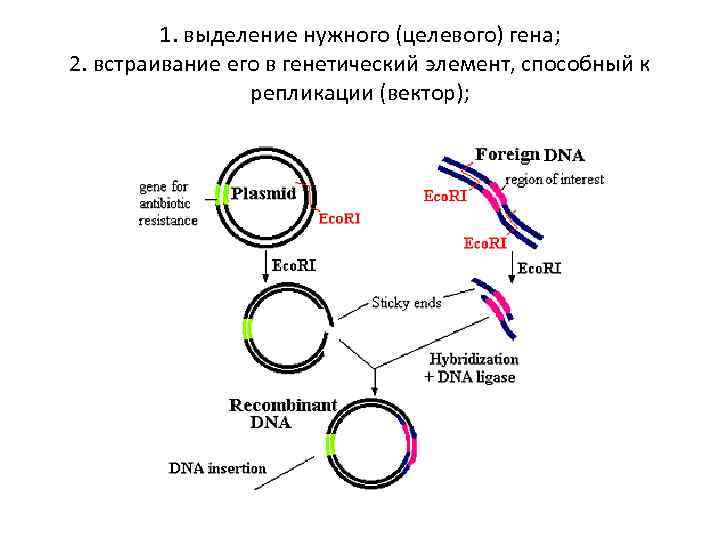
1. выделение нужного (целевого) гена; 2. встраивание его в генетический элемент, способный к репликации (вектор);
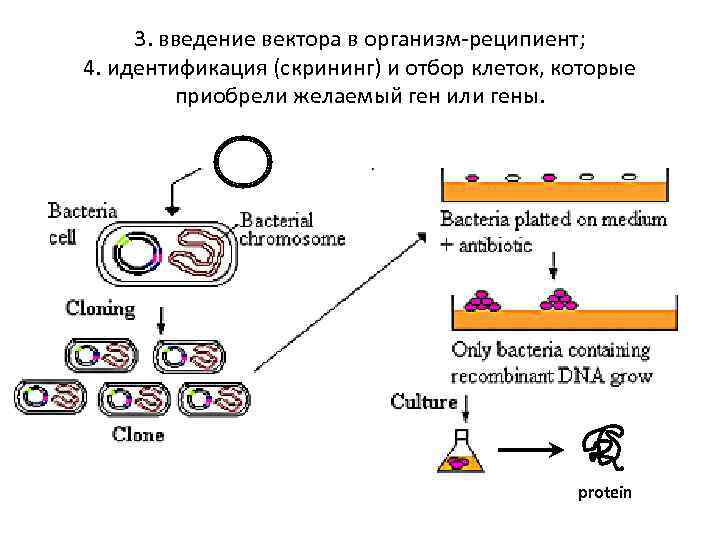
3. введение вектора в организм-реципиент; 4. идентификация (скрининг) и отбор клеток, которые приобрели желаемый ген или гены. protein

Используемые системы экспресии Клетки: - Бактерии Esherichia coli и Bacillus subtilis - Дрожжи Saccharomyces cerevisae и Pichia pastoris - Линии клеток млекопитающих CHO, BHK, A-293 -Трансгенные животные - Трансгенные растения

• • Особенности и преимущества использования трансгенных растений В клетках происходят гликозилирование и фолдинг белков, сходные с таковым в клетках млекопитающих, Культивирование растений не требует дорогостоящего оборудования, Доступность рекомбинантного препарата в количествах, достаточных для клинических испытаний и широкого терапевтического использования, Растительные клетки не содержат в своём составе патогенные для человека вирусы, а также прионы, При использовании трансгенных растений в качестве "съедобных вакцин" выделение белка в чистом виде не требуется, Перенос фрагментов экзогенной ДНК в растительный геном и регенерация у растений происходят значительно проще по сравнению с животными, Аппарат транскрипции и трансляции у растений может быть адаптирован не только для накопления гомологичных белков, не синтезируемых данным видом растения, но и для синтеза гетерологичных белков как бактериального, так и животного происхождения, Растения in vivo могут служить благоприятной средой для развития различных организмов - бактерий и вирусов, геном которых может быть модифицирован и адаптирован для синтеза соответствующих гетерологич-ных белков

Что уже имееться? Растения-продуценты антител : • Соя - Вирус простого герпеса 2 • Пшеница, рис - Терапия рака; раковый эмбриональный антиген Фармацевтические белки, полученные в трансгенных растениях • Сывороточный альбумин (табак) - Цирроз печени, ожоги, хирургия • b-интерферон (табак) - Лечение гепатитов С и В • Интерлейкин-2 (картофель) - Иммунотерапия рака • a-1 -антитрипсин (рис) - Фиброзный кистоз, кровотечени Антигены, экспрессированные в растениях: • Hbs. Ag (картофель, салат, табак) - Вирус гепатита В • Гликопротеин вируса бешенства (томаты) - Вирус бешенства
белки и инженерия 2003.ppt