Лекция 02 Аминокислоты, пептиды, белки - строение биол роль.ppt
- Количество слайдов: 78

Структура, свойства и функции аминокислот, пептидов и белков

Из огромного количества информации о белках, аминокислотах и пептидах известно, что 1. Аминокислоты - аминопроизводные низших карбоновых кислот. 2. Белки – линейные полимеры аминокислот, соединенных пептидными связями. Последнее - химически точно, но для молекулярной биологии, данных об их пространственной структуре и функциях – недостаточно! Термин белок происходит от немецкого слова «eiwei» (английское «egg whites» ), что означает яичный белок или вообще белок). Протеин – греч «протос» – первичный.

По функциональному значению аминокислоты условно можно разделить на три группы: 1. Никогда не 2. Стандартные = провходят в теиногенные = канонибелки: β-ала- ческие. Это 20 вариантов нин, орни-тин, α-аминокислот, как γ- и ωмономеров полипептида. аминомасля- На них рассчитан ные кислоты и генетический код, т. е. др. способ записи, хранения и воспроизведения наследственной информации. 3. Редкие, минорные - модификации стандартных аминокислот с помощью Е, уже после трансляции, при фолдинге полипептидов ~100.
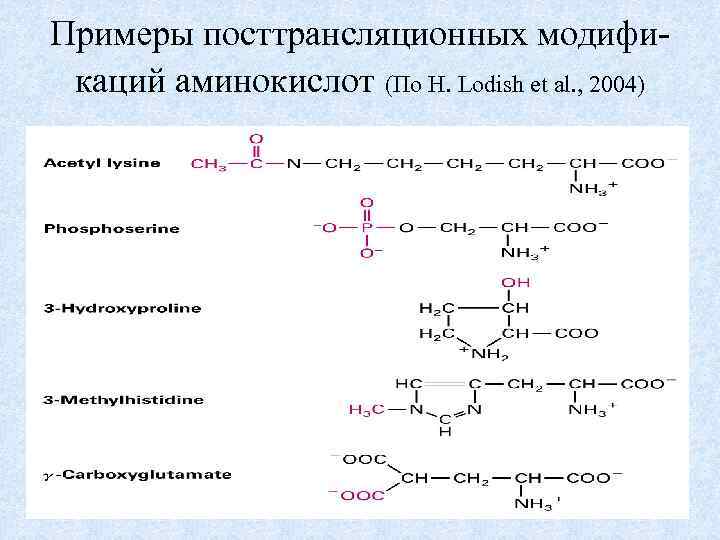
Примеры посттрансляционных модификаций аминокислот (По H. Lodish et al. , 2004) 4
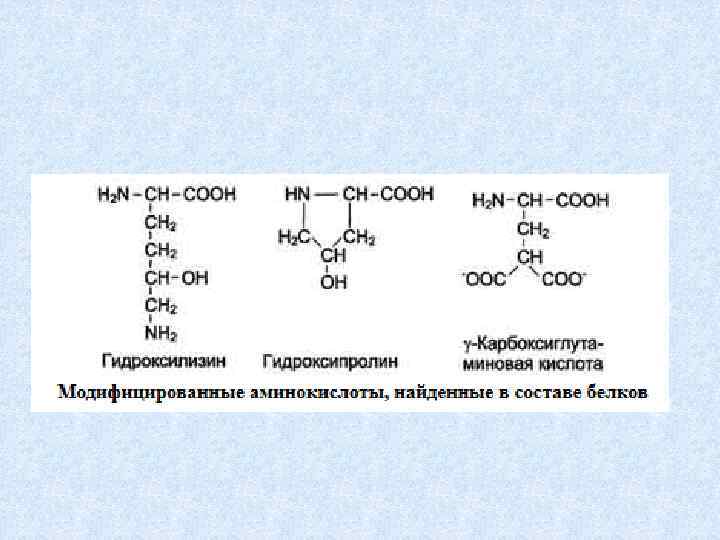
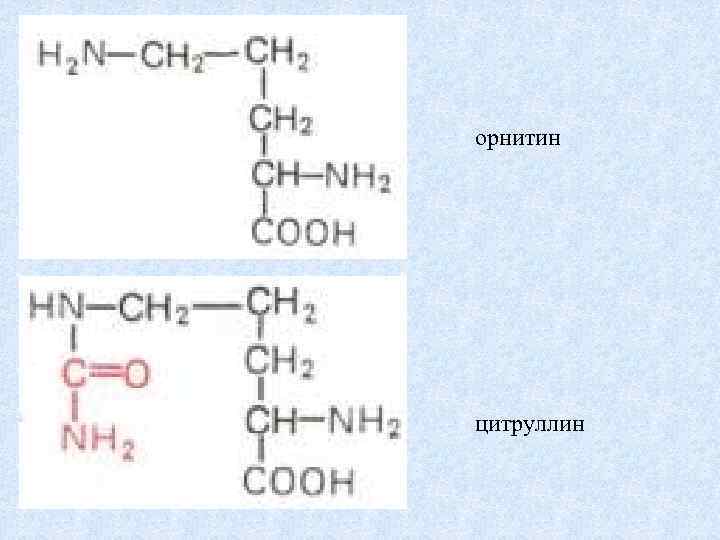
орнитин цитруллин

Биологические функции аминокислот: 1) Структурные элементы пептидов и белков; 2) Структурные элементы других природных соединений (коферментов, желчных кислот, антибиотиков, фосфолипидов и т. д. ); 3) Переносчики сигналов (нейромедиаторы или предшественники медиаторов, нейромедиаторов и гормонов); 4) Важные метаболиты (например глутаминовая кислота служит источником азота при синтезах)
Классификация протеиногенных аминокислот По химической природе радикала По степени заменимости в организме По полярности

Классификация протеиногенных аминокислот по строению радикала: 1) алифатические (глицин, аланин, валин, лейцин, изолейцин, метионин, пролин; 2) ароматические (фенилаланин, тирозин, триптофан; 3) алифатические, содержащие гидроксильную группу (серин, треонин); 4) алифатические, содержащие сульфгидрильную группу (цистеин); 5) основные (лизин, аргинин, гистидин); 6) кислые (аспарагиновая и глутаминовая кислоты); 7) алифатические, содержащие карбоксамидную группу (аспарагин, глутамин).

Аминокислоты классифицируются на заменимые и незаменимые (эссенциальные). 1. Незаменимые (эссенциальные) аминокислоты не могут синтезироваться в организме и должны поступать с пищей. Они необходимы для обеспечения и поддержания роста: аргинин, валин, гистидин, изолейцин, лизин, метионин, треонин, триптофан, фенилаланин (шесть аминокислот 1 -й группы, одна – второй и три – четвертой). 2. Заменимые аминокислоты. Организм может синтезировать около 10 аминокислот для обеспечения биологических потребностей, поэтому поступление их с пищей не обязательно (аланин, аспарагиновая кислота, цистеин, глутаминовая кислота, глутамин, глицин, пролин, серин, тирозин).

Биполярный ион аминокислоты (цвиттер-ион) На диссоциацию аминокислот оказывает влияние p. H среды. В очень кислых растворах NH 2 протонирована полностью, щелочных растворах – COOH – группа депротонирована.

Изменение суммарного заряда аминокислот в зависимости от р. Н среды

Пептиды

Пептиды: Чтение и написание пептида начинают со свободной = N -концевой Н 2 N-группы и заканчивают свободным = Сконцевым карбоксилом (СООН) • Изменение последовательности аминокислотных остатков (АКО) недопустимо, т. к. меняет свойства пептида также, как перестановка букв - смысл слова. • Зная, что молекулярные массы = М аминокислот var от 57 Да у глицина = Gly = G и до 194 Да у триптофана = Trp = W, с учетом частот их встречаемости, среднюю М АКО можно ~принять за 100 Да. Тогда, зная М пептида, можно примерно оценить в нем число АКО, и наоборот, зная его длину в АКО – найти молекулярную массу в Да. 14

Пептиды из трех - пятидесяти АКО • редко имеют стабильные конформации молекул, а потому и редко выполняют существенные биологические функции. • Устойчивость же их структурам обычно придают макроциклы и др. нестандартные модификации функциональных групп. • См. учебники, руководство Ю. А. Овчинникова, 1987 и 3 справочника О. А. Гомазкова, изданных в 90 -х гг. по > чем 600 биологически важным пептидам. 15

Примеры функционально важных пептидов: Защитные 1. Глутатион 2. Карнозин 3. Ансерин и др. Антибиотики 1. Актиномицин D 2. Грамицидины 3. Валиномицин и др. Алкалоиды Сигнальные 1. Энкефалины и эндорфины. 2. Либерины и статины 3. Гастрин, секре. Токсины и тин, брадикиантитоксины нин 1. Аманитин, 1. Эрготамин 4. Вазопрессин = 2. Мелиттин, 2. Пандамин и др. = АДГ. 3. Фаллои 5. Окситоцин 16 дин и др.
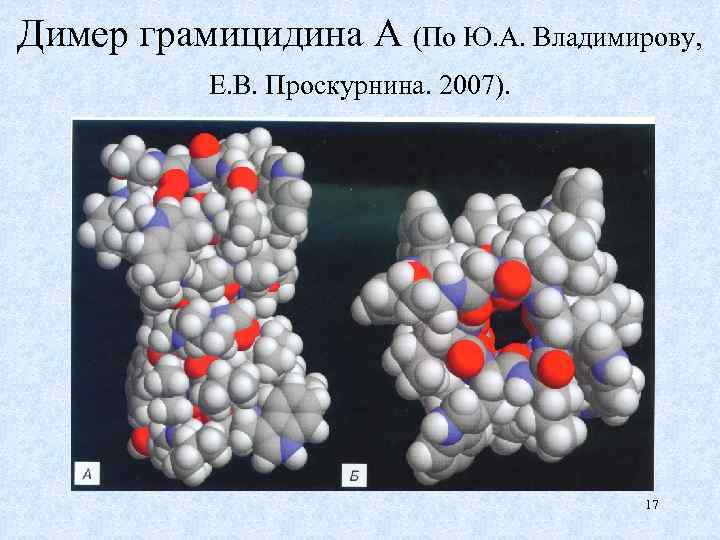
Димер грамицидина А (По Ю. А. Владимирову, Е. В. Проскурнина. 2007). 17
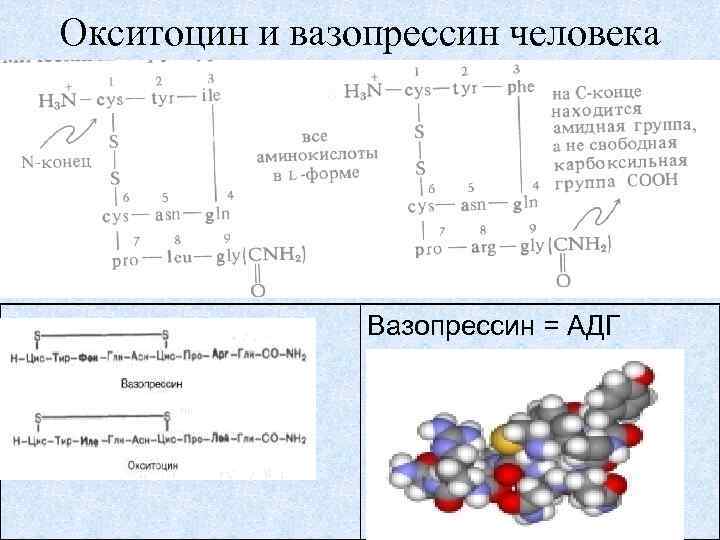
Окситоцин и вазопрессин человека Вазопрессин = АДГ 18

100 лет известны их функции стимуляции: Вазопрессин Окситоцин 1. Сокращение гладких 1. Сокращения матки при мышц, особенно стенок родах. сосудов - контроль АД. 2. Секреция молока у кормящих = лактирующих самок 2. Гораздо меньшие дозы ускоряют реабсорбцию млекопитающих. воды в почках, в связи с чем возникает сильный Но зачем этот нейромедиатор антидиуретический эфи гормон = трансмиттер фект. Поэтому его предпосекретируется всю жизнь, чтительно считать и назыв т. ч. и у самцов вать антидиуретическим позвоночных? гормоном = АДГ. 19

«В мире науки» . 2008, 8, 52 -58. Пол Зак. Нейробиология доверия. • Автор – экономист и к окситоцину шел очень кружным путем. • В 1998 г. по заказу Всемирного банка разрабаты-вал математическую модель описания социаль-ных, юридических и экономических факторов доверия. • В ходе работ его группа нашла, что в бедных стра-нах, как правило, уровень доверия низок. Ведь у жителей мало долговременных инвестиций, созда-ющих рабочие места и повышающих доходы населения. • Разработали компьютерный тест оценки доверия, стали учить этологию, а П. Зак получил второй диплом по компьютерной томографии = МРТ. 20
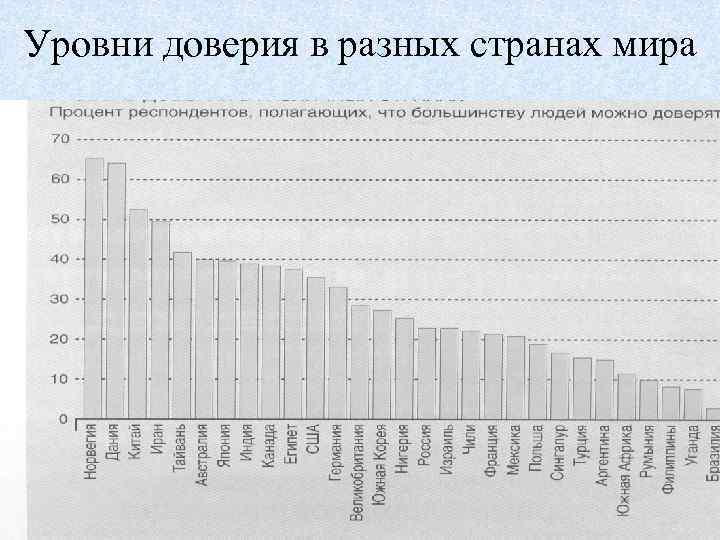
Уровни доверия в разных странах мира 21

Выяснили, что 100 млн. лет назад, у рыб появился нонапептид вазотоцин. • В период нереста = овуляции, он снижал естественный страх самки от приближения самца, чтобы плюсы генетического разнообразия от полового размножения, подавили риск стать едой для партнера. • У млекопитающих из вазотоцина возникли 2 пептида: окситоцин и Арг-вазопрессин. Видимо, тоже способствуют доверию и привязанности особей: 1. Концентрация окситоцина в крови max. при оргазме. 2. Он побуждает мышей кормить потомство и, по отрицательной обратной связи, создает у детенышей чувство привязанность к матери. 3. У самцов мышей, видов склонных к моногамии и заботе о потомстве, рецепторы к окситоцину концентрируются вблизи центра удовольствия гипоталамуса, модулируя секрецию дофамина = ДА и вознаграждая носителей за «примерное поведение» . 22 У полигамных видов, награды другие!
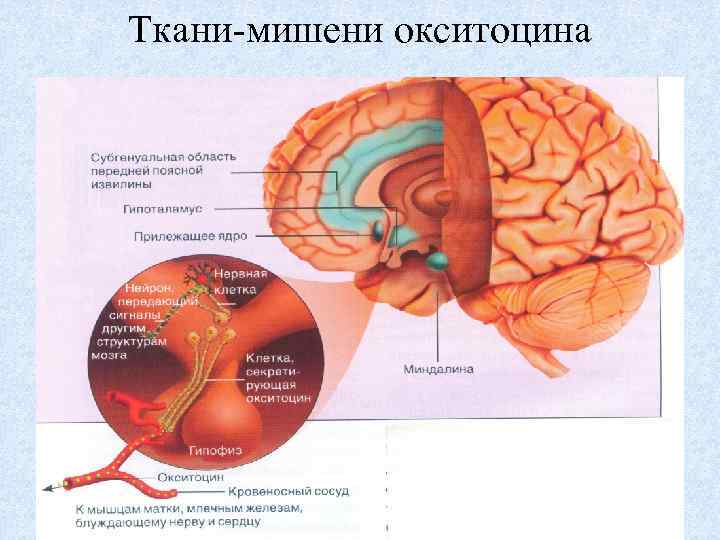
Ткани-мишени окситоцина 23

Социальные взаимодействия рушатся при разных стрессах и болезнях. Поэтому лаборатория P. Zak уже нашла, что: 1. Уровень окситоцина снижен при аутизме. Т. к. его введение не повышает числа социальных контактов, возможно аутизм связан с дисфункцией рецепторов окситоцина. 2. Больные с поражением мозга в областях, в норме богатых окситоцином, затрудняются определить, кто заслуживает их доверия.

Белки

Классификации белков До настоящего времен нет единой и стройной классификации, учитывающей различные параметры белков. В основе имеющихся классификаций обычно лежит один признак. Так, белки можно классифицировать: по форме молекул (глобулярные или фибриллярные); по молекулярной массе (низкомолекулярные, высокомолекулярные и др. ); по химическому строению (наличие или отсутствие небелковой части); по выполняемым функциям (транспортные, защитные, структурные белки и др. ); по локализации в клетке (ядерные, цито-плазматические, лизосомальные и др. ); по локализации в организме (белки крови, печени, сердца и др. ); по возможности адаптивно регулировать количество данных белков: белки, синтезирующиеся с постоянной скоростью (конститутивные), и белки, синтез которых может усиливаться при воздействии факторов среды (индуцибельные); по продолжительности жизни в клетке (от очень быстро обновляющихся белков, с Т 1/2 менее 1 ч, до очень медленно обновляющихся белков, Т 1/2 которых исчисляют неделями и месяцами); по схожим участкам первичной структуры и родственным функциям (семейства белков).

Исходя из структуры и локализации бел-ков, А. В. Финкельштейн и О. Б. Птицын (2002) поделили их на 3 класса: Фибриллярные Чаще заметны внеклеточные, напр. покровные С механической функцией Мембранные Глобулярные Пограничные = Внутри- и интегральные и внеклеточные поверхностные Избирательный = Катализ, защита, векторный транссигнализация порт, и др. сигнализация, секреция и т. д. Подробней см. : «Введение в физику белка» : http: //phys. protres. ru/lectures/protein_physics/index. html

Окончание слайда Фибриллярные Мембранные Глобулярные, Задачу быть как можно длинней и прочней, решают монотонно повторяющиеся экзоны генов, проявляясь при их экспрессии однообразными АКП = 1 o. Как внутри блоков, так и меж ними, все решают Н-связи. Регулярные трансмембранные части интегральных белков ограничены толщиной мембран (7 -10 нм). Как и у фибриллярных, эти «столбы» = «колонны» α-спиралей безводной липидной фазы прошиты Н-связями, а «петли» выступают во внешнюю/ внутреннюю водную фазу. особенно небольшие, наименее регулярны и существуют в воде. Их структуру держат гидрофобные взаимодействия углеводородных групп между отдаленными участками полипептида и/или контакты с кофактором. 28

Функции белков чрезвычайно разнообразны, но всегда • основаны на физических и высокоспецифичных взаимодействиях их молекул с лигандом, т. е. другой молекулой, комплементарной активному центру = АЦ или сайту данного белка, с которой он не только контактирует, но и «работает» = функционирует. • Как разрушение, так и небольшие изменения структуры молекул белков, могут вести к резким изменениям или утрате их активности. Отсюда и нынешняя степень аналогии: сравнение молекул белка с гибким замком, который отпирают/запирают гибким ключом. • Т. о. , для понимания функций молекул белков и др. биополимеров, нужно знать природу образования их достаточно «жестких» пространственных или трехмерных = 3 D структур, как основы стабильности и способности к самоорганизации. 29
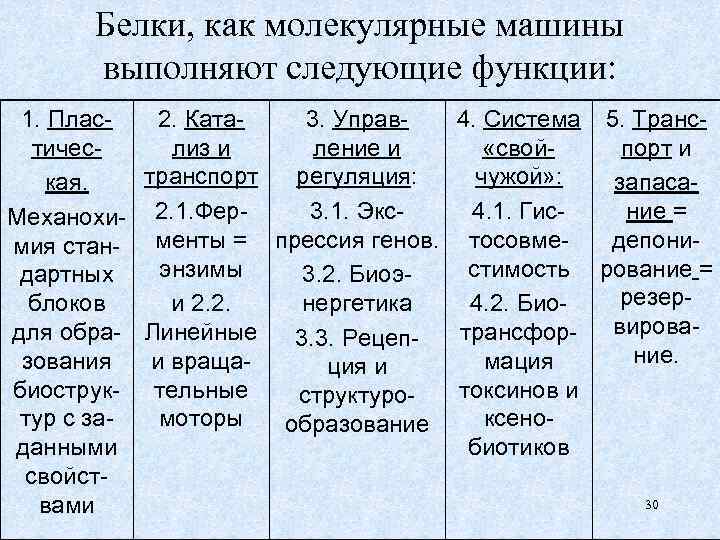
Белки, как молекулярные машины выполняют следующие функции: 1. Плас2. Ката 3. Управ 4. Система 5. Транстичеслиз и ление и «свойпорт и транспорт регуляция: чужой» : кая. запасание = 3. 1. Экс4. 1. Гис. Механохи- 2. 1. Фердепонимия стан- менты = прессия генов. тосовмеэнзимы стимость рование = дартных 3. 2. Биоэрезерблоков и 2. 2. нергетика 4. 2. Биодля обра- Линейные трансфор- вирова 3. 3. Рецепние. зования и вращамация и биострук- тельные токсинов и структуротур с замоторы ксенообразование данными биотиков свойст30 вами

Пластическую роль в клетках играют: Структурные белки: 1. Рибосом. 2. Октамеры пар гистонов Н 2 а, Н 2 b, Н 3 и Н 4, образующих кор нуклеосом, как основы хромосом. 3. Микрофиламенты из G-актина, микротрубки α- и β-тубули нов, промежуточные волокна из α-кератина цитоскелета. 4. Они же армируют биомембраны интегральными белками, а межклеточное в-во – фибриллами коллагена и эластина. 5. Создают внеклеточные структуры и защитные покровы коконов, паутины, раковин, панцирей, чешуй, перьев, волос и т. д. , о чем уже говорили. Продолжим? • О пятитомной Гистологии А. Хэм и Д. Кормак, 1982, думаю вы знаете. • Советую: Л. Г. Гарстукова, С. Л. Кузнецов, В. Г. Деревянко. 31 Наглядная гистология. М. МИА. 2008. 204 с.

1. Структурные: образуют микрофиламенты и микротрубки цитоскелета, армируют биомембраны интегральными белками, а межклеточное в-во - фибриллами коллагена и эластина. Также создают защитные покровы коконов, раковин, панцирей, чешуй, перьев, волос и др. 2. Важнейшая и почти монопольная функция белков — Е катализ химических реакций в клетках и вокруг них. 3. 1. Факторы транскрипции = МГСУ (В. Ратнер). 3. 2. Крайне многосторонняя функция: от поглощения света и до механохимических процессов аккумуляции АТФ, перемещения органоидов, клеток и свечения. 3. 3. Рецепция внутри- и межклеточных сигналов, например гормонов, интерлейкинов, факторов роста = GF и др. 4. Белки гистосовместимости и близкого им иммунитета опознают "свои" клетки, обеспечивая их правильное размещение в организмах и, связывают «чужие» молекулы и клетки. 5. Проламины и глютелины злаков; Mb – О 2; Hb – О 2 и СО 2; калбиндины – Са 2+; ферритин – железо; транскортин и секспротеин - стероидные гормоны и т. д.
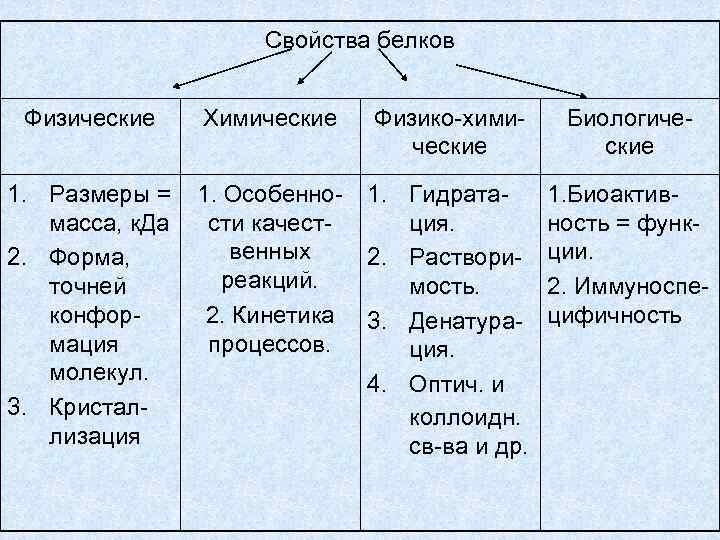
Свойства белков Физические Химические Физико-химические Биологические 1. Размеры = масса, к. Да 2. Форма, точней конформация молекул. 3. Кристаллизация 1. Особенности качественных реакций. 2. Кинетика процессов. 1. Гидратация. 2. Растворимость. 3. Денатурация. 4. Оптич. и коллоидн. св-ва и др. 1. Биоактивность = функции. 2. Иммуноспецифичность

Структура белков описывается с помощью трех уровней организации их молекул: • Первичной структурой - полипептид, в котором монотонно чередуются плоские пептидные группы NH-CO и α-С-атомы АКО. Валентные углы у каждого из α-С-атомов подвижны, как шарниры. При том, каждый из них содержит один из 20 возможных типов боковых R стандартных АКО. • К вторичные структуры - регулярные сегменты упаковки полипептида, фиксированные Н-связями разных пептидных групп. • Третичные структуры – нерегулярные, уникальные свертывания регулярных сегментов, зависящие от R АКП, фиксирующих любые слабые взаимодействия и определяющих пространственную упаковку полипептида, а та, в свою очередь, свойства и функции любого белка. Обратное — 34 неверно!

Терминология пространственной организации молекул белка (Г. Шульц и Р. Ширмер, 1982) Первичная структура полипептида = 1 о = АКП ↓ Вторичные структуры = 2 о = участки регулярной локальной упаковки фрагментов полипептида. ↓ Третичная структура = 3 о = конформация молекулы = полная упаковка полимера в пространстве. Все виды слабых взаимодействий. ↓ Четвертичная = 4 о = олигомеры субъединиц. То же ↓ Надмолекулярные ансамбли разного состава = 5 о ↓ Свойства и функции 35
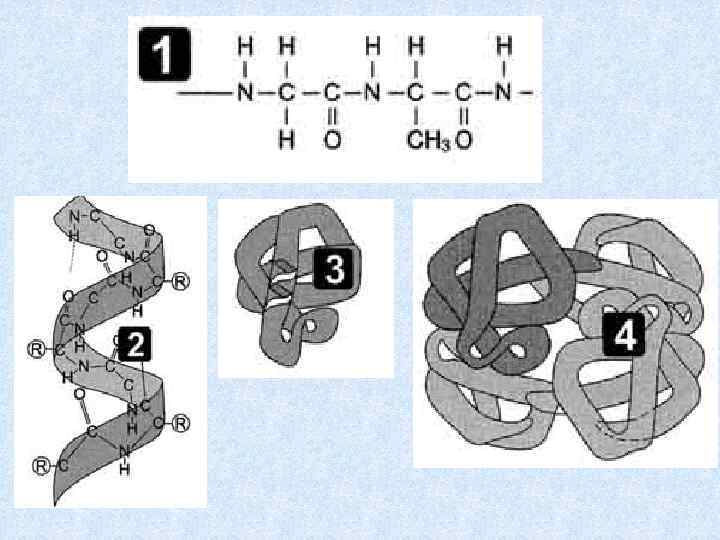

Несмотря на все различия 1 о полипептидов в длине и АКП, • В их подавляющем большинстве регулярно встречаются источники Н-связей: NH и С=О пептидных групп. Они и фиксируют отрезки «стандартных упаковок» или периодических - объемных вторичных структур, типа αспиралей или β-складок - β-слоев разной величины, предсказанных еще Л. Полингом и соавт. в 1950 г. 37

Регулярный остов полипептида: • Но это - понятие химии, его можно разместить на плоскости, а говоря о белках – подразумевают объемную структуру с биологической функцией.
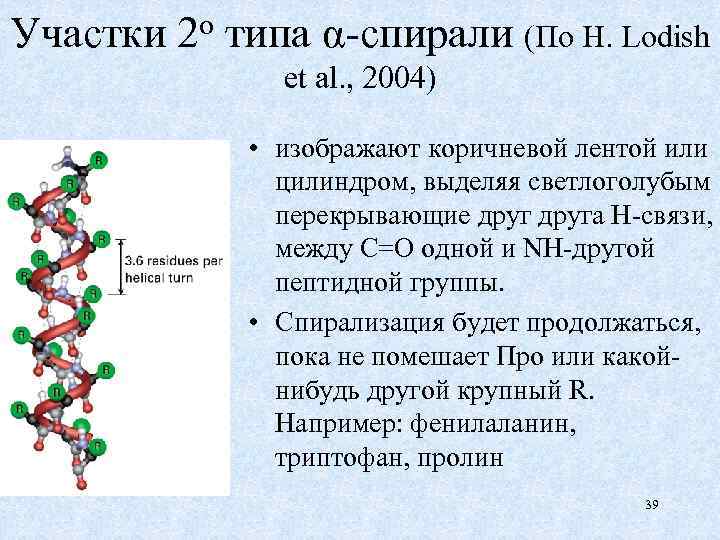
Участки 2 о типа α-спирали (По H. Lodish et al. , 2004) • изображают коричневой лентой или цилиндром, выделяя светлоголубым перекрывающие друга Н-связи, между С=О одной и NH-другой пептидной группы. • Спирализация будет продолжаться, пока не помешает Про или какойнибудь другой крупный R. Например: фенилаланин, триптофан, пролин 39
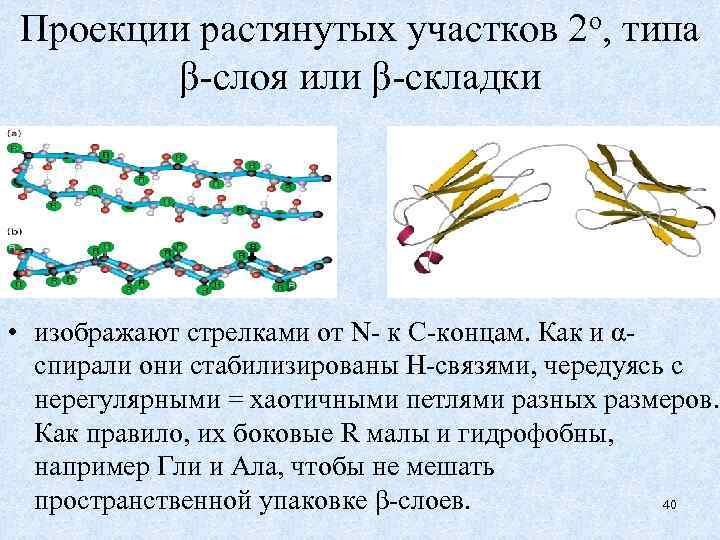
Проекции растянутых участков 2 о, типа β-слоя или β-складки • изображают стрелками от N- к С-концам. Как и αспирали они стабилизированы Н-связями, чередуясь с нерегулярными = хаотичными петлями разных размеров. Как правило, их боковые R малы и гидрофобны, например Гли и Ала, чтобы не мешать пространственной упаковке β-слоев. 40

Обычно, любой такой гидрофобный «штабель» сложен в ядро, как в • в γ-кристаллине, отвечающем за прозрачность хрусталика позвоночных. Цветом от синего к красному выделен ход полипептида: с N-конца к С-концу молекулы. • Как правило, нерегулярные петли находятся на периферии глобул и, практически никогда в них не входят, создавая за счет ионных связей, гидрофильное окружение молекул. • Попытки классификации белков на 5 типов: «чистых» α- и β- и «смешанных» : a/β, a&β и a+β ограничено применимы для малых 41 полипептидов и отдельных доменов.
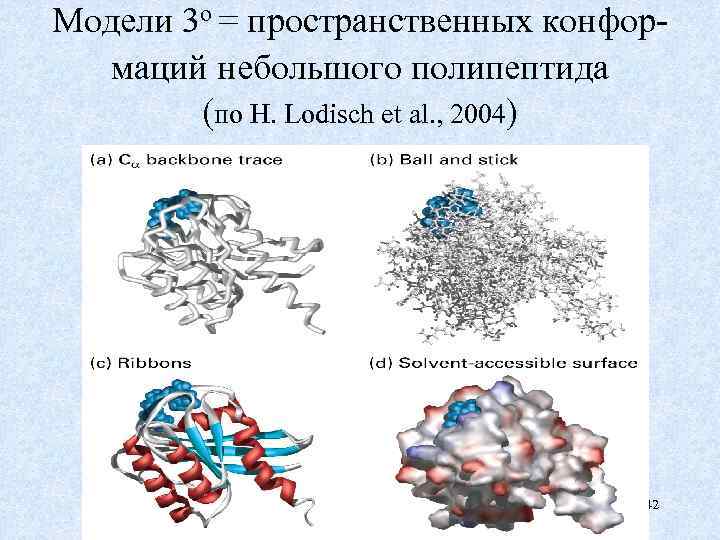
Модели 3 о = пространственных конформаций небольшого полипептида (по H. Lodisch et al. , 2004) 42

Продолжение слайда • С помощью таких моделей изучают специфику функционирования небольших (50 - 250 АКО) белков, в зависимости от геометрических и физи-ко-химических свойств поверхности их глобул. • Глядя на левую пару моделей можно думать, что внутри молекулы есть пустоты, т. е. она "мягкая". Но справа видно, что атомы упираются друг в друга, т. е. полипептид упакован плотно. • Т. о. ради удобства изучения «скелета» , 2 о и 3 о, приходится «сбривать» R глобул или делать их "прозрачными", выделяя те или иные особенности структуры полипептида. 43
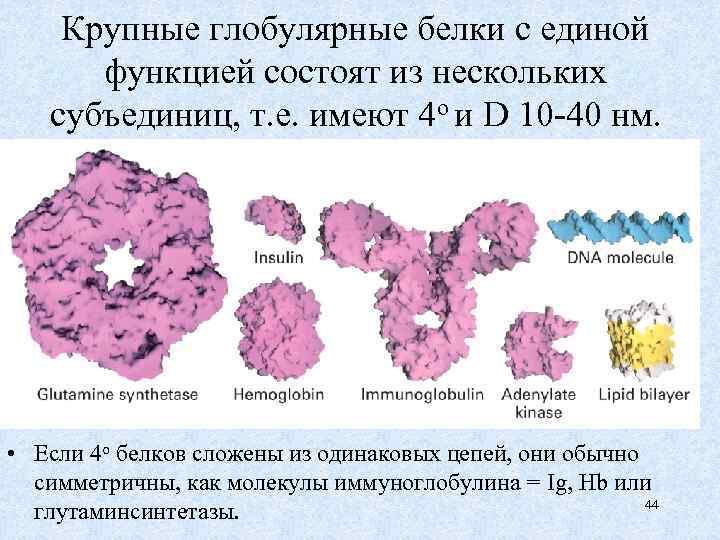
Крупные глобулярные белки с единой функцией состоят из нескольких субъединиц, т. е. имеют 4 о и D 10 -40 нм. • Если 4 о белков сложены из одинаковых цепей, они обычно симметричны, как молекулы иммуноглобулина = Ig, Hb или 44 глутаминсинтетазы.
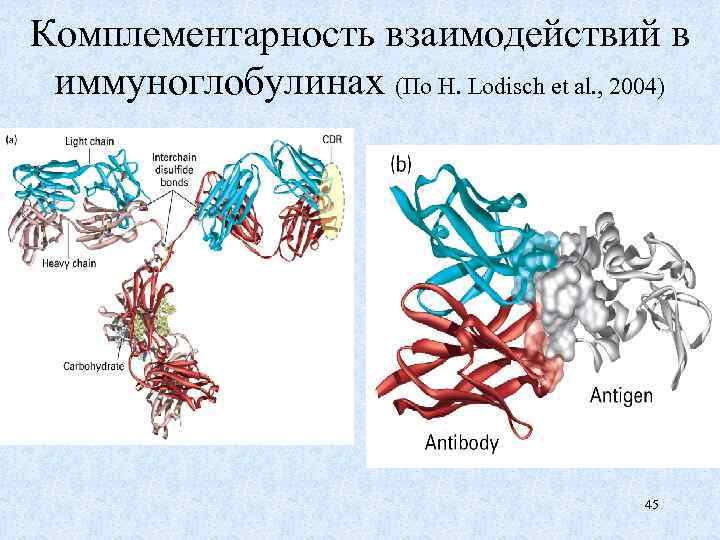
Комплементарность взаимодействий в иммуноглобулинах (По H. Lodisch et al. , 2004) 45
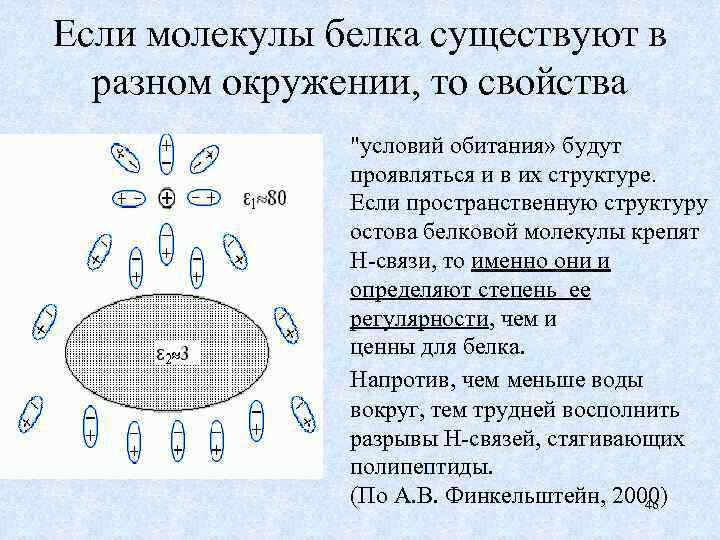
Если молекулы белка существуют в разном окружении, то свойства "условий обитания» будут проявляться и в их структуре. Если пространственную структуру остова белковой молекулы крепят Н-связи, то именно они и определяют степень ее регулярности, чем и ценны для белка. Напротив, чем меньше воды вокруг, тем трудней восполнить разрывы Н-связей, стягивающих полипептиды. (По А. В. Финкельштейн, 2000) 46

К 70 -х гг. ХХ в. заметили, что • Между регулярной 2 о и уникальной 3 о структурами белков, детально описывающими упаковку их атомов, есть промежуточные уровни взаимного расположения α- и/или β-участков. • В этих «сверхвторичных структурах» = «мотивах укладки» белковых цепей = доменах глобул, проявляется структурное сходство белков и в меньшей степени, их связи с эволюцией и функцией молекул. 47
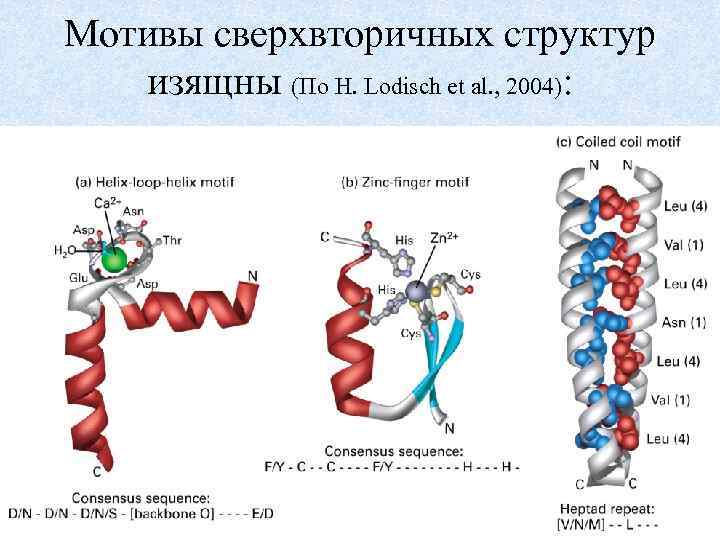
Мотивы сверхвторичных структур изящны (По H. Lodisch et al. , 2004): 48
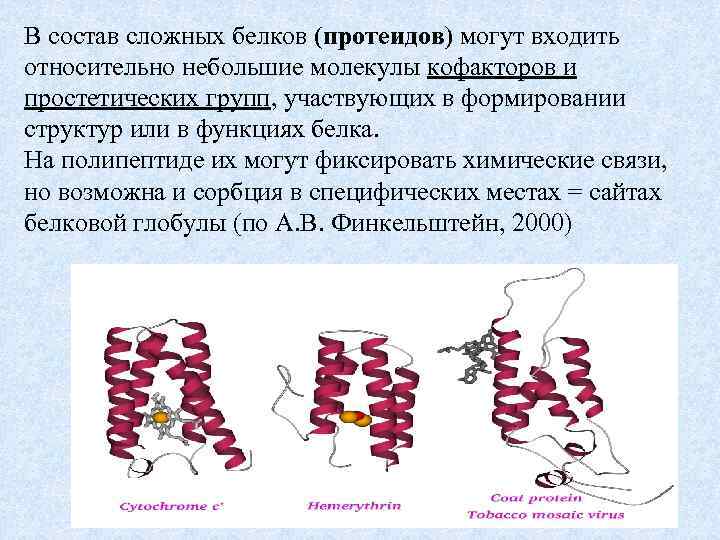
В состав сложных белков (протеидов) могут входить относительно небольшие молекулы кофакторов и простетических групп, участвующих в формировании структур или в функциях белка. На полипептиде их могут фиксировать химические связи, но возможна и сорбция в специфических местах = сайтах белковой глобулы (по А. В. Финкельштейн, 2000) 49

Что ж такое домены? Сайт http: //www. bio. cmu. edu/courses/ 03231/Prot. Struc. htm: дал 3 определения: 1. По структуре полипептида. 2. По его функции. 3. По сдвигам аминокислотной последовательности домена в эволюции. 50

Схема трехдоменной структуры полипептида (биохимия) • Домен - обособленная в пространстве часть структуры полипептида, имеющая: 1. Собственное гидрофобное ядро. 2. Сравнительно мало контактов с другими его частями. 3. Гибкие и неупорядоченные участки = линкеры, соединяющие домены в сверхвторичные мотивы и 3 О белка. 51
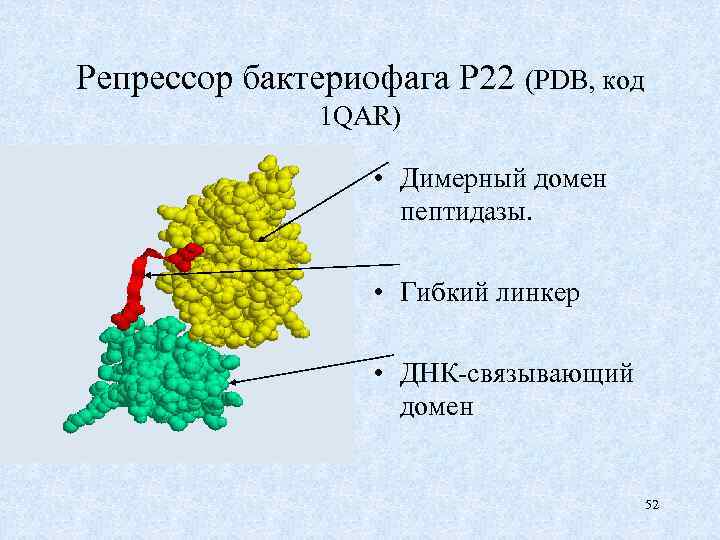
Репрессор бактериофага P 22 (PDB, код 1 QAR) • Димерный домен пептидазы. • Гибкий линкер • ДНК-связывающий домен 52
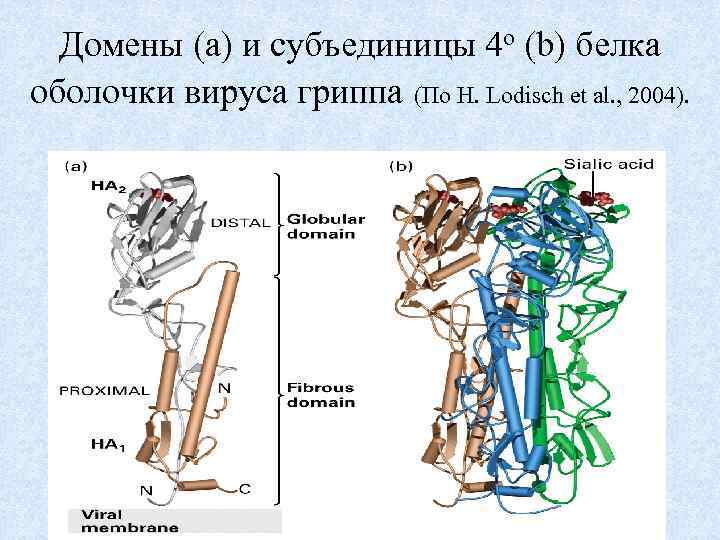
Домены (а) и субъединицы 4 о (b) белка оболочки вируса гриппа (По H. Lodisch et al. , 2004). 53
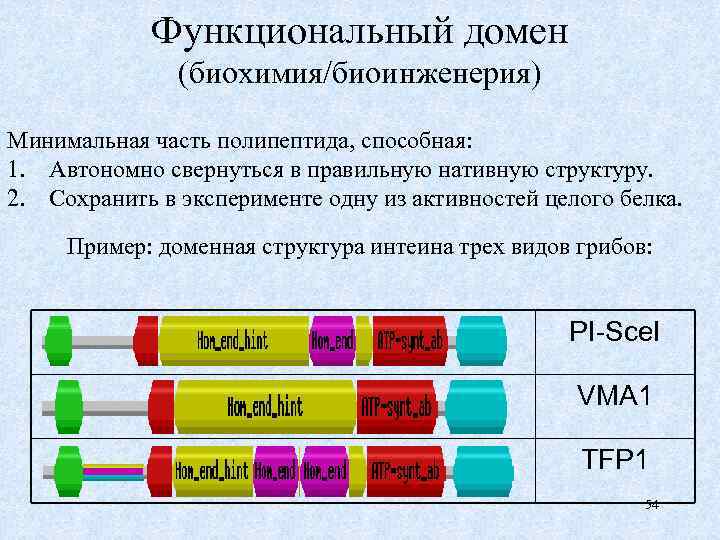
Функциональный домен (биохимия/биоинженерия) Минимальная часть полипептида, способная: 1. Автономно свернуться в правильную нативную структуру. 2. Сохранить в эксперименте одну из активностей целого белка. Пример: доменная структура интеина трех видов грибов: PI-Sce. I VMA 1 TFP 1 54

Эволюционный домен (биоинформатика) Длинный непрерывный участок полипептида, который: 1. Эволюционирует существенно медленней других участков. 2. Замечен в перемешивании доменов (domain schuffling). Так, 65 разных гомеобелков из БД Pfam позволили считать, что 55
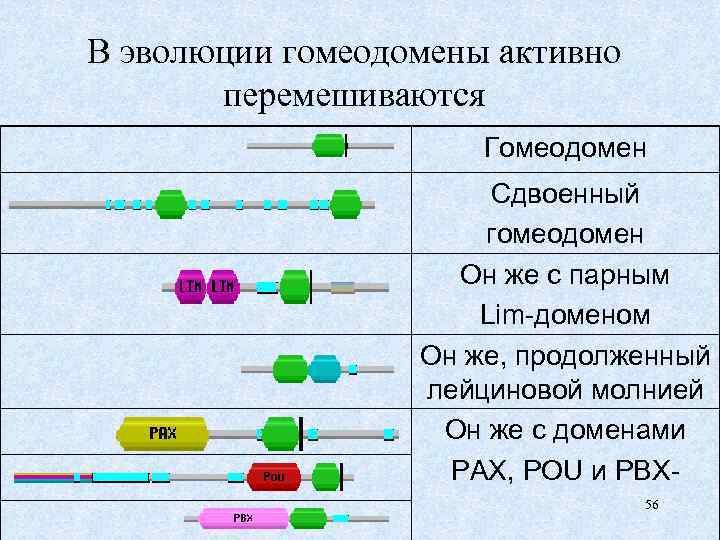
В эволюции гомеодомены активно перемешиваются Гомеодомен Сдвоенный гомеодомен Он же с парным Lim-доменом Он же, продолженный лейциновой молнией Он же с доменами PAX, POU и PBX 56
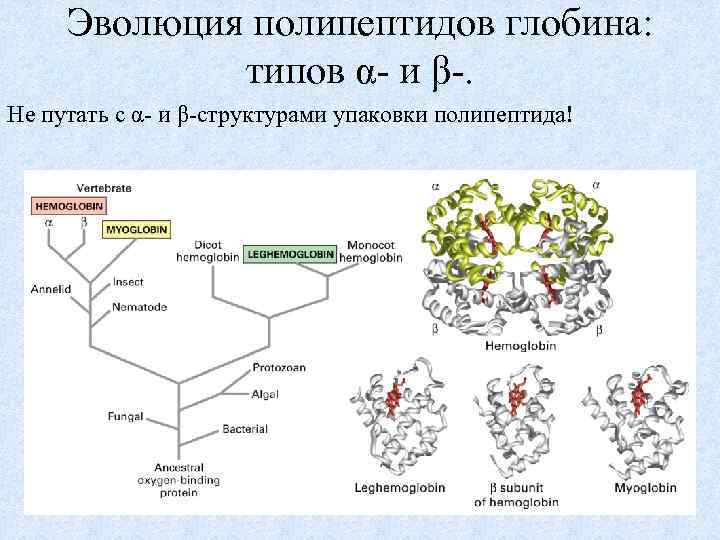
Эволюция полипептидов глобина: типов α- и β-. Не путать с α- и β-структурами упаковки полипептида! 57
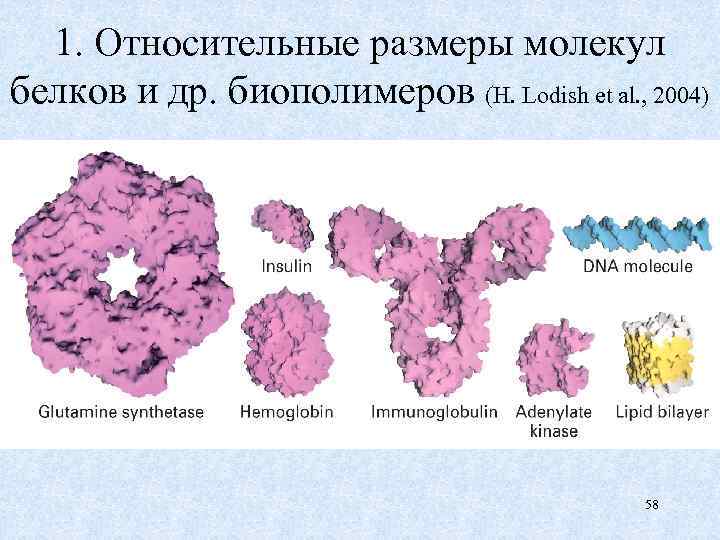
1. Относительные размеры молекул белков и др. биополимеров (H. Lodish et al. , 2004) 58

Комментарий к слайду 58 Сопоставив размеры молекул белков с D ДНК = 2 нм и толщиной липидного бислоя = 7 -10 нм, отметим: 1. Разнообразие форм и широкий диапазон вариаций массы белков от 51 АКО ~5 к. Да у сигнальной молекулы инсулина, до 800 к. Да у Е глутаминсинтетазы. Стабильные конформации > 50 АКО, а самые длинные полипептиды (> 1000 АКО) у проколлагена и миодистрофина. 2. Выраженность пятичленной S-S-петли у инсулина и активного центра = АЦ у Е аденилаткиназы. 3. Наличие S-S-мостиков только в молекулах инсулина и Ig, функционирующих вне клеток! 4. Неясность роли симметрии у модульных молекул белков 4 о: Hb, Ig и глутаминсинтетазы. 59
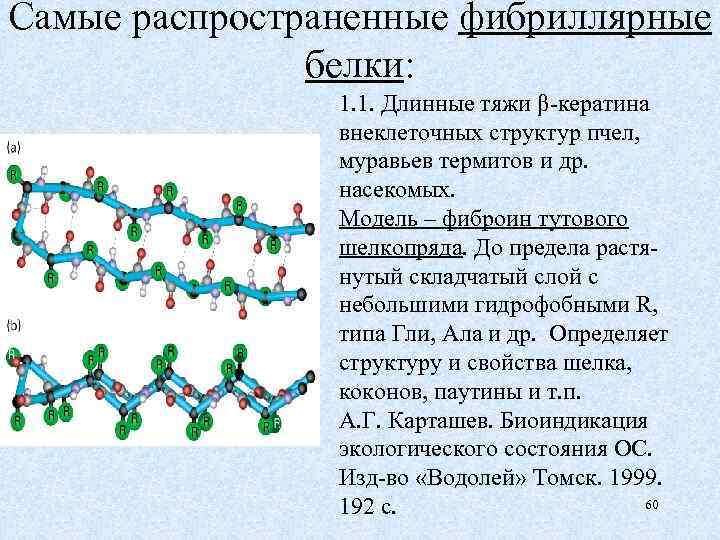
Самые распространенные фибриллярные белки: 1. 1. Длинные тяжи β-кератина внеклеточных структур пчел, муравьев термитов и др. насекомых. Модель – фиброин тутового шелкопряда. До предела растянутый складчатый слой с небольшими гидрофобными R, типа Гли, Ала и др. Определяет структуру и свойства шелка, коконов, паутины и т. п. А. Г. Карташев. Биоиндикация экологического состояния ОС. Изд-во «Водолей» Томск. 1999. 60 192 с.

1. 2. α-Кератины промежуточных волокон цитоскелета эукариот • • • Жгуты α-спиралей создают св-ва гидрофильной пружины. С помощью управляющих белков они собираются и во внеклеточные структуры покровов позвоночных животных. См. : Албертс и др. Молекулярная биология клетки в 4 -х тт. М. «Мир» . 1994. Модели: α-кератин волос позвоночных, тропомиозин и большая часть молекулы миозина. 61
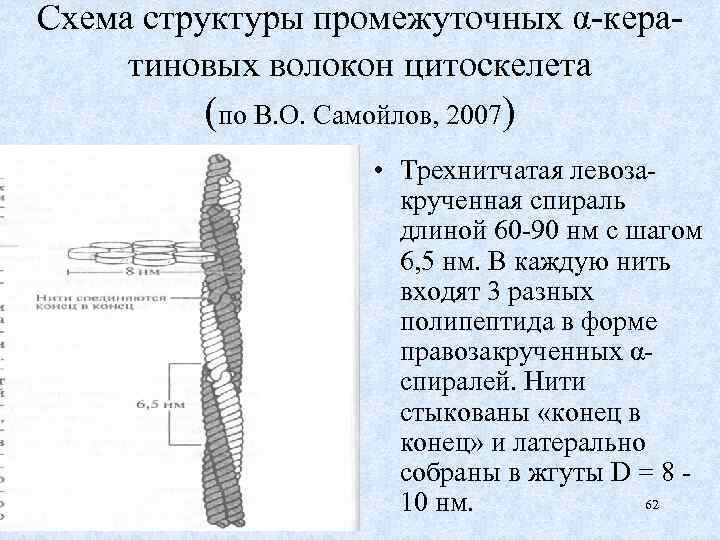
Схема структуры промежуточных α-кератиновых волокон цитоскелета (по В. О. Самойлов, 2007) • Трехнитчатая левозакрученная спираль длиной 60 -90 нм с шагом 6, 5 нм. В каждую нить входят 3 разных полипептида в форме правозакрученных αспиралей. Нити стыкованы «конец в конец» и латерально собраны в жгуты D = 8 62 10 нм.

Димеры тубулина создают микротрубки для: 1. Поддержания формы клеток. 2. Направления потоков веществ и органелл, перемещающихся в цитоплазме. 3. Разведения хромосом веретена при митозе. 63
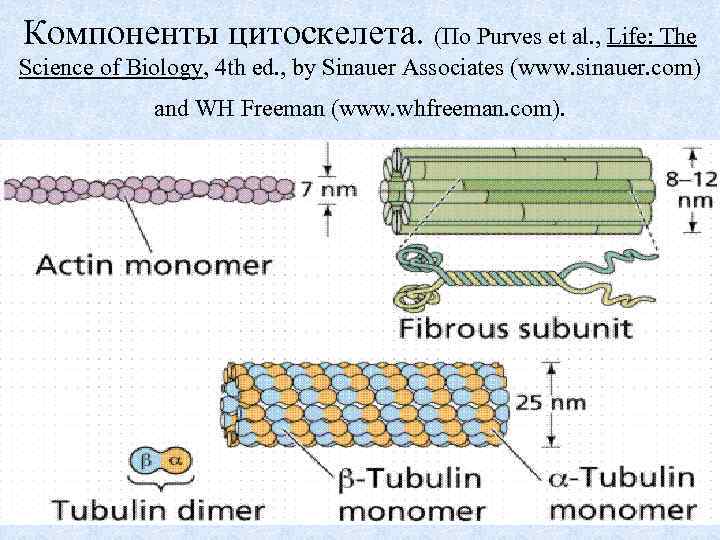
Компоненты цитоскелета. (По Purves et al. , Life: The Science of Biology, 4 th ed. , by Sinauer Associates (www. sinauer. com) and WH Freeman (www. whfreeman. com). 64
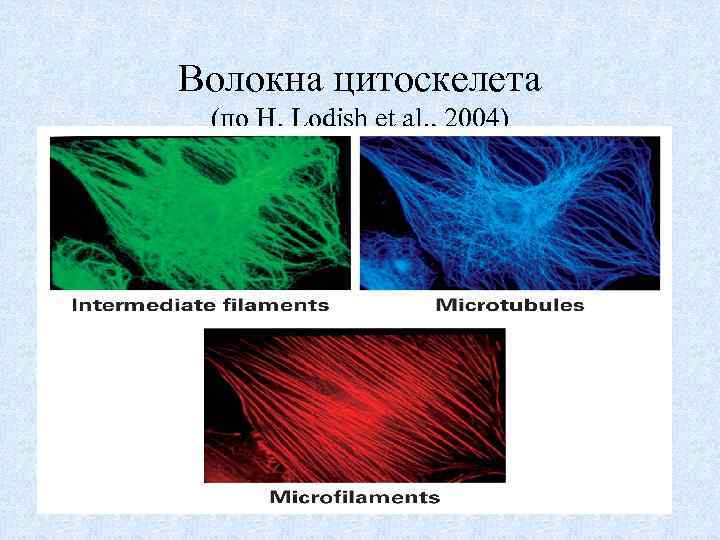
Волокна цитоскелета (по H. Lodish et al. , 2004) 65
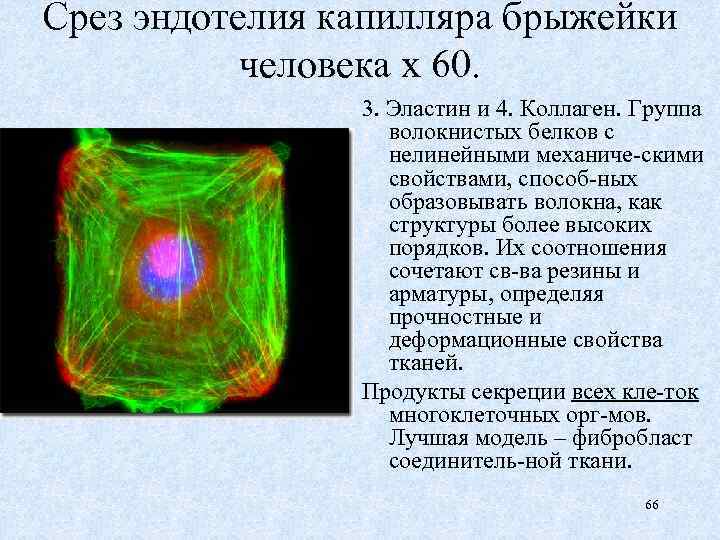
Срез эндотелия капилляра брыжейки человека х 60. 3. Эластин и 4. Коллаген. Группа волокнистых белков с нелинейными механиче-скими свойствами, способ-ных образовывать волокна, как структуры более высоких порядков. Их соотношения сочетают св-ва резины и арматуры, определяя прочностные и деформационные свойства тканей. Продукты секреции всех кле-ток многоклеточных орг-мов. Лучшая модель – фибробласт соединитель-ной ткани. 66
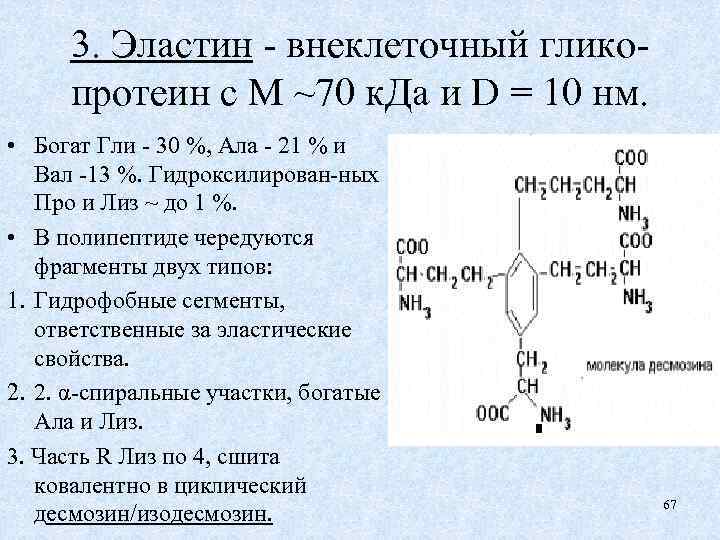
3. Эластин - внеклеточный гликопротеин с М ~70 к. Да и D = 10 нм. • Богат Гли - 30 %, Ала - 21 % и Вал -13 %. Гидроксилирован-ных Про и Лиз ~ до 1 %. • В полипептиде чередуются фрагменты двух типов: 1. Гидрофобные сегменты, ответственные за эластические свойства. 2. 2. α-спиральные участки, богатые Ала и Лиз. 3. Часть R Лиз по 4, сшита ковалентно в циклический десмозин/изодесмозин. 67
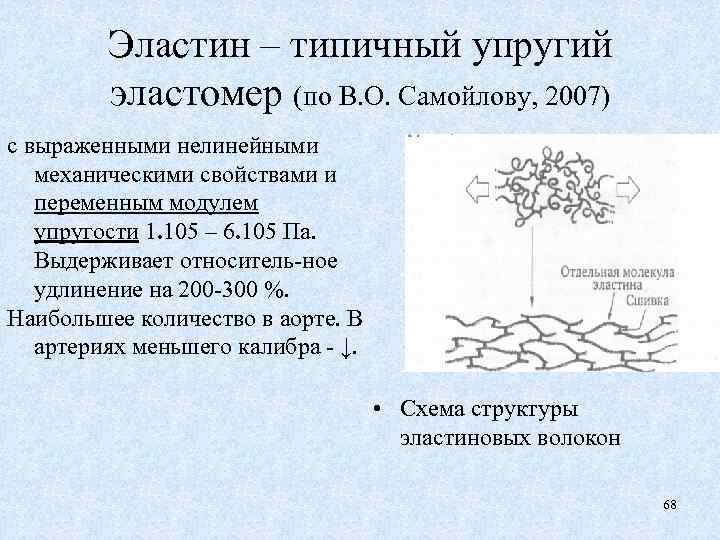
Эластин – типичный упругий эластомер (по В. О. Самойлову, 2007) с выраженными нелинейными механическими свойствами и переменным модулем упругости 1. 105 – 6. 105 Па. Выдерживает относитель-ное удлинение на 200 -300 %. Наибольшее количество в аорте. В артериях меньшего калибра - ↓. • Схема структуры эластиновых волокон 68
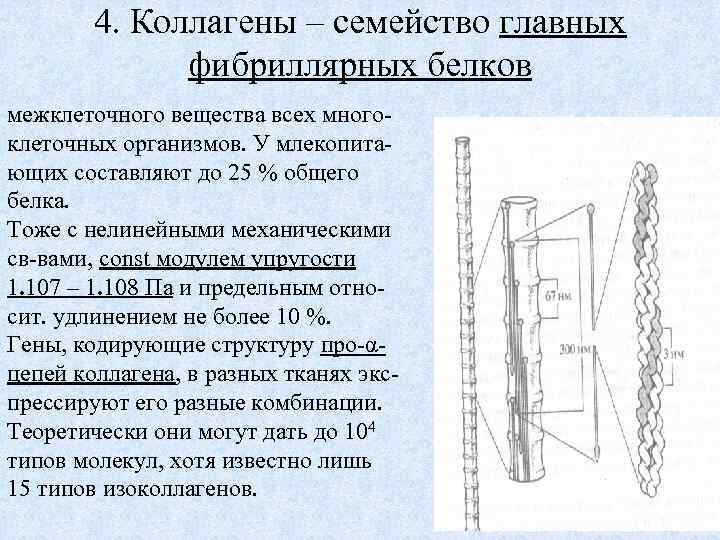
4. Коллагены – семейство главных фибриллярных белков межклеточного вещества всех многоклеточных организмов. У млекопитающих составляют до 25 % общего белка. Тоже с нелинейными механическими св-вами, const модулем упругости 1. 107 – 1. 108 Па и предельным относит. удлинением не более 10 %. Гены, кодирующие структуру про-αцепей коллагена, в разных тканях экспрессируют его разные комбинации. Теоретически они могут дать до 104 типов молекул, хотя известно лишь 15 типов изоколлагенов. 69

Изоколлагены Типы Групповое название I - III Формирующие фибриллы Образуют коллагеновые волокна IX, XII Ассоциируемые с фибриллами Обеспечивают соединение волокон с клеткой и др. молекулами внеклеточного матрикса IV, VII Формирующие сетевидные структуры Функция Сети базальных мембран, связывающих слои эпителиев с подлежащей 70 соединительной тканью.
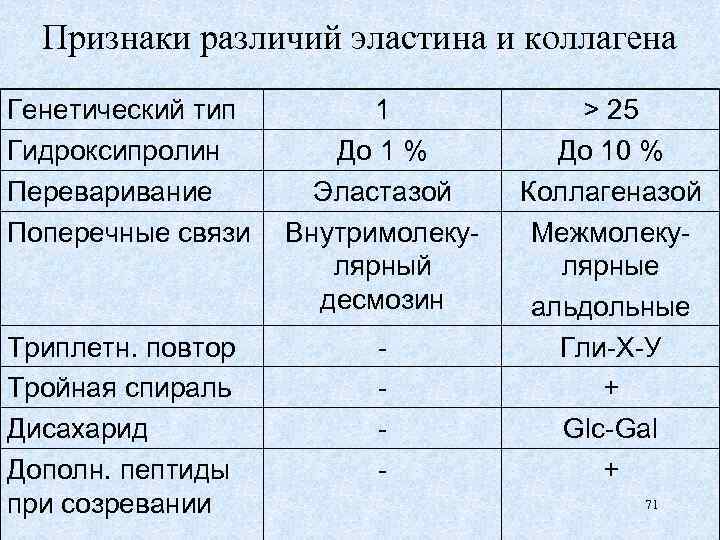
Признаки различий эластина и коллагена Генетический тип Гидроксипролин Переваривание Поперечные связи 1 До 1 % Эластазой Внутримолекулярный десмозин Триплетн. повтор Тройная спираль Дисахарид Дополн. пептиды при созревании - > 25 До 10 % Коллагеназой Межмолекулярные альдольные Гли-Х-У + Glc-Gal + 71

Повторы простых конструкций в молекулах фибриллярных белков • приводят к их уникальным биомеханическим свойствам и, прежде всего, износостойкости. Поэтому информацию об их структуре и св-вах можно найти в лит-ре по кожевенной, текстильной и пищевой промышленности, музейному делу, таксидермии и даже парикмахерскому искусству. • К сожалению, эти исследования in vitro позволяют судить лишь о пассивном механическом поведении тканей, но не их 72 функциях in vivo.

Физико-химические свойства белков 1. Растворимость. Белки формируют коллоидные растворы, что обусловлено размером частиц (размеры частиц 0, 1 -0, 001 мкм). Для растворов белков характерны следующие характеристики: низкое осмотическое давление, высокая вязкость, низкая способность к диффузии. В лабораторной практике используют 2 свойства коллоидных растворов белков: нефелометрическое определение количества белка на основе эффекта Тиндаля; диализ – очистка белков от низкомолекулярных примесей.

2. Амфотерность белков. Белки обладают кислыми и основными свойствами из-за присутствия карбоксильных и аминогрупп. Изоэлектрическая точка белков (p. I) – значение р. Н, при котором суммарный заряд белка равен нулю. В p. I белок электронейтрален с минимальной растворимостью, максимальной преципитацией и наименьшей буферной способностью. Изоэлектрическая точка определяется количеством NH 2 и СООН групп в молекуле белка. Если количество NH 2 и СООН групп равны, р. I лежит в слабокислой среде (ионизация карбоксильных групп несколько выше, чем аминных) при р. Н≤ 7. Если количество NH 2>СООН, то p. I лежит в щелочной среде. Если количество NH 2<СООН, то p. I лежит в кислой среде. При р. Н>p. I заряд белка всегда отрицательный, так карбоксильные группы переходят в форму СОО-, а аминные группы в форму NH 2. При р. Н<р. I заряд белка положительный, т. к. при уменьшении р. Н все больше аминогрупп переходит в форму NH 3+, а диссоциация карбоксильных групп подавляется

3. Способность к осаждению (преципитации). Существуют два фактора устойчивости белков в коллоидном растворе: заряд и гидратная оболочка. Белки могут быть преципитированы путем дегидратации и/или нейтрализации полярных групп. Преципитация в р. I. Белки мало растворимы в изоэлектрической точке. Например, белок молока казеин сворачивается, если молоко кислое. Это объясняется тем, что молочная кислота, образуемая бактериями, снижает р. Н, приближая его к изоэлектрической точке казеина (p. I= 4, 6).

Высаливание. Процесс преципитации добавлением нейтральных солей (сульфата аммония или сульфата натрия) называется высаливанием. Этот процесс объясняется дегидратацией молекул белков солями, что приводит к молекулярной агрегации и преципитации. Количество соли, необходимой для преципитации, зависит от молекулярной массы белка. Чем больше молекулярная масса белка, тем меньше соли необходимо для преципитации. Например, глобулины сыворотке осаждаются полунасыщенным раствором сульфата аммония, в то время как альбумин – насыщенным раствором. Высаливание используется для разделения белков сыворотки крови. Добавление незначительного количества нейтральных солей повышает растворимость белков

Осаждение солями тяжелых металлов. Ионы тяжелых металлов (Pb 2+, Hg 2+, Fe 2+, Zn 2+, Cd 2+) вызывают осаждение белков. Металлы имеют положительный заряд и в щелочной среде вызывают преципитацию белков. Осаждение анионами или алкалоидными реактивами. Белки осаждаются трихлоруксусной кислотой, сульфосалициловой кислотой, пикриновой кислотой, таниновой кислотой. Белки являются катионами и добавление анионов кислот приводит к образованию комплексов белок-анион.

Изоэлектрическое фокусирование. Метод основан на том, что в изоэлектрической точке белок теряет заряд и теряет подвижность в электрическом поле. Трубку с гелем заполняют амфолинами, создающими градиент р. Н. В электрическом поле белок будет передвигаться до того значения, где он войдет в свое изоэлектрическое состояние и, потеряв заряд, остановится.
Лекция 02 Аминокислоты, пептиды, белки - строение биол роль.ppt