СТРУКТУРА НУКЛЕИНОВЫХ КИСЛОТ.ppt
- Количество слайдов: 71
 СТРУКТУРА НУКЛЕИНОВЫХ КИСЛОТ лекция 1
СТРУКТУРА НУКЛЕИНОВЫХ КИСЛОТ лекция 1

 Хронология открытий, подготовивших создание Уотсоном и Криком модели двойной спирали ДНК 1868 г. Обнаружен нуклеин. Современное название - хроматин. Фридрих Мишер 1889 г. Нуклеин разделен на нуклеиновую кислоту и белок. Появился термин "нуклеиновая кислота". Рихард Альтман 1900 г. Все азотистые основания были описаны химиками. 1909 г. В нуклеиновых кислотах обнаружены фосфорная кислота и рибоза. Левин 1930 г. Найдена дезоксирибоза. Левин 1938 г. 1947 г. 1953 г. Рентгеноструктурный анализ показал, что расстояние между нуклеотидами в ДНК 3, 4 Å. При этом азотистые основания уложены стопками. Уильям Астбюри, Флорин Белл С помощью прямого и обратного титрования установлено, что в ДНК есть водородные связи между группами N-H и C=O. Гулланд С помощью кислотного гидролиза ДНК с последующей хроматографией и количественным анализом установлены закономерности: А/Т=1; Г/Ц=1; (Г+Ц)/(А+Т)=К - коэффициент специфичности, постоянен для каждого вида. Эрвин Чаргафф
Хронология открытий, подготовивших создание Уотсоном и Криком модели двойной спирали ДНК 1868 г. Обнаружен нуклеин. Современное название - хроматин. Фридрих Мишер 1889 г. Нуклеин разделен на нуклеиновую кислоту и белок. Появился термин "нуклеиновая кислота". Рихард Альтман 1900 г. Все азотистые основания были описаны химиками. 1909 г. В нуклеиновых кислотах обнаружены фосфорная кислота и рибоза. Левин 1930 г. Найдена дезоксирибоза. Левин 1938 г. 1947 г. 1953 г. Рентгеноструктурный анализ показал, что расстояние между нуклеотидами в ДНК 3, 4 Å. При этом азотистые основания уложены стопками. Уильям Астбюри, Флорин Белл С помощью прямого и обратного титрования установлено, что в ДНК есть водородные связи между группами N-H и C=O. Гулланд С помощью кислотного гидролиза ДНК с последующей хроматографией и количественным анализом установлены закономерности: А/Т=1; Г/Ц=1; (Г+Ц)/(А+Т)=К - коэффициент специфичности, постоянен для каждого вида. Эрвин Чаргафф
 • Правила Чаргаффа. В ДНК всегда А/Т=1; Г/Ц=1; (Г+Ц)/(А+Т)=К коэффициент специфичности, постоянен для каждого вида.
• Правила Чаргаффа. В ДНК всегда А/Т=1; Г/Ц=1; (Г+Ц)/(А+Т)=К коэффициент специфичности, постоянен для каждого вида.
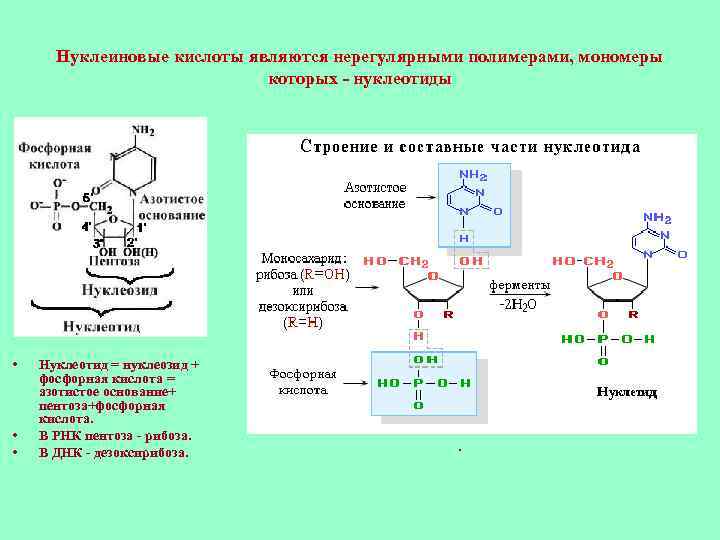 Нуклеиновые кислоты являются нерегулярными полимерами, мономеры которых - нуклеотиды • • • Нуклеотид = нуклеозид + фосфорная кислота = азотистое основание+ пентоза+фосфорная кислота. В РНК пентоза - рибоза. В ДНК - дезоксирибоза. .
Нуклеиновые кислоты являются нерегулярными полимерами, мономеры которых - нуклеотиды • • • Нуклеотид = нуклеозид + фосфорная кислота = азотистое основание+ пентоза+фосфорная кислота. В РНК пентоза - рибоза. В ДНК - дезоксирибоза. .
 Оснований таутомерия • Переход протонов, связанных с атомами азота, в гетеро- циклических молекулах на другие свободные атомы азота либо на атомы кислорода кетогруппы приводит к существованию этих молекул в растворе в разных таутомерных формах, быстро переходящих одна в другую. Такой тип таутомерии с прототропными переходами сильно зависит от диэлектрической постоянной раствора и p. K соответствующего гетероатома. • В незамещенных основаниях (см. Рис. Основания ) может происходить прототропная миграция от одного эндоциклического азота к другому, типа N 7 -H <--> N 9 -H в пуринах и N 1 -H <--> N 3 -H в пиримидинах. В случае гетероциклов нуклеозидов происходят кето<--->енол и амино<--->имино переходы. • Изменение в положении атома водорода существенно изменяет характер образуемых основанием водородных связей : кетогруппа с акцепторными свойствами в енольной форме становится донором, а отдающая водород аминогруппа при преходе в форму замещенного имина - акцептором. Если, однако, в последнем случае свзь N-H способна менять ориентацию, то иминогруппа может выступать и в роли донора. В результате таутомерных превращений урацил и гуанин в енольной форме при спаривании могут имитировать цитозин и аденин, а цитозин и аденин в иминоформе - урацил и гуанин. • В растворе обычные кето- и аминоформы всегда превалируют над енольной и иминоформами, доля которых, как правило, не превышает 0, 1 %. Эта величина может сильно меняться для модифицированных оснований или для оснований в составе комплементарной пары.
Оснований таутомерия • Переход протонов, связанных с атомами азота, в гетеро- циклических молекулах на другие свободные атомы азота либо на атомы кислорода кетогруппы приводит к существованию этих молекул в растворе в разных таутомерных формах, быстро переходящих одна в другую. Такой тип таутомерии с прототропными переходами сильно зависит от диэлектрической постоянной раствора и p. K соответствующего гетероатома. • В незамещенных основаниях (см. Рис. Основания ) может происходить прототропная миграция от одного эндоциклического азота к другому, типа N 7 -H <--> N 9 -H в пуринах и N 1 -H <--> N 3 -H в пиримидинах. В случае гетероциклов нуклеозидов происходят кето<--->енол и амино<--->имино переходы. • Изменение в положении атома водорода существенно изменяет характер образуемых основанием водородных связей : кетогруппа с акцепторными свойствами в енольной форме становится донором, а отдающая водород аминогруппа при преходе в форму замещенного имина - акцептором. Если, однако, в последнем случае свзь N-H способна менять ориентацию, то иминогруппа может выступать и в роли донора. В результате таутомерных превращений урацил и гуанин в енольной форме при спаривании могут имитировать цитозин и аденин, а цитозин и аденин в иминоформе - урацил и гуанин. • В растворе обычные кето- и аминоформы всегда превалируют над енольной и иминоформами, доля которых, как правило, не превышает 0, 1 %. Эта величина может сильно меняться для модифицированных оснований или для оснований в составе комплементарной пары.
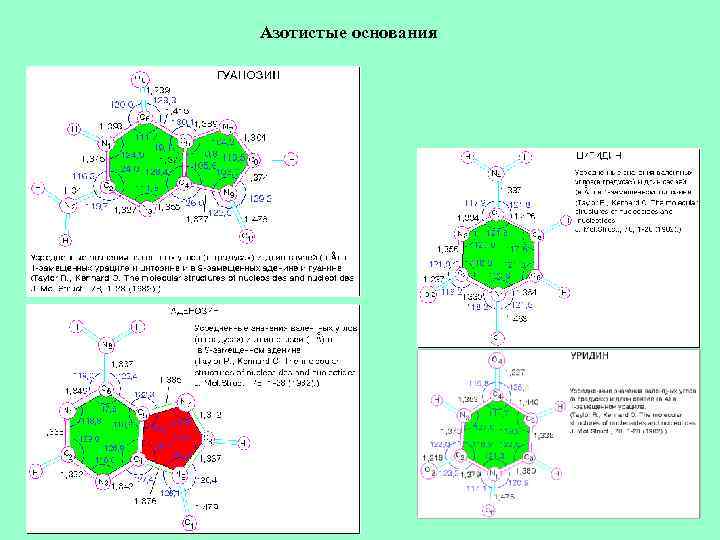 Азотистые основания
Азотистые основания
 Пиримидины: структура • Пиримидины: структура • Все пиримидины являются производными гетероциклического соединения - пиримидина. Основные пиримидины, найденные в РНК , - урацил и цитозин; в ДНК - тимин и цитозин. Основания в составе всех нуклеозидов и нуклеотидов замещены, и на Рис. Основания они приведены именно в таком виде. • Для описания этих оснований используются следующие обозначения: урацил - Ura, цитозин - Cyt, тимин - Thy. В некоторых нуклеиновых кислотах найдены метилированные и другие производные пиримидина. • Биологическая роль пиримидинов не ограничена нуклеиновыми кислотами. Некоторые пиримидиновые нуклеотиды играют важную роль в процессах обмена углеводов и липидов. Витамин В 1 (тиамин) - пиримидиновое производное. • Все пиримидины способны к таутомерным превращениям, смотри Таутомерия оснований.
Пиримидины: структура • Пиримидины: структура • Все пиримидины являются производными гетероциклического соединения - пиримидина. Основные пиримидины, найденные в РНК , - урацил и цитозин; в ДНК - тимин и цитозин. Основания в составе всех нуклеозидов и нуклеотидов замещены, и на Рис. Основания они приведены именно в таком виде. • Для описания этих оснований используются следующие обозначения: урацил - Ura, цитозин - Cyt, тимин - Thy. В некоторых нуклеиновых кислотах найдены метилированные и другие производные пиримидина. • Биологическая роль пиримидинов не ограничена нуклеиновыми кислотами. Некоторые пиримидиновые нуклеотиды играют важную роль в процессах обмена углеводов и липидов. Витамин В 1 (тиамин) - пиримидиновое производное. • Все пиримидины способны к таутомерным превращениям, смотри Таутомерия оснований.
 Пурины: структура • Пурин, давший название всей группе, содержит шестичленное пиримидиновое кольцо, сочлененное со вторым кольцом, образованным еще двумя атомами азота и одним атомом углерода. Аденин (Ade) и гуанин (Guo) - основные пурины нуклеиновых кислот (смотри Рис. Основания ). Подобно пиримидинам, пурины склонны к таутомерии ( Таутомерия оснований ). • В ДНК с самым различным нуклеотидным составом отношения Аde/Thy и Guo/Cyt всегда равны единице. Эта закономерность строения ДНК известна в литературе как правило Чаргаффа.
Пурины: структура • Пурин, давший название всей группе, содержит шестичленное пиримидиновое кольцо, сочлененное со вторым кольцом, образованным еще двумя атомами азота и одним атомом углерода. Аденин (Ade) и гуанин (Guo) - основные пурины нуклеиновых кислот (смотри Рис. Основания ). Подобно пиримидинам, пурины склонны к таутомерии ( Таутомерия оснований ). • В ДНК с самым различным нуклеотидным составом отношения Аde/Thy и Guo/Cyt всегда равны единице. Эта закономерность строения ДНК известна в литературе как правило Чаргаффа.
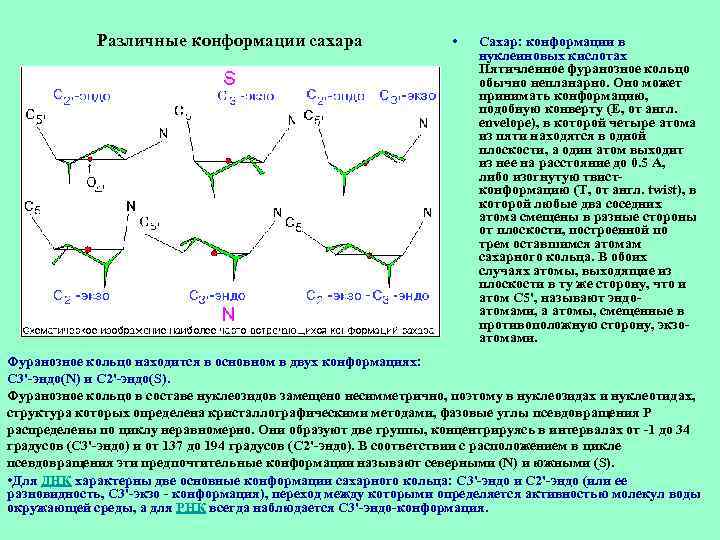 Различные конформации сахара • Сахар: конформации в нуклеиновых кислотах Пятичленное фуранозное кольцо обычно непланарно. Оно может принимать конформацию, подобную конверту (E, от англ. envelope), в которой четыре атома из пяти находятся в одной плоскости, а один атом выходит из нее на расстояние до 0. 5 А, либо изогнутую твистконформацию (T, от англ. twist), в которой любые два соседних атома смещены в разные стороны от плоскости, построенной по трем оставшимся атомам сахарного кольца. В обоих случаях атомы, выходящие из плоскости в ту же сторону, что и атом С 5', называют эндоатомами, а атомы, смещенные в противоположную сторону, экзоатомами. Фуранозное кольцо находится в основном в двух конформациях: С 3'-эндо(N) и С 2'-эндо(S). Фуранозное кольцо в составе нуклеозидов замещено несимметрично, поэтому в нуклеозидах и нуклеотидах, структура которых определена кристаллографическими методами, фазовые углы псевдовращения Р распределены по циклу неравномерно. Они образуют две группы, концентрируясь в интервалах от -1 до 34 градусов (С 3'-эндо) и от 137 до 194 градусов (С 2'-эндо). В соответствии с расположением в цикле псевдовращения эти предпочтительные конформации называют северными (N) и южными (S). • Для ДНК характерны две основные конформации сахарного кольца: С 3'-эндо и С 2'-эндо (или ее разновидность, С 3'-экзо - конформация), переход между которыми определяется активностью молекул воды окружающей среды, а для РНК всегда наблюдается С 3'-эндо-конформация.
Различные конформации сахара • Сахар: конформации в нуклеиновых кислотах Пятичленное фуранозное кольцо обычно непланарно. Оно может принимать конформацию, подобную конверту (E, от англ. envelope), в которой четыре атома из пяти находятся в одной плоскости, а один атом выходит из нее на расстояние до 0. 5 А, либо изогнутую твистконформацию (T, от англ. twist), в которой любые два соседних атома смещены в разные стороны от плоскости, построенной по трем оставшимся атомам сахарного кольца. В обоих случаях атомы, выходящие из плоскости в ту же сторону, что и атом С 5', называют эндоатомами, а атомы, смещенные в противоположную сторону, экзоатомами. Фуранозное кольцо находится в основном в двух конформациях: С 3'-эндо(N) и С 2'-эндо(S). Фуранозное кольцо в составе нуклеозидов замещено несимметрично, поэтому в нуклеозидах и нуклеотидах, структура которых определена кристаллографическими методами, фазовые углы псевдовращения Р распределены по циклу неравномерно. Они образуют две группы, концентрируясь в интервалах от -1 до 34 градусов (С 3'-эндо) и от 137 до 194 градусов (С 2'-эндо). В соответствии с расположением в цикле псевдовращения эти предпочтительные конформации называют северными (N) и южными (S). • Для ДНК характерны две основные конформации сахарного кольца: С 3'-эндо и С 2'-эндо (или ее разновидность, С 3'-экзо - конформация), переход между которыми определяется активностью молекул воды окружающей среды, а для РНК всегда наблюдается С 3'-эндо-конформация.
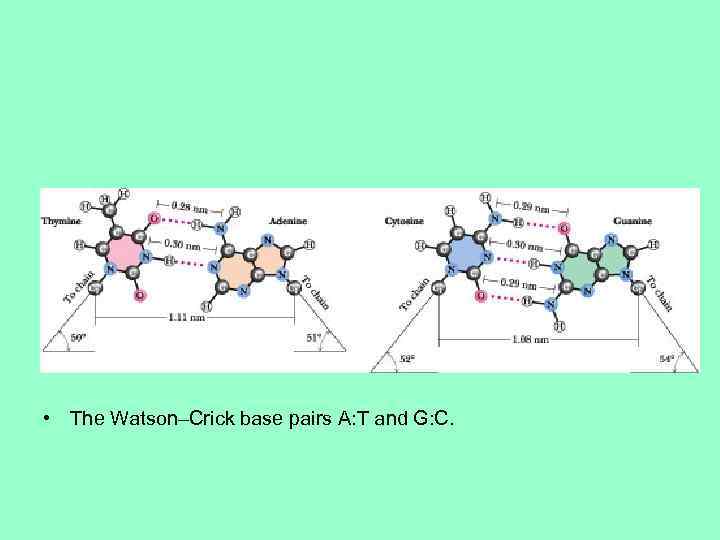 • The Watson–Crick base pairs A: T and G: C.
• The Watson–Crick base pairs A: T and G: C.
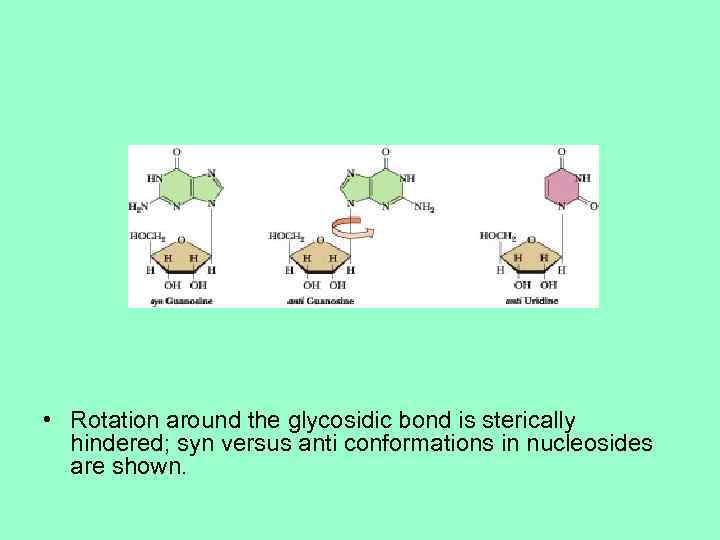 • Rotation around the glycosidic bond is sterically hindered; syn versus anti conformations in nucleosides are shown.
• Rotation around the glycosidic bond is sterically hindered; syn versus anti conformations in nucleosides are shown.
 НУКЛЕОЗИДЫ: СТРУКТУРА • Нуклеозиды - это N-гликозиды пиримидиновых или пуриновых оснований, в которых 1 -й углеродный атом сахара - пентозы связан гликозидной связью с атомом N 1 пиримидина или атомом N 9 пурина. Пентозы всегда присутствуют в фуранозной форме. Существует два ряда нуклеозидов: рибонуклеозиды, которые содержат в качестве сахарного компонента D-рибозу, и 2'-дезоксирибонуклеотиды, содержащие 2 -дезокси-D-рибозу ( Рис. Рибозы и дезоксирибозы ). Далее см. Основные конформации сахара в нуклеиновых кислотах • Гликозидная связь в нуклеотидах • В нуклеозидах и нуклеотидах N-гликозидная связь - это связь между 1 -м углеродным атомом сахара - пентозы и атомом N 1 пиримидина или N 9 пурина. N-гликозидная связь имеет бета- конфигурацию. • Для пиримидиновых нуклеозидов длина связи С 1'-N максимальна и составляет 1. 52 А при торсионном угле вращения, определяемом через атомы - (О 4'- С 1'- N 1 - С 2), и равным примерно 180 град. По мере его приближения к -140 град. длина N-гликозидной связи уменьшается до 1. 48 А практически линейно. В пуриновых нуклеозидах длина гликозидной связи менее вариабельна и составляет примерно 1. 46 А.
НУКЛЕОЗИДЫ: СТРУКТУРА • Нуклеозиды - это N-гликозиды пиримидиновых или пуриновых оснований, в которых 1 -й углеродный атом сахара - пентозы связан гликозидной связью с атомом N 1 пиримидина или атомом N 9 пурина. Пентозы всегда присутствуют в фуранозной форме. Существует два ряда нуклеозидов: рибонуклеозиды, которые содержат в качестве сахарного компонента D-рибозу, и 2'-дезоксирибонуклеотиды, содержащие 2 -дезокси-D-рибозу ( Рис. Рибозы и дезоксирибозы ). Далее см. Основные конформации сахара в нуклеиновых кислотах • Гликозидная связь в нуклеотидах • В нуклеозидах и нуклеотидах N-гликозидная связь - это связь между 1 -м углеродным атомом сахара - пентозы и атомом N 1 пиримидина или N 9 пурина. N-гликозидная связь имеет бета- конфигурацию. • Для пиримидиновых нуклеозидов длина связи С 1'-N максимальна и составляет 1. 52 А при торсионном угле вращения, определяемом через атомы - (О 4'- С 1'- N 1 - С 2), и равным примерно 180 град. По мере его приближения к -140 град. длина N-гликозидной связи уменьшается до 1. 48 А практически линейно. В пуриновых нуклеозидах длина гликозидной связи менее вариабельна и составляет примерно 1. 46 А.
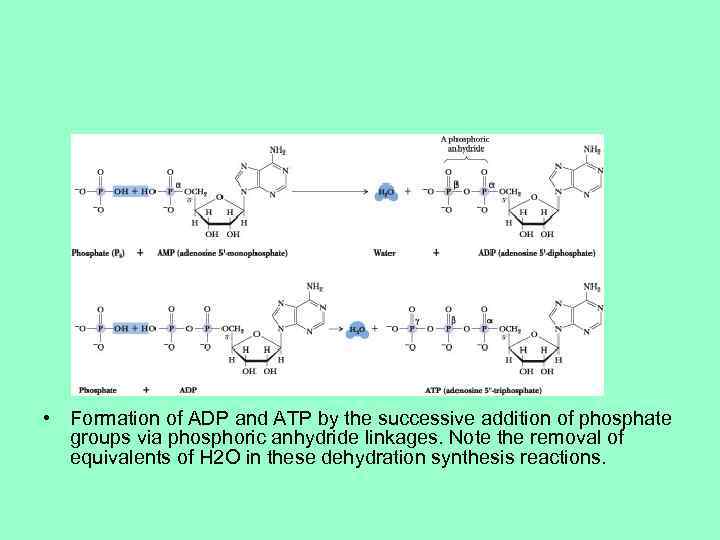 • Formation of ADP and ATP by the successive addition of phosphate groups via phosphoric anhydride linkages. Note the removal of equivalents of H 2 O in these dehydration synthesis reactions.
• Formation of ADP and ATP by the successive addition of phosphate groups via phosphoric anhydride linkages. Note the removal of equivalents of H 2 O in these dehydration synthesis reactions.
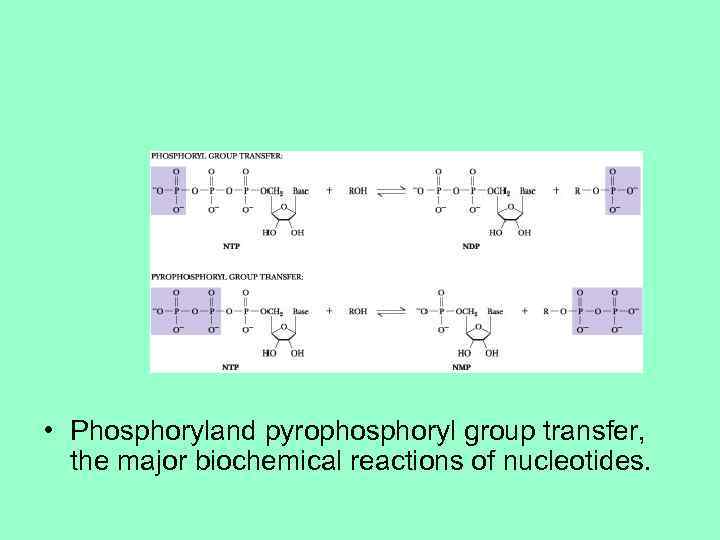 • Phosphoryland pyrophosphoryl group transfer, the major biochemical reactions of nucleotides.
• Phosphoryland pyrophosphoryl group transfer, the major biochemical reactions of nucleotides.
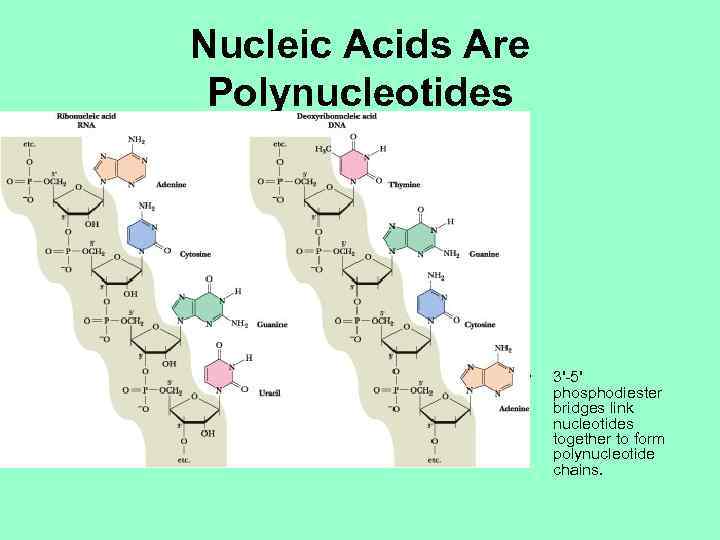 Nucleic Acids Are Polynucleotides • 3'-5' phosphodiester bridges link nucleotides together to form polynucleotide chains.
Nucleic Acids Are Polynucleotides • 3'-5' phosphodiester bridges link nucleotides together to form polynucleotide chains.
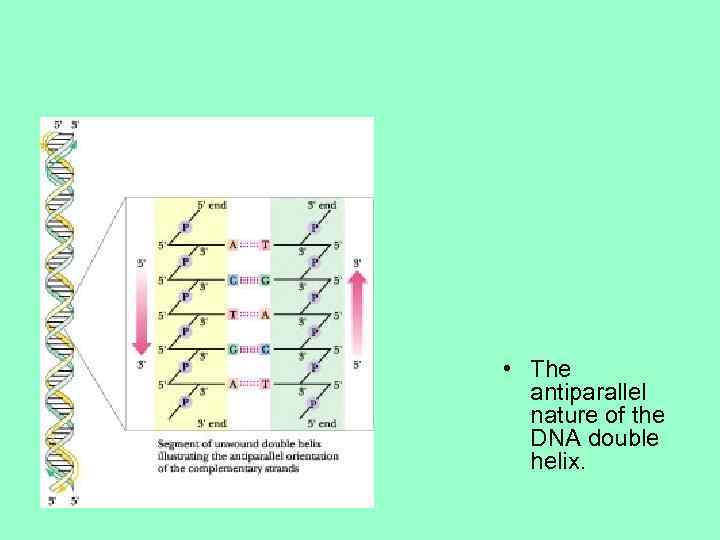 • The antiparallel nature of the DNA double helix.
• The antiparallel nature of the DNA double helix.
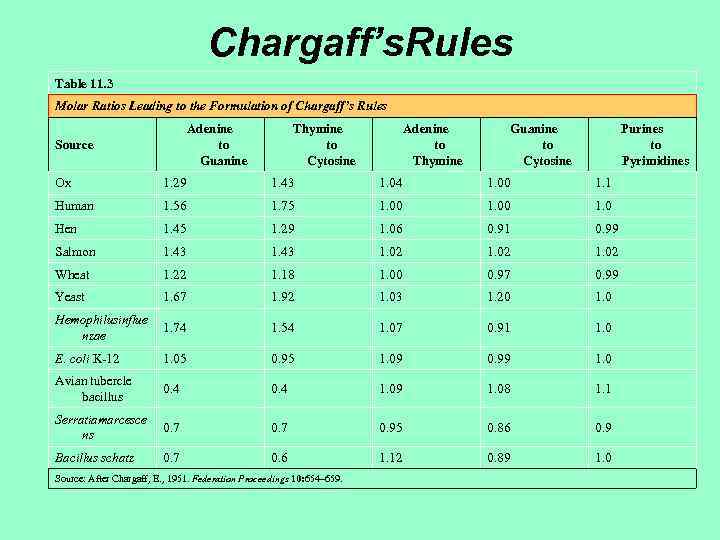 Chargaff’s. Rules Table 11. 3 Molar Ratios Leading to the Formulation of Chargaff’s Rules Adenine to Guanine Source Thymine to Cytosine Adenine to Thymine Guanine to Cytosine Purines to Pyrimidines Ox 1. 29 1. 43 1. 04 1. 00 1. 1 Human 1. 56 1. 75 1. 00 1. 0 Hen 1. 45 1. 29 1. 06 0. 91 0. 99 Salmon 1. 43 1. 02 Wheat 1. 22 1. 18 1. 00 0. 97 0. 99 Yeast 1. 67 1. 92 1. 03 1. 20 1. 0 Hemophilusinflue nzae 1. 74 1. 54 1. 07 0. 91 1. 0 E. coli K-12 1. 05 0. 95 1. 09 0. 99 1. 0 Avian tubercle bacillus 0. 4 1. 09 1. 08 1. 1 Serratiamarcesce ns 0. 7 0. 95 0. 86 0. 9 Bacillus schatz 0. 7 0. 6 1. 12 0. 89 1. 0 Source: After Chargaff, E. , 1951. Federation Proceedings 10: 654– 659.
Chargaff’s. Rules Table 11. 3 Molar Ratios Leading to the Formulation of Chargaff’s Rules Adenine to Guanine Source Thymine to Cytosine Adenine to Thymine Guanine to Cytosine Purines to Pyrimidines Ox 1. 29 1. 43 1. 04 1. 00 1. 1 Human 1. 56 1. 75 1. 00 1. 0 Hen 1. 45 1. 29 1. 06 0. 91 0. 99 Salmon 1. 43 1. 02 Wheat 1. 22 1. 18 1. 00 0. 97 0. 99 Yeast 1. 67 1. 92 1. 03 1. 20 1. 0 Hemophilusinflue nzae 1. 74 1. 54 1. 07 0. 91 1. 0 E. coli K-12 1. 05 0. 95 1. 09 0. 99 1. 0 Avian tubercle bacillus 0. 4 1. 09 1. 08 1. 1 Serratiamarcesce ns 0. 7 0. 95 0. 86 0. 9 Bacillus schatz 0. 7 0. 6 1. 12 0. 89 1. 0 Source: After Chargaff, E. , 1951. Federation Proceedings 10: 654– 659.
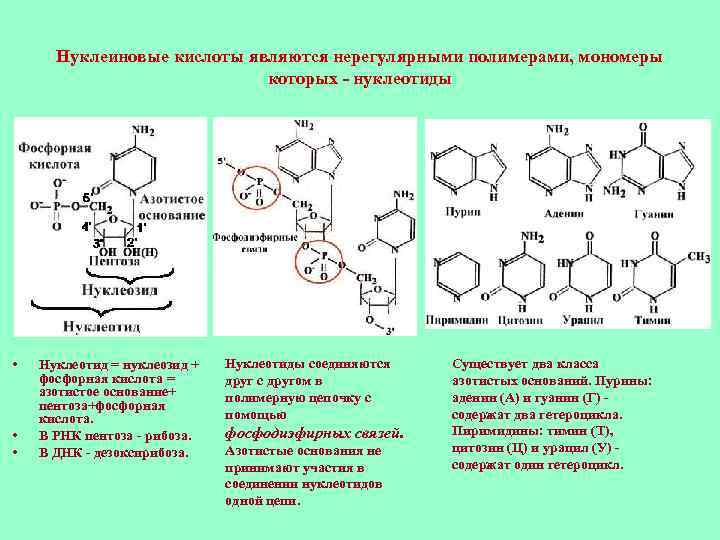 Нуклеиновые кислоты являются нерегулярными полимерами, мономеры которых - нуклеотиды • • • Нуклеотид = нуклеозид + фосфорная кислота = азотистое основание+ пентоза+фосфорная кислота. В РНК пентоза - рибоза. В ДНК - дезоксирибоза. Нуклеотиды соединяются друг с другом в полимерную цепочку с помощью фосфодиэфирных связей. Азотистые основания не принимают участия в соединении нуклеотидов одной цепи. Существует два класса азотистых оснований. Пурины: аденин (А) и гуанин (Г) - содержат два гетероцикла. Пиримидины: тимин (Т), цитозин (Ц) и урацил (У) - содержат один гетероцикл.
Нуклеиновые кислоты являются нерегулярными полимерами, мономеры которых - нуклеотиды • • • Нуклеотид = нуклеозид + фосфорная кислота = азотистое основание+ пентоза+фосфорная кислота. В РНК пентоза - рибоза. В ДНК - дезоксирибоза. Нуклеотиды соединяются друг с другом в полимерную цепочку с помощью фосфодиэфирных связей. Азотистые основания не принимают участия в соединении нуклеотидов одной цепи. Существует два класса азотистых оснований. Пурины: аденин (А) и гуанин (Г) - содержат два гетероцикла. Пиримидины: тимин (Т), цитозин (Ц) и урацил (У) - содержат один гетероцикл.
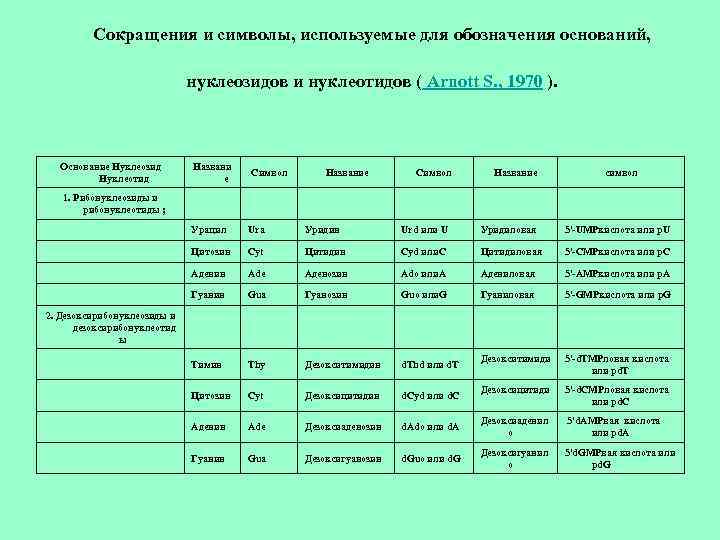 Сокращения и символы, используемые для обозначения оснований, нуклеозидов и нуклеотидов ( Arnott S. , 1970 ). Основание Нуклеозид Нуклеотид Названи е Символ Название символ 1. Рибонуклеозиды и рибонуклеотиды ; Урацил Ura Уридин Urd или U Уридиловая 5'-UMPкислота или p. U Цитозин Cyt Цитидин Cyd или. C Цитидиловая 5'-CMPкислота или p. C Аденин Ade Аденозин Ado или. A Адениловая 5'-AMPкислота или p. A Гуанин Gua Гуанозин Guo или. G Гуаниловая 5'-GMPкислота или p. G Тимин Thy Дезокситимидин d. Thd или d. T Дезокситимиди 5'-d. TMPловая кислота или pd. T Цитозин Cyt Дезоксицитидин d. Cyd или d. C Дезоксицитиди 5'-d. CMPловая кислота или pd. C Аденин Ade Дезоксиаденозин d. Ado или d. A Дезоксиаденил о 5'd. AMPвая кислота или pd. A Гуанин Gua Дезоксигуанозин d. Guo или d. G Дезоксигуанил о 5'd. GMPвая кислота или pd. G 2. Дезоксирибонуклеозиды и дезоксирибонуклеотид ы
Сокращения и символы, используемые для обозначения оснований, нуклеозидов и нуклеотидов ( Arnott S. , 1970 ). Основание Нуклеозид Нуклеотид Названи е Символ Название символ 1. Рибонуклеозиды и рибонуклеотиды ; Урацил Ura Уридин Urd или U Уридиловая 5'-UMPкислота или p. U Цитозин Cyt Цитидин Cyd или. C Цитидиловая 5'-CMPкислота или p. C Аденин Ade Аденозин Ado или. A Адениловая 5'-AMPкислота или p. A Гуанин Gua Гуанозин Guo или. G Гуаниловая 5'-GMPкислота или p. G Тимин Thy Дезокситимидин d. Thd или d. T Дезокситимиди 5'-d. TMPловая кислота или pd. T Цитозин Cyt Дезоксицитидин d. Cyd или d. C Дезоксицитиди 5'-d. CMPловая кислота или pd. C Аденин Ade Дезоксиаденозин d. Ado или d. A Дезоксиаденил о 5'd. AMPвая кислота или pd. A Гуанин Gua Дезоксигуанозин d. Guo или d. G Дезоксигуанил о 5'd. GMPвая кислота или pd. G 2. Дезоксирибонуклеозиды и дезоксирибонуклеотид ы
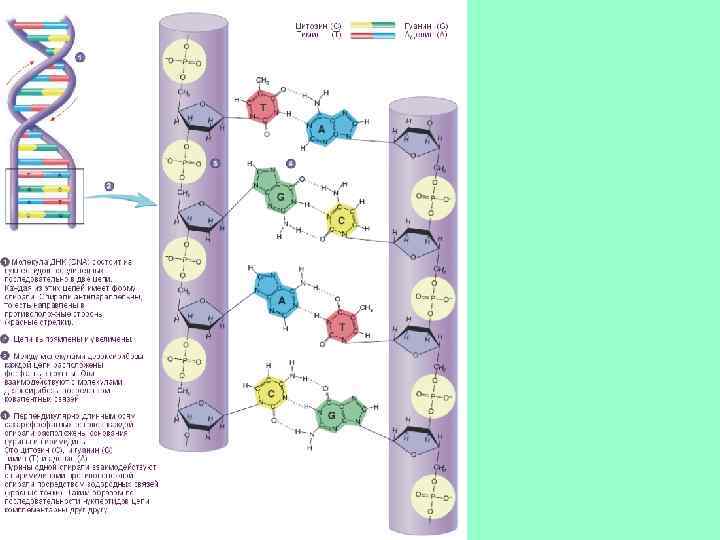
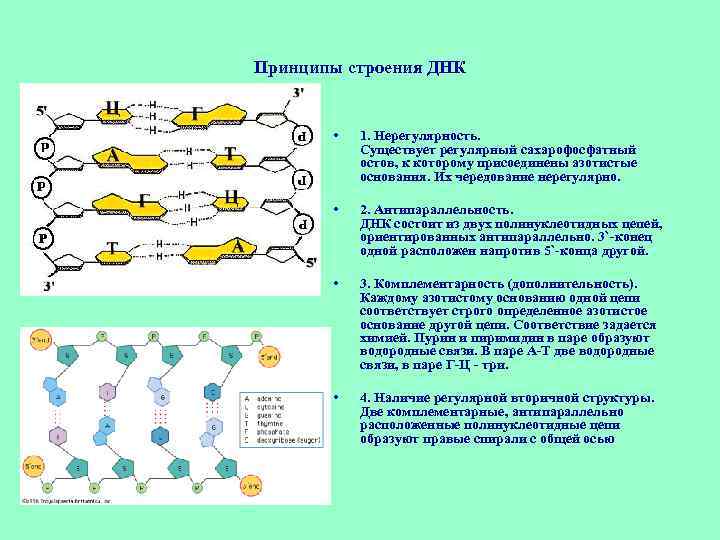 Принципы строения ДНК • 1. Нерегулярность. Существует регулярный сахарофосфатный остов, к которому присоединены азотистые основания. Их чередование нерегулярно. • 2. Антипараллельность. ДНК состоит из двух полинуклеотидных цепей, ориентированных антипараллельно. 3`-конец одной расположен напротив 5`-конца другой. • 3. Комплементарность (дополнительность). Каждому азотистому основанию одной цепи соответствует строго определенное азотистое основание другой цепи. Соответствие задается химией. Пурин и пиримидин в паре образуют водородные связи. В паре A-Т две водородные связи, в паре Г-Ц - три. • 4. Наличие регулярной вторичной структуры. Две комплементарные, антипараллельно расположенные полинуклеотидные цепи образуют правые спирали с общей осью
Принципы строения ДНК • 1. Нерегулярность. Существует регулярный сахарофосфатный остов, к которому присоединены азотистые основания. Их чередование нерегулярно. • 2. Антипараллельность. ДНК состоит из двух полинуклеотидных цепей, ориентированных антипараллельно. 3`-конец одной расположен напротив 5`-конца другой. • 3. Комплементарность (дополнительность). Каждому азотистому основанию одной цепи соответствует строго определенное азотистое основание другой цепи. Соответствие задается химией. Пурин и пиримидин в паре образуют водородные связи. В паре A-Т две водородные связи, в паре Г-Ц - три. • 4. Наличие регулярной вторичной структуры. Две комплементарные, антипараллельно расположенные полинуклеотидные цепи образуют правые спирали с общей осью
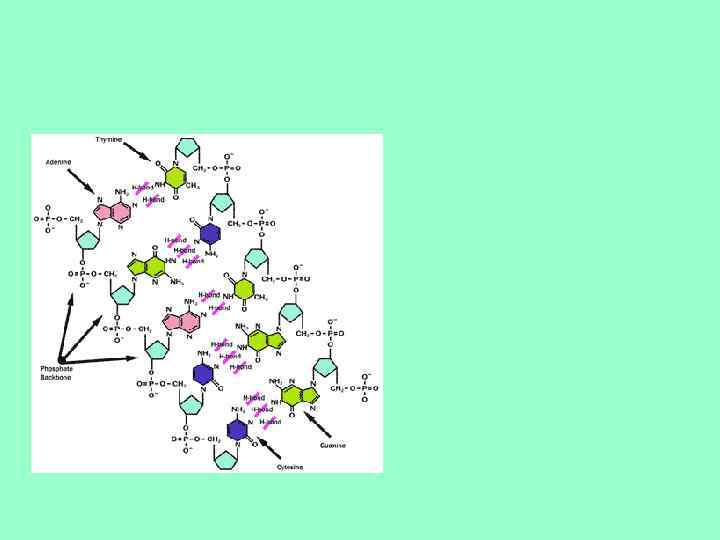
 Формы двойной спирали ДНК • • • Существуют несколько форм двойной спирали ДНК. В основной - В-форме на виток приходится 10 комплементарных пар. Плоскости азотистых оснований перпендикулярны оси спирали. Соседние комплементарные пары повернуты друг относительно друга на 36. Диаметр спирали 20Å, причем пуриновый нуклеотид занимает 12Å, а пиримидиновый - 8Å. А-форма - 11 пар азотистых оснований на виток. Плоскости азотистых оснований отклонены от нормали к оси спирали на 20. Отсюда следует наличие внутренней пустоты диаметром 5Å. Высота витка 28Å. Такие же параметры у гибрида из одной цепи ДНК и одной цепи РНК. С-форма - шаг спирали 31Å, 9. 3 пар оснований на виток, угол наклона к перпендикуляру 6. Все три формы - правозакрученные спирали. Есть еще несколько форм правых спиралей и всего одна левая спираль (Z -форма). Высота витка в Zформе -44. 5 Å, на виток приходится 12 пар нуклеотидов. Ни А-, ни Z- формы не могут существовать в водном растворе без дополнительных воздействий (белки или суперспирализация).
Формы двойной спирали ДНК • • • Существуют несколько форм двойной спирали ДНК. В основной - В-форме на виток приходится 10 комплементарных пар. Плоскости азотистых оснований перпендикулярны оси спирали. Соседние комплементарные пары повернуты друг относительно друга на 36. Диаметр спирали 20Å, причем пуриновый нуклеотид занимает 12Å, а пиримидиновый - 8Å. А-форма - 11 пар азотистых оснований на виток. Плоскости азотистых оснований отклонены от нормали к оси спирали на 20. Отсюда следует наличие внутренней пустоты диаметром 5Å. Высота витка 28Å. Такие же параметры у гибрида из одной цепи ДНК и одной цепи РНК. С-форма - шаг спирали 31Å, 9. 3 пар оснований на виток, угол наклона к перпендикуляру 6. Все три формы - правозакрученные спирали. Есть еще несколько форм правых спиралей и всего одна левая спираль (Z -форма). Высота витка в Zформе -44. 5 Å, на виток приходится 12 пар нуклеотидов. Ни А-, ни Z- формы не могут существовать в водном растворе без дополнительных воздействий (белки или суперспирализация).
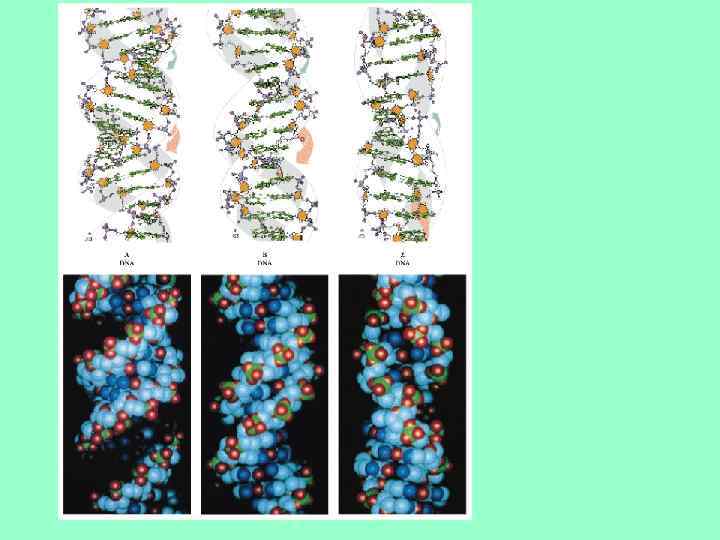
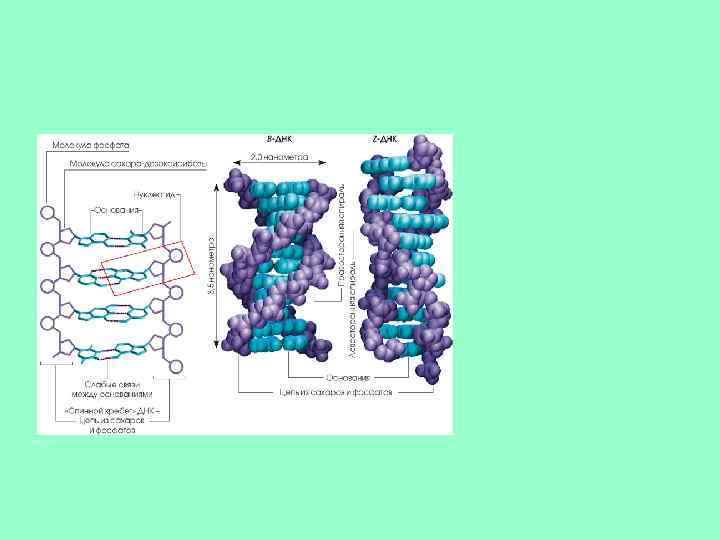
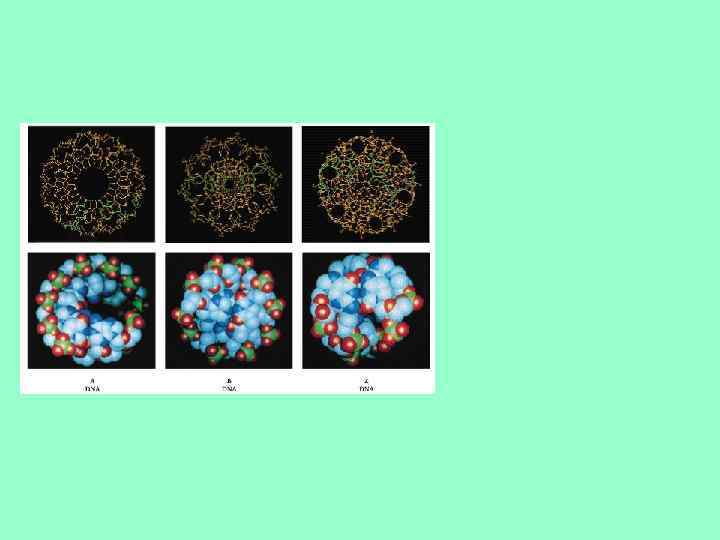
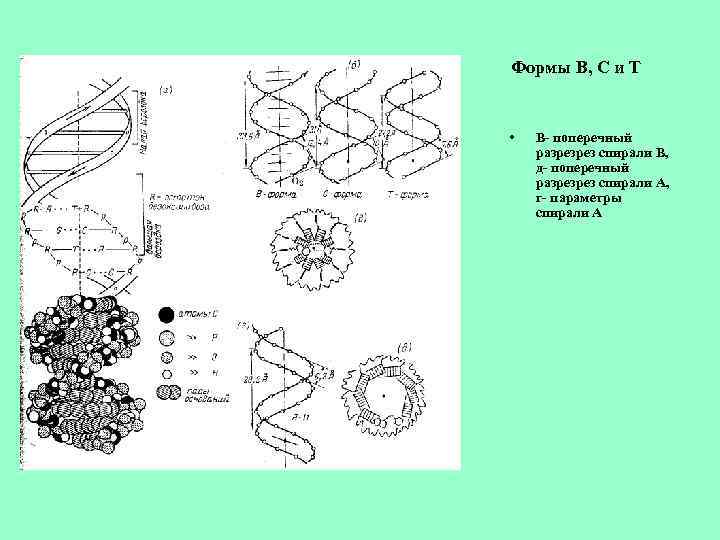 Формы В, С и Т • В- поперечный разрезрез спирали В, д- поперечный разрезрез спирали А, г- параметры спирали А
Формы В, С и Т • В- поперечный разрезрез спирали В, д- поперечный разрезрез спирали А, г- параметры спирали А
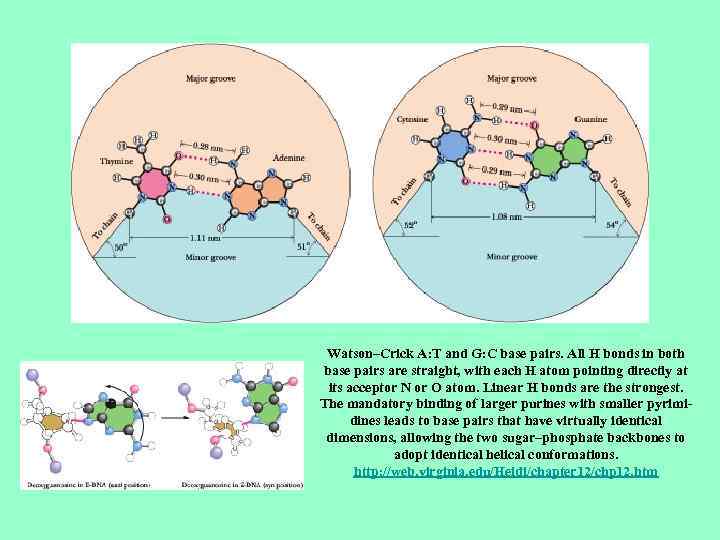 Watson–Crick A: T and G: C base pairs. All H bonds in both base pairs are straight, with each H atom pointing directly at its acceptor N or O atom. Linear H bonds are the strongest. The mandatory binding of larger purines with smaller pyrimidines leads to base pairs that have virtually identical dimensions, allowing the two sugar–phosphate backbones to adopt identical helical conformations. http: //web. virginia. edu/Heidi/chapter 12/chp 12. htm
Watson–Crick A: T and G: C base pairs. All H bonds in both base pairs are straight, with each H atom pointing directly at its acceptor N or O atom. Linear H bonds are the strongest. The mandatory binding of larger purines with smaller pyrimidines leads to base pairs that have virtually identical dimensions, allowing the two sugar–phosphate backbones to adopt identical helical conformations. http: //web. virginia. edu/Heidi/chapter 12/chp 12. htm
 • • • Шаг спирали Шаг cпирали - это расстояние вдоль оси спирали, соответствующее одному полному витку (повороту на 360 град. ). Если n - число пар нуклеотидов на один виток, а h - расстояние между двумя соседними нуклеотидами вдоль оси спирали, то шаг спирали Р будет связан с этими величинами соотношением Р=nh. Для целочисленных спиралей n целое, но вообще говоря, оно может быть любым (см. Рис. Параметры спирали ). ДНК: Угол спирального вращения (t)- это угол между двумя соседними нуклеотидами, t = 360/n, где n - число пар оснований на виток спирали (см. Рис. Параметры спирали ). основания: геометрия комплементарных Полинуклеотидные цепи в двойной спирали удерживаются вместе в результате комплементарного спаривания оснований (Рис. Схема водородных связей в РНК (ДНК)). Основания образуют комплексы, стабилизируемые водородными связями. Множество таких комплексов обнаружено при кристаллографических исследованиях как изолированных оснований, нуклеозидов и нуклеотидов , так и комплексов, составленных из двух или более соединений этого типа ( Voet D. and Rich A. , 1970 ). Если предположить, что стабильная пара оснований должна содержать как минимум две водородные связи , N-H. . . O и N-H. . . N, то четыре основания, замещенные по гликозидному азоту (N 1 в пиримидинах и N 9 в пуринах), могут образовывать 28 различных пар ( Donohue J. and Trueblood K. N. , 1960 , Donohue J. , 1956 ). Среди этих 28 пар имеются пары, не обладающие никакой симметрией, а также пары, гликозидные связи C 1'--N которых связаны осями симметрии второго порядка, которые располагаются в плоскости, перпендикулярной плоскости оснований, или в плоскости оснований. При этом в гомопуриновых и в гомопиримидиновых парах оснований ось симметрии второго порядка в точности переводит одно основание в другое. В симметричных гетеропуриновых и гетеропиримидиновых парах, а также в уотсон-криковских пурин-пиримидиновых парах ось симметрии связывает только гликозидные связи C 1'--N, но не основания в целом, и поэтому называется псевдоосью симметрии. При совместной кристаллизации мономерных производных аденина и урацила наблюдается образование пар А - U, но они никогда не являются уотсон-криковскими. Обнаруженная схема спаривания в комплексе 9 -этиладенина и 1 -метилтимина носит название хугстиновской , по имени открывшего ее в 1963 г. К. Хугстина ( Hoogsteen K. , 1963 ). При исследовании G - C пар в кристаллах наблюдается только уотсон-криковское спаривание, что, вероятно, обусловлено наличием трех водородных связей в этой структуре. Схематичное изображение уотсон-криковских пар оснований дано на Рис. Схема водородных связей в РНК(ДНК). Связи С 1'-N(гликозидные связи) каждой цепи и соответствующие сахарофосфатные остовы, находящиеся в антипараллельной ориентации, связаны псевдоосью симметрии 2 -го порядка. Такая же псевдосимметрия характерна для двухцепочечных ДНК и РНК. Обычно центр пар не совпадает с осью спирали, а смещен от нее на некоторое расстояние D (см. Рис. Геометрия связанных пар ). Кроме того, плоскость пар не строго перпендикулярна оси. Ее отклонение от перпендикулярного положения определяется двумя углами - углом наклона ( ilt) и t углом крена (roll) пары. Спаренные основания не обязятельно компланарны. Они могут быть повернуты друг относительно друга (вокруг длинной оси пары, проходящей через С 6 -атом пиримидина и С 8 -атом пурина) на угол пропеллера (propeller), который равен двугранному углу между нормалями к плоскостям оснований ( Зенгер В. , 1987 ). Молекулы двухцепочечных РНК и ДНК имеют характерные желобки.
• • • Шаг спирали Шаг cпирали - это расстояние вдоль оси спирали, соответствующее одному полному витку (повороту на 360 град. ). Если n - число пар нуклеотидов на один виток, а h - расстояние между двумя соседними нуклеотидами вдоль оси спирали, то шаг спирали Р будет связан с этими величинами соотношением Р=nh. Для целочисленных спиралей n целое, но вообще говоря, оно может быть любым (см. Рис. Параметры спирали ). ДНК: Угол спирального вращения (t)- это угол между двумя соседними нуклеотидами, t = 360/n, где n - число пар оснований на виток спирали (см. Рис. Параметры спирали ). основания: геометрия комплементарных Полинуклеотидные цепи в двойной спирали удерживаются вместе в результате комплементарного спаривания оснований (Рис. Схема водородных связей в РНК (ДНК)). Основания образуют комплексы, стабилизируемые водородными связями. Множество таких комплексов обнаружено при кристаллографических исследованиях как изолированных оснований, нуклеозидов и нуклеотидов , так и комплексов, составленных из двух или более соединений этого типа ( Voet D. and Rich A. , 1970 ). Если предположить, что стабильная пара оснований должна содержать как минимум две водородные связи , N-H. . . O и N-H. . . N, то четыре основания, замещенные по гликозидному азоту (N 1 в пиримидинах и N 9 в пуринах), могут образовывать 28 различных пар ( Donohue J. and Trueblood K. N. , 1960 , Donohue J. , 1956 ). Среди этих 28 пар имеются пары, не обладающие никакой симметрией, а также пары, гликозидные связи C 1'--N которых связаны осями симметрии второго порядка, которые располагаются в плоскости, перпендикулярной плоскости оснований, или в плоскости оснований. При этом в гомопуриновых и в гомопиримидиновых парах оснований ось симметрии второго порядка в точности переводит одно основание в другое. В симметричных гетеропуриновых и гетеропиримидиновых парах, а также в уотсон-криковских пурин-пиримидиновых парах ось симметрии связывает только гликозидные связи C 1'--N, но не основания в целом, и поэтому называется псевдоосью симметрии. При совместной кристаллизации мономерных производных аденина и урацила наблюдается образование пар А - U, но они никогда не являются уотсон-криковскими. Обнаруженная схема спаривания в комплексе 9 -этиладенина и 1 -метилтимина носит название хугстиновской , по имени открывшего ее в 1963 г. К. Хугстина ( Hoogsteen K. , 1963 ). При исследовании G - C пар в кристаллах наблюдается только уотсон-криковское спаривание, что, вероятно, обусловлено наличием трех водородных связей в этой структуре. Схематичное изображение уотсон-криковских пар оснований дано на Рис. Схема водородных связей в РНК(ДНК). Связи С 1'-N(гликозидные связи) каждой цепи и соответствующие сахарофосфатные остовы, находящиеся в антипараллельной ориентации, связаны псевдоосью симметрии 2 -го порядка. Такая же псевдосимметрия характерна для двухцепочечных ДНК и РНК. Обычно центр пар не совпадает с осью спирали, а смещен от нее на некоторое расстояние D (см. Рис. Геометрия связанных пар ). Кроме того, плоскость пар не строго перпендикулярна оси. Ее отклонение от перпендикулярного положения определяется двумя углами - углом наклона ( ilt) и t углом крена (roll) пары. Спаренные основания не обязятельно компланарны. Они могут быть повернуты друг относительно друга (вокруг длинной оси пары, проходящей через С 6 -атом пиримидина и С 8 -атом пурина) на угол пропеллера (propeller), который равен двугранному углу между нормалями к плоскостям оснований ( Зенгер В. , 1987 ). Молекулы двухцепочечных РНК и ДНК имеют характерные желобки.
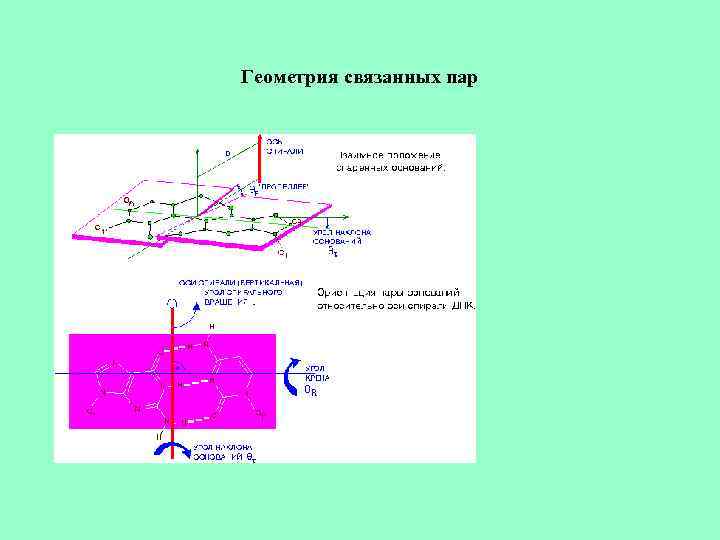 Геометрия связанных пар
Геометрия связанных пар
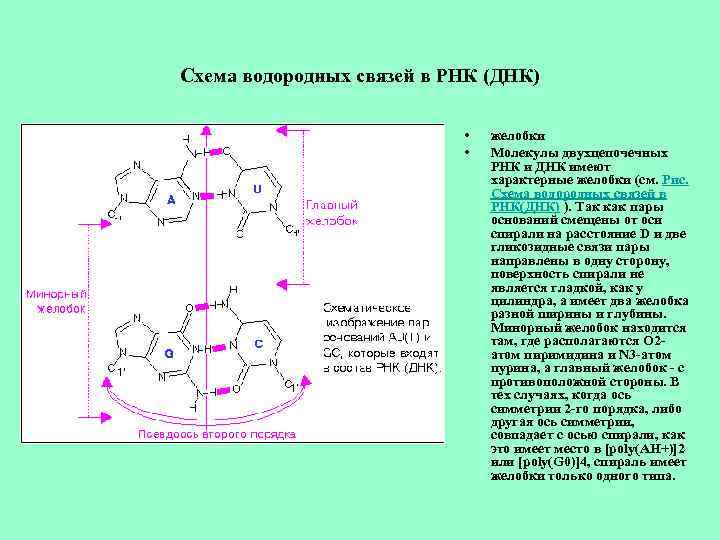 Схема водородных связей в РНК (ДНК) • • желобки Молекулы двухцепочечных РНК и ДНК имеют характерные желобки (см. Рис. Схема водородных связей в РНК(ДНК) ). Так как пары оснований смещены от оси спирали на расстояние D и две гликозидные связи пары направлены в одну сторону, поверхность спирали не является гладкой, как у цилиндра, а имеет два желобка разной ширины и глубины. Минорный желобок находится там, где располагаются О 2 атом пиримидина и N 3 -атом пурина, а главный желобок - с противоположной стороны. В тех случаях, когда ось симметрии 2 -го порядка, либо другая ось симметрии, совпадает с осью спирали, как это имеет место в [poly(AH+)]2 или [poly(G 0)]4, спираль имеет желобки только одного типа.
Схема водородных связей в РНК (ДНК) • • желобки Молекулы двухцепочечных РНК и ДНК имеют характерные желобки (см. Рис. Схема водородных связей в РНК(ДНК) ). Так как пары оснований смещены от оси спирали на расстояние D и две гликозидные связи пары направлены в одну сторону, поверхность спирали не является гладкой, как у цилиндра, а имеет два желобка разной ширины и глубины. Минорный желобок находится там, где располагаются О 2 атом пиримидина и N 3 -атом пурина, а главный желобок - с противоположной стороны. В тех случаях, когда ось симметрии 2 -го порядка, либо другая ось симметрии, совпадает с осью спирали, как это имеет место в [poly(AH+)]2 или [poly(G 0)]4, спираль имеет желобки только одного типа.
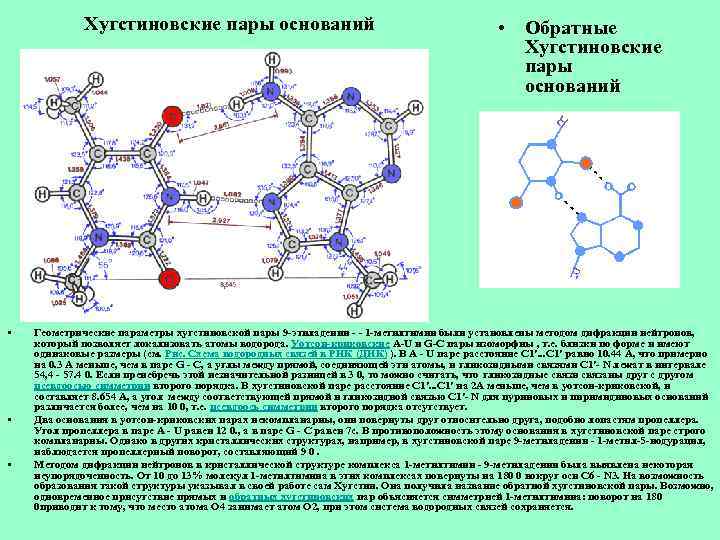 Хугстиновские пары оснований • • Обратные Хугстиновские пары оснований Геометрические параметры хугстиновской пары 9 -этиладенин - - 1 -метилтимин были установлены методом дифракции нейтронов, который позволяет локализовать атомы водорода. Уотсон-криковские А-U и G-C пары изоморфны , т. е. близки по форме и имеют одинаковые размеры (см. Рис. Схема водородных связей в РНК (ДНК) ). В А - U паре расстояние C 1'. . . C 1' равно 10. 44 А, что примерно на 0. 3 А меньше, чем в паре G - C, а углы между прямой, соединяющей эти атомы, и гликозидными связями C 1'- N лежат в интервале 54, 4 - 57. 4 0. Если пренебречь этой незначительной разницей в 3 0, то можно считать, что гликозидные связи связаны друг с другом псевдоосью симметрии второго порядка. В хугстиновской паре расстояние C 1'. . . C 1' на 2 А меньше, чем в уотсон-криковской, и составляет 8. 654 А, а угол между соответствующей прямой и гликозидной связью C 1'- N для пуриновых и пиримидиновых оснований различается более, чем на 10 0, т. е. псевдоось симметрии второго порядка отсутствует. Два основания в уотсон-криковских парах некомпланарны, они повернуты друг относительно друга, подобно лопастям пропеллера. Угол пропеллера в паре А - U равен 12 0. , а в паре G - C равен 7 c. В противоположность этому основания в хугстиновской паре строго компланарны. Однако в других кристаллических структурах, например, в хугстиновской паре 9 -метиладенин - 1 -метил-5 -иодурацил, наблюдается пропеллерный поворот, составляющий 9 0. Методом дифракции нейтронов в кристаллической структуре комплекса 1 -метилтимин - 9 -метиладенин была выявлена некоторая неупорядоченность. От 10 до 13% молекул 1 -метилтимина в этих комплексах повернуты на 180 0 вокруг оси C 6 - N 3. На возможность образования такой структуры указывал в своей работе сам Хугстин. Она получила название обратной хугстиновской пары. Возможно, одновременное присутствие прямых и обратных хугстиновских пар объясняется симметрией 1 -метилтимина: поворот на 180 0 приводит к тому, что место атома О 4 занимает атом О 2, при этом система водородных связей сохраняется.
Хугстиновские пары оснований • • Обратные Хугстиновские пары оснований Геометрические параметры хугстиновской пары 9 -этиладенин - - 1 -метилтимин были установлены методом дифракции нейтронов, который позволяет локализовать атомы водорода. Уотсон-криковские А-U и G-C пары изоморфны , т. е. близки по форме и имеют одинаковые размеры (см. Рис. Схема водородных связей в РНК (ДНК) ). В А - U паре расстояние C 1'. . . C 1' равно 10. 44 А, что примерно на 0. 3 А меньше, чем в паре G - C, а углы между прямой, соединяющей эти атомы, и гликозидными связями C 1'- N лежат в интервале 54, 4 - 57. 4 0. Если пренебречь этой незначительной разницей в 3 0, то можно считать, что гликозидные связи связаны друг с другом псевдоосью симметрии второго порядка. В хугстиновской паре расстояние C 1'. . . C 1' на 2 А меньше, чем в уотсон-криковской, и составляет 8. 654 А, а угол между соответствующей прямой и гликозидной связью C 1'- N для пуриновых и пиримидиновых оснований различается более, чем на 10 0, т. е. псевдоось симметрии второго порядка отсутствует. Два основания в уотсон-криковских парах некомпланарны, они повернуты друг относительно друга, подобно лопастям пропеллера. Угол пропеллера в паре А - U равен 12 0. , а в паре G - C равен 7 c. В противоположность этому основания в хугстиновской паре строго компланарны. Однако в других кристаллических структурах, например, в хугстиновской паре 9 -метиладенин - 1 -метил-5 -иодурацил, наблюдается пропеллерный поворот, составляющий 9 0. Методом дифракции нейтронов в кристаллической структуре комплекса 1 -метилтимин - 9 -метиладенин была выявлена некоторая неупорядоченность. От 10 до 13% молекул 1 -метилтимина в этих комплексах повернуты на 180 0 вокруг оси C 6 - N 3. На возможность образования такой структуры указывал в своей работе сам Хугстин. Она получила название обратной хугстиновской пары. Возможно, одновременное присутствие прямых и обратных хугстиновских пар объясняется симметрией 1 -метилтимина: поворот на 180 0 приводит к тому, что место атома О 4 занимает атом О 2, при этом система водородных связей сохраняется.
 Нуклеотиды • • Нуклеотиды представляют собой фосфорнокислые эфиры нуклеозидов , в которых фосфорная кислота связана сложноэфирной связью с одной из свободных гидроксильных групп сахарного кольца. Фосфорилирование дезоксирибонуклеозида может осуществляться по положениям С 3' и С 5'( система нумерации атомов в нуклеотидах дана в разделе " Нуклеиновые кислоты: символы "), так как атомы С 1' и С 4' включены в фуранозное кольцо, а атом С 2' не имеет гидроксильной группы. Оба типа замещенных фосфатов найдены в дезоксирибонуклеозидах, выделенных после гидролиза ДНК. В РНК только положения 1'и 4'недоступны для этерификации, зaмещение же по С 2', С 3' и С 5' возможно. Нуклеотиды являются сильными кислотами. Они называются, со- ответственно, адениловой, гуаниловой, тимидиловой, цитидиловой и уридиловой кислотами. С помощью фосфатных групп могут образовываться также циклические диэфиры нуклеозидов путем формирования фосфородиэфирных связей между 2'- и 3'-гидроксилами или между 3'- и 5'-гидроксилами в рибонуклеотидах и между 3'- и 5'-гидроксилами в дезоксирибонуклеотидах. Одним из таких диэфиров является аденозин-3', 5'-циклофосфат (3', 5'-АМР, с. АМР, А>p), который играет важную роль так называемого "второго посредника". В богатых энергией ди- и трифосфатах олигофосфатный остаток присоединяется к сахару по 5'-положению; в результате образуется, например, аденозинтрифосфат (ATP, ppp. A, Ado-5'PPP). В зависимости от степени гидролиза аденозинтрифосфата могут образоваться аденозиндифосфат (ADP, pp. A) или аденозинмонофосфат- адениловая кислота (5'-AMP). Аналогичным образом образуются олигофосфаты других нуклеотидов. Все они играют важную роль в биосинтезе полинуклеотидов. Особое место занимает кофермент никотинамид- адениндинуклеотид (NADP+), состоящий из разделенных пирофосфатной группировкой Ado и никотинамидрибозида (Nir): Ado-5'PP 5'-Nir.
Нуклеотиды • • Нуклеотиды представляют собой фосфорнокислые эфиры нуклеозидов , в которых фосфорная кислота связана сложноэфирной связью с одной из свободных гидроксильных групп сахарного кольца. Фосфорилирование дезоксирибонуклеозида может осуществляться по положениям С 3' и С 5'( система нумерации атомов в нуклеотидах дана в разделе " Нуклеиновые кислоты: символы "), так как атомы С 1' и С 4' включены в фуранозное кольцо, а атом С 2' не имеет гидроксильной группы. Оба типа замещенных фосфатов найдены в дезоксирибонуклеозидах, выделенных после гидролиза ДНК. В РНК только положения 1'и 4'недоступны для этерификации, зaмещение же по С 2', С 3' и С 5' возможно. Нуклеотиды являются сильными кислотами. Они называются, со- ответственно, адениловой, гуаниловой, тимидиловой, цитидиловой и уридиловой кислотами. С помощью фосфатных групп могут образовываться также циклические диэфиры нуклеозидов путем формирования фосфородиэфирных связей между 2'- и 3'-гидроксилами или между 3'- и 5'-гидроксилами в рибонуклеотидах и между 3'- и 5'-гидроксилами в дезоксирибонуклеотидах. Одним из таких диэфиров является аденозин-3', 5'-циклофосфат (3', 5'-АМР, с. АМР, А>p), который играет важную роль так называемого "второго посредника". В богатых энергией ди- и трифосфатах олигофосфатный остаток присоединяется к сахару по 5'-положению; в результате образуется, например, аденозинтрифосфат (ATP, ppp. A, Ado-5'PPP). В зависимости от степени гидролиза аденозинтрифосфата могут образоваться аденозиндифосфат (ADP, pp. A) или аденозинмонофосфат- адениловая кислота (5'-AMP). Аналогичным образом образуются олигофосфаты других нуклеотидов. Все они играют важную роль в биосинтезе полинуклеотидов. Особое место занимает кофермент никотинамид- адениндинуклеотид (NADP+), состоящий из разделенных пирофосфатной группировкой Ado и никотинамидрибозида (Nir): Ado-5'PP 5'-Nir.
 нуклеотидный состав • Для двухцепочечных молекул ДНК всегда мольные доли аденина и тимина равны, также как и мольные доли гуанина и цитозина. Этот факт, открытый и изученный Э. Чаргаффом ( правила Чаргаффа ), был одним из важнейших среди тех данных, которые привели к открытию двойной спирали ДНК. Он означает, что для описания состава молекулы ДНК необходима только одна переменная - мольная доля G+C. GC-содержание природных ДНК существенно различается. Для ДНК некоторых бактерий это 75%, у животных молекула ДНК содержит 40 -45% GC, причем ДНК близких организмов обычно имеют сходный GC- состав. Сателлитная ДНК краба, например, содержит всего 5% GC. Биологическая роль таких сателлитов недостаточно ясна, но известно, что они состоят из регулярно повторяющихся коротких последовательностей. Видимо, существование столь широкого интервала значений GC-содержания без потери способности организмов хранить необходимую генетическую информацию возможно благодаря вырожденности генетического кода и тому факту, что часть ДНК не кодирует никаких белковых последовательностей. • В состав некоторых ДНК входят необычные основания, например, в ДНК Т-четных фагов преобладает глюкозилированный 5 -гидрокси- метилцитозин. Он образует с гуанином такие же пары оснований, и правила Чаргаффа остаются справедливыми. ДНК фага SP 2 содержит урацил вместо тимина. Некоторые основания отдельных ДНК метилированы, такая модификация служит механизмом защиты против внутриклеточных рестриктаз. • Большинство природных молекул РНК являются одноцепочечными, правила Чаргаффа выполняются лишь для небольшого числа двухнитевых вирусных РНК.
нуклеотидный состав • Для двухцепочечных молекул ДНК всегда мольные доли аденина и тимина равны, также как и мольные доли гуанина и цитозина. Этот факт, открытый и изученный Э. Чаргаффом ( правила Чаргаффа ), был одним из важнейших среди тех данных, которые привели к открытию двойной спирали ДНК. Он означает, что для описания состава молекулы ДНК необходима только одна переменная - мольная доля G+C. GC-содержание природных ДНК существенно различается. Для ДНК некоторых бактерий это 75%, у животных молекула ДНК содержит 40 -45% GC, причем ДНК близких организмов обычно имеют сходный GC- состав. Сателлитная ДНК краба, например, содержит всего 5% GC. Биологическая роль таких сателлитов недостаточно ясна, но известно, что они состоят из регулярно повторяющихся коротких последовательностей. Видимо, существование столь широкого интервала значений GC-содержания без потери способности организмов хранить необходимую генетическую информацию возможно благодаря вырожденности генетического кода и тому факту, что часть ДНК не кодирует никаких белковых последовательностей. • В состав некоторых ДНК входят необычные основания, например, в ДНК Т-четных фагов преобладает глюкозилированный 5 -гидрокси- метилцитозин. Он образует с гуанином такие же пары оснований, и правила Чаргаффа остаются справедливыми. ДНК фага SP 2 содержит урацил вместо тимина. Некоторые основания отдельных ДНК метилированы, такая модификация служит механизмом защиты против внутриклеточных рестриктаз. • Большинство природных молекул РНК являются одноцепочечными, правила Чаргаффа выполняются лишь для небольшого числа двухнитевых вирусных РНК.
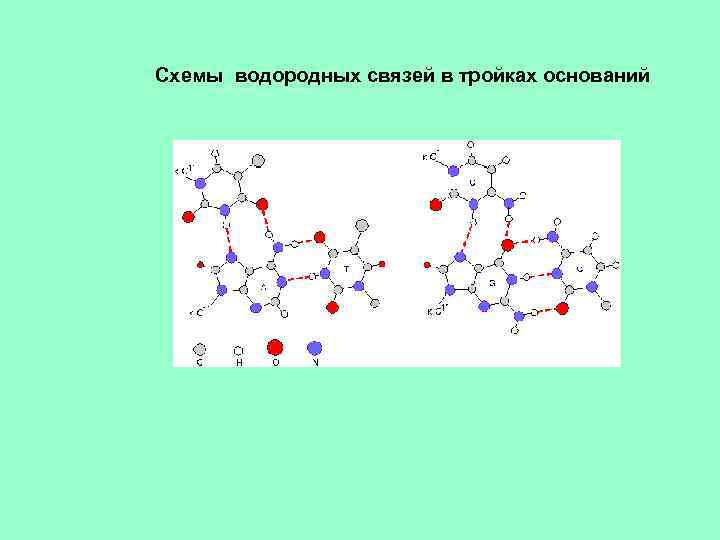 Схемы водородных связей в тройках оснований
Схемы водородных связей в тройках оснований
 • • • • • Полинуклеотидная цепь: структура Нуклеотиды , соединяясь друг с другом 3', 5'-фосфорнодиэфирной связью, образуют олигонуклеотиды (длина от 2 до 12 пар оснований) и полинуклеотиды. Линейная полимерная цепочка ДНК ( РНК ) представляет собой сахаро-фосфатный остов, к которому "привешены" основания с помощью гликозидной связи. Две такие цепочки образуют за счет спаривания комплементарных оснований ( Рис. ДНК ) как бы "лестницу", поручнями которой являются антипараллельные сахаро- фосфатные цепи, а перекладинами - пары оснований. Такая "лестница" закручивается в правую двойную спираль, пары оснований образуют стопку в центре спирали (см. ДНК и РНК ). Конформация полинуклеотидной цепи определяется набором торсионных углов (или углов вращения группы атомов относительно связи) сахарофосфатного остова. Система нумерации атомов и определение торсионных углов для полинуклеотидной цепи даны на Рис. Полинуклеотидная цепь. Вращение вокруг N-гликозидной связи : Син/анти-конформации ( Рис. Анти- и син-конформации пурина и пиримидина ). В зависимости от взаимной ориентации основания и сахарного кольца (т. е. от величины угла вращения вокруг N-гликозидной связи) в нуклеозидах различаются две основные конформации - син и анти. Они определяются торсионным углом: О 4'- С 1'- N 9 - С 4 Пурины О 4'- С 1'- N 1 - С 2 Пиримидины В анти-конформации шестичленное кольцо пурина и атом О 2 пиримидина направлены от сахара, тогда как в син-конформации они нависают над кольцом либо направлены в его сторону. Пиримидиновые нуклеозиды, как правило, находятся в анти-ориентации относительно гликозидной связи с С 3'-эндо- конформацией рибозы и С 2'-эндо- конформацией дезоксирибозы. (О конформациях сахара смотри раздел Нуклеозиды ). В случае пуриновых нуклеозидов анти- и син-конформации встречаются одинаково часто, если сахар пребывает в С 2'-эндо- конформации. В случае конформации сахара С 3'-эндо, равновесие сдвигается в сторону анти. В растворе между син- и анти-конформациями наблюдается быстрый равновесный переход. Син-конформация стабилизируется взаимодействием О 5'-H. . . N 3(пурины) и О 5'-Н. . . О 2(пиримидины), а также наличием объемных заместителей при атомах С 8 (в пуринах) и С 6 (в пиримидинах). Вращение относительно связи С 4'-C 5'. Вращение вокруг экзоциклической связи С 4'-С 5'в нуклеотидах и нуклеиновых кислотах играет решающую роль в расположении 5'- фосфатной группы относительно сахара и основания. Вращаясь вокруг связи С 4'-С 5', атом О 5' по-разному ориентируется относительно фуранозного кольца. Реально это вращение приводит к трем конформациям, которые принято описывать двумя торсионными углами: Фoo (О 5'-С 4'-О 4') и Фoc (О 5'-С 4'-С 3'), либо угловыми интервалами (+) или (-) (гош или транс) (см. Таблицу I). Для описания ориентации атома О 5' относительно связи C 4'-C 5' IUPAC-IUB ( IUPAC-IUB, 1983 ) рекомендует использовать угол Фос. Если угол вращения Фос лежит в +ск-области, основание и атом O 5' располагаются над сахарным фрагментом, а в -ск - или anобластях они направлены от сахарного фрагмента. Вращение относительно эфирных связей С-О и Р-О. Вращение вокруг связей С-О и Р-О заторможено. Ориентация фосфатных групп относительно связей С-О такова, что для С 5'-O 5'- связи торсионный угол лежит в области an, а для связи С 3'-О 3' соответствующий торсионный угол немного смещается в сторону больших углов (220 град. ), в область -ск. Из-за гош-эффекта торсионные углы, определяющие ориентацию относительно эфирных связей Р-О 5' и О 3'-Р (см. Рис. Полинуклеотидная цепь ) лежат в основном в областях +ск и -ск. В одноцепочечных полинуклеотидах ориентация относительно связей Р-О такова, что указанные выше углы лежат строго в областях -ск либо an/-ск или в области - ск/an, а в спиральных структурах со спаренными основаниями оба эти угла лежат только в
• • • • • Полинуклеотидная цепь: структура Нуклеотиды , соединяясь друг с другом 3', 5'-фосфорнодиэфирной связью, образуют олигонуклеотиды (длина от 2 до 12 пар оснований) и полинуклеотиды. Линейная полимерная цепочка ДНК ( РНК ) представляет собой сахаро-фосфатный остов, к которому "привешены" основания с помощью гликозидной связи. Две такие цепочки образуют за счет спаривания комплементарных оснований ( Рис. ДНК ) как бы "лестницу", поручнями которой являются антипараллельные сахаро- фосфатные цепи, а перекладинами - пары оснований. Такая "лестница" закручивается в правую двойную спираль, пары оснований образуют стопку в центре спирали (см. ДНК и РНК ). Конформация полинуклеотидной цепи определяется набором торсионных углов (или углов вращения группы атомов относительно связи) сахарофосфатного остова. Система нумерации атомов и определение торсионных углов для полинуклеотидной цепи даны на Рис. Полинуклеотидная цепь. Вращение вокруг N-гликозидной связи : Син/анти-конформации ( Рис. Анти- и син-конформации пурина и пиримидина ). В зависимости от взаимной ориентации основания и сахарного кольца (т. е. от величины угла вращения вокруг N-гликозидной связи) в нуклеозидах различаются две основные конформации - син и анти. Они определяются торсионным углом: О 4'- С 1'- N 9 - С 4 Пурины О 4'- С 1'- N 1 - С 2 Пиримидины В анти-конформации шестичленное кольцо пурина и атом О 2 пиримидина направлены от сахара, тогда как в син-конформации они нависают над кольцом либо направлены в его сторону. Пиримидиновые нуклеозиды, как правило, находятся в анти-ориентации относительно гликозидной связи с С 3'-эндо- конформацией рибозы и С 2'-эндо- конформацией дезоксирибозы. (О конформациях сахара смотри раздел Нуклеозиды ). В случае пуриновых нуклеозидов анти- и син-конформации встречаются одинаково часто, если сахар пребывает в С 2'-эндо- конформации. В случае конформации сахара С 3'-эндо, равновесие сдвигается в сторону анти. В растворе между син- и анти-конформациями наблюдается быстрый равновесный переход. Син-конформация стабилизируется взаимодействием О 5'-H. . . N 3(пурины) и О 5'-Н. . . О 2(пиримидины), а также наличием объемных заместителей при атомах С 8 (в пуринах) и С 6 (в пиримидинах). Вращение относительно связи С 4'-C 5'. Вращение вокруг экзоциклической связи С 4'-С 5'в нуклеотидах и нуклеиновых кислотах играет решающую роль в расположении 5'- фосфатной группы относительно сахара и основания. Вращаясь вокруг связи С 4'-С 5', атом О 5' по-разному ориентируется относительно фуранозного кольца. Реально это вращение приводит к трем конформациям, которые принято описывать двумя торсионными углами: Фoo (О 5'-С 4'-О 4') и Фoc (О 5'-С 4'-С 3'), либо угловыми интервалами (+) или (-) (гош или транс) (см. Таблицу I). Для описания ориентации атома О 5' относительно связи C 4'-C 5' IUPAC-IUB ( IUPAC-IUB, 1983 ) рекомендует использовать угол Фос. Если угол вращения Фос лежит в +ск-области, основание и атом O 5' располагаются над сахарным фрагментом, а в -ск - или anобластях они направлены от сахарного фрагмента. Вращение относительно эфирных связей С-О и Р-О. Вращение вокруг связей С-О и Р-О заторможено. Ориентация фосфатных групп относительно связей С-О такова, что для С 5'-O 5'- связи торсионный угол лежит в области an, а для связи С 3'-О 3' соответствующий торсионный угол немного смещается в сторону больших углов (220 град. ), в область -ск. Из-за гош-эффекта торсионные углы, определяющие ориентацию относительно эфирных связей Р-О 5' и О 3'-Р (см. Рис. Полинуклеотидная цепь ) лежат в основном в областях +ск и -ск. В одноцепочечных полинуклеотидах ориентация относительно связей Р-О такова, что указанные выше углы лежат строго в областях -ск либо an/-ск или в области - ск/an, а в спиральных структурах со спаренными основаниями оба эти угла лежат только в
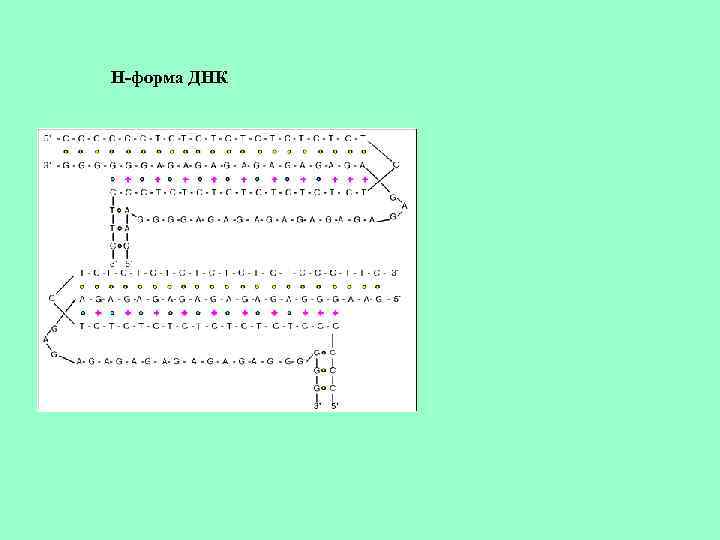 H-форма ДНК
H-форма ДНК
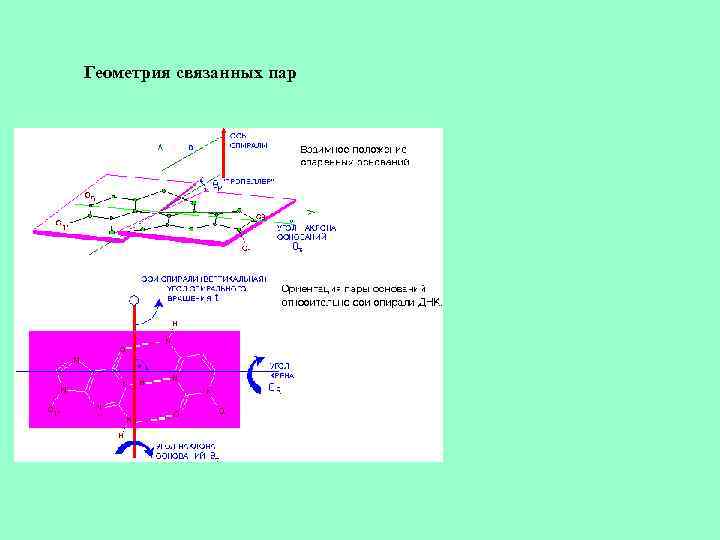 Геометрия связанных пар
Геометрия связанных пар
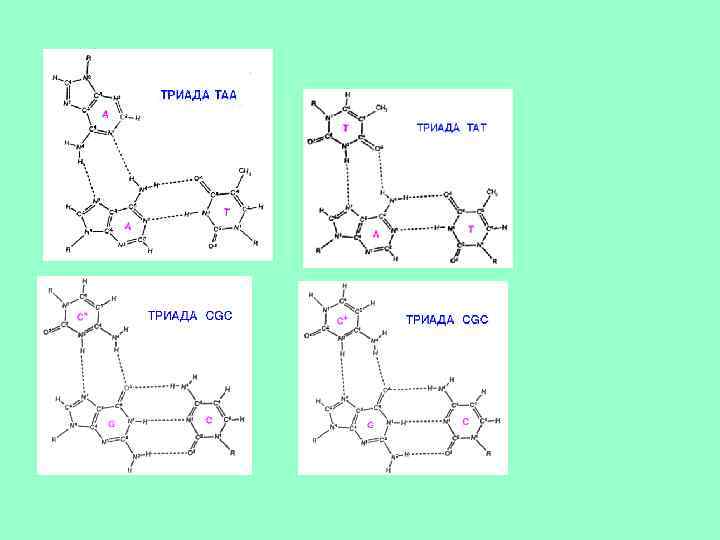
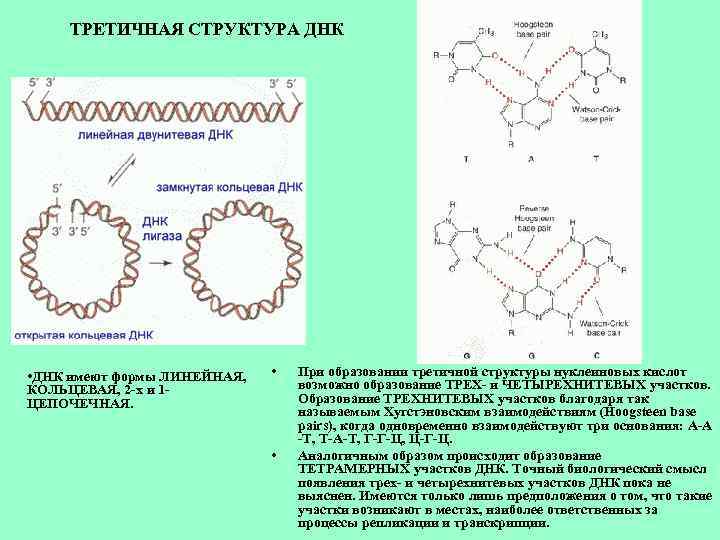 ТРЕТИЧНАЯ СТРУКТУРА ДНК • ДНК имеют формы ЛИНЕЙНАЯ, КОЛЬЦЕВАЯ, 2 -х и 1 ЦЕПОЧЕЧНАЯ. • • При образовании третичной структуры нуклеиновых кислот возможно образование ТРЕХ- и ЧЕТЫРЕХНИТЕВЫХ участков. Образование ТРЕХНИТЕВЫХ участков благодаря так называемым Хугстэновским взаимодействиям (Hoogsteen base pairs), когда одновременно взаимодействуют три основания: А-А -Т, Т-А-Т, Г-Г-Ц, Ц-Г-Ц. Аналогичным образом происходит образование ТЕТРАМЕРНЫХ участков ДНК. Точный биологический смысл появления трех- и четырехнитевых участков ДНК пока не выяснен. Имеются только лишь предположения о том, что такие участки возникают в местах, наиболее ответственных за процессы репликации и транскрипции.
ТРЕТИЧНАЯ СТРУКТУРА ДНК • ДНК имеют формы ЛИНЕЙНАЯ, КОЛЬЦЕВАЯ, 2 -х и 1 ЦЕПОЧЕЧНАЯ. • • При образовании третичной структуры нуклеиновых кислот возможно образование ТРЕХ- и ЧЕТЫРЕХНИТЕВЫХ участков. Образование ТРЕХНИТЕВЫХ участков благодаря так называемым Хугстэновским взаимодействиям (Hoogsteen base pairs), когда одновременно взаимодействуют три основания: А-А -Т, Т-А-Т, Г-Г-Ц, Ц-Г-Ц. Аналогичным образом происходит образование ТЕТРАМЕРНЫХ участков ДНК. Точный биологический смысл появления трех- и четырехнитевых участков ДНК пока не выяснен. Имеются только лишь предположения о том, что такие участки возникают в местах, наиболее ответственных за процессы репликации и транскрипции.
 Основные характеристики спиралей ДНК • В основной - В-форме на виток приходится 10 комплементарных пар. Плоскости азотистых оснований перпендикулярны оси спирали. Соседние комплементарные пары повернуты друг относительно друга на 36. Диаметр спирали 20Å, причем пуриновый нуклеотид занимает 12Å, а пиримидиновый - 8Å. • А-форма - 11 пар азотистых оснований на виток. Плоскости азотистых оснований отклонены от нормали к оси спирали на 20. Отсюда следует наличие внутренней пустоты диаметром 5Å. Высота витка 28Å. Такие же параметры у гибрида из одной цепи ДНК и одной цепи РНК. • С-форма - шаг спирали 31Å, 9. 3 пар оснований на виток, угол наклона к перпендикуляру 6. • Все три формы - правозакрученные спирали. • Есть еще несколько форм правых спиралей и всего одна левая спираль (Z -форма). Высота витка в Z-форме -44. 5 Å, на виток приходится 12 пар нуклеотидов. Ни А-, ни Z- формы не могут существовать в водном растворе без дополнительных воздействий (белки или суперспирализация).
Основные характеристики спиралей ДНК • В основной - В-форме на виток приходится 10 комплементарных пар. Плоскости азотистых оснований перпендикулярны оси спирали. Соседние комплементарные пары повернуты друг относительно друга на 36. Диаметр спирали 20Å, причем пуриновый нуклеотид занимает 12Å, а пиримидиновый - 8Å. • А-форма - 11 пар азотистых оснований на виток. Плоскости азотистых оснований отклонены от нормали к оси спирали на 20. Отсюда следует наличие внутренней пустоты диаметром 5Å. Высота витка 28Å. Такие же параметры у гибрида из одной цепи ДНК и одной цепи РНК. • С-форма - шаг спирали 31Å, 9. 3 пар оснований на виток, угол наклона к перпендикуляру 6. • Все три формы - правозакрученные спирали. • Есть еще несколько форм правых спиралей и всего одна левая спираль (Z -форма). Высота витка в Z-форме -44. 5 Å, на виток приходится 12 пар нуклеотидов. Ни А-, ни Z- формы не могут существовать в водном растворе без дополнительных воздействий (белки или суперспирализация).
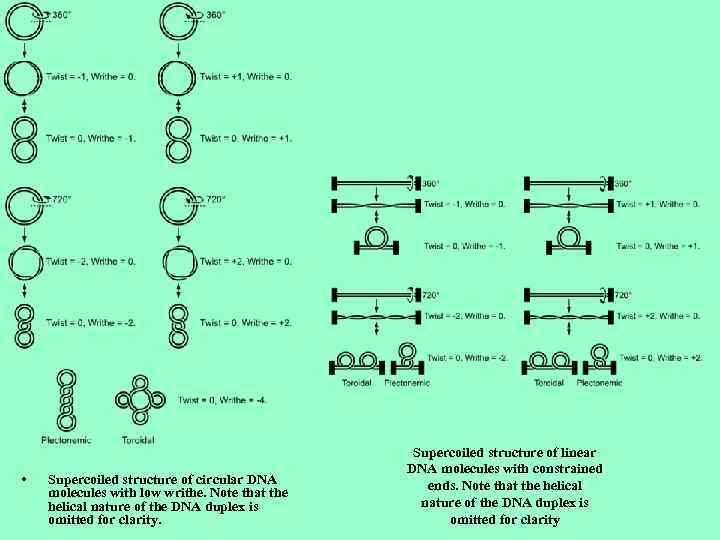 • Supercoiled structure of circular DNA molecules with low writhe. Note that the helical nature of the DNA duplex is omitted for clarity. Supercoiled structure of linear DNA molecules with constrained ends. Note that the helical nature of the DNA duplex is omitted for clarity
• Supercoiled structure of circular DNA molecules with low writhe. Note that the helical nature of the DNA duplex is omitted for clarity. Supercoiled structure of linear DNA molecules with constrained ends. Note that the helical nature of the DNA duplex is omitted for clarity
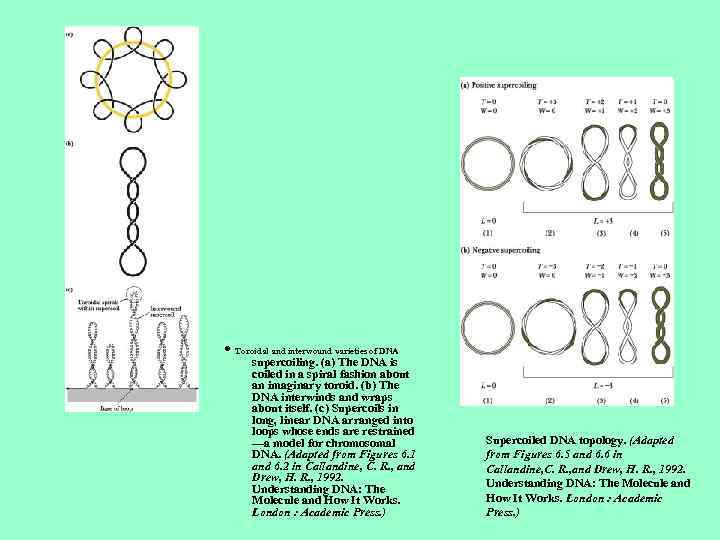 • Toroidal and interwound varieties of DNA supercoiling. (a) The DNA is coiled in a spiral fashion about an imaginary toroid. (b) The DNA interwinds and wraps about itself. (c) Supercoils in long, linear DNA arranged into loops whose ends are restrained —a model for chromosomal DNA. (Adapted from Figures 6. 1 and 6. 2 in Callandine, C. R. , and Drew, H. R. , 1992. Understanding DNA: The Molecule and How It Works. London : Academic Press. ) Supercoiled DNA topology. (Adapted from Figures 6. 5 and 6. 6 in Callandine, C. R. , and Drew, H. R. , 1992. Understanding DNA: The Molecule and How It Works. London : Academic Press. )
• Toroidal and interwound varieties of DNA supercoiling. (a) The DNA is coiled in a spiral fashion about an imaginary toroid. (b) The DNA interwinds and wraps about itself. (c) Supercoils in long, linear DNA arranged into loops whose ends are restrained —a model for chromosomal DNA. (Adapted from Figures 6. 1 and 6. 2 in Callandine, C. R. , and Drew, H. R. , 1992. Understanding DNA: The Molecule and How It Works. London : Academic Press. ) Supercoiled DNA topology. (Adapted from Figures 6. 5 and 6. 6 in Callandine, C. R. , and Drew, H. R. , 1992. Understanding DNA: The Molecule and How It Works. London : Academic Press. )
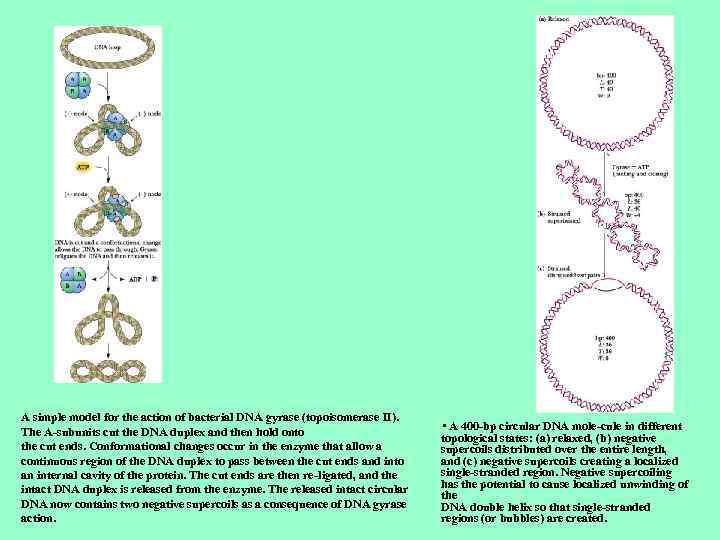 A simple model for the action of bacterial DNA gyrase (topoisomerase II). The A-subunits cut the DNA duplex and then hold onto the cut ends. Conformational changes occur in the enzyme that allow a continuous region of the DNA duplex to pass between the cut ends and into an internal cavity of the protein. The cut ends are then re-ligated, and the intact DNA duplex is released from the enzyme. The released intact circular DNA now contains two negative supercoils as a consequence of DNA gyrase action. • A 400 -bp circular DNA mole-cule in different topological states: (a) relaxed, (b) negative supercoils distributed over the entire length, and (c) negative supercoils creating a localized single-stranded region. Negative supercoiling has the potential to cause localized unwinding of the DNA double helix so that single-stranded regions (or bubbles) are created.
A simple model for the action of bacterial DNA gyrase (topoisomerase II). The A-subunits cut the DNA duplex and then hold onto the cut ends. Conformational changes occur in the enzyme that allow a continuous region of the DNA duplex to pass between the cut ends and into an internal cavity of the protein. The cut ends are then re-ligated, and the intact DNA duplex is released from the enzyme. The released intact circular DNA now contains two negative supercoils as a consequence of DNA gyrase action. • A 400 -bp circular DNA mole-cule in different topological states: (a) relaxed, (b) negative supercoils distributed over the entire length, and (c) negative supercoils creating a localized single-stranded region. Negative supercoiling has the potential to cause localized unwinding of the DNA double helix so that single-stranded regions (or bubbles) are created.
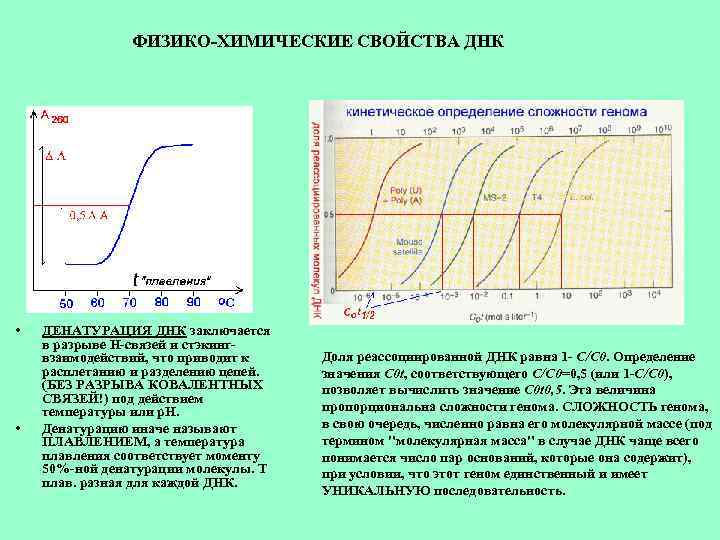 ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ДНК • • ДЕНАТУРАЦИЯ ДНК заключается в разрыве Н-связей и стэкингвзаимодействий, что приводит к расплетанию и разделению цепей. (БЕЗ РАЗРЫВА КОВАЛЕНТНЫХ СВЯЗЕЙ!) под действием температуры или р. Н. Денатурацию иначе называют ПЛАВЛЕНИЕМ, а температура плавления соответствует моменту 50%-ной денатурации молекулы. Т плав. разная для каждой ДНК. Доля реассоциированной ДНК равна 1 - C/C 0. Определение значения C 0 t, соответствующего C/C 0=0, 5 (или 1 -C/C 0), позволяет вычислить значение C 0 t 0, 5. Эта величина пропорциональна сложности генома. СЛОЖНОСТЬ генома, в свою очередь, численно равна его молекулярной массе (под термином "молекулярная масса" в случае ДНК чаще всего понимается число пар оснований, которые она содержит), при условии, что этот геном единственный и имеет УНИКАЛЬНУЮ последовательность.
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ДНК • • ДЕНАТУРАЦИЯ ДНК заключается в разрыве Н-связей и стэкингвзаимодействий, что приводит к расплетанию и разделению цепей. (БЕЗ РАЗРЫВА КОВАЛЕНТНЫХ СВЯЗЕЙ!) под действием температуры или р. Н. Денатурацию иначе называют ПЛАВЛЕНИЕМ, а температура плавления соответствует моменту 50%-ной денатурации молекулы. Т плав. разная для каждой ДНК. Доля реассоциированной ДНК равна 1 - C/C 0. Определение значения C 0 t, соответствующего C/C 0=0, 5 (или 1 -C/C 0), позволяет вычислить значение C 0 t 0, 5. Эта величина пропорциональна сложности генома. СЛОЖНОСТЬ генома, в свою очередь, численно равна его молекулярной массе (под термином "молекулярная масса" в случае ДНК чаще всего понимается число пар оснований, которые она содержит), при условии, что этот геном единственный и имеет УНИКАЛЬНУЮ последовательность.
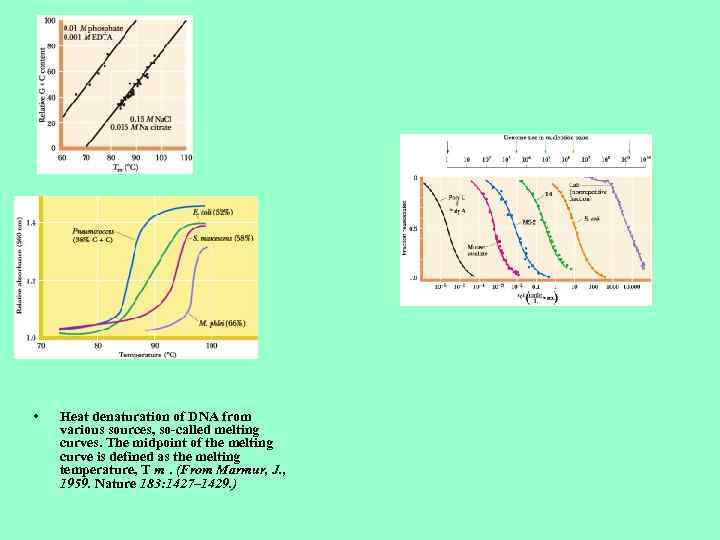 • Heat denaturation of DNA from various sources, so-called melting curves. The midpoint of the melting curve is defined as the melting temperature, T m. (From Marmur, J. , 1959. Nature 183: 1427– 1429. )
• Heat denaturation of DNA from various sources, so-called melting curves. The midpoint of the melting curve is defined as the melting temperature, T m. (From Marmur, J. , 1959. Nature 183: 1427– 1429. )
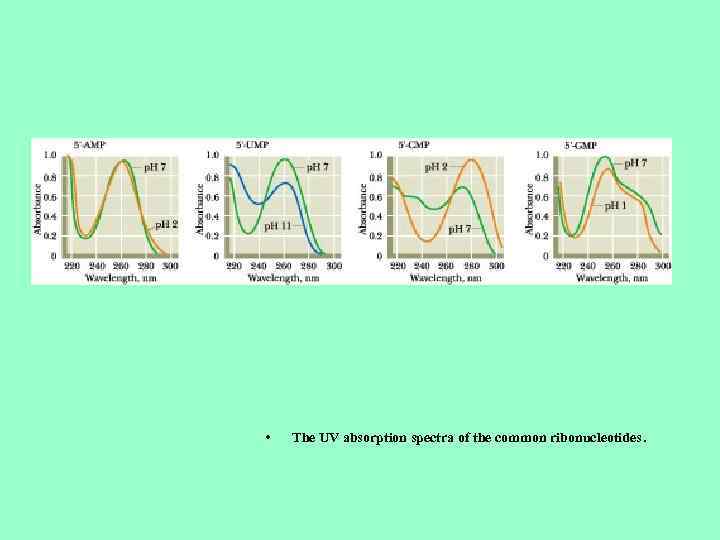 • The UV absorption spectra of the common ribonucleotides .
• The UV absorption spectra of the common ribonucleotides .
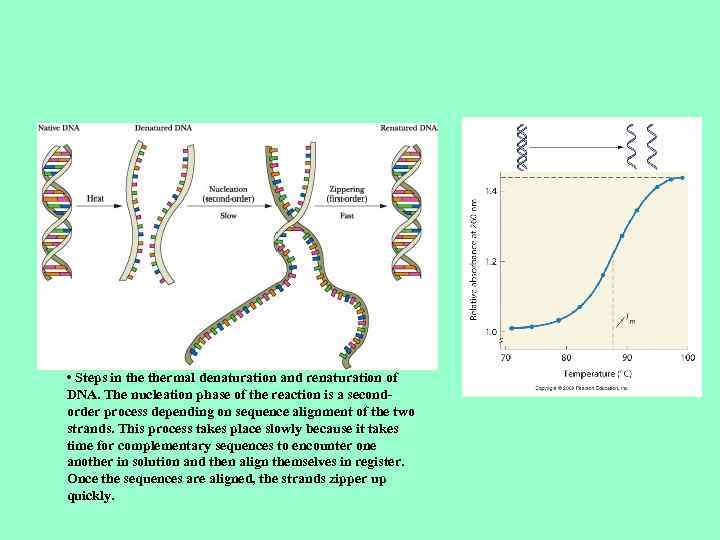 • Steps in thermal denaturation and renaturation of DNA. The nucleation phase of the reaction is a secondorder process depending on sequence alignment of the two strands. This process takes place slowly because it takes time for complementary sequences to encounter one another in solution and then align themselves in register. Once the sequences are aligned, the strands zipper up quickly.
• Steps in thermal denaturation and renaturation of DNA. The nucleation phase of the reaction is a secondorder process depending on sequence alignment of the two strands. This process takes place slowly because it takes time for complementary sequences to encounter one another in solution and then align themselves in register. Once the sequences are aligned, the strands zipper up quickly.
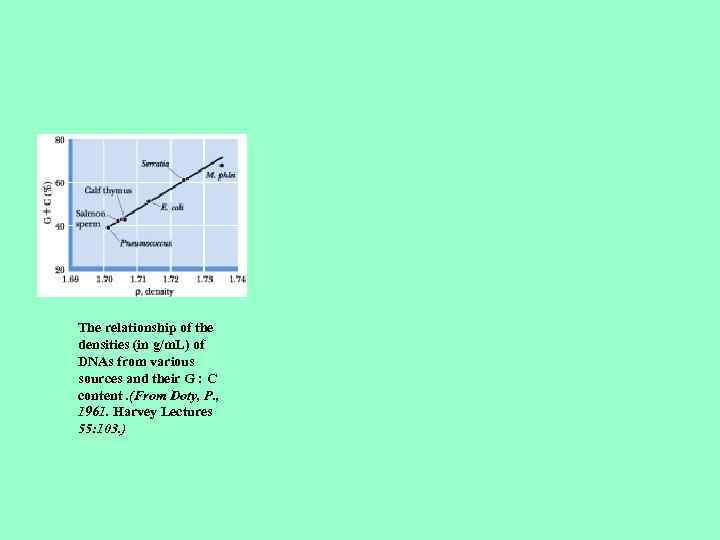 The relationship of the densities (in g/m. L) of DNAs from various sources and their G : C content. (From Doty, P. , 1961. Harvey Lectures 55: 103. )
The relationship of the densities (in g/m. L) of DNAs from various sources and their G : C content. (From Doty, P. , 1961. Harvey Lectures 55: 103. )
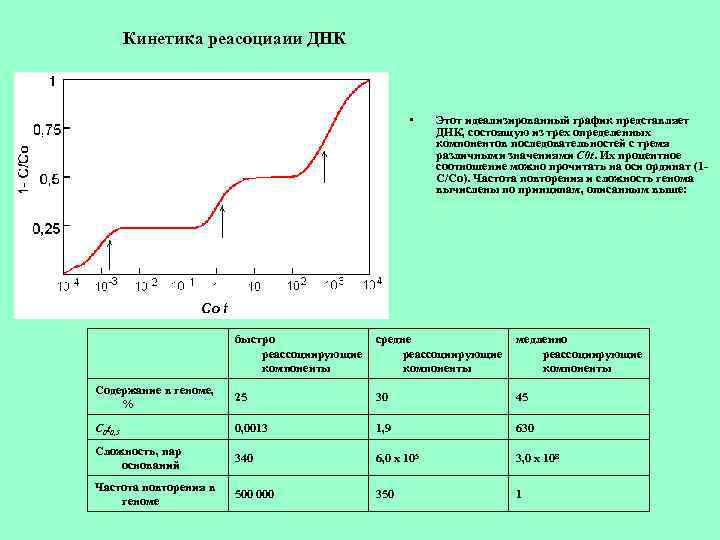 Кинетика реасоциаии ДНК • Этот идеализированный график представляет ДНК, состоящую из трех определенных компонентов последовательностей с тремя различными значениями C 0 t. Их процентное соотношение можно прочитать на оси ординат (1 С/Со). Частота повторения и сложность генома вычислены по принципам, описанным выше: быстро реассоциирующие компоненты средне реассоциирующие компоненты медленно реассоциирующие компоненты Содержание в геноме, % 25 30 45 C 0 t 0, 5 0, 0013 1, 9 630 Сложность, пар оснований 340 6, 0 х 105 3, 0 x 108 Частота повторения в геноме 500 000 350 1
Кинетика реасоциаии ДНК • Этот идеализированный график представляет ДНК, состоящую из трех определенных компонентов последовательностей с тремя различными значениями C 0 t. Их процентное соотношение можно прочитать на оси ординат (1 С/Со). Частота повторения и сложность генома вычислены по принципам, описанным выше: быстро реассоциирующие компоненты средне реассоциирующие компоненты медленно реассоциирующие компоненты Содержание в геноме, % 25 30 45 C 0 t 0, 5 0, 0013 1, 9 630 Сложность, пар оснований 340 6, 0 х 105 3, 0 x 108 Частота повторения в геноме 500 000 350 1
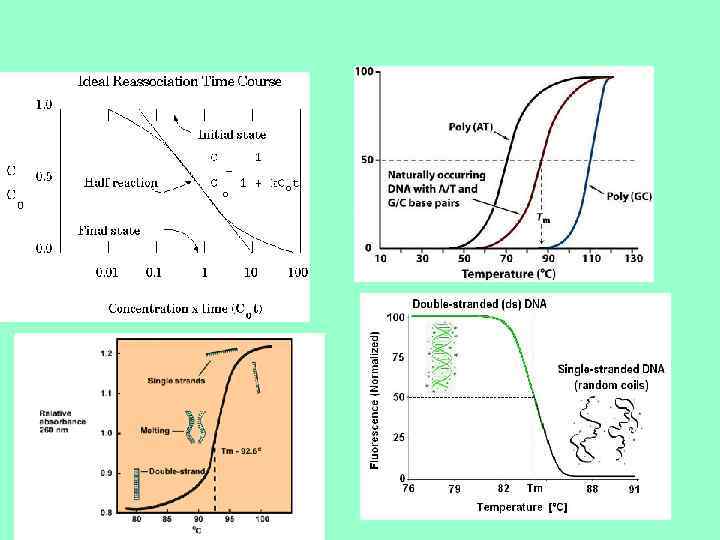
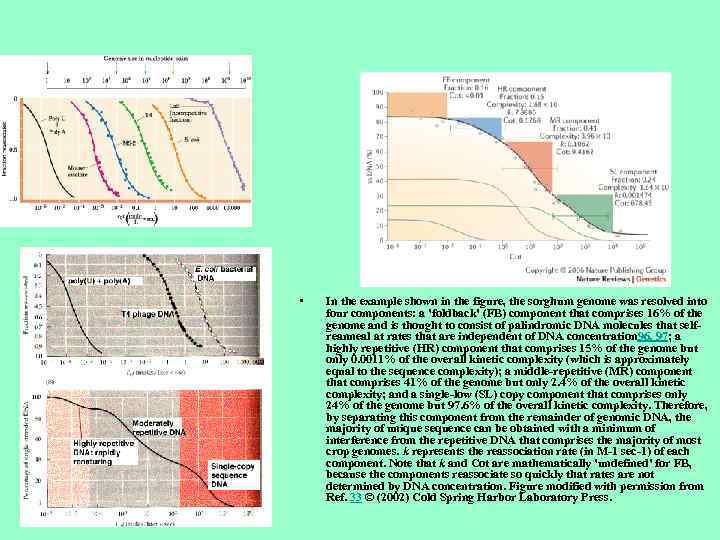 • In the example shown in the figure, the sorghum genome was resolved into four components: a 'foldback' (FB) component that comprises 16% of the genome and is thought to consist of palindromic DNA molecules that selfreanneal at rates that are independent of DNA concentration 96, 97; a highly repetitive (HR) component that comprises 15% of the genome but only 0. 0011% of the overall kinetic complexity (which is approximately equal to the sequence complexity); a middle-repetitive (MR) component that comprises 41% of the genome but only 2. 4% of the overall kinetic complexity; and a single-low (SL) copy component that comprises only 24% of the genome but 97. 6% of the overall kinetic complexity. Therefore, by separating this component from the remainder of genomic DNA, the majority of unique sequence can be obtained with a minimum of interference from the repetitive DNA that comprises the majority of most crop genomes. k represents the reassociation rate (in M-1 sec-1) of each component. Note that k and Cot are mathematically 'undefined' for FB, because the components reassociate so quickly that rates are not determined by DNA concentration. Figure modified with permission from Ref. 33 © (2002) Cold Spring Harbor Laboratory Press.
• In the example shown in the figure, the sorghum genome was resolved into four components: a 'foldback' (FB) component that comprises 16% of the genome and is thought to consist of palindromic DNA molecules that selfreanneal at rates that are independent of DNA concentration 96, 97; a highly repetitive (HR) component that comprises 15% of the genome but only 0. 0011% of the overall kinetic complexity (which is approximately equal to the sequence complexity); a middle-repetitive (MR) component that comprises 41% of the genome but only 2. 4% of the overall kinetic complexity; and a single-low (SL) copy component that comprises only 24% of the genome but 97. 6% of the overall kinetic complexity. Therefore, by separating this component from the remainder of genomic DNA, the majority of unique sequence can be obtained with a minimum of interference from the repetitive DNA that comprises the majority of most crop genomes. k represents the reassociation rate (in M-1 sec-1) of each component. Note that k and Cot are mathematically 'undefined' for FB, because the components reassociate so quickly that rates are not determined by DNA concentration. Figure modified with permission from Ref. 33 © (2002) Cold Spring Harbor Laboratory Press.
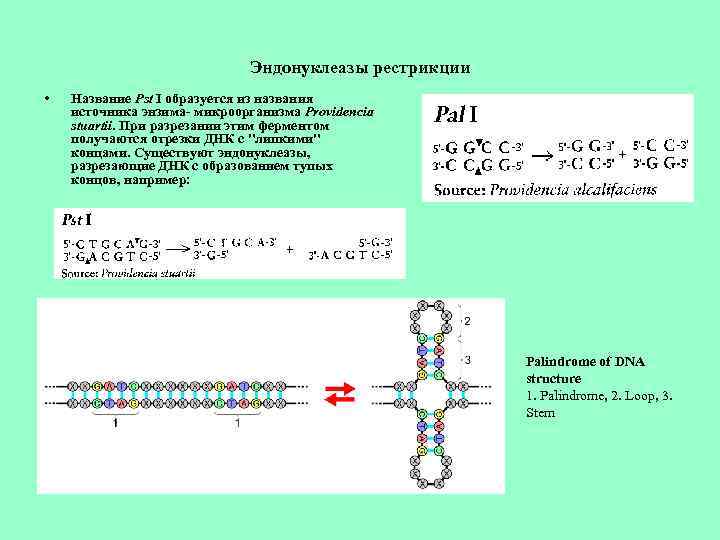 Эндонуклеазы рестрикции • Название Pst I образуется из названия источника энзима- микроорганизма Providencia stuartii. При разрезании этим ферментом получаются отрезки ДНК с "липкими" концами. Существуют эндонуклеазы, разрезающие ДНК с образованием тупых концов, например: Palindrome of DNA structure 1. Palindrome, 2. Loop, 3. Stem
Эндонуклеазы рестрикции • Название Pst I образуется из названия источника энзима- микроорганизма Providencia stuartii. При разрезании этим ферментом получаются отрезки ДНК с "липкими" концами. Существуют эндонуклеазы, разрезающие ДНК с образованием тупых концов, например: Palindrome of DNA structure 1. Palindrome, 2. Loop, 3. Stem
 Формы разрывов двухцепочечных ДНК под действием рестриктаз • а - 5'-выступающие (1), 3'-выступающие "липкие" (2) и "тупые" (3) концы ДНК, образующиеся под действием рестриктаз Bam. HI, Kpn. I и Pvu. II соответственно. Стрелками обозначены места разрывов цепей ДНК, пунктирной линией - ось симметрии сайтов рестрикции; б - лигирование с потерей сайта рестрикции
Формы разрывов двухцепочечных ДНК под действием рестриктаз • а - 5'-выступающие (1), 3'-выступающие "липкие" (2) и "тупые" (3) концы ДНК, образующиеся под действием рестриктаз Bam. HI, Kpn. I и Pvu. II соответственно. Стрелками обозначены места разрывов цепей ДНК, пунктирной линией - ось симметрии сайтов рестрикции; б - лигирование с потерей сайта рестрикции
 Эндонуклеазная активность рестриктаз • • • Специфичность узнавания последовательности ДНК и характер эндонуклеазной активности трех рестриктаз. Нае. III оставляет "тупой" конец, а другие ферменты - одноцепочечные концы. X - любой нуклеотид.
Эндонуклеазная активность рестриктаз • • • Специфичность узнавания последовательности ДНК и характер эндонуклеазной активности трех рестриктаз. Нае. III оставляет "тупой" конец, а другие ферменты - одноцепочечные концы. X - любой нуклеотид.
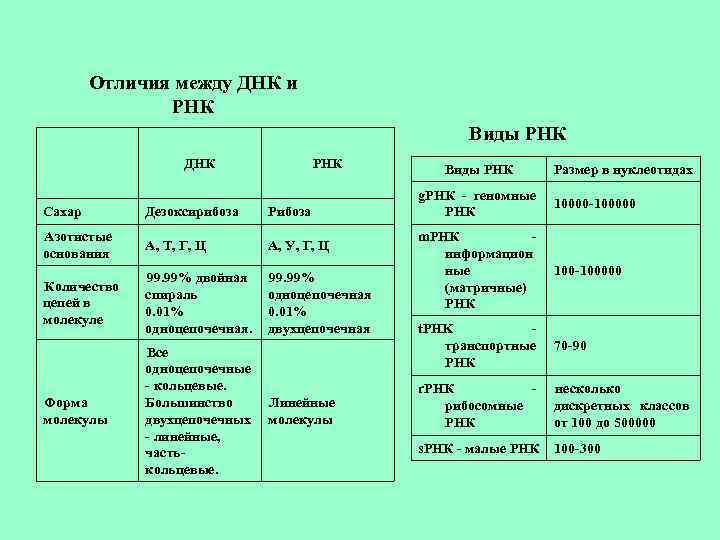 Отличия между ДНК и РНК Виды РНК ДНК РНК Сахар Дезоксирибоза Рибоза Азотистые основания А, Т, Г, Ц А, У, Г, Ц Количество цепей в молекуле 99. 99% двойная спираль 0. 01% одноцепочечная. 99. 99% одноцепочечная 0. 01% двухцепочечная Форма молекулы Все одноцепочечные - кольцевые. Линейные Большинство двухцепочечных молекулы - линейные, часть- кольцевые. Виды РНК Размер в нуклеотидах g. РНК - геномные РНК 10000 -100000 m. РНК - информацион ные (матричные) РНК 100 -100000 t. PHK - транспортные РНК 70 -90 r. РНК - рибосомные РНК несколько дискретных классов от 100 до 500000 s. РНК - малые РНК 100 -300
Отличия между ДНК и РНК Виды РНК ДНК РНК Сахар Дезоксирибоза Рибоза Азотистые основания А, Т, Г, Ц А, У, Г, Ц Количество цепей в молекуле 99. 99% двойная спираль 0. 01% одноцепочечная. 99. 99% одноцепочечная 0. 01% двухцепочечная Форма молекулы Все одноцепочечные - кольцевые. Линейные Большинство двухцепочечных молекулы - линейные, часть- кольцевые. Виды РНК Размер в нуклеотидах g. РНК - геномные РНК 10000 -100000 m. РНК - информацион ные (матричные) РНК 100 -100000 t. PHK - транспортные РНК 70 -90 r. РНК - рибосомные РНК несколько дискретных классов от 100 до 500000 s. РНК - малые РНК 100 -300
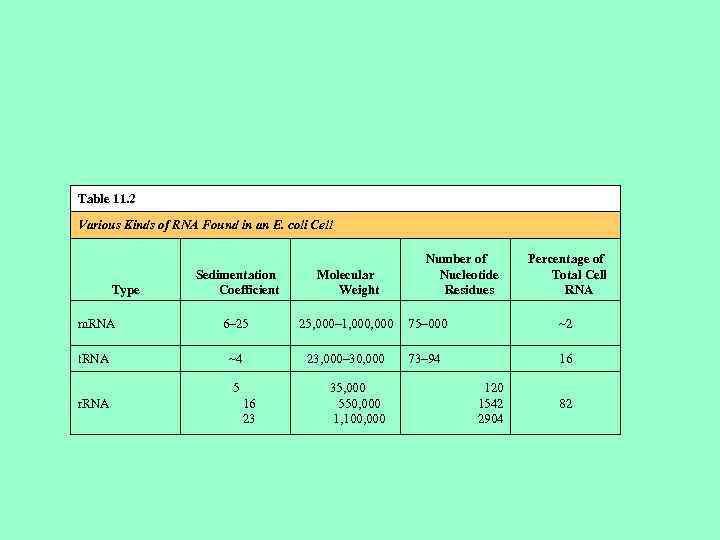 Table 11. 2 Various Kinds of RNA Found in an E. coli Cell Number of Nucleotide Residues Percentage of Total Cell RNA Sedimentation Coefficient Molecular Weight m. RNA 6– 25 25, 000– 1, 000 75– 000 ~2 t. RNA ~4 23, 000– 30, 000 73– 94 16 Type 5 r. RNA 16 23 35, 000 550, 000 1, 100, 000 120 1542 2904 82
Table 11. 2 Various Kinds of RNA Found in an E. coli Cell Number of Nucleotide Residues Percentage of Total Cell RNA Sedimentation Coefficient Molecular Weight m. RNA 6– 25 25, 000– 1, 000 75– 000 ~2 t. RNA ~4 23, 000– 30, 000 73– 94 16 Type 5 r. RNA 16 23 35, 000 550, 000 1, 100, 000 120 1542 2904 82
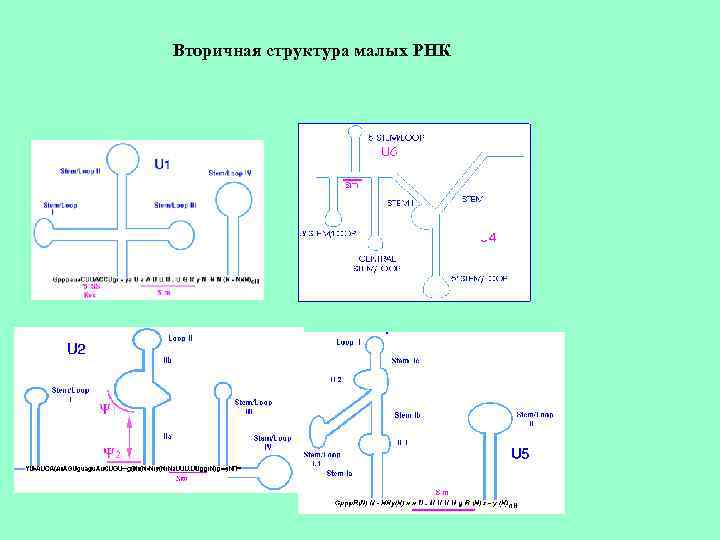 Вторичная структура малых РНК
Вторичная структура малых РНК
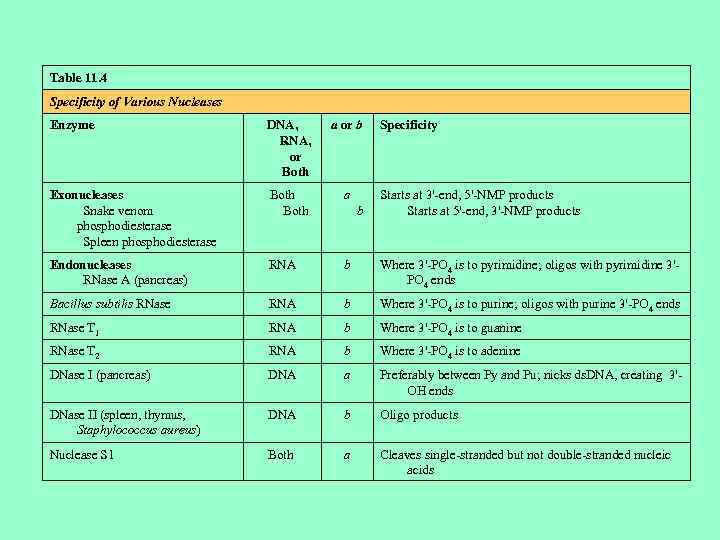 Table 11. 4 Specificity of Various Nucleases Enzyme DNA, RNA, or Both a or b Exonucleases Snake venom phosphodiesterase Spleen phosphodiesterase Both a Endonucleases RNase A (pancreas) RNA b Where 3'-PO 4 is to pyrimidine; oligos with pyrimidine 3'PO 4 ends Bacillus subtilis RNase RNA b Where 3'-PO 4 is to purine; oligos with purine 3'-PO 4 ends RNase T 1 RNA b Where 3'-PO 4 is to guanine RNase T 2 RNA b Where 3'-PO 4 is to adenine DNase I (pancreas) DNA a Preferably between Py and Pu; nicks ds. DNA, creating 3'OH ends DNase II (spleen, thymus, Staphylococcus aureus) DNA b Oligo products Nuclease S 1 Both a Cleaves single-stranded but not double-stranded nucleic acids b Specificity Starts at 3'-end, 5'-NMP products Starts at 5'-end, 3'-NMP products
Table 11. 4 Specificity of Various Nucleases Enzyme DNA, RNA, or Both a or b Exonucleases Snake venom phosphodiesterase Spleen phosphodiesterase Both a Endonucleases RNase A (pancreas) RNA b Where 3'-PO 4 is to pyrimidine; oligos with pyrimidine 3'PO 4 ends Bacillus subtilis RNase RNA b Where 3'-PO 4 is to purine; oligos with purine 3'-PO 4 ends RNase T 1 RNA b Where 3'-PO 4 is to guanine RNase T 2 RNA b Where 3'-PO 4 is to adenine DNase I (pancreas) DNA a Preferably between Py and Pu; nicks ds. DNA, creating 3'OH ends DNase II (spleen, thymus, Staphylococcus aureus) DNA b Oligo products Nuclease S 1 Both a Cleaves single-stranded but not double-stranded nucleic acids b Specificity Starts at 3'-end, 5'-NMP products Starts at 5'-end, 3'-NMP products
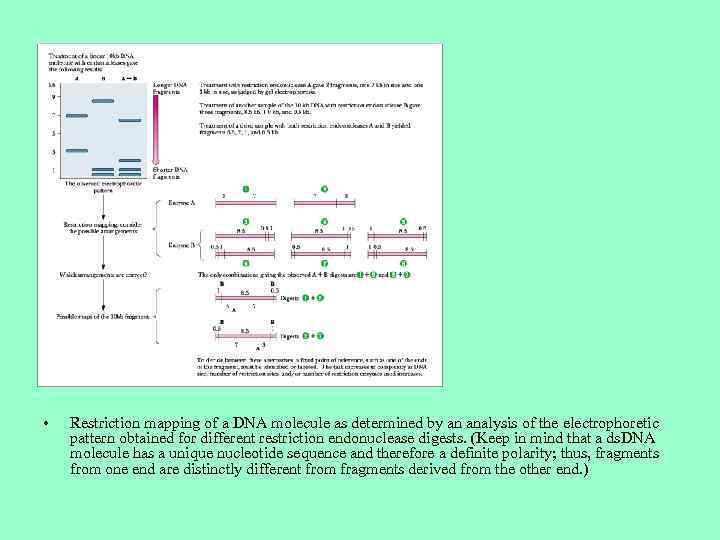 • Restriction mapping of a DNA molecule as determined by an analysis of the electrophoretic pattern obtained for different restriction endonuclease digests. (Keep in mind that a ds. DNA molecule has a unique nucleotide sequence and therefore a definite polarity; thus, fragments from one end are distinctly different from fragments derived from the other end. )
• Restriction mapping of a DNA molecule as determined by an analysis of the electrophoretic pattern obtained for different restriction endonuclease digests. (Keep in mind that a ds. DNA molecule has a unique nucleotide sequence and therefore a definite polarity; thus, fragments from one end are distinctly different from fragments derived from the other end. )
 Функции ДНК • 1. ДНК является носителем генетической информации. Функция обеспечивается фактом существования генетического кода. • 2. Воспроизведение и передача генетической информации в поколениях клеток и организмов. Функция обеспечивается процессом репликации. • 3. Реализация генетической информации в виде белков, а также любых других соединений, образующихся с помощью белков-ферментов. Функция обеспечивается процессами транскрипции и трансляции.
Функции ДНК • 1. ДНК является носителем генетической информации. Функция обеспечивается фактом существования генетического кода. • 2. Воспроизведение и передача генетической информации в поколениях клеток и организмов. Функция обеспечивается процессом репликации. • 3. Реализация генетической информации в виде белков, а также любых других соединений, образующихся с помощью белков-ферментов. Функция обеспечивается процессами транскрипции и трансляции.

 • • Джеймс Дью и Уо тсон • • • Джеймс Дью и Уо тсон (англ. James Dewey Watson, род. 6 апреля 1928, Чикаго, Иллинойс) — американский биолог. Лауреат Нобелевской премии по физиологии и медицине 1962 г. — совместно с Фрэнсисом Криком и Морисом Х. Ф. Уилкинсом за открытие структуры молекулы ДНК. С детства, благодаря отцу, Джеймс был зачарован наблюдениями за жизнью птиц. В возрасте 12 лет Уотсон участвовал в популярной радиовикторине Quiz Kids для интеллектуальных молодых людей. Благодаря либеральной политике Роберта Хатчинса он поступил в колледж в возрасте 15 лет. Прочитав книгу Эрвина Шрёдингера «Что такое жизнь с точки зрения физики? » Уотсон изменил свои профессиональные интересы с изучения орнитологии на изучение генетики. В 1947 году получил степень бакалавра зоологии в университете Чикаго. В 1951 году поступил в Кавендишскую лабораторию Кембриджского университета, где изучал структуру белков. Там познакомился с физиком Фрэнсисом Криком, который интересовался биологией. В 1952 году Уотсон и Крик стали работать над моделированием структуры ДНК. Используя Правила Чаргаффа и рентгенограммы Розалинды Франклин и Мориса Уилкинса построили двухспиральную модель. Результаты работы опубликовали в апреле 1953 года в журнале Nature. 25 лет руководил научным институтом Колд Спринг Харбор, где вел исследования генетики рака. С 1989 года по 1992 год — организатор и руководитель проекта «Геном человека» по расшифровке последовательности человеческой ДНК, в это же время возглавляет секретный проект «Фауст» [1][неавторитетный источник? 15 дней] В 2007 году высказался в пользу того, что представители разных рас имеют различные интеллектуальные способности, что обусловлено генетически. В связи с нарушением политкорректности от него потребовали публичных извинений, а в октябре 2007 года Уотсон официально ушел с поста руководителя лаборатории, где он работал. Вместе с тем он продолжает руководить исследованиями в той же лаборатории. По сообщению издания «Индепендент» , исследование ДНК самого Джеймса Уотсона обнаружило высокую концентрацию африканских и, в меньшей мере, азиатских генов[1]. Позже выяснилось, что анализ базировался на ошибочной версии генома. [2] Сейчас работает над поиском генов психических заболеваний. [3] Википедия
• • Джеймс Дью и Уо тсон • • • Джеймс Дью и Уо тсон (англ. James Dewey Watson, род. 6 апреля 1928, Чикаго, Иллинойс) — американский биолог. Лауреат Нобелевской премии по физиологии и медицине 1962 г. — совместно с Фрэнсисом Криком и Морисом Х. Ф. Уилкинсом за открытие структуры молекулы ДНК. С детства, благодаря отцу, Джеймс был зачарован наблюдениями за жизнью птиц. В возрасте 12 лет Уотсон участвовал в популярной радиовикторине Quiz Kids для интеллектуальных молодых людей. Благодаря либеральной политике Роберта Хатчинса он поступил в колледж в возрасте 15 лет. Прочитав книгу Эрвина Шрёдингера «Что такое жизнь с точки зрения физики? » Уотсон изменил свои профессиональные интересы с изучения орнитологии на изучение генетики. В 1947 году получил степень бакалавра зоологии в университете Чикаго. В 1951 году поступил в Кавендишскую лабораторию Кембриджского университета, где изучал структуру белков. Там познакомился с физиком Фрэнсисом Криком, который интересовался биологией. В 1952 году Уотсон и Крик стали работать над моделированием структуры ДНК. Используя Правила Чаргаффа и рентгенограммы Розалинды Франклин и Мориса Уилкинса построили двухспиральную модель. Результаты работы опубликовали в апреле 1953 года в журнале Nature. 25 лет руководил научным институтом Колд Спринг Харбор, где вел исследования генетики рака. С 1989 года по 1992 год — организатор и руководитель проекта «Геном человека» по расшифровке последовательности человеческой ДНК, в это же время возглавляет секретный проект «Фауст» [1][неавторитетный источник? 15 дней] В 2007 году высказался в пользу того, что представители разных рас имеют различные интеллектуальные способности, что обусловлено генетически. В связи с нарушением политкорректности от него потребовали публичных извинений, а в октябре 2007 года Уотсон официально ушел с поста руководителя лаборатории, где он работал. Вместе с тем он продолжает руководить исследованиями в той же лаборатории. По сообщению издания «Индепендент» , исследование ДНК самого Джеймса Уотсона обнаружило высокую концентрацию африканских и, в меньшей мере, азиатских генов[1]. Позже выяснилось, что анализ базировался на ошибочной версии генома. [2] Сейчас работает над поиском генов психических заболеваний. [3] Википедия
 • • Фрэнсис Крик • • • Фрэнсис Крик (англ. Francis Crick, 8 июня 1916, Нортгемптон — 28 июля 2004, Сан-Диего, Калифорния) — британский молекулярный биолог, врач и нейробиолог. Лауреат Нобелевской премии по физиологии и медицине 1962 г. — совместно с Джеймсом Д. Уотсоном и Морисом Х. Ф. Уилкинсом с формулировкой «за открытия, касающиеся молекулярной структуры нуклеиновых кислот и их значения для передачи информации в живых системах» . [1] Такжи Крик известен тем, что сформулировал центральную догму молекулярной биологии В статье, опубликованной в журнале Nature в 1961 году, Крик с соавторами предположили четыре свойства генетического кода[2]: три азотистых основания (триплет) кодируют одну аминокислоту триплеты генетического кода не перекрываются последовательности триплетов считываются с определенной начальной точки, знаки препинания внутри кодирующей последовательности отсутствуют генетический код вырожден — одна аминокислота может быть закодирована разными триплетами Википедия
• • Фрэнсис Крик • • • Фрэнсис Крик (англ. Francis Crick, 8 июня 1916, Нортгемптон — 28 июля 2004, Сан-Диего, Калифорния) — британский молекулярный биолог, врач и нейробиолог. Лауреат Нобелевской премии по физиологии и медицине 1962 г. — совместно с Джеймсом Д. Уотсоном и Морисом Х. Ф. Уилкинсом с формулировкой «за открытия, касающиеся молекулярной структуры нуклеиновых кислот и их значения для передачи информации в живых системах» . [1] Такжи Крик известен тем, что сформулировал центральную догму молекулярной биологии В статье, опубликованной в журнале Nature в 1961 году, Крик с соавторами предположили четыре свойства генетического кода[2]: три азотистых основания (триплет) кодируют одну аминокислоту триплеты генетического кода не перекрываются последовательности триплетов считываются с определенной начальной точки, знаки препинания внутри кодирующей последовательности отсутствуют генетический код вырожден — одна аминокислота может быть закодирована разными триплетами Википедия
 • • Уилкинс Морис Хью Фредерик • Уилкинс (Wilkins) Морис Хью Фредерик (15. 12. 1916, Понгароа, Новая Зеландия), английский биофизик, удостоенный в 1962 Нобелевской премии по физиологии и медицине (совместно с Дж. Уотсоном и Ф. Криком) за открытия в области молекулярной генетики. Вместе с семьёй в возрасте шести лет переехал в Англию. Окончил Кембриджский университет; в 1940 получил степень доктора философии в Бирмингемском университете. Во время Второй мировой войны занимался радарами. В течение двух лет работал в Калифорнийском университете в Беркли в рамках Манхаттанского проекта. С 1946 работал в Кингз-колледже в Лондоне (с 1962 возглавлял отдел молекулярной биологии, с 1970 – профессор биофизики, с 1981 – почётный профессор). Уилкинс известен своими работами по рентгеноструктурному анализу дезоксирибонуклеиновой кислоты (ДНК). Исследуя рассеяние рентгеновских лучей на кристаллах ДНК, он со своими коллегами по Кингзколледжу получил данные, свидетельствующие о том, что молекула ДНК – регулярная структура, имеющая форму спирали. Эти результаты послужили основанием для построения Уотсоном и Криком знаменитой модели ДНК – двойной спирали. Впоследствии Уилкинс исследовал структуру рибонуклеиновых кислот (РНК) – молекул, участвующих в синтезе белков в клетке. Автор ряда работ по биофизике нервной системы. Выдающиеся биологи
• • Уилкинс Морис Хью Фредерик • Уилкинс (Wilkins) Морис Хью Фредерик (15. 12. 1916, Понгароа, Новая Зеландия), английский биофизик, удостоенный в 1962 Нобелевской премии по физиологии и медицине (совместно с Дж. Уотсоном и Ф. Криком) за открытия в области молекулярной генетики. Вместе с семьёй в возрасте шести лет переехал в Англию. Окончил Кембриджский университет; в 1940 получил степень доктора философии в Бирмингемском университете. Во время Второй мировой войны занимался радарами. В течение двух лет работал в Калифорнийском университете в Беркли в рамках Манхаттанского проекта. С 1946 работал в Кингз-колледже в Лондоне (с 1962 возглавлял отдел молекулярной биологии, с 1970 – профессор биофизики, с 1981 – почётный профессор). Уилкинс известен своими работами по рентгеноструктурному анализу дезоксирибонуклеиновой кислоты (ДНК). Исследуя рассеяние рентгеновских лучей на кристаллах ДНК, он со своими коллегами по Кингзколледжу получил данные, свидетельствующие о том, что молекула ДНК – регулярная структура, имеющая форму спирали. Эти результаты послужили основанием для построения Уотсоном и Криком знаменитой модели ДНК – двойной спирали. Впоследствии Уилкинс исследовал структуру рибонуклеиновых кислот (РНК) – молекул, участвующих в синтезе белков в клетке. Автор ряда работ по биофизике нервной системы. Выдающиеся биологи
 • • Розалинда получала лучшие в мире рентгенограммы ДНК • Розалинд Франклин (англ. Rosalind Franklin) (25 июля 1920 — 16 апреля 1958) — английский биофизик и учёный-рентгенограф, занималась изучением структуры ДНК. Родилась в Лондоне в состоятельной еврейской семье. Окончив школу, поступила в Кембриджский университет, где получила звание кандидата наук по физической химии. После войны переехала в Париж, где занималась исследованиями в области применения рентгеноструктурного анализа. В 1950 году вернулась в Англию для работы в Лондонском университете над исследованием структуры ДНК. Сделанные Розалиндой Франклин снимки отличались особой чёткостью и, по некоторым сведениям, послужили основанием для выводов о структуре ДНК, сделанных и опубликованных впоследствии в журнале «Nature» работавшими в Кавендишской лаборатории Кембриджского университета Джеймсом Уотсоном и Фрэнсисом Криком. За это открытие Уотсон и Крик получили Нобелевскую премию в 1962 году. Розалинды Франклин к тому моменту уже не было в живых. Частый контакт с рентгеновским излучением стал причиной ракового заболевания, от которого она скончалась 16 апреля 1958 года в возрасте 37 лет. В 2002 году вышла книга Брэнды Мэдокс «Розалинд Франклин: забытая леди ДНК» , в которой были освещены ранее неизвестные подробности работы Розалинды Франклин и её причастности к открытию структуры ДНК.
• • Розалинда получала лучшие в мире рентгенограммы ДНК • Розалинд Франклин (англ. Rosalind Franklin) (25 июля 1920 — 16 апреля 1958) — английский биофизик и учёный-рентгенограф, занималась изучением структуры ДНК. Родилась в Лондоне в состоятельной еврейской семье. Окончив школу, поступила в Кембриджский университет, где получила звание кандидата наук по физической химии. После войны переехала в Париж, где занималась исследованиями в области применения рентгеноструктурного анализа. В 1950 году вернулась в Англию для работы в Лондонском университете над исследованием структуры ДНК. Сделанные Розалиндой Франклин снимки отличались особой чёткостью и, по некоторым сведениям, послужили основанием для выводов о структуре ДНК, сделанных и опубликованных впоследствии в журнале «Nature» работавшими в Кавендишской лаборатории Кембриджского университета Джеймсом Уотсоном и Фрэнсисом Криком. За это открытие Уотсон и Крик получили Нобелевскую премию в 1962 году. Розалинды Франклин к тому моменту уже не было в живых. Частый контакт с рентгеновским излучением стал причиной ракового заболевания, от которого она скончалась 16 апреля 1958 года в возрасте 37 лет. В 2002 году вышла книга Брэнды Мэдокс «Розалинд Франклин: забытая леди ДНК» , в которой были освещены ранее неизвестные подробности работы Розалинды Франклин и её причастности к открытию структуры ДНК.
 • • Чаргафф Эрвин (Chargaff) (р. 1905 на территории нынешней Украины), американский биохимик. По происхождению австриец. С 1928 в США. Исследовал химический состав и структуру нуклеиновых кислот. Определил количественное соотношение азотистых оснований, входящих в их состав (правило Чаргаффа), установил видовую специфичность ДНК. 1945 год (события в Японии) сильно повлиял на представление Чаргаффа о роли науки. Он понял, что это не новый вид бизнеса, а часть общечеловеческой культуры. Возможно, после этих событий у ученого проснулся талант публициста. Это уже не ученому, а публицисту Ервину Чаргаффу принадлежат слова: "уровень развития государства определяется тремя составляющими: отношением к деревьям отношением к детям отношением к родному языку. "
• • Чаргафф Эрвин (Chargaff) (р. 1905 на территории нынешней Украины), американский биохимик. По происхождению австриец. С 1928 в США. Исследовал химический состав и структуру нуклеиновых кислот. Определил количественное соотношение азотистых оснований, входящих в их состав (правило Чаргаффа), установил видовую специфичность ДНК. 1945 год (события в Японии) сильно повлиял на представление Чаргаффа о роли науки. Он понял, что это не новый вид бизнеса, а часть общечеловеческой культуры. Возможно, после этих событий у ученого проснулся талант публициста. Это уже не ученому, а публицисту Ервину Чаргаффу принадлежат слова: "уровень развития государства определяется тремя составляющими: отношением к деревьям отношением к детям отношением к родному языку. "

 • • • Взаимодействия между основаниями могут быть двух типов: а) между основаниями, лежащими в одной плоскости, - горизонтальное взаимодействие, реализующееся путем образования водородных связей , и б) между основаниями, уложенными одно над другим, - стэкинг-взаимодействие, которое обусловлено в основном дисперсионными лондоновскими силами и гидрофобными эффектами. "Горизонтальная" ассоциация оснований наблюдается в неводных растворах, а также в газообразном и кристаллическом состояниях. Помимо этого, в твердой фазе основания почти всегда располагаются параллельно одно над другим на расстоянии вандерваальсового радиуса, приблизительно 3. 4 А. Такое расположение является результатом не горизонтальных, а вертикальных взаимодействий. Стопки образуются и в водных растворах, преобладают они и в кристаллических структурах. При этом оказывается, что стэкинг-взаимодействие между основаниями довольно специфично: полярные заместители одного основания, -NH 2, =N-, =O или галогены, нависают над ароматическим кольцом соседнего основания. Такого рода специфичность стэкинга даже более выражена, чем специфичность при образовании водородных связей. Например, в кристаллах дезоксиаденозинмоногидрата, аденозин-5'-фосфата, аденозин- 5'-бромурацила пурины вступают в стэкингвзаимодействие по одной и той же схеме, хотя пространственная группа кристаллов, размеры элементарной ячейки, молекулярная упаковка и система водородных связей различаются. Специфичность стэкинга проявляется также и в галогензамещенных основаниях. Атомы галогенов располагаются над примыкающими ароматическими гетероциклами на расстоянии, даже меньшем чем сумма вандерваальсовых радиусов для атомов галогена и атомов гетероцикла. Такая специфичность связана с электронной структурой оснований и определяется главным образом диполь-дипольными взаимодействиями и дисперсионными лондоновскими силами. В кристаллах некоторых протонированных пиримидиновых оснований и нуклеотидов стэкинг не наблюдается вообще. Это позволяет думать, что заряженные пиримидины не вступают в стэкинг-взаимодействие. В случае протонированных пуринов стэкинг тем не менее имеет место, но носит другой характер, чем у незаряженных пуринов: атом N нависает над атомом N 7 примыкающего основания. Анализ типов стэкинга в кристаллах оснований, нуклеозидов и нуклеотидов показывает, что, по-видимому, главную роль в стабилизации стэкинга играет взаимодействие между постоянными и индуцированными диполями; в роли постоянного диполя, влияющего на пи-злектронную систему соседнего основания, выступают группы C=O и C-NH 2. В водных растворах основания и нуклеозиды образуют ассоциаты с помощью вертикальных взаимодействий, причем помимо димеров образуются ассоциаты более высокого порядка. Процесс образования стопок обратим, причем увеличение свободной энергии на всех этапах одинаково, что означает, что присоединение одного основания к другому основанию или к стопке оснований носит аддитивный, некооперативный характер, так что процесс можно считать изодесмическим. Исследования методом ЯМР показывают, что в стэкинге принимает участие шестичленное пиримидиновое, а не пятичленное имидазольное кольцо и что ориентация гетероцикла в стопке зависит от типа основания. Процесс агрегации лимитируется только диффузией, в его основе лежат слабые взаимодействия. Интенсивность стэкинга между пуриновыми и пиримидиновыми основаниями уменьшается в следующем порядке: Пурин - Пурин > Пиримидин - Пиримидин. В олиго- и полинуклеотидах стэкинг между соседними основаниями приводит к формированию стабильной одноцепочечной спиральной структуры. Стабильность таких структур также подчиняется указанным выше закономерностям: при комнатной температуре poly(A) представляет собой в основном спиральную структуру, а poly(U) находится преимущественно в состоянии разупорядоченного клубка. Спаривание оснований путем образования водородных связей зависит от состава пары оснований, тогда как стэкинг зависит как от состава, так и от последовательности.
• • • Взаимодействия между основаниями могут быть двух типов: а) между основаниями, лежащими в одной плоскости, - горизонтальное взаимодействие, реализующееся путем образования водородных связей , и б) между основаниями, уложенными одно над другим, - стэкинг-взаимодействие, которое обусловлено в основном дисперсионными лондоновскими силами и гидрофобными эффектами. "Горизонтальная" ассоциация оснований наблюдается в неводных растворах, а также в газообразном и кристаллическом состояниях. Помимо этого, в твердой фазе основания почти всегда располагаются параллельно одно над другим на расстоянии вандерваальсового радиуса, приблизительно 3. 4 А. Такое расположение является результатом не горизонтальных, а вертикальных взаимодействий. Стопки образуются и в водных растворах, преобладают они и в кристаллических структурах. При этом оказывается, что стэкинг-взаимодействие между основаниями довольно специфично: полярные заместители одного основания, -NH 2, =N-, =O или галогены, нависают над ароматическим кольцом соседнего основания. Такого рода специфичность стэкинга даже более выражена, чем специфичность при образовании водородных связей. Например, в кристаллах дезоксиаденозинмоногидрата, аденозин-5'-фосфата, аденозин- 5'-бромурацила пурины вступают в стэкингвзаимодействие по одной и той же схеме, хотя пространственная группа кристаллов, размеры элементарной ячейки, молекулярная упаковка и система водородных связей различаются. Специфичность стэкинга проявляется также и в галогензамещенных основаниях. Атомы галогенов располагаются над примыкающими ароматическими гетероциклами на расстоянии, даже меньшем чем сумма вандерваальсовых радиусов для атомов галогена и атомов гетероцикла. Такая специфичность связана с электронной структурой оснований и определяется главным образом диполь-дипольными взаимодействиями и дисперсионными лондоновскими силами. В кристаллах некоторых протонированных пиримидиновых оснований и нуклеотидов стэкинг не наблюдается вообще. Это позволяет думать, что заряженные пиримидины не вступают в стэкинг-взаимодействие. В случае протонированных пуринов стэкинг тем не менее имеет место, но носит другой характер, чем у незаряженных пуринов: атом N нависает над атомом N 7 примыкающего основания. Анализ типов стэкинга в кристаллах оснований, нуклеозидов и нуклеотидов показывает, что, по-видимому, главную роль в стабилизации стэкинга играет взаимодействие между постоянными и индуцированными диполями; в роли постоянного диполя, влияющего на пи-злектронную систему соседнего основания, выступают группы C=O и C-NH 2. В водных растворах основания и нуклеозиды образуют ассоциаты с помощью вертикальных взаимодействий, причем помимо димеров образуются ассоциаты более высокого порядка. Процесс образования стопок обратим, причем увеличение свободной энергии на всех этапах одинаково, что означает, что присоединение одного основания к другому основанию или к стопке оснований носит аддитивный, некооперативный характер, так что процесс можно считать изодесмическим. Исследования методом ЯМР показывают, что в стэкинге принимает участие шестичленное пиримидиновое, а не пятичленное имидазольное кольцо и что ориентация гетероцикла в стопке зависит от типа основания. Процесс агрегации лимитируется только диффузией, в его основе лежат слабые взаимодействия. Интенсивность стэкинга между пуриновыми и пиримидиновыми основаниями уменьшается в следующем порядке: Пурин - Пурин > Пиримидин - Пиримидин. В олиго- и полинуклеотидах стэкинг между соседними основаниями приводит к формированию стабильной одноцепочечной спиральной структуры. Стабильность таких структур также подчиняется указанным выше закономерностям: при комнатной температуре poly(A) представляет собой в основном спиральную структуру, а poly(U) находится преимущественно в состоянии разупорядоченного клубка. Спаривание оснований путем образования водородных связей зависит от состава пары оснований, тогда как стэкинг зависит как от состава, так и от последовательности.
 Сахар: конформации в нуклеиновых кислотах • • • Пятичленное фуранозное кольцо обычно непланарно. Оно может принимать конформацию, подобную конверту (E, от англ. envelope), в которой четыре атома из пяти находятся в одной плоскости, а один атом выходит из нее на расстояние до 0. 5 А, либо изогнутую твист-конформацию (T, от англ. twist), в которой любые два соседних атома смещены в разные стороны от плоскости, построенной по трем оставшимся атомам сахарного кольца. В обоих случаях атомы, выходящие из плоскости в ту же сторону, что и атом С 5', называют эндо-атомами, а атомы, смещенные в противоположную сторону, экзо-атомами. Соответствующим образом обозначаются и конформации сахарных колец (см. Рис. Различные конформации сахара ). Обычно четыре атома, определяющие плоскость кольца в Е-кон- формации, редко бывают строго компланарными, а смещение атомов от плоскости кольца в Т-конформации редко бывает симметричным. Большее отклонение от планарности называют главным выступом (major puckering), меньшее - минорным (minor puckering). При сокращенной записи символы эндо- и экзо-атомов ставят перед или после букв Е и Т в зависимости от того, о каком выступе идет речь - о главном или минорном. Несимметричная C 3'эндо-C 2'-экзо- твист-конформация с C 3'-главным и C 2'-минорным выступами, обозначается - 3 Т 2, а подобная ей симметричная - 2 Т 3, C 2'-эндо-конверт обозначается - 2 Е, C 3'-экзо-конверт - 3 Е. Описанные способы обозначения конформаций сахара являются приближенными и не могут отразить все промежуточные состояния, в которых находятся эти соединения. Для более полного анализа конформаций пятичленных колец использовали метод, основанный на понятии псевдовращения. Фуранозное кольцо находится в основном в двух конформациях: С 3'-эндо(N) и С 2'-эндо(S). Фуранозное кольцо в составе нуклеозидов замещено несимметрично, поэтому в нуклеозидах и нуклеотидах, структура которых определена кристаллографическими методами, фазовые углы псевдовращения Р распределены по циклу неравномерно. Они образуют две группы, концентрируясь в интервалах от -1 до 34 градусов (С 3'-эндо) и от 137 до 194 градусов (С 2'-эндо). В соответствии с расположением в цикле псевдовращения эти предпочтительные конформации называют северными (N) и южными (S) (смотри Рис. Различные конформации сахара ). В растворе между этими конформациями поддерживается динамическое равновесие. Быстрый переход от одной конформации к другой происходит с образованием промежуточной О 4'-эндо-конформации. Разность энергий этих двух состояний невелика: по теоретическим оценкам она составляет 0. 6 - 3. 8 ккал/моль, а экспериментально полученная величина равна 4. 7 ккал/моль. Положение равновесия между конформациями С 2'-эндо и С 3'-эндо определяется электроотрицательностью заместителей при атомах С 2' и С 3'. Конформация сахара в нуклеозидах зависит также от характера модификации основания. Для ДНК характерны две основные конформации сахарного кольца: С 3'-эндо и С 2'-эндо (или ее разновидность, С 3'-экзо - конформация), переход между которыми определяется активностью молекул воды окружающей среды, а для РНК всегда наблюдается С 3'-эндо-конформация.
Сахар: конформации в нуклеиновых кислотах • • • Пятичленное фуранозное кольцо обычно непланарно. Оно может принимать конформацию, подобную конверту (E, от англ. envelope), в которой четыре атома из пяти находятся в одной плоскости, а один атом выходит из нее на расстояние до 0. 5 А, либо изогнутую твист-конформацию (T, от англ. twist), в которой любые два соседних атома смещены в разные стороны от плоскости, построенной по трем оставшимся атомам сахарного кольца. В обоих случаях атомы, выходящие из плоскости в ту же сторону, что и атом С 5', называют эндо-атомами, а атомы, смещенные в противоположную сторону, экзо-атомами. Соответствующим образом обозначаются и конформации сахарных колец (см. Рис. Различные конформации сахара ). Обычно четыре атома, определяющие плоскость кольца в Е-кон- формации, редко бывают строго компланарными, а смещение атомов от плоскости кольца в Т-конформации редко бывает симметричным. Большее отклонение от планарности называют главным выступом (major puckering), меньшее - минорным (minor puckering). При сокращенной записи символы эндо- и экзо-атомов ставят перед или после букв Е и Т в зависимости от того, о каком выступе идет речь - о главном или минорном. Несимметричная C 3'эндо-C 2'-экзо- твист-конформация с C 3'-главным и C 2'-минорным выступами, обозначается - 3 Т 2, а подобная ей симметричная - 2 Т 3, C 2'-эндо-конверт обозначается - 2 Е, C 3'-экзо-конверт - 3 Е. Описанные способы обозначения конформаций сахара являются приближенными и не могут отразить все промежуточные состояния, в которых находятся эти соединения. Для более полного анализа конформаций пятичленных колец использовали метод, основанный на понятии псевдовращения. Фуранозное кольцо находится в основном в двух конформациях: С 3'-эндо(N) и С 2'-эндо(S). Фуранозное кольцо в составе нуклеозидов замещено несимметрично, поэтому в нуклеозидах и нуклеотидах, структура которых определена кристаллографическими методами, фазовые углы псевдовращения Р распределены по циклу неравномерно. Они образуют две группы, концентрируясь в интервалах от -1 до 34 градусов (С 3'-эндо) и от 137 до 194 градусов (С 2'-эндо). В соответствии с расположением в цикле псевдовращения эти предпочтительные конформации называют северными (N) и южными (S) (смотри Рис. Различные конформации сахара ). В растворе между этими конформациями поддерживается динамическое равновесие. Быстрый переход от одной конформации к другой происходит с образованием промежуточной О 4'-эндо-конформации. Разность энергий этих двух состояний невелика: по теоретическим оценкам она составляет 0. 6 - 3. 8 ккал/моль, а экспериментально полученная величина равна 4. 7 ккал/моль. Положение равновесия между конформациями С 2'-эндо и С 3'-эндо определяется электроотрицательностью заместителей при атомах С 2' и С 3'. Конформация сахара в нуклеозидах зависит также от характера модификации основания. Для ДНК характерны две основные конформации сахарного кольца: С 3'-эндо и С 2'-эндо (или ее разновидность, С 3'-экзо - конформация), переход между которыми определяется активностью молекул воды окружающей среды, а для РНК всегда наблюдается С 3'-эндо-конформация.


