2- СТРУКТУРА НУКЛЕИНОВЫХ КИСЛОТ-red.ppt
- Количество слайдов: 88
 СТРУКТУРА НУКЛЕИНОВЫХ КИСЛОТ лекция 1 1
СТРУКТУРА НУКЛЕИНОВЫХ КИСЛОТ лекция 1 1
 2
2
 Хронология открытий, подготовивших создание Уотсоном и Криком модели двойной спирали ДНК 1868 г. Обнаружен нуклеин. Современное название - хроматин. Фридрих Мишер 1889 г. Нуклеин разделен на нуклеиновую кислоту и белок. Появился термин "нуклеиновая кислота". Рихард Альтман 1900 г. Все азотистые основания были описаны химиками. 1909 г. В нуклеиновых кислотах обнаружены фосфорная кислота и рибоза. Левен 1930 г. Найдена дезоксирибоза. Левен 1938 г. Рентгеноструктурный анализ показал, что расстояние между нуклеотидами в ДНК 3, 4 Å. При этом азотистые основания уложены стопками. Уильям Астбюри, Флорин Белл 1947 г. С помощью прямого и обратного титрования установлено, что в ДНК есть водородные связи между группами N-H и C=O. Гулланд 1953 г. С помощью кислотного гидролиза ДНК с последующей хроматографией и количественным анализом установлены 3 закономерности: А/Т=1; Г/Ц=1; (Г+Ц)/(А+Т)=К - коэффициент специфичности, постоянен для каждого вида. Эрвин Чаргафф
Хронология открытий, подготовивших создание Уотсоном и Криком модели двойной спирали ДНК 1868 г. Обнаружен нуклеин. Современное название - хроматин. Фридрих Мишер 1889 г. Нуклеин разделен на нуклеиновую кислоту и белок. Появился термин "нуклеиновая кислота". Рихард Альтман 1900 г. Все азотистые основания были описаны химиками. 1909 г. В нуклеиновых кислотах обнаружены фосфорная кислота и рибоза. Левен 1930 г. Найдена дезоксирибоза. Левен 1938 г. Рентгеноструктурный анализ показал, что расстояние между нуклеотидами в ДНК 3, 4 Å. При этом азотистые основания уложены стопками. Уильям Астбюри, Флорин Белл 1947 г. С помощью прямого и обратного титрования установлено, что в ДНК есть водородные связи между группами N-H и C=O. Гулланд 1953 г. С помощью кислотного гидролиза ДНК с последующей хроматографией и количественным анализом установлены 3 закономерности: А/Т=1; Г/Ц=1; (Г+Ц)/(А+Т)=К - коэффициент специфичности, постоянен для каждого вида. Эрвин Чаргафф
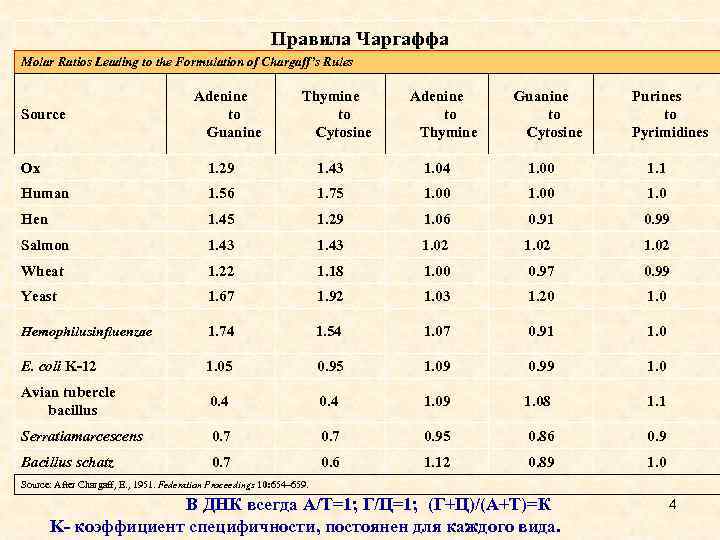 Правила Чаргаффа Molar Ratios Leading to the Formulation of Chargaff’s Rules Source Adenine to Guanine Thymine to Cytosine Adenine to Thymine Guanine to Cytosine Purines to Pyrimidines Ox 1. 29 1. 43 1. 04 1. 00 1. 1 Human 1. 56 1. 75 1. 00 1. 0 Hen 1. 45 1. 29 1. 06 0. 91 0. 99 Salmon 1. 43 1. 02 Wheat 1. 22 1. 18 1. 00 0. 97 0. 99 Yeast 1. 67 1. 92 1. 03 1. 20 1. 0 Hemophilusinfluenzae 1. 74 1. 54 1. 07 0. 91 1. 0 E. coli K-12 1. 05 0. 95 1. 09 0. 99 1. 0 Avian tubercle bacillus 0. 4 1. 09 1. 08 1. 1 Serratiamarcescens 0. 7 0. 95 0. 86 0. 9 Bacillus schatz 0. 7 0. 6 1. 12 0. 89 1. 0 Source: After Chargaff, E. , 1951. Federation Proceedings 10: 654– 659. В ДНК всегда А/Т=1; Г/Ц=1; (Г+Ц)/(А+Т)=К K- коэффициент специфичности, постоянен для каждого вида. 4
Правила Чаргаффа Molar Ratios Leading to the Formulation of Chargaff’s Rules Source Adenine to Guanine Thymine to Cytosine Adenine to Thymine Guanine to Cytosine Purines to Pyrimidines Ox 1. 29 1. 43 1. 04 1. 00 1. 1 Human 1. 56 1. 75 1. 00 1. 0 Hen 1. 45 1. 29 1. 06 0. 91 0. 99 Salmon 1. 43 1. 02 Wheat 1. 22 1. 18 1. 00 0. 97 0. 99 Yeast 1. 67 1. 92 1. 03 1. 20 1. 0 Hemophilusinfluenzae 1. 74 1. 54 1. 07 0. 91 1. 0 E. coli K-12 1. 05 0. 95 1. 09 0. 99 1. 0 Avian tubercle bacillus 0. 4 1. 09 1. 08 1. 1 Serratiamarcescens 0. 7 0. 95 0. 86 0. 9 Bacillus schatz 0. 7 0. 6 1. 12 0. 89 1. 0 Source: After Chargaff, E. , 1951. Federation Proceedings 10: 654– 659. В ДНК всегда А/Т=1; Г/Ц=1; (Г+Ц)/(А+Т)=К K- коэффициент специфичности, постоянен для каждого вида. 4
 Нуклеотидный состав • Этот факт, открытый и изученный Э. Чаргаффом (правила Чаргафа), был одним из важнейших среди тех данных, которые привели к открытию двойной спирали ДНК. Он означает, что для описания состава молекулы ДНК необходима только одна переменная - мольная доля G+C. • GC-содержание природных ДНК существенно различается. Для ДНК некоторых бактерий это 75%, у животных молекула ДНК содержит 40 -45% GC, причем ДНК близких организмов обычно имеют сходный GC- состав. • Видимо, существование столь широкого интервала значений GC-содержания без потери способности организмов хранить необходимую генетическую информацию возможно благодаря вырожденности генетического кода и тому факту, что часть ДНК не кодирует никаких белковых последовательностей. • В состав некоторых ДНК входят необычные основания, например, в ДНК Тчетных фагов преобладает глюкозилированный 5 -гидрокси- метилцитозин. Он образует с гуанином такие же пары оснований, и правила Чаргаффа остаются справедливыми. ДНК фага SP 2 содержит урацил вместо тимина. Некоторые основания отдельных ДНК метилированы, такая модификация служит механизмом защиты против внутриклеточных рестриктаз. • Большинство природных молекул РНК являются одноцепочечными, правила Чаргаффа выполняются лишь для небольшого числа двухнитевых вирусных РНК. 5
Нуклеотидный состав • Этот факт, открытый и изученный Э. Чаргаффом (правила Чаргафа), был одним из важнейших среди тех данных, которые привели к открытию двойной спирали ДНК. Он означает, что для описания состава молекулы ДНК необходима только одна переменная - мольная доля G+C. • GC-содержание природных ДНК существенно различается. Для ДНК некоторых бактерий это 75%, у животных молекула ДНК содержит 40 -45% GC, причем ДНК близких организмов обычно имеют сходный GC- состав. • Видимо, существование столь широкого интервала значений GC-содержания без потери способности организмов хранить необходимую генетическую информацию возможно благодаря вырожденности генетического кода и тому факту, что часть ДНК не кодирует никаких белковых последовательностей. • В состав некоторых ДНК входят необычные основания, например, в ДНК Тчетных фагов преобладает глюкозилированный 5 -гидрокси- метилцитозин. Он образует с гуанином такие же пары оснований, и правила Чаргаффа остаются справедливыми. ДНК фага SP 2 содержит урацил вместо тимина. Некоторые основания отдельных ДНК метилированы, такая модификация служит механизмом защиты против внутриклеточных рестриктаз. • Большинство природных молекул РНК являются одноцепочечными, правила Чаргаффа выполняются лишь для небольшого числа двухнитевых вирусных РНК. 5
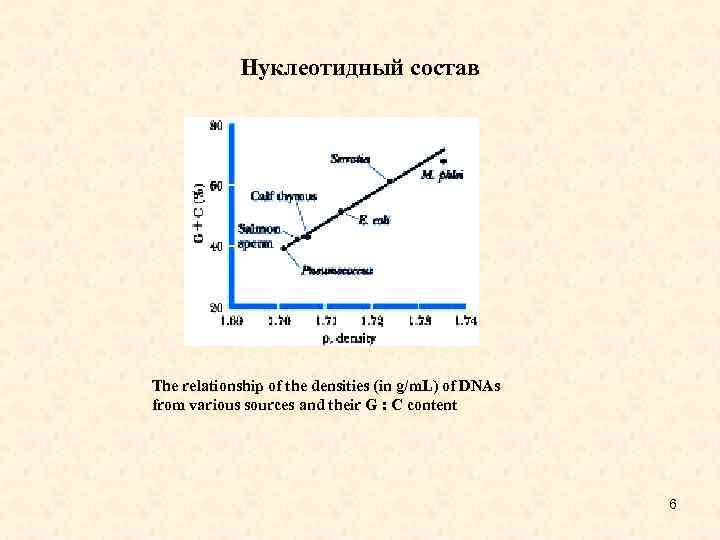 Нуклеотидный состав The relationship of the densities (in g/m. L) of DNAs from various sources and their G : C content 6
Нуклеотидный состав The relationship of the densities (in g/m. L) of DNAs from various sources and their G : C content 6
 . 7
. 7
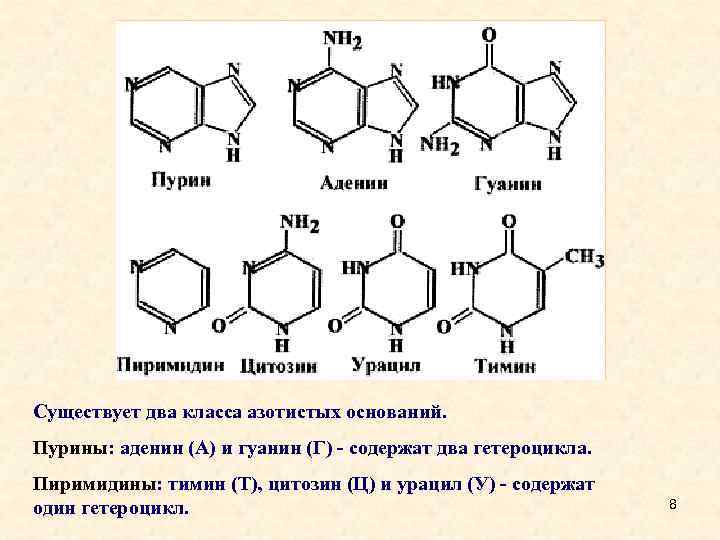 Существует два класса азотистых оснований. Пурины: аденин (А) и гуанин (Г) - содержат два гетероцикла. Пиримидины: тимин (Т), цитозин (Ц) и урацил (У) - содержат один гетероцикл. 8
Существует два класса азотистых оснований. Пурины: аденин (А) и гуанин (Г) - содержат два гетероцикла. Пиримидины: тимин (Т), цитозин (Ц) и урацил (У) - содержат один гетероцикл. 8
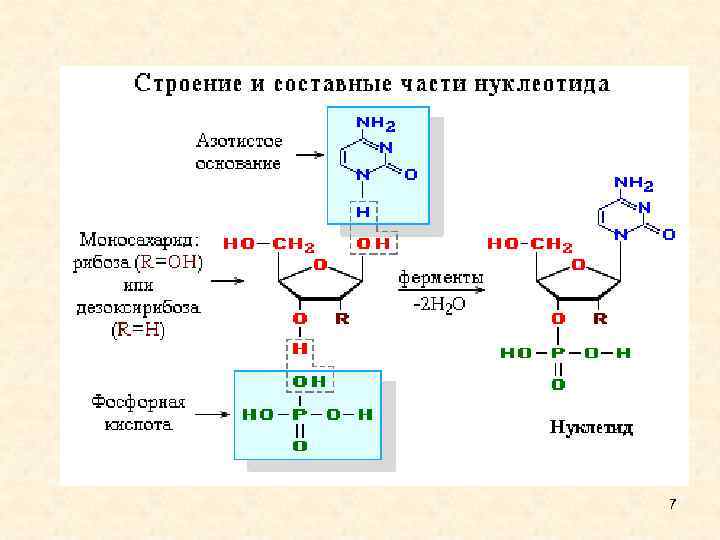
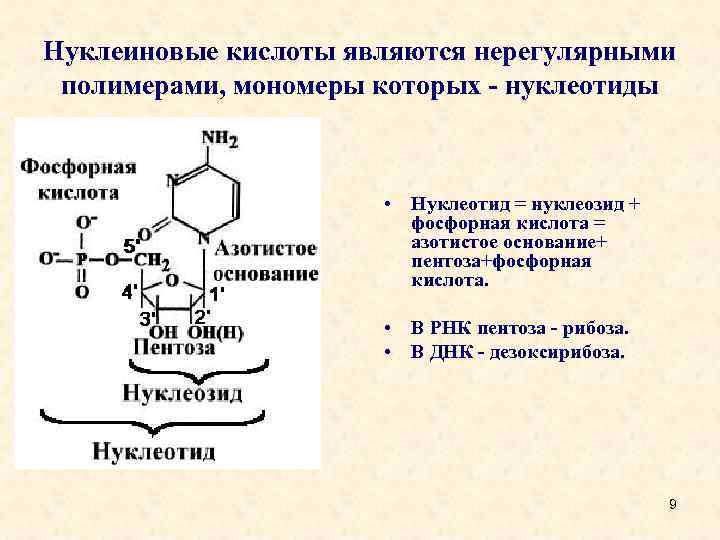 Нуклеиновые кислоты являются нерегулярными полимерами, мономеры которых - нуклеотиды • Нуклеотид = нуклеозид + фосфорная кислота = азотистое основание+ пентоза+фосфорная кислота. • В РНК пентоза - рибоза. • В ДНК - дезоксирибоза. 9
Нуклеиновые кислоты являются нерегулярными полимерами, мономеры которых - нуклеотиды • Нуклеотид = нуклеозид + фосфорная кислота = азотистое основание+ пентоза+фосфорная кислота. • В РНК пентоза - рибоза. • В ДНК - дезоксирибоза. 9
 НУКЛЕОЗИДЫ И НУКЛЕОТИДЫ • Нуклеозиды - это N-гликозиды пиримидиновых или пуриновых оснований, в которых 1 -й углеродный атом сахара (пентозы) связан гликозидной связью с атомом N 1 пиримидина или атомом N 9 пурина. Пентозы всегда присутствуют в фуранозной форме. Существует два ряда нуклеозидов: рибонуклеозиды, которые содержат в качестве сахарного компонента D-рибозу, и 2'-дезоксирибонуклеотиды, содержащие 2 -дезокси-D-рибозу. • Гликозидная связь. В нуклеозидах и нуклеотидах N-гликозидная связь - это связь между 1 -м углеродным атомом сахара - пентозы и атомом N 1 пиримидина или N 9 пурина. N-гликозидная связь имеет бета- конфигурацию. • Для пиримидиновых нуклеозидов длина связи С 1'-N максимальна и составляет 1. 52 А при торсионном угле вращения, определяемом через атомы - (О 4'- С 1'- N 1 - С 2), и равным примерно 180 град. По мере его приближения к -140 град. длина N-гликозидной связи уменьшается до 1. 48 А практически линейно. • В пуриновых нуклеозидах длина гликозидной связи менее вариабельна и составляет примерно 1. 46 А. 10
НУКЛЕОЗИДЫ И НУКЛЕОТИДЫ • Нуклеозиды - это N-гликозиды пиримидиновых или пуриновых оснований, в которых 1 -й углеродный атом сахара (пентозы) связан гликозидной связью с атомом N 1 пиримидина или атомом N 9 пурина. Пентозы всегда присутствуют в фуранозной форме. Существует два ряда нуклеозидов: рибонуклеозиды, которые содержат в качестве сахарного компонента D-рибозу, и 2'-дезоксирибонуклеотиды, содержащие 2 -дезокси-D-рибозу. • Гликозидная связь. В нуклеозидах и нуклеотидах N-гликозидная связь - это связь между 1 -м углеродным атомом сахара - пентозы и атомом N 1 пиримидина или N 9 пурина. N-гликозидная связь имеет бета- конфигурацию. • Для пиримидиновых нуклеозидов длина связи С 1'-N максимальна и составляет 1. 52 А при торсионном угле вращения, определяемом через атомы - (О 4'- С 1'- N 1 - С 2), и равным примерно 180 град. По мере его приближения к -140 град. длина N-гликозидной связи уменьшается до 1. 48 А практически линейно. • В пуриновых нуклеозидах длина гликозидной связи менее вариабельна и составляет примерно 1. 46 А. 10
 НУКЛЕОЗИДЫ И НУКЛЕОТИДЫ Нуклеотиды представляют собой фосфорнокислые эфиры нуклеозидов, в которых фосфорная кислота связана сложноэфирной связью с одной из свободных гидроксильных групп сахарного кольца. • Фосфорилирование дезоксирибонуклеозида может осуществляться по положениям С 3' и С 5', так как атомы С 1' и С 4' включены в фуранозное кольцо, а атом С 2' не имеет гидроксильной группы. В РНК только положения 1'и 4'недоступны для этерификации, зaмещение по С 2', С 3' и С 5' возможно. • Нуклеотиды являются сильными кислотами. Они называются, адениловой, гуаниловой, тимидиловой, цитидиловой и уридиловой кислотами. 11
НУКЛЕОЗИДЫ И НУКЛЕОТИДЫ Нуклеотиды представляют собой фосфорнокислые эфиры нуклеозидов, в которых фосфорная кислота связана сложноэфирной связью с одной из свободных гидроксильных групп сахарного кольца. • Фосфорилирование дезоксирибонуклеозида может осуществляться по положениям С 3' и С 5', так как атомы С 1' и С 4' включены в фуранозное кольцо, а атом С 2' не имеет гидроксильной группы. В РНК только положения 1'и 4'недоступны для этерификации, зaмещение по С 2', С 3' и С 5' возможно. • Нуклеотиды являются сильными кислотами. Они называются, адениловой, гуаниловой, тимидиловой, цитидиловой и уридиловой кислотами. 11
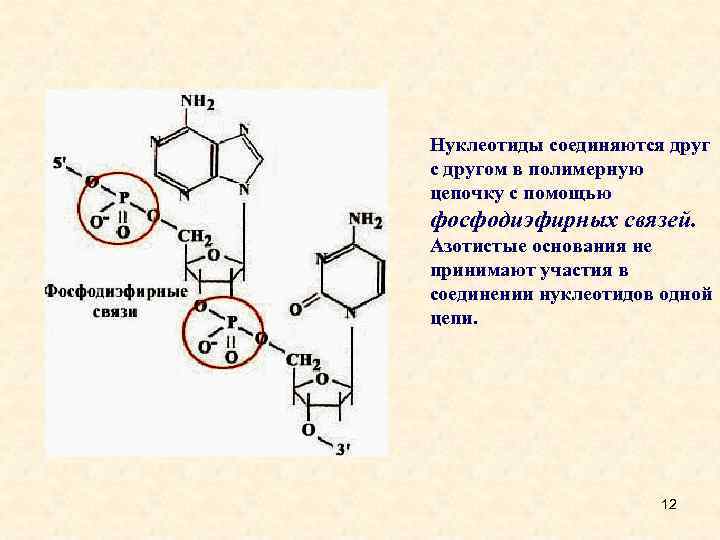 Нуклеотиды соединяются друг с другом в полимерную цепочку с помощью фосфодиэфирных связей. Азотистые основания не принимают участия в соединении нуклеотидов одной цепи. 12
Нуклеотиды соединяются друг с другом в полимерную цепочку с помощью фосфодиэфирных связей. Азотистые основания не принимают участия в соединении нуклеотидов одной цепи. 12
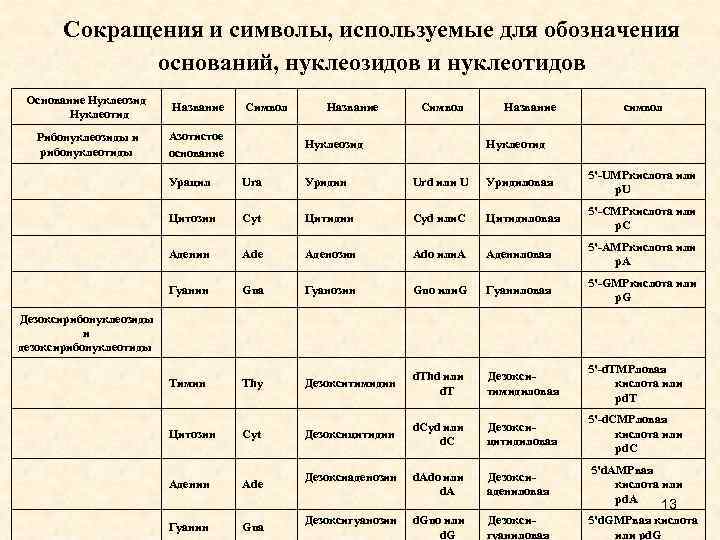 Сокращения и символы, используемые для обозначения оснований, нуклеозидов и нуклеотидов Основание Нуклеозид Нуклеотид Название Рибонуклеозиды и рибонуклеотиды Азотистое основание Символ Название Символ Нуклеозид Название символ Нуклеотид Урацил Ura Уридин Urd или U Уридиловая 5'-UMPкислота или p. U Цитозин Cyt Цитидин Cyd или. C Цитидиловая 5'-CMPкислота или p. C Аденин Ade Аденозин Ado или. A Адениловая 5'-AMPкислота или p. A Гуанин Gua Гуанозин Guo или. G Гуаниловая 5'-GMPкислота или p. G Тимин Thy Дезокситимидин d. Thd или d. T Дезокситимидиловая 5'-d. TMPловая кислота или pd. T Cyt d. Cyd или Дезоксицитидин d. C Дезоксицитидиловая 5'-d. CMPловая кислота или pd. C Ade Дезоксиаденозин d. Ado или d. A Дезоксиадениловая 5'd. AMPвая кислота или pd. A Дезоксигуанозин d. Guo или d. G Дезоксигуаниловая 5'd. GMPвая кислота или pd. G Дезоксирибонуклеозиды и дезоксирибонуклеотиды Цитозин Аденин Гуанин Gua 13
Сокращения и символы, используемые для обозначения оснований, нуклеозидов и нуклеотидов Основание Нуклеозид Нуклеотид Название Рибонуклеозиды и рибонуклеотиды Азотистое основание Символ Название Символ Нуклеозид Название символ Нуклеотид Урацил Ura Уридин Urd или U Уридиловая 5'-UMPкислота или p. U Цитозин Cyt Цитидин Cyd или. C Цитидиловая 5'-CMPкислота или p. C Аденин Ade Аденозин Ado или. A Адениловая 5'-AMPкислота или p. A Гуанин Gua Гуанозин Guo или. G Гуаниловая 5'-GMPкислота или p. G Тимин Thy Дезокситимидин d. Thd или d. T Дезокситимидиловая 5'-d. TMPловая кислота или pd. T Cyt d. Cyd или Дезоксицитидин d. C Дезоксицитидиловая 5'-d. CMPловая кислота или pd. C Ade Дезоксиаденозин d. Ado или d. A Дезоксиадениловая 5'd. AMPвая кислота или pd. A Дезоксигуанозин d. Guo или d. G Дезоксигуаниловая 5'd. GMPвая кислота или pd. G Дезоксирибонуклеозиды и дезоксирибонуклеотиды Цитозин Аденин Гуанин Gua 13
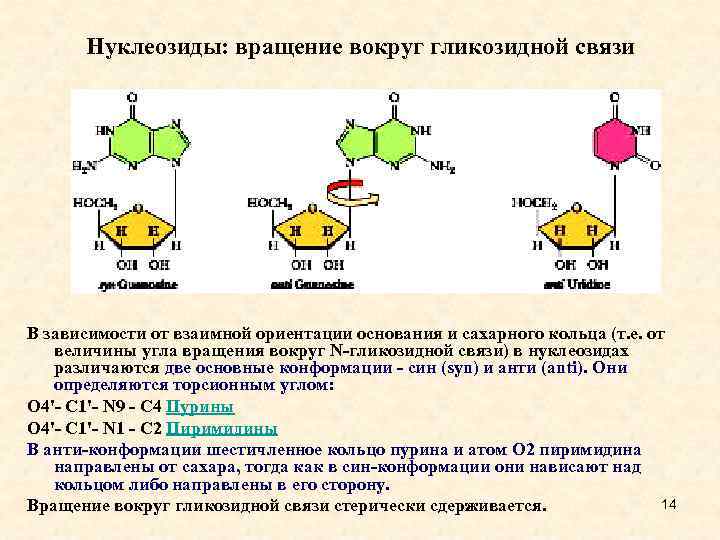 Нуклеозиды: вращение вокруг гликозидной связи В зависимости от взаимной ориентации основания и сахарного кольца (т. е. от величины угла вращения вокруг N-гликозидной связи) в нуклеозидах различаются две основные конформации - син (syn) и анти (anti). Они определяются торсионным углом: О 4'- С 1'- N 9 - С 4 Пурины О 4'- С 1'- N 1 - С 2 Пиримидины В анти-конформации шестичленное кольцо пурина и атом О 2 пиримидина направлены от сахара, тогда как в син-конформации они нависают над кольцом либо направлены в его сторону. 14 Вращение вокруг гликозидной связи стерически сдерживается.
Нуклеозиды: вращение вокруг гликозидной связи В зависимости от взаимной ориентации основания и сахарного кольца (т. е. от величины угла вращения вокруг N-гликозидной связи) в нуклеозидах различаются две основные конформации - син (syn) и анти (anti). Они определяются торсионным углом: О 4'- С 1'- N 9 - С 4 Пурины О 4'- С 1'- N 1 - С 2 Пиримидины В анти-конформации шестичленное кольцо пурина и атом О 2 пиримидина направлены от сахара, тогда как в син-конформации они нависают над кольцом либо направлены в его сторону. 14 Вращение вокруг гликозидной связи стерически сдерживается.
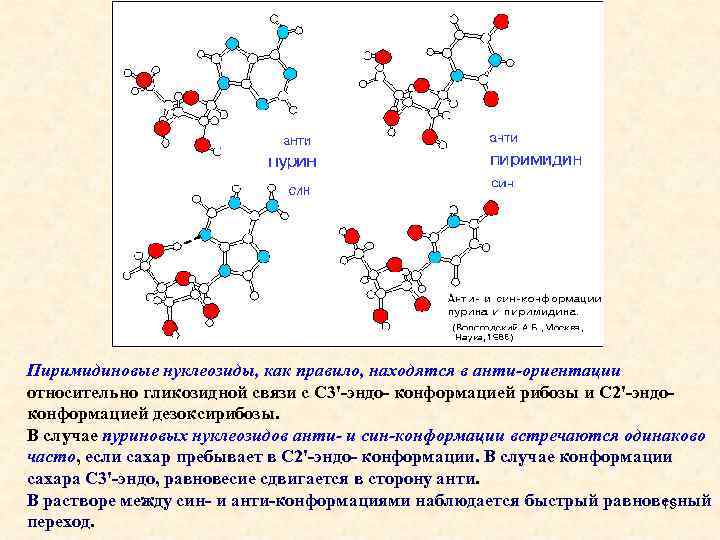 Пиримидиновые нуклеозиды, как правило, находятся в анти-ориентации относительно гликозидной связи с С 3'-эндо- конформацией рибозы и С 2'-эндо- конформацией дезоксирибозы. В случае пуриновых нуклеозидов анти- и син-конформации встречаются одинаково часто, если сахар пребывает в С 2'-эндо- конформации. В случае конформации сахара С 3'-эндо, равновесие сдвигается в сторону анти. В растворе между син- и анти-конформациями наблюдается быстрый равновесный 15 переход.
Пиримидиновые нуклеозиды, как правило, находятся в анти-ориентации относительно гликозидной связи с С 3'-эндо- конформацией рибозы и С 2'-эндо- конформацией дезоксирибозы. В случае пуриновых нуклеозидов анти- и син-конформации встречаются одинаково часто, если сахар пребывает в С 2'-эндо- конформации. В случае конформации сахара С 3'-эндо, равновесие сдвигается в сторону анти. В растворе между син- и анти-конформациями наблюдается быстрый равновесный 15 переход.
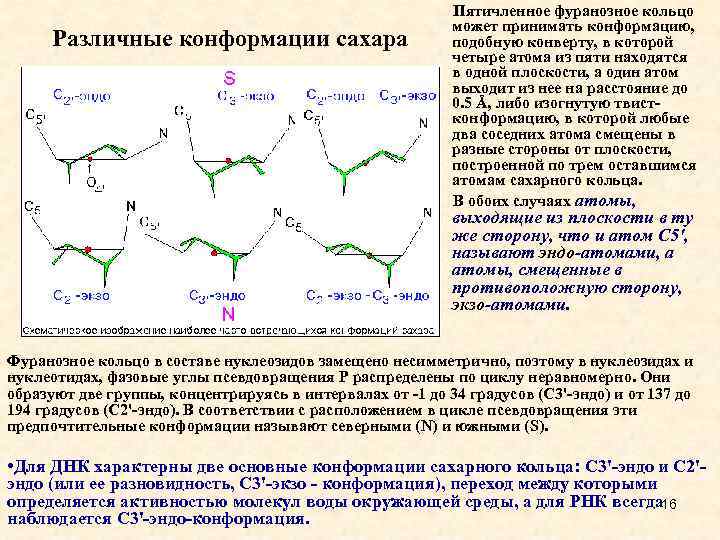 Различные конформации сахара Пятичленное фуранозное кольцо может принимать конформацию, подобную конверту, в которой четыре атома из пяти находятся в одной плоскости, а один атом выходит из нее на расстояние до 0. 5 Å, либо изогнутую твистконформацию, в которой любые два соседних атома смещены в разные стороны от плоскости, построенной по трем оставшимся атомам сахарного кольца. В обоих случаях атомы, выходящие из плоскости в ту же сторону, что и атом С 5', называют эндо-атомами, а атомы, смещенные в противоположную сторону, экзо-атомами. Фуранозное кольцо в составе нуклеозидов замещено несимметрично, поэтому в нуклеозидах и нуклеотидах, фазовые углы псевдовращения Р распределены по циклу неравномерно. Они образуют две группы, концентрируясь в интервалах от -1 до 34 градусов (С 3'-эндо) и от 137 до 194 градусов (С 2'-эндо). В соответствии с расположением в цикле псевдовращения эти предпочтительные конформации называют северными (N) и южными (S). • Для ДНК характерны две основные конформации сахарного кольца: С 3'-эндо и С 2'эндо (или ее разновидность, С 3'-экзо - конформация), переход между которыми определяется активностью молекул воды окружающей среды, а для РНК всегда 16 наблюдается С 3'-эндо-конформация.
Различные конформации сахара Пятичленное фуранозное кольцо может принимать конформацию, подобную конверту, в которой четыре атома из пяти находятся в одной плоскости, а один атом выходит из нее на расстояние до 0. 5 Å, либо изогнутую твистконформацию, в которой любые два соседних атома смещены в разные стороны от плоскости, построенной по трем оставшимся атомам сахарного кольца. В обоих случаях атомы, выходящие из плоскости в ту же сторону, что и атом С 5', называют эндо-атомами, а атомы, смещенные в противоположную сторону, экзо-атомами. Фуранозное кольцо в составе нуклеозидов замещено несимметрично, поэтому в нуклеозидах и нуклеотидах, фазовые углы псевдовращения Р распределены по циклу неравномерно. Они образуют две группы, концентрируясь в интервалах от -1 до 34 градусов (С 3'-эндо) и от 137 до 194 градусов (С 2'-эндо). В соответствии с расположением в цикле псевдовращения эти предпочтительные конформации называют северными (N) и южными (S). • Для ДНК характерны две основные конформации сахарного кольца: С 3'-эндо и С 2'эндо (или ее разновидность, С 3'-экзо - конформация), переход между которыми определяется активностью молекул воды окружающей среды, а для РНК всегда 16 наблюдается С 3'-эндо-конформация.
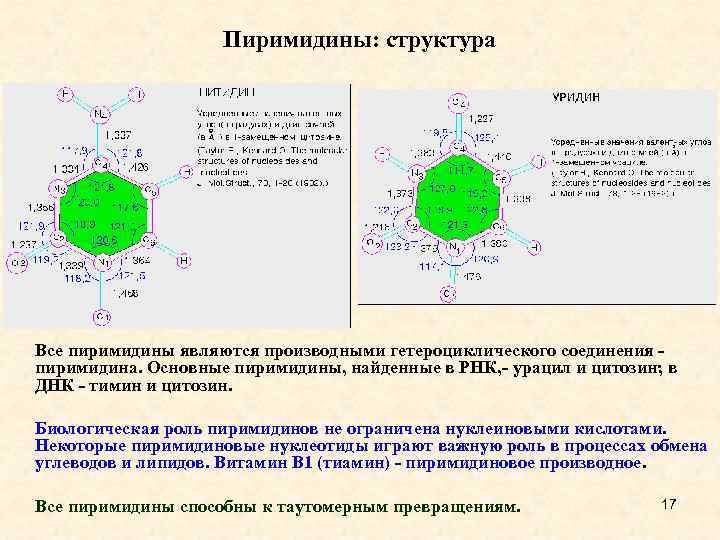 Пиримидины: структура Все пиримидины являются производными гетероциклического соединения - пиримидина. Основные пиримидины, найденные в РНК, - урацил и цитозин; в ДНК - тимин и цитозин. Биологическая роль пиримидинов не ограничена нуклеиновыми кислотами. Некоторые пиримидиновые нуклеотиды играют важную роль в процессах обмена углеводов и липидов. Витамин В 1 (тиамин) - пиримидиновое производное. Все пиримидины способны к таутомерным превращениям. 17
Пиримидины: структура Все пиримидины являются производными гетероциклического соединения - пиримидина. Основные пиримидины, найденные в РНК, - урацил и цитозин; в ДНК - тимин и цитозин. Биологическая роль пиримидинов не ограничена нуклеиновыми кислотами. Некоторые пиримидиновые нуклеотиды играют важную роль в процессах обмена углеводов и липидов. Витамин В 1 (тиамин) - пиримидиновое производное. Все пиримидины способны к таутомерным превращениям. 17
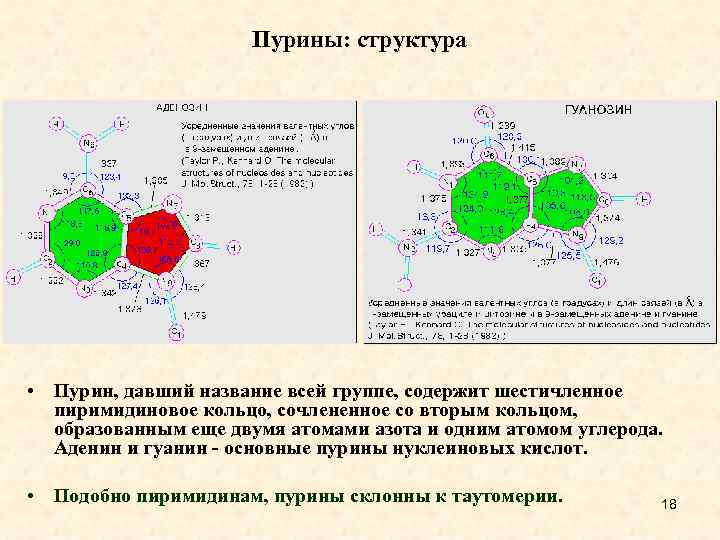 Пурины: структура • Пурин, давший название всей группе, содержит шестичленное пиримидиновое кольцо, сочлененное со вторым кольцом, образованным еще двумя атомами азота и одним атомом углерода. Аденин и гуанин - основные пурины нуклеиновых кислот. • Подобно пиримидинам, пурины склонны к таутомерии. 18
Пурины: структура • Пурин, давший название всей группе, содержит шестичленное пиримидиновое кольцо, сочлененное со вторым кольцом, образованным еще двумя атомами азота и одним атомом углерода. Аденин и гуанин - основные пурины нуклеиновых кислот. • Подобно пиримидинам, пурины склонны к таутомерии. 18
 • Tаутомерия оснований В гетороциклах протоны, связанные с азотом, могут переходить на другие атомы азота или на атомы кислорода кетогруппы. Поэтому в растворах будет существовать равновесие различных таутомерных структур, быстро переходящих друг в друга. В результате таутомерых превращений U и G в енольной форме при спаривании могут имитировать С и А, а С и А в иминоформе - U и G, что может привести к мутациям в ДНК. • В растворе обычные кето- и аминоформы всегда превалируют над енольной и имино-формами, доля которых, как правило, не превышает 0, 1 %. Эта величина может сильно меняться для модифицированных оснований или для оснований в составе комплементарной пары. 19
• Tаутомерия оснований В гетороциклах протоны, связанные с азотом, могут переходить на другие атомы азота или на атомы кислорода кетогруппы. Поэтому в растворах будет существовать равновесие различных таутомерных структур, быстро переходящих друг в друга. В результате таутомерых превращений U и G в енольной форме при спаривании могут имитировать С и А, а С и А в иминоформе - U и G, что может привести к мутациям в ДНК. • В растворе обычные кето- и аминоформы всегда превалируют над енольной и имино-формами, доля которых, как правило, не превышает 0, 1 %. Эта величина может сильно меняться для модифицированных оснований или для оснований в составе комплементарной пары. 19
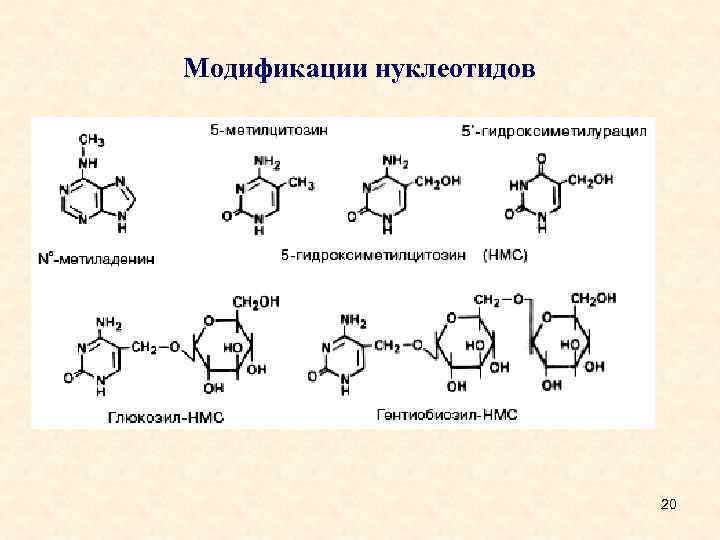 Модификации нуклеотидов 20
Модификации нуклеотидов 20
 • Нуклеотиды в ДНК могут подвергаться модификациям: 5 метилцитозин, 5 -гидроксиметилурацил, N-метиладенин. • В ДНК некоторых бактериофагов к гидроксиметильной группе гидроксиметилцитозина присоединены с помощью гликозидной связи моно- или дисахариды. • ДНК большинства низших эукариот и беспозвоночных содержат относительно мало 5 -метилцитозина и N 6 -метиладенина. • У позвоночных метилирование оснований играет важную роль в регуляции экспрессии генов, причем наиболее распространен 5 метилцитозин. • Показано, что более 95% метильных групп в ДНК позвоночных содержится в остатках цитозина редко встречающихся Cp. Gдинуклеотидов и более 50% таких динуклеотидов метилировано. У растений 5 -метилцитозин можно обнаружить в динуклеотидах и тринуклеотидах CNG (N – C, А или Т). 21
• Нуклеотиды в ДНК могут подвергаться модификациям: 5 метилцитозин, 5 -гидроксиметилурацил, N-метиладенин. • В ДНК некоторых бактериофагов к гидроксиметильной группе гидроксиметилцитозина присоединены с помощью гликозидной связи моно- или дисахариды. • ДНК большинства низших эукариот и беспозвоночных содержат относительно мало 5 -метилцитозина и N 6 -метиладенина. • У позвоночных метилирование оснований играет важную роль в регуляции экспрессии генов, причем наиболее распространен 5 метилцитозин. • Показано, что более 95% метильных групп в ДНК позвоночных содержится в остатках цитозина редко встречающихся Cp. Gдинуклеотидов и более 50% таких динуклеотидов метилировано. У растений 5 -метилцитозин можно обнаружить в динуклеотидах и тринуклеотидах CNG (N – C, А или Т). 21
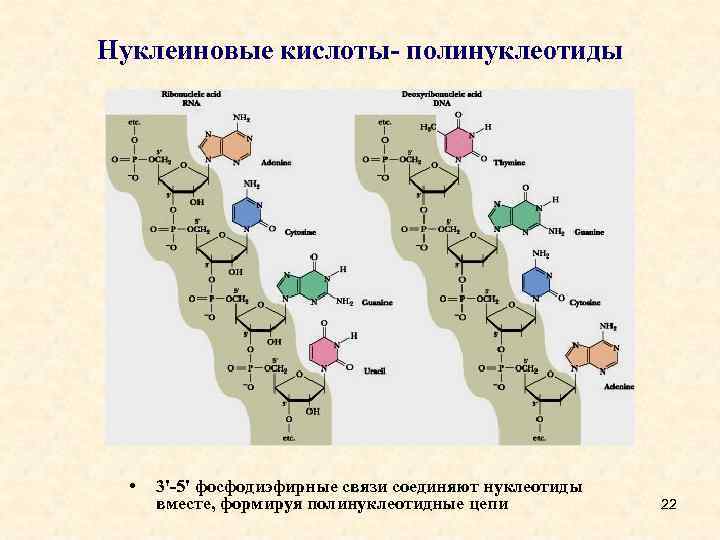 Нуклеиновые кислоты- полинуклеотиды • 3'-5' фосфодиэфирные связи соединяют нуклеотиды вместе, формируя полинуклеотидные цепи 22
Нуклеиновые кислоты- полинуклеотиды • 3'-5' фосфодиэфирные связи соединяют нуклеотиды вместе, формируя полинуклеотидные цепи 22
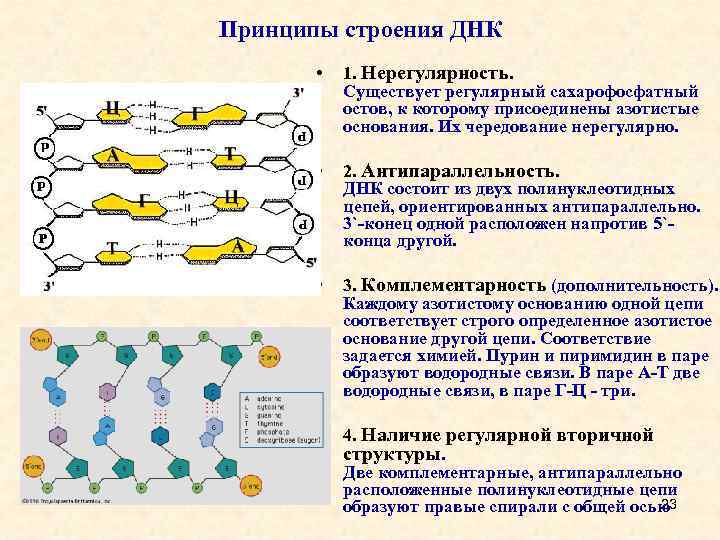 Принципы строения ДНК • 1. Нерегулярность. Существует регулярный сахарофосфатный остов, к которому присоединены азотистые основания. Их чередование нерегулярно. • 2. Антипараллельность. ДНК состоит из двух полинуклеотидных цепей, ориентированных антипараллельно. 3`-конец одной расположен напротив 5`конца другой. • 3. Комплементарность (дополнительность). Каждому азотистому основанию одной цепи соответствует строго определенное азотистое основание другой цепи. Соответствие задается химией. Пурин и пиримидин в паре образуют водородные связи. В паре A-Т две водородные связи, в паре Г-Ц - три. • 4. Наличие регулярной вторичной структуры. Две комплементарные, антипараллельно расположенные полинуклеотидные цепи 23 образуют правые спирали с общей осью
Принципы строения ДНК • 1. Нерегулярность. Существует регулярный сахарофосфатный остов, к которому присоединены азотистые основания. Их чередование нерегулярно. • 2. Антипараллельность. ДНК состоит из двух полинуклеотидных цепей, ориентированных антипараллельно. 3`-конец одной расположен напротив 5`конца другой. • 3. Комплементарность (дополнительность). Каждому азотистому основанию одной цепи соответствует строго определенное азотистое основание другой цепи. Соответствие задается химией. Пурин и пиримидин в паре образуют водородные связи. В паре A-Т две водородные связи, в паре Г-Ц - три. • 4. Наличие регулярной вторичной структуры. Две комплементарные, антипараллельно расположенные полинуклеотидные цепи 23 образуют правые спирали с общей осью
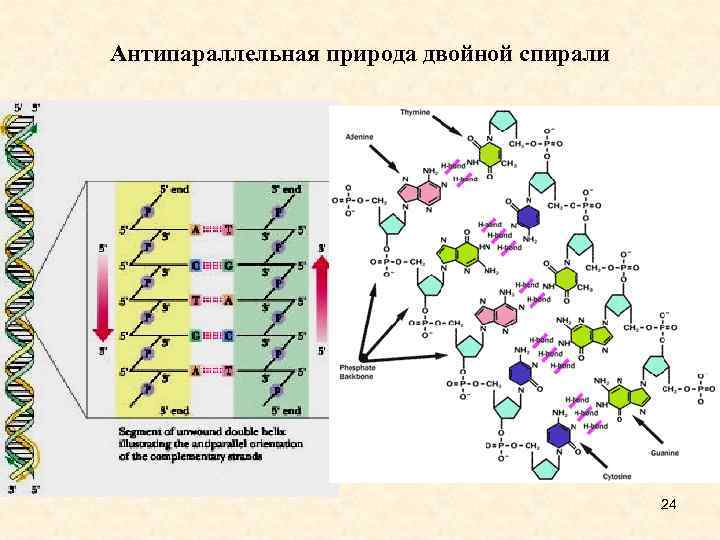 Антипараллельная природа двойной спирали 24
Антипараллельная природа двойной спирали 24
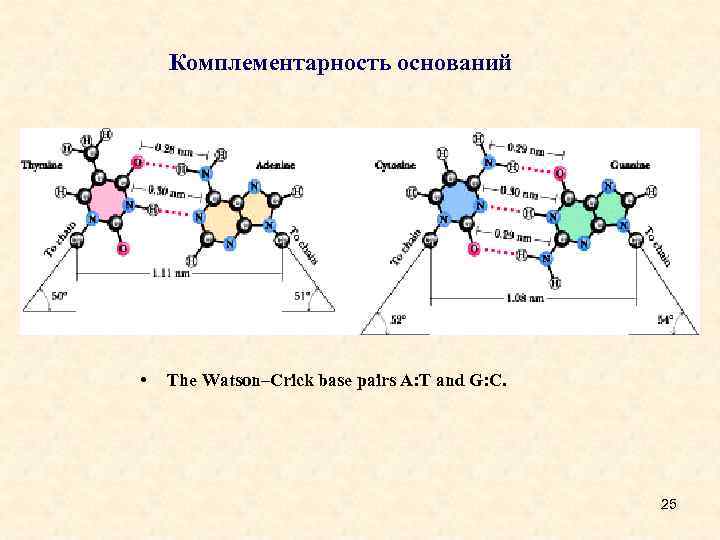 Комплементарность оснований • The Watson–Crick base pairs A: T and G: C. 25
Комплементарность оснований • The Watson–Crick base pairs A: T and G: C. 25
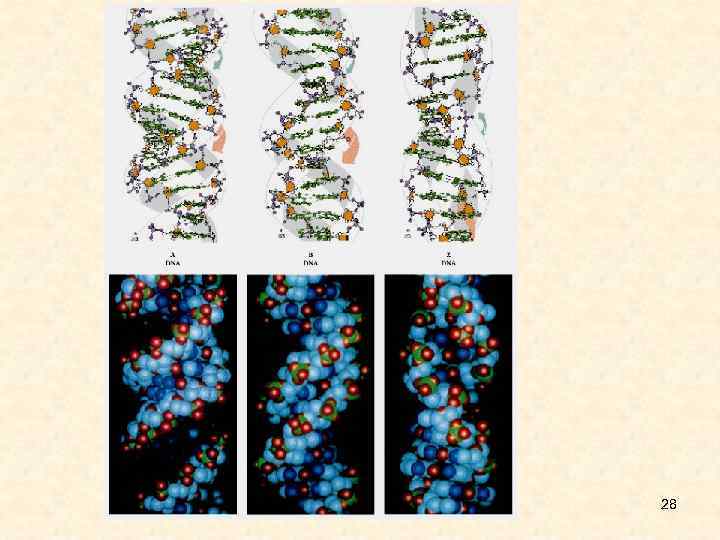
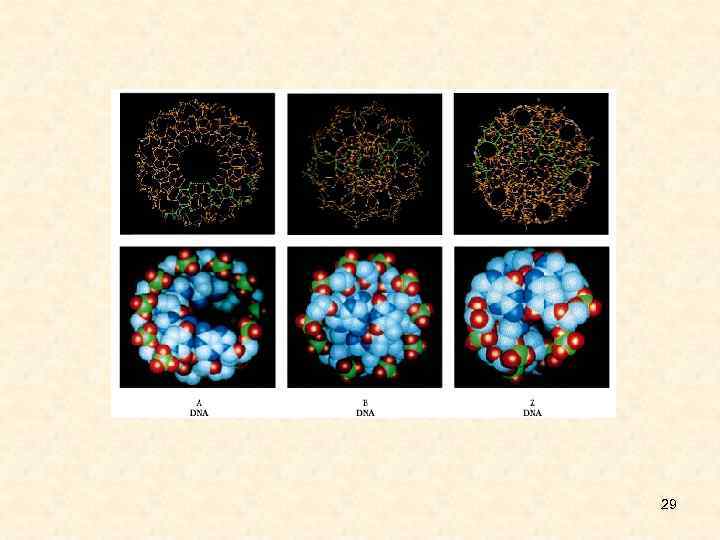
 Формы двойной спирали ДНК • Существуют несколько форм двойной спирали ДНК. • В основной - В-форме (паракристаллическая, Н 2 О>40%) на виток приходится 10 комплементарных пар. Плоскости азотистых оснований перпендикулярны оси спирали. Соседние комплементарные пары повернуты друг относительно друга на 360. Диаметр спирали 20Å, причем пуриновый нуклеотид занимает 12Å, а пиримидиновый - 8Å. • А-форма (кристаллическая, Н 2 О<40%) - 11 пар азотистых оснований на виток. Плоскости азотистых оснований отклонены от нормали к оси спирали на 200. Отсюда следует наличие внутренней пустоты диаметром 5Å. Высота витка 28Å. Такие же параметры у гибрида из одной цепи ДНК и одной цепи РНК. • С-форма - шаг спирали 31Å, 9. 3 пар оснований на виток, угол наклона к перпендикуляру 60. • Все три формы - правозакрученные спирали. • Есть еще несколько форм правых спиралей и всего одна левая спираль (Z -форма). Высота витка в Z-форме -44. 5 Å, на виток приходится 12 пар нуклеотидов. Ни А-, ни Z- формы не могут существовать в водном растворе без 26 дополнительных воздействий (белки или суперспирализация).
Формы двойной спирали ДНК • Существуют несколько форм двойной спирали ДНК. • В основной - В-форме (паракристаллическая, Н 2 О>40%) на виток приходится 10 комплементарных пар. Плоскости азотистых оснований перпендикулярны оси спирали. Соседние комплементарные пары повернуты друг относительно друга на 360. Диаметр спирали 20Å, причем пуриновый нуклеотид занимает 12Å, а пиримидиновый - 8Å. • А-форма (кристаллическая, Н 2 О<40%) - 11 пар азотистых оснований на виток. Плоскости азотистых оснований отклонены от нормали к оси спирали на 200. Отсюда следует наличие внутренней пустоты диаметром 5Å. Высота витка 28Å. Такие же параметры у гибрида из одной цепи ДНК и одной цепи РНК. • С-форма - шаг спирали 31Å, 9. 3 пар оснований на виток, угол наклона к перпендикуляру 60. • Все три формы - правозакрученные спирали. • Есть еще несколько форм правых спиралей и всего одна левая спираль (Z -форма). Высота витка в Z-форме -44. 5 Å, на виток приходится 12 пар нуклеотидов. Ни А-, ни Z- формы не могут существовать в водном растворе без 26 дополнительных воздействий (белки или суперспирализация).
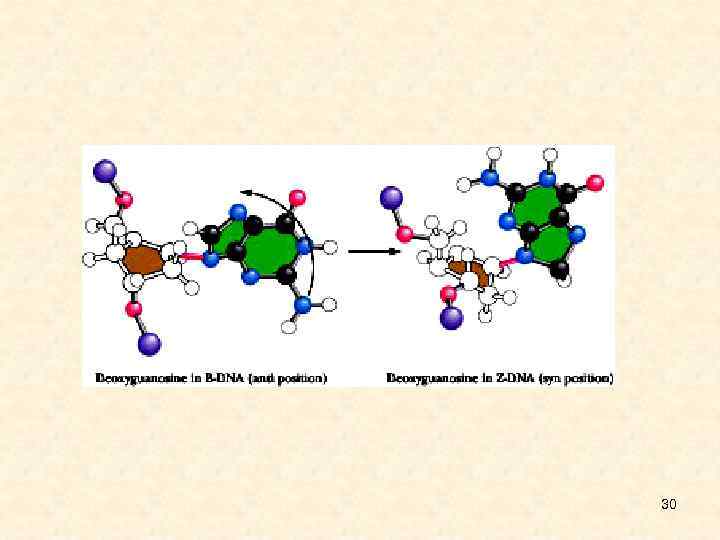
 • При исследовании ДНК различными методами обнаружено наличие различных форм ДНК образуемые при различных условиях (концентрации солей, влажность), некоторые из которых способны существовать в живых организмах. Существуют A, B, C, D, T-семейства форм ДНК, которые могут быть подразделены на различные подтипы (C', C''). В-ДНК - основное состояние ДНК показанное на кристаллах и в водных растворах. С-ДНК - форма существующая при пониженной концентрации Na и влажности 44 - • • 66%, если GC=31 -72%. А-ДНК - такая форма образуется у гибридов ДНК-РНК, следовательно при транскрипции ДНК переходит в А-форму, в месте контакта RNA-pol. Для этой формы характерно наличие внутренней пустоты диаметром 5Å. Z-ДНК - левозакрученная форма Переходу B-->Z способстует наличие GC-5' последовательности являющейся местом метилирования у организмов. Такие последовательности в плазмидах при сверхспирализации переходят из B в Z форму. При B-->Z переходе участок в 11 пн имеет переходную форму между левой и правой спиралью. Z-ДНК обнаружена в междисках политенных хромосом D. melanogaster. Полинуклеотид GC-5' находясь в В-форме при низкой концентрации соли образует нуклеосомы. При высоких концентрациях соли полинуклеотид GC-5' переходит в Zформу которая не образует нуклеосом. А-, Z- формы не могут существовать в водном растворе без дополнительных воздействий (белки, суперспирализация). D-DNA - AT-богатые участки ДНК фага Т 2, у которого цитозин заменен на 5'гидроксиметилцитозин, единственная из известных природных ДНК находится в Dформе. Кроме того ДНК фага гликозилирована более чем на 70%. Двойная спираль D-ДНК закручена сильнее чем B-ДНК и имеет глубокий малый желоб 27 - удобнуюю полость для размещения воды и катионов.
• При исследовании ДНК различными методами обнаружено наличие различных форм ДНК образуемые при различных условиях (концентрации солей, влажность), некоторые из которых способны существовать в живых организмах. Существуют A, B, C, D, T-семейства форм ДНК, которые могут быть подразделены на различные подтипы (C', C''). В-ДНК - основное состояние ДНК показанное на кристаллах и в водных растворах. С-ДНК - форма существующая при пониженной концентрации Na и влажности 44 - • • 66%, если GC=31 -72%. А-ДНК - такая форма образуется у гибридов ДНК-РНК, следовательно при транскрипции ДНК переходит в А-форму, в месте контакта RNA-pol. Для этой формы характерно наличие внутренней пустоты диаметром 5Å. Z-ДНК - левозакрученная форма Переходу B-->Z способстует наличие GC-5' последовательности являющейся местом метилирования у организмов. Такие последовательности в плазмидах при сверхспирализации переходят из B в Z форму. При B-->Z переходе участок в 11 пн имеет переходную форму между левой и правой спиралью. Z-ДНК обнаружена в междисках политенных хромосом D. melanogaster. Полинуклеотид GC-5' находясь в В-форме при низкой концентрации соли образует нуклеосомы. При высоких концентрациях соли полинуклеотид GC-5' переходит в Zформу которая не образует нуклеосом. А-, Z- формы не могут существовать в водном растворе без дополнительных воздействий (белки, суперспирализация). D-DNA - AT-богатые участки ДНК фага Т 2, у которого цитозин заменен на 5'гидроксиметилцитозин, единственная из известных природных ДНК находится в Dформе. Кроме того ДНК фага гликозилирована более чем на 70%. Двойная спираль D-ДНК закручена сильнее чем B-ДНК и имеет глубокий малый желоб 27 - удобнуюю полость для размещения воды и катионов.
 28
28
 29
29
 30
30
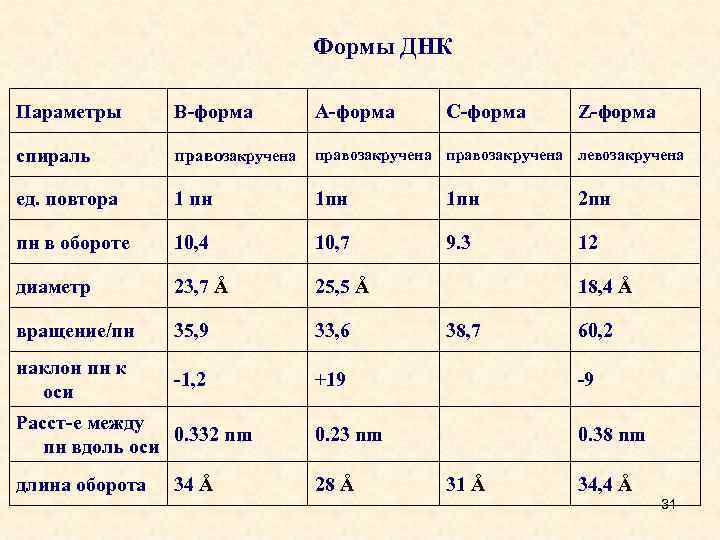 Формы ДНК Параметры B-форма А-форма спираль правозакручена левозакручена ед. повтора 1 пн 1 пн 2 пн пн в обороте 10, 4 10, 7 9. 3 12 диаметр 23, 7 Å 25, 5 Å 18, 4 Å вращение/пн 35, 9 33, 6 38, 7 60, 2 наклон пн к оси -1, 2 +19 -9 Расст-е между 0. 332 nm пн вдоль оси 0. 23 nm 0. 38 nm длина оборота 28 Å 31 Å 34, 4 Å 34 Å С-форма Z-форма 31
Формы ДНК Параметры B-форма А-форма спираль правозакручена левозакручена ед. повтора 1 пн 1 пн 2 пн пн в обороте 10, 4 10, 7 9. 3 12 диаметр 23, 7 Å 25, 5 Å 18, 4 Å вращение/пн 35, 9 33, 6 38, 7 60, 2 наклон пн к оси -1, 2 +19 -9 Расст-е между 0. 332 nm пн вдоль оси 0. 23 nm 0. 38 nm длина оборота 28 Å 31 Å 34, 4 Å 34 Å С-форма Z-форма 31
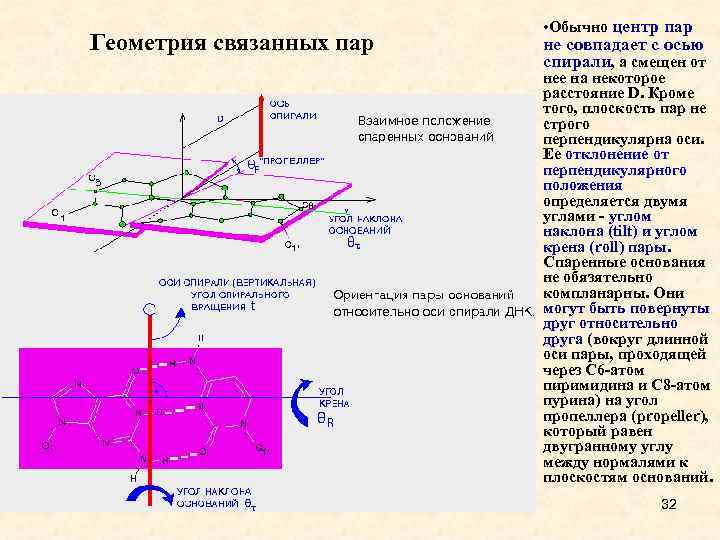 Геометрия связанных пар • Обычно центр пар не совпадает с осью спирали, а смещен от нее на некоторое расстояние D. Кроме того, плоскость пар не строго перпендикулярна оси. Ее отклонение от перпендикулярного положения определяется двумя углами - углом наклона (tilt) и углом крена (roll) пары. Спаренные основания не обязятельно компланарны. Они могут быть повернуты друг относительно друга (вокруг длинной оси пары, проходящей через С 6 -атом пиримидина и С 8 -атом пурина) на угол пропеллера (propeller), который равен двугранному углу между нормалями к плоскостям оснований. 32
Геометрия связанных пар • Обычно центр пар не совпадает с осью спирали, а смещен от нее на некоторое расстояние D. Кроме того, плоскость пар не строго перпендикулярна оси. Ее отклонение от перпендикулярного положения определяется двумя углами - углом наклона (tilt) и углом крена (roll) пары. Спаренные основания не обязятельно компланарны. Они могут быть повернуты друг относительно друга (вокруг длинной оси пары, проходящей через С 6 -атом пиримидина и С 8 -атом пурина) на угол пропеллера (propeller), который равен двугранному углу между нормалями к плоскостям оснований. 32
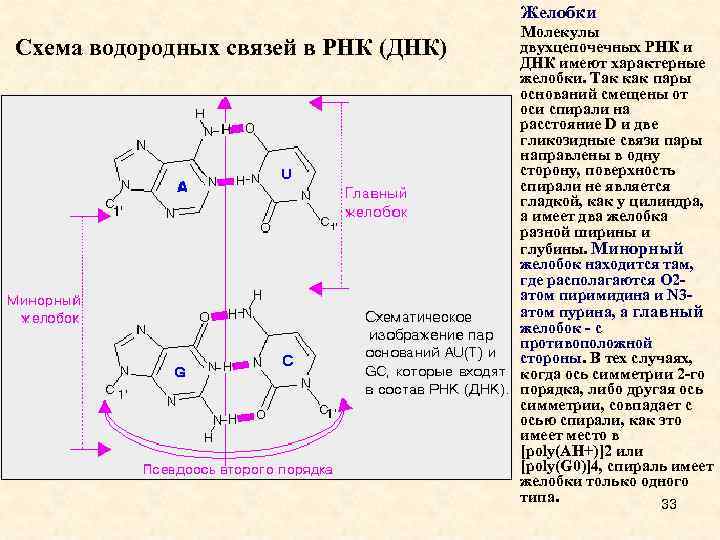 Желобки Схема водородных связей в РНК (ДНК) Молекулы двухцепочечных РНК и ДНК имеют характерные желобки. Так как пары оснований смещены от оси спирали на расстояние D и две гликозидные связи пары направлены в одну сторону, поверхность спирали не является гладкой, как у цилиндра, а имеет два желобка разной ширины и глубины. Минорный желобок находится там, где располагаются О 2 атом пиримидина и N 3 атом пурина, а главный желобок - с противоположной стороны. В тех случаях, когда ось симметрии 2 -го порядка, либо другая ось симметрии, совпадает с осью спирали, как это имеет место в [poly(AH+)]2 или [poly(G 0)]4, спираль имеет желобки только одного типа. 33
Желобки Схема водородных связей в РНК (ДНК) Молекулы двухцепочечных РНК и ДНК имеют характерные желобки. Так как пары оснований смещены от оси спирали на расстояние D и две гликозидные связи пары направлены в одну сторону, поверхность спирали не является гладкой, как у цилиндра, а имеет два желобка разной ширины и глубины. Минорный желобок находится там, где располагаются О 2 атом пиримидина и N 3 атом пурина, а главный желобок - с противоположной стороны. В тех случаях, когда ось симметрии 2 -го порядка, либо другая ось симметрии, совпадает с осью спирали, как это имеет место в [poly(AH+)]2 или [poly(G 0)]4, спираль имеет желобки только одного типа. 33
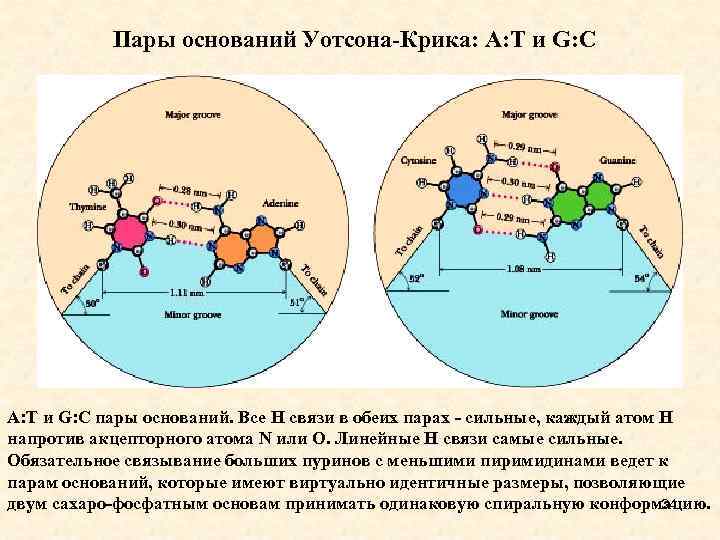 Пары оснований Уотсона-Крика: А: Т и G: C A: T и G: C пары оснований. Все H связи в обеих парах - сильные, каждый атом H напротив акцепторного атома N или O. Линейные H связи самые сильные. Обязательное связывание больших пуринов с меньшими пиримидинами ведет к парам оснований, которые имеют виртуально идентичные размеры, позволяющие 34 двум сахаро-фосфатным основам принимать одинаковую спиральную конформацию.
Пары оснований Уотсона-Крика: А: Т и G: C A: T и G: C пары оснований. Все H связи в обеих парах - сильные, каждый атом H напротив акцепторного атома N или O. Линейные H связи самые сильные. Обязательное связывание больших пуринов с меньшими пиримидинами ведет к парам оснований, которые имеют виртуально идентичные размеры, позволяющие 34 двум сахаро-фосфатным основам принимать одинаковую спиральную конформацию.
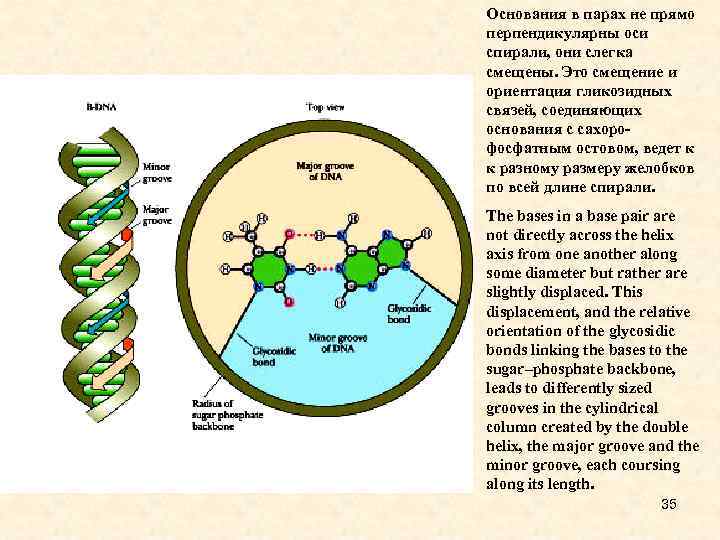 Основания в парах не прямо перпендикулярны оси спирали, они слегка смещены. Это смещение и ориентация гликозидных связей, соединяющих основания с сахорофосфатным остовом, ведет к к разному размеру желобков по всей длине спирали. The bases in a base pair are not directly across the helix axis from one another along some diameter but rather are slightly displaced. This displacement, and the relative orientation of the glycosidic bonds linking the bases to the sugar–phosphate backbone, leads to differently sized grooves in the cylindrical column created by the double helix, the major groove and the minor groove, each coursing along its length. 35
Основания в парах не прямо перпендикулярны оси спирали, они слегка смещены. Это смещение и ориентация гликозидных связей, соединяющих основания с сахорофосфатным остовом, ведет к к разному размеру желобков по всей длине спирали. The bases in a base pair are not directly across the helix axis from one another along some diameter but rather are slightly displaced. This displacement, and the relative orientation of the glycosidic bonds linking the bases to the sugar–phosphate backbone, leads to differently sized grooves in the cylindrical column created by the double helix, the major groove and the minor groove, each coursing along its length. 35
 Шаг спирали Шаг cпирали - это расстояние вдоль оси спирали, соответствующее одному полному витку (повороту на 360 град. ). Если n - число пар нуклеотидов на один виток, а h - расстояние между двумя соседними нуклеотидами вдоль оси спирали, то шаг спирали Р будет связан с этими величинами соотношением Р=nh. Для целочисленных спиралей n целое, но вообще говоря, оно может быть любым. ДНК: Угол спирального вращения (t)- это угол между двумя соседними нуклеотидами, t = 360/n, где n - число пар оснований на виток спирали. основания: геометрия комплементарных Связи С 1'-N(гликозидные связи) каждой цепи и соответствующие сахарофосфатные остовы, находящиеся в антипараллельной ориентации, связаны псевдоосью симметрии 2 -го порядка. Такая же псевдосимметрия характерна для двухцепочечных ДНК и РНК. В симметричных гетеропуриновых и гетеропиримидиновых парах, а также в уотсон-криковских пуринпиримидиновых парах ось симметрии связывает только гликозидные связи 36 C 1'--N, но не основания в целом, и поэтому называется псевдоосью
Шаг спирали Шаг cпирали - это расстояние вдоль оси спирали, соответствующее одному полному витку (повороту на 360 град. ). Если n - число пар нуклеотидов на один виток, а h - расстояние между двумя соседними нуклеотидами вдоль оси спирали, то шаг спирали Р будет связан с этими величинами соотношением Р=nh. Для целочисленных спиралей n целое, но вообще говоря, оно может быть любым. ДНК: Угол спирального вращения (t)- это угол между двумя соседними нуклеотидами, t = 360/n, где n - число пар оснований на виток спирали. основания: геометрия комплементарных Связи С 1'-N(гликозидные связи) каждой цепи и соответствующие сахарофосфатные остовы, находящиеся в антипараллельной ориентации, связаны псевдоосью симметрии 2 -го порядка. Такая же псевдосимметрия характерна для двухцепочечных ДНК и РНК. В симметричных гетеропуриновых и гетеропиримидиновых парах, а также в уотсон-криковских пуринпиримидиновых парах ось симметрии связывает только гликозидные связи 36 C 1'--N, но не основания в целом, и поэтому называется псевдоосью
 • Стекинг взаимодействие Основания в цепи ДНК лежат друг над другом в стопке, что обеспечивает дополнительную стабилизацию цепи - стекинг взаимодействие. Величина стекинг взаимодействия между основаниями: пурин>пиримидин-пурин>пиримидин-пиримидин В олиго- и полинуклеотидах стэкинг между соседними основаниями приводит к формированию стабильной одноцепочечной спиральной структуры (poly. A) а отсутствие стекинга к разупорядоченному клубку (poly. U) Энергия стекинг взаимодействий ~ -3 - -15 ккал/моль Сахарофосфатный остов снаружи, основания внутри, дезоксиробозофосфаты соединены фосфодиэфирными связями. ОНгруппы фосфата соединены с ОН-группой 3'- и 5'-углеродами дезоксирибозы. Ошибочное спаривание может происходить, когда тимин находится в енольной форме или цитозин находится в имино форме. 38
• Стекинг взаимодействие Основания в цепи ДНК лежат друг над другом в стопке, что обеспечивает дополнительную стабилизацию цепи - стекинг взаимодействие. Величина стекинг взаимодействия между основаниями: пурин>пиримидин-пурин>пиримидин-пиримидин В олиго- и полинуклеотидах стэкинг между соседними основаниями приводит к формированию стабильной одноцепочечной спиральной структуры (poly. A) а отсутствие стекинга к разупорядоченному клубку (poly. U) Энергия стекинг взаимодействий ~ -3 - -15 ккал/моль Сахарофосфатный остов снаружи, основания внутри, дезоксиробозофосфаты соединены фосфодиэфирными связями. ОНгруппы фосфата соединены с ОН-группой 3'- и 5'-углеродами дезоксирибозы. Ошибочное спаривание может происходить, когда тимин находится в енольной форме или цитозин находится в имино форме. 38
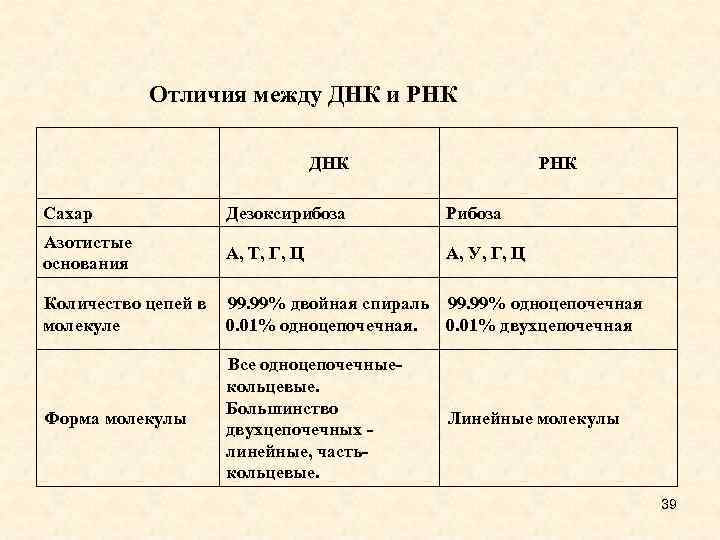 Отличия между ДНК и РНК ДНК РНК Сахар Дезоксирибоза Рибоза Азотистые основания А, Т, Г, Ц А, У, Г, Ц Количество цепей в 99. 99% двойная спираль 99. 99% одноцепочечная молекуле 0. 01% одноцепочечная. 0. 01% двухцепочечная Форма молекулы Все одноцепочечные- кольцевые. Большинство двухцепочечных - линейные, часть- кольцевые. Линейные молекулы 39
Отличия между ДНК и РНК ДНК РНК Сахар Дезоксирибоза Рибоза Азотистые основания А, Т, Г, Ц А, У, Г, Ц Количество цепей в 99. 99% двойная спираль 99. 99% одноцепочечная молекуле 0. 01% одноцепочечная. 0. 01% двухцепочечная Форма молекулы Все одноцепочечные- кольцевые. Большинство двухцепочечных - линейные, часть- кольцевые. Линейные молекулы 39
 Виды РНК Размер в нуклеотидах g. РНК - геномные РНК 10000 -100000 m. РНК - информационные (матричные) РНК 100 -100000 t. PHK - транспортные РНК 70 -90 r. РНК - рибосомные РНК несколько дискретных классов от 100 до 500000 s. РНК - малые РНК 100 -300 микро. РНК - mi. RNA <30 40
Виды РНК Размер в нуклеотидах g. РНК - геномные РНК 10000 -100000 m. РНК - информационные (матричные) РНК 100 -100000 t. PHK - транспортные РНК 70 -90 r. РНК - рибосомные РНК несколько дискретных классов от 100 до 500000 s. РНК - малые РНК 100 -300 микро. РНК - mi. RNA <30 40
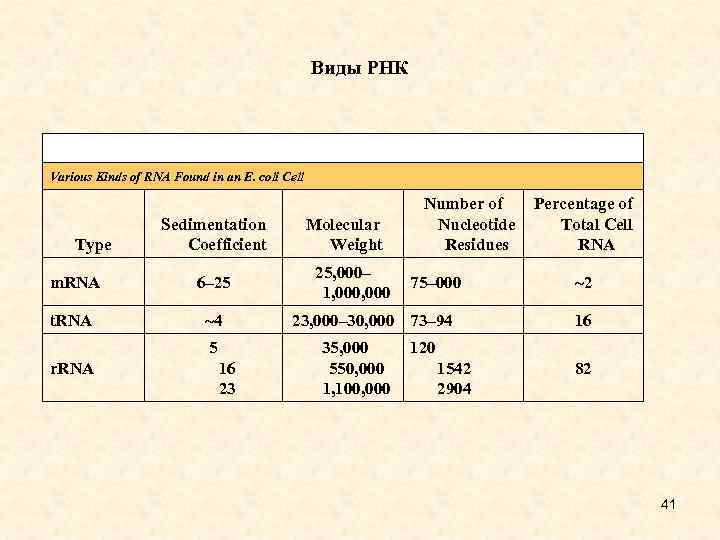 Виды РНК Various Kinds of RNA Found in an E. coli Cell Type Sedimentation Coefficient m. RNA 6– 25 t. RNA ~4 5 r. RNA 16 23 Molecular Weight 25, 000– 1, 000 Number of Nucleotide Residues 75– 000 23, 000– 30, 000 73– 94 35, 000 550, 000 1, 100, 000 Percentage of Total Cell RNA ~2 16 120 1542 2904 82 41
Виды РНК Various Kinds of RNA Found in an E. coli Cell Type Sedimentation Coefficient m. RNA 6– 25 t. RNA ~4 5 r. RNA 16 23 Molecular Weight 25, 000– 1, 000 Number of Nucleotide Residues 75– 000 23, 000– 30, 000 73– 94 35, 000 550, 000 1, 100, 000 Percentage of Total Cell RNA ~2 16 120 1542 2904 82 41
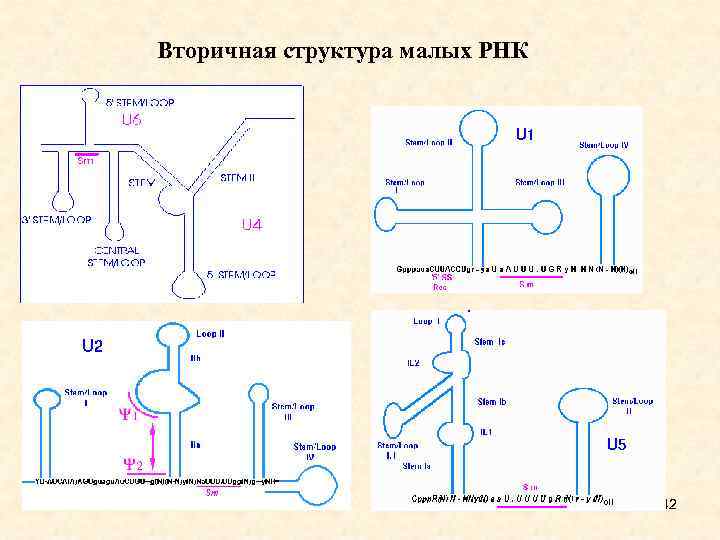 Вторичная структура малых РНК 42
Вторичная структура малых РНК 42
 микро. РНК многоклеточных организмов (из: Bartel, 2004; http: //ars. elscdn. com/content/image/1 -s 2. 0 S 0092867404000455 -gr 1. jpg). А, В и С - структуры стебель-петля для микро. РНК lin-4 и let-7; mir-1, mir-34 и mir-124 C. elegans (гомологи обнаружены у дрозофилы и млекопитающих) и mi. R-165 a, mi. R-172 a 2, JAW Arabidopsis (гомологи найдены у риса и других растений), соответственно. Синим цветом выделены микро. РНК, подтвержденные экспериментально, красным – прогнозированные.
микро. РНК многоклеточных организмов (из: Bartel, 2004; http: //ars. elscdn. com/content/image/1 -s 2. 0 S 0092867404000455 -gr 1. jpg). А, В и С - структуры стебель-петля для микро. РНК lin-4 и let-7; mir-1, mir-34 и mir-124 C. elegans (гомологи обнаружены у дрозофилы и млекопитающих) и mi. R-165 a, mi. R-172 a 2, JAW Arabidopsis (гомологи найдены у риса и других растений), соответственно. Синим цветом выделены микро. РНК, подтвержденные экспериментально, красным – прогнозированные.
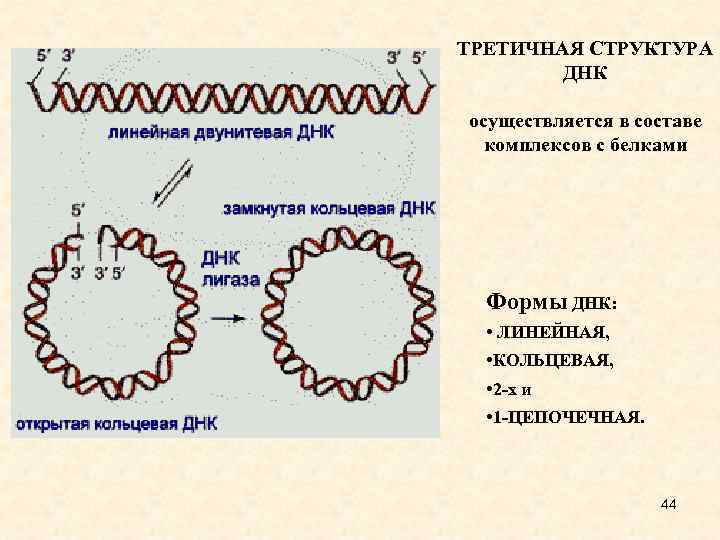 ТРЕТИЧНАЯ СТРУКТУРА ДНК осуществляется в составе комплексов с белками Формы ДНК: • ЛИНЕЙНАЯ, • КОЛЬЦЕВАЯ, • 2 -х и • 1 -ЦЕПОЧЕЧНАЯ. 44
ТРЕТИЧНАЯ СТРУКТУРА ДНК осуществляется в составе комплексов с белками Формы ДНК: • ЛИНЕЙНАЯ, • КОЛЬЦЕВАЯ, • 2 -х и • 1 -ЦЕПОЧЕЧНАЯ. 44
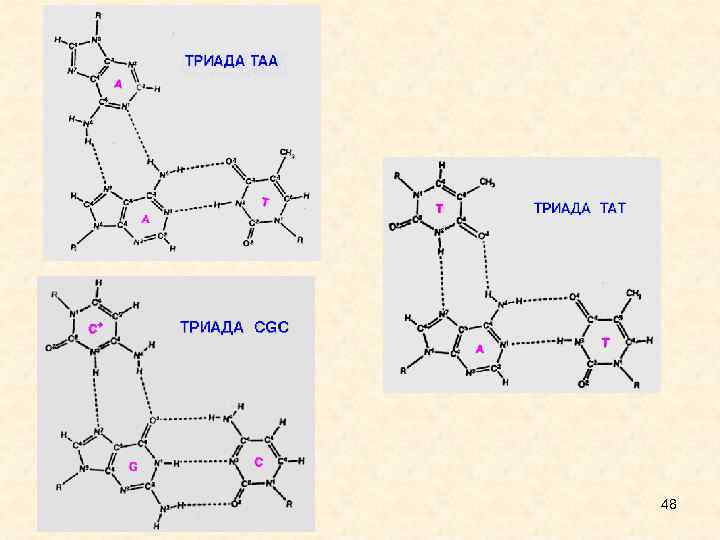
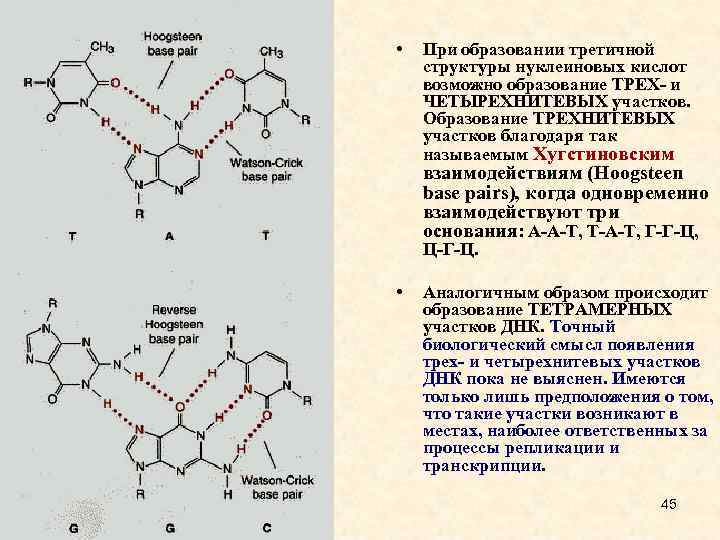 • При образовании третичной структуры нуклеиновых кислот возможно образование ТРЕХ- и ЧЕТЫРЕХНИТЕВЫХ участков. Образование ТРЕХНИТЕВЫХ участков благодаря так называемым Хугстиновским взаимодействиям (Hoogsteen base pairs), когда одновременно взаимодействуют три основания: А-А-Т, Т-А-Т, Г-Г-Ц, Ц-Г-Ц. • Аналогичным образом происходит образование ТЕТРАМЕРНЫХ участков ДНК. Точный биологический смысл появления трех- и четырехнитевых участков ДНК пока не выяснен. Имеются только лишь предположения о том, что такие участки возникают в местах, наиболее ответственных за процессы репликации и транскрипции. 45
• При образовании третичной структуры нуклеиновых кислот возможно образование ТРЕХ- и ЧЕТЫРЕХНИТЕВЫХ участков. Образование ТРЕХНИТЕВЫХ участков благодаря так называемым Хугстиновским взаимодействиям (Hoogsteen base pairs), когда одновременно взаимодействуют три основания: А-А-Т, Т-А-Т, Г-Г-Ц, Ц-Г-Ц. • Аналогичным образом происходит образование ТЕТРАМЕРНЫХ участков ДНК. Точный биологический смысл появления трех- и четырехнитевых участков ДНК пока не выяснен. Имеются только лишь предположения о том, что такие участки возникают в местах, наиболее ответственных за процессы репликации и транскрипции. 45
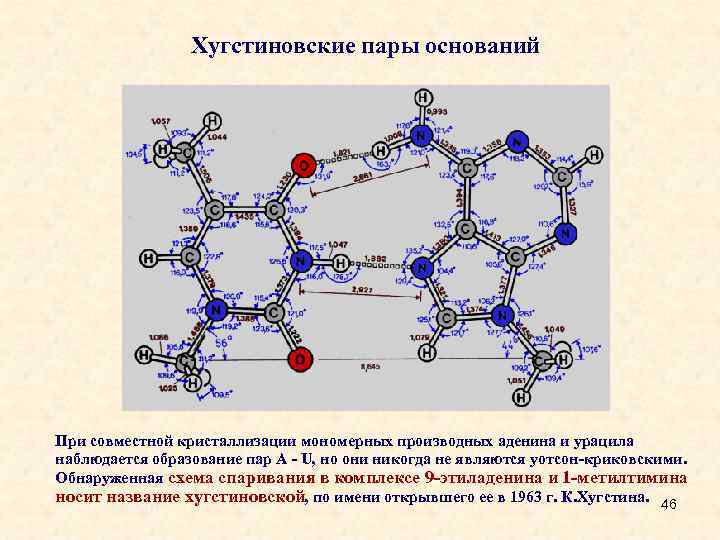 Хугстиновские пары оснований При совместной кристаллизации мономерных производных аденина и урацила наблюдается образование пар А - U, но они никогда не являются уотсон-криковскими. Обнаруженная схема спаривания в комплексе 9 -этиладенина и 1 -метилтимина носит название хугстиновской, по имени открывшего ее в 1963 г. К. Хугстина. 46
Хугстиновские пары оснований При совместной кристаллизации мономерных производных аденина и урацила наблюдается образование пар А - U, но они никогда не являются уотсон-криковскими. Обнаруженная схема спаривания в комплексе 9 -этиладенина и 1 -метилтимина носит название хугстиновской, по имени открывшего ее в 1963 г. К. Хугстина. 46
 • Уотсон-Криковские А-U и G-C пары изоморфны, т. е. близки по форме и имеют одинаковые размеры. В А - U паре расстояние C 1'. . . C 1' равно 10. 44 Å, что примерно на 0. 3 Å меньше, чем в паре G - C, а углы между прямой, соединяющей эти атомы, и гликозидными связями C 1'- N лежат в интервале 54, 4 - 57. 40. Если пренебречь этой незначительной разницей в 30, то можно считать, что гликозидные связи связаны друг с другом псевдоосью симметрии второго порядка. • В хугстиновской паре расстояние C 1'. . . C 1' на 2 Å меньше, чем в уотсон- криковской, и составляет 8. 654 Å, а угол между соответствующей прямой и гликозидной связью C 1'- N для пуриновых и пиримидиновых оснований различается более, чем на 100, т. е. псевдоось симметрии второго порядка отсутствует. • Два основания в уотсон-криковских парах некомпланарны, они повернуты друг относительно друга, подобно лопастям пропеллера. Угол пропеллера в паре А - U равен 120, а в паре G - C равен 70. В противоположность этому основания в хугстиновской паре строго компланарны. Однако в других кристаллических структурах, например, в хугстиновской паре 9 -метиладенин - 1 -метил-5 -иодурацил, наблюдается пропеллерный поворот, составляющий 90. 47
• Уотсон-Криковские А-U и G-C пары изоморфны, т. е. близки по форме и имеют одинаковые размеры. В А - U паре расстояние C 1'. . . C 1' равно 10. 44 Å, что примерно на 0. 3 Å меньше, чем в паре G - C, а углы между прямой, соединяющей эти атомы, и гликозидными связями C 1'- N лежат в интервале 54, 4 - 57. 40. Если пренебречь этой незначительной разницей в 30, то можно считать, что гликозидные связи связаны друг с другом псевдоосью симметрии второго порядка. • В хугстиновской паре расстояние C 1'. . . C 1' на 2 Å меньше, чем в уотсон- криковской, и составляет 8. 654 Å, а угол между соответствующей прямой и гликозидной связью C 1'- N для пуриновых и пиримидиновых оснований различается более, чем на 100, т. е. псевдоось симметрии второго порядка отсутствует. • Два основания в уотсон-криковских парах некомпланарны, они повернуты друг относительно друга, подобно лопастям пропеллера. Угол пропеллера в паре А - U равен 120, а в паре G - C равен 70. В противоположность этому основания в хугстиновской паре строго компланарны. Однако в других кристаллических структурах, например, в хугстиновской паре 9 -метиладенин - 1 -метил-5 -иодурацил, наблюдается пропеллерный поворот, составляющий 90. 47
 48
48
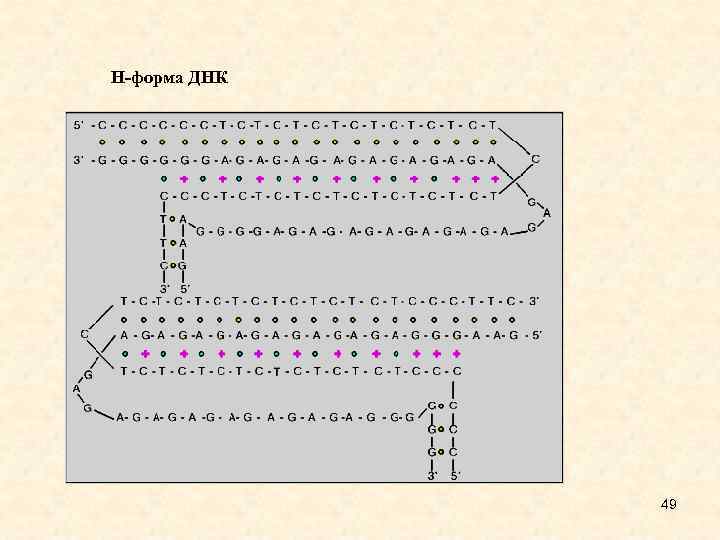 H-форма ДНК 49
H-форма ДНК 49
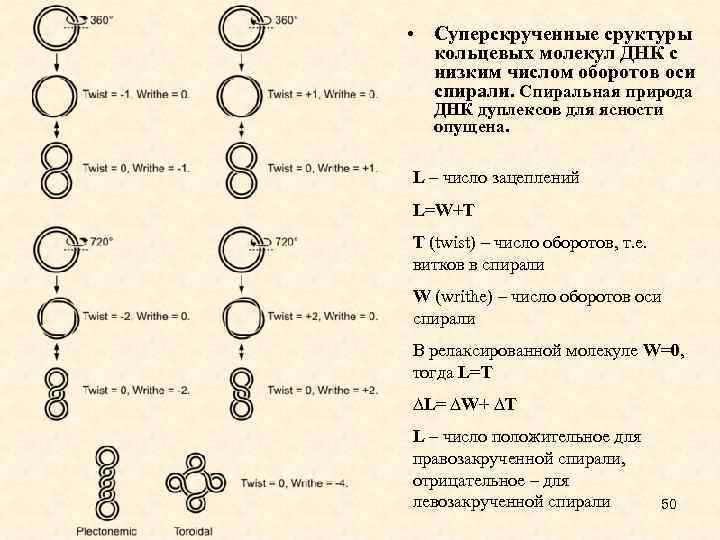 • Суперскрученные сруктуры кольцевых молекул ДНК с низким числом оборотов оси спирали. Спиральная природа ДНК дуплексов для ясности опущена. L – число зацеплений L=W+T T (twist) – число оборотов, т. е. витков в спирали W (writhe) – число оборотов оси спирали В релаксированной молекуле W=0, тогда L=T ∆L= ∆W+ ∆T L – число положительное для правозакрученной спирали, отрицательное – для левозакрученной спирали 50
• Суперскрученные сруктуры кольцевых молекул ДНК с низким числом оборотов оси спирали. Спиральная природа ДНК дуплексов для ясности опущена. L – число зацеплений L=W+T T (twist) – число оборотов, т. е. витков в спирали W (writhe) – число оборотов оси спирали В релаксированной молекуле W=0, тогда L=T ∆L= ∆W+ ∆T L – число положительное для правозакрученной спирали, отрицательное – для левозакрученной спирали 50
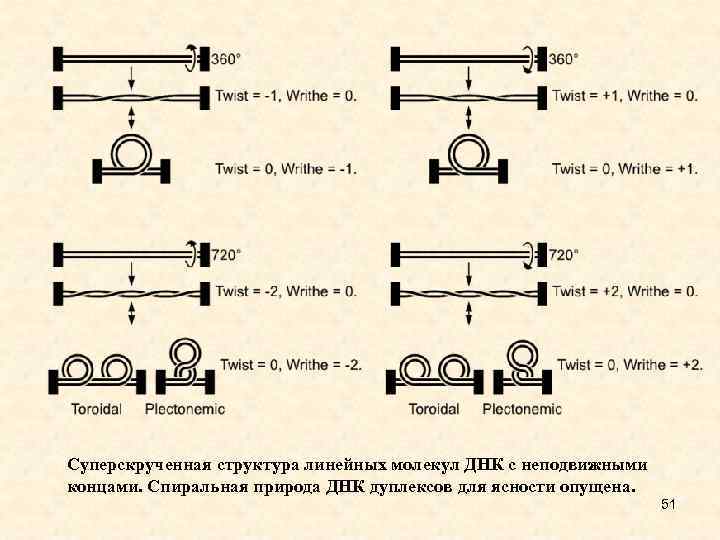 Суперскрученная структура линейных молекул ДНК с неподвижными концами. Спиральная природа ДНК дуплексов для ясности опущена. 51
Суперскрученная структура линейных молекул ДНК с неподвижными концами. Спиральная природа ДНК дуплексов для ясности опущена. 51
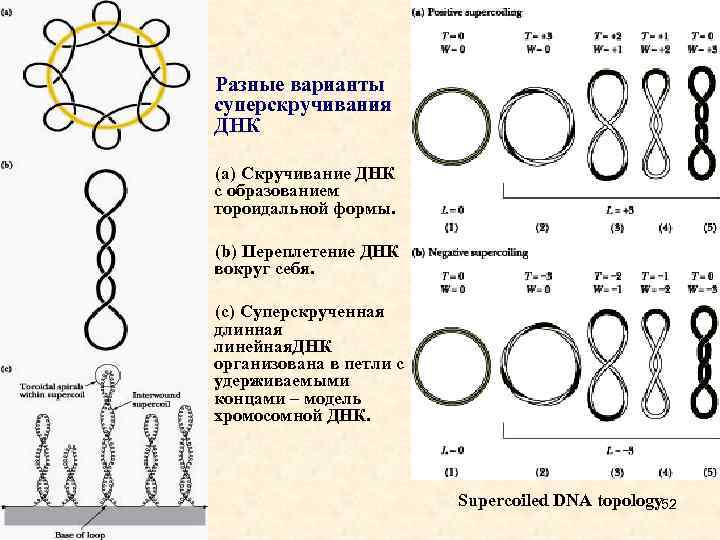 Разные варианты суперскручивания ДНК (a) Скручивание ДНК с образованием тороидальной формы. (b) Переплетение ДНК вокруг себя. (c) Суперскрученная длинная линейная. ДНК организована в петли с удерживаемыми концами – модель хромосомной ДНК. Supercoiled DNA topology 52
Разные варианты суперскручивания ДНК (a) Скручивание ДНК с образованием тороидальной формы. (b) Переплетение ДНК вокруг себя. (c) Суперскрученная длинная линейная. ДНК организована в петли с удерживаемыми концами – модель хромосомной ДНК. Supercoiled DNA topology 52
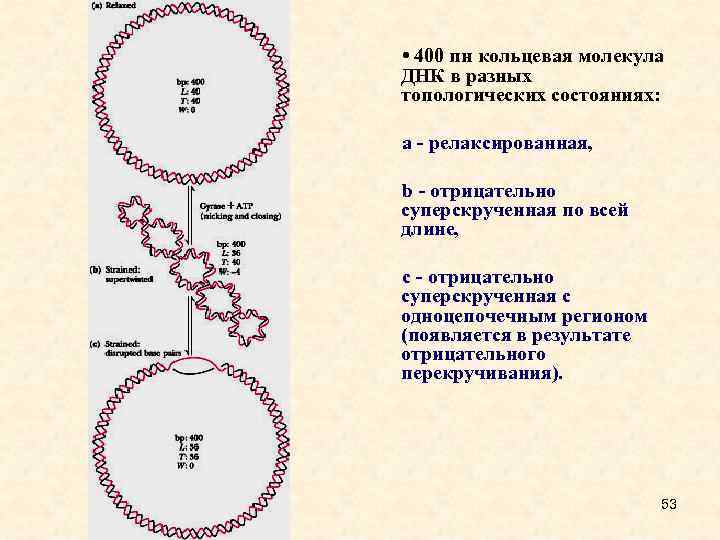 • 400 пн кольцевая молекула ДНК в разных топологических состояниях: a - релаксированная, b - отрицательно суперскрученная по всей длине, c - отрицательно суперскрученная с одноцепочечным регионом (появляется в результате отрицательного перекручивания). 53
• 400 пн кольцевая молекула ДНК в разных топологических состояниях: a - релаксированная, b - отрицательно суперскрученная по всей длине, c - отрицательно суперскрученная с одноцепочечным регионом (появляется в результате отрицательного перекручивания). 53
 • Суперспиральный виток образуется, когда 2 -цепочечная ДНК делает один оборот в том же направлении, в котором закручена сама двойная спираль (положительная суперспирализация), или в противоволожном направлении (отрицательная суперспирализация). Положительная суперспирализация «перекручивает» двойную спираль, а отрицательная – «не докручивает» . • Число зацеплений определяет, сколько раз две цепи замкнутой молекулы пересекают друга в пространстве. Число зацеплений не может быть изменено никакой деформацией молекулы, за исключением одной, включающей разрыв и воссоединение цепей. • Топологические перестройки ДНК – основной аспект, который надо учитывать при рассмотрении всех ее функциональных активностей – рекомбинации, репликации и транскрипции. Для всех этих процессов дуплексная структура ДНК служит препятствием. • Одинаковые молекулы, отличающиеся только числом зацеплений, называются топологическими изомерами. Ферменты, с помощью которых топологические изомеры могут превращаться из одной формы в другую, получили название топоизомераз. 54
• Суперспиральный виток образуется, когда 2 -цепочечная ДНК делает один оборот в том же направлении, в котором закручена сама двойная спираль (положительная суперспирализация), или в противоволожном направлении (отрицательная суперспирализация). Положительная суперспирализация «перекручивает» двойную спираль, а отрицательная – «не докручивает» . • Число зацеплений определяет, сколько раз две цепи замкнутой молекулы пересекают друга в пространстве. Число зацеплений не может быть изменено никакой деформацией молекулы, за исключением одной, включающей разрыв и воссоединение цепей. • Топологические перестройки ДНК – основной аспект, который надо учитывать при рассмотрении всех ее функциональных активностей – рекомбинации, репликации и транскрипции. Для всех этих процессов дуплексная структура ДНК служит препятствием. • Одинаковые молекулы, отличающиеся только числом зацеплений, называются топологическими изомерами. Ферменты, с помощью которых топологические изомеры могут превращаться из одной формы в другую, получили название топоизомераз. 54
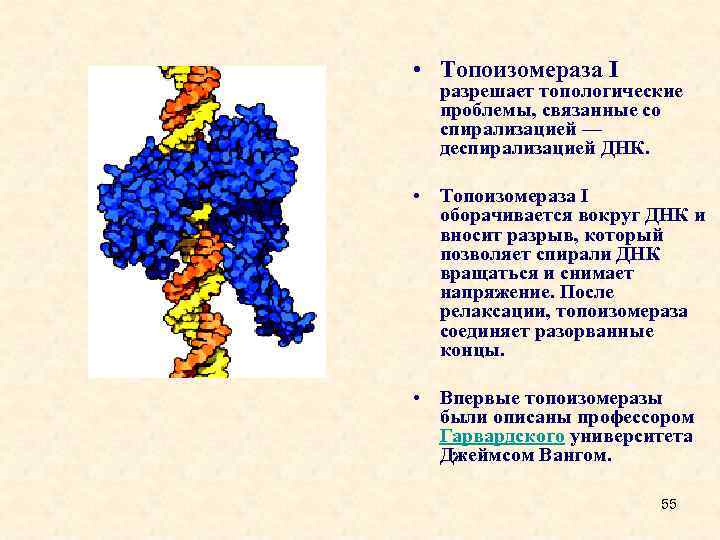 • Топоизомераза I разрешает топологические проблемы, связанные со спирализацией — деспирализацией ДНК. • Топоизомераза I оборачивается вокруг ДНК и вносит разрыв, который позволяет спирали ДНК вращаться и снимает напряжение. После релаксации, топоизомераза соединяет разорванные концы. • Впервые топоизомеразы были описаны профессором Гарвардского университета Джеймсом Вангом. 55
• Топоизомераза I разрешает топологические проблемы, связанные со спирализацией — деспирализацией ДНК. • Топоизомераза I оборачивается вокруг ДНК и вносит разрыв, который позволяет спирали ДНК вращаться и снимает напряжение. После релаксации, топоизомераза соединяет разорванные концы. • Впервые топоизомеразы были описаны профессором Гарвардского университета Джеймсом Вангом. 55
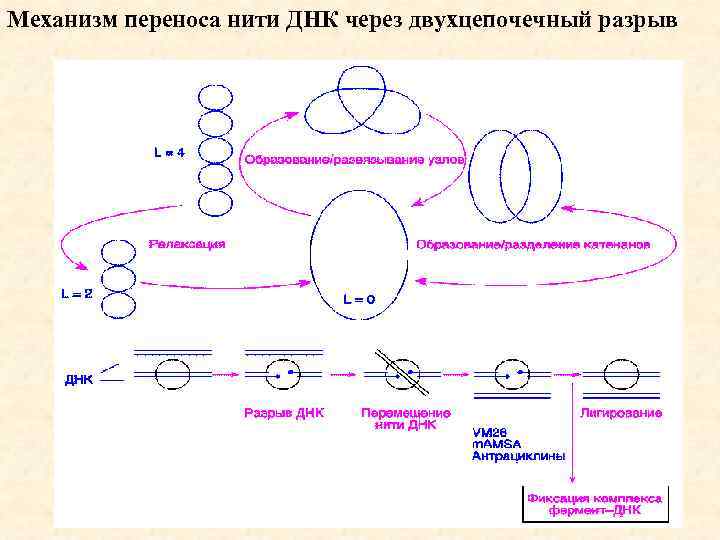 Механизм переноса нити ДНК через двухцепочечный разрыв 56
Механизм переноса нити ДНК через двухцепочечный разрыв 56
 • Точками отмечены места ковалентного присоединения фермента к 5'концам ДНК в двухцепочечных разрывах. VM 26, m. AMSA, антрациклины - ингибиторы топоизомеразы II, фиксирующие ковалентный комплекс фермент-ДНК и предотвращающие лигирование двухцепочечного разрыва; L - число зацеплений ДНК в суперскрученной молекуле. • КАТЕНАНЫ (от лат. catena - цепь), соединения, молекулы которых состоят из двух или более циклов, продетых один сквозь другой подобно звеньям цепи (напр. , ф-ла I). Циклы связаны между собой не химической, а т. наз. топологической (механической) связью. Известны катенаны с двумя и тремя циклами - [2] - и [3] - катенаны соответственно. 57
• Точками отмечены места ковалентного присоединения фермента к 5'концам ДНК в двухцепочечных разрывах. VM 26, m. AMSA, антрациклины - ингибиторы топоизомеразы II, фиксирующие ковалентный комплекс фермент-ДНК и предотвращающие лигирование двухцепочечного разрыва; L - число зацеплений ДНК в суперскрученной молекуле. • КАТЕНАНЫ (от лат. catena - цепь), соединения, молекулы которых состоят из двух или более циклов, продетых один сквозь другой подобно звеньям цепи (напр. , ф-ла I). Циклы связаны между собой не химической, а т. наз. топологической (механической) связью. Известны катенаны с двумя и тремя циклами - [2] - и [3] - катенаны соответственно. 57
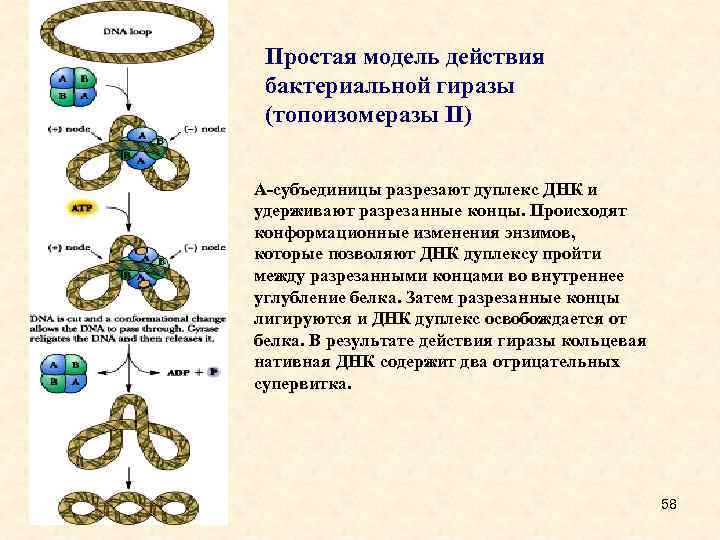 Простая модель действия бактериальной гиразы (топоизомеразы II) А-субъединицы разрезают дуплекс ДНК и удерживают разрезанные концы. Происходят конформационные изменения энзимов, которые позволяют ДНК дуплексу пройти между разрезанными концами во внутреннее углубление белка. Затем разрезанные концы лигируются и ДНК дуплекс освобождается от белка. В результате действия гиразы кольцевая нативная ДНК содержит два отрицательных супервитка. 58
Простая модель действия бактериальной гиразы (топоизомеразы II) А-субъединицы разрезают дуплекс ДНК и удерживают разрезанные концы. Происходят конформационные изменения энзимов, которые позволяют ДНК дуплексу пройти между разрезанными концами во внутреннее углубление белка. Затем разрезанные концы лигируются и ДНК дуплекс освобождается от белка. В результате действия гиразы кольцевая нативная ДНК содержит два отрицательных супервитка. 58
 Физико-химические свойства ДНК 59
Физико-химические свойства ДНК 59
 • кислотно-основные свойства • хелатирующая способность • способность к денатурации • оптические свойства • коллоидные свойства • осмотические свойства • высокая вязкость раствора
• кислотно-основные свойства • хелатирующая способность • способность к денатурации • оптические свойства • коллоидные свойства • осмотические свойства • высокая вязкость раствора
 Кислотно-основные свойства • В физиологических условиях (р. Н~7. 4) фосфатные группы в молекулах НК полностью ионизированы, т. е. в живых клетках НК имеют форму анионов и несут множество отрицательных зарядов. Поэтому НК эффективно связываются с основными белками (гистонами), суммарный заряд которых положительный. Взаимодействие с гистонами стабилизирует двойную спираль ДНК. На кислотноосновные свойства НК влияют и азотистые основания, главным образом через прочность водородных связей и стэкинг-взаимодействия, которые стабилизируют вторичную структуру ДНК.
Кислотно-основные свойства • В физиологических условиях (р. Н~7. 4) фосфатные группы в молекулах НК полностью ионизированы, т. е. в живых клетках НК имеют форму анионов и несут множество отрицательных зарядов. Поэтому НК эффективно связываются с основными белками (гистонами), суммарный заряд которых положительный. Взаимодействие с гистонами стабилизирует двойную спираль ДНК. На кислотноосновные свойства НК влияют и азотистые основания, главным образом через прочность водородных связей и стэкинг-взаимодействия, которые стабилизируют вторичную структуру ДНК.
 Хелатирующая способность • В водных растворах НК - активные полидентантные лиганды. Полидентантность обусловлена наличием ионизированных фосфатных групп и полярных групп азотистых оснований, которые способны образовывать координационные связи с катионами металлов. Связи с катионами щелочных металлов – лабильные, щелочноземельных – более прочные, dметаллов – стабильные.
Хелатирующая способность • В водных растворах НК - активные полидентантные лиганды. Полидентантность обусловлена наличием ионизированных фосфатных групп и полярных групп азотистых оснований, которые способны образовывать координационные связи с катионами металлов. Связи с катионами щелочных металлов – лабильные, щелочноземельных – более прочные, dметаллов – стабильные.
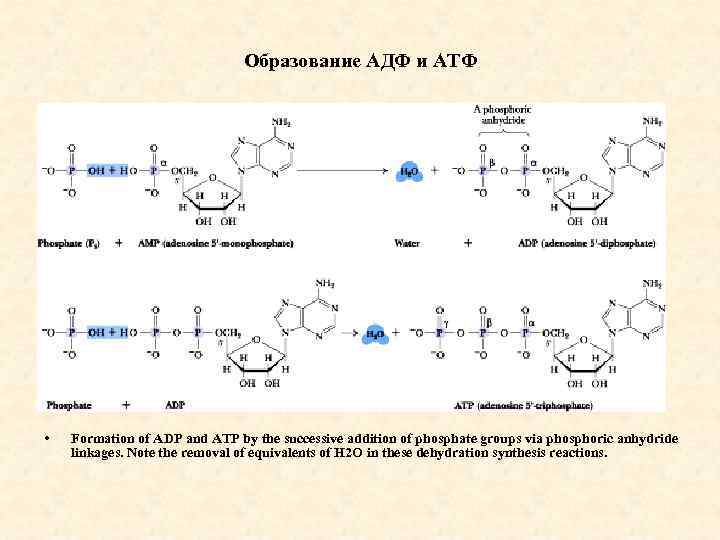 Образование АДФ и АТФ • Formation of ADP and ATP by the successive addition of phosphate groups via phosphoric anhydride linkages. Note the removal of equivalents of H 2 O in these dehydration synthesis reactions.
Образование АДФ и АТФ • Formation of ADP and ATP by the successive addition of phosphate groups via phosphoric anhydride linkages. Note the removal of equivalents of H 2 O in these dehydration synthesis reactions.
 Денатурация • Воздействие внешних факторов, приводящих к ослаблению или нарушению водородных связей или стэкинг-взаимодействий приводит к денатурации ДНК. Разрушение двойной спирали увеличивается интенсивность поглощения УФ света азотистыми основаниями – гиперхромный эффект. При образовании двойной спирали поглощение снижается – гипохромный эффект. Плавление ДНК. Молекулярная гибридизация.
Денатурация • Воздействие внешних факторов, приводящих к ослаблению или нарушению водородных связей или стэкинг-взаимодействий приводит к денатурации ДНК. Разрушение двойной спирали увеличивается интенсивность поглощения УФ света азотистыми основаниями – гиперхромный эффект. При образовании двойной спирали поглощение снижается – гипохромный эффект. Плавление ДНК. Молекулярная гибридизация.
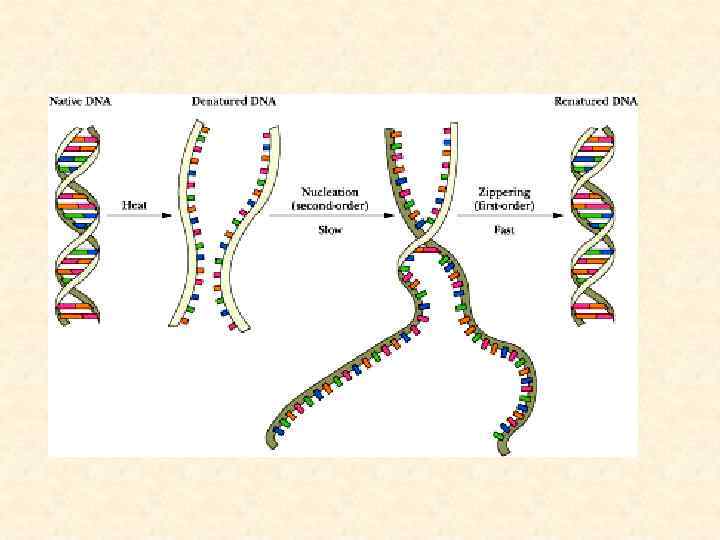
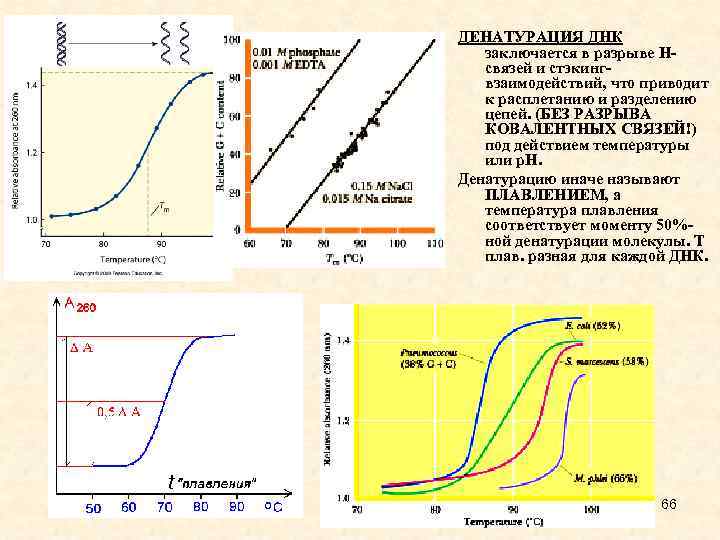 ДЕНАТУРАЦИЯ ДНК заключается в разрыве Нсвязей и стэкингвзаимодействий, что приводит к расплетанию и разделению цепей. (БЕЗ РАЗРЫВА КОВАЛЕНТНЫХ СВЯЗЕЙ!) под действием температуры или р. Н. Денатурацию иначе называют ПЛАВЛЕНИЕМ, а температура плавления соответствует моменту 50%ной денатурации молекулы. Т плав. разная для каждой ДНК. 66
ДЕНАТУРАЦИЯ ДНК заключается в разрыве Нсвязей и стэкингвзаимодействий, что приводит к расплетанию и разделению цепей. (БЕЗ РАЗРЫВА КОВАЛЕНТНЫХ СВЯЗЕЙ!) под действием температуры или р. Н. Денатурацию иначе называют ПЛАВЛЕНИЕМ, а температура плавления соответствует моменту 50%ной денатурации молекулы. Т плав. разная для каждой ДНК. 66
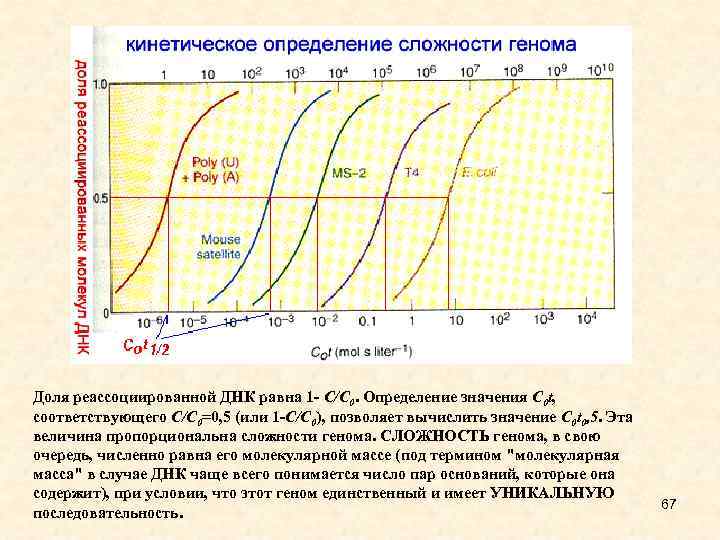 Доля реассоциированной ДНК равна 1 - C/C 0. Определение значения C 0 t, соответствующего C/C 0=0, 5 (или 1 -C/C 0), позволяет вычислить значение C 0 t 0, 5. Эта величина пропорциональна сложности генома. СЛОЖНОСТЬ генома, в свою очередь, численно равна его молекулярной массе (под термином "молекулярная масса" в случае ДНК чаще всего понимается число пар оснований, которые она содержит), при условии, что этот геном единственный и имеет УНИКАЛЬНУЮ последовательность. 67
Доля реассоциированной ДНК равна 1 - C/C 0. Определение значения C 0 t, соответствующего C/C 0=0, 5 (или 1 -C/C 0), позволяет вычислить значение C 0 t 0, 5. Эта величина пропорциональна сложности генома. СЛОЖНОСТЬ генома, в свою очередь, численно равна его молекулярной массе (под термином "молекулярная масса" в случае ДНК чаще всего понимается число пар оснований, которые она содержит), при условии, что этот геном единственный и имеет УНИКАЛЬНУЮ последовательность. 67
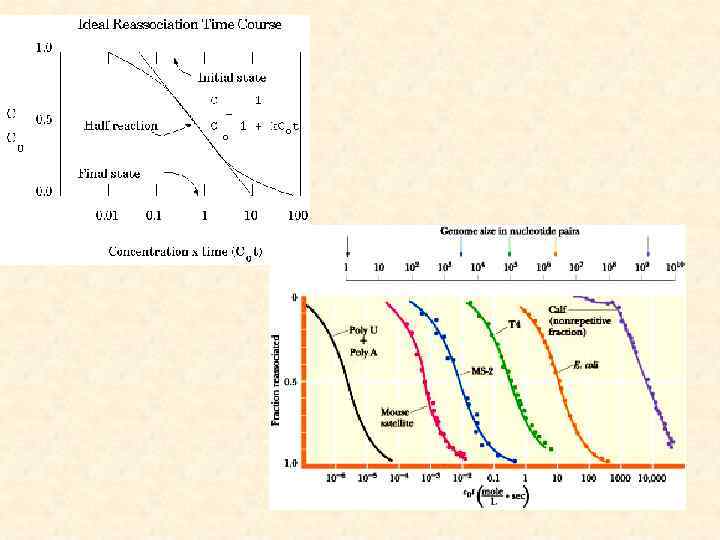
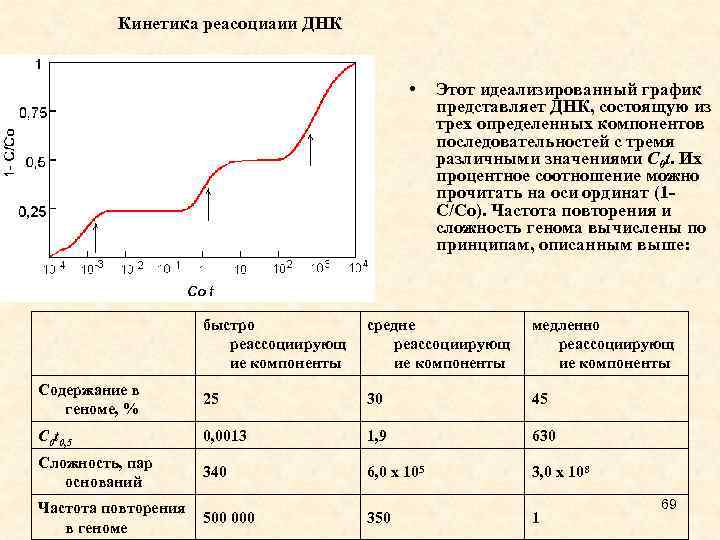 Кинетика реасоциаии ДНК • Этот идеализированный график представляет ДНК, состоящую из трех определенных компонентов последовательностей с тремя различными значениями C 0 t. Их процентное соотношение можно прочитать на оси ординат (1 С/Со). Частота повторения и сложность генома вычислены по принципам, описанным выше: быстро реассоциирующ ие компоненты средне реассоциирующ ие компоненты медленно реассоциирующ ие компоненты Содержание в геноме, % 25 30 45 C 0 t 0, 5 0, 0013 1, 9 630 Сложность, пар оснований 340 6, 0 х 105 3, 0 x 108 350 1 Частота повторения 500 000 в геноме 69
Кинетика реасоциаии ДНК • Этот идеализированный график представляет ДНК, состоящую из трех определенных компонентов последовательностей с тремя различными значениями C 0 t. Их процентное соотношение можно прочитать на оси ординат (1 С/Со). Частота повторения и сложность генома вычислены по принципам, описанным выше: быстро реассоциирующ ие компоненты средне реассоциирующ ие компоненты медленно реассоциирующ ие компоненты Содержание в геноме, % 25 30 45 C 0 t 0, 5 0, 0013 1, 9 630 Сложность, пар оснований 340 6, 0 х 105 3, 0 x 108 350 1 Частота повторения 500 000 в геноме 69
 70
70
 Жидкокристаллическое состояние НК • Нуклеотиды анизотропны, анизотропность усиливается с образованием комплементарной пары азотистых оснований. Поэтому в растворе отдельные фрагменты молекулы ДНК могут находиться в жидкокристаллической форме. Число и ориентация таких фрагментов в пространстве сильно влияют на состояние и биологические функции ДНК в клетке. Установлено, что жидкокристаллические состояния НК и их комплексов с белками играют важную роль в передаче наследственной информации, а также биосинтезе НК и белков.
Жидкокристаллическое состояние НК • Нуклеотиды анизотропны, анизотропность усиливается с образованием комплементарной пары азотистых оснований. Поэтому в растворе отдельные фрагменты молекулы ДНК могут находиться в жидкокристаллической форме. Число и ориентация таких фрагментов в пространстве сильно влияют на состояние и биологические функции ДНК в клетке. Установлено, что жидкокристаллические состояния НК и их комплексов с белками играют важную роль в передаче наследственной информации, а также биосинтезе НК и белков.
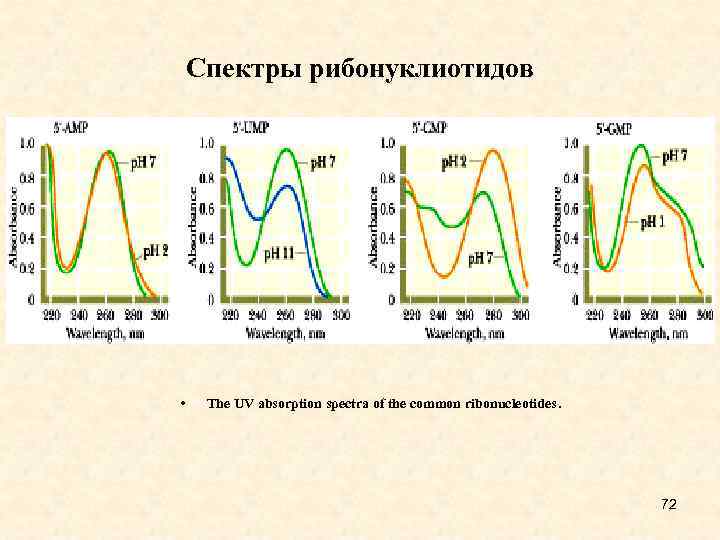 Cпектры рибонуклиотидов • The UV absorption spectra of the common ribonucleotides . 72
Cпектры рибонуклиотидов • The UV absorption spectra of the common ribonucleotides . 72
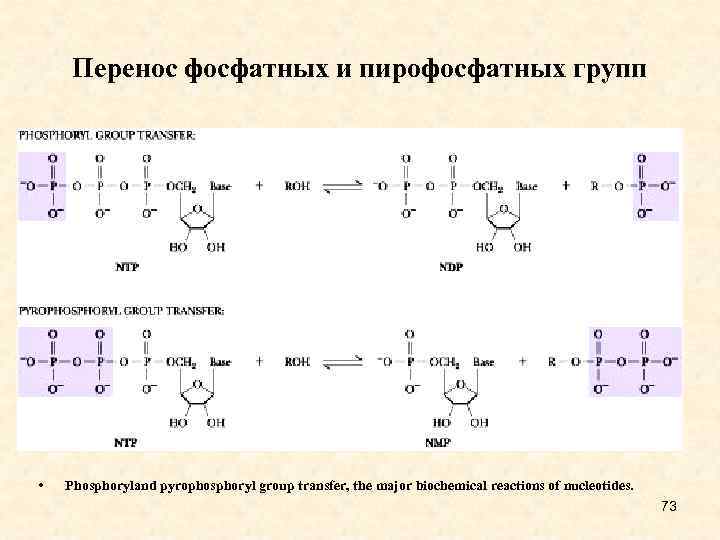 Перенос фосфатных и пирофосфатных групп • Phosphoryland pyrophosphoryl group transfer, the major biochemical reactions of nucleotides. 73
Перенос фосфатных и пирофосфатных групп • Phosphoryland pyrophosphoryl group transfer, the major biochemical reactions of nucleotides. 73
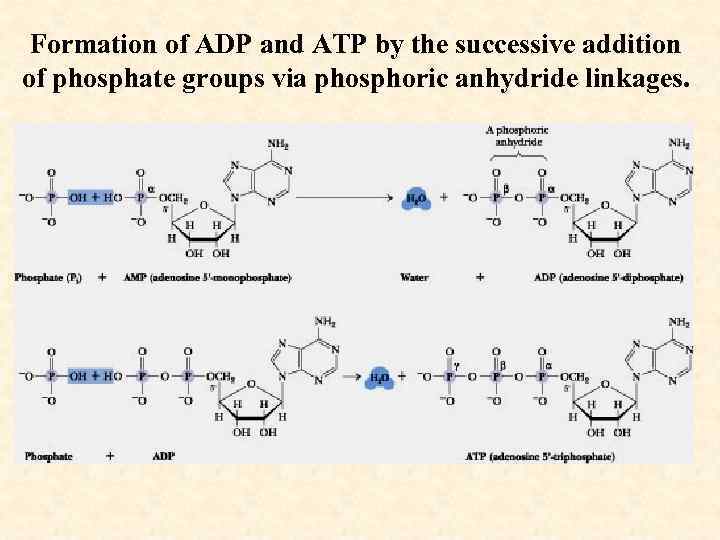 Formation of ADP and ATP by the successive addition of phosphate groups via phosphoric anhydride linkages.
Formation of ADP and ATP by the successive addition of phosphate groups via phosphoric anhydride linkages.
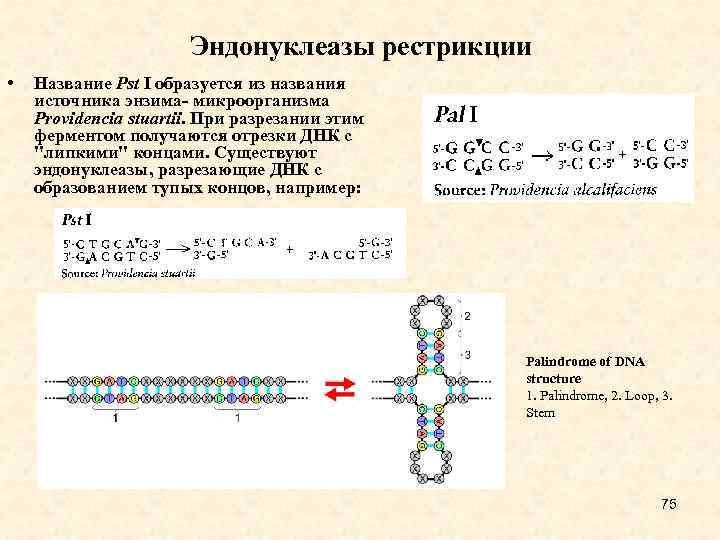 Эндонуклеазы рестрикции • Название Pst I образуется из названия источника энзима- микроорганизма Providencia stuartii. При разрезании этим ферментом получаются отрезки ДНК с "липкими" концами. Существуют эндонуклеазы, разрезающие ДНК с образованием тупых концов, например: Palindrome of DNA structure 1. Palindrome, 2. Loop, 3. Stem 75
Эндонуклеазы рестрикции • Название Pst I образуется из названия источника энзима- микроорганизма Providencia stuartii. При разрезании этим ферментом получаются отрезки ДНК с "липкими" концами. Существуют эндонуклеазы, разрезающие ДНК с образованием тупых концов, например: Palindrome of DNA structure 1. Palindrome, 2. Loop, 3. Stem 75
 Формы разрывов двухцепочечных ДНК под действием рестриктаз • а - 5'-выступающие (1), 3'-выступающие "липкие" (2) и "тупые" (3) концы ДНК, образующиеся под действием рестриктаз Bam. HI, Kpn. I и Pvu. II соответственно. Стрелками обозначены места разрывов цепей ДНК, пунктирной линией - ось 76 симметрии сайтов рестрикции; б - лигирование с потерей сайта рестрикции
Формы разрывов двухцепочечных ДНК под действием рестриктаз • а - 5'-выступающие (1), 3'-выступающие "липкие" (2) и "тупые" (3) концы ДНК, образующиеся под действием рестриктаз Bam. HI, Kpn. I и Pvu. II соответственно. Стрелками обозначены места разрывов цепей ДНК, пунктирной линией - ось 76 симметрии сайтов рестрикции; б - лигирование с потерей сайта рестрикции
 Эндонуклеазная активность рестриктаз • • • Специфичность узнавания последовательности ДНК и характер эндонуклеазной активности трех рестриктаз. Нае. III оставляет "тупой" конец, а другие ферменты - одноцепочечные концы. X - любой нуклеотид. 77
Эндонуклеазная активность рестриктаз • • • Специфичность узнавания последовательности ДНК и характер эндонуклеазной активности трех рестриктаз. Нае. III оставляет "тупой" конец, а другие ферменты - одноцепочечные концы. X - любой нуклеотид. 77
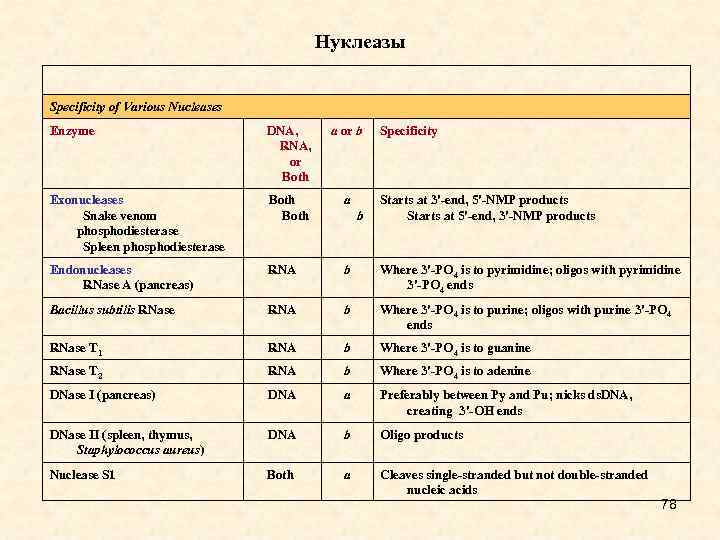 Нуклеазы Specificity of Various Nucleases Enzyme DNA, RNA, or Both a or b Exonucleases Snake venom phosphodiesterase Spleen phosphodiesterase Both a Endonucleases RNase A (pancreas) RNA b Where 3'-PO 4 is to pyrimidine; oligos with pyrimidine 3'-PO 4 ends Bacillus subtilis RNase RNA b Where 3'-PO 4 is to purine; oligos with purine 3'-PO 4 ends RNase T 1 RNA b Where 3'-PO 4 is to guanine RNase T 2 RNA b Where 3'-PO 4 is to adenine DNase I (pancreas) DNA a Preferably between Py and Pu; nicks ds. DNA, creating 3'-OH ends DNase II (spleen, thymus, Staphylococcus aureus) DNA b Oligo products Nuclease S 1 Both a Cleaves single-stranded but not double-stranded nucleic acids b Specificity Starts at 3'-end, 5'-NMP products Starts at 5'-end, 3'-NMP products 78
Нуклеазы Specificity of Various Nucleases Enzyme DNA, RNA, or Both a or b Exonucleases Snake venom phosphodiesterase Spleen phosphodiesterase Both a Endonucleases RNase A (pancreas) RNA b Where 3'-PO 4 is to pyrimidine; oligos with pyrimidine 3'-PO 4 ends Bacillus subtilis RNase RNA b Where 3'-PO 4 is to purine; oligos with purine 3'-PO 4 ends RNase T 1 RNA b Where 3'-PO 4 is to guanine RNase T 2 RNA b Where 3'-PO 4 is to adenine DNase I (pancreas) DNA a Preferably between Py and Pu; nicks ds. DNA, creating 3'-OH ends DNase II (spleen, thymus, Staphylococcus aureus) DNA b Oligo products Nuclease S 1 Both a Cleaves single-stranded but not double-stranded nucleic acids b Specificity Starts at 3'-end, 5'-NMP products Starts at 5'-end, 3'-NMP products 78
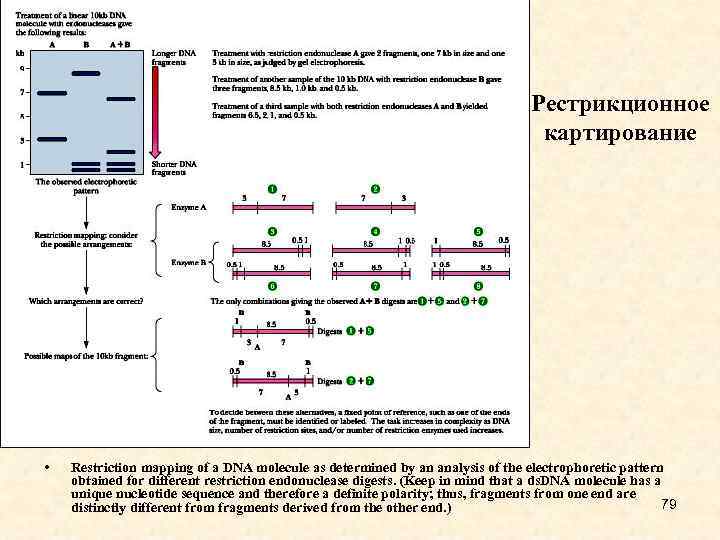 Рестрикционное картирование • Restriction mapping of a DNA molecule as determined by an analysis of the electrophoretic pattern obtained for different restriction endonuclease digests. (Keep in mind that a ds. DNA molecule has a unique nucleotide sequence and therefore a definite polarity; thus, fragments from one end are 79 distinctly different from fragments derived from the other end. )
Рестрикционное картирование • Restriction mapping of a DNA molecule as determined by an analysis of the electrophoretic pattern obtained for different restriction endonuclease digests. (Keep in mind that a ds. DNA molecule has a unique nucleotide sequence and therefore a definite polarity; thus, fragments from one end are 79 distinctly different from fragments derived from the other end. )
 Функции ДНК • 1. ДНК является носителем генетической информации. Функция обеспечивается фактом существования генетического кода. • 2. Воспроизведение и передача генетической информации в поколениях клеток и организмов. Функция обеспечивается процессом репликации. • 3. Реализация генетической информации в виде белков, а также любых других соединений, образующихся с помощью белковферментов. Функция обеспечивается процессами транскрипции и трансляции. 80
Функции ДНК • 1. ДНК является носителем генетической информации. Функция обеспечивается фактом существования генетического кода. • 2. Воспроизведение и передача генетической информации в поколениях клеток и организмов. Функция обеспечивается процессом репликации. • 3. Реализация генетической информации в виде белков, а также любых других соединений, образующихся с помощью белковферментов. Функция обеспечивается процессами транскрипции и трансляции. 80

 Основоположники молекулярной биологии 82
Основоположники молекулярной биологии 82
 83
83
 • • • Джеймс Дью и Уо тсон (англ. James Dewey Watson, род. 6 апреля 1928, Чикаго, Иллинойс) — американский биолог. Лауреат Нобелевской премии по физиологии и • медицине 1962 г. — совместно с Фрэнсисом Криком и Морисом Х. Ф. Уилкинсом за открытие структуры • молекулы ДНК. С детства, благодаря отцу, Джеймс был зачарован наблюдениями за жизнью птиц. В возрасте 12 лет Уотсон участвовал в популярной радиовикторине Quiz Kids для интеллектуальных молодых людей. Благодаря либеральной политике Роберта Хатчинса он поступил в колледж в возрасте 15 лет. Прочитав книгу Эрвина Шрёдингера «Что такое жизнь с точки зрения физики? » Уотсон изменил свои профессиональные интересы с изучения орнитологии на изучение генетики. В 1947 году получил степень бакалавра зоологии в университете Чикаго. В 1951 году поступил в Кавендишскую лабораторию Кембриджского университета, где изучал структуру белков. Там познакомился с физиком Фрэнсисом Криком, который интересовался биологией. В 1952 году Уотсон и Крик стали работать над моделированием структуры ДНК. Используя Правила Чаргаффа и рентгенограммы Розалинды Франклин и Мориса Уилкинса построили двухспиральную модель. Результаты работы опубликовали в апреле 1953 года в журнале Nature. 25 лет руководил научным институтом Колд Спринг Харбор, где вел исследования генетики рака. С 1989 года по 1992 год — организатор и руководитель проекта «Геном человека» по расшифровке последовательности человеческой ДНК, в это же время возглавляет секретный проект «Фауст» В 2007 году высказался в пользу того, что представители разных рас имеют различные интеллектуальные способности, что обусловлено генетически. В связи с нарушением политкорректности от него потребовали публичных извинений, а в октябре 2007 года Уотсон официально ушел с поста руководителя лаборатории, где он работал. Вместе с тем он продолжает руководить исследованиями в той же лаборатории. По сообщению издания «Индепендент» , исследование ДНК самого Джеймса Уотсона обнаружило высокую концентрацию африканских и, в меньшей мере, азиатских генов. Позже выяснилось, что анализ базировался на ошибочной версии генома. 84 Сейчас работает над поиском генов психических заболеваний.
• • • Джеймс Дью и Уо тсон (англ. James Dewey Watson, род. 6 апреля 1928, Чикаго, Иллинойс) — американский биолог. Лауреат Нобелевской премии по физиологии и • медицине 1962 г. — совместно с Фрэнсисом Криком и Морисом Х. Ф. Уилкинсом за открытие структуры • молекулы ДНК. С детства, благодаря отцу, Джеймс был зачарован наблюдениями за жизнью птиц. В возрасте 12 лет Уотсон участвовал в популярной радиовикторине Quiz Kids для интеллектуальных молодых людей. Благодаря либеральной политике Роберта Хатчинса он поступил в колледж в возрасте 15 лет. Прочитав книгу Эрвина Шрёдингера «Что такое жизнь с точки зрения физики? » Уотсон изменил свои профессиональные интересы с изучения орнитологии на изучение генетики. В 1947 году получил степень бакалавра зоологии в университете Чикаго. В 1951 году поступил в Кавендишскую лабораторию Кембриджского университета, где изучал структуру белков. Там познакомился с физиком Фрэнсисом Криком, который интересовался биологией. В 1952 году Уотсон и Крик стали работать над моделированием структуры ДНК. Используя Правила Чаргаффа и рентгенограммы Розалинды Франклин и Мориса Уилкинса построили двухспиральную модель. Результаты работы опубликовали в апреле 1953 года в журнале Nature. 25 лет руководил научным институтом Колд Спринг Харбор, где вел исследования генетики рака. С 1989 года по 1992 год — организатор и руководитель проекта «Геном человека» по расшифровке последовательности человеческой ДНК, в это же время возглавляет секретный проект «Фауст» В 2007 году высказался в пользу того, что представители разных рас имеют различные интеллектуальные способности, что обусловлено генетически. В связи с нарушением политкорректности от него потребовали публичных извинений, а в октябре 2007 года Уотсон официально ушел с поста руководителя лаборатории, где он работал. Вместе с тем он продолжает руководить исследованиями в той же лаборатории. По сообщению издания «Индепендент» , исследование ДНК самого Джеймса Уотсона обнаружило высокую концентрацию африканских и, в меньшей мере, азиатских генов. Позже выяснилось, что анализ базировался на ошибочной версии генома. 84 Сейчас работает над поиском генов психических заболеваний.
 • • • Фрэнсис Крик (англ. Francis Crick, 8 июня 1916, Нортгемптон — 28 июля 2004, Сан-Диего, Калифорния) — британский молекулярный биолог, врач и нейробиолог. Лауреат Нобелевской премии по физиологии и медицине 1962 г. — совместно с Джеймсом Д. Уотсоном и Морисом Х. Ф. Уилкинсом с формулировкой «за открытия, касающиеся молекулярной структуры нуклеиновых кислот и их значения для передачи информации в живых системах» . Такжи Крик известен тем, что сформулировал центральную догму молекулярной биологии В статье, опубликованной в журнале Nature в 1961 году, Крик с соавторами предположили четыре свойства генетического кода: три азотистых основания (триплет) кодируют одну аминокислоту триплеты генетического кода не перекрываются последовательности триплетов считываются с определенной начальной точки, знаки препинания внутри кодирующей последовательности отсутствуют генетический код вырожден — одна аминокислота может быть закодирована 85 разными триплетами
• • • Фрэнсис Крик (англ. Francis Crick, 8 июня 1916, Нортгемптон — 28 июля 2004, Сан-Диего, Калифорния) — британский молекулярный биолог, врач и нейробиолог. Лауреат Нобелевской премии по физиологии и медицине 1962 г. — совместно с Джеймсом Д. Уотсоном и Морисом Х. Ф. Уилкинсом с формулировкой «за открытия, касающиеся молекулярной структуры нуклеиновых кислот и их значения для передачи информации в живых системах» . Такжи Крик известен тем, что сформулировал центральную догму молекулярной биологии В статье, опубликованной в журнале Nature в 1961 году, Крик с соавторами предположили четыре свойства генетического кода: три азотистых основания (триплет) кодируют одну аминокислоту триплеты генетического кода не перекрываются последовательности триплетов считываются с определенной начальной точки, знаки препинания внутри кодирующей последовательности отсутствуют генетический код вырожден — одна аминокислота может быть закодирована 85 разными триплетами
 • • Уилкинс (Wilkins) Морис Хью Фредерик (15. 12. 1916, Понгароа, Новая Зеландия), английский биофизик, удостоенный в 1962 Нобелевской премии по физиологии и медицине (совместно с Дж. Уотсоном и Ф. Криком) за открытия в области молекулярной генетики. Вместе с семьёй в возрасте шести лет переехал в Англию. Окончил Кембриджский университет; в 1940 получил степень доктора философии в Бирмингемском университете. Во время Второй мировой войны занимался радарами. В течение двух лет работал в Калифорнийском университете в Беркли в рамках Манхаттанского проекта. С 1946 работал в Кингз-колледже в Лондоне (с 1962 возглавлял отдел молекулярной биологии, с 1970 – профессор биофизики, с 1981 – почётный профессор). Уилкинс известен своими работами по рентгеноструктурному анализу дезоксирибонуклеиновой кислоты (ДНК). Исследуя рассеяние рентгеновских лучей на кристаллах ДНК, он со своими коллегами по Кингзколледжу получил данные, свидетельствующие о том, что молекула ДНК – регулярная структура, имеющая форму спирали. Эти результаты послужили основанием для построения Уотсоном и Криком знаменитой модели ДНК – двойной спирали. Впоследствии Уилкинс Морис Хью Фредерик • Уилкинс исследовал структуру рибонуклеиновых кислот (РНК) – молекул, участвующих в синтезе белков в клетке. Автор ряда работ по биофизике нервной системы. Выдающиеся биологи 86
• • Уилкинс (Wilkins) Морис Хью Фредерик (15. 12. 1916, Понгароа, Новая Зеландия), английский биофизик, удостоенный в 1962 Нобелевской премии по физиологии и медицине (совместно с Дж. Уотсоном и Ф. Криком) за открытия в области молекулярной генетики. Вместе с семьёй в возрасте шести лет переехал в Англию. Окончил Кембриджский университет; в 1940 получил степень доктора философии в Бирмингемском университете. Во время Второй мировой войны занимался радарами. В течение двух лет работал в Калифорнийском университете в Беркли в рамках Манхаттанского проекта. С 1946 работал в Кингз-колледже в Лондоне (с 1962 возглавлял отдел молекулярной биологии, с 1970 – профессор биофизики, с 1981 – почётный профессор). Уилкинс известен своими работами по рентгеноструктурному анализу дезоксирибонуклеиновой кислоты (ДНК). Исследуя рассеяние рентгеновских лучей на кристаллах ДНК, он со своими коллегами по Кингзколледжу получил данные, свидетельствующие о том, что молекула ДНК – регулярная структура, имеющая форму спирали. Эти результаты послужили основанием для построения Уотсоном и Криком знаменитой модели ДНК – двойной спирали. Впоследствии Уилкинс Морис Хью Фредерик • Уилкинс исследовал структуру рибонуклеиновых кислот (РНК) – молекул, участвующих в синтезе белков в клетке. Автор ряда работ по биофизике нервной системы. Выдающиеся биологи 86
 • • Розалинда получала лучшие в мире рентгенограммы ДНК • Розалинд Франклин (англ. Rosalind Franklin) (25 июля 1920 — 16 апреля 1958) — английский биофизик и учёный-рентгенограф, занималась изучением структуры ДНК. Родилась в Лондоне в состоятельной еврейской семье. Окончив школу, поступила в Кембриджский университет, где получила звание кандидата наук по физической химии. После войны переехала в Париж, где занималась исследованиями в области применения рентгеноструктурного анализа. В 1950 году вернулась в Англию для работы в Лондонском университете над исследованием структуры ДНК. Сделанные Розалиндой Франклин снимки отличались особой чёткостью и, по некоторым сведениям, послужили основанием для выводов о структуре ДНК, сделанных и опубликованных впоследствии в журнале «Nature» работавшими в Кавендишской лаборатории Кембриджского университета Джеймсом Уотсоном и Фрэнсисом Криком. За это открытие Уотсон и Крик получили Нобелевскую премию в 1962 году. Розалинды Франклин к тому моменту уже не было в живых. Частый контакт с рентгеновским излучением стал причиной ракового заболевания, от которого она скончалась 16 апреля 1958 года в возрасте 37 лет. В 2002 году вышла книга Брэнды Мэдокс «Розалинд Франклин: забытая леди ДНК» , в которой были освещены ранее неизвестные подробности работы Розалинды Франклин и её причастности к открытию структуры ДНК. 87
• • Розалинда получала лучшие в мире рентгенограммы ДНК • Розалинд Франклин (англ. Rosalind Franklin) (25 июля 1920 — 16 апреля 1958) — английский биофизик и учёный-рентгенограф, занималась изучением структуры ДНК. Родилась в Лондоне в состоятельной еврейской семье. Окончив школу, поступила в Кембриджский университет, где получила звание кандидата наук по физической химии. После войны переехала в Париж, где занималась исследованиями в области применения рентгеноструктурного анализа. В 1950 году вернулась в Англию для работы в Лондонском университете над исследованием структуры ДНК. Сделанные Розалиндой Франклин снимки отличались особой чёткостью и, по некоторым сведениям, послужили основанием для выводов о структуре ДНК, сделанных и опубликованных впоследствии в журнале «Nature» работавшими в Кавендишской лаборатории Кембриджского университета Джеймсом Уотсоном и Фрэнсисом Криком. За это открытие Уотсон и Крик получили Нобелевскую премию в 1962 году. Розалинды Франклин к тому моменту уже не было в живых. Частый контакт с рентгеновским излучением стал причиной ракового заболевания, от которого она скончалась 16 апреля 1958 года в возрасте 37 лет. В 2002 году вышла книга Брэнды Мэдокс «Розалинд Франклин: забытая леди ДНК» , в которой были освещены ранее неизвестные подробности работы Розалинды Франклин и её причастности к открытию структуры ДНК. 87
 • • • Чаргафф Эрвин (Chargaff) (р. 1905 на территории нынешней Украины), американский биохимик. По происхождению австриец. С 1928 в США. Исследовал химический состав и структуру нуклеиновых кислот. Определил количественное соотношение азотистых оснований, входящих в их состав (правило Чаргаффа), установил видовую специфичность ДНК. 1945 год (события в Японии) сильно повлиял на представление Чаргаффа о роли науки. Он понял, что это не новый вид бизнеса, а часть общечеловеческой культуры. Возможно, после этих событий у ученого проснулся талант публициста. Это уже не ученому, а публицисту Ервину Чаргаффу принадлежат слова: "уровень развития государства определяется тремя составляющими: отношением к деревьям отношением к детям отношением к родному языку. " 88
• • • Чаргафф Эрвин (Chargaff) (р. 1905 на территории нынешней Украины), американский биохимик. По происхождению австриец. С 1928 в США. Исследовал химический состав и структуру нуклеиновых кислот. Определил количественное соотношение азотистых оснований, входящих в их состав (правило Чаргаффа), установил видовую специфичность ДНК. 1945 год (события в Японии) сильно повлиял на представление Чаргаффа о роли науки. Он понял, что это не новый вид бизнеса, а часть общечеловеческой культуры. Возможно, после этих событий у ученого проснулся талант публициста. Это уже не ученому, а публицисту Ервину Чаргаффу принадлежат слова: "уровень развития государства определяется тремя составляющими: отношением к деревьям отношением к детям отношением к родному языку. " 88
 89
89


