пара.ppt
- Количество слайдов: 34

 Структура і функції мітохондрій • Гепард, чия здатність до аеробного метаболізму робить його однією із найшвидших тварин
Структура і функції мітохондрій • Гепард, чия здатність до аеробного метаболізму робить його однією із найшвидших тварин
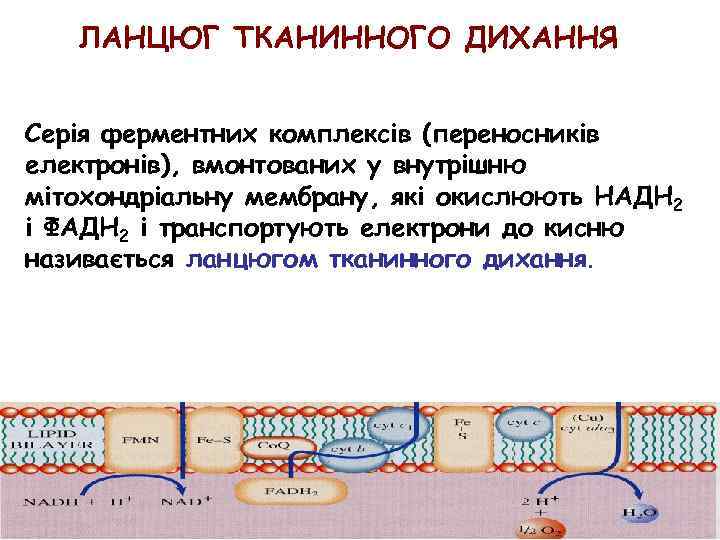 ЛАНЦЮГ ТКАНИННОГО ДИХАННЯ Серія ферментних комплексів (переносників електронів), вмонтованих у внутрішню мітохондріальну мембрану, які окислюють НАДH 2 і ФАДH 2 і транспортують електрони до кисню називається ланцюгом тканинного дихання.
ЛАНЦЮГ ТКАНИННОГО ДИХАННЯ Серія ферментних комплексів (переносників електронів), вмонтованих у внутрішню мітохондріальну мембрану, які окислюють НАДH 2 і ФАДH 2 і транспортують електрони до кисню називається ланцюгом тканинного дихання.
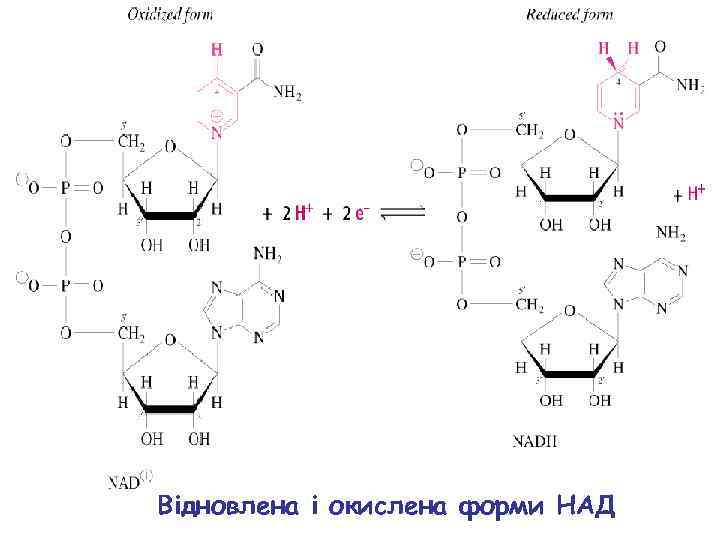 Відновлена і окислена форми НАД
Відновлена і окислена форми НАД
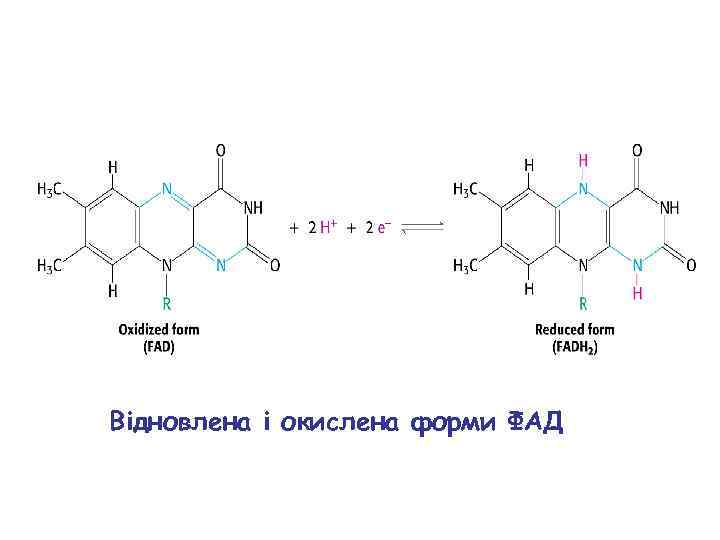 Відновлена і окислена форми ФАД
Відновлена і окислена форми ФАД
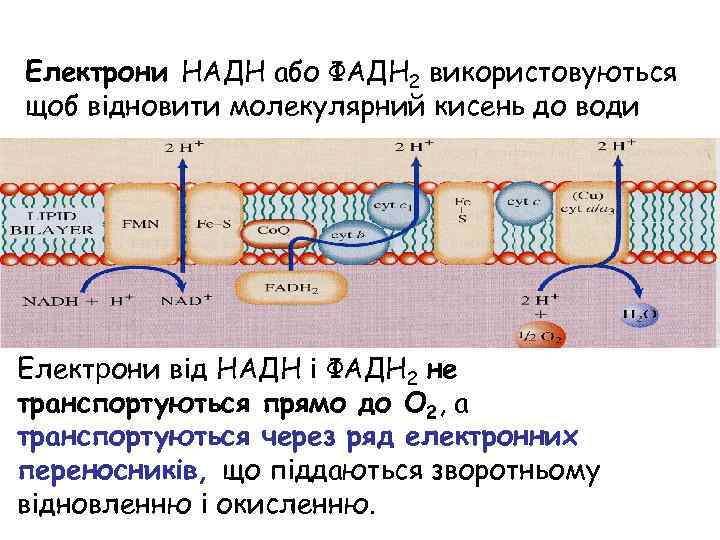 Електрони НАДН або ФАДH 2 використовуються щоб відновити молекулярний кисень до води Електрони від НАДН і ФАДH 2 не транспортуються прямо до O 2, а транспортуються через ряд електронних переносників, що піддаються зворотньому відновленню і окисленню.
Електрони НАДН або ФАДH 2 використовуються щоб відновити молекулярний кисень до води Електрони від НАДН і ФАДH 2 не транспортуються прямо до O 2, а транспортуються через ряд електронних переносників, що піддаються зворотньому відновленню і окисленню.
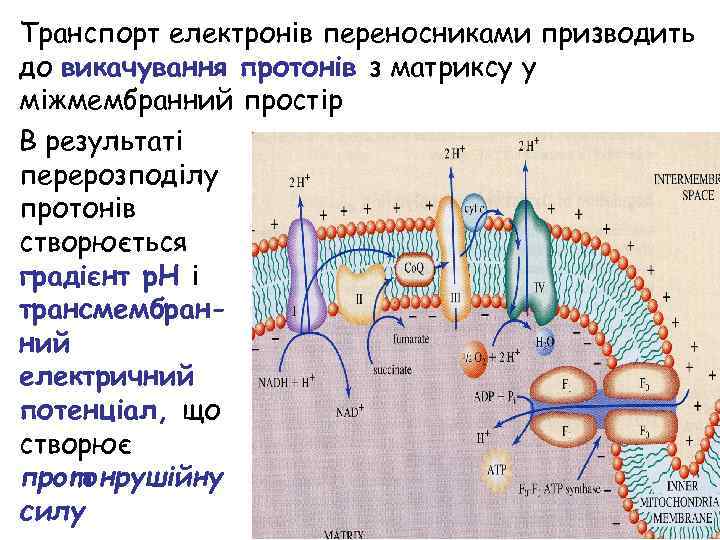 Транспорт електронів переносниками призводить до викачування протонів з матриксу у міжмембранний простір В результаті перерозподілу протонів створюється градієнт p. H і трансмембранний електричний потенціал, що створює протонрушійну силу
Транспорт електронів переносниками призводить до викачування протонів з матриксу у міжмембранний простір В результаті перерозподілу протонів створюється градієнт p. H і трансмембранний електричний потенціал, що створює протонрушійну силу
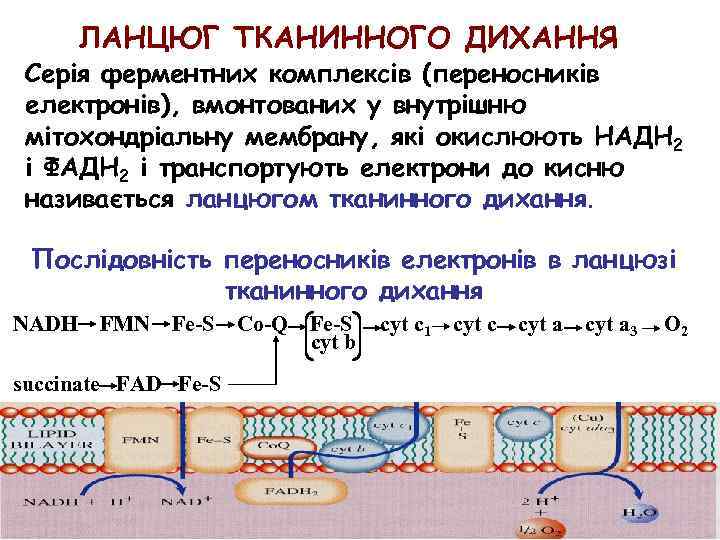 ЛАНЦЮГ ТКАНИННОГО ДИХАННЯ Серія ферментних комплексів (переносників електронів), вмонтованих у внутрішню мітохондріальну мембрану, які окислюють НАДH 2 і ФАДH 2 і транспортують електрони до кисню називається ланцюгом тканинного дихання. Послідовність переносників електронів в ланцюзі тканинного дихання NADH FMN Fe-S succinate FAD Fe-S Co-Q Fe-S cyt b cyt c 1 cyt c cyt a 3 O 2
ЛАНЦЮГ ТКАНИННОГО ДИХАННЯ Серія ферментних комплексів (переносників електронів), вмонтованих у внутрішню мітохондріальну мембрану, які окислюють НАДH 2 і ФАДH 2 і транспортують електрони до кисню називається ланцюгом тканинного дихання. Послідовність переносників електронів в ланцюзі тканинного дихання NADH FMN Fe-S succinate FAD Fe-S Co-Q Fe-S cyt b cyt c 1 cyt c cyt a 3 O 2
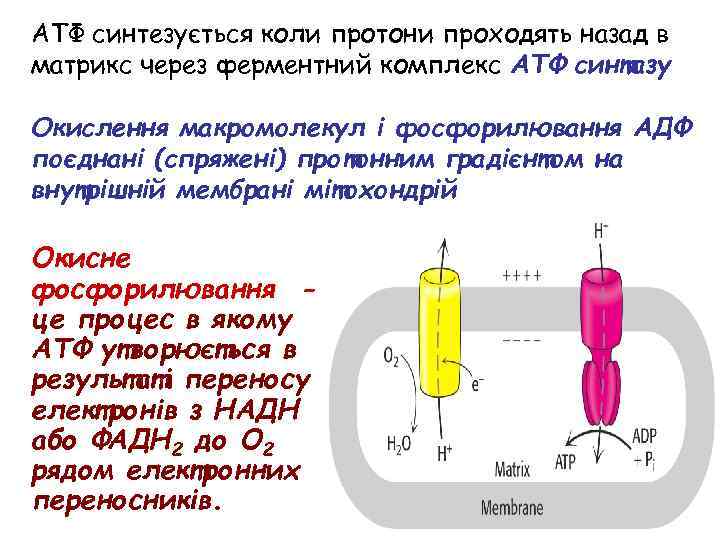 АТФ синтезується коли протони проходять назад в матрикс через ферментний комплекс АТФ синтазу Окислення макромолекул і фосфорилювання АДФ поєднані (спряжені) протонним градієнтом на внутрішній мембрані мітохондрій Окисне фосфорилювання це процес в якому АТФ утворюється в результаті переносу електронів з НАДН або ФАДH 2 до O 2 рядом електронних переносників.
АТФ синтезується коли протони проходять назад в матрикс через ферментний комплекс АТФ синтазу Окислення макромолекул і фосфорилювання АДФ поєднані (спряжені) протонним градієнтом на внутрішній мембрані мітохондрій Окисне фосфорилювання це процес в якому АТФ утворюється в результаті переносу електронів з НАДН або ФАДH 2 до O 2 рядом електронних переносників.
 Високоенергетчні електрони: Редокс потенціали і Зміни вільної енергії При окисному фосфорилюванні електрон трансферний потенціал НАДН або ФАДH 2 перетворюється у фосфорил трансферний потенціал АТФ. Фосфорил трансферний потенціал – це G°' (енергія, що звільняється під час гідролізу фосфатної сполуки). G°' для АТФ = -7. 3 ккал/моль Електрон трансферний потенціал позначається E'o, (також називається редокс потенціал, або окислювально-відновний потенціал).
Високоенергетчні електрони: Редокс потенціали і Зміни вільної енергії При окисному фосфорилюванні електрон трансферний потенціал НАДН або ФАДH 2 перетворюється у фосфорил трансферний потенціал АТФ. Фосфорил трансферний потенціал – це G°' (енергія, що звільняється під час гідролізу фосфатної сполуки). G°' для АТФ = -7. 3 ккал/моль Електрон трансферний потенціал позначається E'o, (також називається редокс потенціал, або окислювально-відновний потенціал).
 E'o (редокс потенціал) це здатність сполуки до відновлення (як легко вона може прийняти електрон). Всі компоненти порівнюються з редокс потенціалом водню, який дорівнює 0. 0 V. Чим більше E'o переносника в ланцюгу тканинного дихання, тим вища його здатність функціонувати як акцептор електронів (окислювальний фактор). Елекрони “течуть” через електрон-транспортний ланцюг спонтанно у напрямку підвищення редокс-потенціалу. E'o НАДН = -0. 32 V (сильний відновлювальний агент) E'o O 2 = +0. 82 V (сильний окислювальний агент) NADH FMN Fe-S Co-Q succinate FAD Fe-S cyt b cyt c 1 cyt c cyt a 3 O 2
E'o (редокс потенціал) це здатність сполуки до відновлення (як легко вона може прийняти електрон). Всі компоненти порівнюються з редокс потенціалом водню, який дорівнює 0. 0 V. Чим більше E'o переносника в ланцюгу тканинного дихання, тим вища його здатність функціонувати як акцептор електронів (окислювальний фактор). Елекрони “течуть” через електрон-транспортний ланцюг спонтанно у напрямку підвищення редокс-потенціалу. E'o НАДН = -0. 32 V (сильний відновлювальний агент) E'o O 2 = +0. 82 V (сильний окислювальний агент) NADH FMN Fe-S Co-Q succinate FAD Fe-S cyt b cyt c 1 cyt c cyt a 3 O 2
 Важлива характеристика електрон-транспортного ланцюга – кількість енергії, що звільняється при проходженні електрона з одного переносника на інший. Ця енергія може бути розрахована за формуою: Go’=-n. F E’o n – число електронів, що транспортується з одного переносника на інший; F – константа Фарадея (23. 06 кал/вольт моль); E’o – різниця редокс-потенціалів між двома переносниками. Коли два електрони проходять з НАДH до O 2 : Go’=-2*96, 5*(+0, 82 -(-0, 32)) = -52. 6 kcal/mol
Важлива характеристика електрон-транспортного ланцюга – кількість енергії, що звільняється при проходженні електрона з одного переносника на інший. Ця енергія може бути розрахована за формуою: Go’=-n. F E’o n – число електронів, що транспортується з одного переносника на інший; F – константа Фарадея (23. 06 кал/вольт моль); E’o – різниця редокс-потенціалів між двома переносниками. Коли два електрони проходять з НАДH до O 2 : Go’=-2*96, 5*(+0, 82 -(-0, 32)) = -52. 6 kcal/mol
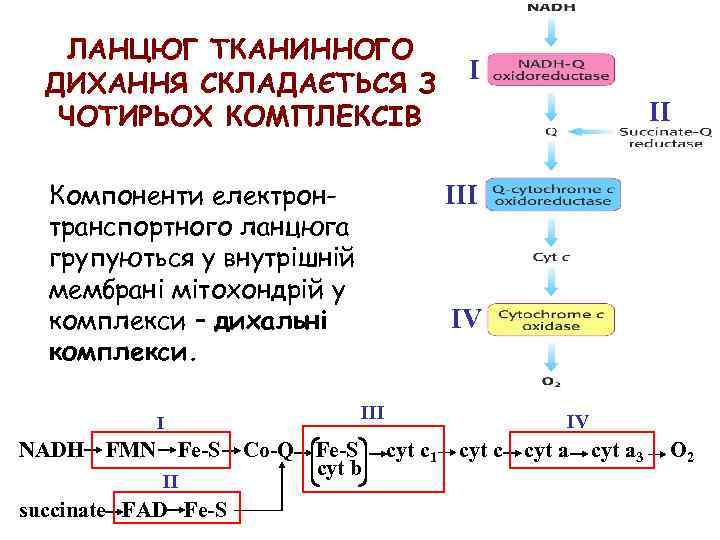 ЛАНЦЮГ ТКАНИННОГО ДИХАННЯ СКЛАДАЄТЬСЯ З ЧОТИРЬОХ КОМПЛЕКСІВ Компоненти електронтранспортного ланцюга групуються у внутрішній мембрані мітохондрій у комплекси – дихальні комплекси. I NADH FMN Fe-S Co-Q II succinate FAD Fe-S I II IV III Fe-S cyt b IV cyt c 1 cyt c cyt a 3 O 2
ЛАНЦЮГ ТКАНИННОГО ДИХАННЯ СКЛАДАЄТЬСЯ З ЧОТИРЬОХ КОМПЛЕКСІВ Компоненти електронтранспортного ланцюга групуються у внутрішній мембрані мітохондрій у комплекси – дихальні комплекси. I NADH FMN Fe-S Co-Q II succinate FAD Fe-S I II IV III Fe-S cyt b IV cyt c 1 cyt c cyt a 3 O 2
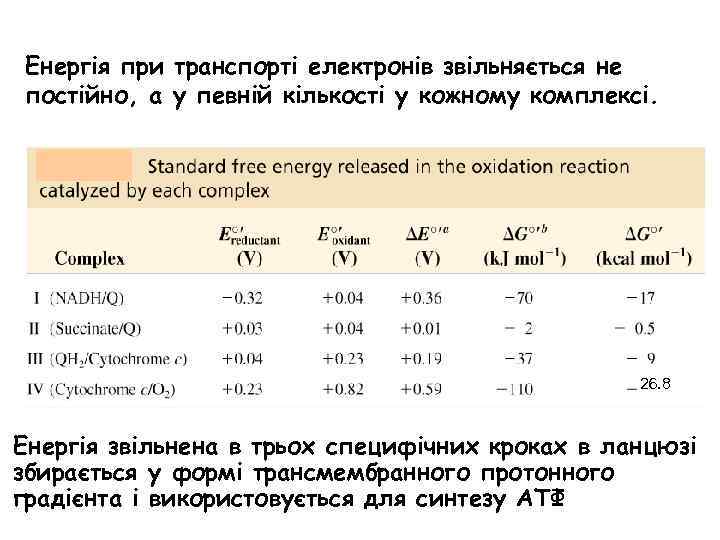 Енергія при транспорті електронів звільняється не постійно, а у певній кількості у кожному комплексі. 26. 8 Енергія звільнена в трьох специфічних кроках в ланцюзі збирається у формі трансмембранного протонного градієнта і використовується для синтезу АТФ
Енергія при транспорті електронів звільняється не постійно, а у певній кількості у кожному комплексі. 26. 8 Енергія звільнена в трьох специфічних кроках в ланцюзі збирається у формі трансмембранного протонного градієнта і використовується для синтезу АТФ
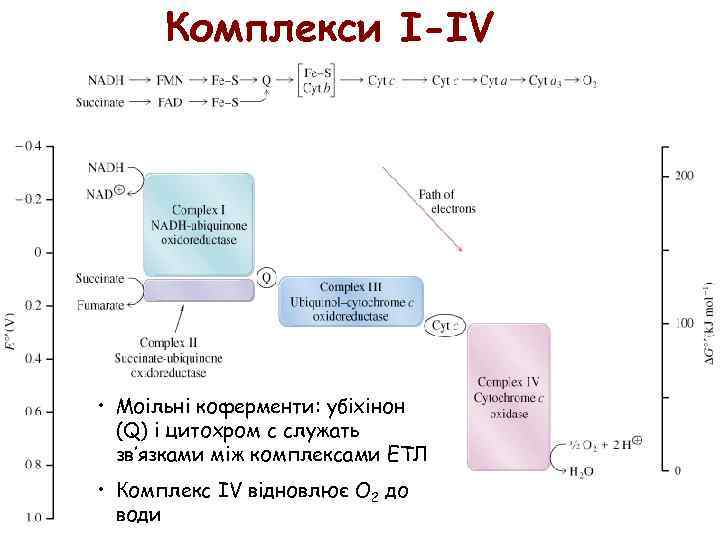 Комплекси I-IV • Моільні коферменти: убіхінон (Q) і цитохром с служать зв’язками між комплексами ЕТЛ • Комплекс IV відновлює O 2 до води
Комплекси I-IV • Моільні коферменти: убіхінон (Q) і цитохром с служать зв’язками між комплексами ЕТЛ • Комплекс IV відновлює O 2 до води
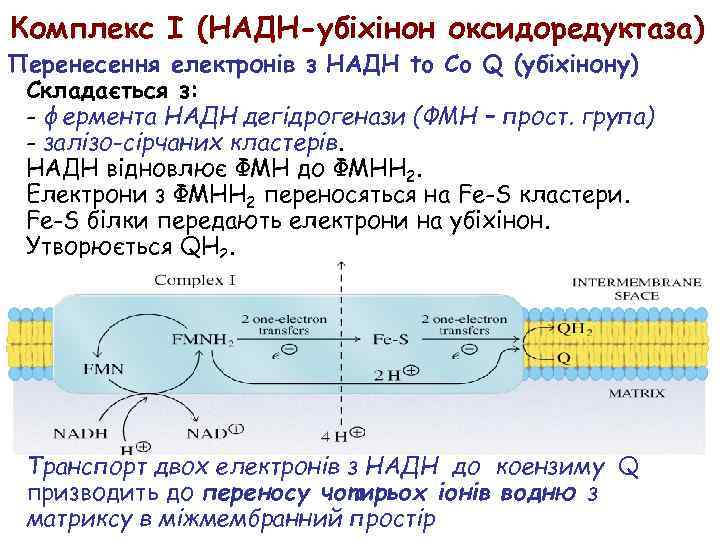 Комплекс I (НАДH-убіхінон оксидоредуктаза) Перенесення електронів з НАДH to Co Q (убіхінону) Складається з: - фермента НАДH дегідрогенази (ФМН – прост. група) - залізо-сірчаних кластерів. НАДH відновлює ФМН до ФМНH 2. Електрони з ФМНH 2 переносяться на Fe-S кластери. Fe-S білки передають електрони на убіхінон. Утворюється QH 2. Транспорт двох електронів з НАДH до коензиму Q призводить до переносу чотирьох іонів водню з матриксу в міжмембранний простір
Комплекс I (НАДH-убіхінон оксидоредуктаза) Перенесення електронів з НАДH to Co Q (убіхінону) Складається з: - фермента НАДH дегідрогенази (ФМН – прост. група) - залізо-сірчаних кластерів. НАДH відновлює ФМН до ФМНH 2. Електрони з ФМНH 2 переносяться на Fe-S кластери. Fe-S білки передають електрони на убіхінон. Утворюється QH 2. Транспорт двох електронів з НАДH до коензиму Q призводить до переносу чотирьох іонів водню з матриксу в міжмембранний простір
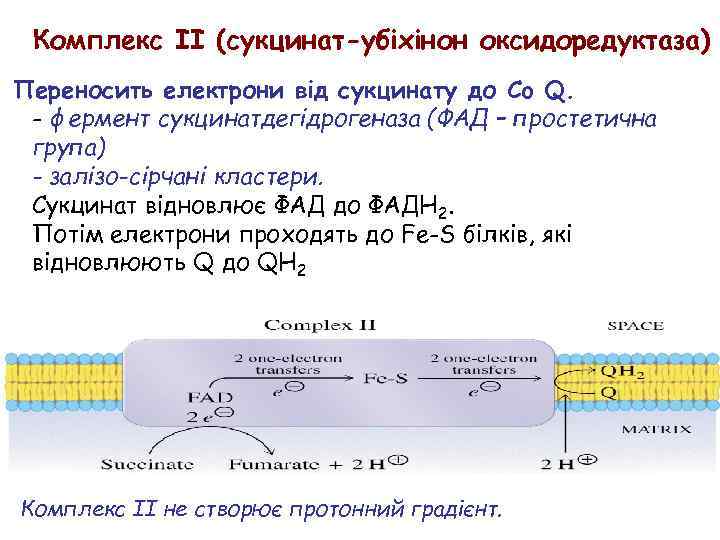 Комплекс II (сукцинат-убіхінон оксидоредуктаза) Переносить електрони від сукцинату до Co Q. - фермент сукцинатдегідрогеназа (ФАД – простетична група) - залізо-сірчані кластери. Сукцинат відновлює ФАД до ФАДH 2. Потім електрони проходять до Fe-S білків, які відновлюють Q до QH 2 Комплекс II не створює протонний градієнт.
Комплекс II (сукцинат-убіхінон оксидоредуктаза) Переносить електрони від сукцинату до Co Q. - фермент сукцинатдегідрогеназа (ФАД – простетична група) - залізо-сірчані кластери. Сукцинат відновлює ФАД до ФАДH 2. Потім електрони проходять до Fe-S білків, які відновлюють Q до QH 2 Комплекс II не створює протонний градієнт.
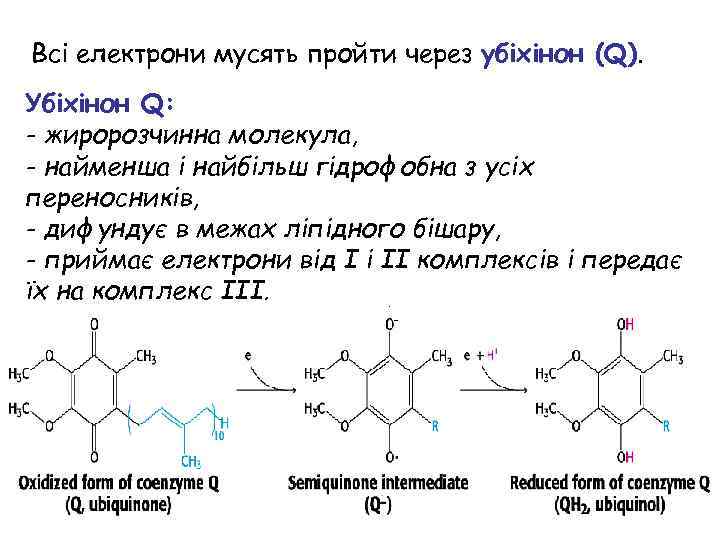 Всі електрони мусять пройти через убіхінон (Q). Убіхінон Q: - жиророзчинна молекула, - найменша і найбільш гідрофобна з усіх переносників, - дифундує в межах ліпідного бішару, - приймає електрони від I і II комплексів і передає їх на комплекс III.
Всі електрони мусять пройти через убіхінон (Q). Убіхінон Q: - жиророзчинна молекула, - найменша і найбільш гідрофобна з усіх переносників, - дифундує в межах ліпідного бішару, - приймає електрони від I і II комплексів і передає їх на комплекс III.
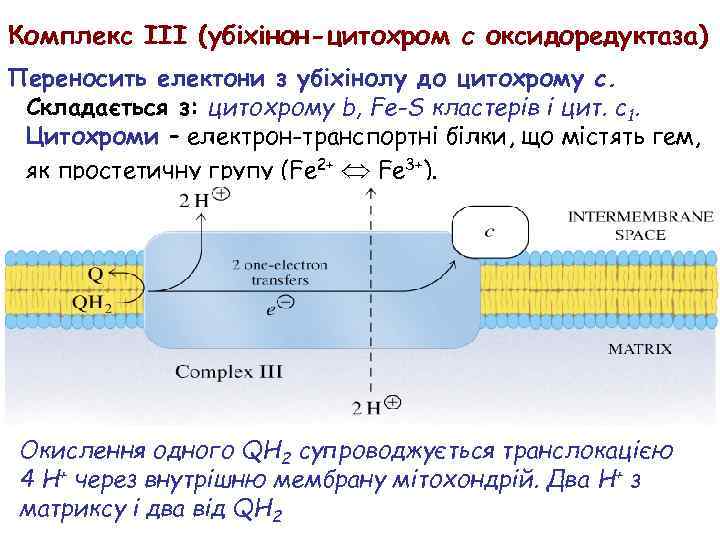 Комплекс III (убіхінон-цитохром c оксидоредуктаза) Переносить електони з убіхінолу до цитохрому c. Складається з: цитохрому b, Fe-S кластерів і цит. c 1. Цитохроми – електрон-транспортні білки, що містять гем, як простетичну групу (Fe 2+ Fe 3+). Окислення одного QH 2 супроводжується транслокацією 4 H+ через внутрішню мембрану мітохондрій. Два H+ з матриксу і два від QH 2
Комплекс III (убіхінон-цитохром c оксидоредуктаза) Переносить електони з убіхінолу до цитохрому c. Складається з: цитохрому b, Fe-S кластерів і цит. c 1. Цитохроми – електрон-транспортні білки, що містять гем, як простетичну групу (Fe 2+ Fe 3+). Окислення одного QH 2 супроводжується транслокацією 4 H+ через внутрішню мембрану мітохондрій. Два H+ з матриксу і два від QH 2
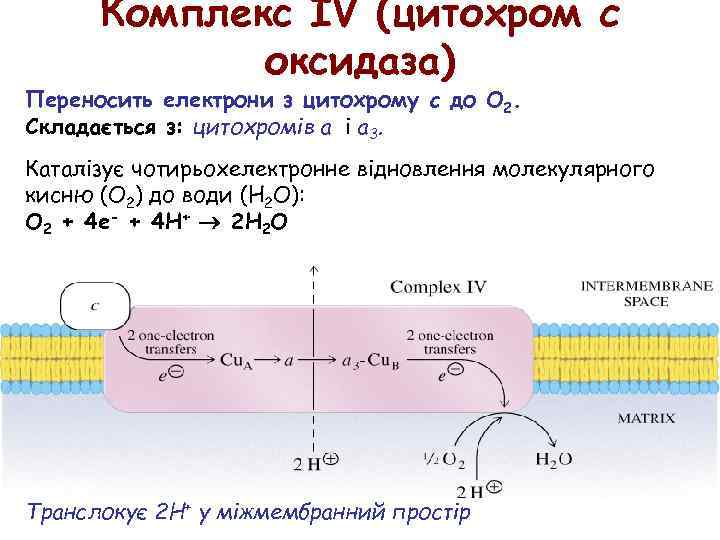 Комплекс IV (цитохром c оксидаза) Переносить електрони з цитохрому c до O 2. Складається з: цитохромів a і a 3. Каталізує чотирьохелектронне відновлення молекулярного кисню (O 2) до води (H 2 O): O 2 + 4 e- + 4 H+ 2 H 2 O Транслокує 2 H+ у міжмембранний простір
Комплекс IV (цитохром c оксидаза) Переносить електрони з цитохрому c до O 2. Складається з: цитохромів a і a 3. Каталізує чотирьохелектронне відновлення молекулярного кисню (O 2) до води (H 2 O): O 2 + 4 e- + 4 H+ 2 H 2 O Транслокує 2 H+ у міжмембранний простір

 Окисне фосфорилювання створює АТФ, що є універсальною формою енергії в живих організмах ОКИСНЕ ФОСФОРИЛЮВАННЯ
Окисне фосфорилювання створює АТФ, що є універсальною формою енергії в живих організмах ОКИСНЕ ФОСФОРИЛЮВАННЯ
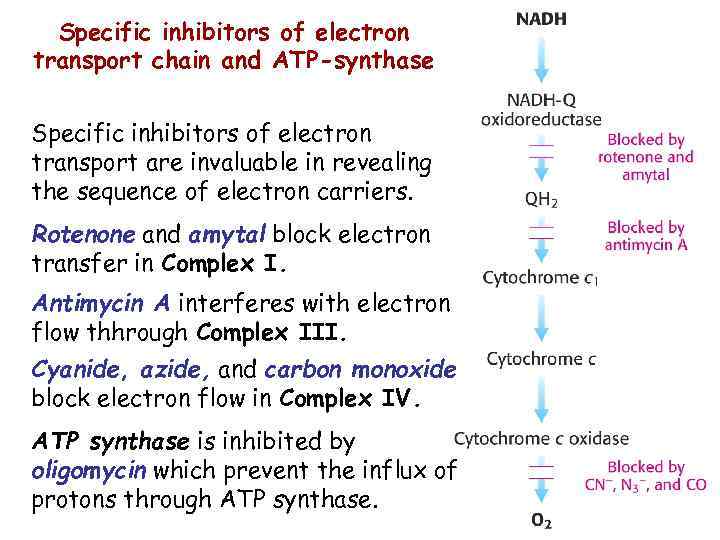 Specific inhibitors of electron transport chain and ATP-synthase Specific inhibitors of electron transport are invaluable in revealing the sequence of electron carriers. Rotenone and amytal block electron transfer in Complex I. Antimycin A interferes with electron flow thhrough Complex III. Cyanide, azide, and carbon monoxide block electron flow in Complex IV. ATP synthase is inhibited by oligomycin which prevent the influx of protons through ATP synthase.
Specific inhibitors of electron transport chain and ATP-synthase Specific inhibitors of electron transport are invaluable in revealing the sequence of electron carriers. Rotenone and amytal block electron transfer in Complex I. Antimycin A interferes with electron flow thhrough Complex III. Cyanide, azide, and carbon monoxide block electron flow in Complex IV. ATP synthase is inhibited by oligomycin which prevent the influx of protons through ATP synthase.
 Хеміосмотична теорія • Запропонована Пітером Мітчелом в 1960 (Нобелівська премія, 1978) • Хеміосмотична теорія: транспорт електронів і синтез АТФ поєднані протонним градієнтом через внутрішню мембрану мітохондрій
Хеміосмотична теорія • Запропонована Пітером Мітчелом в 1960 (Нобелівська премія, 1978) • Хеміосмотична теорія: транспорт електронів і синтез АТФ поєднані протонним градієнтом через внутрішню мембрану мітохондрій
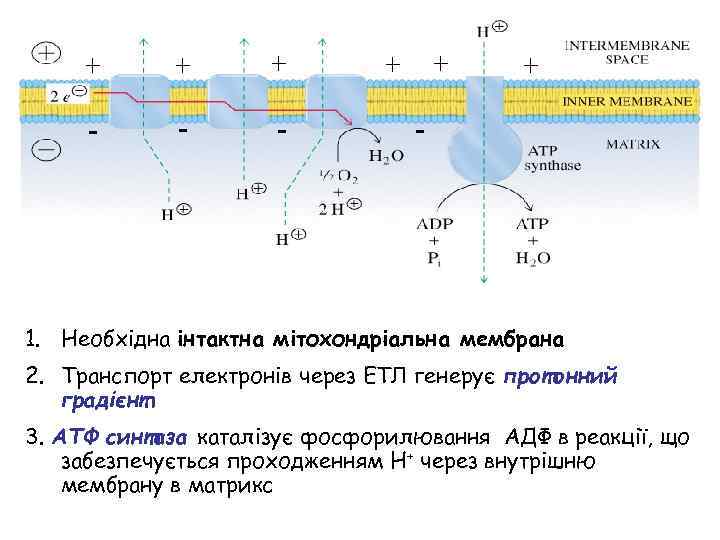 + + + - - - + + + - 1. Необхідна інтактна мітохондріальна мембрана 2. Транспорт електронів через ЕТЛ генерує протонний градієнт 3. AТФ синтаза каталізує фосфорилювання АДФ в реакції, що забезпечується проходженням Н+ через внутрішню мембрану в матрикс
+ + + - - - + + + - 1. Необхідна інтактна мітохондріальна мембрана 2. Транспорт електронів через ЕТЛ генерує протонний градієнт 3. AТФ синтаза каталізує фосфорилювання АДФ в реакції, що забезпечується проходженням Н+ через внутрішню мембрану в матрикс
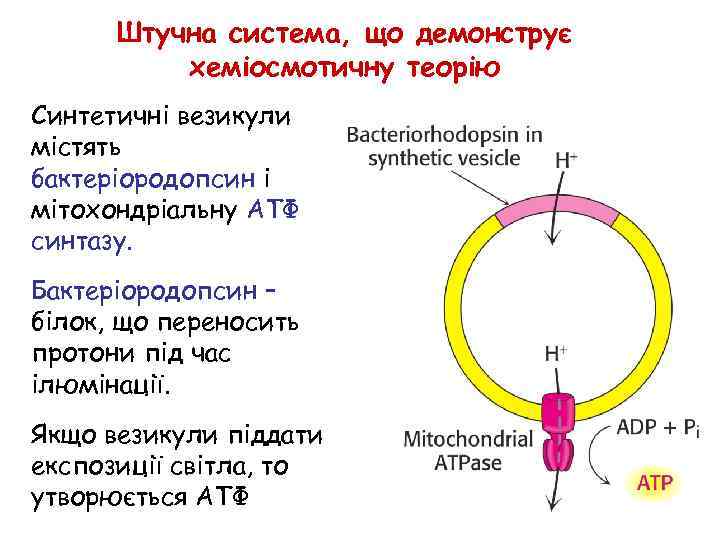 Штучна система, що демонструє хеміосмотичну теорію Синтетичні везикули містять бактеріородопсин і мітохондріальну АТФ синтазу. Бактеріородопсин – білок, що переносить протони під час ілюмінації. Якщо везикули піддати експозиції світла, то утворюється АТФ
Штучна система, що демонструє хеміосмотичну теорію Синтетичні везикули містять бактеріородопсин і мітохондріальну АТФ синтазу. Бактеріородопсин – білок, що переносить протони під час ілюмінації. Якщо везикули піддати експозиції світла, то утворюється АТФ
 АТФ синтаза Дві субодиниці, Fo і F 1 містить каталітичні субодиниці, де АДФ і Pi зв’язуються. F 0 пронизує мембрану і служить як протонний канал. Енергія, що звільняється при “падінні” протонів використовується для синтезу АТФ.
АТФ синтаза Дві субодиниці, Fo і F 1 містить каталітичні субодиниці, де АДФ і Pi зв’язуються. F 0 пронизує мембрану і служить як протонний канал. Енергія, що звільняється при “падінні” протонів використовується для синтезу АТФ.
 РЕГУЛЯЦІЯ ОКИСНОГО ФОСФОРИЛЮВАННЯ Спряження тканинного дихання з окисним фосфорилюванням Транспорт електронів тісно поєднаний з фосфорилюванням. АТФ не може бути синтезовано окисним фосфорилюванням якщо нема енергії звільненої при електронному транспорті. Електрони не проходять через електрон-транспортний ланцюг якщо АДФ не фосфорилюється до АТФ. Важливі регулятори: НАДН, O 2, AДФ Внутрішньомітохондріальне співвідношення АТФ/АДФ є контрольним механізмом Високе співвідношення інгібує так як АТФ аллостерично зв’язується з комлексом IV
РЕГУЛЯЦІЯ ОКИСНОГО ФОСФОРИЛЮВАННЯ Спряження тканинного дихання з окисним фосфорилюванням Транспорт електронів тісно поєднаний з фосфорилюванням. АТФ не може бути синтезовано окисним фосфорилюванням якщо нема енергії звільненої при електронному транспорті. Електрони не проходять через електрон-транспортний ланцюг якщо АДФ не фосфорилюється до АТФ. Важливі регулятори: НАДН, O 2, AДФ Внутрішньомітохондріальне співвідношення АТФ/АДФ є контрольним механізмом Високе співвідношення інгібує так як АТФ аллостерично зв’язується з комлексом IV
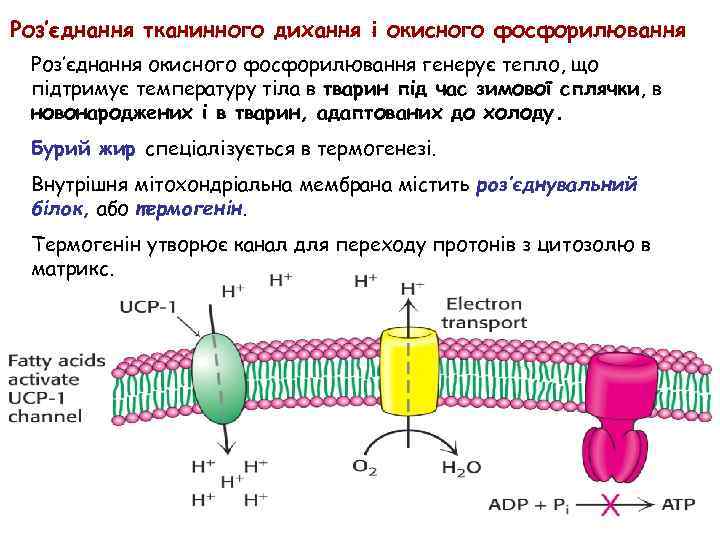 Роз’єднання тканинного дихання і окисного фосфорилювання Роз’єднання окисного фосфорилювання генерує тепло, що підтримує температуру тіла в тварин під час зимової сплячки, в новонароджених і в тварин, адаптованих до холоду. Бурий жир спеціалізується в термогенезі. Внутрішня мітохондріальна мембрана містить роз’єднувальний білок, або термогенін. Термогенін утворює канал для переходу протонів з цитозолю в матрикс.
Роз’єднання тканинного дихання і окисного фосфорилювання Роз’єднання окисного фосфорилювання генерує тепло, що підтримує температуру тіла в тварин під час зимової сплячки, в новонароджених і в тварин, адаптованих до холоду. Бурий жир спеціалізується в термогенезі. Внутрішня мітохондріальна мембрана містить роз’єднувальний білок, або термогенін. Термогенін утворює канал для переходу протонів з цитозолю в матрикс.
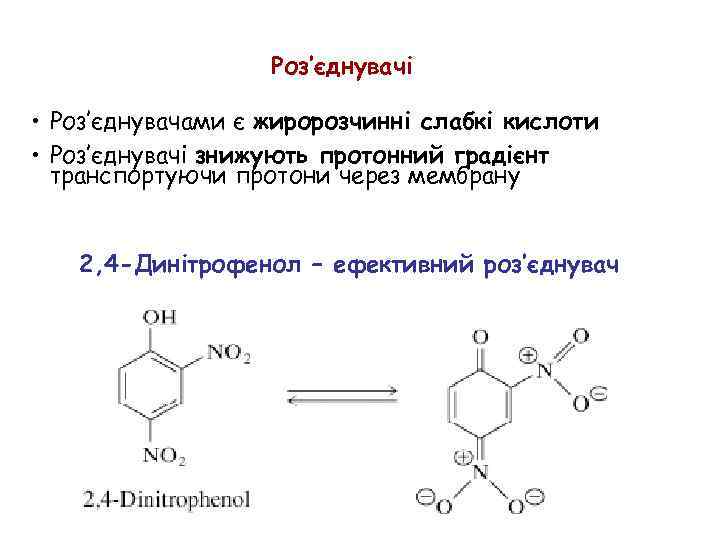 Роз’єднувачі • Роз’єднувачами є жиророзчинні слабкі кислоти • Роз’єднувачі знижують протонний градієнт транспортуючи протони через мембрану 2, 4 -Динітрофенол – ефективний роз’єднувач
Роз’єднувачі • Роз’єднувачами є жиророзчинні слабкі кислоти • Роз’єднувачі знижують протонний градієнт транспортуючи протони через мембрану 2, 4 -Динітрофенол – ефективний роз’єднувач

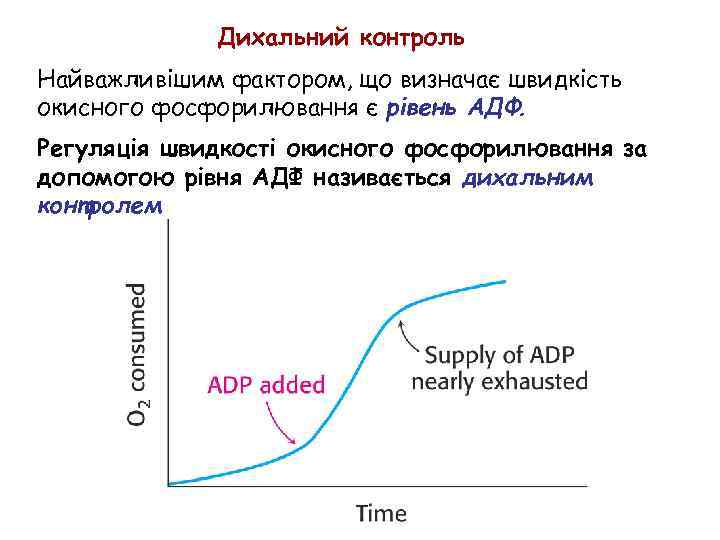 Дихальний контроль Найважливішим фактором, що визначає швидкість окисного фосфорилювання є рівень АДФ. Регуляція швидкості окисного фосфорилювання за допомогою рівня АДФ називається дихальним контролем
Дихальний контроль Найважливішим фактором, що визначає швидкість окисного фосфорилювання є рівень АДФ. Регуляція швидкості окисного фосфорилювання за допомогою рівня АДФ називається дихальним контролем
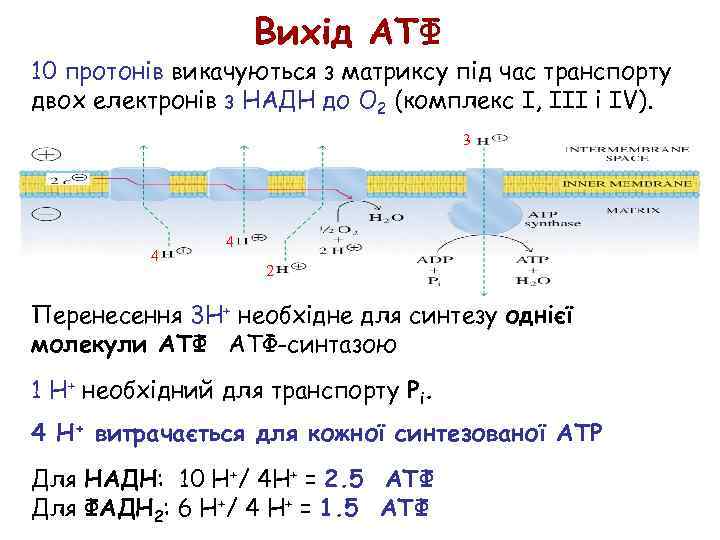 Вихід АТФ 10 протонів викачуються з матриксу під час транспорту двох електронів з НАДН до O 2 (комплекс I, III і IV). 3 Six protons are pumped out of the matrix during the two electrons flowing from FADH 2 to O 2 (Complex III and IV). 4 4 2 Перенесення 3 H+ необхідне для синтезу однієї молекули АТФ-синтазою 1 H+ необхідний для транспорту Pi. 4 H+ витрачається для кожної синтезованої АTP Для НАДН: 10 H+/ 4 H+ = 2. 5 АТФ Для ФАДН 2: 6 H+/ 4 H+ = 1. 5 ATФ
Вихід АТФ 10 протонів викачуються з матриксу під час транспорту двох електронів з НАДН до O 2 (комплекс I, III і IV). 3 Six protons are pumped out of the matrix during the two electrons flowing from FADH 2 to O 2 (Complex III and IV). 4 4 2 Перенесення 3 H+ необхідне для синтезу однієї молекули АТФ-синтазою 1 H+ необхідний для транспорту Pi. 4 H+ витрачається для кожної синтезованої АTP Для НАДН: 10 H+/ 4 H+ = 2. 5 АТФ Для ФАДН 2: 6 H+/ 4 H+ = 1. 5 ATФ
 Дякую за увагу…=)
Дякую за увагу…=)


