Л 2 Структура.pptx
- Количество слайдов: 32
 СТРУКТУРА ФЕРМЕНТОВ
СТРУКТУРА ФЕРМЕНТОВ
 Ферменты делятся на простые и сложные. Простые ферменты – однокомпонентные, состоят только из полипептидной (аминокислотной) части.
Ферменты делятся на простые и сложные. Простые ферменты – однокомпонентные, состоят только из полипептидной (аминокислотной) части.
 Сложные ферменты – двухкомпонентные, кроме полипептида (апофермента) содержат дополнительный компонент небелковой природы (кофактор). Апофермент + Кофактор = Холофермент
Сложные ферменты – двухкомпонентные, кроме полипептида (апофермента) содержат дополнительный компонент небелковой природы (кофактор). Апофермент + Кофактор = Холофермент
 Кофакторы: ØКоферменты – растворимые кофакторы, связаны с апоферментом нековалентными взаимодействиям; имеют высокую Кд с апобелком. ØПростетические группы – нерастворимые кофакторы, связаны с апоферментом ковалентными связями; имеют низкую Кд с апобелком.
Кофакторы: ØКоферменты – растворимые кофакторы, связаны с апоферментом нековалентными взаимодействиям; имеют высокую Кд с апобелком. ØПростетические группы – нерастворимые кофакторы, связаны с апоферментом ковалентными связями; имеют низкую Кд с апобелком.
 Функции кофакторов: Ø Кофакторы - промежуточные переносчики атомов или функциональных групп. Ø Кофакторы принимают участие в формировании активных центров сложных ферментов.
Функции кофакторов: Ø Кофакторы - промежуточные переносчики атомов или функциональных групп. Ø Кофакторы принимают участие в формировании активных центров сложных ферментов.
 Кофакторы каталитически неактивны (без апофермента). Кофакторы не проявляют специфичность (ни в отношении апофермента, ни в отношении субстратов).
Кофакторы каталитически неактивны (без апофермента). Кофакторы не проявляют специфичность (ни в отношении апофермента, ни в отношении субстратов).
 Классификация кофакторов Кофакторы – производные органических соединений: Ø Кофакторы алифатического ряда (например, глутатион); Ø Кофакторы ароматического ряда (например, убихинон); Ø Кофакторы гетроциклического ряда (например, пиридоксальфосфат).
Классификация кофакторов Кофакторы – производные органических соединений: Ø Кофакторы алифатического ряда (например, глутатион); Ø Кофакторы ароматического ряда (например, убихинон); Ø Кофакторы гетроциклического ряда (например, пиридоксальфосфат).
 В зависимости от выполняемых функций (типа катализируемой реакции): Ø Кофакторы, участвующие в катализе окислительно-восстановительных реакций (например, ФАД, ФМН, липоевая кислота, гем, глутатион, убихинон).
В зависимости от выполняемых функций (типа катализируемой реакции): Ø Кофакторы, участвующие в катализе окислительно-восстановительных реакций (например, ФАД, ФМН, липоевая кислота, гем, глутатион, убихинон).
 Ø Кофакторы, участвующие в катализе реакций переноса атомов и функциональных групп (например, нуклеозидди- и нуклеозидтрифосфаты, кофермент А, тетрагидрофолиевая кислота, пиридоксальфосфат).
Ø Кофакторы, участвующие в катализе реакций переноса атомов и функциональных групп (например, нуклеозидди- и нуклеозидтрифосфаты, кофермент А, тетрагидрофолиевая кислота, пиридоксальфосфат).
 Ø Кофакторы, участвующие в катализе реакций синтеза и изомеризации (например, тиаминпирофосфат, биотин, глутатион, пиридоксальфосфат).
Ø Кофакторы, участвующие в катализе реакций синтеза и изомеризации (например, тиаминпирофосфат, биотин, глутатион, пиридоксальфосфат).
 Большинство органических кофакторов являются производными водорастворимых витаминов.
Большинство органических кофакторов являются производными водорастворимых витаминов.
 Кофактор Тиаминпирофосфат (ТПФ) Флавинмононуклеотид (ФМН) Флавинадениндинуклеотид (ФАД) Никотинамиддинуклеотид (НАД+) Никотинамиддинуклеотидфосфат (НАДФ+) Пиридоксальфосфат Коэнзим А Биоцитин Витамин Тиамин (В 1) Тип катализируемой реакции Декарбоксилирование -кетокислот Рибофлавин Окислительно(В 2) восстановительные реакции Никотинамид Окислительно(В 5, или РР) восстановительные реакции Пиридоксин (В 6) Пантотеновая кислота (В 3) Биотин (Н) Перенос аминогрупп Перенос групп ацильных Карбоксилирование/ декарбоксилирование
Кофактор Тиаминпирофосфат (ТПФ) Флавинмононуклеотид (ФМН) Флавинадениндинуклеотид (ФАД) Никотинамиддинуклеотид (НАД+) Никотинамиддинуклеотидфосфат (НАДФ+) Пиридоксальфосфат Коэнзим А Биоцитин Витамин Тиамин (В 1) Тип катализируемой реакции Декарбоксилирование -кетокислот Рибофлавин Окислительно(В 2) восстановительные реакции Никотинамид Окислительно(В 5, или РР) восстановительные реакции Пиридоксин (В 6) Пантотеновая кислота (В 3) Биотин (Н) Перенос аминогрупп Перенос групп ацильных Карбоксилирование/ декарбоксилирование
 МЕТАЛЛОЗАВИСИМЫЕ ФЕРМЕНТЫ Функции металлов в сложных ферментах: участие в катализе. Металл находится в зоне активного центра (в каталитическом участке). Например: тирозиназа (2 Cu 2+), моноаминооксидаза (4 Cu 2+), церулоплазмин (8 Cu 2+). стабилизация структуры апофермента. Металл находится вне зоны активного центра (вне каталитической зоны). Например: транскетолаза (Cа 2+).
МЕТАЛЛОЗАВИСИМЫЕ ФЕРМЕНТЫ Функции металлов в сложных ферментах: участие в катализе. Металл находится в зоне активного центра (в каталитическом участке). Например: тирозиназа (2 Cu 2+), моноаминооксидаза (4 Cu 2+), церулоплазмин (8 Cu 2+). стабилизация структуры апофермента. Металл находится вне зоны активного центра (вне каталитической зоны). Например: транскетолаза (Cа 2+).
 связывание субстрата. Металл располагается в зоне активного центра (в субстратсвязывающем участке). Например: гексокиназа (Mg 2+). связывание субстрата и катализ. Металл находится в зоне активного центра. Например: пируваткиназа (Мg 2+, K+), аргиназа (Мn 2+), щелочная фосфатаза (2 Zn 2+).
связывание субстрата. Металл располагается в зоне активного центра (в субстратсвязывающем участке). Например: гексокиназа (Mg 2+). связывание субстрата и катализ. Металл находится в зоне активного центра. Например: пируваткиназа (Мg 2+, K+), аргиназа (Мn 2+), щелочная фосфатаза (2 Zn 2+).
 Многие сложные ферменты могут содержать и органические, и неорганические (металлы) кофакторы. Например, Zn 2+-содержащая НАД+зависимая алкогольдегидрогеназа.
Многие сложные ферменты могут содержать и органические, и неорганические (металлы) кофакторы. Например, Zn 2+-содержащая НАД+зависимая алкогольдегидрогеназа.
 СТРУКТУРНАЯ ОРГАНИЗАЦИЯ АПОФЕРМЕНТА Апофермент (полипептидная часть) имеет как минимум третичный уровень организации, т. е. имеет пространственную структуру, или конформацию.
СТРУКТУРНАЯ ОРГАНИЗАЦИЯ АПОФЕРМЕНТА Апофермент (полипептидная часть) имеет как минимум третичный уровень организации, т. е. имеет пространственную структуру, или конформацию.
 В пределах одной полипептидной цепи – апофермента – могут быть сформированы участки с различной вторичной структурой: α-спирали и β-структуры. .
В пределах одной полипептидной цепи – апофермента – могут быть сформированы участки с различной вторичной структурой: α-спирали и β-структуры. .
 Цитохром с – только α-спирализованные структуры; химотрипсин – два домена, сформированные только β-структурами; карбангидраза человека – β-складчатая структура, образованная 10 антипараллельных участками. ; лактатдегидрогеназа – упорядоченные βструктуры располагаются в центре молекулы, а α-спиральные участки различной длины на поверхности.
Цитохром с – только α-спирализованные структуры; химотрипсин – два домена, сформированные только β-структурами; карбангидраза человека – β-складчатая структура, образованная 10 антипараллельных участками. ; лактатдегидрогеназа – упорядоченные βструктуры располагаются в центре молекулы, а α-спиральные участки различной длины на поверхности.
 Конформация – третичная структура белка – пространственная организация полипептидной цепи.
Конформация – третичная структура белка – пространственная организация полипептидной цепи.
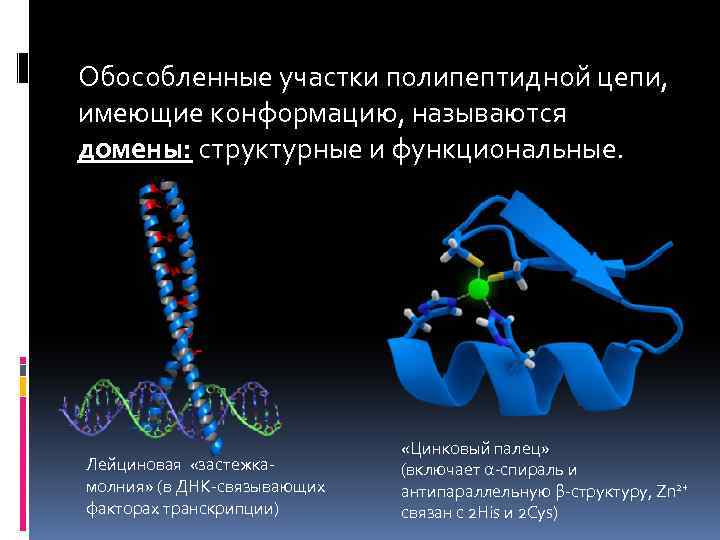 Обособленные участки полипептидной цепи, имеющие конформацию, называются домены: структурные и функциональные. Лейциновая «застежкамолния» (в ДНК-связывающих факторах транскрипции) «Цинковый палец» (включает α-спираль и антипараллельную β-структуру, Zn 2+ связан с 2 His и 2 Cys)
Обособленные участки полипептидной цепи, имеющие конформацию, называются домены: структурные и функциональные. Лейциновая «застежкамолния» (в ДНК-связывающих факторах транскрипции) «Цинковый палец» (включает α-спираль и антипараллельную β-структуру, Zn 2+ связан с 2 His и 2 Cys)
 Неполярные аминокислотные остатки в белковой глобуле формируют одно или несколько гидрофобных ядер, которое окружено оболочкой из полярных аминокислот.
Неполярные аминокислотные остатки в белковой глобуле формируют одно или несколько гидрофобных ядер, которое окружено оболочкой из полярных аминокислот.
 На гидрофильной поверхности молекулы белка, часто имеются гидрофобные участки ( «пятна» ), которые играют важную роль при связывании лигандов (кофакторов, субстратов, активаторов и ингибиторов) и во взаимодействии с другими белковыми молекулами.
На гидрофильной поверхности молекулы белка, часто имеются гидрофобные участки ( «пятна» ), которые играют важную роль при связывании лигандов (кофакторов, субстратов, активаторов и ингибиторов) и во взаимодействии с другими белковыми молекулами.
 Четвертичная структура – пространственная организация нескольких полипептидных цепей. Это не обязательный уровень организации белковой молекулы.
Четвертичная структура – пространственная организация нескольких полипептидных цепей. Это не обязательный уровень организации белковой молекулы.
 Функции четвертичной структуры: объединение нескольких взаимосвязанных функций в одной структуре (каталитическая и регуляторная); участие субъединиц в формировании функциональных зон (активного центра); обеспечение взаимодействия с протяженными структурами (наличие нескольких зон связывания); регуляторная функция (ассоциация/диссоциация субъединиц)
Функции четвертичной структуры: объединение нескольких взаимосвязанных функций в одной структуре (каталитическая и регуляторная); участие субъединиц в формировании функциональных зон (активного центра); обеспечение взаимодействия с протяженными структурами (наличие нескольких зон связывания); регуляторная функция (ассоциация/диссоциация субъединиц)
 СТРУКТУРА АКТИВНОГО ЦЕНТРА Область фермента, в которой происходит связывание и превращение субстрата, называется активным центром.
СТРУКТУРА АКТИВНОГО ЦЕНТРА Область фермента, в которой происходит связывание и превращение субстрата, называется активным центром.
 Активный центр формируется при сворачивании полипептида в глобулярную структуру. Активный центр фермента (по Малеру и Кордесу). Темные полосы - участки полипептидной цепи фермента; R - аминокислотные остатки и их порядковые номера.
Активный центр формируется при сворачивании полипептида в глобулярную структуру. Активный центр фермента (по Малеру и Кордесу). Темные полосы - участки полипептидной цепи фермента; R - аминокислотные остатки и их порядковые номера.
 Происходит сближение функциональных групп аминокислотных остатков: имидазольная группа гистидина, ОН-группа серина или тирозина, SH-группа цистеина, ε-аминогруппа лизина, COOH-группы аспарагиновой и глутаминовой кислот и др.
Происходит сближение функциональных групп аминокислотных остатков: имидазольная группа гистидина, ОН-группа серина или тирозина, SH-группа цистеина, ε-аминогруппа лизина, COOH-группы аспарагиновой и глутаминовой кислот и др.
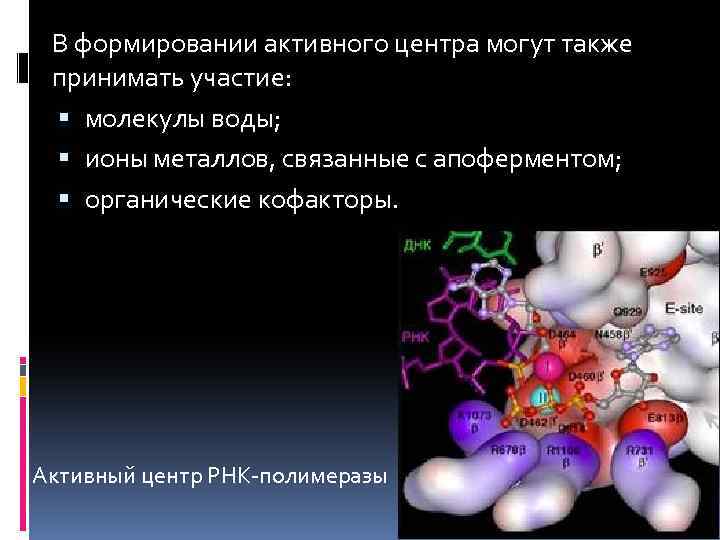 В формировании активного центра могут также принимать участие: молекулы воды; ионы металлов, связанные с апоферментом; органические кофакторы. Активный центр РНК-полимеразы
В формировании активного центра могут также принимать участие: молекулы воды; ионы металлов, связанные с апоферментом; органические кофакторы. Активный центр РНК-полимеразы
 Активный центр помещается в углублениях на поверхности белка. Микросреда активного центра отличается: более низкой диэлектрической проницаемостью (присущей органическим растворителям) по сравнению с водой; пониженной полярностью по сравнению с водой; повышенной микровязкостью.
Активный центр помещается в углублениях на поверхности белка. Микросреда активного центра отличается: более низкой диэлектрической проницаемостью (присущей органическим растворителям) по сравнению с водой; пониженной полярностью по сравнению с водой; повышенной микровязкостью.
 Структурные особенности активного центра позволяют эффективно сорбировать субстрат (многоточечно связывать) и связывать взаимодействовать с ним функциональным группам фермента.
Структурные особенности активного центра позволяют эффективно сорбировать субстрат (многоточечно связывать) и связывать взаимодействовать с ним функциональным группам фермента.
 В активном центре различают две зоны: центр связывания субстрата, каталитический центр.
В активном центре различают две зоны: центр связывания субстрата, каталитический центр.
 У многих ферментов имеется дополнительный регуляторный центр (аллостерический, «аллос» - другой). другой С аллостерическим центром фермента взаимодействуют вещества, влияющие на его каталитическую активность.
У многих ферментов имеется дополнительный регуляторный центр (аллостерический, «аллос» - другой). другой С аллостерическим центром фермента взаимодействуют вещества, влияющие на его каталитическую активность.


