lecture_11.ppt
- Количество слайдов: 51
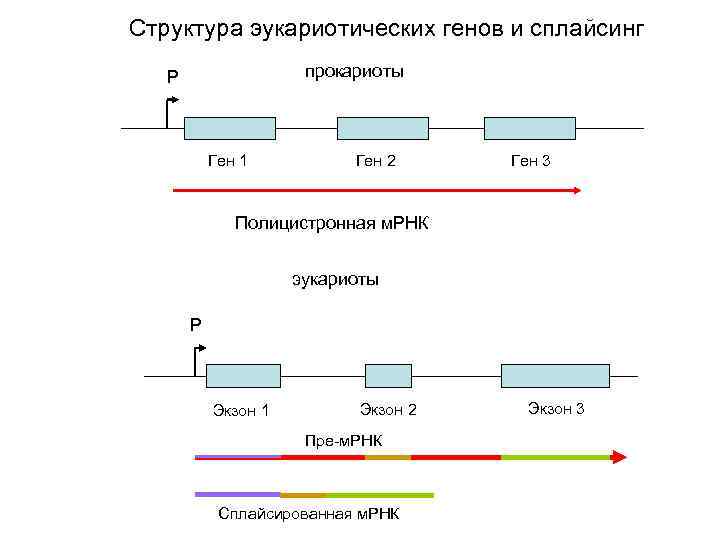 Структура эукариотических генов и сплайсинг прокариоты Р Ген 1 Ген 2 Ген 3 Полицистронная м. РНК эукариоты Р Экзон 1 Экзон 2 Пре-м. РНК Сплайсированная м. РНК Экзон 3
Структура эукариотических генов и сплайсинг прокариоты Р Ген 1 Ген 2 Ген 3 Полицистронная м. РНК эукариоты Р Экзон 1 Экзон 2 Пре-м. РНК Сплайсированная м. РНК Экзон 3
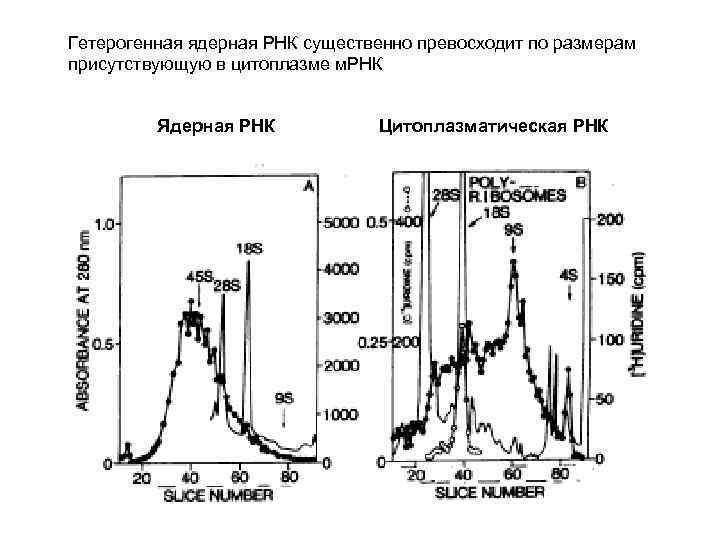 Гетерогенная ядерная РНК существенно превосходит по размерам присутствующую в цитоплазме м. РНК Ядерная РНК Цитоплазматическая РНК
Гетерогенная ядерная РНК существенно превосходит по размерам присутствующую в цитоплазме м. РНК Ядерная РНК Цитоплазматическая РНК
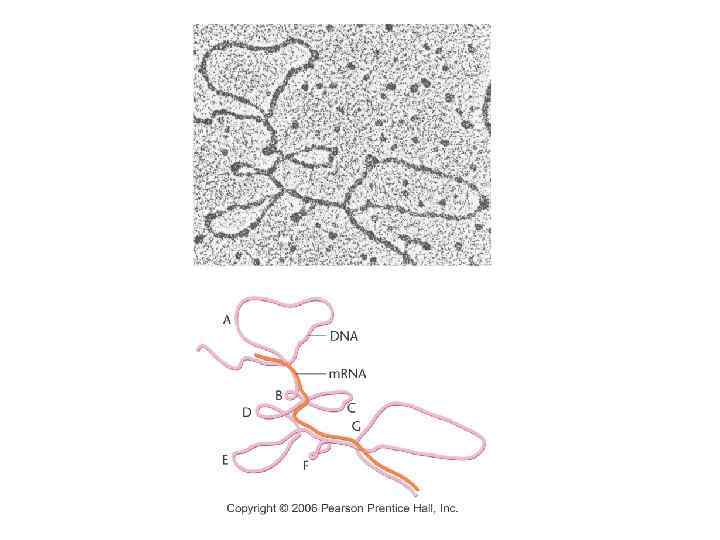
 Открытие сплайсинга (1977) • P. Sharp and R. Roberts - 1993 Нобелевская Премия по физиологии и медицине • Экспериментальный подход - R-loop Analysis – Клонированные гены (глобиновые гены, овальбуминовые гены, некоторые аденовирусные гены) гибридизовали с препаратами РНК в условиях, когда РНК вытесняет идентичную цепь ДНК, и анализировали под электронным микроскопом
Открытие сплайсинга (1977) • P. Sharp and R. Roberts - 1993 Нобелевская Премия по физиологии и медицине • Экспериментальный подход - R-loop Analysis – Клонированные гены (глобиновые гены, овальбуминовые гены, некоторые аденовирусные гены) гибридизовали с препаратами РНК в условиях, когда РНК вытесняет идентичную цепь ДНК, и анализировали под электронным микроскопом
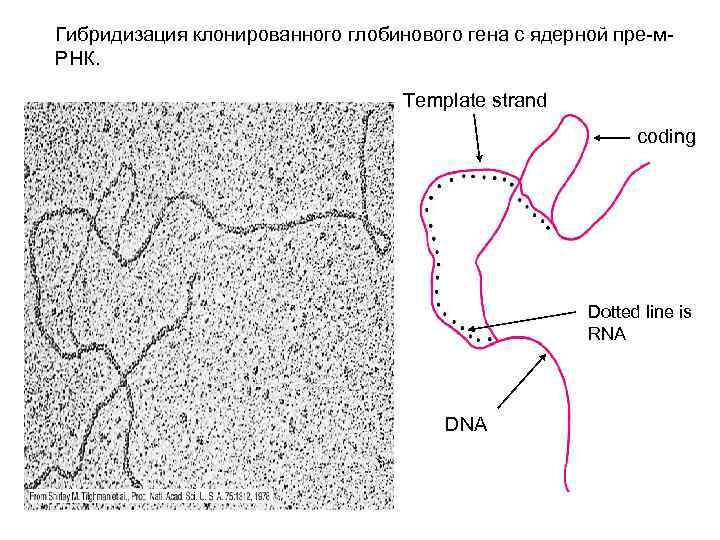 Гибридизация клонированного глобинового гена с ядерной пре-м. РНК. Template strand coding Dotted line is RNA DNA
Гибридизация клонированного глобинового гена с ядерной пре-м. РНК. Template strand coding Dotted line is RNA DNA
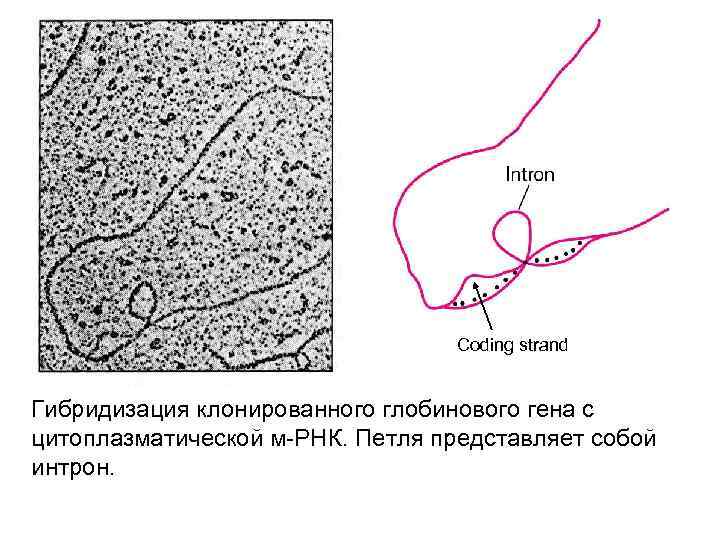 Coding strand Гибридизация клонированного глобинового гена с цитоплазматической м-РНК. Петля представляет собой интрон.
Coding strand Гибридизация клонированного глобинового гена с цитоплазматической м-РНК. Петля представляет собой интрон.
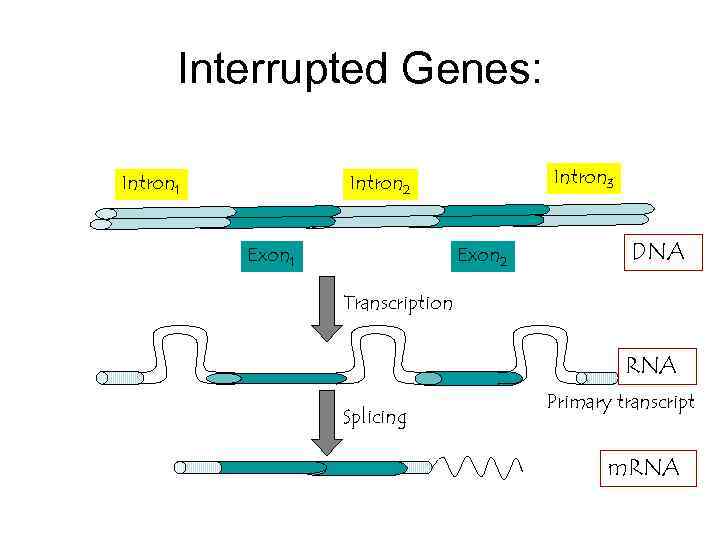 Interrupted Genes: Intron 1 Intron 3 Intron 2 Exon 1 Exon 2 DNA Transcription RNA Splicing Primary transcript m. RNA
Interrupted Genes: Intron 1 Intron 3 Intron 2 Exon 1 Exon 2 DNA Transcription RNA Splicing Primary transcript m. RNA
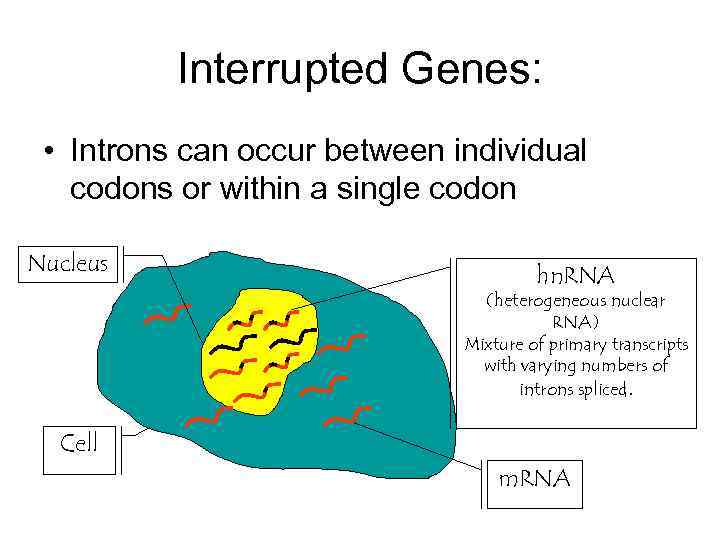 Interrupted Genes: • Introns can occur between individual codons or within a single codon Nucleus hn. RNA (heterogeneous nuclear RNA) Mixture of primary transcripts with varying numbers of introns spliced. Cell m. RNA
Interrupted Genes: • Introns can occur between individual codons or within a single codon Nucleus hn. RNA (heterogeneous nuclear RNA) Mixture of primary transcripts with varying numbers of introns spliced. Cell m. RNA
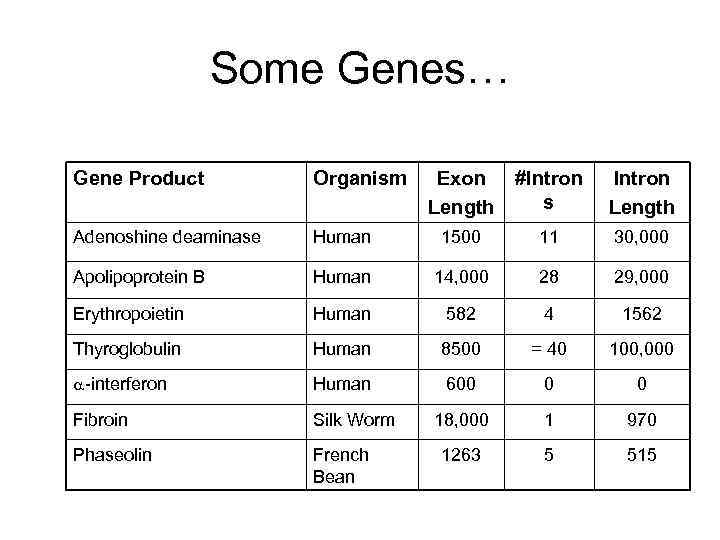 Some Genes… Gene Product Organism Exon Length #Intron s Intron Length Adenoshine deaminase Human 1500 11 30, 000 Apolipoprotein B Human 14, 000 28 29, 000 Erythropoietin Human 582 4 1562 Thyroglobulin Human 8500 = 40 100, 000 -interferon Human 600 0 0 Fibroin Silk Worm 18, 000 1 970 Phaseolin French Bean 1263 5 515
Some Genes… Gene Product Organism Exon Length #Intron s Intron Length Adenoshine deaminase Human 1500 11 30, 000 Apolipoprotein B Human 14, 000 28 29, 000 Erythropoietin Human 582 4 1562 Thyroglobulin Human 8500 = 40 100, 000 -interferon Human 600 0 0 Fibroin Silk Worm 18, 000 1 970 Phaseolin French Bean 1263 5 515
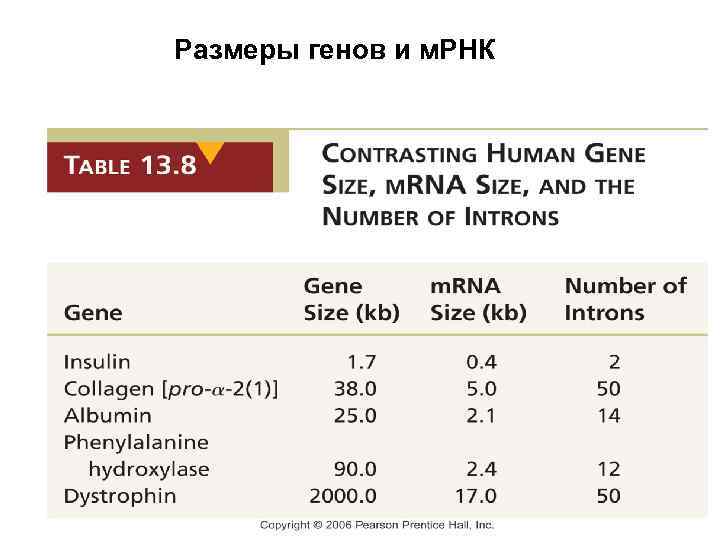 Размеры генов и м. РНК
Размеры генов и м. РНК
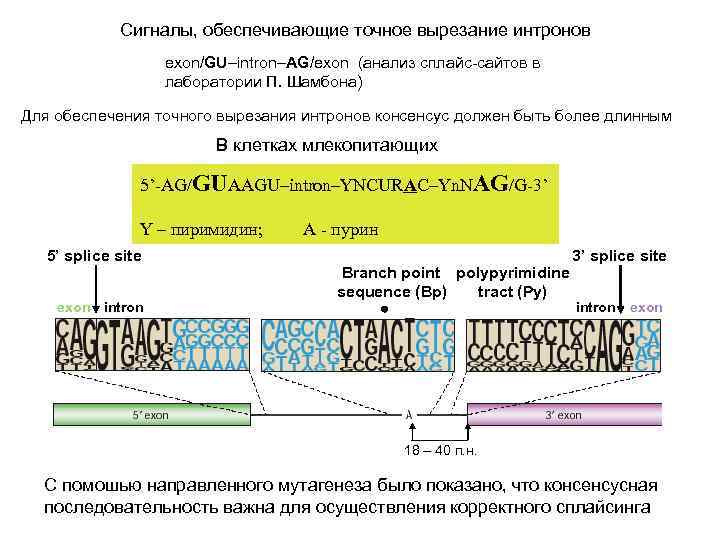 Сигналы, обеспечивающие точное вырезание интронов exon/GU–intron–AG/exon (анализ сплайс-сайтов в лаборатории П. Шамбона) Для обеспечения точного вырезания интронов консенсус должен быть более длинным В клетках млекопитающих 5’-AG/GUAAGU–intron–YNCURAC–Yn. NAG/G-3’ Y – пиримидин; 5’ splice site exon intron A - пурин Branch point polypyrimidine sequence (Bp) tract (Py) 3’ splice site intron exon 18 – 40 п. н. С помошью направленного мутагенеза было показано, что консенсусная последовательность важна для осуществления корректного сплайсинга
Сигналы, обеспечивающие точное вырезание интронов exon/GU–intron–AG/exon (анализ сплайс-сайтов в лаборатории П. Шамбона) Для обеспечения точного вырезания интронов консенсус должен быть более длинным В клетках млекопитающих 5’-AG/GUAAGU–intron–YNCURAC–Yn. NAG/G-3’ Y – пиримидин; 5’ splice site exon intron A - пурин Branch point polypyrimidine sequence (Bp) tract (Py) 3’ splice site intron exon 18 – 40 п. н. С помошью направленного мутагенеза было показано, что консенсусная последовательность важна для осуществления корректного сплайсинга
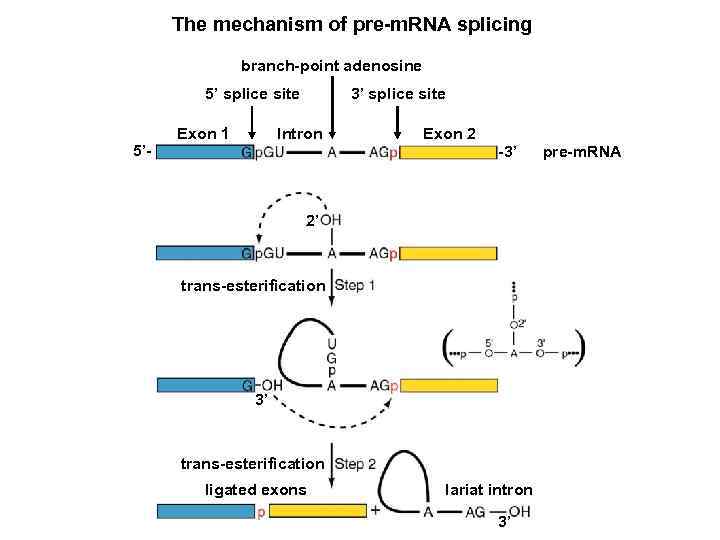 The mechanism of pre-m. RNA splicing branch-point adenosine 5’ splice site 5’- Exon 1 3’ splice site Intron Exon 2 -3’ 2’ trans-esterification 3’ trans-esterification ligated exons lariat intron 3’ pre-m. RNA
The mechanism of pre-m. RNA splicing branch-point adenosine 5’ splice site 5’- Exon 1 3’ splice site Intron Exon 2 -3’ 2’ trans-esterification 3’ trans-esterification ligated exons lariat intron 3’ pre-m. RNA
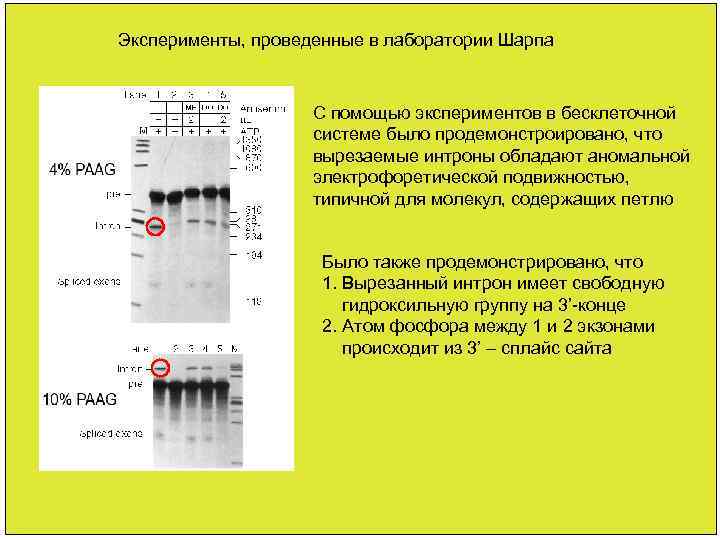 Эксперименты, проведенные в лаборатории Шарпа C помощью экспериментов в бесклеточной системе было продемонстроировано, что вырезаемые интроны обладают аномальной электрофоретической подвижностью, типичной для молекул, содержащих петлю Эти продукты обладают анамальной электрофоретической подвижностью, что и позволило подтвердить их существование Было также продемонстрировано, что 1. Вырезанный интрон имеет свободную гидроксильную группу на 3’-конце 2. Атом фосфора между 1 и 2 экзонами происходит из 3’ – сплайс сайта
Эксперименты, проведенные в лаборатории Шарпа C помощью экспериментов в бесклеточной системе было продемонстроировано, что вырезаемые интроны обладают аномальной электрофоретической подвижностью, типичной для молекул, содержащих петлю Эти продукты обладают анамальной электрофоретической подвижностью, что и позволило подтвердить их существование Было также продемонстрировано, что 1. Вырезанный интрон имеет свободную гидроксильную группу на 3’-конце 2. Атом фосфора между 1 и 2 экзонами происходит из 3’ – сплайс сайта
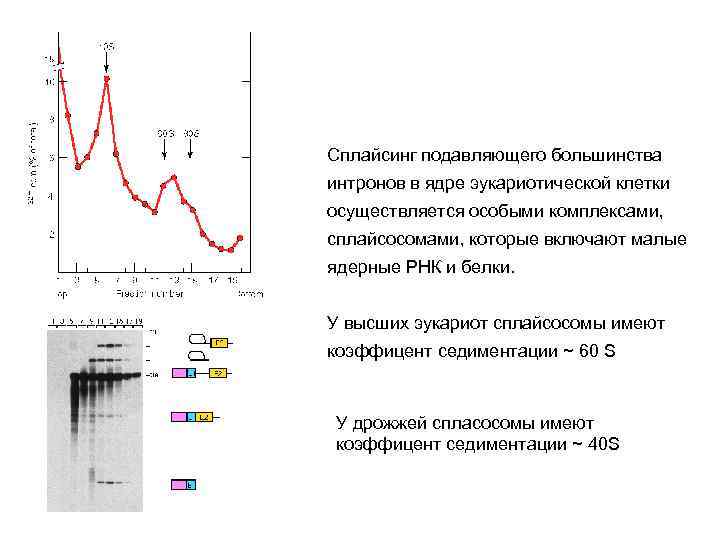 Сплайсинг подавляющего большинства интронов в ядре эукариотической клетки осуществляется особыми комплексами, сплайсосомами, которые включают малые ядерные РНК и белки. У высших эукариот сплайсосомы имеют коэффицент седиментации ~ 60 S У дрожжей спласосомы имеют коэффицент седиментации ~ 40 S
Сплайсинг подавляющего большинства интронов в ядре эукариотической клетки осуществляется особыми комплексами, сплайсосомами, которые включают малые ядерные РНК и белки. У высших эукариот сплайсосомы имеют коэффицент седиментации ~ 60 S У дрожжей спласосомы имеют коэффицент седиментации ~ 40 S
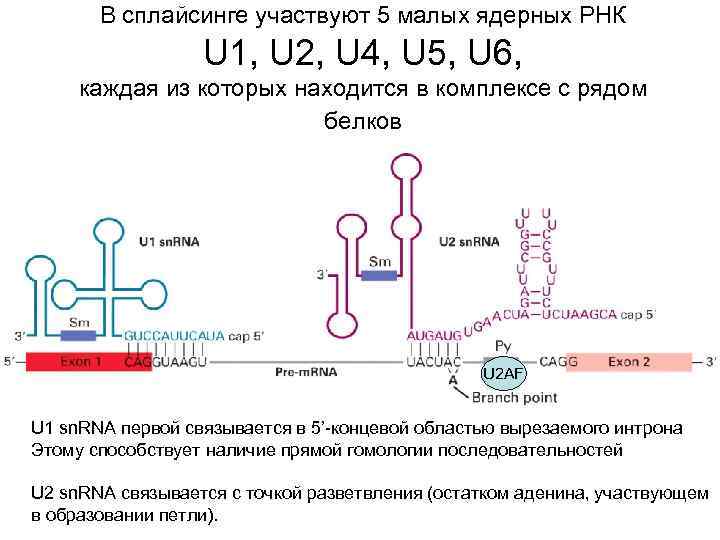 В сплайсинге участвуют 5 малых ядерных РНК U 1, U 2, U 4, U 5, U 6, каждая из которых находится в комплексе с рядом белков U 2 AF U 1 sn. RNA первой связывается в 5’-концевой областью вырезаемого интрона Этому способствует наличие прямой гомологии последовательностей U 2 sn. RNA связывается с точкой разветвления (остатком аденина, участвующем в образовании петли).
В сплайсинге участвуют 5 малых ядерных РНК U 1, U 2, U 4, U 5, U 6, каждая из которых находится в комплексе с рядом белков U 2 AF U 1 sn. RNA первой связывается в 5’-концевой областью вырезаемого интрона Этому способствует наличие прямой гомологии последовательностей U 2 sn. RNA связывается с точкой разветвления (остатком аденина, участвующем в образовании петли).
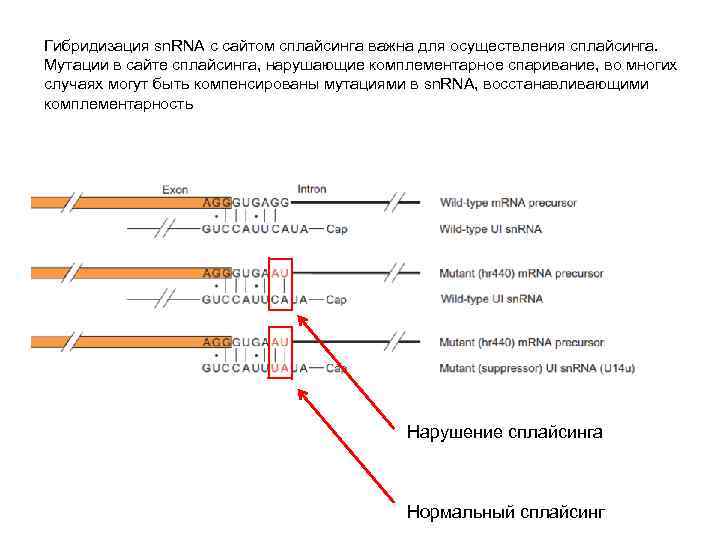 Гибридизация sn. RNA с сайтом сплайсинга важна для осуществления сплайсинга. Мутации в сайте сплайсинга, нарушающие комплементарное спаривание, во многих случаях могут быть компенсированы мутациями в sn. RNA, восстанавливающими комплементарность Нарушение сплайсинга Нормальный сплайсинг
Гибридизация sn. RNA с сайтом сплайсинга важна для осуществления сплайсинга. Мутации в сайте сплайсинга, нарушающие комплементарное спаривание, во многих случаях могут быть компенсированы мутациями в sn. RNA, восстанавливающими комплементарность Нарушение сплайсинга Нормальный сплайсинг
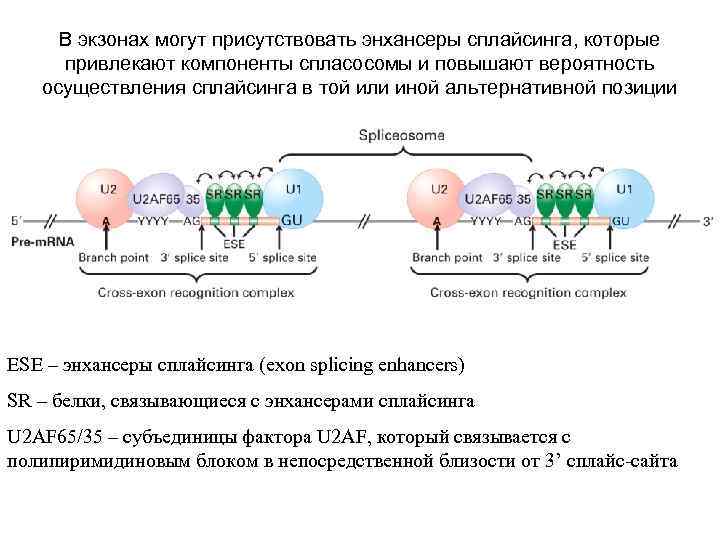 В экзонах могут присутствовать энхансеры сплайсинга, которые привлекают компоненты спласосомы и повышают вероятность осуществления сплайсинга в той или иной альтернативной позиции ESE – энхансеры сплайсинга (exon splicing enhancers) SR – белки, связывающиеся с энхансерами сплайсинга U 2 AF 65/35 – субъединицы фактора U 2 AF, который связывается с полипиримидиновым блоком в непосредственной близости от 3’ сплайс-сайта
В экзонах могут присутствовать энхансеры сплайсинга, которые привлекают компоненты спласосомы и повышают вероятность осуществления сплайсинга в той или иной альтернативной позиции ESE – энхансеры сплайсинга (exon splicing enhancers) SR – белки, связывающиеся с энхансерами сплайсинга U 2 AF 65/35 – субъединицы фактора U 2 AF, который связывается с полипиримидиновым блоком в непосредственной близости от 3’ сплайс-сайта
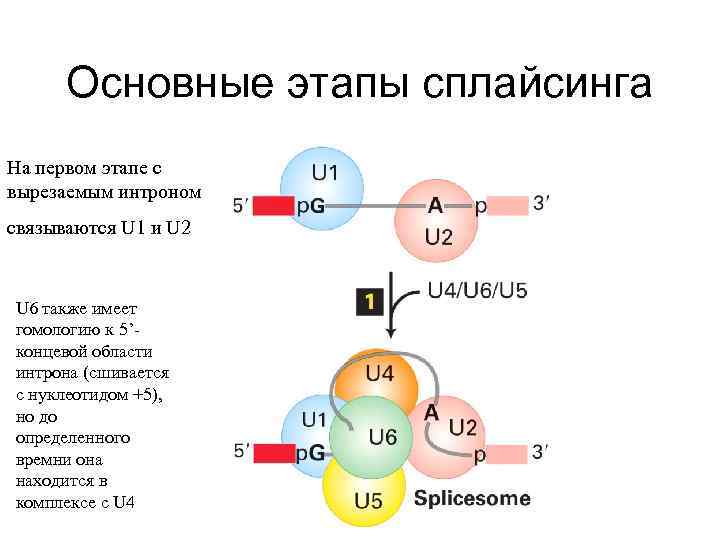 Основные этапы сплайсинга На первом этапе с вырезаемым интроном связываются U 1 и U 2 U 6 также имеет гомологию к 5’концевой области интрона (сшивается с нуклеотидом +5), но до определенного времни она находится в комплексе с U 4
Основные этапы сплайсинга На первом этапе с вырезаемым интроном связываются U 1 и U 2 U 6 также имеет гомологию к 5’концевой области интрона (сшивается с нуклеотидом +5), но до определенного времни она находится в комплексе с U 4
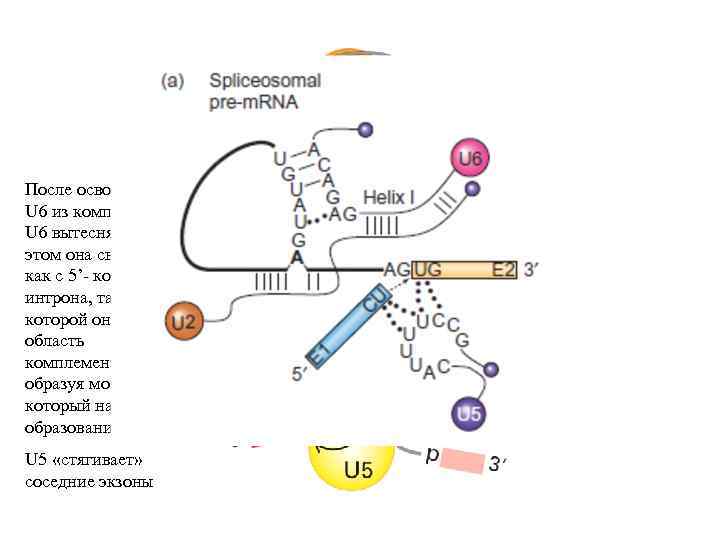 После освобождения U 6 из комплекса с U 4, U 6 вытесняет U 1. При этом она связывается как с 5’- концом интрона, так и с U 2 (c которой она имеет область комплементарности), образуя мостик, который направляет образование петли. U 5 «стягивает» соседние экзоны
После освобождения U 6 из комплекса с U 4, U 6 вытесняет U 1. При этом она связывается как с 5’- концом интрона, так и с U 2 (c которой она имеет область комплементарности), образуя мостик, который направляет образование петли. U 5 «стягивает» соседние экзоны
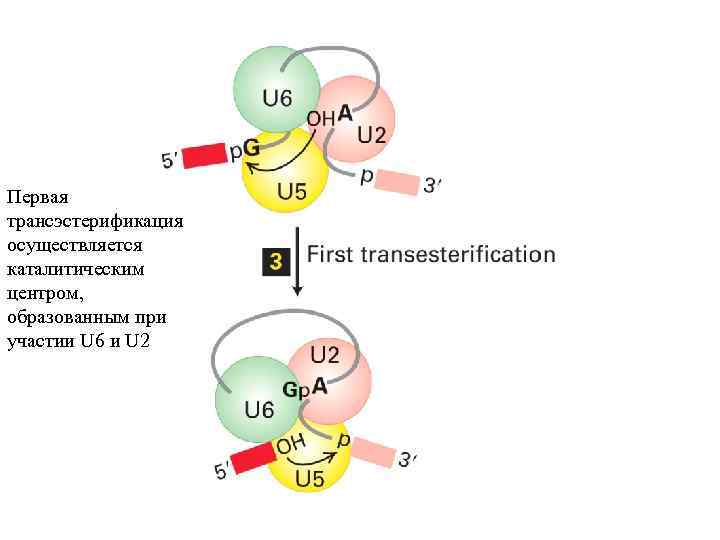 Первая трансэстерификация осуществляется каталитическим центром, образованным при участии U 6 и U 2
Первая трансэстерификация осуществляется каталитическим центром, образованным при участии U 6 и U 2
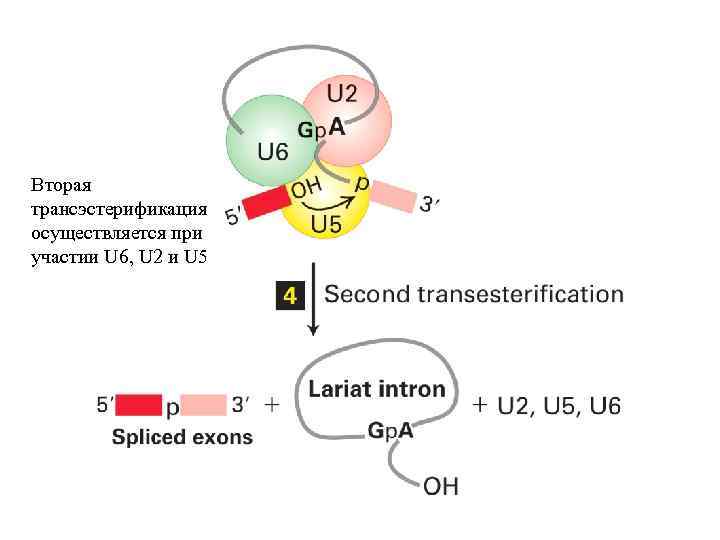 Вторая трансэстерификация осуществляется при участии U 6, U 2 и U 5
Вторая трансэстерификация осуществляется при участии U 6, U 2 и U 5
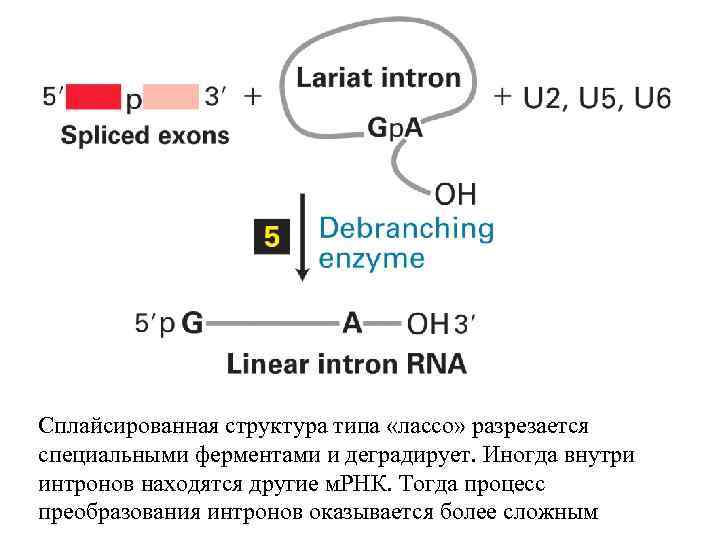 Сплайсированная структура типа «лассо» разрезается специальными ферментами и деградирует. Иногда внутри интронов находятся другие м. РНК. Тогда процесс преобразования интронов оказывается более сложным
Сплайсированная структура типа «лассо» разрезается специальными ферментами и деградирует. Иногда внутри интронов находятся другие м. РНК. Тогда процесс преобразования интронов оказывается более сложным
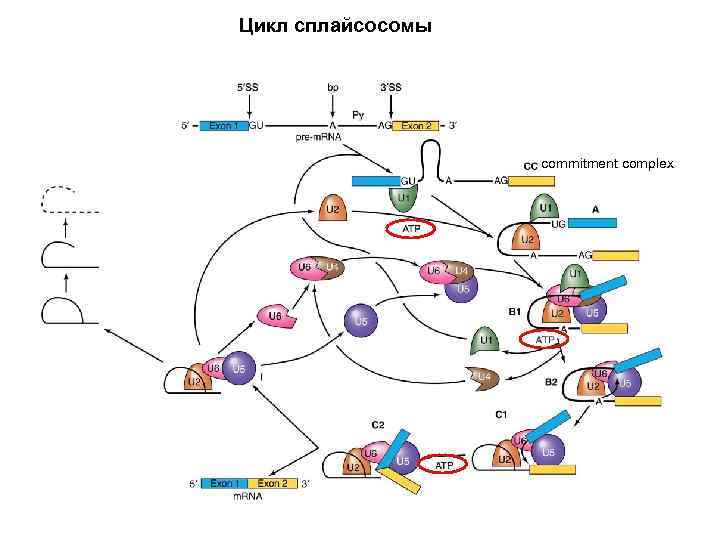 Цикл сплайсосомы commitment complex
Цикл сплайсосомы commitment complex
 Для правильного выбора 3’ сплайс-сайта необходимы также факторы сплайсинга Slu 7 и U 2 AF фактор сплайсинга SC 35 необходим для формирования начального комплекса (commitment complex), включающего U 1 sn. RNA
Для правильного выбора 3’ сплайс-сайта необходимы также факторы сплайсинга Slu 7 и U 2 AF фактор сплайсинга SC 35 необходим для формирования начального комплекса (commitment complex), включающего U 1 sn. RNA
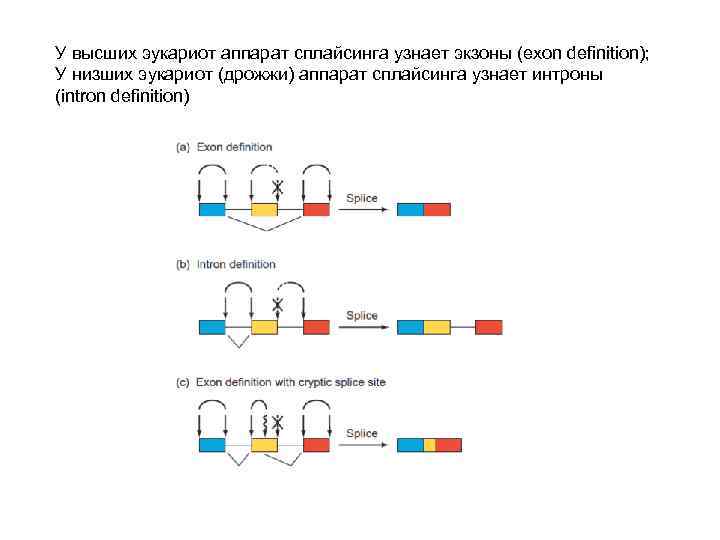 У высших эукариот аппарат сплайсинга узнает экзоны (exon definition); У низших эукариот (дрожжи) аппарат сплайсинга узнает интроны (intron definition)
У высших эукариот аппарат сплайсинга узнает экзоны (exon definition); У низших эукариот (дрожжи) аппарат сплайсинга узнает интроны (intron definition)
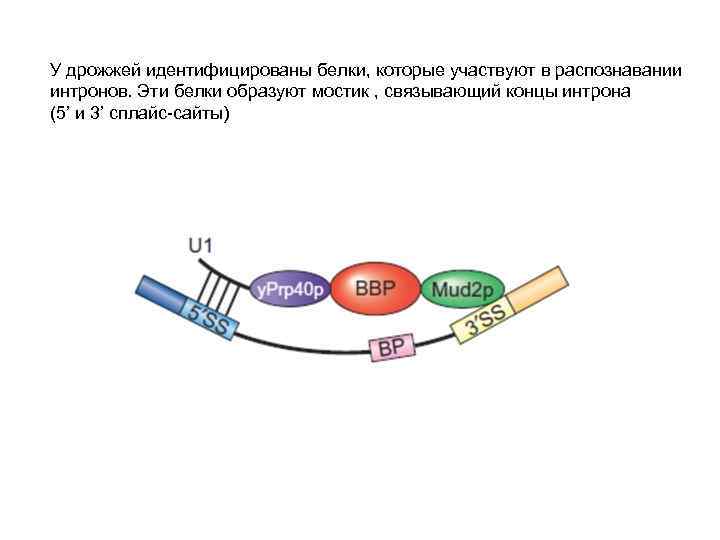 У дрожжей идентифицированы белки, которые участвуют в распознавании интронов. Эти белки образуют мостик , связывающий концы интрона (5’ и 3’ сплайс-сайты)
У дрожжей идентифицированы белки, которые участвуют в распознавании интронов. Эти белки образуют мостик , связывающий концы интрона (5’ и 3’ сплайс-сайты)
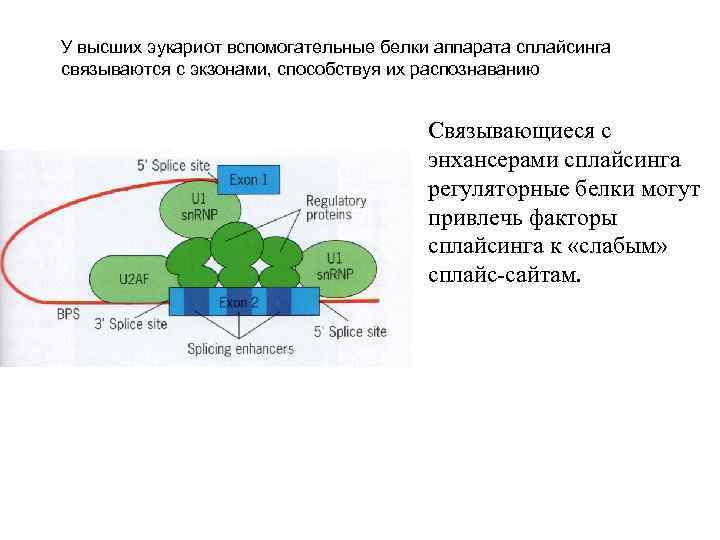 У высших эукариот вспомогательные белки аппарата сплайсинга связываются с экзонами, способствуя их распознаванию Связывающиеся с энхансерами сплайсинга регуляторные белки могут привлечь факторы сплайсинга к «слабым» сплайс-сайтам.
У высших эукариот вспомогательные белки аппарата сплайсинга связываются с экзонами, способствуя их распознаванию Связывающиеся с энхансерами сплайсинга регуляторные белки могут привлечь факторы сплайсинга к «слабым» сплайс-сайтам.
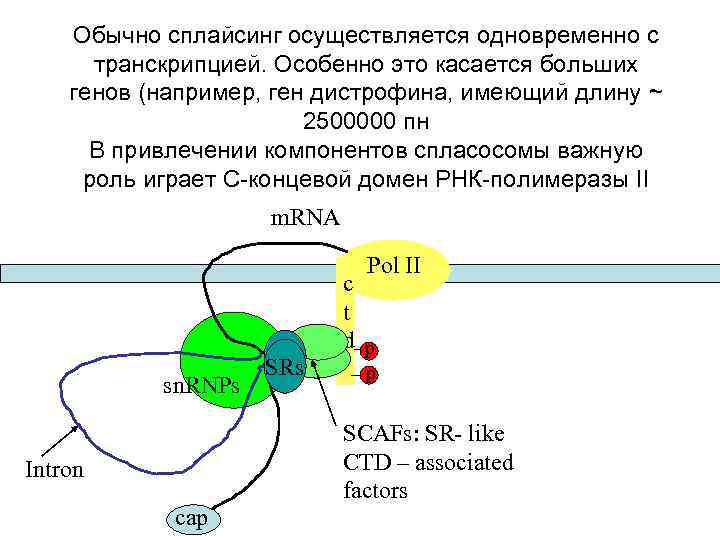 Обычно сплайсинг осуществляется одновременно с транскрипцией. Особенно это касается больших генов (например, ген дистрофина, имеющий длину ~ 2500000 пн В привлечении компонентов спласосомы важную роль играет C-концевой домен РНК-полимеразы II m. RNA Pol II sn. RNPs Intron cap SRs c t d p p SCAFs: SR- like CTD – associated factors
Обычно сплайсинг осуществляется одновременно с транскрипцией. Особенно это касается больших генов (например, ген дистрофина, имеющий длину ~ 2500000 пн В привлечении компонентов спласосомы важную роль играет C-концевой домен РНК-полимеразы II m. RNA Pol II sn. RNPs Intron cap SRs c t d p p SCAFs: SR- like CTD – associated factors
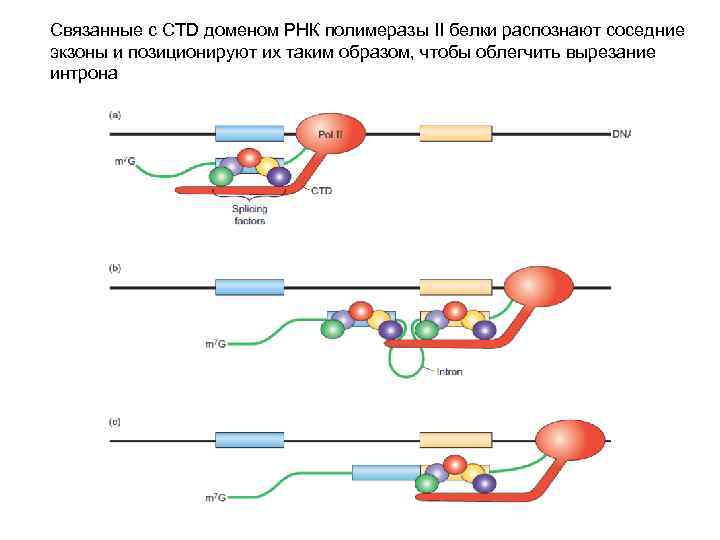 Связанные с CTD доменом РНК полимеразы II белки распознают соседние экзоны и позиционируют их таким образом, чтобы облегчить вырезание интрона
Связанные с CTD доменом РНК полимеразы II белки распознают соседние экзоны и позиционируют их таким образом, чтобы облегчить вырезание интрона
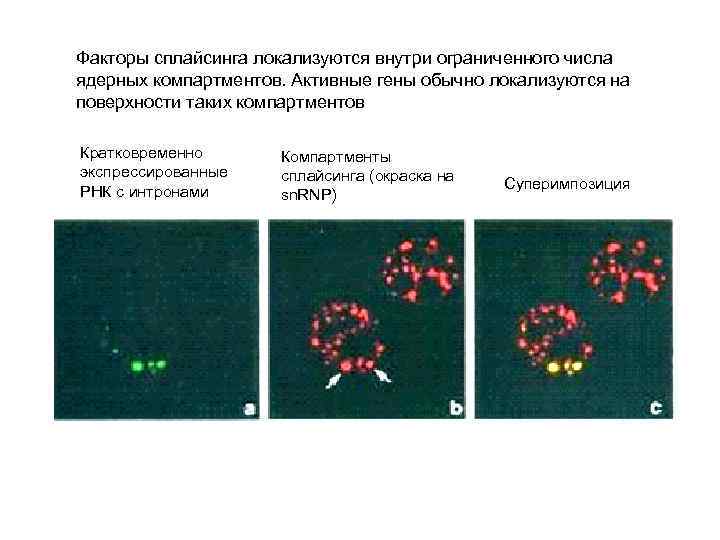 Факторы сплайсинга локализуются внутри ограниченного числa ядерных компартментов. Активные гены обычно локализуются на поверхности таких компартментов Кратковременно экспрессированные РНК с интронами Компартменты сплайсинга (окраска на sn. RNP) Суперимпозиция
Факторы сплайсинга локализуются внутри ограниченного числa ядерных компартментов. Активные гены обычно локализуются на поверхности таких компартментов Кратковременно экспрессированные РНК с интронами Компартменты сплайсинга (окраска на sn. RNP) Суперимпозиция
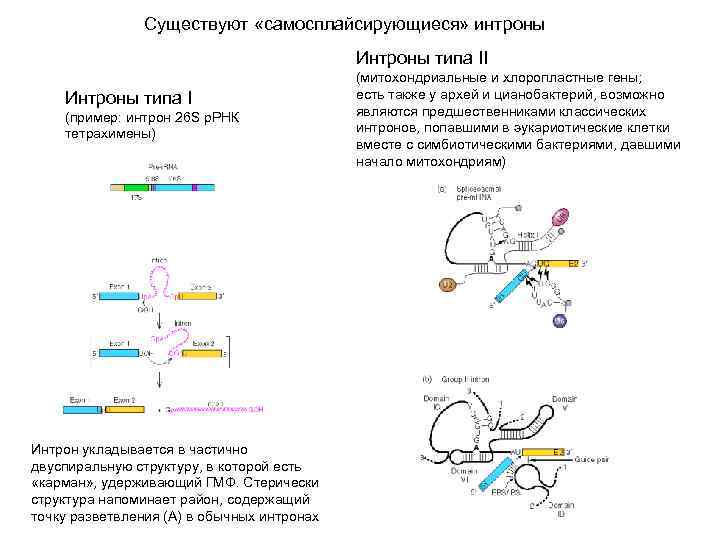 Существуют «самосплайсирующиеся» интроны Интроны типа II Интроны типа I (пример: интрон 26 S р. РНК тетрахимены) Интрон укладывается в частично двуспиральную структуру, в которой есть «карман» , удерживающий ГМФ. Стерически структура напоминает район, содержащий точку разветвления (А) в обычных интронах (митохондриальные и хлоропластные гены; есть также у архей и цианобактерий, возможно являются предшественниками классических интронов, попавшими в эукариотические клетки вместе с симбиотическими бактериями, давшими начало митохондриям)
Существуют «самосплайсирующиеся» интроны Интроны типа II Интроны типа I (пример: интрон 26 S р. РНК тетрахимены) Интрон укладывается в частично двуспиральную структуру, в которой есть «карман» , удерживающий ГМФ. Стерически структура напоминает район, содержащий точку разветвления (А) в обычных интронах (митохондриальные и хлоропластные гены; есть также у архей и цианобактерий, возможно являются предшественниками классических интронов, попавшими в эукариотические клетки вместе с симбиотическими бактериями, давшими начало митохондриям)
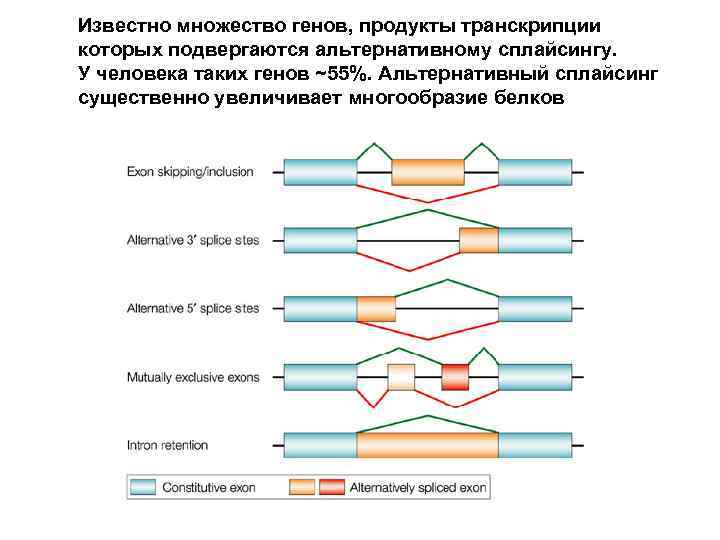 Известно множество генов, продукты транскрипции которых подвергаются альтернативному сплайсингу. У человека таких генов ~55%. Альтернативный сплайсинг существенно увеличивает многообразие белков
Известно множество генов, продукты транскрипции которых подвергаются альтернативному сплайсингу. У человека таких генов ~55%. Альтернативный сплайсинг существенно увеличивает многообразие белков
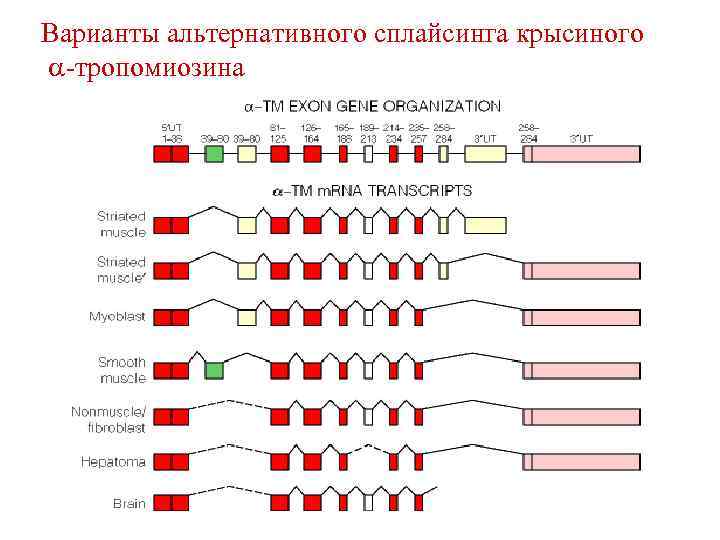 Варианты альтернативного сплайсинга крысиного -тропомиозина
Варианты альтернативного сплайсинга крысиного -тропомиозина
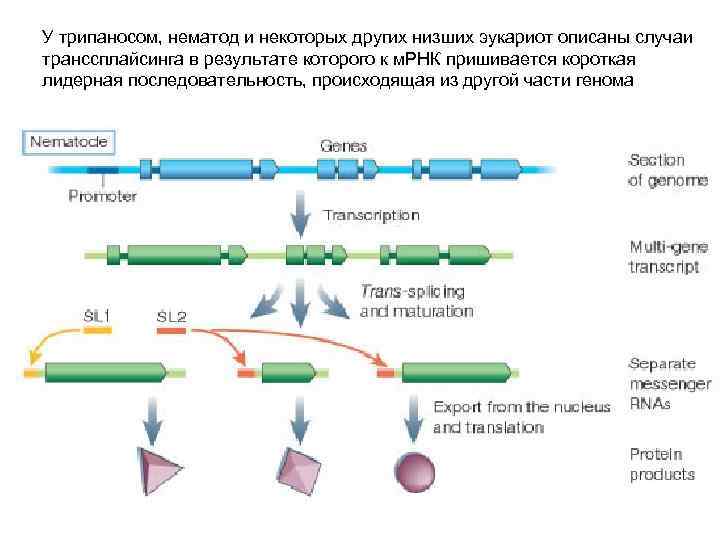 У трипаносом, нематод и некоторых других низших эукариот описаны случаи транссплайсинга в результате которого к м. РНК пришивается короткая лидерная последовательность, происходящая из другой части генома
У трипаносом, нематод и некоторых других низших эукариот описаны случаи транссплайсинга в результате которого к м. РНК пришивается короткая лидерная последовательность, происходящая из другой части генома
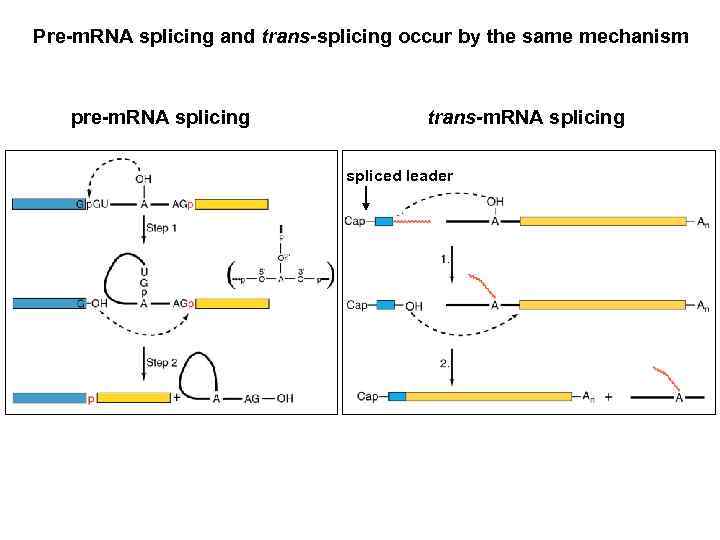 Pre-m. RNA splicing and trans-splicing occur by the same mechanism pre-m. RNA splicing trans-m. RNA splicing spliced leader
Pre-m. RNA splicing and trans-splicing occur by the same mechanism pre-m. RNA splicing trans-m. RNA splicing spliced leader
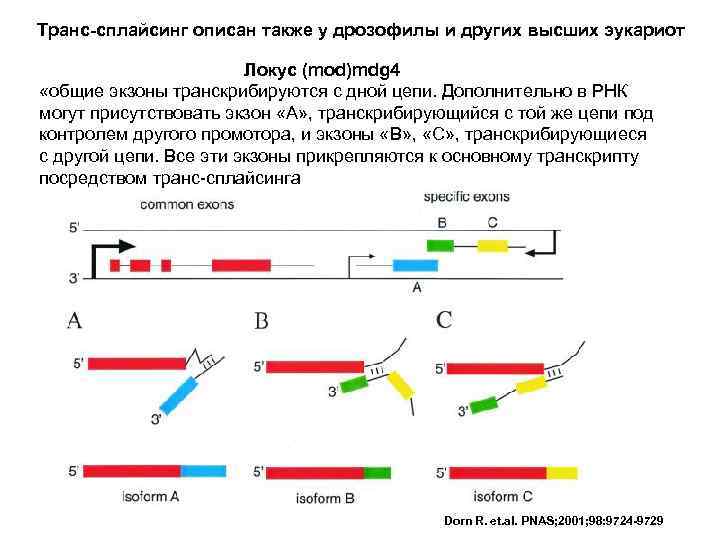 Транс-сплайсинг описан также у дрозофилы и других высших эукариот Локус (mod)mdg 4 «общие экзоны транскрибируются с дной цепи. Дополнительно в РНК могут присутствовать экзон «А» , транскрибирующийся с той же цепи под контролем другого промотора, и экзоны «B» , «С» , транскрибирующиеся с другой цепи. Все эти экзоны прикрепляются к основному транскрипту посредством транс-сплайсинга Dorn R. et. al. PNAS; 2001; 98: 9724 -9729
Транс-сплайсинг описан также у дрозофилы и других высших эукариот Локус (mod)mdg 4 «общие экзоны транскрибируются с дной цепи. Дополнительно в РНК могут присутствовать экзон «А» , транскрибирующийся с той же цепи под контролем другого промотора, и экзоны «B» , «С» , транскрибирующиеся с другой цепи. Все эти экзоны прикрепляются к основному транскрипту посредством транс-сплайсинга Dorn R. et. al. PNAS; 2001; 98: 9724 -9729
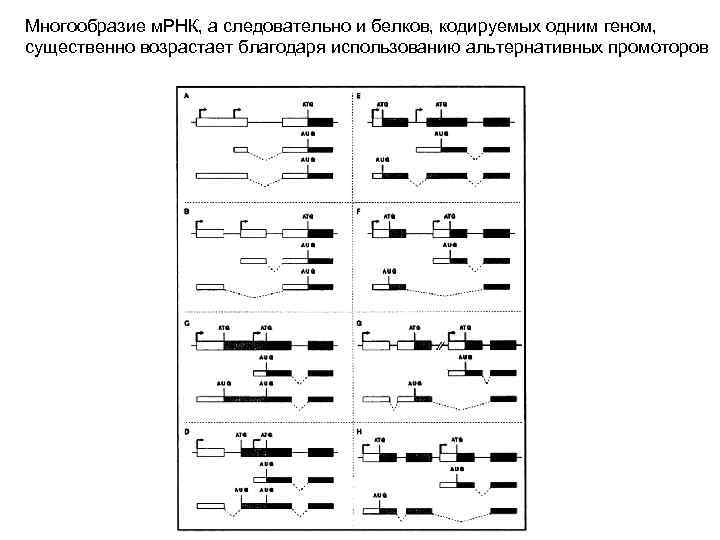 Многообразие м. РНК, а следовательно и белков, кодируемых одним геном, существенно возрастает благодаря использованию альтернативных промоторов
Многообразие м. РНК, а следовательно и белков, кодируемых одним геном, существенно возрастает благодаря использованию альтернативных промоторов
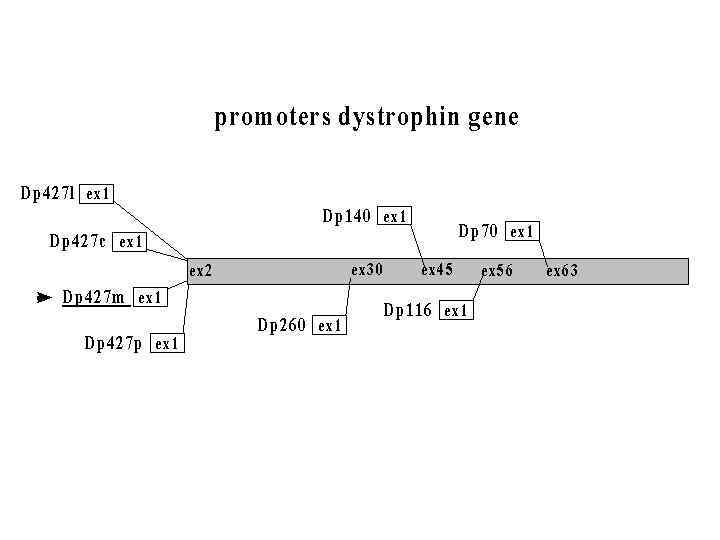
 В классической молекулярной биологии геном называли последовательность ДНК, кодирующую определенный белок У высших эукариот такого рода ген формируется только на уровне м. РНК
В классической молекулярной биологии геном называли последовательность ДНК, кодирующую определенный белок У высших эукариот такого рода ген формируется только на уровне м. РНК
 Преобразования 5’ конца м РНК (присоединение 7 -метилгуанина) • Cap – Защищает РНК от экзонуклеазного расщепления – Спсобствует трансляции – Способствует транспорту РНК из ядра в цитоплазму
Преобразования 5’ конца м РНК (присоединение 7 -метилгуанина) • Cap – Защищает РНК от экзонуклеазного расщепления – Спсобствует трансляции – Способствует транспорту РНК из ядра в цитоплазму
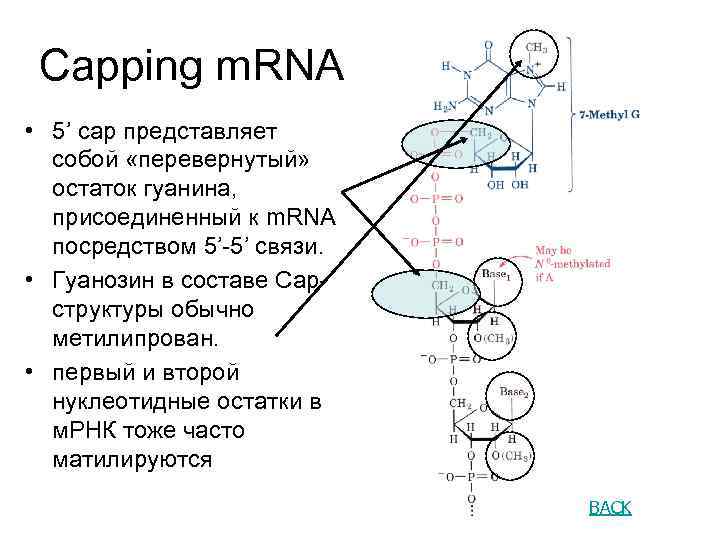 Capping m. RNA • 5’ cap представляет собой «перевернутый» остаток гуанина, присоединенный к m. RNA посредством 5’-5’ связи. • Гуанозин в составе Capструктуры обычно метилипрован. • первый и второй нуклеотидные остатки в м. РНК тоже часто матилируются BACK
Capping m. RNA • 5’ cap представляет собой «перевернутый» остаток гуанина, присоединенный к m. RNA посредством 5’-5’ связи. • Гуанозин в составе Capструктуры обычно метилипрован. • первый и второй нуклеотидные остатки в м. РНК тоже часто матилируются BACK
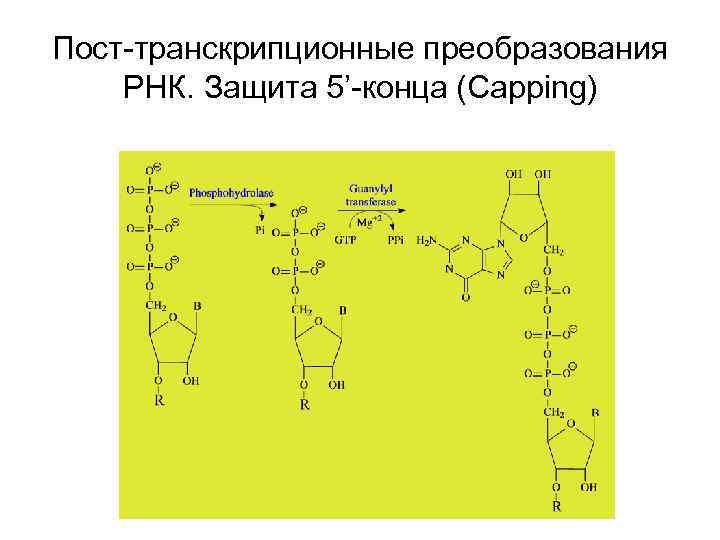 Пост-транскрипционные преобразования РНК. Защита 5’-конца (Capping)
Пост-транскрипционные преобразования РНК. Защита 5’-конца (Capping)
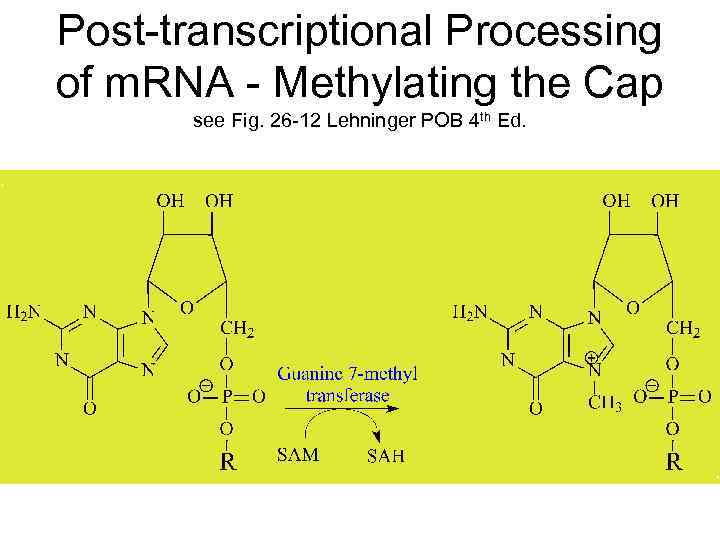 Post-transcriptional Processing of m. RNA - Methylating the Cap see Fig. 26 -12 Lehninger POB 4 th Ed.
Post-transcriptional Processing of m. RNA - Methylating the Cap see Fig. 26 -12 Lehninger POB 4 th Ed.
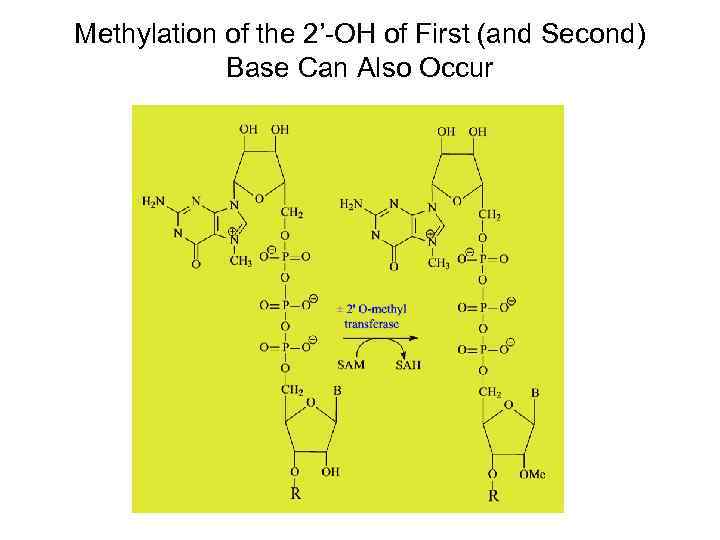 Methylation of the 2’-OH of First (and Second) Base Can Also Occur
Methylation of the 2’-OH of First (and Second) Base Can Also Occur
 Зачем нужен «кэп» ? Защита 5’ конца РНК от нуклеаз Транспорт РНК из ядра в цитоплазму Инициация трансляции
Зачем нужен «кэп» ? Защита 5’ конца РНК от нуклеаз Транспорт РНК из ядра в цитоплазму Инициация трансляции
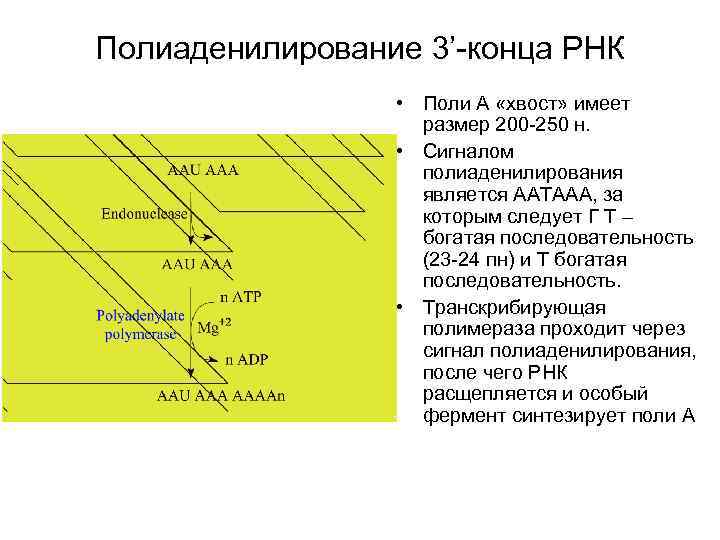 Полиаденилирование 3’-конца РНК • Поли А «хвост» имеет размер 200 -250 н. • Сигналом полиаденилирования является AAТAAA, за которым следует Г Т – богатая последовательность (23 -24 пн) и Т богатая последовательность. • Транскрибирующая полимераза проходит через сигнал полиаденилирования, после чего РНК расщепляется и особый фермент синтезирует поли А
Полиаденилирование 3’-конца РНК • Поли А «хвост» имеет размер 200 -250 н. • Сигналом полиаденилирования является AAТAAA, за которым следует Г Т – богатая последовательность (23 -24 пн) и Т богатая последовательность. • Транскрибирующая полимераза проходит через сигнал полиаденилирования, после чего РНК расщепляется и особый фермент синтезирует поли А
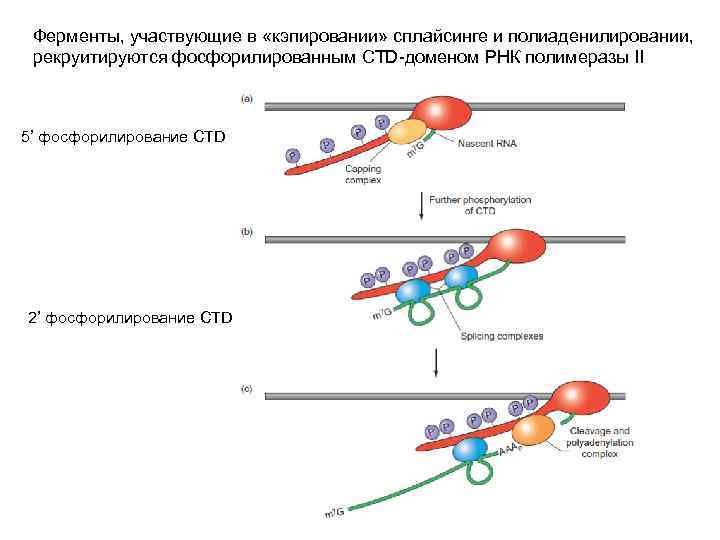 Ферменты, участвующие в «кэпировании» сплайсинге и полиаденилировании, рекруитируются фосфорилированным CTD-доменом РНК полимеразы II 5’ фосфорилирование CTD 2’ фосфорилирование CTD
Ферменты, участвующие в «кэпировании» сплайсинге и полиаденилировании, рекруитируются фосфорилированным CTD-доменом РНК полимеразы II 5’ фосфорилирование CTD 2’ фосфорилирование CTD
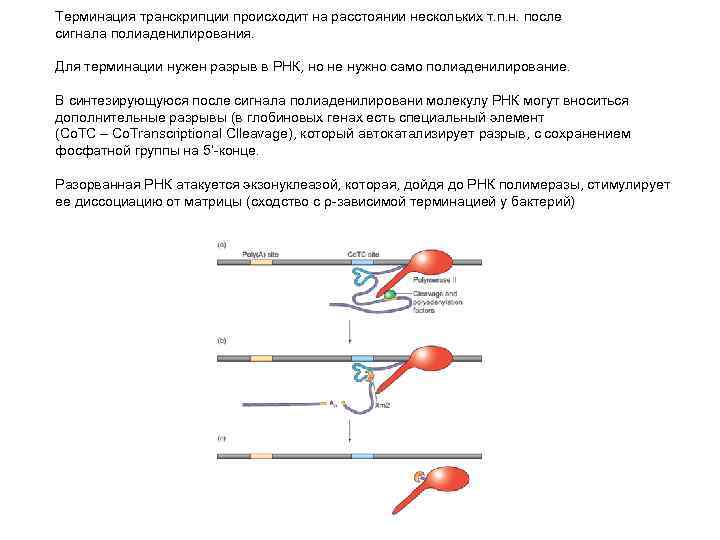 Терминация транскрипции происходит на расстоянии нескольких т. п. н. после сигнала полиаденилирования. Для терминации нужен разрыв в РНК, но не нужно само полиаденилирование. В синтезирующуюся после сигнала полиаденилировани молекулу РНК могут вноситься дополнительные разрывы (в глобиновых генах есть специальный элемент (Co. TC – Co. Transcriptional Clleavage), который автокатализирует разрыв, с сохранением фосфатной группы на 5’-конце. Разорванная РНК атакуется экзонуклеазой, которая, дойдя до РНК полимеразы, стимулирует ее диссоциацию от матрицы (cходство с ρ-зависимой терминацией у бактерий)
Терминация транскрипции происходит на расстоянии нескольких т. п. н. после сигнала полиаденилирования. Для терминации нужен разрыв в РНК, но не нужно само полиаденилирование. В синтезирующуюся после сигнала полиаденилировани молекулу РНК могут вноситься дополнительные разрывы (в глобиновых генах есть специальный элемент (Co. TC – Co. Transcriptional Clleavage), который автокатализирует разрыв, с сохранением фосфатной группы на 5’-конце. Разорванная РНК атакуется экзонуклеазой, которая, дойдя до РНК полимеразы, стимулирует ее диссоциацию от матрицы (cходство с ρ-зависимой терминацией у бактерий)
 У трипаносом существует процесс уридилового редактирования кинетопластных РНК Процесс редактирования осуществляется в направлении от 3’ конца РНК к 5’ концу при участии особых гидовых РНК, которые также кодируются геномом кинетопласта часть последовательности РНК цитохром-оксидазы после редактирования. Красным показаны вставленные остатки уридина. Над последовательностью показаны выброшенные остатки урацила
У трипаносом существует процесс уридилового редактирования кинетопластных РНК Процесс редактирования осуществляется в направлении от 3’ конца РНК к 5’ концу при участии особых гидовых РНК, которые также кодируются геномом кинетопласта часть последовательности РНК цитохром-оксидазы после редактирования. Красным показаны вставленные остатки уридина. Над последовательностью показаны выброшенные остатки урацила
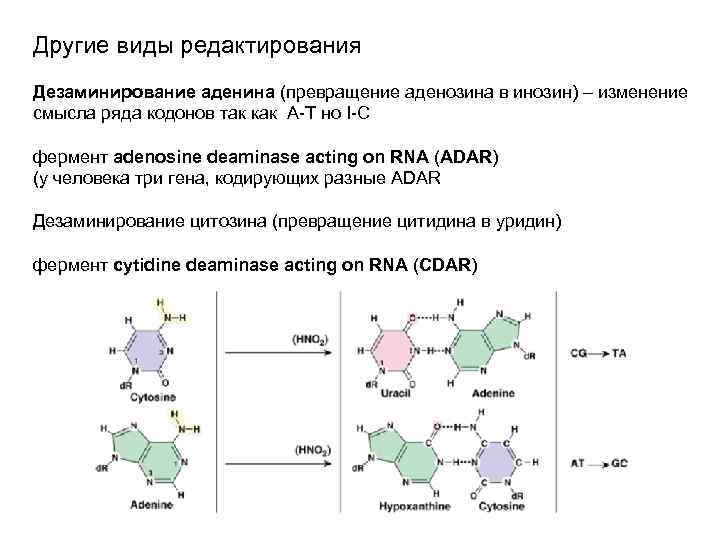 Другие виды редактирования Дезаминирование аденина (превращение аденозина в инозин) – изменение смысла ряда кодонов так как A-T но I-C фермент adenosine deaminase acting on RNA (ADAR) (у человека три гена, кодирующих разные ADAR Дезаминирование цитозина (превращение цитидина в уридин) фермент cytidine deaminase acting on RNA (CDAR)
Другие виды редактирования Дезаминирование аденина (превращение аденозина в инозин) – изменение смысла ряда кодонов так как A-T но I-C фермент adenosine deaminase acting on RNA (ADAR) (у человека три гена, кодирующих разные ADAR Дезаминирование цитозина (превращение цитидина в уридин) фермент cytidine deaminase acting on RNA (CDAR)


