Кристаллическое состояние.ppt
- Количество слайдов: 21
 Строение вещества в конденсированном состоянии Кристаллическое состояние
Строение вещества в конденсированном состоянии Кристаллическое состояние
 Для кристаллического состояния характерно строго определенное расположение частиц во всем объеме кристалла, т. е в расположении частиц существует дальний порядок. Это обусловливает анизотропию кристаллического вещества – различие физических свойств кристалла в разных направлениях.
Для кристаллического состояния характерно строго определенное расположение частиц во всем объеме кристалла, т. е в расположении частиц существует дальний порядок. Это обусловливает анизотропию кристаллического вещества – различие физических свойств кристалла в разных направлениях.
 Кристаллическая решетка характерное для кристалла расположение атомов, ионов или молекул, обладающее периодической повторяемостью в трех измерениях. Различают четыре основных типа структур кристаллических веществ, или кристаллических решеток, - атомную, ионную, металлическую и молекулярную.
Кристаллическая решетка характерное для кристалла расположение атомов, ионов или молекул, обладающее периодической повторяемостью в трех измерениях. Различают четыре основных типа структур кристаллических веществ, или кристаллических решеток, - атомную, ионную, металлическую и молекулярную.
 1. В узлах атомной кристаллической решетки находятся атомы одинаковых или различных элементов, соединенные между собой ковалентными связями, например, С(алмаз).
1. В узлах атомной кристаллической решетки находятся атомы одинаковых или различных элементов, соединенные между собой ковалентными связями, например, С(алмаз).
 2. Ионные кристаллические решетки построены из положительно и отрицательно заряженных ионов, между которыми действуют электростатические (кулоновские) силы притяжения, например, Na. Cl. + - + - +
2. Ионные кристаллические решетки построены из положительно и отрицательно заряженных ионов, между которыми действуют электростатические (кулоновские) силы притяжения, например, Na. Cl. + - + - +
 3. Металлическая кристаллическая решетка состоит из катионов металла, между которыми относительно свободно перемещаются валентные электроны. Отрицательный заряд таких электронов компенсирует + заряды катионов металла и удерживает их в узлах кристаллической решетки + + +
3. Металлическая кристаллическая решетка состоит из катионов металла, между которыми относительно свободно перемещаются валентные электроны. Отрицательный заряд таких электронов компенсирует + заряды катионов металла и удерживает их в узлах кристаллической решетки + + +
 4. В узлах молекулярной кристаллической решетки расположены молекулы, связанные между собой слабыми межмолекулярными связями. Между неполярными молекулами действуют дисперсионные силы; между полярными молекулами – дисперсионные, ориентационные и индукционные силы. +- + - + - + +- +- +-
4. В узлах молекулярной кристаллической решетки расположены молекулы, связанные между собой слабыми межмолекулярными связями. Между неполярными молекулами действуют дисперсионные силы; между полярными молекулами – дисперсионные, ориентационные и индукционные силы. +- + - + - + +- +- +-
 Энергия кристаллической решетки равна энергии, которую необходимо затратить на удаление составных частей кристаллической решетки на бесконечно большое расстояние друг от друга, измеряется в к. Дж/моль. Полиморфизм (многоформенность) – способность одного и того же вещества образовывать различные кристаллические формы в зависимости от условий.
Энергия кристаллической решетки равна энергии, которую необходимо затратить на удаление составных частей кристаллической решетки на бесконечно большое расстояние друг от друга, измеряется в к. Дж/моль. Полиморфизм (многоформенность) – способность одного и того же вещества образовывать различные кристаллические формы в зависимости от условий.
 Различные кристаллические формы одного и того же вещества называются полиморфными модификациями (алмаз, графит, карбин ). Существование различных веществ в одной и той же кристаллической форме называется изоморфизмом (равноформенностью), а такие вещества изоморфными.
Различные кристаллические формы одного и того же вещества называются полиморфными модификациями (алмаз, графит, карбин ). Существование различных веществ в одной и той же кристаллической форме называется изоморфизмом (равноформенностью), а такие вещества изоморфными.
 Зонная теория проводимости кристаллов Кристалл - единая система взаимодействующих частиц. Зонная теория - это теория молекулярных орбиталей для системы с большим (N=1023) числом частиц. В кристалле количество молекулярных орбиталей должно равняться сумме орбиталей атомов, образующих кристалл.
Зонная теория проводимости кристаллов Кристалл - единая система взаимодействующих частиц. Зонная теория - это теория молекулярных орбиталей для системы с большим (N=1023) числом частиц. В кристалле количество молекулярных орбиталей должно равняться сумме орбиталей атомов, образующих кристалл.
 Взаимодействие в кристалле большого числа атомов (N=1 O 23) приводит к появлению практически сплошного спектра энергий молекулярных орбиталей, т. е. к образованию энергетической зоны. Электроны могут находиться только на строго определенных энергетических уровнях и в кристалле также существуют зоны разрешенных и запрещенных энергий.
Взаимодействие в кристалле большого числа атомов (N=1 O 23) приводит к появлению практически сплошного спектра энергий молекулярных орбиталей, т. е. к образованию энергетической зоны. Электроны могут находиться только на строго определенных энергетических уровнях и в кристалле также существуют зоны разрешенных и запрещенных энергий.
 Энергетические уровни, на которых находятся валентные электроны, образуют валентную зону. Совокупность свободных, не занятых электронами уровней (валентных орбиталей), расположенных энергетически выше валентной зоны, в некоторых случаях в пределах ее, называется зоной проводимости.
Энергетические уровни, на которых находятся валентные электроны, образуют валентную зону. Совокупность свободных, не занятых электронами уровней (валентных орбиталей), расположенных энергетически выше валентной зоны, в некоторых случаях в пределах ее, называется зоной проводимости.
 В зависимости от природы взаимодействующих атомов и типа кристаллической решетки валентная зона и зона проводимости могут перекрываться или не перекрываться друг с другом. В последнем случае между валентной зоной и зоной проводимости возникает энергетический разрыв, называемый запрещенной зоной.
В зависимости от природы взаимодействующих атомов и типа кристаллической решетки валентная зона и зона проводимости могут перекрываться или не перекрываться друг с другом. В последнем случае между валентной зоной и зоной проводимости возникает энергетический разрыв, называемый запрещенной зоной.
 В зависимости от ширины запрещенной зоны Е все кристаллические вещества подразделяются на проводники (металлы), полупроводники и диэлектрики (изоляторы). В металлах валентная зона и зона проводимости перекрываются между собой, т. е. Е =0.
В зависимости от ширины запрещенной зоны Е все кристаллические вещества подразделяются на проводники (металлы), полупроводники и диэлектрики (изоляторы). В металлах валентная зона и зона проводимости перекрываются между собой, т. е. Е =0.
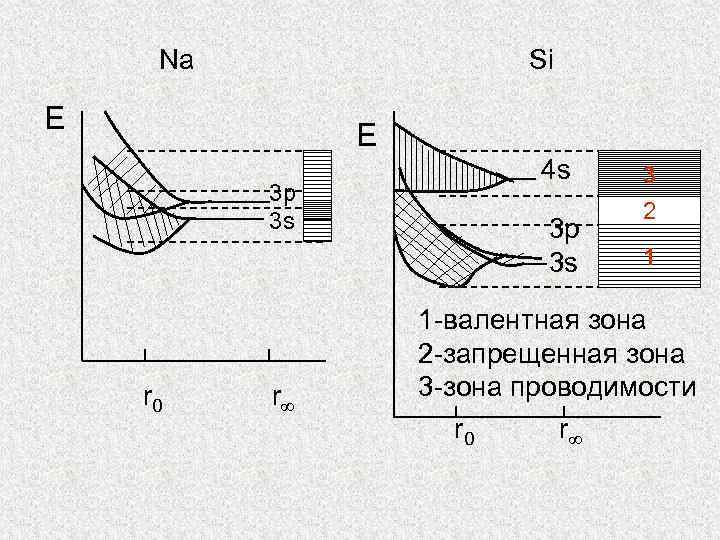 Na Si E E 3 p 3 s r 0 r 4 s 3 p 3 s 3 2 1 1 -валентная зона 2 -запрещенная зона 3 -зона проводимости r 0 r
Na Si E E 3 p 3 s r 0 r 4 s 3 p 3 s 3 2 1 1 -валентная зона 2 -запрещенная зона 3 -зона проводимости r 0 r
 Вещества, у которых ширина запрещенной зоны составляет 0, 1 -4, 0 э. В, относятся к полупроводникам. У проводников с увеличением температуры электрическая проводимость растет, у полупроводников уменьшается. Вещества, у которых ширина запрещенной зоны превышает 4 э. В, относятся к изоляторам (алмаз).
Вещества, у которых ширина запрещенной зоны составляет 0, 1 -4, 0 э. В, относятся к полупроводникам. У проводников с увеличением температуры электрическая проводимость растет, у полупроводников уменьшается. Вещества, у которых ширина запрещенной зоны превышает 4 э. В, относятся к изоляторам (алмаз).
 Для ионных кристаллов ширина запрещенной зоны составляет около 6 э. В. У молекулярных кристаллов энергетические уровни локализованы в пределах молекул и энергетические зоны не возникают. Поэтому указанные вещества относятся к изоляторам.
Для ионных кристаллов ширина запрещенной зоны составляет около 6 э. В. У молекулярных кристаллов энергетические уровни локализованы в пределах молекул и энергетические зоны не возникают. Поэтому указанные вещества относятся к изоляторам.
 Жидкое состояние Для жидкого агрегатного состояния характерны изотропия - одинаковость физических свойств по всем направлениям и текучесть способность легко изменять внешнюю форму под воздействием малых нагрузок. По высокой плотности и малой сжимаемости жидкости близки к твердым телам.
Жидкое состояние Для жидкого агрегатного состояния характерны изотропия - одинаковость физических свойств по всем направлениям и текучесть способность легко изменять внешнюю форму под воздействием малых нагрузок. По высокой плотности и малой сжимаемости жидкости близки к твердым телам.
 В жидкостях существует ближний порядок в расположении молекул, который проявляется в том, что число соседних молекул у каждой молекулы, а также их взаимное расположение в среднем для всех молекул в объеме жидкости одинаково. У жидкостей сильно выражена самодиффузия, т. е. непрерывные переходы молекул с места на место.
В жидкостях существует ближний порядок в расположении молекул, который проявляется в том, что число соседних молекул у каждой молекулы, а также их взаимное расположение в среднем для всех молекул в объеме жидкости одинаково. У жидкостей сильно выражена самодиффузия, т. е. непрерывные переходы молекул с места на место.
 Аморфное состояние характеризуется изотропностью и отсутствием четко фиксируемой точки плавления. Для такого состояния в расположении частиц наблюдается только ближний порядок. Аморфные вещества встречаются в двух формах: в форме однородного компактного твердого материала, получаемого при переохлаждении жидкости, и в форме дисперсного материала (порошка).
Аморфное состояние характеризуется изотропностью и отсутствием четко фиксируемой точки плавления. Для такого состояния в расположении частиц наблюдается только ближний порядок. Аморфные вещества встречаются в двух формах: в форме однородного компактного твердого материала, получаемого при переохлаждении жидкости, и в форме дисперсного материала (порошка).
 Твердый аморфный материал, который образуется при переохлаждении жидкости, называется стеклом. Стекло можно определить и как продукт плавления, перешедший при охлаждении в твердое состояние без кристаллизации. Аморфное состояние вещества является термодинамически нестабильным и при благоприятных условиях переходит в кристаллическое.
Твердый аморфный материал, который образуется при переохлаждении жидкости, называется стеклом. Стекло можно определить и как продукт плавления, перешедший при охлаждении в твердое состояние без кристаллизации. Аморфное состояние вещества является термодинамически нестабильным и при благоприятных условиях переходит в кристаллическое.


