 Строение вещества
Строение вещества
 Строение жидкости и твёрдого тела • В зависимости от условий (температура, давление) химические вещества могут быть в различных агрегатных состояниях. • Различают газообразное, жидкое, твёрдое и плазменное состояния веществ. • Эти агрегатные состояния, кроме плазменного, отличаются друг от друга величиной и природой сил, действующих между частицами.
Строение жидкости и твёрдого тела • В зависимости от условий (температура, давление) химические вещества могут быть в различных агрегатных состояниях. • Различают газообразное, жидкое, твёрдое и плазменное состояния веществ. • Эти агрегатные состояния, кроме плазменного, отличаются друг от друга величиной и природой сил, действующих между частицами.
 • Если вещество состоит из атомов неметаллических элементов, то его атомы связаны друг с другом ковалентной связью. • Если вещество состоит из атомов металлических элементов /металлы/, то его атомы связаны металлической связью. • Если вещество имеет ионное строение, то образующие его ионы удерживаются силами электростатического притяжения – ионная связь
• Если вещество состоит из атомов неметаллических элементов, то его атомы связаны друг с другом ковалентной связью. • Если вещество состоит из атомов металлических элементов /металлы/, то его атомы связаны металлической связью. • Если вещество имеет ионное строение, то образующие его ионы удерживаются силами электростатического притяжения – ионная связь
 • В веществах с молекулярной структурой между молекулами, независимо от того, являются они полярными или нет, возникает межмолекулярное взаимодействие за счет сил Ван-дер-Ваальса • Это слабые взаимодействия между нейтральными молекулами за счет дипольного взаимодействия у полярных молекул и наведённых временных диполей у неполярных молекул.
• В веществах с молекулярной структурой между молекулами, независимо от того, являются они полярными или нет, возникает межмолекулярное взаимодействие за счет сил Ван-дер-Ваальса • Это слабые взаимодействия между нейтральными молекулами за счет дипольного взаимодействия у полярных молекул и наведённых временных диполей у неполярных молекул.
 • Эти связи характеризуются отсутствием насыщенности и направленности. • Однако они проявляются на больших расстояниях. • К межмолекулярным силам относится водородная связь – связь, образуемая атомом водорода, находящемся между двумя атомами с высокой электроотрицательностью (фтор, кислород, азот). Например вещество вода в жидком состоянии.
• Эти связи характеризуются отсутствием насыщенности и направленности. • Однако они проявляются на больших расстояниях. • К межмолекулярным силам относится водородная связь – связь, образуемая атомом водорода, находящемся между двумя атомами с высокой электроотрицательностью (фтор, кислород, азот). Например вещество вода в жидком состоянии.
 В молекуле воды электронная пара связи О-Н смещена к атому кислорода ( электроотрицательность О=3, 5; Н=2, 1) Атом водорода поляризован положительно /несёт частичный положительный заряд/, а атом кислорода – отрицательно /несет частичный отрицательный/. • Между частично заряженным /положительно поляризованным/ атомом водорода одной молекулы и отрицательно поляризованным атомом кислорода второй молекулы возникает водородная связь
В молекуле воды электронная пара связи О-Н смещена к атому кислорода ( электроотрицательность О=3, 5; Н=2, 1) Атом водорода поляризован положительно /несёт частичный положительный заряд/, а атом кислорода – отрицательно /несет частичный отрицательный/. • Между частично заряженным /положительно поляризованным/ атомом водорода одной молекулы и отрицательно поляризованным атомом кислорода второй молекулы возникает водородная связь
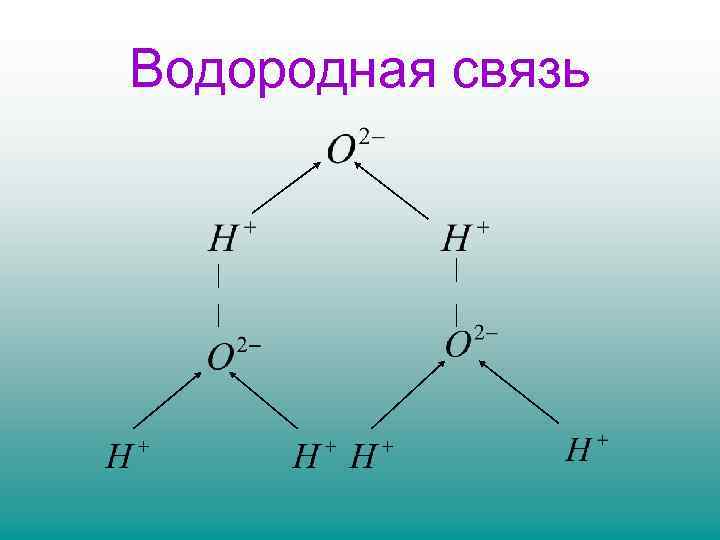 Водородная связь
Водородная связь
 Твёрдые тела Могут быть в кристаллической и аморфной форме. Классификация кристаллических соединений:
Твёрдые тела Могут быть в кристаллической и аморфной форме. Классификация кристаллических соединений:
 1. По типу химической связи: а) металлические б) ионные в) ковалентные г) межмолекулярные д) тетрагональные е) ромбовидные
1. По типу химической связи: а) металлические б) ионные в) ковалентные г) межмолекулярные д) тетрагональные е) ромбовидные
 2. По симметрии кристаллов: а) кубический б) гексагональные в) тетрагональные г) ромбовидные
2. По симметрии кристаллов: а) кубический б) гексагональные в) тетрагональные г) ромбовидные
 Аморфное состояние • Характеризуется отсутствием упорядоченности структуры, не имеет определённой температуры плавления. • Твёрдое аморфное состояние можно рассматривать как переохлаждённую жидкость, обладающую текучестью. • Типичным примером может служить стекло.
Аморфное состояние • Характеризуется отсутствием упорядоченности структуры, не имеет определённой температуры плавления. • Твёрдое аморфное состояние можно рассматривать как переохлаждённую жидкость, обладающую текучестью. • Типичным примером может служить стекло.