строение вещества.ppt
- Количество слайдов: 35
 СТРОЕНИЕ ВЕЩЕСТВА СТРОЕНИЕ АТОМА И ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Литература Коровин Н. В. Общая химия. ─ Высш. шк. , 2000. 558 с. Гл. первая, §§ 1. 1 -1. 5 https: //yadi. sk/d/i. K 3 e. IO 3 kkvv. Hj Страничка «в контакте» https: //vk. com/public 131559854 Адрес электронной почты lgkkn@rambler. ru
СТРОЕНИЕ ВЕЩЕСТВА СТРОЕНИЕ АТОМА И ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Литература Коровин Н. В. Общая химия. ─ Высш. шк. , 2000. 558 с. Гл. первая, §§ 1. 1 -1. 5 https: //yadi. sk/d/i. K 3 e. IO 3 kkvv. Hj Страничка «в контакте» https: //vk. com/public 131559854 Адрес электронной почты lgkkn@rambler. ru
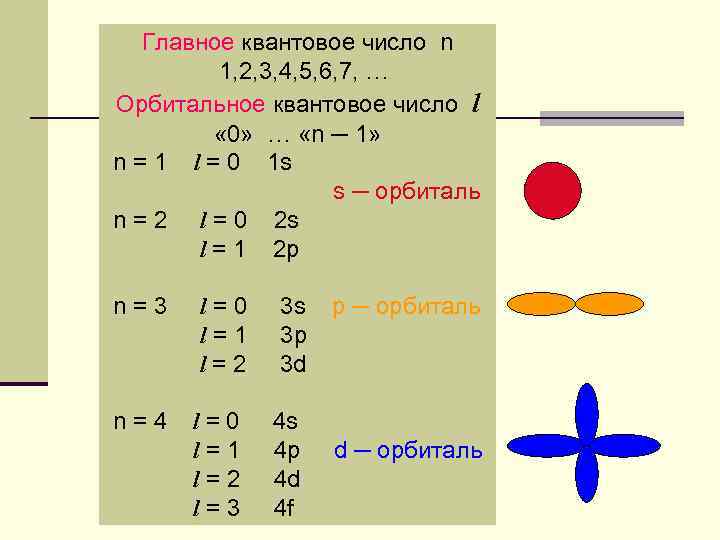 Главное квантовое число n 1, 2, 3, 4, 5, 6, 7, … Орбитальное квантовое число l « 0» … «n ─ 1» n = 1 l = 0 1 s s ─ орбиталь n = 2 l = 0 2 s l = 1 2 p n=3 l=0 l=1 l=2 3 s 3 p 3 d n=4 l=0 l=1 l=2 l=3 4 s 4 p 4 d 4 f p ─ орбиталь d ─ орбиталь
Главное квантовое число n 1, 2, 3, 4, 5, 6, 7, … Орбитальное квантовое число l « 0» … «n ─ 1» n = 1 l = 0 1 s s ─ орбиталь n = 2 l = 0 2 s l = 1 2 p n=3 l=0 l=1 l=2 3 s 3 p 3 d n=4 l=0 l=1 l=2 l=3 4 s 4 p 4 d 4 f p ─ орбиталь d ─ орбиталь
 Магнитное квантовое число –l, …, 0, …, + l; N(ml) = (2 l + 1) = N(AO) l = 0 ml = 0 l = 1 ml = ─ 1; 0; +1 l = 2 ml = ─ 2; ─ 1; 0; +1; +2 l = 3 ml = ─ 3; ─ 2; ─ 1; 0; +1; +2; +3 s-орбиталь р -орбиталь d -орбиталь Спиновое квантовое число ms = + ½; ─ ½
Магнитное квантовое число –l, …, 0, …, + l; N(ml) = (2 l + 1) = N(AO) l = 0 ml = 0 l = 1 ml = ─ 1; 0; +1 l = 2 ml = ─ 2; ─ 1; 0; +1; +2 l = 3 ml = ─ 3; ─ 2; ─ 1; 0; +1; +2; +3 s-орбиталь р -орбиталь d -орбиталь Спиновое квантовое число ms = + ½; ─ ½
 Принцип Паули. В атоме не может быть двух электронов, имеющих одинаковый набор квантовых чисел АО 1 s: n=1 l =0 ms= –½; +½ AO 3 p: n=3 l =1 ml = – 1; 0; +1 ms= –½; +½ На одной АО максимально может быть только два электрона 2 (2 l + 1) s-орбиталь: 2 электрона р-орбиталь: 6 электронов d-орбиталь: 10 электронов f-орбиталь: 14 электронов
Принцип Паули. В атоме не может быть двух электронов, имеющих одинаковый набор квантовых чисел АО 1 s: n=1 l =0 ms= –½; +½ AO 3 p: n=3 l =1 ml = – 1; 0; +1 ms= –½; +½ На одной АО максимально может быть только два электрона 2 (2 l + 1) s-орбиталь: 2 электрона р-орбиталь: 6 электронов d-орбиталь: 10 электронов f-орбиталь: 14 электронов
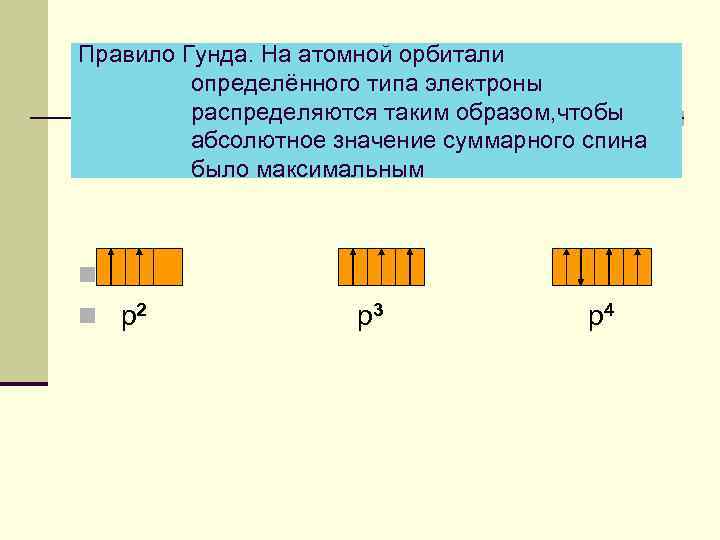 Правило Гунда. На атомной орбитали определённого типа электроны распределяются таким образом, чтобы абсолютное значение суммарного спина было максимальным n n р2 р3 р4
Правило Гунда. На атомной орбитали определённого типа электроны распределяются таким образом, чтобы абсолютное значение суммарного спина было максимальным n n р2 р3 р4
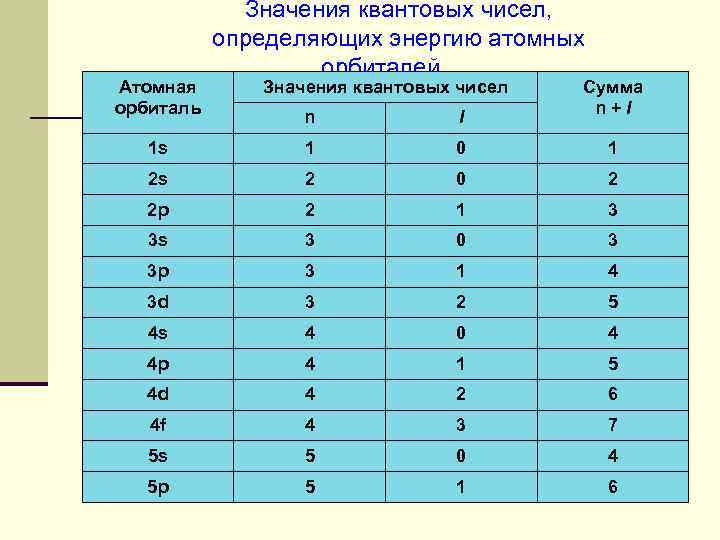 Атомная орбиталь Значения квантовых чисел, определяющих энергию атомных орбиталей Значения квантовых чисел Cумма n+l n l 1 s 1 0 1 2 s 2 0 2 2 p 2 1 3 3 s 3 0 3 3 p 3 1 4 3 d 3 2 5 4 s 4 0 4 4 p 4 1 5 4 d 4 2 6 4 f 4 3 7 5 s 5 0 4 5 p 5 1 6
Атомная орбиталь Значения квантовых чисел, определяющих энергию атомных орбиталей Значения квантовых чисел Cумма n+l n l 1 s 1 0 1 2 s 2 0 2 2 p 2 1 3 3 s 3 0 3 3 p 3 1 4 3 d 3 2 5 4 s 4 0 4 4 p 4 1 5 4 d 4 2 6 4 f 4 3 7 5 s 5 0 4 5 p 5 1 6
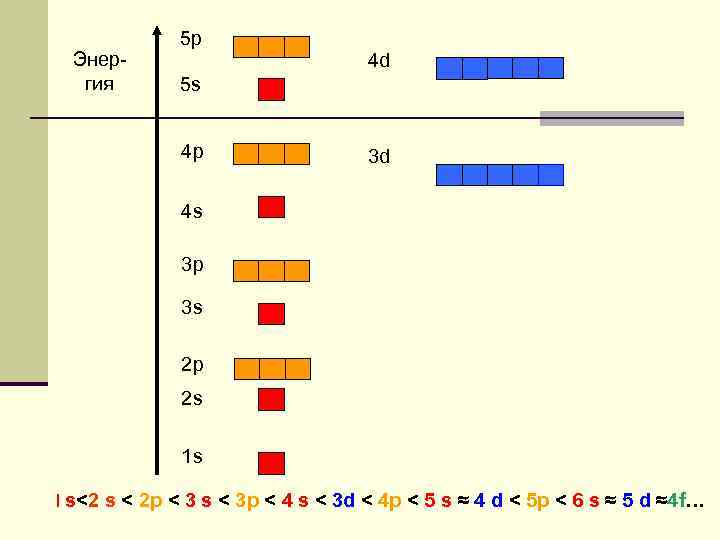 Энергия 5 p 4 d 5 s 4 p 3 d 4 s 3 p 3 s 2 p 2 s 1 s l s<2 s < 2 р < 3 s < 3 р < 4 s < 3 d < 4 р < 5 s ≈ 4 d < 5 р < 6 s ≈ 5 d ≈4 f…
Энергия 5 p 4 d 5 s 4 p 3 d 4 s 3 p 3 s 2 p 2 s 1 s l s<2 s < 2 р < 3 s < 3 р < 4 s < 3 d < 4 р < 5 s ≈ 4 d < 5 р < 6 s ≈ 5 d ≈4 f…
 Электронные формулы и распределение валентных электронов s 1 Н 1 s 1 2 He 1 s 2 3 Li 1 s 22 s 1 n=1 s n=1 n=2 s p 10 Ne 1 s 22 p 6 n=2 s p s 6 C 1 s 22 p 2 p n=2 s 21 Sc 1 s 22 p 63 s 23 p 63 d 14 s 2 p n=4 n=3 d
Электронные формулы и распределение валентных электронов s 1 Н 1 s 1 2 He 1 s 2 3 Li 1 s 22 s 1 n=1 s n=1 n=2 s p 10 Ne 1 s 22 p 6 n=2 s p s 6 C 1 s 22 p 2 p n=2 s 21 Sc 1 s 22 p 63 s 23 p 63 d 14 s 2 p n=4 n=3 d
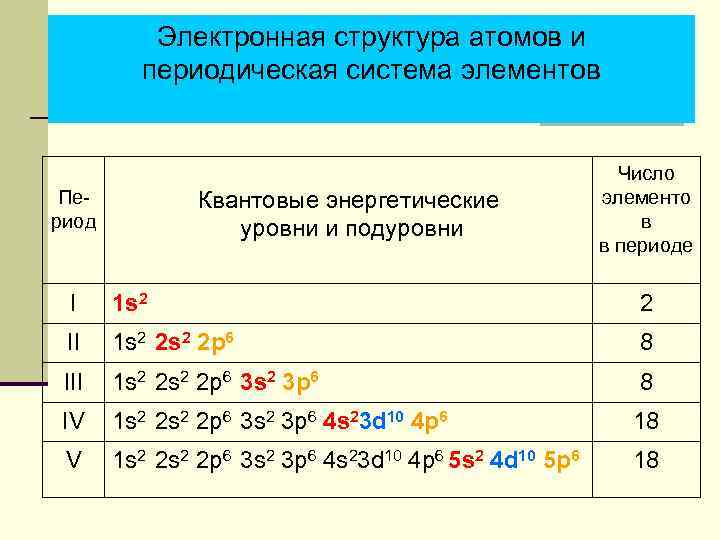 Электронная структура атомов и периодическая система элементов Период Квантовые энергетические уровни и подуровни Число элементо в в периоде I 1 s 2 2 II 1 s 2 2 p 6 8 III 1 s 2 2 p 6 3 s 2 3 p 6 8 IV 1 s 2 2 p 6 3 s 2 3 p 6 4 s 23 d 10 4 p 6 18 V 1 s 2 2 p 6 3 s 2 3 p 6 4 s 23 d 10 4 p 6 5 s 2 4 d 10 5 p 6 18
Электронная структура атомов и периодическая система элементов Период Квантовые энергетические уровни и подуровни Число элементо в в периоде I 1 s 2 2 II 1 s 2 2 p 6 8 III 1 s 2 2 p 6 3 s 2 3 p 6 8 IV 1 s 2 2 p 6 3 s 2 3 p 6 4 s 23 d 10 4 p 6 18 V 1 s 2 2 p 6 3 s 2 3 p 6 4 s 23 d 10 4 p 6 5 s 2 4 d 10 5 p 6 18
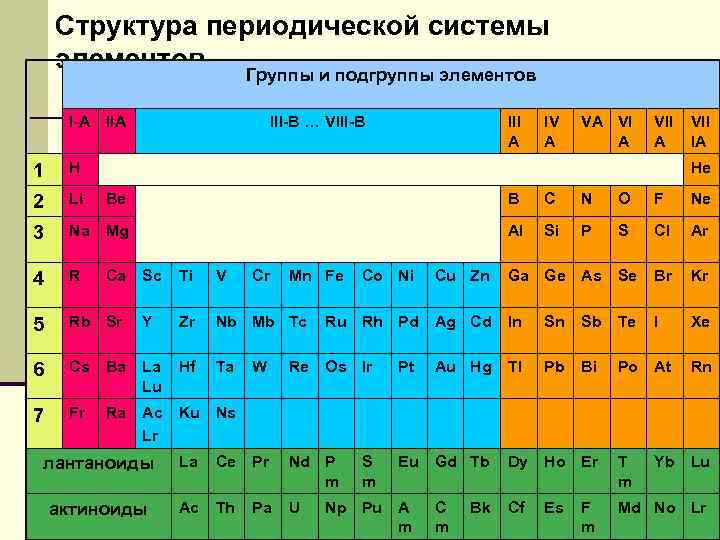 Структура периодической системы элементов Группы и подгруппы элементов I-A III-B … VIII-B III A IV A VA VII IA 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 R Ca 5 Sc Ti V Rb Sr Y Zr 6 Cs Ba La Lu Hf 7 Fr Ra Ac Lr Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Nb Mb Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe Ta Os Ir Pt Au Hg Tl Pb Bi Po At Rn Ku Ns Eu Gd Tb Dy Ho Er T m Yb Lu A m Cf Es Md No Lr W Re лантанoиды La Ce Pr Nd P m актиноиды Ac Th Pa U S m Np Pu Bk F m
Структура периодической системы элементов Группы и подгруппы элементов I-A III-B … VIII-B III A IV A VA VII IA 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 R Ca 5 Sc Ti V Rb Sr Y Zr 6 Cs Ba La Lu Hf 7 Fr Ra Ac Lr Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Nb Mb Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe Ta Os Ir Pt Au Hg Tl Pb Bi Po At Rn Ku Ns Eu Gd Tb Dy Ho Er T m Yb Lu A m Cf Es Md No Lr W Re лантанoиды La Ce Pr Nd P m актиноиды Ac Th Pa U S m Np Pu Bk F m
 Изменение энергии ионизации и сродства к электрону в периодах и группах периодической системы Энергия ионизации ─ I Сродство к электрону ─ E F Li неметаллы E I металлы Cs I E At
Изменение энергии ионизации и сродства к электрону в периодах и группах периодической системы Энергия ионизации ─ I Сродство к электрону ─ E F Li неметаллы E I металлы Cs I E At
 Металлы и неметаллы в периодической системе Группы и подгруппы элементов I-A III-B … VIII-B III A IV A VA VII IA 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 R Ca 5 Sc Ti V Rb Sr Y Zr 6 Cs Ba La Lu Hf 7 Fr Ra Ac Lr Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Nb Mb Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe Ta Os Ir Pt Au Hg Tl Pb Bi Po At Rn Ku Ns Eu Gd Tb Dy Ho Er T m Yb Lu A m Cf Es Md No Lr W Re лантанoиды La Ce Pr Nd P m актиноиды Ac Th Pa U S m Np Pu Bk F m
Металлы и неметаллы в периодической системе Группы и подгруппы элементов I-A III-B … VIII-B III A IV A VA VII IA 1 H He 2 Li Be B C N O F Ne 3 Na Mg Al Si P S Cl Ar 4 R Ca 5 Sc Ti V Rb Sr Y Zr 6 Cs Ba La Lu Hf 7 Fr Ra Ac Lr Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Nb Mb Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe Ta Os Ir Pt Au Hg Tl Pb Bi Po At Rn Ku Ns Eu Gd Tb Dy Ho Er T m Yb Lu A m Cf Es Md No Lr W Re лантанoиды La Ce Pr Nd P m актиноиды Ac Th Pa U S m Np Pu Bk F m
 Кислотно-основные свойства соединений элементов третьего периода I Na II Mg III Al металлы Na 2 O Mg. O основные Na. OH Mg(OH)2 основания Al 2 O 3 амфотерный Al(OH)3 IV Si V P S VII Cl немталлы Si. O 2 P 2 O 5 SO 3 Cl 2 O 7 кислотные H 2 Si. O 3 H 3 PO 4 H 2 SO 4 амфотерный гидроксид Усиление основных свойств Усиление VI кислоты кислотных свойств HCl. O 4
Кислотно-основные свойства соединений элементов третьего периода I Na II Mg III Al металлы Na 2 O Mg. O основные Na. OH Mg(OH)2 основания Al 2 O 3 амфотерный Al(OH)3 IV Si V P S VII Cl немталлы Si. O 2 P 2 O 5 SO 3 Cl 2 O 7 кислотные H 2 Si. O 3 H 3 PO 4 H 2 SO 4 амфотерный гидроксид Усиление основных свойств Усиление VI кислоты кислотных свойств HCl. O 4
 Химическая связь Литература Коровин Н. В. Общая химия. – М. : Высш. шк. , 2000. ─ 558 с. §§ 2. 1 -2. 4
Химическая связь Литература Коровин Н. В. Общая химия. – М. : Высш. шк. , 2000. ─ 558 с. §§ 2. 1 -2. 4
 Энергия системы из двух сближающихся атомов водорода Эн ерги я Отталкивание ↑↑ r o = 0, 074 нм ↑↓ Притяжение Расстояние между ядрами
Энергия системы из двух сближающихся атомов водорода Эн ерги я Отталкивание ↑↑ r o = 0, 074 нм ↑↓ Притяжение Расстояние между ядрами
 Схема перекрывания электронных облаков при образовании молекулы водорода Н + ↑ 0, 053 нм Н → ↓ Н 2 ↓↑ 0, 074 нм
Схема перекрывания электронных облаков при образовании молекулы водорода Н + ↑ 0, 053 нм Н → ↓ Н 2 ↓↑ 0, 074 нм
 Обменный механизм образования химической связи в молекуле азота N 1 s 22 p 3 7 s p AO N n=2 N 2
Обменный механизм образования химической связи в молекуле азота N 1 s 22 p 3 7 s p AO N n=2 N 2
 Валентность элементов в основном (В) и в возбуждённом состоянии (В )٭ Элемент Основное состояние 2 s В 2 p Возбуждённое состояние 2 s В ٭ 2 p Li ↑ 1 Be ↑↓ 0 ↑ ↑ B ↑↓ ↑ 1 ↑ ↑ ↑ C ↑↓ ↑ ↑ 2 ↑ ↑ 4 N ↑↓ ↑ ↑ ↑ 3 O ↑↓ ↑↓ ↑ ↑ 2 F ↑↓ ↑↓ ↑↓ ↑ 1 Ne ↑↓ ↑↓ 0 2 3
Валентность элементов в основном (В) и в возбуждённом состоянии (В )٭ Элемент Основное состояние 2 s В 2 p Возбуждённое состояние 2 s В ٭ 2 p Li ↑ 1 Be ↑↓ 0 ↑ ↑ B ↑↓ ↑ 1 ↑ ↑ ↑ C ↑↓ ↑ ↑ 2 ↑ ↑ 4 N ↑↓ ↑ ↑ ↑ 3 O ↑↓ ↑↓ ↑ ↑ 2 F ↑↓ ↑↓ ↑↓ ↑ 1 Ne ↑↓ ↑↓ 0 2 3
 Обменный механизм образования химической связи в молекуле SO 2 2 s 2 p O ٭ 3 s S ٭ O ٭ 3 p 3 d
Обменный механизм образования химической связи в молекуле SO 2 2 s 2 p O ٭ 3 s S ٭ O ٭ 3 p 3 d
![Донорно-акцепторный механизм образования ковалентной связи в ионе [NH 4]+ H H N H + Донорно-акцепторный механизм образования ковалентной связи в ионе [NH 4]+ H H N H +](https://present5.com/presentation/35230225_450581119/image-20.jpg) Донорно-акцепторный механизм образования ковалентной связи в ионе [NH 4]+ H H N H + H+ → H H N N H H+ + H
Донорно-акцепторный механизм образования ковалентной связи в ионе [NH 4]+ H H N H + H+ → H H N N H H+ + H
 Перекрывание атомных орбиталей при образовании σ- и π-связей σ – связь π – связь
Перекрывание атомных орбиталей при образовании σ- и π-связей σ – связь π – связь
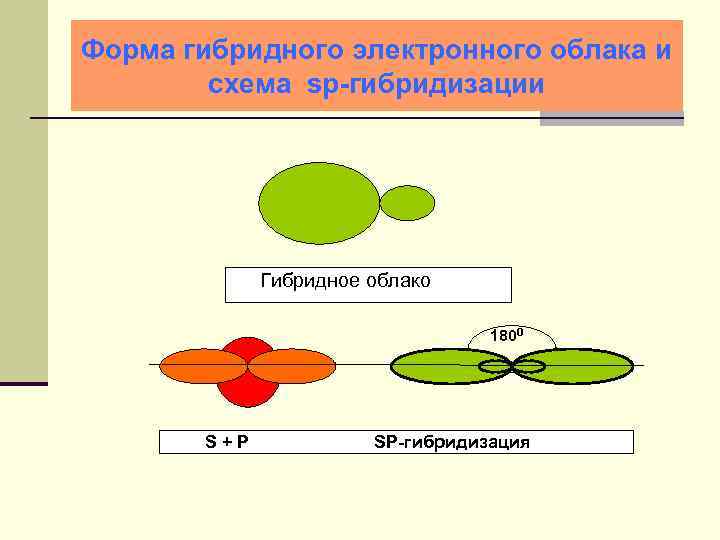 Форма гибридного электронного облака и схема sp-гибридизации Гибридное облако 1800 S+P SP-гибридизация
Форма гибридного электронного облака и схема sp-гибридизации Гибридное облако 1800 S+P SP-гибридизация
 Пространственная конфигурация молекулы Be. Cl 2 Be 1 s 22 s 2 4 s p s n=2 p Be* s 17 Cl Cl 1 s 22 p 63 s 23 p 5 Be p n=3 Cl
Пространственная конфигурация молекулы Be. Cl 2 Be 1 s 22 s 2 4 s p s n=2 p Be* s 17 Cl Cl 1 s 22 p 63 s 23 p 5 Be p n=3 Cl
 Схемы sp 2 - и sp 3 -гибридизации 1200 S + 2 P SP 2 -гибридизация 1090 S + 3 P SP 3 -гибридизация
Схемы sp 2 - и sp 3 -гибридизации 1200 S + 2 P SP 2 -гибридизация 1090 S + 3 P SP 3 -гибридизация
 Пространственная конфигурация некоторых соединений Тип гибридизации центрального атома Конфигурация Валентный молекулы угол связи Примеры соединений sp Линейная 180 0 Zn. Cl 2, Ca. Cl 2, Be. Cl 2, CO 2 sp 2 Плоская тригональна я 120 0 BCl 3, CO 32‾, Al. F 3 sp 3 Тетраэдр 109 0 28 ′ CH 4, NH 3, H 2 O, Si. H 4
Пространственная конфигурация некоторых соединений Тип гибридизации центрального атома Конфигурация Валентный молекулы угол связи Примеры соединений sp Линейная 180 0 Zn. Cl 2, Ca. Cl 2, Be. Cl 2, CO 2 sp 2 Плоская тригональна я 120 0 BCl 3, CO 32‾, Al. F 3 sp 3 Тетраэдр 109 0 28 ′ CH 4, NH 3, H 2 O, Si. H 4
 Диполь молекулы хлороводорода +0, 17 - 0, 17 H Cl l μ = q×l
Диполь молекулы хлороводорода +0, 17 - 0, 17 H Cl l μ = q×l
 Относительная электроотрицательность атомов Период Группы 1 2 3 4 5 6 7 I H 2, 10 II Li 0, 98 Be 1, 50 B 2, 00 C 2, 50 N 3, 07 O 3, 50 F 4, 00 III Na 0, 93 Mg 1, 20 Al 1, 60 Si 1, 80 P 2, 20 S 2, 60 Cl 3, 00 IV K 0, 91 Ca 1, 04 Ga 1, 80 Ge 1, 80 As 2, 10 Se 2, 50 Br 2, 80 V Rb 0, 89 Sr 0, 99 In 1, 50 Sn 1, 80 Sb 1, 80 Te 2, 10 J 2, 60
Относительная электроотрицательность атомов Период Группы 1 2 3 4 5 6 7 I H 2, 10 II Li 0, 98 Be 1, 50 B 2, 00 C 2, 50 N 3, 07 O 3, 50 F 4, 00 III Na 0, 93 Mg 1, 20 Al 1, 60 Si 1, 80 P 2, 20 S 2, 60 Cl 3, 00 IV K 0, 91 Ca 1, 04 Ga 1, 80 Ge 1, 80 As 2, 10 Se 2, 50 Br 2, 80 V Rb 0, 89 Sr 0, 99 In 1, 50 Sn 1, 80 Sb 1, 80 Te 2, 10 J 2, 60
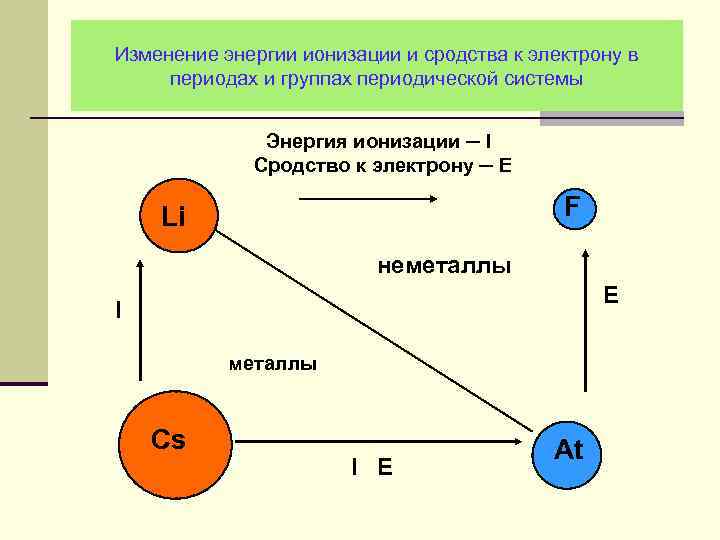 Изменение энергии ионизации и сродства к электрону в периодах и группах периодической системы Энергия ионизации ─ I Сродство к электрону ─ E F Li неметаллы E I металлы Cs I E At
Изменение энергии ионизации и сродства к электрону в периодах и группах периодической системы Энергия ионизации ─ I Сродство к электрону ─ E F Li неметаллы E I металлы Cs I E At
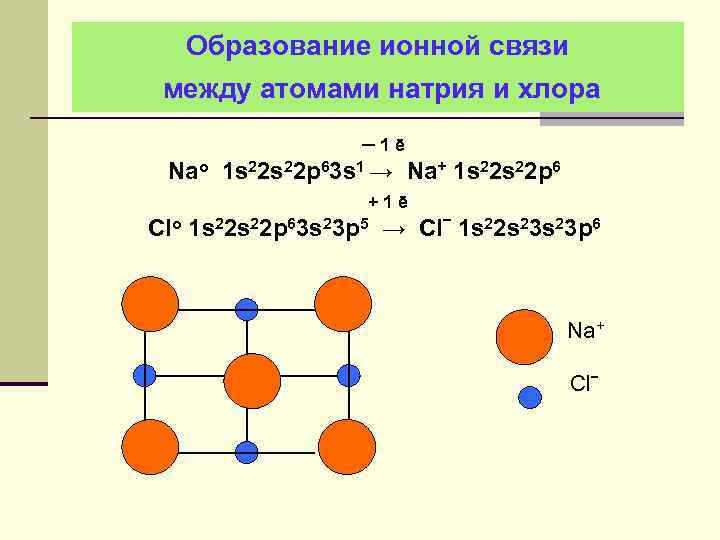 Образование ионной связи между атомами натрия и хлора ─1ē Nao 1 s 22 p 63 s 1 → Na+ 1 s 22 p 6 +1ē Clo 1 s 22 p 63 s 23 p 5 → Clˉ 1 s 22 s 23 p 6 Na+ Clˉ
Образование ионной связи между атомами натрия и хлора ─1ē Nao 1 s 22 p 63 s 1 → Na+ 1 s 22 p 6 +1ē Clo 1 s 22 p 63 s 23 p 5 → Clˉ 1 s 22 s 23 p 6 Na+ Clˉ
 Степень ионности связи в зависимости от разности электроотрицательности атомов элементов Разность ЭО Степень ионности, % 0, 2 1 1, 8 55 0, 4 4 2, 0 63 0, 6 9 2, 2 70 0, 8 15 2, 4 76 1, 0 22 2, 6 82 1, 2 30 2, 8 86 1, 4 39 3, 0 89 1, 6 47 3, 2 92
Степень ионности связи в зависимости от разности электроотрицательности атомов элементов Разность ЭО Степень ионности, % 0, 2 1 1, 8 55 0, 4 4 2, 0 63 0, 6 9 2, 2 70 0, 8 15 2, 4 76 1, 0 22 2, 6 82 1, 2 30 2, 8 86 1, 4 39 3, 0 89 1, 6 47 3, 2 92
 Линейная комбинация АО (метод ЛКАО) ψАВ = аψА ± bψ В ψАВ ─ волновая функция электрона в молекуле ψА, ψВ ─ волновая функция атомов «А» и «В» а, b ─ коэффициенты, учитывающие долю каждой АО в образовании МО
Линейная комбинация АО (метод ЛКАО) ψАВ = аψА ± bψ В ψАВ ─ волновая функция электрона в молекуле ψА, ψВ ─ волновая функция атомов «А» и «В» а, b ─ коэффициенты, учитывающие долю каждой АО в образовании МО
 Схема энергетических уровней атомных и молекулярных орбиталей МО* (разрыхляющая) АО АО МО (связывающая)
Схема энергетических уровней атомных и молекулярных орбиталей МО* (разрыхляющая) АО АО МО (связывающая)
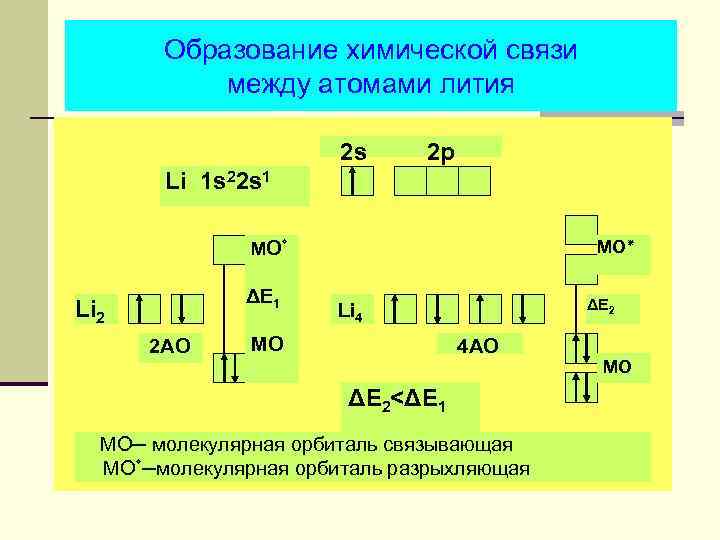 Образование химической связи между атомами лития 2 s 2 p Li 1 s 22 s 1 MO ٭ МO ٭ ΔE 1 Li 2 2 AO ΔE 2 Li 4 MO 4 AO ΔE 2<ΔE 1 МО─ молекулярная орбиталь связывающая МО ─٭ молекулярная орбиталь разрыхляющая MO
Образование химической связи между атомами лития 2 s 2 p Li 1 s 22 s 1 MO ٭ МO ٭ ΔE 1 Li 2 2 AO ΔE 2 Li 4 MO 4 AO ΔE 2<ΔE 1 МО─ молекулярная орбиталь связывающая МО ─٭ молекулярная орбиталь разрыхляющая MO
 Схема образования металлической связи МО ٭ МО 10 23 АО ē ē Незаполненные МО Заполненные МО 10 23 МО + + Схема кристаллической решётки металла + + ─ атом металла + ─ ион металла ─ электрон
Схема образования металлической связи МО ٭ МО 10 23 АО ē ē Незаполненные МО Заполненные МО 10 23 МО + + Схема кристаллической решётки металла + + ─ атом металла + ─ ион металла ─ электрон
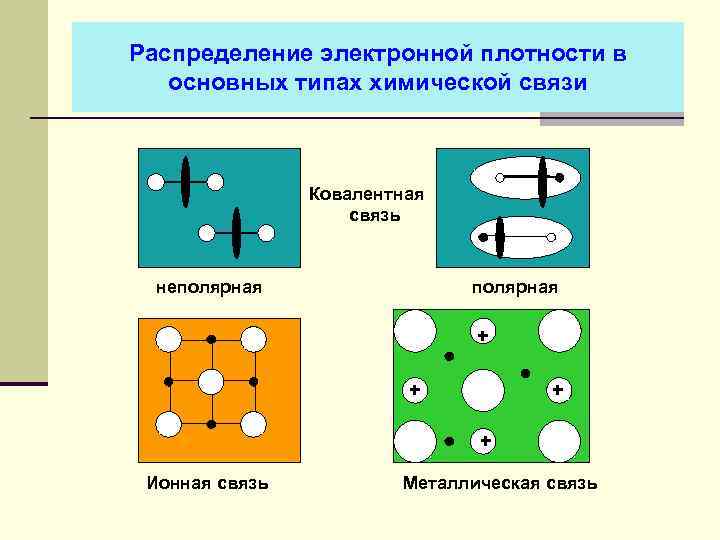 Распределение электронной плотности в основных типах химической связи Ковалентная связь неполярная + + Ионная связь Металлическая связь
Распределение электронной плотности в основных типах химической связи Ковалентная связь неполярная + + Ионная связь Металлическая связь


