Строение, свойства и функции белков..pptx
- Количество слайдов: 49

Строение, свойства и функции белков

Биохимия – наука фундаментальная, биологическая. Развитие биологии и медицины невозможно без применения методов и принципов современной биологической химии. • Биохимия изучает химические основы жизнедеятельности организмов в норме и при патологии. • Биохимия устанавливает связь между молекулярной структурой и биологической функцией химических компонентов живой материи • Изучает биогенез главных классов органических веществ в организме

• Белки – это полимерные молекулы, мономерами которых являются всего 20 α – аминокислот • Набор и порядок соединения аминокислот в белке определяется строением генов в ДНК индивидуумов • Каждый белок в соответствии с его специфической структурой выполняет свойственную ему функцию • Набор белков данного организма определяет его фенотипические особенности, а также наличие наследственных болезней или предрасположенность к их развитию

Особенности белков, определяющие жизнедеятельность живых организмов • Бесконечное разнообразие структуры и вместе с тем высокая видовая специфичность (предопределяет многообразие организмов, выживаемость); • Крайнее многообразие физических и химических превращений (многообразие функций); • Способность к внутримолекулярным взаимодействиям; • Способность отвечать на внешнее воздействие закономерным изменением конфигурации с последующим восстановлением структуры (приспособляемость); • Склонность к взаимодействию с другими химическими соединениями и образованию надмолекулярных комплексов и структур; • Наличие биокаталитических свойств.
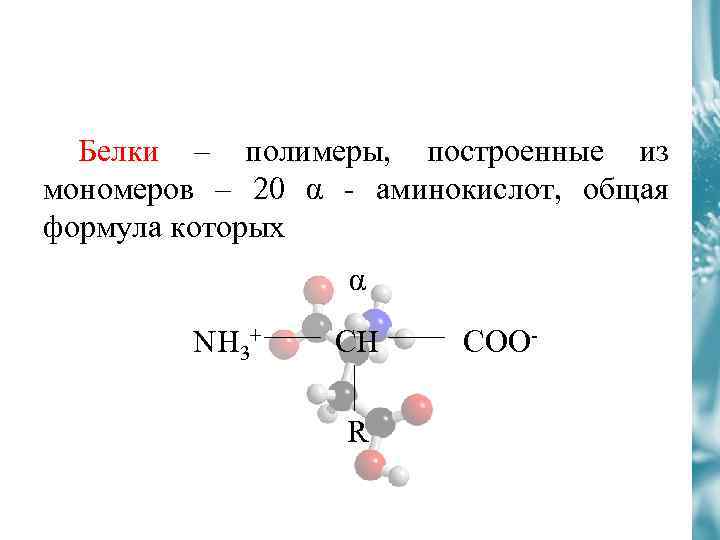
Белки – полимеры, построенные из мономеров – 20 α - аминокислот, общая формула которых α NH 3+ CH R COO-

• Аминокислоты различаются по строению, размерами, физико-химическими свойствами радикалов, присоединенных к α-углеродному атому • Функциональные группы аминокислоты определяют особенности свойств разных αаминокислот • Встречающиеся в α-аминокислотых радикалы можно разделить на несколько групп: • - анионные группы – СОО • - катионные группы – NH 3+, =NH+, NH 2 -C=NH+; • - полярные незаря- – OH, – CO – NH 2, – SH; • женные группы • - неполярные группы – СН 3, алифатические цепи, ароматические циклы.
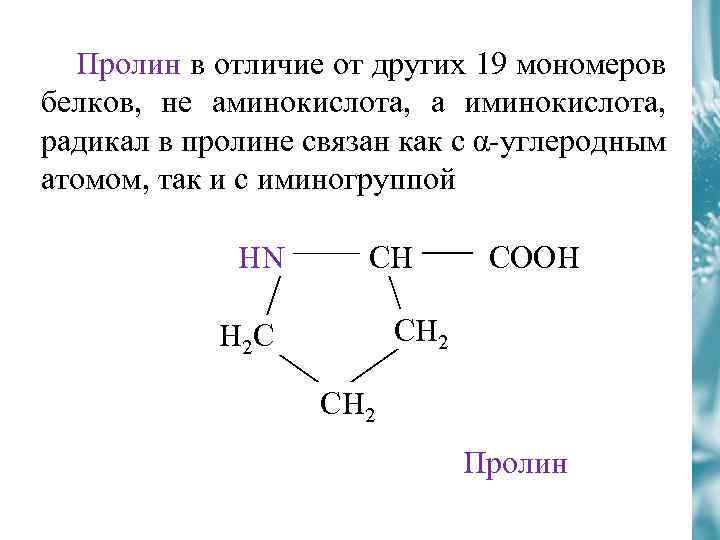
Пролин в отличие от других 19 мономеров белков, не аминокислота, а иминокислота, радикал в пролине связан как с α-углеродным атомом, так и с иминогруппой HN CH CООH CH 2 H 2 C CH 2 Пролин

1. Аминокислоты различают по растворимости в воде. Это связано со способностью радикалов взаимодействовать с водой (гидратироваться) 2. К гидрофильным относятся радикалы, содержащие анионные, катионные и полярные незаряженные функциональные группы 3. К гидрофобным относятся радикалы, содержащие метильные группы, алифатические цепи или циклы.
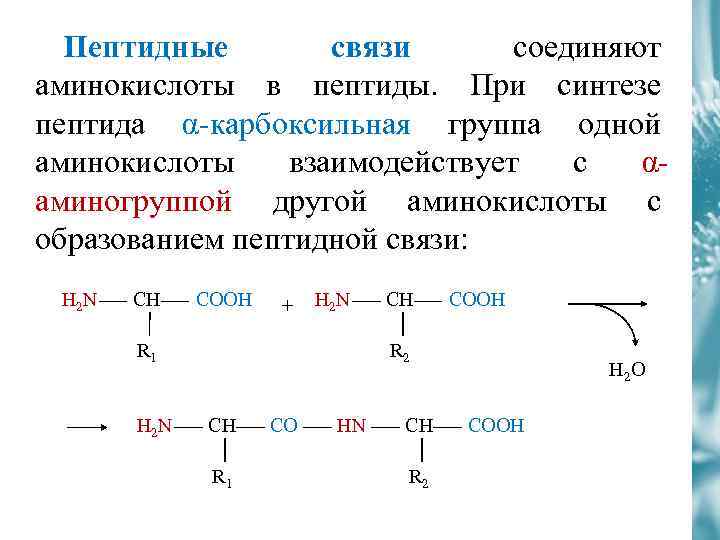
Пептидные связи соединяют аминокислоты в пептиды. При синтезе пептида α-карбоксильная группа одной аминокислоты взаимодействует с αаминогруппой другой аминокислоты с образованием пептидной связи: H 2 N СH COOH + H 2 N R 1 H 2 N СH COOH R 2 СH R 1 CO HN СH R 2 H 2 O COOH
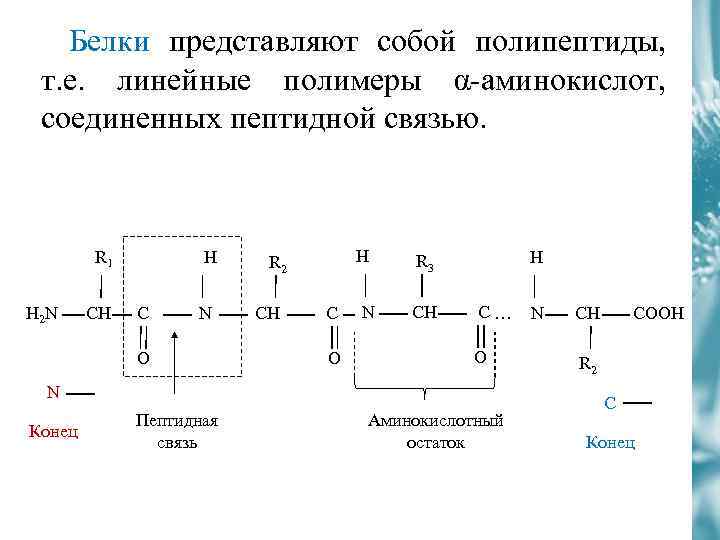
Белки представляют собой полипептиды, т. е. линейные полимеры α-аминокислот, соединенных пептидной связью. R 1 H 2 N СH H C N O H R 2 СH C O N H R 3 СH C… O N Конец Пептидная связь Аминокислотный остаток N СH COOH R 2 С Конец

Цепь повторяющихся групп – NH – CO – образует полипептидный остов. В каждом белке или пептиде можно выделить: • N-конец - имеющий свободную αаминогруппу (-NН 2); • С-конец - имеющий свободную карбоксильную группу(-СООН). Пептиды записывают и читают с Nконца к C-концу.
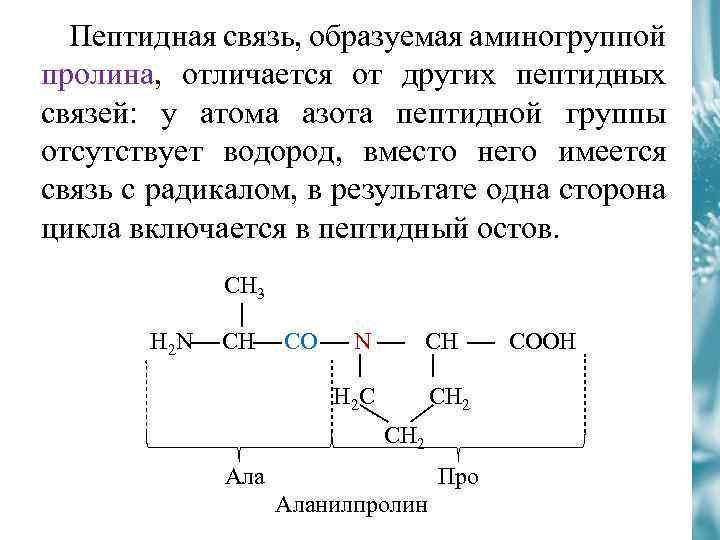
Пептидная связь, образуемая аминогруппой пролина, отличается от других пептидных связей: у атома азота пептидной группы отсутствует водород, вместо него имеется связь с радикалом, в результате одна сторона цикла включается в пептидный остов. CH 3 H 2 N СH CO N СH H 2 C CH 2 Ала Про Аланилпролин COOH

Первичная структура белков. 1. Аминокислотные остатки в пептидных цепях разных белков чередуются не случайным образом, а расположены в определенном порядке. 2. Линейная последовательность или порядок чередования аминокислотных остатков в полипептидной цепи называется первичная структура белка.

Свойства первичной структуры белка 1. Детерминированность – последовательность аминокислот в белке генетически закодирована. Информация об аминокислотной последовательности содержится в ДНК. 2. Уникальность – для каждого белка в организме характерна своя определенная последовательность аминокислот. 3. Универсальность – белки выполняющие одинаковые функции, в различных организмах имеют одинаковую или сходную первичную структуру. 4. В природных белках одна и та же аминокислота не встречается подряд более 3 раз.

Уровни организации белковой молекулы • Первичная структура определена генетически, но точность воспроизведения не абсолютна; • Замена аминокислот в полипептидной цепи со сходными по структуре и физико-химическим свойствам не приводит к изменениям функции белковой молекулы или функция изменяется незначительно (взаимозаменяемые аминокислоты: глу -асп, гли-ала, лей-илей, консервативная, нерадикальная замена); • Замена аминокислот в полипептидной цепи с различными по структуре и физико-химическим свойствам приводит к резким изменениям функции белковой молекулы (невзаимозаменяемые аминокислоты: глу-вал, асп-фен, радикальная замена).
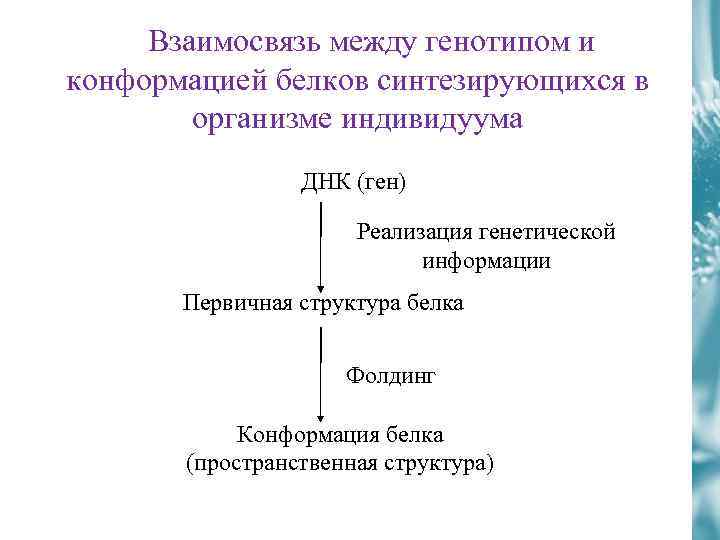
Взаимосвязь между генотипом и конформацией белков синтезирующихся в организме индивидуума ДНК (ген) Реализация генетической информации Первичная структура белка Фолдинг Конформация белка (пространственная структура)

1. Последовательность аминокислотных остатков в полипептидной цепи можно рассматривать как форму записи информации. 2. Эта информация определяет пространственную укладку линейной пептидной цепи в более компактную трехмерную структуру, называемую конформацией белка. 3. Процесс формирования функционально активной конформации белка носит название фолдинг.

• При взаимодействии функциональных групп и радикалов аминокислот полипептидной цепи между собой и молекулами растворителя согласно 2 принципу термодинамики (любая замкнутая система стремится к изменению состояния, когда ее внутренняя энергия будет наименьшей) возникает пространственная трехмерная структура, которую называют конформацией. • Наиболее стабильной является нативная конформация, обладающая наименьшей свободной энергией и возникающая в физиологических условиях (оптимум температуры, р. Н). Это дает возможность выделять белки и использовать в научных, диагностических и лечебных целях.

Вторичная структура белков – это пространственная структура, формирующаяся в результате образования водородных связей между функциональными группами – С = О и – NH – пептидного остова. При этом пептидная цепь может приобретать регулярные структуры двух типов: α-спирали и β-структуры.
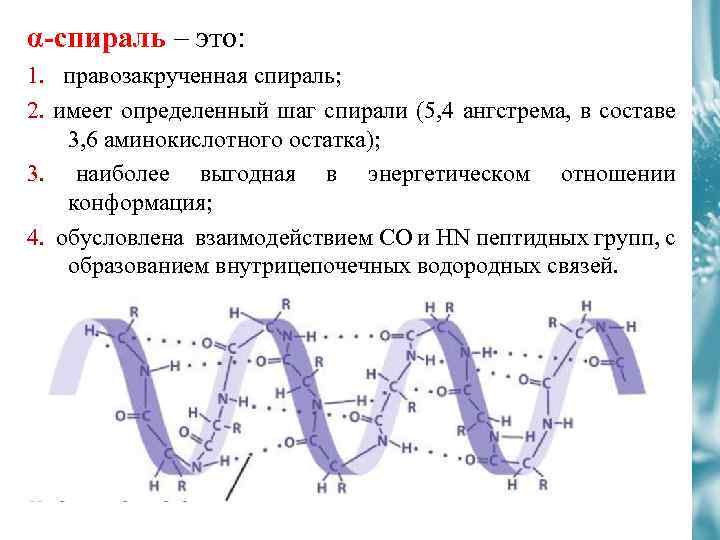
α-спираль – это: 1. правозакрученная спираль; 2. имеет определенный шаг спирали (5, 4 ангстрема, в составе 3, 6 аминокислотного остатка); 3. наиболее выгодная в энергетическом отношении конформация; 4. обусловлена взаимодействием СО и НN пептидных групп, с образованием внутрицепочечных водородных связей.

Основные особенности α-спирали 1. Имеет вид регулярной спирали. 2. Водородные связи в пределах одной полипептидной цепи возникают между атомом Н в группе –NH и карбоксильным кислородом (> C = O … HN <) 3. α-спираль стабилизируется водородными связями, которые возникают между каждой первой и четвертой аминокислотой. Шаг спирали включает 3, 6 аминокислотных остатка

Основные особенности α-спирали 1. В α-спирали водородные связи образуются между атомами кислорода карбонильной группы и водородом амидного азота 4 ой от него аминокислоты (> C = O … HN <) 2. Боковые цепи аминокислотных остатков располагаются по периферии спирали, не участвуя в образовании вторичной структуры 3. α-спираль регулярна, имеет винтовую симметрию 4. Формирование α-спирали происходит по часовой стрелке (правый ход спирали), так как природные белки состоят из L-аминокислот. 5. Для каждого белка характерна своя степень спирализации полипептидой цепи (гемоглобин – 75%, муоцим – 42%, пепсин – 30%). Спирализованные участки чередуются с линейными.

Основные особенности α-спирали 6. Объемные радикалы или радикалы несущие одинаковые заряды, препятствуют формированию α-спирали 7. Остаток пролина имеющий кольцевидную структуру, прерывает α-спираль, так как из-за отсутствия водорода у атома азота в пептидной цепи невозможно образовать водородную связь. HN H 2 C CH CООH CH 2 8. Связь между азотом и. CH 2 α—углеродным атомом входит в состав цикла пролина, поэтому пептидный остов в этом месте приобретает изгиб.
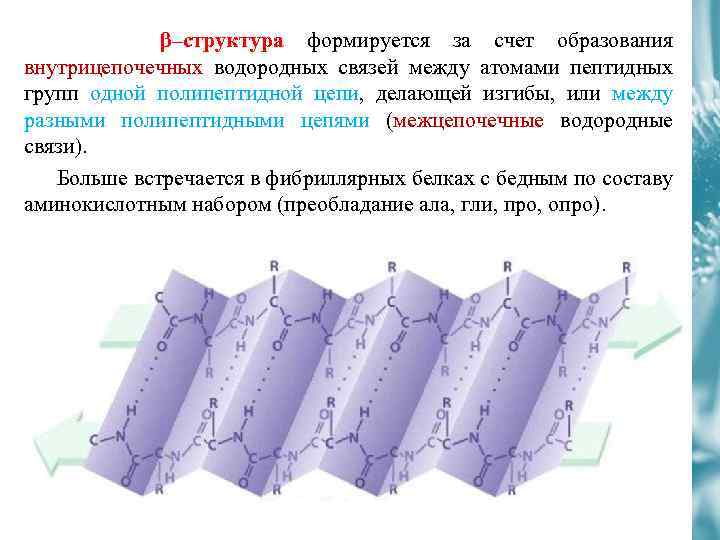
β–структура формируется за счет образования внутрицепочечных водородных связей между атомами пептидных групп одной полипептидной цепи, делающей изгибы, или между разными полипептидными цепями (межцепочечные водородные связи). Больше встречается в фибриллярных белках с бедным по составу аминокислотным набором (преобладание ала, гли, про, опро).
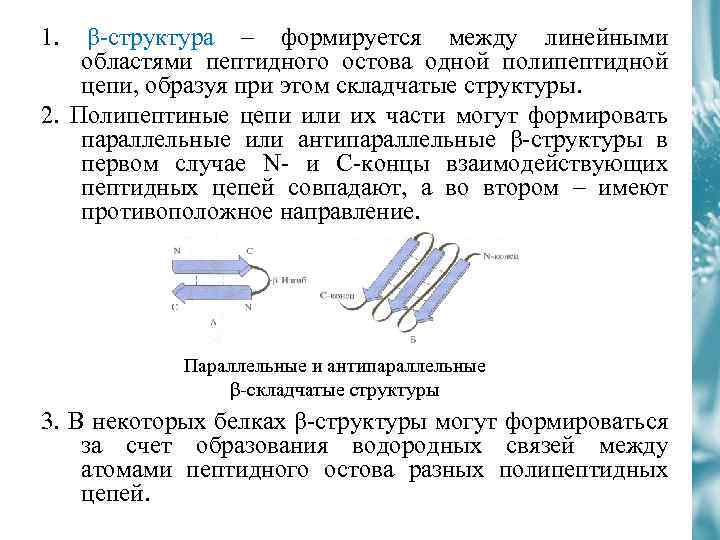
1. β-структура – формируется между линейными областями пептидного остова одной полипептидной цепи, образуя при этом складчатые структуры. 2. Полипептиные цепи или их части могут формировать параллельные или антипараллельные β-структуры в первом случае N- и С-концы взаимодействующих пептидных цепей совпадают, а во втором – имеют противоположное направление. Параллельные и антипараллельные β-складчатые структуры 3. В некоторых белках β-структуры могут формироваться за счет образования водородных связей между атомами пептидного остова разных полипептидных цепей.

По наличию α-спиралей β-структур глобулярные белки могут быть разделены на четыре категории: 1. В первую категорию включены белки, в которых имеются только α-спирали, например миоглобин и гемоглобин. Вторичная структура миоглобина

По наличию α-спиралей β-структур глобулярные белки могут быть разделены на четыре категории: 2. Во вторую категорию входят белки в которых имеются и α-спирали и β-структуры. Вторичная структура триозофосфатизомеразы и домена пируваткиназы
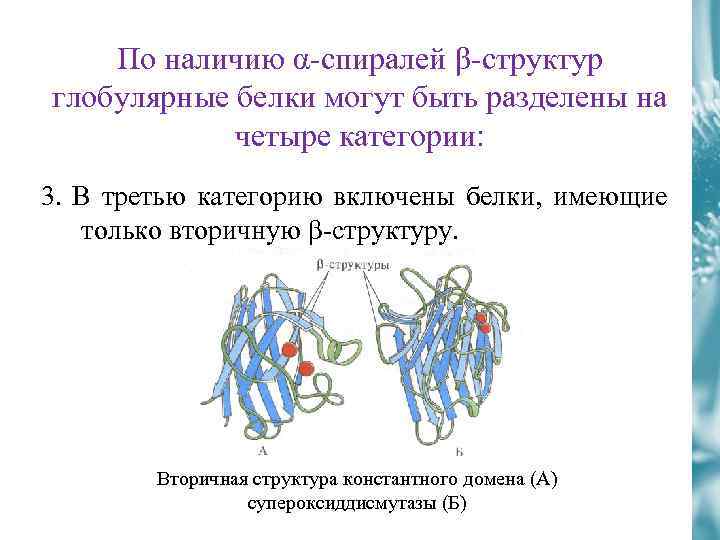
По наличию α-спиралей β-структур глобулярные белки могут быть разделены на четыре категории: 3. В третью категорию включены белки, имеющие только вторичную β-структуру. Вторичная структура константного домена (А) супероксиддисмутазы (Б)

По наличию α-спиралей β-структур глобулярные белки могут быть разделены на четыре категории: 4. В четвертую категорию включены белки, имеющие в своем составе незначительное количество регулярных вторичных структур. К таким белками можно отнести небольшие, богатые цистеином белки или металлопротеины.

Степень спирализации у различных белков различна (гемоглобин – 75% спирализация, пепсин – 28%, химотрипсин – 11% и т. д. ). Это зависит от: 1. количества аминокислот, участвующих в стабильной спирализации (ала, лей, фен, гис), не участвующих (сер, илей, асп, глу, лиз, арг) и препятствующих спирализации (про, опро); 2. Наличие участков, где близко расположено несколько одинаково заряженных радикалов аминокислот; 3. Наличие участков, где близко расположено несколько объемных радикалов аминокислот (илей, мет, три, лей). В неспирализованных участках пептидные цепи наиболее подвижны и легче атакуются ферментами.

Третичная структура белков – конформация, образующаяся за счет взаимодействия между радикалами аминокислот, которые могут находиться на значительном расстоянии друг от друга в полипептидной цепи. Каждая отдельная полипептидная цепь называется мономером. При укладке полипептидной цепи при взаимодействии с молекулами растворителя принимается энергетически наиболее выгодная форма, характеризующаяся минимумом свободной энергии.

Третичная структура белка – тип конформации, образующийся за счет взаимодействий между радикалами аминокислот, которые могут находиться на значительном расстоянии друг от друга в пептидной цепи. Большинство белков при этом формируют пространственную структуру, напоминающую глобулу (глобулярные белки)
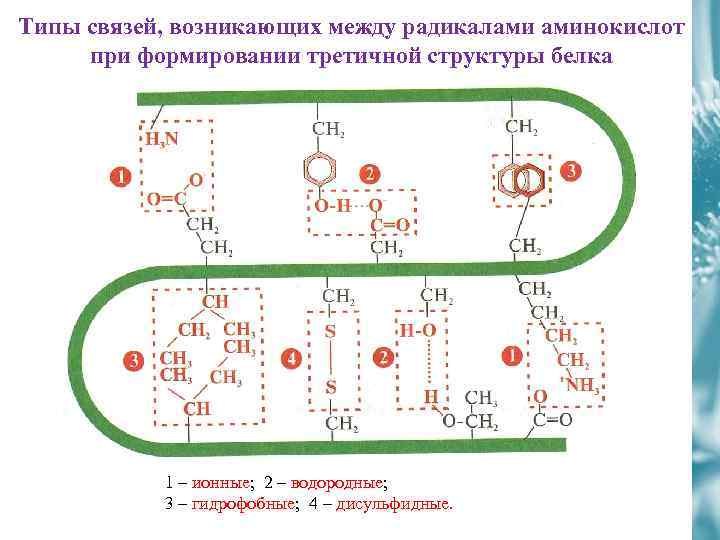
Типы связей, возникающих между радикалами аминокислот при формировании третичной структуры белка 1 – ионные; 2 – водородные; 3 – гидрофобные; 4 – дисульфидные.

Связи стабилизирующие третичную структуру I. Сильные (ковалентные) 1. Дисульфидные: (– S –) 2. Изопептидные: NH 2 и COOH в боковых радикалах 3. Сложноэфирные: ОН и СООН II. Слабые: 1. Полярные а) Водородные СО … HN б) Ионные СОО- и NH 3+ 2. Неполярные а) Гидрофобные взаимодействия С 6 Н 5 и С 6 Н 5 б) Межмолекулярные ван-дер-ваальсовы силы

Третичная структура имеет для белков следующие особенности: • Укладка полипептидной цепи очень плотная; • Все гидрофильные (полярные) радикалы аминокислот расположены на поверхности молекулы белка и гидратированы (лиз, арг, гис, глу, асп, тре, цис, сер, асн, глн); • Почти все гидрофобные (неполярные) радикалы аминокислот находятся в глубине молекулы белка (лей, илей, три, фен, тир, вал, про, опро); • В местах сгибов полипептидной цепи находятся про, опро, в меньшей степени аминокислоты, не участвующие в спирализации; • Белки, выполняющие сходные функции у различных млекопитающих, имеют сходную третичную структуру. Домен – участок полипептидной цепи, который в процессе формирования пространственной структуры приобретает конформацию глобулярного белка.

Образование дисульфидной связи в молекуле белка Большинство внутриклеточных белков не имеет в третичной структуре ковалентных дисульфидных связей. Их наличие характерно для секретируемых клеткой белков, что обеспечивает их большую стабильность во внеклеточных условиях. Так, дисульфидные связи имеются в молекулах инсулина и иммуноглобулинов.

Особенности организации третичной структуры белка: 1. Конформация третичной структуры полипептидной цепи определяется свойствами боковых радикалов аминокислот и микроокружением. 2. Гидрофобные радикалы аминокислот имеют тенденцию к объединению с помощью гидрофобных взаимодействий и межмолекулярных ван-дерваальсовых сил, внутри белковой глобулы образуется плотное гидрофобные ядро. Гидрофильные ионизированные и неионизированные радикалы в основном располагаются на поверхности белка и определяют его растворимость в воде.

Особенности организации третичной структуры белка: 3. При формировании третичной структуры полипептидная цепь делает изгиб в местах нахождения пролина, гидроксипролина, глицина. 4. Процесс сворачивания полипептидной цепи в правильную пространственную структуру называется фолдинг белка. 5. Функционально активная конфармация белка называется нативной конформацией. Изменение внутренней среды (например, концентрации глюкозы, ионов Са 2+, протонов и т. д. ) приводит к изменению конформации и нарушению функций белка.
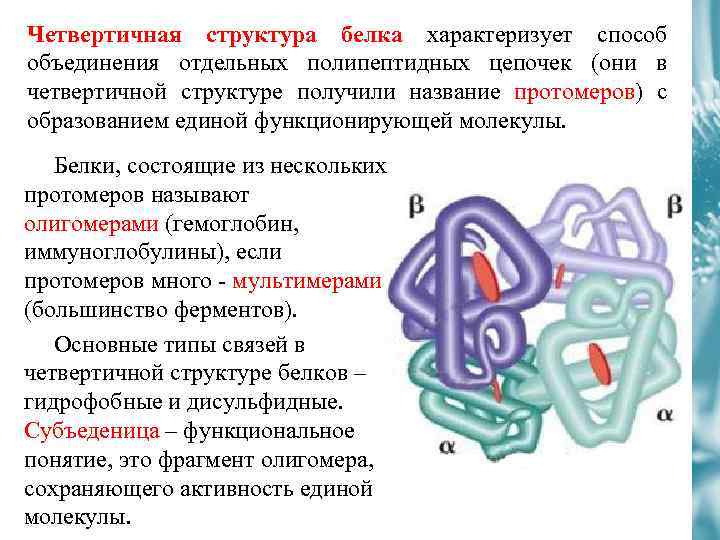
Четвертичная структура белка характеризует способ объединения отдельных полипептидных цепочек (они в четвертичной структуре получили название протомеров) с образованием единой функционирующей молекулы. Белки, состоящие из нескольких протомеров называют олигомерами (гемоглобин, иммуноглобулины), если протомеров много - мультимерами (большинство ферментов). Основные типы связей в четвертичной структуре белков – гидрофобные и дисульфидные. Субъеденица – функциональное понятие, это фрагмент олигомера, сохраняющего активность единой молекулы.

Потеря нативной конформации, сопровождающаяся утратой специфической функции белка называется денатурацией белков (необратимая, обратимая). При этом первичная структура белка не нарушается. Факторы денатурации: высокая температура, интенсивное встряхивание, органические вещества, кислоты, щелочи, соли тяжелых металлов, детергенты (наиболее известны мыла).

Классификация белков • По форме (глобулярные, фибриллярные); • По составу (простые, сложные – нуклео-, глико-, липо-, хромо-, металлопротеиды); • По функции (каталитические, регуляторные, структурные, транспортные, защитные, рецепторные, сократительные).

Особенности строения и функционирования олигомерных белков на примере гемоглобина 1. Многие белки имеют в своем составе несколько полипептидных цепей. Такие белки называют олигомерами, а отдельные цепи – протомерами. Протомеры в олигомерных белках соединены множеством слабых нековалентных связей (гидрофобных, ионных, водородных). Взаимодействие протомеров осуществляется по принципу комплементарности их контактирующих поверхностей.

Особенности строения и функционирования олигомерных белков на примере гемоглобина 2. Количество протомеров олигомерных белках может сильно варьировать: гемоглобин содержит – 4 протомера, фермент аспартатаминотрансфераза – 12 протомеров, а белок вируса табачной мозаики – 2120. 3. Количество и способ соединения протомеров в белке называется четвертичной структурой белка. Это организация нескольких полипептидных цепей с третичной структурой в единую функциональную молекулу белка.

Особенности строения и функционирования олигомерных белков на примере гемоглобина 4. В состав белков могут входить одинаковые или разные по строению протомеры, например, гомодимеры – белки, содержащие два одинаковых протомера, а гетеродимеры – белки, содержащие два разных протомера.

Факторы вызывающие денатурацию Факторы денатурации разрывают гидрофобные, водородные, ионные связи: 1. Высокая t (>500 C) – увеличивающая тепловое движение атомов, что приводит к разрыву слабых связей. 2. Органические вещества (этиловые спирт, фенол и его производные) способны взаимодействовать с функциональными группами белков, что приводит к их конформационным изменениям. Для денатурации в лабораторых условиях часто используют мочевину или гуанидинхлорид, которые образуют водородные связи с амино и карбонильными группами пептидного остова и некоторыми функциональными R АМК.

Факторы вызывающие денатурацию 3. Кислоты, щелочи – изменяя р. Н вызывают перераспределение связей в молекуле белка. 4. Соли тяжелых Ме (Cu, Hg, Ag, Pb). Образуют прочные связи с -SH группами белков изменяя конформацию и активность. 5. Действие детергентов (они амфифильны, содержат гидрофобный углеводороный R и гидрофильную функциональную группу (пример мыла).

Медицинские аспекты конформационной лабильности белков 1. Большинство белковых препаратов необходимо хранить в холодильнике при t не выше 100 С 2. Растворять сухие препараты охлажденной до комнатной t кипяченой водой.

Применение денатурирующих агентов в биологических исследованиях и медицине. 1. Трихлоруксусная кислота – используется для денатурации ферментов, с целью прекращения реакции. 2. Денатурирующие агенты часто используют для стерилизации медицинских инструментов, антисептиков (автоклав). 3. Фенол и его производные (крезол, резорцин) – антисептики ароматического ряда (обладают высокой гидрофобностью, действуют на вегетативные формы бактерий, грибов)

Применение денатурирующих агентов в биологических исследованиях и медицине. 4. Значительное количеств антиcептиков представлено солями тяжелых металлов. Из-за токсичности таких лекарств, их применяют в качестве поверхностных антисептиков. Сулема – дихлорид ртути (Hg. Cl 2) используют для обработки рук и дезинфекции помещений. Антимикробными свойствами обладают и препараты серебра ляпис Ag. NО 3), колларгол (серебро коллоидное), применяется для обработки слизистых оболочек при инфекционных заболеваниях
Строение, свойства и функции белков..pptx