3 строение сплавов.pptx
- Количество слайдов: 17
 Строение сплавов
Строение сплавов
 Основные определения Фаза ‒ совокупность однородных частей сплава (системы), одинаковых по химическому составу атомному строению и отделенных от других частей системы поверхностью раздела Система – совокупность взаимодействующих фаз, образующих сплав. Компоненты сплава (системы) – химические элементы и соединения, из которых может быть образована любая фаза сплава. Число степеней свободы – количество независимых термодинамических переменных, полностью описывающих состояние системы. 1, Число степеней свободы подчиняется правилу фаз Гиббса: f = К – Ф + где К – число компонентов, образующих систему; Ф – количество фаз, находящихся в равновесии.
Основные определения Фаза ‒ совокупность однородных частей сплава (системы), одинаковых по химическому составу атомному строению и отделенных от других частей системы поверхностью раздела Система – совокупность взаимодействующих фаз, образующих сплав. Компоненты сплава (системы) – химические элементы и соединения, из которых может быть образована любая фаза сплава. Число степеней свободы – количество независимых термодинамических переменных, полностью описывающих состояние системы. 1, Число степеней свободы подчиняется правилу фаз Гиббса: f = К – Ф + где К – число компонентов, образующих систему; Ф – количество фаз, находящихся в равновесии.
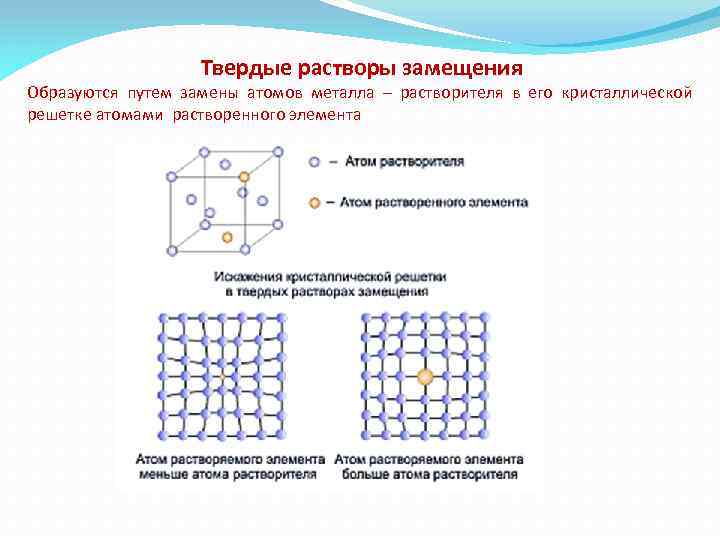 Твердые растворы замещения Образуются путем замены атомов металла – растворителя в его кристаллической решетке атомами растворенного элемента
Твердые растворы замещения Образуются путем замены атомов металла – растворителя в его кристаллической решетке атомами растворенного элемента
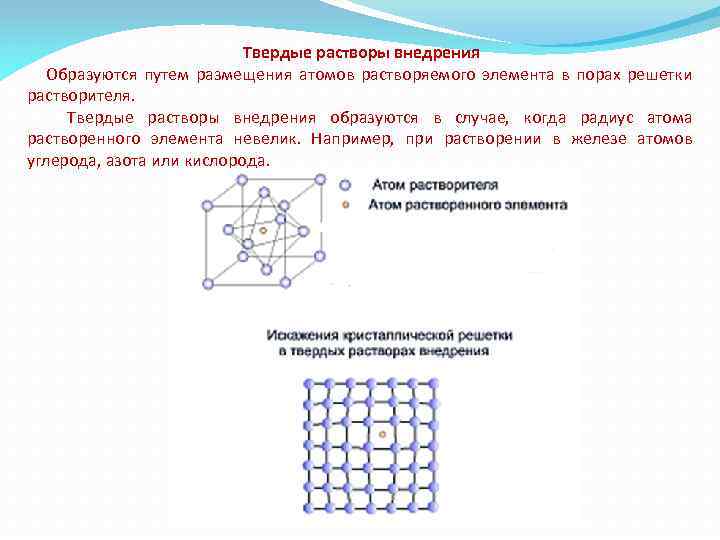 Твердые растворы внедрения Образуются путем размещения атомов растворяемого элемента в порах решетки растворителя. Твердые растворы внедрения образуются в случае, когда радиус атома растворенного элемента невелик. Например, при растворении в железе атомов углерода, азота или кислорода.
Твердые растворы внедрения Образуются путем размещения атомов растворяемого элемента в порах решетки растворителя. Твердые растворы внедрения образуются в случае, когда радиус атома растворенного элемента невелик. Например, при растворении в железе атомов углерода, азота или кислорода.
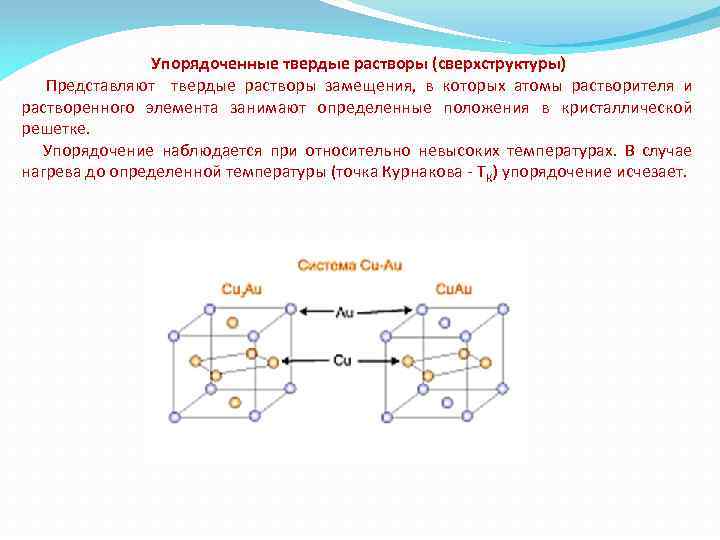 Упорядоченные твердые растворы (сверхструктуры) Представляют твердые растворы замещения, в которых атомы растворителя и растворенного элемента занимают определенные положения в кристаллической решетке. Упорядочение наблюдается при относительно невысоких температурах. В случае нагрева до определенной температуры (точка Курнакова - ТК) упорядочение исчезает.
Упорядоченные твердые растворы (сверхструктуры) Представляют твердые растворы замещения, в которых атомы растворителя и растворенного элемента занимают определенные положения в кристаллической решетке. Упорядочение наблюдается при относительно невысоких температурах. В случае нагрева до определенной температуры (точка Курнакова - ТК) упорядочение исчезает.
 Химические соединения Имеют следующие особенности § состав: может быть выражен простой формулой An. Bm, где A и B – соответствующие элементы, n и m – целые числа; § кристаллическую решетку, отличающуюся от кристаллических решеток элементов, образующих соединение; § свойства, резко отличающиеся от свойств образующих соединение элементов; § постоянную температуру кристаллизации, как и у чистых металлов. Виды химических соединений: o Соединения в нормальной валентностью, в которых атомы разного сорта связаны ионными или ковалентными связями (сульфиды, оксиды и т. п. ) o Металлические соединения. В них преобладает металлический тип межатомной связи: • электронные соединения (фазы Юм-Розери): Cu. Zn, Cu. Zn 3 и др. • фазы внедрения: VC, Ti. C и др. • фазы Лавеса (отношение атомных диаметров металлов ~ 1, 2: Fe 2 W, Fe 2 Mo
Химические соединения Имеют следующие особенности § состав: может быть выражен простой формулой An. Bm, где A и B – соответствующие элементы, n и m – целые числа; § кристаллическую решетку, отличающуюся от кристаллических решеток элементов, образующих соединение; § свойства, резко отличающиеся от свойств образующих соединение элементов; § постоянную температуру кристаллизации, как и у чистых металлов. Виды химических соединений: o Соединения в нормальной валентностью, в которых атомы разного сорта связаны ионными или ковалентными связями (сульфиды, оксиды и т. п. ) o Металлические соединения. В них преобладает металлический тип межатомной связи: • электронные соединения (фазы Юм-Розери): Cu. Zn, Cu. Zn 3 и др. • фазы внедрения: VC, Ti. C и др. • фазы Лавеса (отношение атомных диаметров металлов ~ 1, 2: Fe 2 W, Fe 2 Mo


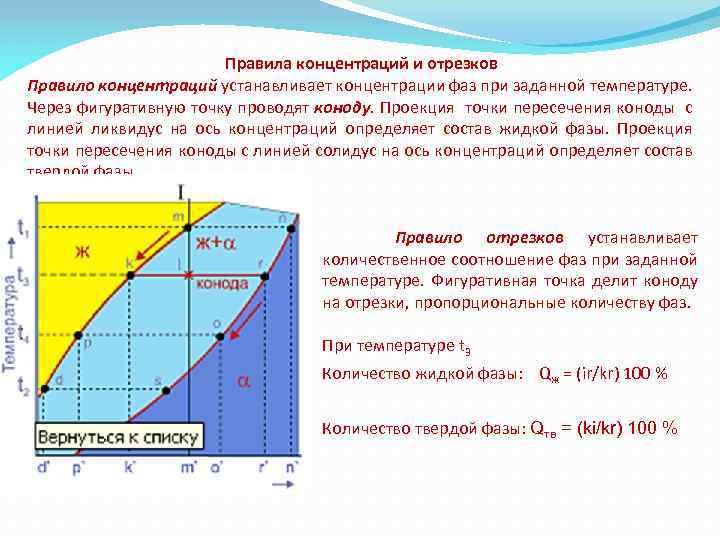 Правила концентраций и отрезков Правило концентраций устанавливает концентрации фаз при заданной температуре. Через фигуративную точку проводят коноду. Проекция точки пересечения коноды с линией ликвидус на ось концентраций определяет состав жидкой фазы. Проекция точки пересечения коноды с линией солидус на ось концентраций определяет состав твердой фазы. Правило отрезков устанавливает количественное соотношение фаз при заданной температуре. Фигуративная точка делит коноду на отрезки, пропорциональные количеству фаз. При температуре t 3 Количество жидкой фазы: Qж = (ir/kr) 100 % Количество твердой фазы: Qтв = (ki/kr) 100 %
Правила концентраций и отрезков Правило концентраций устанавливает концентрации фаз при заданной температуре. Через фигуративную точку проводят коноду. Проекция точки пересечения коноды с линией ликвидус на ось концентраций определяет состав жидкой фазы. Проекция точки пересечения коноды с линией солидус на ось концентраций определяет состав твердой фазы. Правило отрезков устанавливает количественное соотношение фаз при заданной температуре. Фигуративная точка делит коноду на отрезки, пропорциональные количеству фаз. При температуре t 3 Количество жидкой фазы: Qж = (ir/kr) 100 % Количество твердой фазы: Qтв = (ki/kr) 100 %
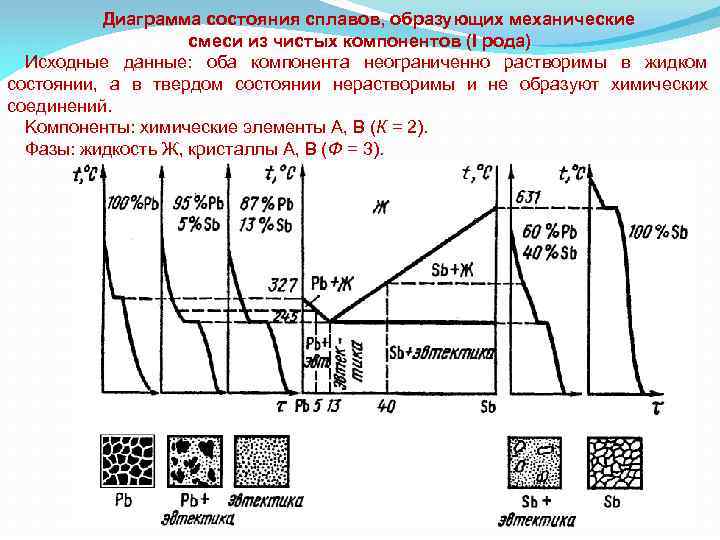 Диаграмма состояния сплавов, образующих механические смеси из чистых компонентов (I рода) Исходные данные: оба компонента неограниченно растворимы в жидком состоянии, а в твердом состоянии нерастворимы и не образуют химических соединений. Kомпоненты: химические элементы А, В (К = 2). Фазы: жидкость Ж, кристаллы А, В (Ф = 3).
Диаграмма состояния сплавов, образующих механические смеси из чистых компонентов (I рода) Исходные данные: оба компонента неограниченно растворимы в жидком состоянии, а в твердом состоянии нерастворимы и не образуют химических соединений. Kомпоненты: химические элементы А, В (К = 2). Фазы: жидкость Ж, кристаллы А, В (Ф = 3).

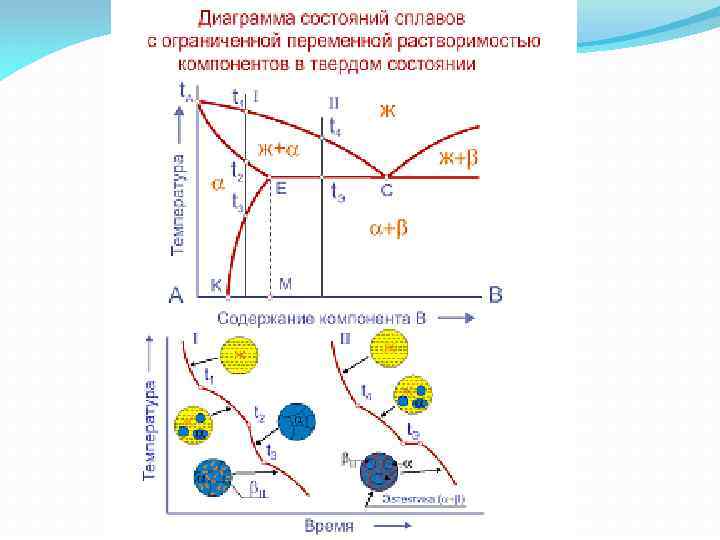
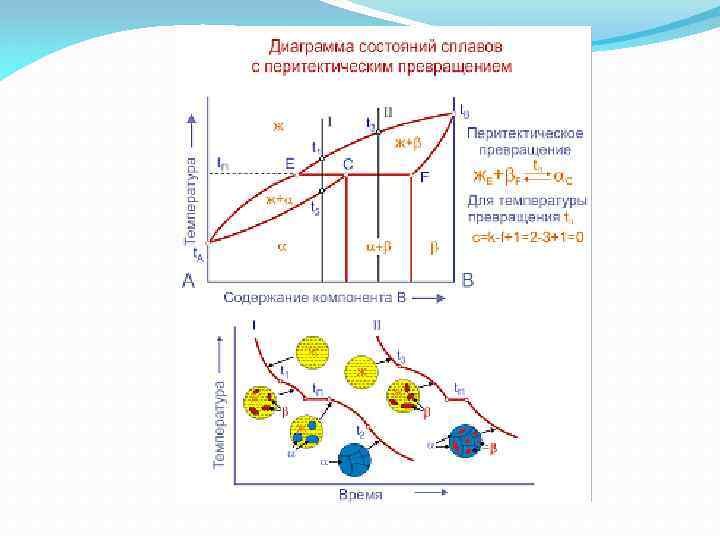

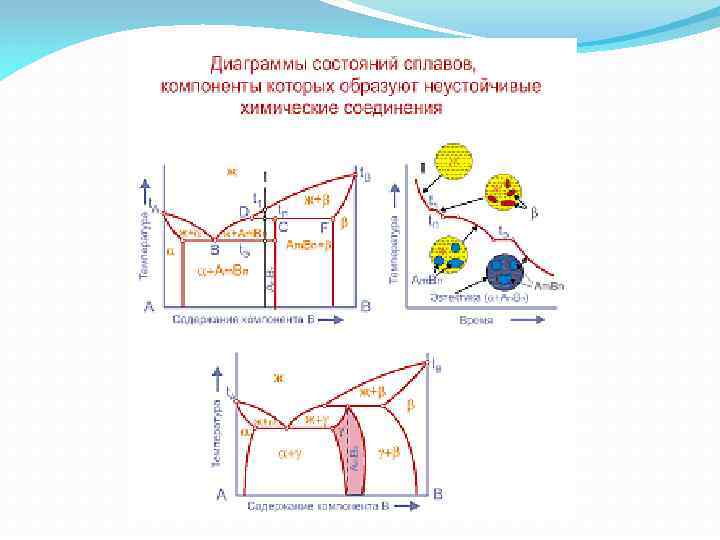
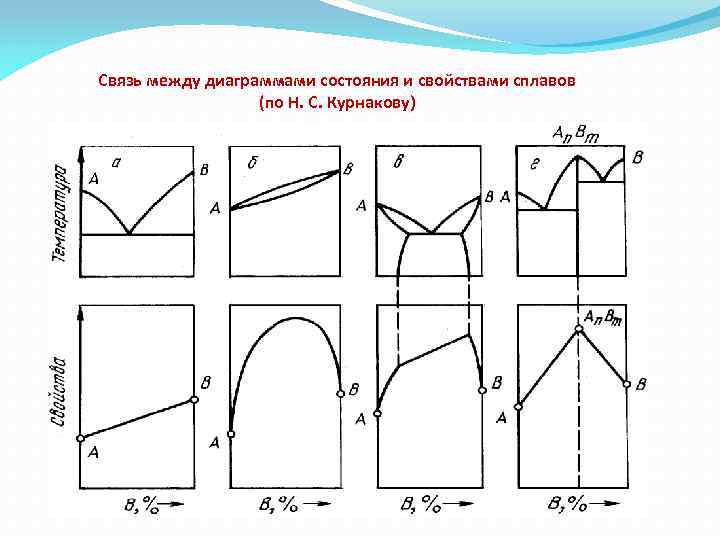 Связь между диаграммами состояния и свойствами сплавов (по Н. С. Курнакову)
Связь между диаграммами состояния и свойствами сплавов (по Н. С. Курнакову)



