L2_СТРОЕНИЕ И СВОЙСТВА БИОПОЛИМЕРОВ.ppt
- Количество слайдов: 52
СТРОЕНИЕ И СВОЙСТВА БИОПОЛИМЕРОВ
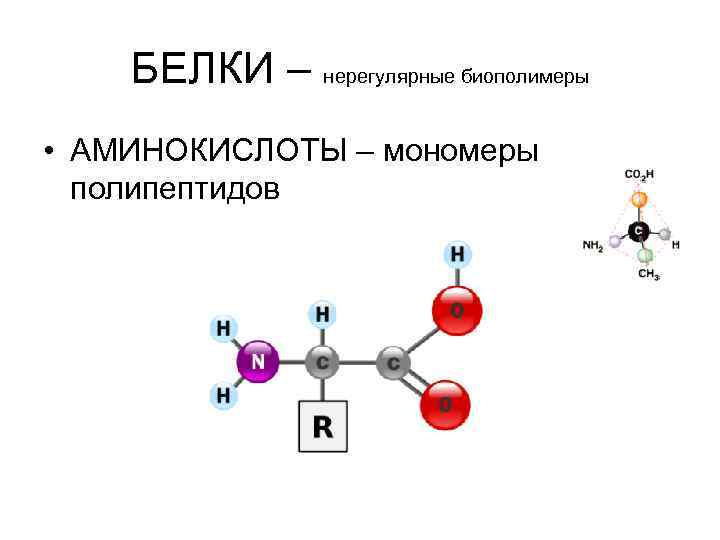
БЕЛКИ – нерегулярные биополимеры • АМИНОКИСЛОТЫ – мономеры полипептидов

Классификация аминокислот • Неполярные, или алифатические
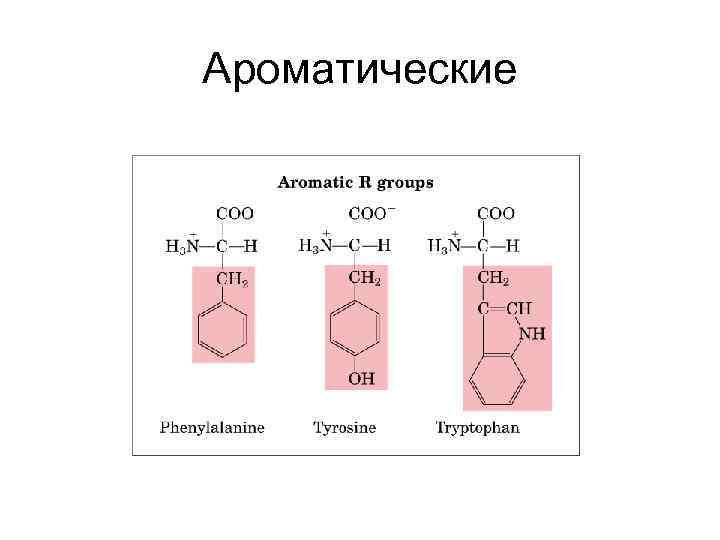
Ароматические

Полярные незаряженные

Положительно заряженные

Отрицательно заряженные
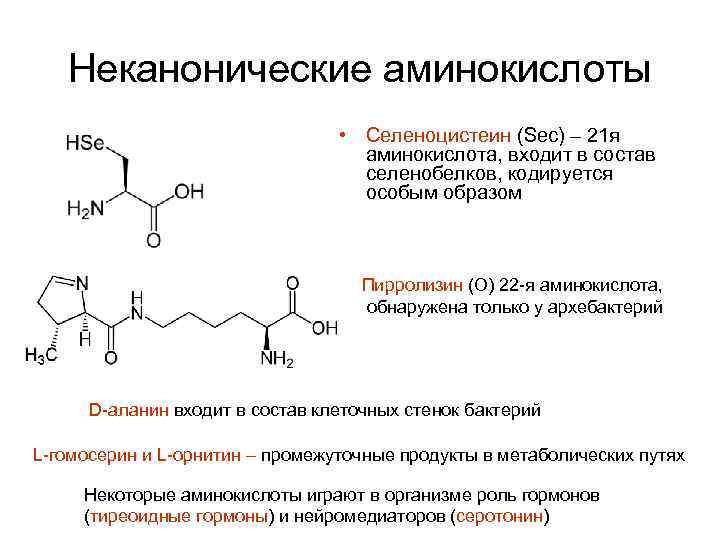
Неканонические аминокислоты • Селеноцистеин (Sec) – 21 я аминокислота, входит в состав селенобелков, кодируется особым образом Пирролизин (О) 22 -я аминокислота, обнаружена только у архебактерий D-аланин входит в состав клеточных стенок бактерий L-гомосерин и L-орнитин – промежуточные продукты в метаболических путях Некоторые аминокислоты играют в организме роль гормонов (тиреоидные гормоны) и нейромедиаторов (серотонин)

НЕЗАМЕНИМЫЕ АМИНОКИСЛОТЫ • не могут быть синтезированы в организме • необходимо поступление в организм с пищей. Для человека: аргинин, валин, гистидин, изолейцин, лизин, метионин, треони н, триптофан и фенилалани н.
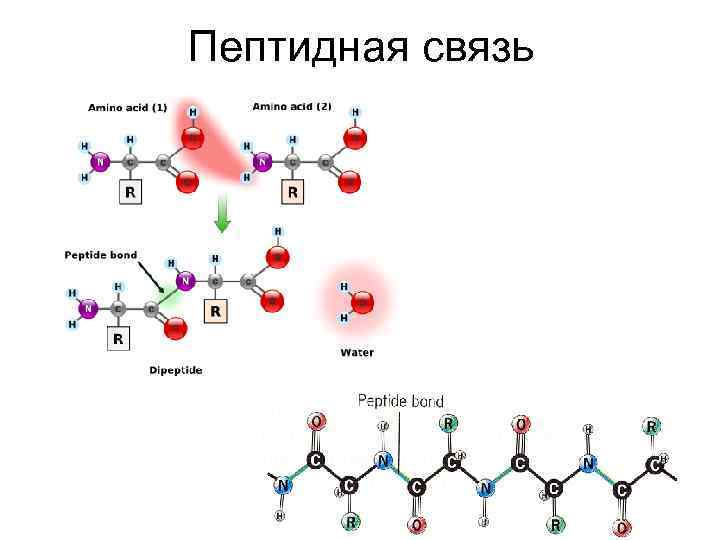
Пептидная связь

• Белки – от 100 до 2000 а/к • Многообразие – число и порядок аминокислот • Упорядоченность структуры
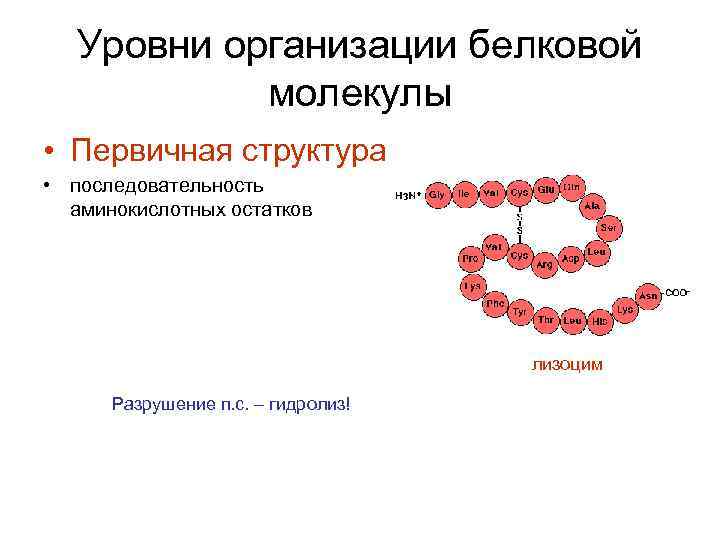
Уровни организации белковой молекулы • Первичная структура • последовательность аминокислотных остатков лизоцим Разрушение п. с. – гидролиз!

Вторичная структура белка • упорядочивание за счет водородных связей Альфа спирали Лайнус Карл Полинг (1901 -1994)
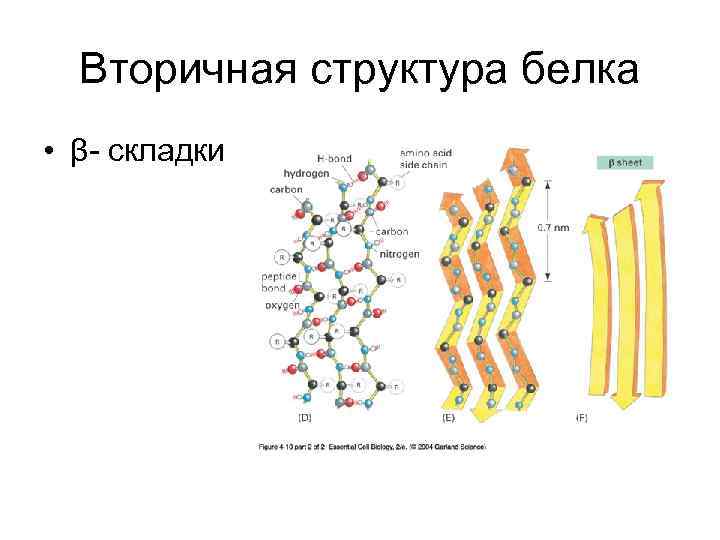
Вторичная структура белка • β- складки

Прионы • Инфекционные белки. • Pr. PC нормальный мембранный белок нервных клеток • Pr. PSc «патологическая» конформация. Pr. PC Pr. PSc α-спирали –> β-складки
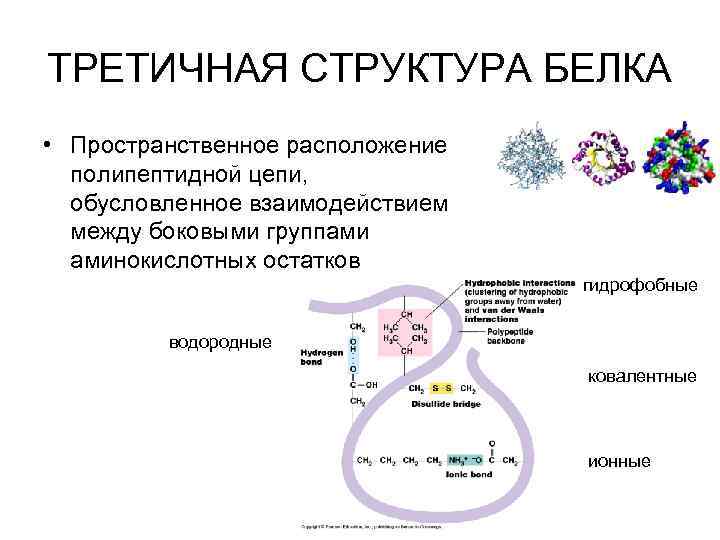
ТРЕТИЧНАЯ СТРУКТУРА БЕЛКА • Пространственное расположение полипептидной цепи, обусловленное взаимодействием между боковыми группами аминокислотных остатков гидрофобные водородные ковалентные ионные
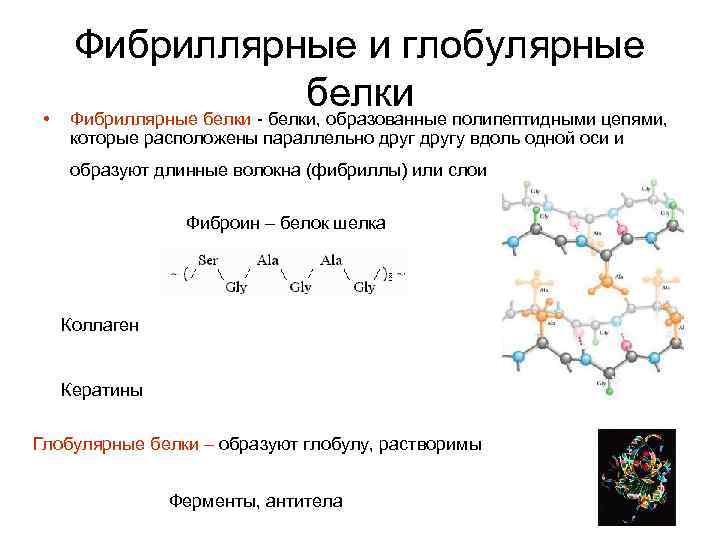
• Фибриллярные и глобулярные белки Фибриллярные белки - белки, образованные полипептидными цепями, которые расположены параллельно другу вдоль одной оси и образуют длинные волокна (фибриллы) или слои Фиброин – белок шелка Коллаген Кератины Глобулярные белки – образуют глобулу, растворимы Ферменты, антитела
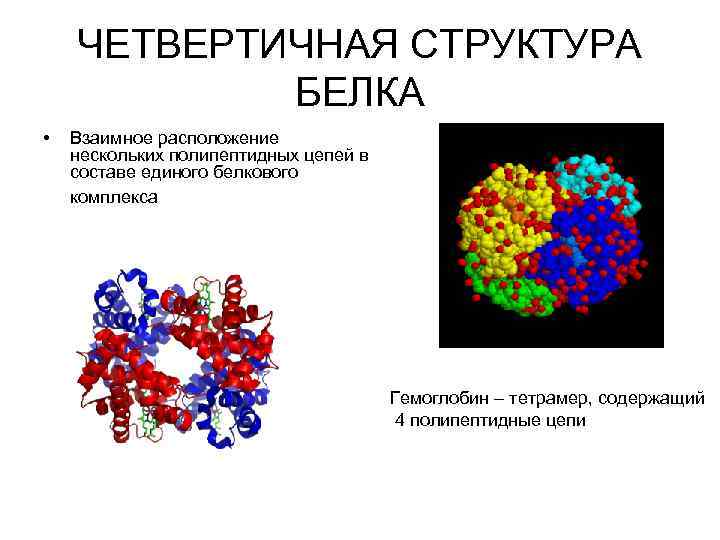
ЧЕТВЕРТИЧНАЯ СТРУКТУРА БЕЛКА • Взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса Гемоглобин – тетрамер, содержащий 4 полипептидные цепи
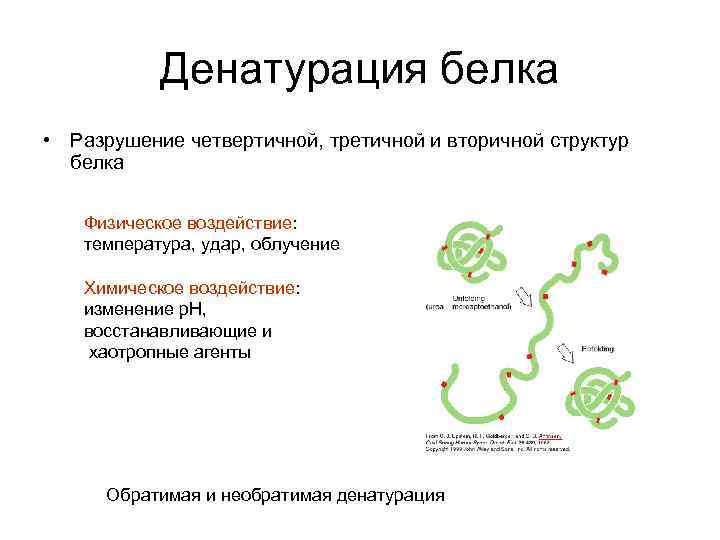
Денатурация белка • Разрушение четвертичной, третичной и вторичной структур белка Физическое воздействие: температура, удар, облучение Химическое воздействие: изменение p. H, восстанавливающие и хаотропные агенты Обратимая и необратимая денатурация
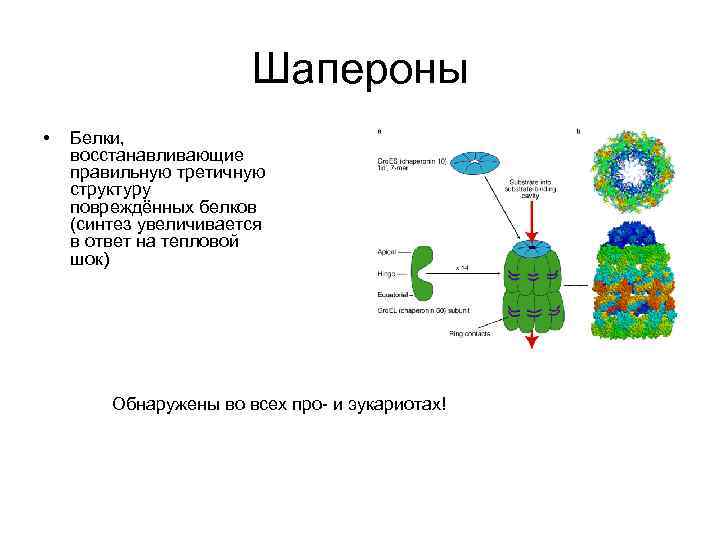
Шапероны • Белки, восстанавливающие правильную третичную структуру повреждённых белков (синтез увеличивается в ответ на тепловой шок) Обнаружены во всех про- и эукариотах!
Физические свойства белков • Размер – в среднем 300 -500 а/к, самый крупный – коннектин 38138 а/к • Заряд (изоэлектрическая точка) Основные белки (гистоны, протамины, p. I=11) Кислые белки (пепсин, p. I=1)

Гидролиз белка • Разрушение первичной структуры ферментативный химический
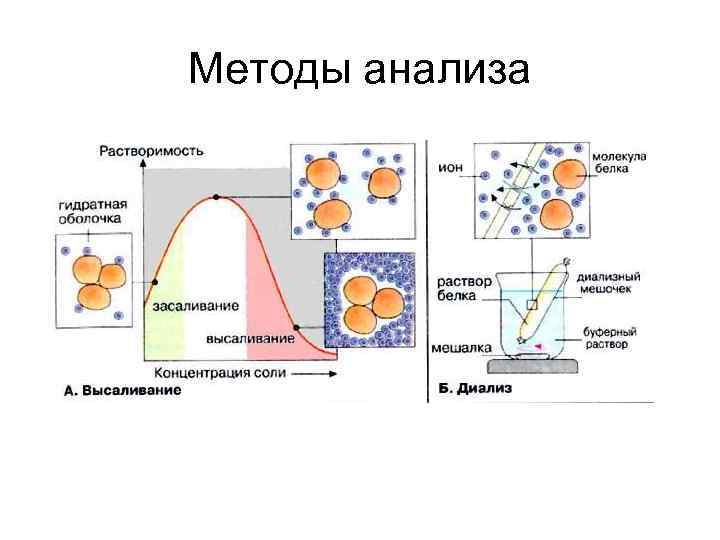
Методы анализа
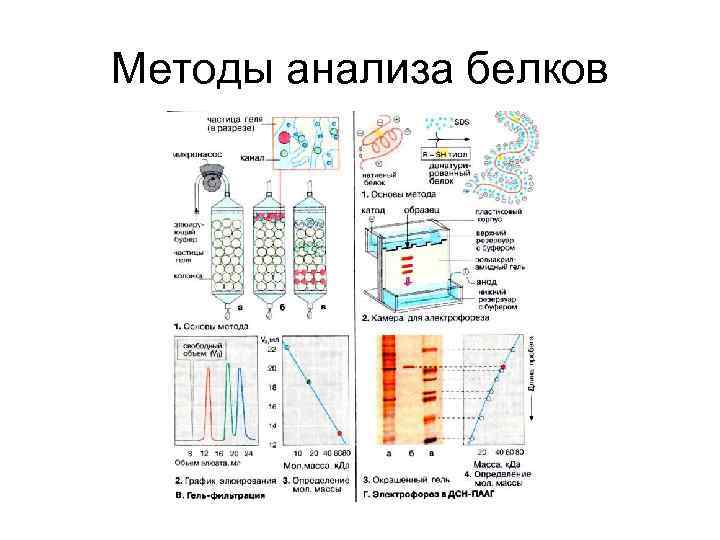
Методы анализа белков
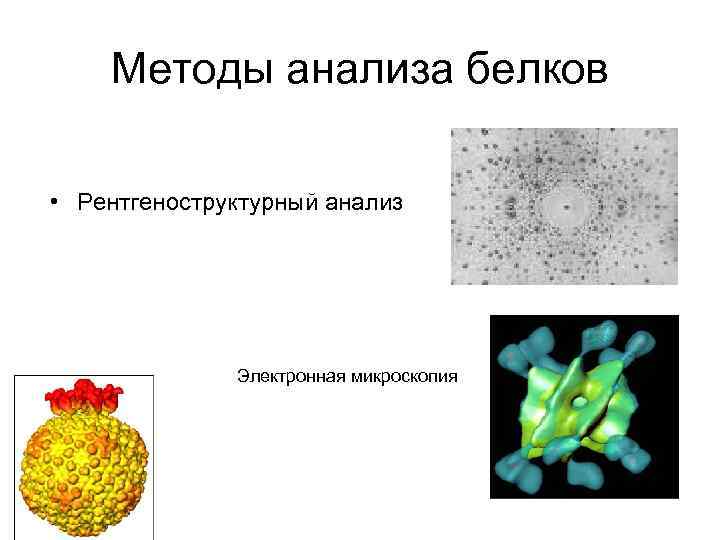
Методы анализа белков • Рентгеноструктурный анализ Электронная микроскопия
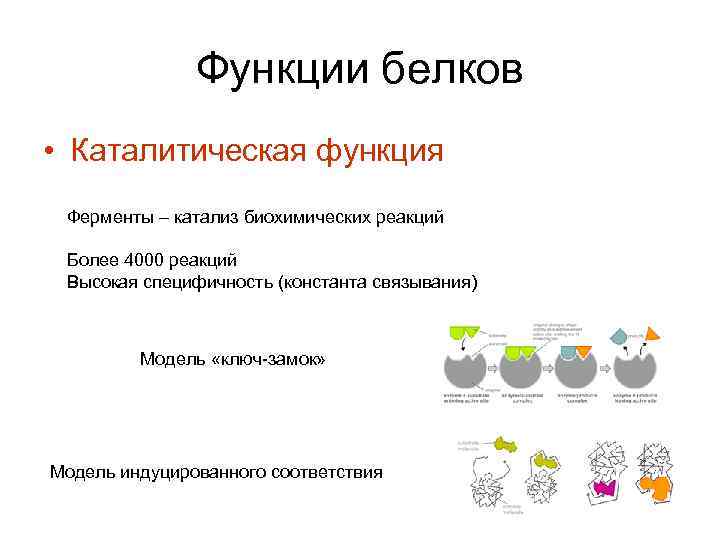
Функции белков • Каталитическая функция Ферменты – катализ биохимических реакций Более 4000 реакций Высокая специфичность (константа связывания) Модель «ключ-замок» Модель индуцированного соответствия

Каталитическая функция белков • Некоторые ферменты нуждаются в кофакторах • это могут быть неорганические молекулы (ионы металлов) или органические соединения (флавин, гем) • Большинство кофакторов связываются с ферментом нековалентно
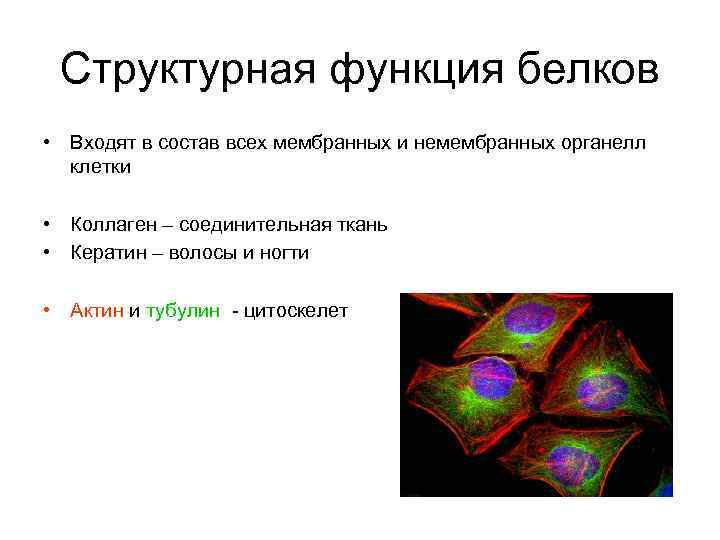
Структурная функция белков • Входят в состав всех мембранных и немембранных органелл клетки • Коллаген – соединительная ткань • Кератин – волосы и ногти • Актин и тубулин - цитоскелет
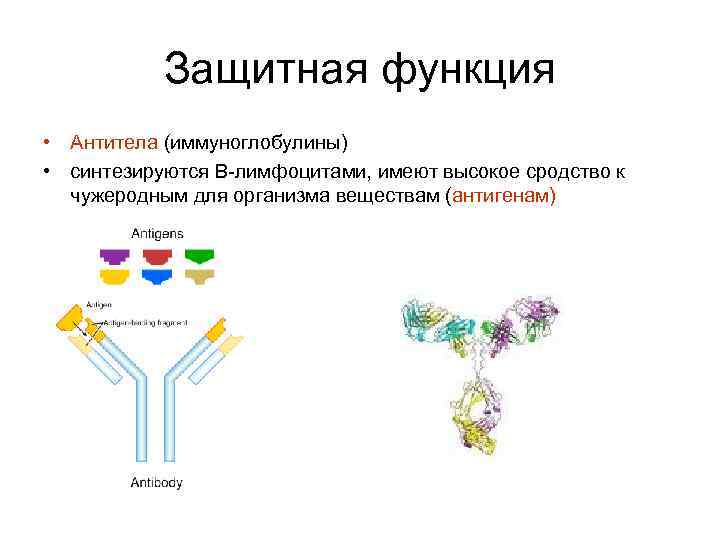
Защитная функция • Антитела (иммуноглобулины) • синтезируются В-лимфоцитами, имеют высокое сродство к чужеродным для организма веществам (антигенам)
Регуляторная функция • Белки – гормоны (инсулин) • Факторы роста • Белки - регуляторы активности генов (активаторы и репрессоры)
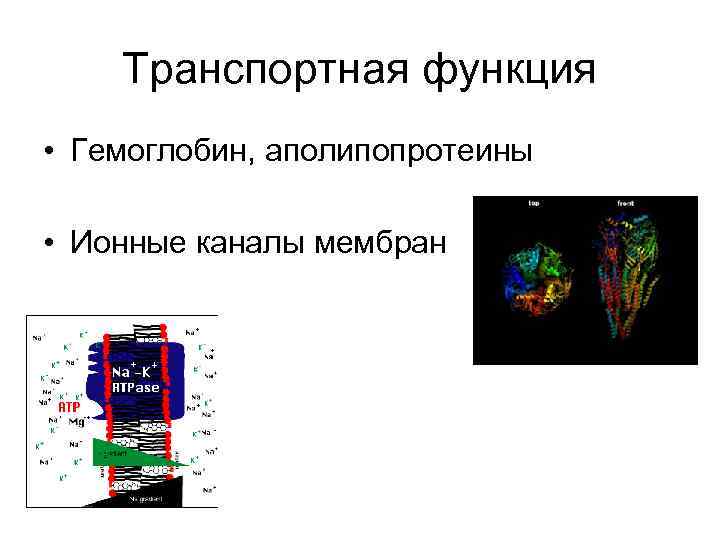
Транспортная функция • Гемоглобин, аполипопротеины • Ионные каналы мембран

Запасная и питательная функции • Овальбумин яйца Казеин молока
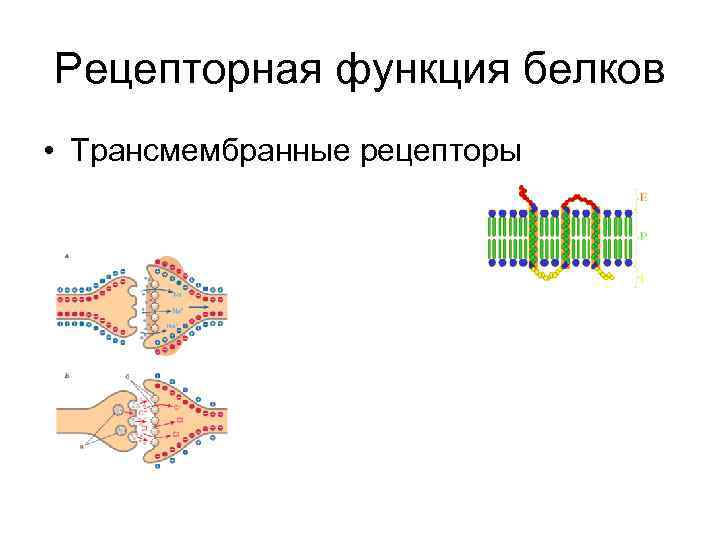
Рецепторная функция белков • Трансмембранные рецепторы
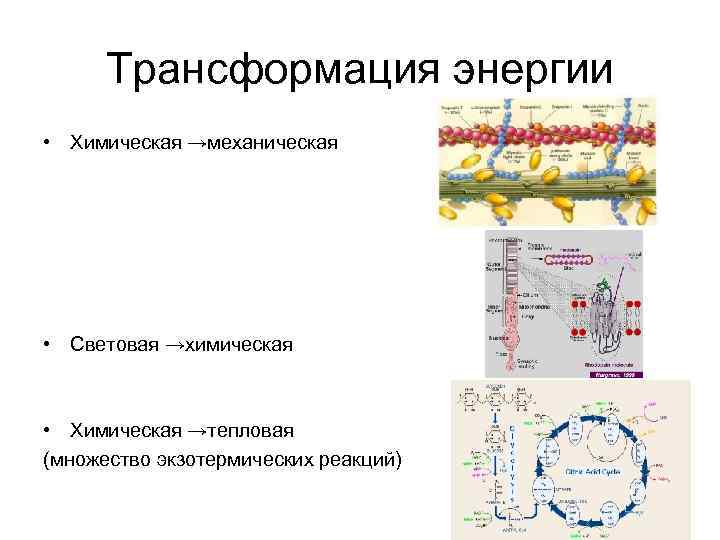
Трансформация энергии • Химическая →механическая • Световая →химическая • Химическая →тепловая (множество экзотермических реакций)
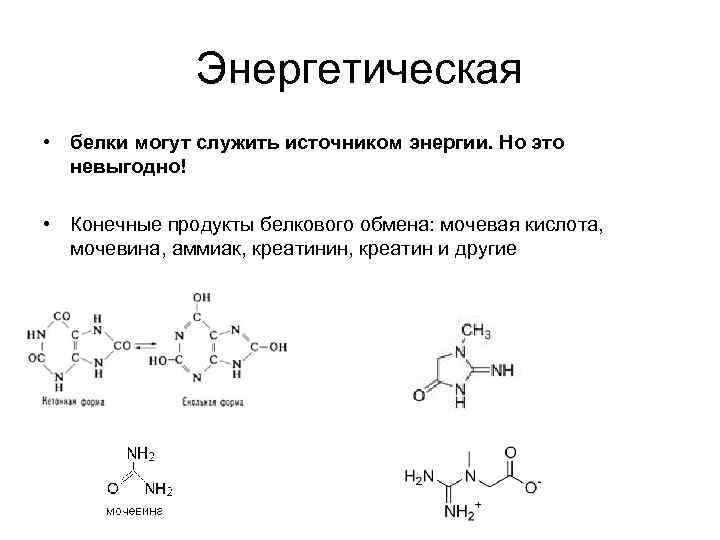
Энергетическая • белки могут служить источником энергии. Но это невыгодно! • Конечные продукты белкового обмена: мочевая кислота, мочевина, аммиак, креатинин, креатин и другие

Нуклеиновые кислоты • (от лат. nucleus — ядро) — высокомолекулярные органические соединения, биополимеры (полинуклеотиды), образованные остатками нуклеотидов. Нуклеиновые кислоты — ДНК и РНК присутствуют в клетках всех живых организмов и выполняют важнейшие функции по хранению, передаче и реализации наследственной информации Открыты в 1869 г Фридрихом Мишером
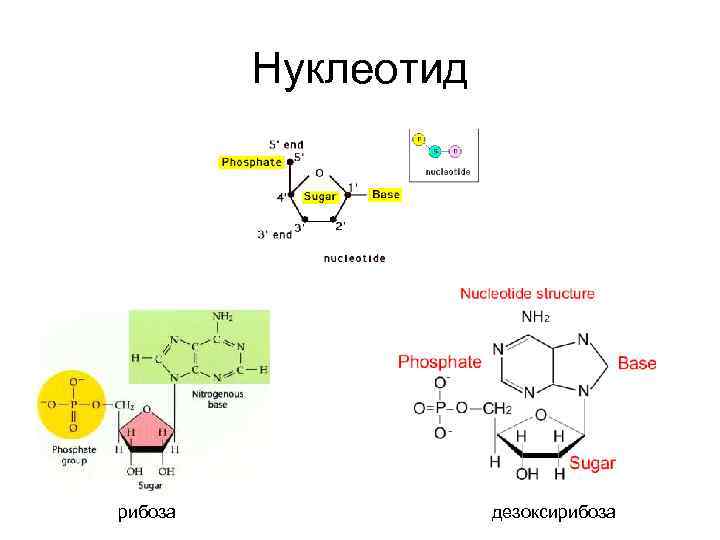
Нуклеотид рибоза дезоксирибоза
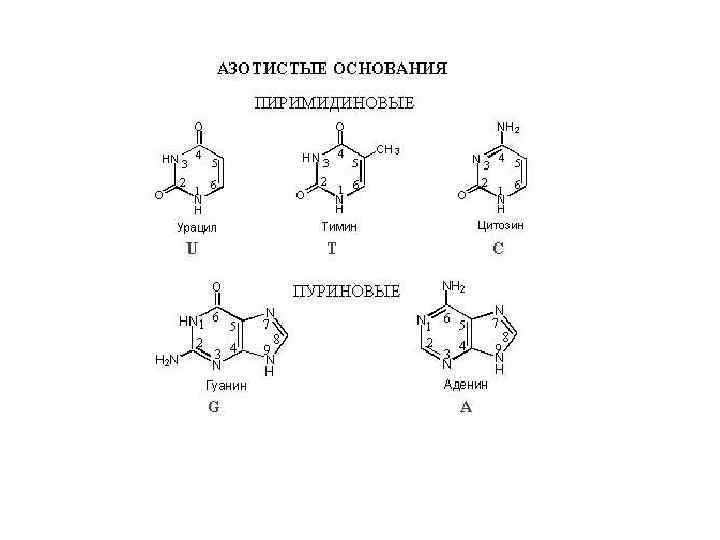
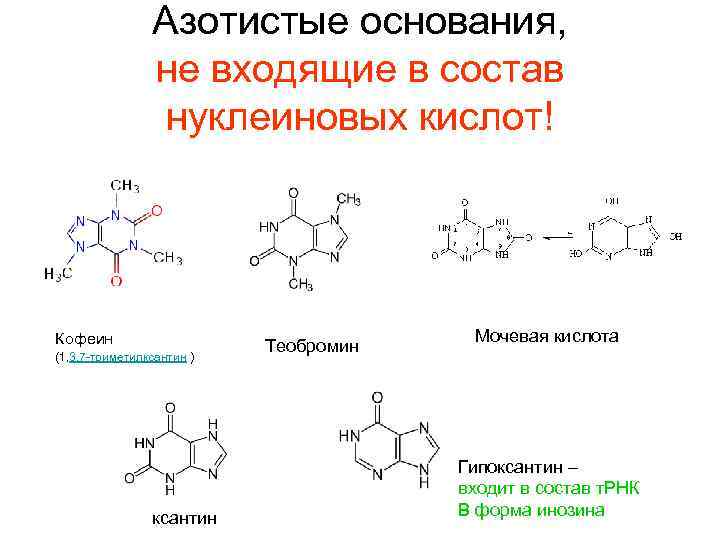
Азотистые основания, не входящие в состав нуклеиновых кислот! Кофеин (1, 3, 7 -триметилксантин ) ксантин Теобромин Мочевая кислота Гипоксантин – входит в состав т. РНК В форма инозина
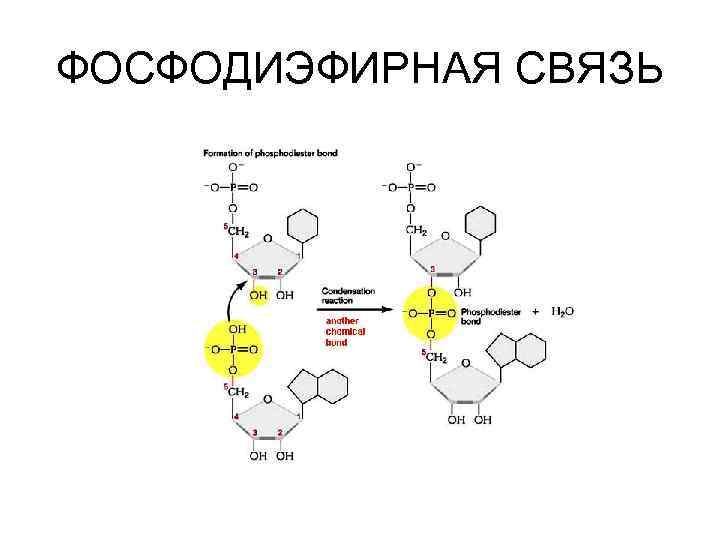
ФОСФОДИЭФИРНАЯ СВЯЗЬ
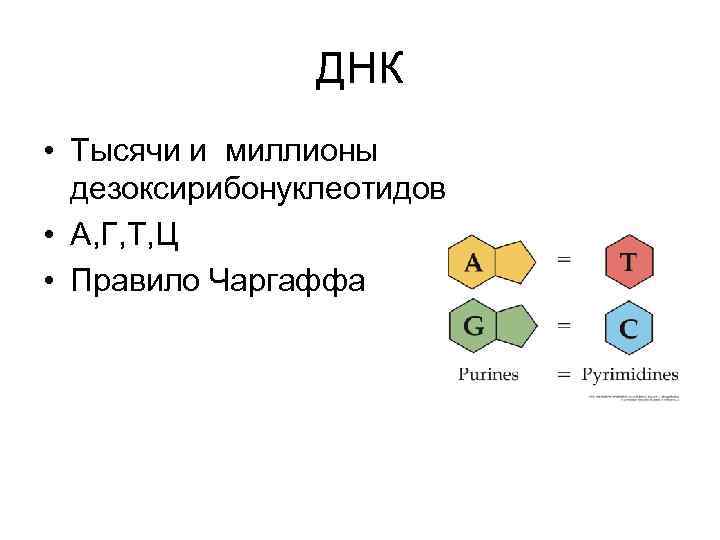
ДНК • Тысячи и миллионы дезоксирибонуклеотидов • А, Г, Т, Ц • Правило Чаргаффа

Модель Уотсона и Крика • 1950 г. М. Уилкинс и Р. Франклин – рентгенограмма ДНК • Крестообразный рисунок – знак двойной спирали • Между последовательными нуклеотидами -0. 34 нм • 10 нуклеотидов на виток спирали • Диаметр 2 нм • Непонятно, как они удерживаются вместе!!!
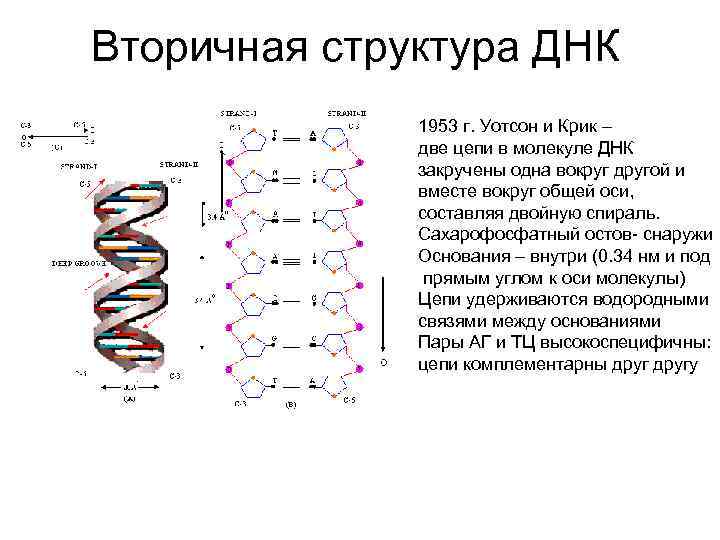
Вторичная структура ДНК 1953 г. Уотсон и Крик – две цепи в молекуле ДНК закручены одна вокруг другой и вместе вокруг общей оси, составляя двойную спираль. Сахарофосфатный остов- снаружи Основания – внутри (0. 34 нм и под прямым углом к оси молекулы) Цепи удерживаются водородными связями между основаниями Пары АГ и ТЦ высокоспецифичны: цепи комплементарны другу
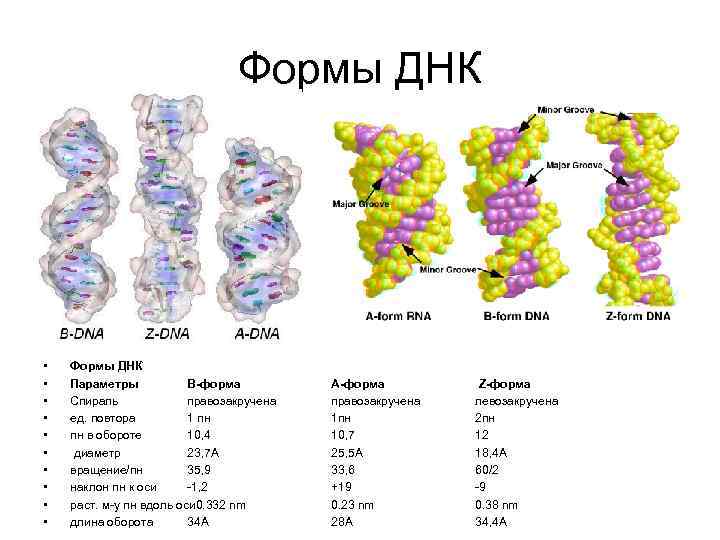
Формы ДНК • • • Формы ДНК Параметры B-форма Спираль правозакручена ед. повтора 1 пн пн в обороте 10, 4 диаметр 23, 7 А вращение/пн 35, 9 наклон пн к оси -1, 2 раст. м-у пн вдоль оси 0. 332 nm длина оборота 34 А А-форма правозакручена 1 пн 10, 7 25, 5 А 33, 6 +19 0. 23 nm 28 А Z-форма левозакручена 2 пн 12 18, 4 А 60/2 -9 0. 38 nm 34, 4 А
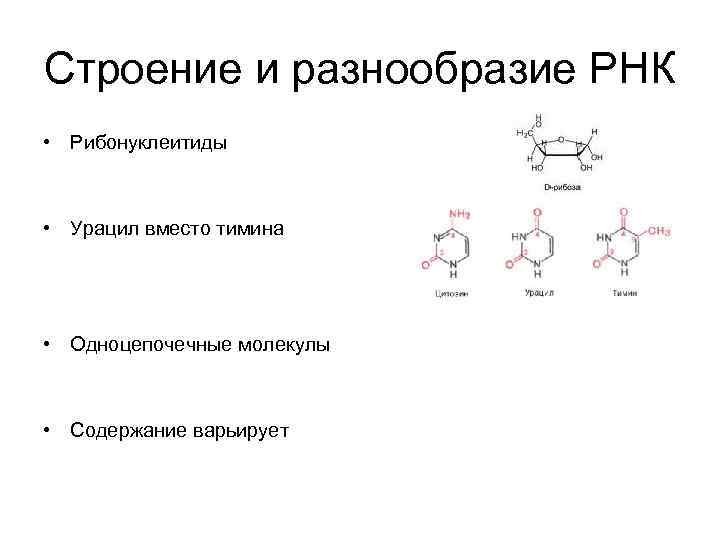
Строение и разнообразие РНК • Рибонуклеитиды • Урацил вместо тимина • Одноцепочечные молекулы • Содержание варьирует
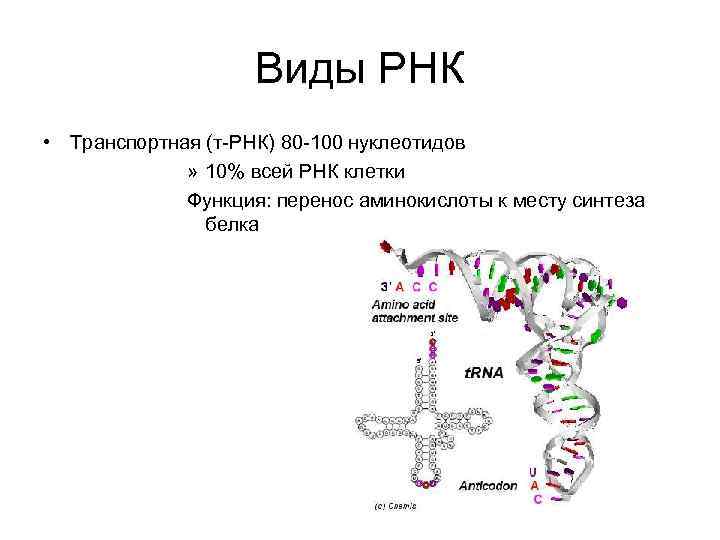
Виды РНК • Транспортная (т-РНК) 80 -100 нуклеотидов » 10% всей РНК клетки Функция: перенос аминокислоты к месту синтеза белка
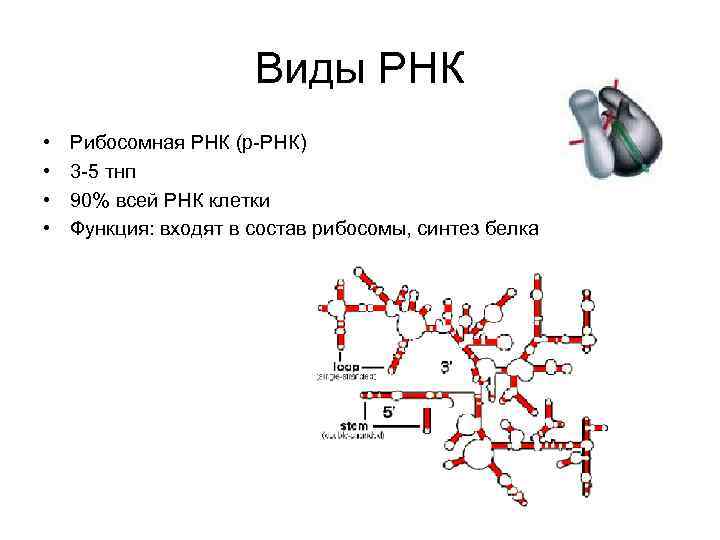
Виды РНК • • Рибосомная РНК (р-РНК) 3 -5 тнп 90% всей РНК клетки Функция: входят в состав рибосомы, синтез белка

ВИДЫ РНК • • Информационная, или матричная РНК (м-РНК) 1 -100 тнп 0. 5 -1% всей РНК клетки Функция: перенос информации о структуре белка от ДНК к месту синтеза белка
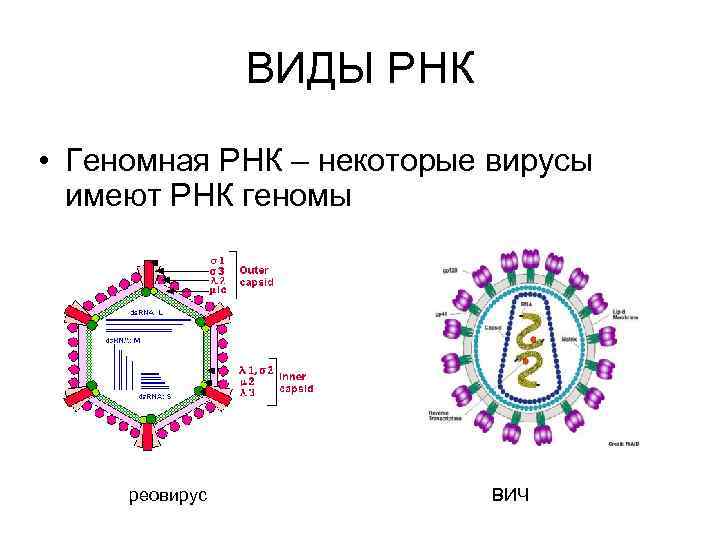
ВИДЫ РНК • Геномная РНК – некоторые вирусы имеют РНК геномы реовирус ВИЧ
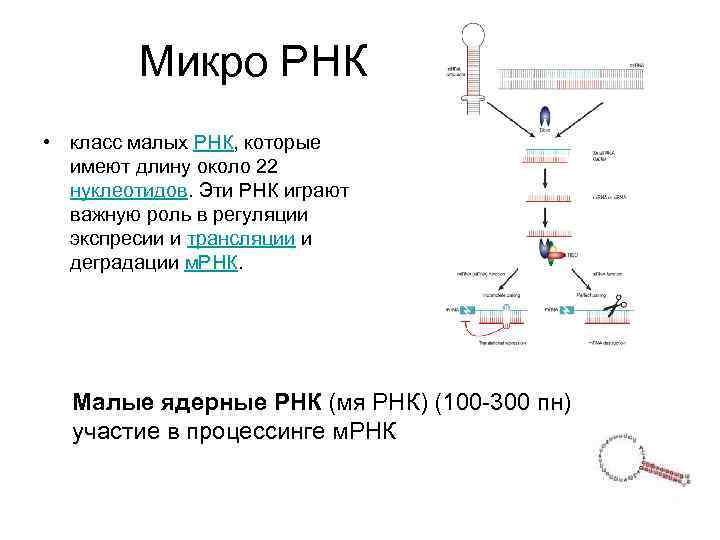
Микро РНК • класс малых РНК, которые имеют длину около 22 нуклеотидов. Эти РНК играют важную роль в регуляции экспресии и трансляции и деградации м. РНК. Малые ядерные РНК (мя РНК) (100 -300 пн) участие в процессинге м. РНК
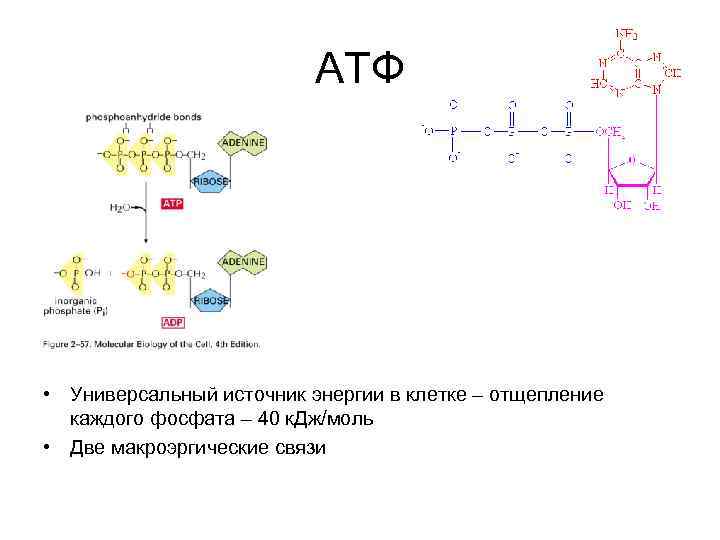
АТФ • Универсальный источник энергии в клетке – отщепление каждого фосфата – 40 к. Дж/моль • Две макроэргические связи
Способы изучения нуклеиновых кислот • Электрофорез • Рестрикционный анализ • Секвенирование
L2_СТРОЕНИЕ И СВОЙСТВА БИОПОЛИМЕРОВ.ppt