строение атома.pptx
- Количество слайдов: 21

СТРОЕНИЕ ЭЛЕКТРОННЫХ ОБОЛОЧЕК АТОМОВ

. Я дерная реа кция — процесс образования новых ядер или частиц при столкновениях ядер или частиц. Впервые ядерную реакцию наблюдал Резерфорд в 1919 году, бомбардируя αчастицами ядра атомов азота
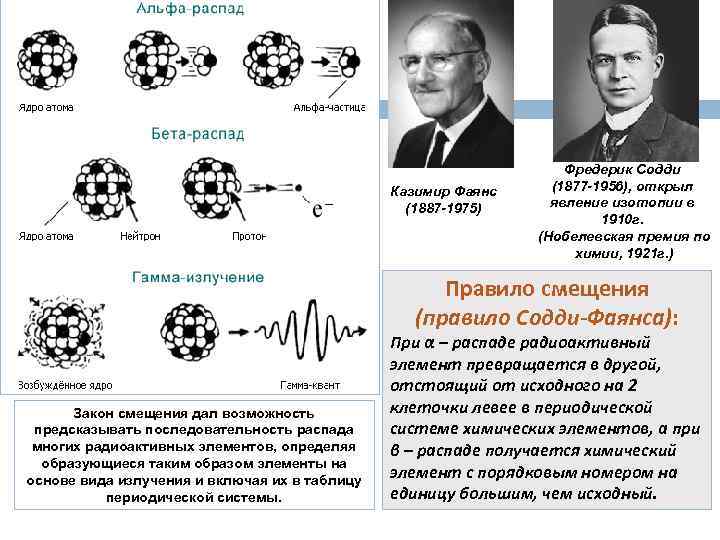
Казимир Фаянс (1887 -1975) Фредерик Содди (1877 -1956), открыл явление изотопии в 1910 г. (Нобелевская премия по химии, 1921 г. ) Правило смещения (правило Содди-Фаянса): Закон смещения дал возможность предсказывать последовательность распада многих радиоактивных элементов, определяя образующиеся таким образом элементы на основе вида излучения и включая их в таблицу периодической системы. При α – распаде радиоактивный элемент превращается в другой, отстоящий от исходного на 2 клеточки левее в периодической системе химических элементов, а при β – распаде получается химический элемент с порядковым номером на единицу большим, чем исходный.

ОБОЗНАЧЕНИЕ ЯДРА АТОМА АЛЬФА α - РАСПАД - характерен для радиоактивных элементов с порядковым номером больше 83 - обязательно выполняется закон сохранения массового и зарядового числа. - часто сопровождается гаммаизлучением. Реакция альфа-распада: БЕТА β - РАСПАД - часто сопровождается гаммаизлучением. - может сопровождаться образованием антинейтрино ( легких электрически нейтральных частиц, обладающих большой проникающей способностью). - обяэательно должен выполняться закон сохранения массового и зарядового числа. Реакция бета-распада: ГАММА γ -распад – это поток электромагнитного излучения с очень короткой длиной волны и очень высокой (интенсивной) частотой, при этом массовое число и заряд ядра не изменяются, а энергия ядра уменьшается. Закон сохранения массового числа и заряда: Сумма зарядов (массовых чисел) продуктов распада равна заряду (массовому числу) исходного ядра

Написание уравнений ядерных реакций
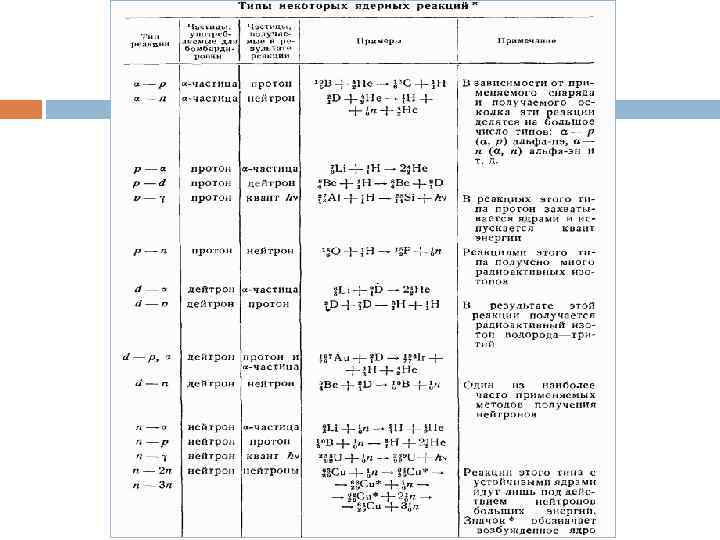

Ответьте на вопросы Чем можно объяснить различие в свойствах элементов? - Причина – различие атомов (различное число протонов и электронов) Чем можно объяснить сходство некоторых элементов? - Причина – сходство внутреннего строения атома

Электронная оболочка Совокупность всех электронов в атоме, окружающих ядро Каждый электрон имеет свою траекторию движения и запас энергии Электроны расположены на различном расстоянии от ядра: чем ближе электрон к ядру, тем он прочнее с ним связан, его труднее вырвать из электронной оболочки По мере удаления от ядра запас энергии электрона увеличивается, а связь с ядром становится слабее
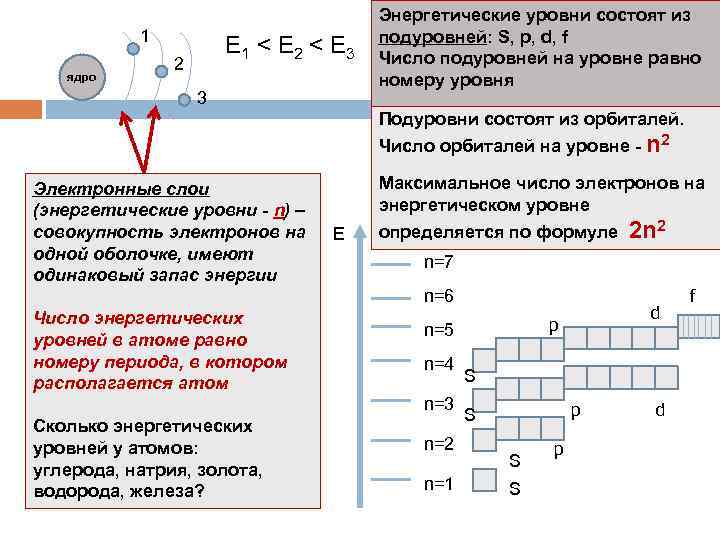
1 ядро Е 1 < E 2 < E 3 2 3 Энергетические уровни состоят из подуровней: S, p, d, f Число подуровней на уровне равно номеру уровня Подуровни состоят из орбиталей. Число орбиталей на уровне - n 2 Электронные слои (энергетические уровни - n) – совокупность электронов на одной оболочке, имеют одинаковый запас энергии Максимальное число электронов на энергетическом уровне Е определяется по формуле n=7 n=6 Число энергетических уровней в атоме равно номеру периода, в котором располагается атом n=4 n=2 n=1 d p n=5 n=3 Сколько энергетических уровней у атомов: углерода, натрия, золота, водорода, железа? 2 n 2 S p S S S p d f

Энергетические уровни, содержащие максимальное число электронов, называются завершенными. Они обладают повышенной устойчивостью и стабильностью Энергетические уровни, содержащие меньшее число электронов, называются незавершенными n=1 – 1 подуровень (S), 2 электрона n=2 – 2 подуровня (S, р), 8 электронов n=3 – 3 подуровня (S, р, d), 18 электронов n=4 – 4 подуровня (S, р, d, f), 32 электрона

Запомните! Электроны, расположенные на последней электронной оболочке, называются внешними. Число внешних электронов для химических элементов главных подгрупп равно номеру группы, в которой находится элемент
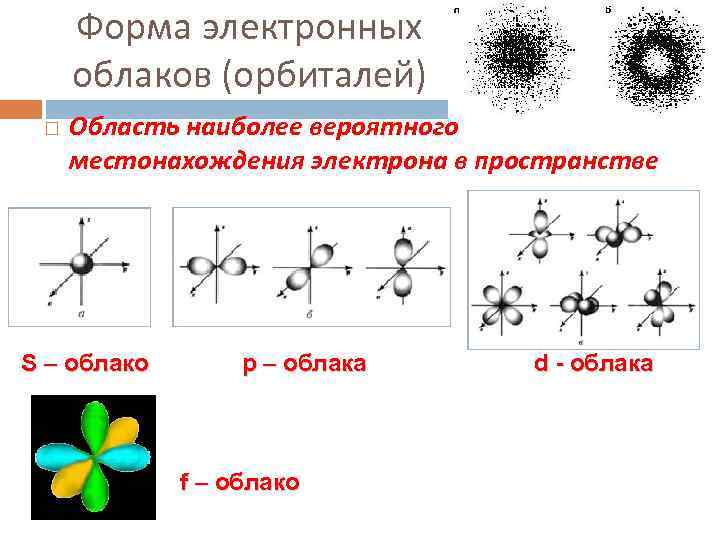
Форма электронных облаков (орбиталей) Область наиболее вероятного местонахождения электрона в пространстве S – облако р – облака f – облако d - облака
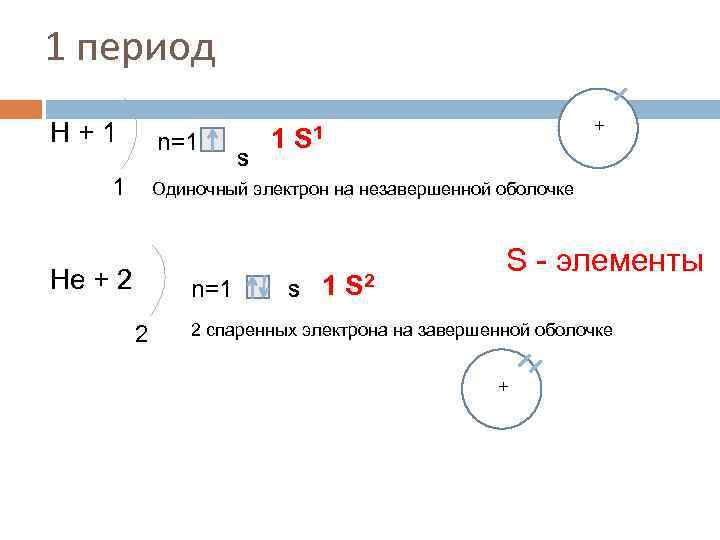
1 период Н+1 n=1 1 S + 1 S 1 Одиночный электрон на незавершенной оболочке Нe + 2 n=1 2 S 1 S 2 S - элементы 2 спаренных электрона на завершенной оболочке +
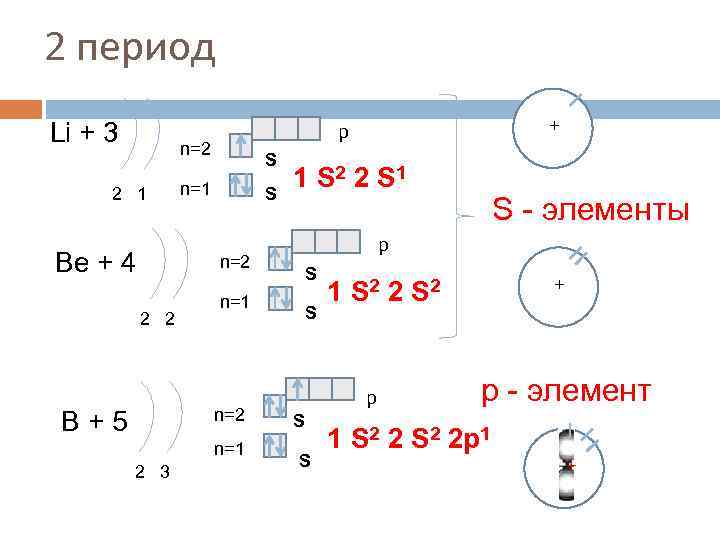
2 период Li + 3 n=2 2 1 Be + 4 S n=1 S n=2 2 2 n=1 n=2 B+5 n=1 2 3 + p 1 S 2 2 S 1 S - элементы p S S + 1 S 2 2 S 2 р - элемент 1 S 2 2 p 1 + +
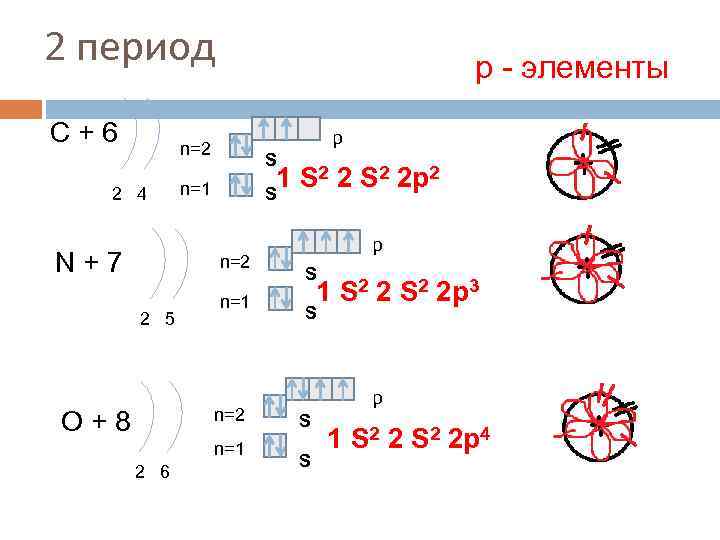
2 период С+6 р - элементы p n=2 2 4 N+7 S 1 S 2 2 p 2 S n=1 n=2 2 5 n=1 n=2 O+8 n=1 2 6 p S 1 S 2 2 p 3 S p S S 1 S 2 2 p 4
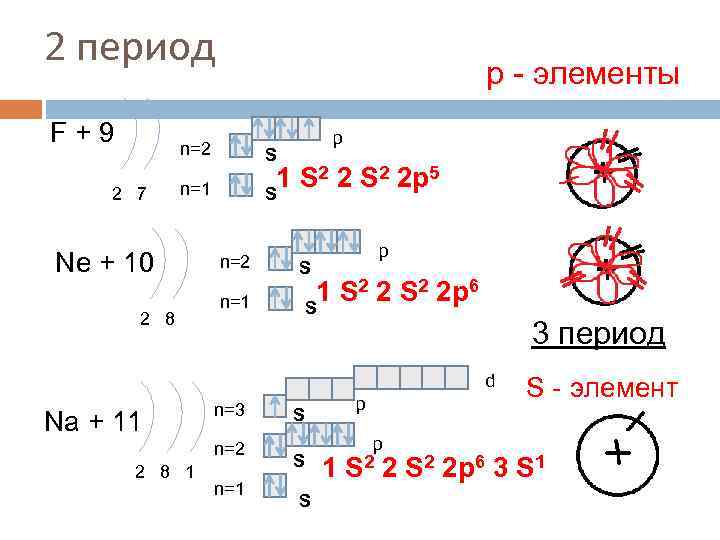
2 период F+9 р - элементы n=2 2 7 S 1 S 2 2 p 5 S n=1 Ne + 10 2 8 p n=2 n=1 p S 1 S 2 2 p 6 S 3 период d Na + 11 n=3 n=2 2 8 1 n=1 p S S S 1 p S 2 2 S - элемент S 2 2 p 6 3 S 1
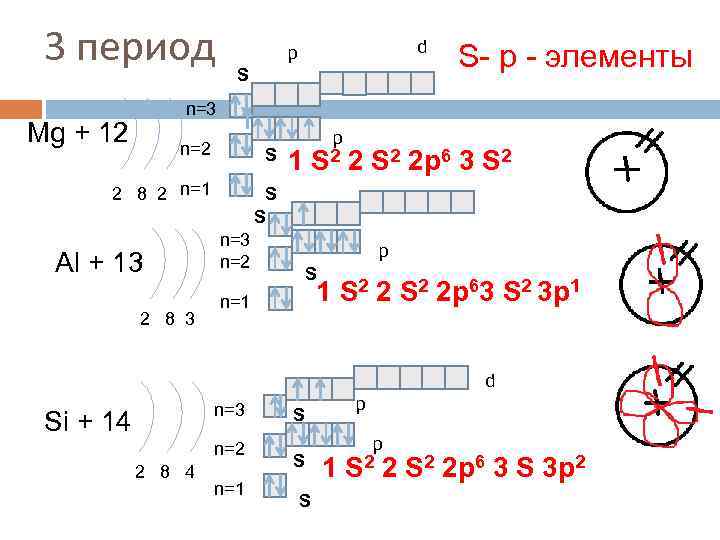
3 период d p S S- р - элементы n=3 Mg + 12 n=2 S 2 8 2 n=1 p S 2 2 S S Al + 13 2 8 3 n=2 1 S 2 2 p 6 3 S 2 p S 1 S 2 2 p 63 S 2 3 p 1 n=1 d n=3 Si + 14 n=2 2 8 4 n=1 p S S S 1 p S 2 2 p 6 3 S 3 p 2
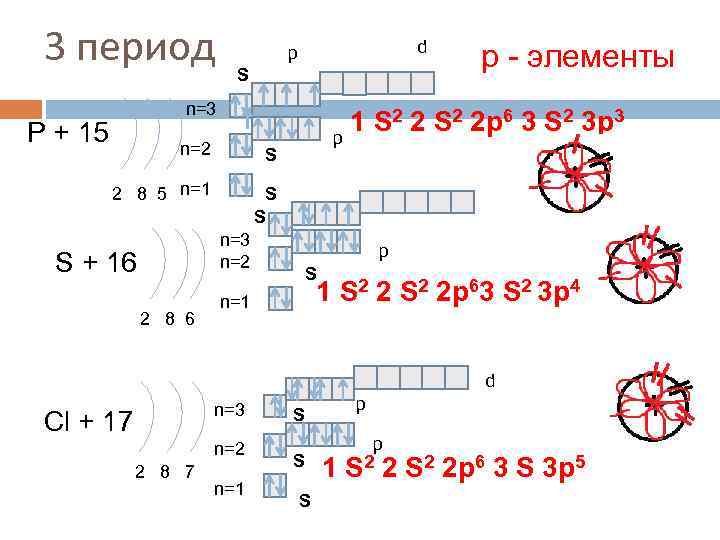
3 период d p S n=3 P + 15 n=2 1 S 2 2 p 6 3 S 2 3 p 3 p S 2 8 5 n=1 р - элементы S S n=3 n=2 S + 16 2 8 6 p S 1 S 2 2 p 63 S 2 3 p 4 n=1 d n=3 Cl + 17 n=2 2 8 7 n=1 p S S S 1 p S 2 2 p 6 3 S 3 p 5
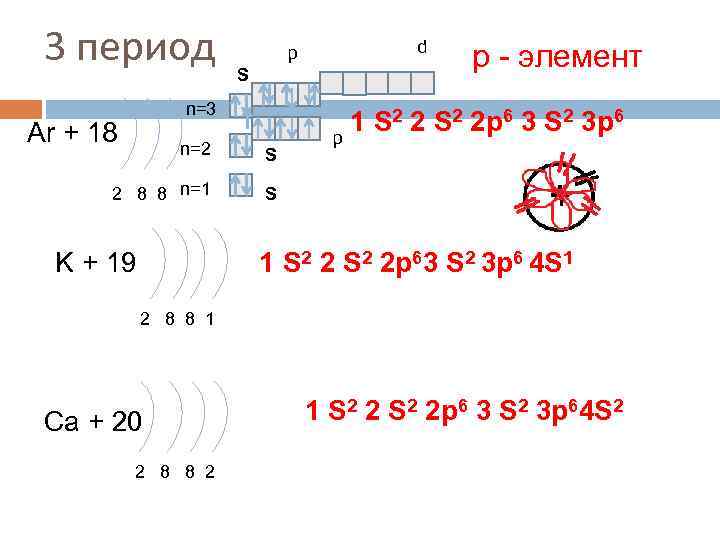
3 период p S n=3 Ar + 18 n=2 S 2 8 8 n=1 d р - элемент 1 S 2 2 p 6 3 S 2 3 p 6 p S 1 S 2 2 p 63 S 2 3 p 6 4 S 1 K + 19 2 8 8 1 Ca + 20 2 8 8 2 1 S 2 2 p 6 3 S 2 3 p 64 S 2

Выводы Причина сходства элементов заключается в одинаковом строении внешних энергетических уровней их атомов Одинаковое строение внешних энергетических уровней периодически (т. е. через определенные промежутки - периоды) повторяется, поэтому периодически повторяются и свойства химических элементов

Домашнее задание Параграф 8, записи в тетради Зарисовать строение химических элементов 3 периода Упражнения 2 -5, стр. 52 -53
строение атома.pptx