834600.ppt
- Количество слайдов: 23

«Строение электронных оболочек атомов химических элементов» 8 класс Учитель химии МКОУ «Сибирякская СОШ» Сиражеева Л. Р.

ВСПОМНИМ ØЧему равно общее количество электронов в атоме? ØЧто такое энергетический уровень? ØКак определить число энергетических уровней? ØКак определить число электронов на внешнем уровне?

ЗАПОМНИМ Электроны, расположенные на последней электронной оболочке, называются внешними. Ø Число внешних электронов для химических элементов главных подгрупп равно номеру группы, в которой находится элемент Ø

Проверим домашнее задание Задания 1. По данным определить, какой это элемент Вариант I а)2 e 8 e 3 e б)2 e 1 e в)2 e 8 e 8 e 2. Определить а)2 период элемент по его 3 группа главная положению в ПСХЭ подгруппа б)5 период 1 группа побочная подгруппа Вариант II а)2 e 4 e б)2 e 8 e 7 e в)1 e а)4 период 3 группа побочная подгруппа б)2 период 6 группа главная подгруппа

Проверьте себя и поставьте оценку, равную количеству правильных ответов Задание 1 Вариант I - а) Al б) Li в)Ar Вариант II - а) С б) С l в)Н Задание 2 Вариант I - а)В б)Аg Вариант II - а) Ga б) O

ТЕМА УРОКА «Строение электронных оболочек атомов химических элементов № 1 -20»

Цель урока: Ø научиться составлять электронные формулы атомов элементов первых трех периодов ПСХЭ; Ø объяснять зависимость и закономерные изменения свойств химических элементов от электронного строения их атомов.

Электронная оболочка Ø Совокупность всех электронов в атоме, окружающих ядро Ø Каждый электрон имеет свою траекторию движения и запас энергии Ø Электроны расположены на различном расстоянии от ядра: чем ближе электрон к ядру, тем он прочнее с ним связан, его труднее вырвать из электронной оболочки Ø По мере удаления от ядра запас энергии электрона увеличивается, а связь с ядром становится слабее

Форма электронных облаков (орбиталей) Область наиболее вероятного местонахождения электрона в пространстве S – облако p- облака d - облака http: //files. school-collection. edu. ru/dlrstore/bb 14 a 035 -aae 7 -11 db-abbd-0800200 c 9 a 66/ch 08_08_08. swf

Алгоритм составления электронных формул. Записываем знак химического элемента и заряд ядра его атома – он равен порядковому номеру элемента. Ø Определяем количество энергетических уровней (оно равно номеру периода) и количество электронов на каждом уровне. Ø Составляем электронную формулу, учитывая порядок заполнения каждого уровня – сначала sэлектроны, затем – р-электроны: номер уровня, вид орбитали и количество электронов на ней. Ø http: //files. school-collection. edu. ru/dlrstore/bb 14 a 033 -aae 7 -11 db-abbd 0800200 c 9 a 66/ch 08_08_06. swf

1 период Н+1 n=1 1 S 1 Одиночный электрон на незавершенной оболочке Нe + 2 n=1 2 S 1 S 2 S - элементы 2 спаренных электрона на завершенной оболочке
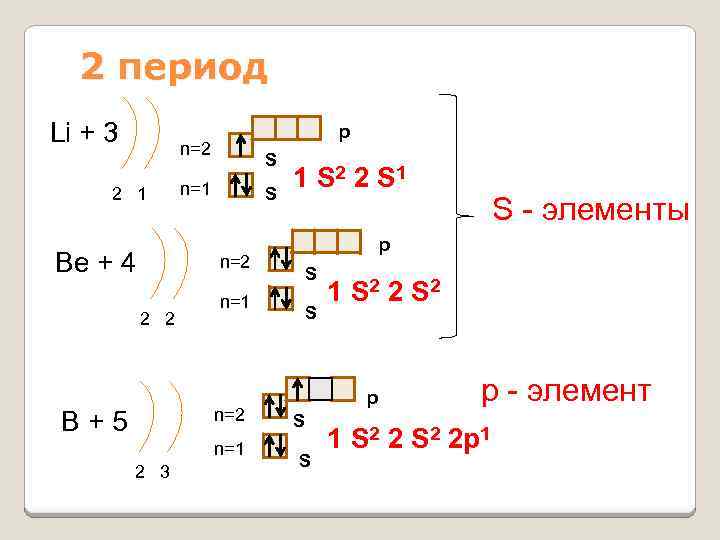
2 период Li + 3 p n=2 2 1 Be + 4 S n=1 S n=2 2 2 n=1 n=2 B+5 n=1 2 3 1 S 2 2 S 1 S - элементы p S S 1 S 2 2 S 2 p S S р - элемент 1 S 2 2 p 1

2 период С+6 p n=2 2 4 N+7 S 1 S 2 2 p 2 S n=1 n=2 2 5 n=1 n=2 O+8 n=1 2 6 р - элементы p S 1 S 2 2 p 3 S p S S 1 S 2 2 p 4
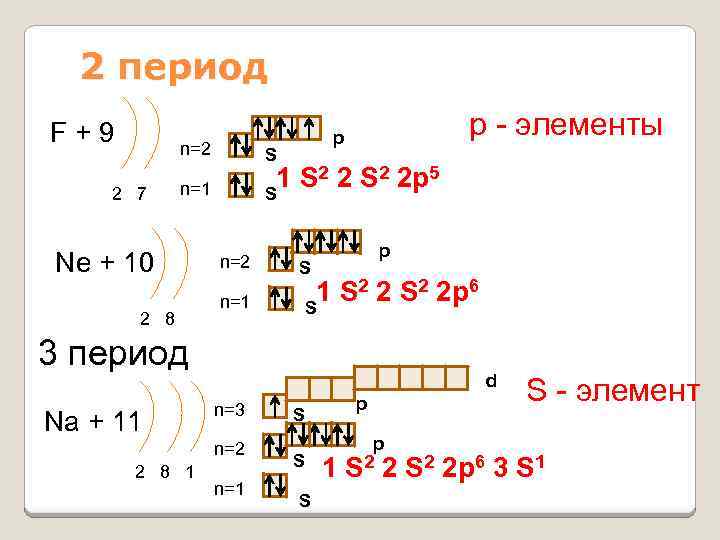
2 период F+9 n=2 2 7 S 1 S 2 2 p 5 S n=1 Ne + 10 2 8 р - элементы p n=2 n=1 p S 1 S 2 2 p 6 S 3 период Na + 11 d n=3 n=2 2 8 1 n=1 p S S S 1 p S 2 2 S - элемент S 2 2 p 6 3 S 1
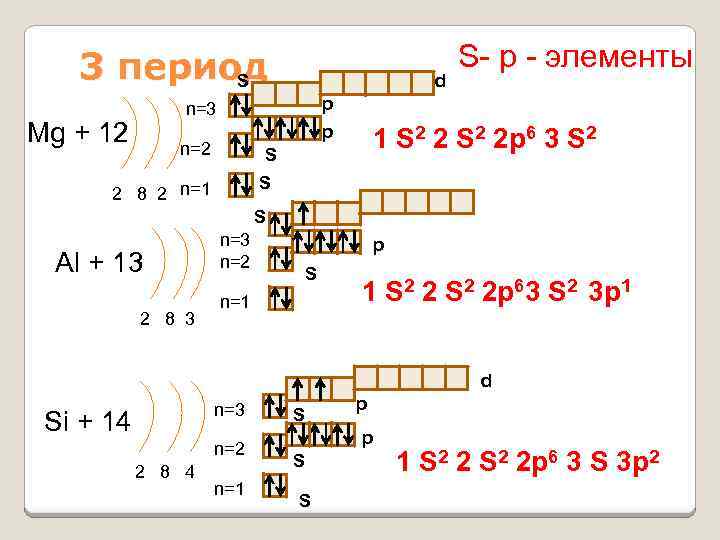
3 период S d p n=3 Mg + 12 S- р - элементы p n=2 1 S 2 2 p 6 3 S 2 S S 2 8 2 n=1 S Al + 13 2 8 3 n=2 p S n=1 1 S 2 2 p 63 S 2 3 p 1 d n=3 Si + 14 n=2 2 8 4 n=1 S p p S S 1 S 2 2 p 6 3 S 3 p 2
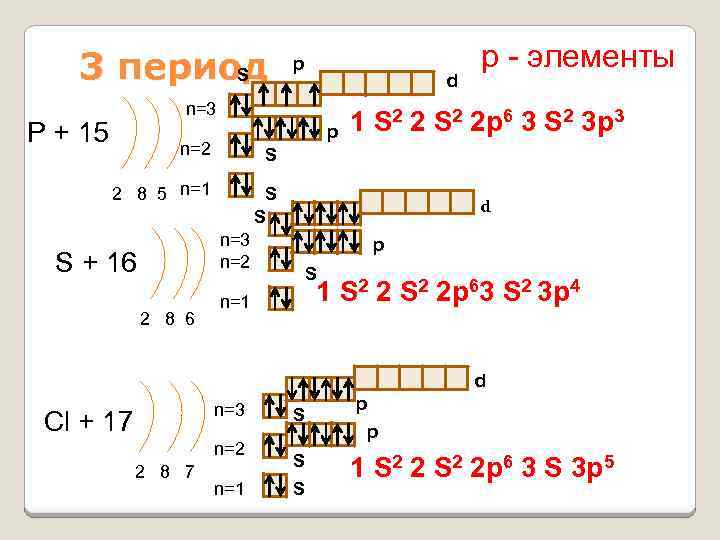
3 период S p d n=3 P + 15 p n=2 1 S 2 2 p 6 3 S 2 3 p 3 S 2 8 5 n=1 р - элементы S S n=3 n=2 S + 16 2 8 6 d p S 1 S 2 2 p 63 S 2 3 p 4 n=1 d n=3 Cl + 17 n=2 2 8 7 n=1 S S S p p 1 S 2 2 p 6 3 S 3 p 5
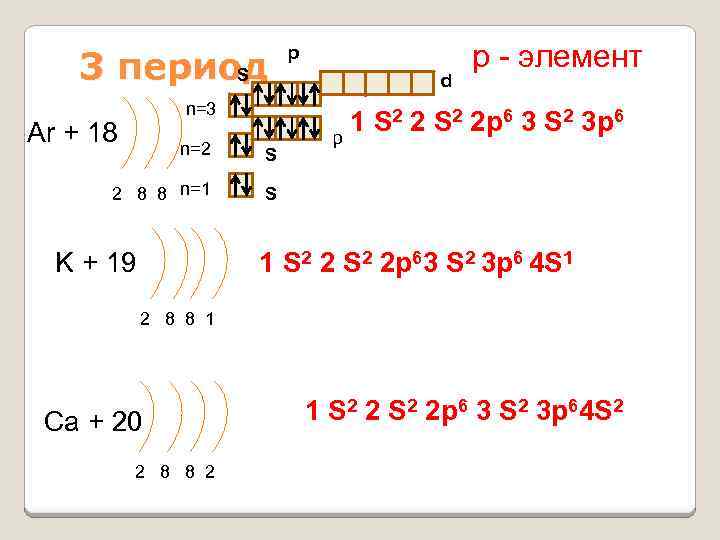
3 период S n=3 Ar + 18 n=2 S 2 8 8 n=1 p d р - элемент 1 S 2 2 p 6 3 S 2 3 p 6 p S K + 19 1 S 2 2 p 63 S 2 3 p 6 4 S 1 2 8 8 1 Ca + 20 2 8 8 2 1 S 2 2 p 6 3 S 2 3 p 64 S 2

Физкультминутка Следим глазами

Закрепление материала Ø Определить число орбиталей http: //files. school-collection. edu. ru/dlrstore/bb 14 a 031 -aae 7 -11 db-abbd-0800200 c 9 a 66/ch 08_08_04. swf Ø Определить число электронов на внешнем электронном уровне http: //files. school-collection. edu. ru/dlrstore/bb 14 a 032 -aae 7 -11 db-abbd-0800200 c 9 a 66/ch 08_08_05. swf Ø Определить общее число электронов на энергетическом уровне http: //files. school-collection. edu. ru/dlrstore/bb 14 a 030 -aae 7 -11 db-abbd-0800200 c 9 a 66/ch 08_08_03. swf Ø тест «электронные формулы атомов элементов» http: //files. school-collection. edu. ru/dlrstore/bb 14 a 038 -aae 7 -11 db-abbd 0800200 c 9 a 66/ch 08_08_11. swf

Ответьте на вопросы ØКакие данные об особенностях строения атома отражает электронная формула? ØВ чем заключается причина сходства элементов, расположенных в одной группе?

Выводы Причина сходства элементов заключается в одинаковом строении внешних энергетических уровней их атомов Ø Одинаковое строение внешних энергетических уровней периодически (т. е. через определенные промежутки - периоды) повторяется, поэтому периодически повторяются и свойства химических элементов Ø

Домашнее задание Ø Повторить основные понятия темы на странице с. 46 -53 учебника Ø Задание № 2, 3 письменно

Ресурсы http: //fcior. edu. ru – сайт Федерального центра информационнообразовательных ресурсов. ФЦИОР реализует концепцию "единого окна" для доступа к любым электронным образовательным ресурсам системы образования РФ и предоставление единой современной технологической платформы для существующих и вновь создаваемых электронных образовательных ресурсов. http: //rusedu. ru – Архив учебных программ и презентаций. На сайте представлены разработки уроков с использованием ИКТ, программы, пособия и методики. http: //openclass. ru – «Открытый класс» . http: //school–collection. edu. ru - «Единая коллекция цифровых образовательных ресурсов» http: //lyalyasirazhee. ucoz. ru - адрес личного сайта
834600.ppt