строение атома.pptx
- Количество слайдов: 27
 Строение атома.
Строение атома.
 Пудинг с изюмом « Пудинг с изюмом» 1904 г. Дж. Томсон «О структуре атома»
Пудинг с изюмом « Пудинг с изюмом» 1904 г. Дж. Томсон «О структуре атома»
 Планетарная модель Резерфорд Э. Атом состоит из положительно заряженного ядра и электронов, движущихся вокруг ядра по замкнутым орбитам. Подобно движению планет вокруг Солнца
Планетарная модель Резерфорд Э. Атом состоит из положительно заряженного ядра и электронов, движущихся вокруг ядра по замкнутым орбитам. Подобно движению планет вокруг Солнца
 Квантовая модель 1913 г. Н. Бор Первый постулат. Электрон движется вокруг ядра по строго определенным замкнутым стационарным орбитам в соответствии с разрешенными значениями энергии, при этом энергии не поглощается и не излучается. Второй постулат. Электрон может переходить из одного разрешенного энергетического состояния в другое, что сопровождается излечением или поглощением кванта энергии Электрон- частица, движущаяся по строго определенной скорости по строго определенным траекториям
Квантовая модель 1913 г. Н. Бор Первый постулат. Электрон движется вокруг ядра по строго определенным замкнутым стационарным орбитам в соответствии с разрешенными значениями энергии, при этом энергии не поглощается и не излучается. Второй постулат. Электрон может переходить из одного разрешенного энергетического состояния в другое, что сопровождается излечением или поглощением кванта энергии Электрон- частица, движущаяся по строго определенной скорости по строго определенным траекториям
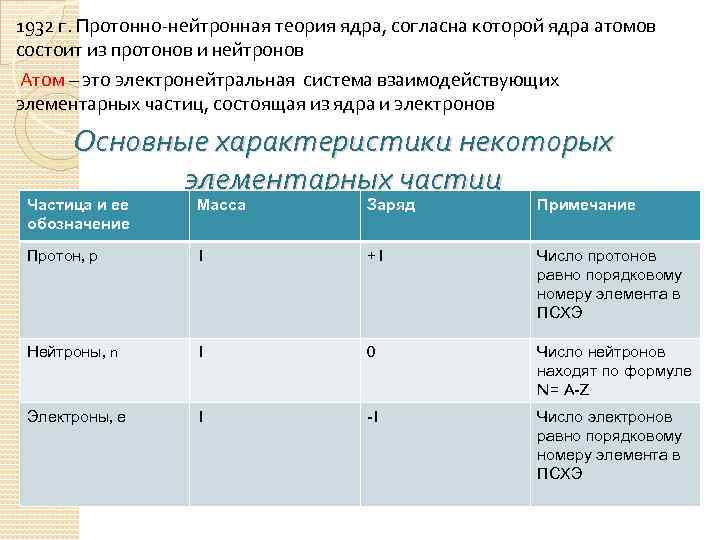 1932 г. Протонно-нейтронная теория ядра, согласна которой ядра атомов состоит из протонов и нейтронов Атом – это электронейтральная система взаимодействующих элементарных частиц, состоящая из ядра и электронов Основные характеристики некоторых элементарных частиц Частица и ее обозначение Масса Заряд Примечание Протон, р 1 +1 Число протонов равно порядковому номеру элемента в ПСХЭ Нейтроны, n 1 0 Число нейтронов находят по формуле N= A-Z Электроны, е 1 -1 Число электронов равно порядковому номеру элемента в ПСХЭ
1932 г. Протонно-нейтронная теория ядра, согласна которой ядра атомов состоит из протонов и нейтронов Атом – это электронейтральная система взаимодействующих элементарных частиц, состоящая из ядра и электронов Основные характеристики некоторых элементарных частиц Частица и ее обозначение Масса Заряд Примечание Протон, р 1 +1 Число протонов равно порядковому номеру элемента в ПСХЭ Нейтроны, n 1 0 Число нейтронов находят по формуле N= A-Z Электроны, е 1 -1 Число электронов равно порядковому номеру элемента в ПСХЭ
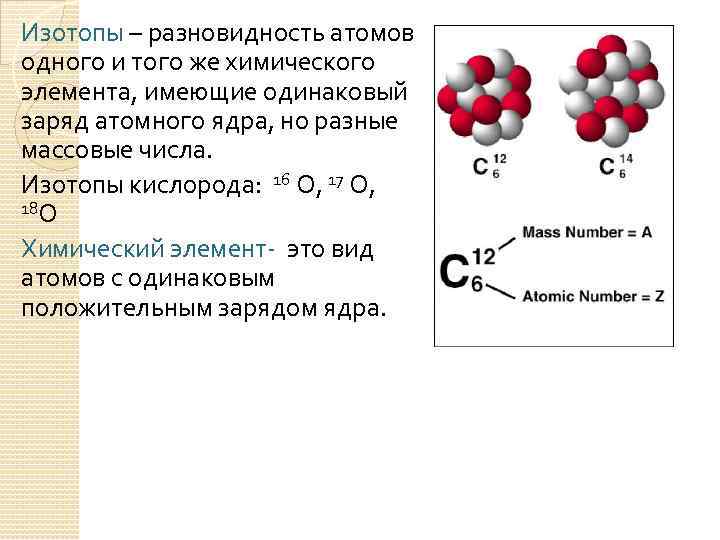 Изотопы – разновидность атомов одного и того же химического элемента, имеющие одинаковый заряд атомного ядра, но разные массовые числа. Изотопы кислорода: 16 О, 17 О, 18 О Химический элемент- это вид атомов с одинаковым положительным зарядом ядра.
Изотопы – разновидность атомов одного и того же химического элемента, имеющие одинаковый заряд атомного ядра, но разные массовые числа. Изотопы кислорода: 16 О, 17 О, 18 О Химический элемент- это вид атомов с одинаковым положительным зарядом ядра.
 Строение электронной оболочки Число электронных слоев, на которых располагаются электроны в атоме конкретного элемента, равно номеру периода в таблице Менделеева, в котором располагается элемент: у атомов элементов 1 го периода - один уровень, 2 -го периода- два, 7 -го периода-семь
Строение электронной оболочки Число электронных слоев, на которых располагаются электроны в атоме конкретного элемента, равно номеру периода в таблице Менделеева, в котором располагается элемент: у атомов элементов 1 го периода - один уровень, 2 -го периода- два, 7 -го периода-семь
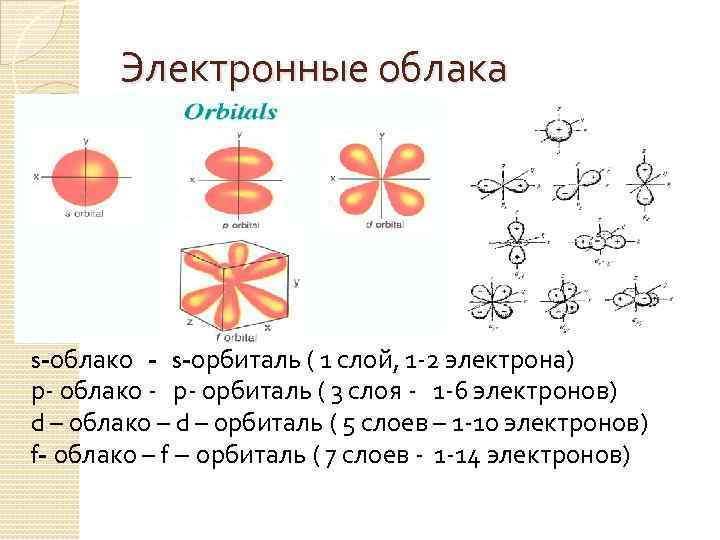 Электронные облака s-облако - s-орбиталь ( 1 слой, 1 -2 электрона) р- облако - р- орбиталь ( 3 слоя - 1 -6 электронов) d – облако – d – орбиталь ( 5 слоев – 1 -10 электронов) f- облако – f – орбиталь ( 7 слоев - 1 -14 электронов)
Электронные облака s-облако - s-орбиталь ( 1 слой, 1 -2 электрона) р- облако - р- орбиталь ( 3 слоя - 1 -6 электронов) d – облако – d – орбиталь ( 5 слоев – 1 -10 электронов) f- облако – f – орбиталь ( 7 слоев - 1 -14 электронов)
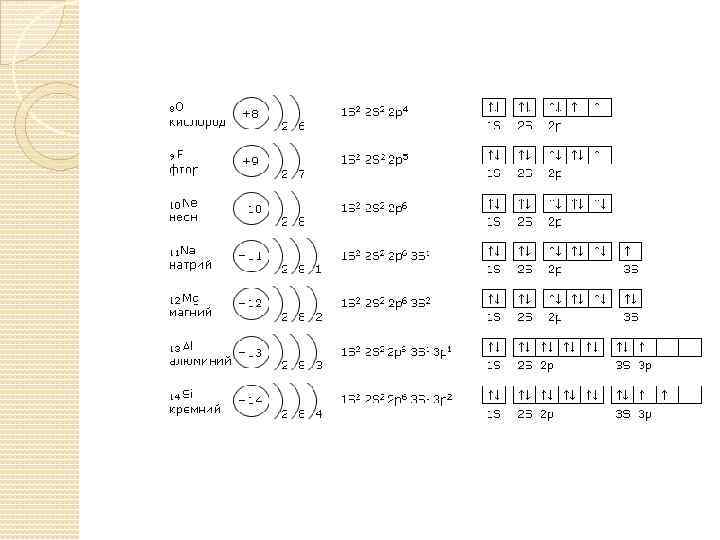
 s, p, d, f- семейства К s элементам относят элементы главных подгрупп I и II групп ПСХЭ К р элементам относят элементы главных подгрупп III и VIII групп ПСХЭ К d и f элементам относят химические элементы побочных подгрупп ПСХЭ О +8 1 s 2 2 p 4 (электронная конфигурация)
s, p, d, f- семейства К s элементам относят элементы главных подгрупп I и II групп ПСХЭ К р элементам относят элементы главных подгрупп III и VIII групп ПСХЭ К d и f элементам относят химические элементы побочных подгрупп ПСХЭ О +8 1 s 2 2 p 4 (электронная конфигурация)
 Очередность заполнения орбиталей электронами Правила заполнения орбиталей электронами: - В первую очередь заполняются орбитали, соответствующие наименьшей энергией (sорбиталь); - Орбитали одинаковой энергии заполняются сначала по одному электрону каждая, эти электроны имеют одинаковые спиновые квантовые числа
Очередность заполнения орбиталей электронами Правила заполнения орбиталей электронами: - В первую очередь заполняются орбитали, соответствующие наименьшей энергией (sорбиталь); - Орбитали одинаковой энергии заполняются сначала по одному электрону каждая, эти электроны имеют одинаковые спиновые квантовые числа
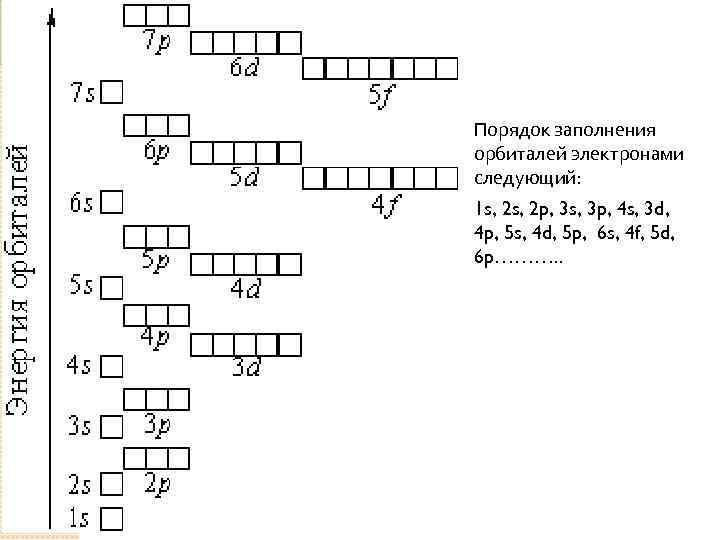 Порядок заполнения орбиталей электронами следующий: 1 s, 2 p, 3 s, 3 p, 4 s, 3 d, 4 p, 5 s, 4 d, 5 p, 6 s, 4 f, 5 d, 6 p………. .
Порядок заполнения орбиталей электронами следующий: 1 s, 2 p, 3 s, 3 p, 4 s, 3 d, 4 p, 5 s, 4 d, 5 p, 6 s, 4 f, 5 d, 6 p………. .
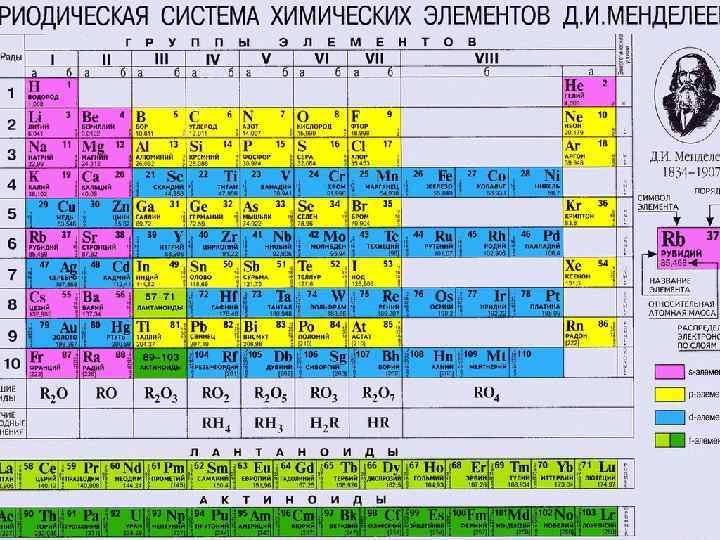
 Периодический закон Д. И. Менделеева
Периодический закон Д. И. Менделеева
 Открытие периодического закона Расположил все известные на тот момент элементы по возрастанию их атомных масс и отметил в нем отрезки - периоды, в которых свойства элементов и образованных ими веществ изменялись сходным образом: q Металлические свойства ослабевали q Неметаллические свойства усиливались q Валентность элемента в высших оксидах увеличивалась от I до VII q Валентность элементов в гидридах увеличивалась с I до III, а затем уменьшалась в летучих водородных соединениях с IV до I q Оксиды от основных через амфотерные сменялись кислотными q Гидроксиды от щелочей через амфотерные гидроксиды сменялись все более сильными кислотами
Открытие периодического закона Расположил все известные на тот момент элементы по возрастанию их атомных масс и отметил в нем отрезки - периоды, в которых свойства элементов и образованных ими веществ изменялись сходным образом: q Металлические свойства ослабевали q Неметаллические свойства усиливались q Валентность элемента в высших оксидах увеличивалась от I до VII q Валентность элементов в гидридах увеличивалась с I до III, а затем уменьшалась в летучих водородных соединениях с IV до I q Оксиды от основных через амфотерные сменялись кислотными q Гидроксиды от щелочей через амфотерные гидроксиды сменялись все более сильными кислотами
 Периодический закон на 1869 год Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от их атомных весов
Периодический закон на 1869 год Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от их атомных весов
 Периодический закон в свете учения о строении атома Заряд ядра атома каждого химического элемента в таблице Менделеева возрастает на единицу по сравнению с зарядом ядра атома предыдущего химического элемента. Заряд атомного ядра совпадает с порядковым номером элементов в таблице Менделеева
Периодический закон в свете учения о строении атома Заряд ядра атома каждого химического элемента в таблице Менделеева возрастает на единицу по сравнению с зарядом ядра атома предыдущего химического элемента. Заряд атомного ядра совпадает с порядковым номером элементов в таблице Менделеева
 Современная формулировка периодического закона Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от величины зарядов ядер их атомов
Современная формулировка периодического закона Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от величины зарядов ядер их атомов
 ПСХЭ Номер периода соответствует числу энергетических уровней в атоме. Номер группы соответствует числу электронов на внешнем энергетическом уровне атомов для элементов главных подгрупп или максимальному числу валентных электронов для элементов обоих подгрупп Валентные электроны- электроны, которые могут принять участие в образовании химической связи Высшая степень окисления элемента = № группы ( максимальная положительная) Низшая степень окисления = 8 – (№группы) ( наиболее отрицательная)
ПСХЭ Номер периода соответствует числу энергетических уровней в атоме. Номер группы соответствует числу электронов на внешнем энергетическом уровне атомов для элементов главных подгрупп или максимальному числу валентных электронов для элементов обоих подгрупп Валентные электроны- электроны, которые могут принять участие в образовании химической связи Высшая степень окисления элемента = № группы ( максимальная положительная) Низшая степень окисления = 8 – (№группы) ( наиболее отрицательная)
 В пределах одного и того же периода металлические свойства ослабевают, а неметаллические усиливаются, так как: Увеличивается заряды атомов атомных ядер элементов; Увеличивается число электронов в атомах элементов не изменяется Число энергетических уровней в атомах элементов не изменяется Радиус атомов уменьшается
В пределах одного и того же периода металлические свойства ослабевают, а неметаллические усиливаются, так как: Увеличивается заряды атомов атомных ядер элементов; Увеличивается число электронов в атомах элементов не изменяется Число энергетических уровней в атомах элементов не изменяется Радиус атомов уменьшается
 В пределах одной и той же группы металлические свойства усиливаются, неметаллические ослабевают, так как Увеличиваются заряды атомных ядер элементов Число электронов на внешнем энергетическом уровне не изменяется Увеличивается число энергетических уровней в атомах Увеличивается радиус атомов
В пределах одной и той же группы металлические свойства усиливаются, неметаллические ослабевают, так как Увеличиваются заряды атомных ядер элементов Число электронов на внешнем энергетическом уровне не изменяется Увеличивается число энергетических уровней в атомах Увеличивается радиус атомов
 Вывод В больших периодах (4 -6) эти изменения происходят медленнее, так как у атомов элементов побочных подгрупп строятся ( до 18 электронов) не внешний , а предвнешний уровень, и только потом начинает достраиваться внешний уровень ( 2 до 8 электронов в соответствии с номером группы).
Вывод В больших периодах (4 -6) эти изменения происходят медленнее, так как у атомов элементов побочных подгрупп строятся ( до 18 электронов) не внешний , а предвнешний уровень, и только потом начинает достраиваться внешний уровень ( 2 до 8 электронов в соответствии с номером группы).
 Примеры характеристики элементов по их положению в ПСХЭ Sn, олово, элемент главной подгруппы 4 группы ПСХЭ. Находится в 5 периоде. Заряд ядра равен 50 (+50). Электронное строение атома: 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 6 4 d 10 5 s 2 5 p 2 Валентными являются электроны 5 периода, их число равно 4. Типичный металл. Образует высший оксид Sn. O 2 гидрид Sn. H 4
Примеры характеристики элементов по их положению в ПСХЭ Sn, олово, элемент главной подгруппы 4 группы ПСХЭ. Находится в 5 периоде. Заряд ядра равен 50 (+50). Электронное строение атома: 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 6 4 d 10 5 s 2 5 p 2 Валентными являются электроны 5 периода, их число равно 4. Типичный металл. Образует высший оксид Sn. O 2 гидрид Sn. H 4
 Примеры характеристики элементов по их положению в ПСХЭ Br, элемент главной подгруппы 7 группы ПСХЭгалоген, находится в 4 периоде. Заряд ядра равен 35 (+35). Электронной строение атома: 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 5 Валентными являются электроны 4 энергетического уровня, их число равно 7. Типичный неметалл. Формулы высшего оксида Br 2 O 7, а водородного соединения HBr
Примеры характеристики элементов по их положению в ПСХЭ Br, элемент главной подгруппы 7 группы ПСХЭгалоген, находится в 4 периоде. Заряд ядра равен 35 (+35). Электронной строение атома: 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 5 Валентными являются электроны 4 энергетического уровня, их число равно 7. Типичный неметалл. Формулы высшего оксида Br 2 O 7, а водородного соединения HBr





