lektsia_po_khimii_2.ppt
- Количество слайдов: 30
 Строение атома. Периодическая система элементов Лекция 2 д. х. н. , доцент кафедры «Промышленная и экологическая безопасность» Подолина Елена Алексеевна
Строение атома. Периодическая система элементов Лекция 2 д. х. н. , доцент кафедры «Промышленная и экологическая безопасность» Подолина Елена Алексеевна
 План лекции Теории строения атома 2. Квантовые числа 3. Периодический закон Д. И. Менделеева 4. Структура периодической системы 5. Характеристика элемента на основании его положения в периодической системе 1.
План лекции Теории строения атома 2. Квантовые числа 3. Периодический закон Д. И. Менделеева 4. Структура периодической системы 5. Характеристика элемента на основании его положения в периодической системе 1.
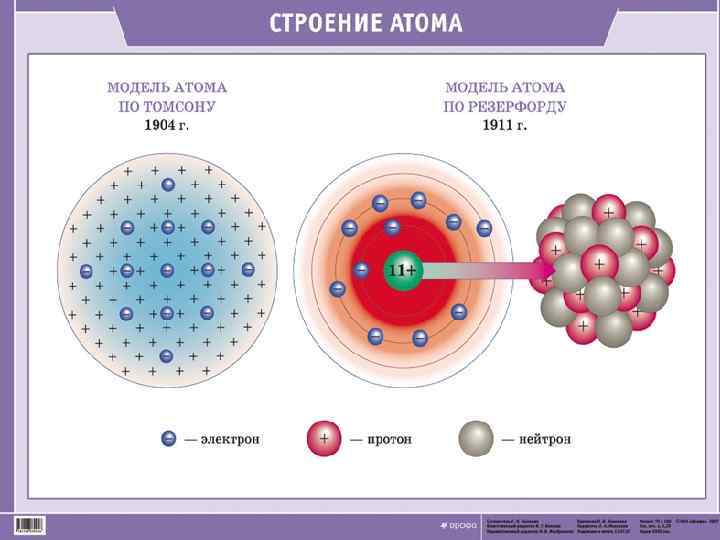
 § 1. Теории строения атома Атом – это электронейтральная система взаимодействующих элементарных частиц, состоящая из ядра (образованного протонами и нейтронами) и электронов. Доказательства сложности строения атома: Открытие рентгеновских лучей (1895 г. , К. Рентген); Открытие катодных лучей (1897 г. , Дж. Томсон); Открытие радиоактивности (1896 г. , А. Беккерель) и ее излечение (1897÷ 1903 гг. , М. Склодовская-Кюри, П. Кюри). Модели строения атома «Пудинг с изюмом» (1902 -1904 гг. , В. Кельвин, Дж. Томсон); Планетарная (1907 г. , Э. Резерфорд); Квантовая модель (1913 г. , Н. Бор). Современные представления о строении атома на основе квантовой механики
§ 1. Теории строения атома Атом – это электронейтральная система взаимодействующих элементарных частиц, состоящая из ядра (образованного протонами и нейтронами) и электронов. Доказательства сложности строения атома: Открытие рентгеновских лучей (1895 г. , К. Рентген); Открытие катодных лучей (1897 г. , Дж. Томсон); Открытие радиоактивности (1896 г. , А. Беккерель) и ее излечение (1897÷ 1903 гг. , М. Склодовская-Кюри, П. Кюри). Модели строения атома «Пудинг с изюмом» (1902 -1904 гг. , В. Кельвин, Дж. Томсон); Планетарная (1907 г. , Э. Резерфорд); Квантовая модель (1913 г. , Н. Бор). Современные представления о строении атома на основе квантовой механики
 1. 1. Модель Дж. Томсона В 1904 г в работе «О структуре атома» Дж. Томсон дал описание модели «пудинг с изюмом» . Согласно этой модели атом представляет собой пудинг сферической формы, имеющий положительный заряд. Внутрь сферы вкраплены, как изюм в пудинге, отрицательно заряженные электроны. Электроны совершают колебательные движения, благодаря которым атом излучает электромагнитную энергию. Атом в целом электронейтрален. Модель атома Дж. Томсона не была подтверждена экспериментальными факторами и осталась гипотезой.
1. 1. Модель Дж. Томсона В 1904 г в работе «О структуре атома» Дж. Томсон дал описание модели «пудинг с изюмом» . Согласно этой модели атом представляет собой пудинг сферической формы, имеющий положительный заряд. Внутрь сферы вкраплены, как изюм в пудинге, отрицательно заряженные электроны. Электроны совершают колебательные движения, благодаря которым атом излучает электромагнитную энергию. Атом в целом электронейтрален. Модель атома Дж. Томсона не была подтверждена экспериментальными факторами и осталась гипотезой.
 1. 2. Планетарная модель Э. Резерфорда Согласно планетарной модели, предложенной Э. Резерфордом, атом состоит из положительно заряженного ядра и электронов, движущихся вокруг ядра по замкнутым орбитам, подобно движению планет вокруг Солнца. По Резерфорду: Вся масса атома сосредоточена в ядре, которое имеет небольшой размер ~10 -12 см и положительный заряд; Вокруг ядра вращаются отрицательно заряженные электроны.
1. 2. Планетарная модель Э. Резерфорда Согласно планетарной модели, предложенной Э. Резерфордом, атом состоит из положительно заряженного ядра и электронов, движущихся вокруг ядра по замкнутым орбитам, подобно движению планет вокруг Солнца. По Резерфорду: Вся масса атома сосредоточена в ядре, которое имеет небольшой размер ~10 -12 см и положительный заряд; Вокруг ядра вращаются отрицательно заряженные электроны.
 Модель Э. Резерфорда не объясняет излучение и поглощение энергии атомом. Если электрон ē вращается вокруг положительного ядра, то должно поддерживаться равенство между центростремительно силой (сила притяжения ē к ядру) и центробежной силой: l 2/r 2=mv 2/r Излучая непрерывно энергию ē, в конечном счете, должен упасть на ядро, а этого не происходит; Спектр излучаемый ē сплошной, а на самом деле – линейчатый. Спектр электромагнитного излучения
Модель Э. Резерфорда не объясняет излучение и поглощение энергии атомом. Если электрон ē вращается вокруг положительного ядра, то должно поддерживаться равенство между центростремительно силой (сила притяжения ē к ядру) и центробежной силой: l 2/r 2=mv 2/r Излучая непрерывно энергию ē, в конечном счете, должен упасть на ядро, а этого не происходит; Спектр излучаемый ē сплошной, а на самом деле – линейчатый. Спектр электромагнитного излучения
 1. 3. Квантовая модель Н. Бора В 1900 г. М. Планк высказал предположение, что вещества поглощают и испускают энергию дискретными порциями, названными им квантами. Энергия кванта Е пропорциональна частоте излучения (колебания)ν: Е=hν, где h – постоянная Планка 6, 626∙ 10 -34 Дж∙с; ν= с/λ, с – скорость света 3∙ 108 м/с ; λ – длина волны (м). В 1913 г. Н. Бор предложил квантовую модель строения атома, основанную на следующих постулатах: Первый постулат: электрон движется вокруг ядра по строго определенным замкнутым стационарным орбитам в соответствии с «разрешенными» значениями энергии Е 1, Е 2…Еn, при этом энергия не поглощается и не излучается; Каждая орбита имеет номер n (1, 2, 3, 4…), который назвали главным квантовым числом. Н. Бор вычислил радиус орбит, так радиус первой орбиты 5, 29∙ 10 -13 м, а радиус других орбит: rn=n 2(5, 29∙ 10 -13) Энергия электрона (э. В) зависела от значения главного квантового числа: Еn=-13, 6(1/n 2) Второй постулат: электрон может переходить из одного разрешенного энергетического состояния в другое, что сопровождается излучением или поглощением кванта энергии.
1. 3. Квантовая модель Н. Бора В 1900 г. М. Планк высказал предположение, что вещества поглощают и испускают энергию дискретными порциями, названными им квантами. Энергия кванта Е пропорциональна частоте излучения (колебания)ν: Е=hν, где h – постоянная Планка 6, 626∙ 10 -34 Дж∙с; ν= с/λ, с – скорость света 3∙ 108 м/с ; λ – длина волны (м). В 1913 г. Н. Бор предложил квантовую модель строения атома, основанную на следующих постулатах: Первый постулат: электрон движется вокруг ядра по строго определенным замкнутым стационарным орбитам в соответствии с «разрешенными» значениями энергии Е 1, Е 2…Еn, при этом энергия не поглощается и не излучается; Каждая орбита имеет номер n (1, 2, 3, 4…), который назвали главным квантовым числом. Н. Бор вычислил радиус орбит, так радиус первой орбиты 5, 29∙ 10 -13 м, а радиус других орбит: rn=n 2(5, 29∙ 10 -13) Энергия электрона (э. В) зависела от значения главного квантового числа: Еn=-13, 6(1/n 2) Второй постулат: электрон может переходить из одного разрешенного энергетического состояния в другое, что сопровождается излучением или поглощением кванта энергии.
 Теория Н. Бора позволила рассчитать энергию электронов, испускаемых при переходе электрона с одного уровня на другой. Теория Н. Бора получила экспериментальное подтверждение, но не смогла объяснить поведение электрона в магнитном поле и все атомные спектральные линии. Теория Н. Бора оказалась непригодной для многоэлектронных атомов.
Теория Н. Бора позволила рассчитать энергию электронов, испускаемых при переходе электрона с одного уровня на другой. Теория Н. Бора получила экспериментальное подтверждение, но не смогла объяснить поведение электрона в магнитном поле и все атомные спектральные линии. Теория Н. Бора оказалась непригодной для многоэлектронных атомов.
 Строение атома водорода
Строение атома водорода
 1. 4. Протонно-нейтронная теория В 1905 г. А. Эйнштейн предсказал, что любое излучение представляет собой поток квантов энергии, фотонами. Из теории Эйнштейна следует, что свет имеет двойственную (корпускулярно-волновую)природу. В 1924 г. Луи де Бройль выдвинул предположение, что электрон также характеризуется корпускулярно-волновым дуализмом. В 1927 г. В. Гейзенберг постулировал принцип неопределенности, согласно которому положение и импульс движения субатомной частицы (микрочастицы) принципиально невозможно определить в любой момент времени с абсолютной точностью. В каждый момент времени можно определить только лишь одно из этих свойств. Э. Шредингер в 1926 г вывел математическое описание электрона в атоме: оператор Лапласа, Е – полная энергия атома, ψ(x, y, z) – волновая функция. В 1932 г. была разработана протонно-нейтронная теория ядра, согласно которой ядра атомов состоят из протонов и нейтронов.
1. 4. Протонно-нейтронная теория В 1905 г. А. Эйнштейн предсказал, что любое излучение представляет собой поток квантов энергии, фотонами. Из теории Эйнштейна следует, что свет имеет двойственную (корпускулярно-волновую)природу. В 1924 г. Луи де Бройль выдвинул предположение, что электрон также характеризуется корпускулярно-волновым дуализмом. В 1927 г. В. Гейзенберг постулировал принцип неопределенности, согласно которому положение и импульс движения субатомной частицы (микрочастицы) принципиально невозможно определить в любой момент времени с абсолютной точностью. В каждый момент времени можно определить только лишь одно из этих свойств. Э. Шредингер в 1926 г вывел математическое описание электрона в атоме: оператор Лапласа, Е – полная энергия атома, ψ(x, y, z) – волновая функция. В 1932 г. была разработана протонно-нейтронная теория ядра, согласно которой ядра атомов состоят из протонов и нейтронов.

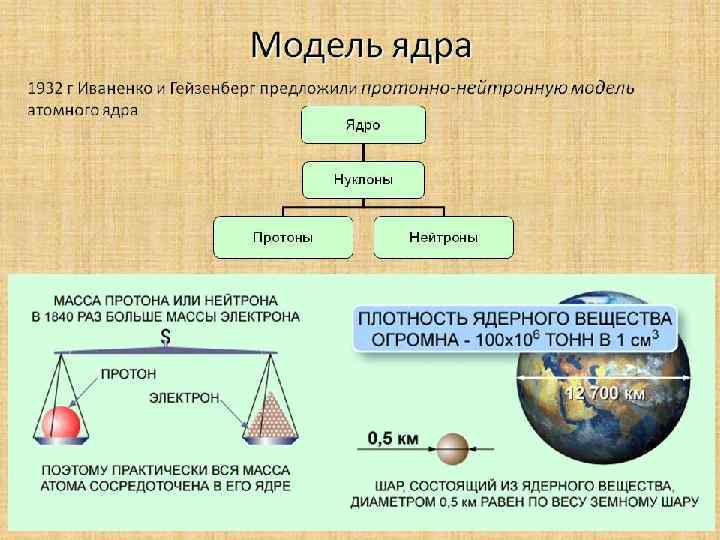
 § 2. Квантовые числа Пространство вокруг ядра, в котором наиболее вероятно пребывание электрона, называют орбиталью. Орбиталь можно однозначно описать с помощью целых чисел, называемых квантовыми и обозначают: главное квантовое число, орбитальное квантовое число, магнитное квантовое число. n – главное квантовое число, которое принимает значения от 1 до ∞, оно характеризует общий запас энергии электрона в атоме и номер стационарной орбиты на которой находится электрон в атоме. Электроны обладающие одним и тем же значением n образуют в атоме энергетический слой. Общее количество электронов в слое N вычисляется по формуле: N=2 n 2 На значение главного квантового числа (n) в периодической системе указывает номер периода, в котором находится химический элемент. значение п 1 2 3 4 5 6 7 обозначение слоя K L M N O P Q число электронов в слое 2 8 18 32 50 72 98
§ 2. Квантовые числа Пространство вокруг ядра, в котором наиболее вероятно пребывание электрона, называют орбиталью. Орбиталь можно однозначно описать с помощью целых чисел, называемых квантовыми и обозначают: главное квантовое число, орбитальное квантовое число, магнитное квантовое число. n – главное квантовое число, которое принимает значения от 1 до ∞, оно характеризует общий запас энергии электрона в атоме и номер стационарной орбиты на которой находится электрон в атоме. Электроны обладающие одним и тем же значением n образуют в атоме энергетический слой. Общее количество электронов в слое N вычисляется по формуле: N=2 n 2 На значение главного квантового числа (n) в периодической системе указывает номер периода, в котором находится химический элемент. значение п 1 2 3 4 5 6 7 обозначение слоя K L M N O P Q число электронов в слое 2 8 18 32 50 72 98
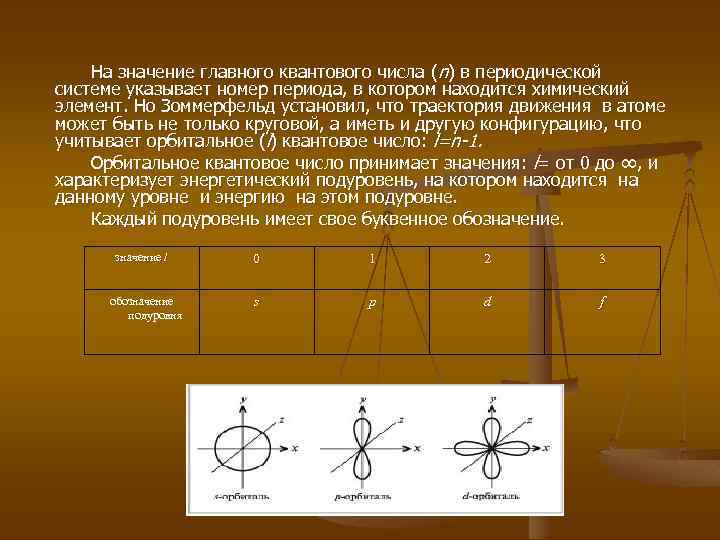 На значение главного квантового числа (n) в периодической системе указывает номер периода, в котором находится химический элемент. Но Зоммерфельд установил, что траектория движения в атоме может быть не только круговой, а иметь и другую конфигурацию, что учитывает орбитальное (l) квантовое число: l=n-1. Орбитальное квантовое число принимает значения: l= от 0 до ∞, и характеризует энергетический подуровень, на котором находится на данному уровне и энергию на этом подуровне. Каждый подуровень имеет свое буквенное обозначение l обозначение подуровня 0 1 2 3 s p d f
На значение главного квантового числа (n) в периодической системе указывает номер периода, в котором находится химический элемент. Но Зоммерфельд установил, что траектория движения в атоме может быть не только круговой, а иметь и другую конфигурацию, что учитывает орбитальное (l) квантовое число: l=n-1. Орбитальное квантовое число принимает значения: l= от 0 до ∞, и характеризует энергетический подуровень, на котором находится на данному уровне и энергию на этом подуровне. Каждый подуровень имеет свое буквенное обозначение l обозначение подуровня 0 1 2 3 s p d f
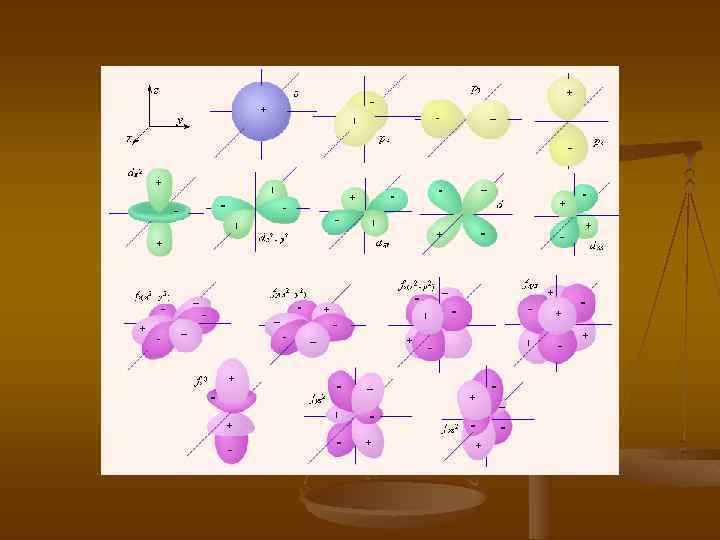
 Для того, чтобы учесть взаимодействие между собой и ядром ввели магнитное квантовое число (ml) оно характеризует положение плоскости атома относительно действия внешней силы. Магнитное квантовое число принимает значения = +l, 0, -l. , каждое значение магнитного квантового числа обозначается квантовой ячейкой, т. е. (ml) показывает число энергетических состояний электрона в атоме . Для того, чтобы учесть вращение электрона вокруг собственной оси ввели спиновое квантовое число s=±½. Положительное значение спинового числа принимают электроны движение, которых описывается почасовой ↑ стрелки, отрицательное - против часовой стрелки ↓. Подведем некоторые итоги: состояние электрона в атоме может быть описано с помощью четырёх квантовых числе. Они характеризуют: спин, энергию электрона, объём и форму пространства, в котором вероятно его пребывание около ядра. При переходе атома из одного квантового состояния в другое, в связи, с чем меняется значения квантовых чисел, происходит перестройка электронного облака, при этом атом поглощает или испускает квант энергии.
Для того, чтобы учесть взаимодействие между собой и ядром ввели магнитное квантовое число (ml) оно характеризует положение плоскости атома относительно действия внешней силы. Магнитное квантовое число принимает значения = +l, 0, -l. , каждое значение магнитного квантового числа обозначается квантовой ячейкой, т. е. (ml) показывает число энергетических состояний электрона в атоме . Для того, чтобы учесть вращение электрона вокруг собственной оси ввели спиновое квантовое число s=±½. Положительное значение спинового числа принимают электроны движение, которых описывается почасовой ↑ стрелки, отрицательное - против часовой стрелки ↓. Подведем некоторые итоги: состояние электрона в атоме может быть описано с помощью четырёх квантовых числе. Они характеризуют: спин, энергию электрона, объём и форму пространства, в котором вероятно его пребывание около ядра. При переходе атома из одного квантового состояния в другое, в связи, с чем меняется значения квантовых чисел, происходит перестройка электронного облака, при этом атом поглощает или испускает квант энергии.
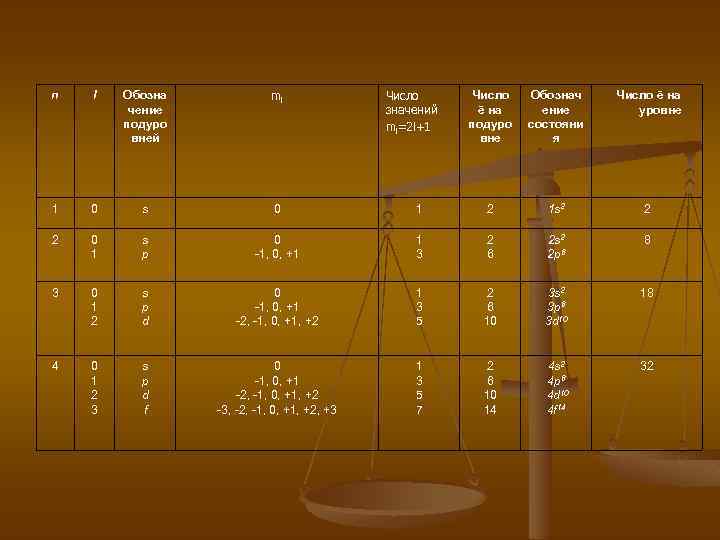 n l Обозна чение подуро вней ml 1 0 s 0 2 0 1 s p 3 0 1 2 4 0 1 2 3 Число значений ml=2 l+1 Число ē на подуро вне Обознач ение состояни я Число ē на уровне 1 2 1 s 2 2 0 -1, 0, +1 1 3 2 6 2 s 2 2 p 6 8 s p d 0 -1, 0, +1 -2, -1, 0, +1, +2 1 3 5 2 6 10 3 s 2 3 p 6 3 d 10 18 s p d f 0 -1, 0, +1 -2, -1, 0, +1, +2 -3, -2, -1, 0, +1, +2, +3 1 3 5 7 2 6 10 14 4 s 2 4 p 6 4 d 10 4 f 14 32
n l Обозна чение подуро вней ml 1 0 s 0 2 0 1 s p 3 0 1 2 4 0 1 2 3 Число значений ml=2 l+1 Число ē на подуро вне Обознач ение состояни я Число ē на уровне 1 2 1 s 2 2 0 -1, 0, +1 1 3 2 6 2 s 2 2 p 6 8 s p d 0 -1, 0, +1 -2, -1, 0, +1, +2 1 3 5 2 6 10 3 s 2 3 p 6 3 d 10 18 s p d f 0 -1, 0, +1 -2, -1, 0, +1, +2 -3, -2, -1, 0, +1, +2, +3 1 3 5 7 2 6 10 14 4 s 2 4 p 6 4 d 10 4 f 14 32
 При составлении электронных конфигураций многоэлектронных атомов учитывают: принцип минимальной энергии, принцип Паули, правила Гунда и Клечковского. Принцип минимальной энергии – электроны в основном состоянии заполняют орбитали в порядке повышения уровня энергии орбиталей; первыми заполняются орбитали с минимальными уровнями энергии. В 1925 г В. Паули высказал принцип: в атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковыми. Согласно этому принципу в одной ячейке могут находиться только два электрона, у которых главное, орбитальное и магнитное числа одинаковые, а спины противоположны. Правило Гунда: в данном подуровне электроны стремятся занять максимальное число свободных орбиталей (квантовых ячеек) с тем, чтобы суммарный спин имел наибольшее значение. Заполнение электронами энергетических уровней в атоме подчиняется правилам Клечковского: Энергия электрона на энергетическом уровне возрастает в порядке увеличения суммы главного квантового числа (п) и орбитального (l) квантовых чисел, т. е. (n+l); если для двух подуровней сумма (n+l) одна и та же, то в первую очередь заполняется тот подуровень, для которого квантовое число имеет наименьшее значение. 1 s 2 2 s 22 p 6 3 s 23 p 6 4 s 23 d 104 p 6 5 s 24 d 105 p 6 6 s 24 f 145 d 10 6 p 6 7 s 25 f 146 d 10 7 p 6 периоды I II IV V VI VII
При составлении электронных конфигураций многоэлектронных атомов учитывают: принцип минимальной энергии, принцип Паули, правила Гунда и Клечковского. Принцип минимальной энергии – электроны в основном состоянии заполняют орбитали в порядке повышения уровня энергии орбиталей; первыми заполняются орбитали с минимальными уровнями энергии. В 1925 г В. Паули высказал принцип: в атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковыми. Согласно этому принципу в одной ячейке могут находиться только два электрона, у которых главное, орбитальное и магнитное числа одинаковые, а спины противоположны. Правило Гунда: в данном подуровне электроны стремятся занять максимальное число свободных орбиталей (квантовых ячеек) с тем, чтобы суммарный спин имел наибольшее значение. Заполнение электронами энергетических уровней в атоме подчиняется правилам Клечковского: Энергия электрона на энергетическом уровне возрастает в порядке увеличения суммы главного квантового числа (п) и орбитального (l) квантовых чисел, т. е. (n+l); если для двух подуровней сумма (n+l) одна и та же, то в первую очередь заполняется тот подуровень, для которого квантовое число имеет наименьшее значение. 1 s 2 2 s 22 p 6 3 s 23 p 6 4 s 23 d 104 p 6 5 s 24 d 105 p 6 6 s 24 f 145 d 10 6 p 6 7 s 25 f 146 d 10 7 p 6 периоды I II IV V VI VII
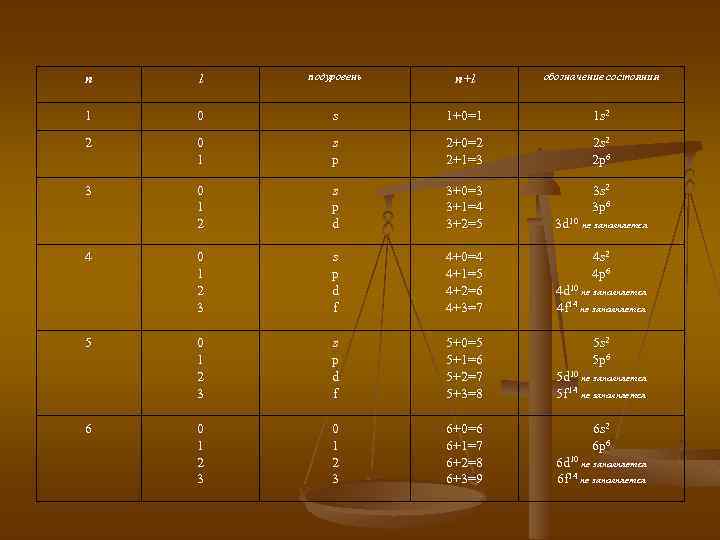 n l подуровень n+ l обозначение состояния 1 0 s 1+0=1 1 s 2 2 0 1 s p 2+0=2 2+1=3 2 s 2 2 p 6 3 0 1 2 s p d 3+0=3 3+1=4 3+2=5 3 s 2 3 p 6 0 1 2 3 s p d f 4+0=4 4+1=5 4+2=6 4+3=7 0 1 2 3 s p d f 5+0=5 5+1=6 5+2=7 5+3=8 0 1 2 3 6+0=6 6+1=7 6+2=8 6+3=9 4 5 6 3 d 10 не заполняется 4 s 2 4 p 6 4 d 10 не заполняется 4 f 14 не заполняется 5 s 2 5 p 6 5 d 10 не заполняется 5 f 14 не заполняется 6 s 2 6 p 6 6 d 10 не заполняется 6 f 14 не заполняется
n l подуровень n+ l обозначение состояния 1 0 s 1+0=1 1 s 2 2 0 1 s p 2+0=2 2+1=3 2 s 2 2 p 6 3 0 1 2 s p d 3+0=3 3+1=4 3+2=5 3 s 2 3 p 6 0 1 2 3 s p d f 4+0=4 4+1=5 4+2=6 4+3=7 0 1 2 3 s p d f 5+0=5 5+1=6 5+2=7 5+3=8 0 1 2 3 6+0=6 6+1=7 6+2=8 6+3=9 4 5 6 3 d 10 не заполняется 4 s 2 4 p 6 4 d 10 не заполняется 4 f 14 не заполняется 5 s 2 5 p 6 5 d 10 не заполняется 5 f 14 не заполняется 6 s 2 6 p 6 6 d 10 не заполняется 6 f 14 не заполняется
 § 3. Периодический закон Д. И. Менделеева Д. И. Менделеев был убежден, что между химическими элементами существует закономерная связь, объединяющая их в единое целое, и пришел к заключению, что в основу систематике элементов должна быть положена относительная атомная масса. Д. И. Менделеев сформулировал периодический закон в 1869 году: Свойства элементов и характер образуемых ими соединений, находятся в периодической зависимости от величины атомных весов элементов. Современная формулировка периодического закона Д. И. Менделеева. Свойства элементов и характер образуемых ими соединений находятся в периодической зависимости от заряда ядер элемента.
§ 3. Периодический закон Д. И. Менделеева Д. И. Менделеев был убежден, что между химическими элементами существует закономерная связь, объединяющая их в единое целое, и пришел к заключению, что в основу систематике элементов должна быть положена относительная атомная масса. Д. И. Менделеев сформулировал периодический закон в 1869 году: Свойства элементов и характер образуемых ими соединений, находятся в периодической зависимости от величины атомных весов элементов. Современная формулировка периодического закона Д. И. Менделеева. Свойства элементов и характер образуемых ими соединений находятся в периодической зависимости от заряда ядер элемента.
 § 4. Структура периодической системы Экспериментальное изучение электронных конфигураций атомов и положения атомов в периодической системе позволяет сделать ряд выводов, придающих физический смысл номеру периода, группы и типу подгруппы и существенно облегчить запись электронных конфигураций атомов: Номер периода указывает на значение главного квантового числа, т. е. на число энергетических уровней в атоме; Номер группы определяет максимальное значение валентности, которую проявляют элементы, находящиеся в ней. Если заполняются s-, p- подуровни, то элементы входят в главную (А) подгруппу (первые 3 периода элементов входят в (А) подгруппу). При заполнении d-, f- подуровней элементы образуют побочную (В) подгруппу; Порядковый номер элемента в системе указывает на положительный заряд ядра в атоме и количество электронов в нем;
§ 4. Структура периодической системы Экспериментальное изучение электронных конфигураций атомов и положения атомов в периодической системе позволяет сделать ряд выводов, придающих физический смысл номеру периода, группы и типу подгруппы и существенно облегчить запись электронных конфигураций атомов: Номер периода указывает на значение главного квантового числа, т. е. на число энергетических уровней в атоме; Номер группы определяет максимальное значение валентности, которую проявляют элементы, находящиеся в ней. Если заполняются s-, p- подуровни, то элементы входят в главную (А) подгруппу (первые 3 периода элементов входят в (А) подгруппу). При заполнении d-, f- подуровней элементы образуют побочную (В) подгруппу; Порядковый номер элемента в системе указывает на положительный заряд ядра в атоме и количество электронов в нем;
 В малых периодах (2 и 3) свойства элементов меняются от металлов до неметаллов, т. к. идет последовательное заполнение s-, p- подуровней; в нечетных рядах свойства меняются от металлов до неметаллов, т. к. заканчивается заполнение d подуровня и идет заполнение p- подуровня. Валентность с точки зрения строения атома количество не спаренных электронов в атоме; Металлические свойства определяются количеством электронов на внешнем электронном уровне. Все металлы имеют от одного до трех электронов на внешнем уровне, неметаллы - от пяти и более; четыре электрона имеют элементы с переходными (амфотерными) свойствами; Возбуждением атома называется переход электрона с одного энергетического подуровня на другой в пределах уровня;
В малых периодах (2 и 3) свойства элементов меняются от металлов до неметаллов, т. к. идет последовательное заполнение s-, p- подуровней; в нечетных рядах свойства меняются от металлов до неметаллов, т. к. заканчивается заполнение d подуровня и идет заполнение p- подуровня. Валентность с точки зрения строения атома количество не спаренных электронов в атоме; Металлические свойства определяются количеством электронов на внешнем электронном уровне. Все металлы имеют от одного до трех электронов на внешнем уровне, неметаллы - от пяти и более; четыре электрона имеют элементы с переходными (амфотерными) свойствами; Возбуждением атома называется переход электрона с одного энергетического подуровня на другой в пределах уровня;
 Большинство физико-химических и химических свойств элементов зависят от строения внешних электронных уровней и подуровней и главной причиной периодичности свойств элементов является периодическое появление однотипных электронных конфигураций внешних электронных подуровней с ростом заряда атома элемента. Среди важнейших периодических свойств атома выделяют следующие: количество электронов на внешней электронной оболочке; атомный и ионный радиусы, определяемые как средние радиусы атома или иона, находимых из экспериментальных данных по межатомным расстояниям в различных соединениях.
Большинство физико-химических и химических свойств элементов зависят от строения внешних электронных уровней и подуровней и главной причиной периодичности свойств элементов является периодическое появление однотипных электронных конфигураций внешних электронных подуровней с ростом заряда атома элемента. Среди важнейших периодических свойств атома выделяют следующие: количество электронов на внешней электронной оболочке; атомный и ионный радиусы, определяемые как средние радиусы атома или иона, находимых из экспериментальных данных по межатомным расстояниям в различных соединениях.
 В пределах одного периода с увеличением заряда ядра атома проявляется тенденция к уменьшению размеров атома, что особенно четко наблюдается в малых периодах. Это связано с тем, что постепенно прибавляющиеся электроны описываются орбиталями с почти равными характеристиками, поэтому увеличивающийся по периоду заряд ядра притягивает электроны с большей силой, что и способствует уменьшению радиуса. В главных и побочных подгруппах сверху вниз растет число электронных оболочек, увеличивается главное квантовое число внешней электронной оболочки, поэтому радиус атомов в приделах группы увеличивается. Атомы, лишившиеся или присоединившие одного или нескольких электронов становятся положительно или отрицательно заряженными частицами или ионами. Потеря атомом электрона приводит к уменьшению его эффективных размеров, а присоединение избыточных электронов – к увеличению, поэтому радиус катиона всегда меньше, чем радиус аниона. В пределах одной группы радиусы одинакового заряда возрастают с увеличением заряда ядра. энергия ионизации, определяемая количеством энергии, необходимой для отрыва электрона от атома (Еи).
В пределах одного периода с увеличением заряда ядра атома проявляется тенденция к уменьшению размеров атома, что особенно четко наблюдается в малых периодах. Это связано с тем, что постепенно прибавляющиеся электроны описываются орбиталями с почти равными характеристиками, поэтому увеличивающийся по периоду заряд ядра притягивает электроны с большей силой, что и способствует уменьшению радиуса. В главных и побочных подгруппах сверху вниз растет число электронных оболочек, увеличивается главное квантовое число внешней электронной оболочки, поэтому радиус атомов в приделах группы увеличивается. Атомы, лишившиеся или присоединившие одного или нескольких электронов становятся положительно или отрицательно заряженными частицами или ионами. Потеря атомом электрона приводит к уменьшению его эффективных размеров, а присоединение избыточных электронов – к увеличению, поэтому радиус катиона всегда меньше, чем радиус аниона. В пределах одной группы радиусы одинакового заряда возрастают с увеличением заряда ядра. энергия ионизации, определяемая количеством энергии, необходимой для отрыва электрона от атома (Еи).
 У элементов одного и того же периода при переходе от щелочных металлов к благородному газу заряд ядра постепенно возрастает, а радиус атома уменьшается, поэтому энергия ионизации постепенно увеличивается, а восстановительные свойства ослабевают. Итак, восстановительная активность атомов по периоду уменьшается, а окислительная активность увеличивается. сродство к электрону, определяемое количеством энергии, выделяющейся присоединении дополнительного электрона к атому (Ее); восстановительная активность (ВА), определяемая способностью атома отдавать электрон другому атому. Количественной мерой восстановительной активности является энергия ионизации. Если Еи увеличивается, то ВА уменьшается и наоборот; окислительная активность (ОА), определяемая способностью атома присоединять электрон от другого атома. Количественной мерой окислительной активности является сродство к электрону. Если Ее увеличивается, то ОА также увеличивается и наоборот; другие периодические свойства: степень окисления, электротрицательность, составы высших водородных соединений, высших кислородных соединений, термодинамические, электролитические свойства.
У элементов одного и того же периода при переходе от щелочных металлов к благородному газу заряд ядра постепенно возрастает, а радиус атома уменьшается, поэтому энергия ионизации постепенно увеличивается, а восстановительные свойства ослабевают. Итак, восстановительная активность атомов по периоду уменьшается, а окислительная активность увеличивается. сродство к электрону, определяемое количеством энергии, выделяющейся присоединении дополнительного электрона к атому (Ее); восстановительная активность (ВА), определяемая способностью атома отдавать электрон другому атому. Количественной мерой восстановительной активности является энергия ионизации. Если Еи увеличивается, то ВА уменьшается и наоборот; окислительная активность (ОА), определяемая способностью атома присоединять электрон от другого атома. Количественной мерой окислительной активности является сродство к электрону. Если Ее увеличивается, то ОА также увеличивается и наоборот; другие периодические свойства: степень окисления, электротрицательность, составы высших водородных соединений, высших кислородных соединений, термодинамические, электролитические свойства.

 Характеристика элемента на основании его положения в периодической системе Рассмотрим на примере химического элемента 33 Х. Общее количество электронов равно 33. Для I периода количество элементов равно 2; для II периода - 8; для III периода -8; для IV периода 18; для VI периода - 32; для VII периода - 32. Поэтому этот химический элемент расположен в IVпериоде; на внешнем уровне - 5 электронов последними заполняются р- электроны, поэтому р- элемент; V-группа главная подгруппа. Электронная формула элемента: 1 s 2; 2 p 6; 3 s 2; 3 p 6; 4 s 2; 3 d 104 p 3. ! У s и p- элементов номера группы определяются по сумме электронов на внешнем уровне на всех подуровнях. У d- элементов валентными являются электроны внешнего s подуровня и не заполненного d подуровней. Искомый элемент находится в главной подгруппе; неметалл; формула кислотного оксида X 2 O 3; X 2 O 5. Х 2 О 3+Н 2 О→НХО 2 Х 2 О 5+Н 2 О→НХО 3
Характеристика элемента на основании его положения в периодической системе Рассмотрим на примере химического элемента 33 Х. Общее количество электронов равно 33. Для I периода количество элементов равно 2; для II периода - 8; для III периода -8; для IV периода 18; для VI периода - 32; для VII периода - 32. Поэтому этот химический элемент расположен в IVпериоде; на внешнем уровне - 5 электронов последними заполняются р- электроны, поэтому р- элемент; V-группа главная подгруппа. Электронная формула элемента: 1 s 2; 2 p 6; 3 s 2; 3 p 6; 4 s 2; 3 d 104 p 3. ! У s и p- элементов номера группы определяются по сумме электронов на внешнем уровне на всех подуровнях. У d- элементов валентными являются электроны внешнего s подуровня и не заполненного d подуровней. Искомый элемент находится в главной подгруппе; неметалл; формула кислотного оксида X 2 O 3; X 2 O 5. Х 2 О 3+Н 2 О→НХО 2 Х 2 О 5+Н 2 О→НХО 3
 Электронно-графическая формула элемента п=1 ↑↓ р-электроны п=2 ↑↓ ↑↓ п=3 ↑↓ ↑↓ п=4 ↑↓ ↑ ↑ ↑ тl 0 +1 0 -1 d-электроны ↑↓ ↑↓ ↑↓ +2 +1 0 -1 f-электроны -2 n=4; l=1; тl=-1; s=+½. Валентность - III. возбужденное состояние: … 4 s 14 p 34 d 1. ХН 3; Х 2 О 5 - формулы соединений с водородом и кислородом.
Электронно-графическая формула элемента п=1 ↑↓ р-электроны п=2 ↑↓ ↑↓ п=3 ↑↓ ↑↓ п=4 ↑↓ ↑ ↑ ↑ тl 0 +1 0 -1 d-электроны ↑↓ ↑↓ ↑↓ +2 +1 0 -1 f-электроны -2 n=4; l=1; тl=-1; s=+½. Валентность - III. возбужденное состояние: … 4 s 14 p 34 d 1. ХН 3; Х 2 О 5 - формулы соединений с водородом и кислородом.
 25 Mn 1 s 2 ; 2 p 6 ; 3 s 2 ; 3 p 6 ; 4 s 2 ; 3 d 5. Этот элемент находится в IV-периоде, d- элемент; находится в VII-группе побочной подгруппе; металл; Mn 2 O 7 - кислотный оксид; Mn 2 O 7+H 2 O→H 2 Mn 2 O 8→ 2 HMn. O 4 Возбужденное состояние… 4 s 14 p 1; валентность - V. Mn. O; Mn 2 O 3; Mn. O 2; Mn 2 O 5; Mn. O 3; Mn 2 O 7 основной амфотерный кислотный У d - элементов наиболее устойчивы те степени окисления, когда с dподуровня отдается четное количество электронов. п=1 ↑↓ р-электроны п=2 ↑↓ ↑↓ п=3 ↑↓ ↑↓ ↑ ↑ ↑ п=4 ↑↓ тl 0 +1 0 -1 +2 +1 0 -1 -2 d-электроны f-электроны
25 Mn 1 s 2 ; 2 p 6 ; 3 s 2 ; 3 p 6 ; 4 s 2 ; 3 d 5. Этот элемент находится в IV-периоде, d- элемент; находится в VII-группе побочной подгруппе; металл; Mn 2 O 7 - кислотный оксид; Mn 2 O 7+H 2 O→H 2 Mn 2 O 8→ 2 HMn. O 4 Возбужденное состояние… 4 s 14 p 1; валентность - V. Mn. O; Mn 2 O 3; Mn. O 2; Mn 2 O 5; Mn. O 3; Mn 2 O 7 основной амфотерный кислотный У d - элементов наиболее устойчивы те степени окисления, когда с dподуровня отдается четное количество электронов. п=1 ↑↓ р-электроны п=2 ↑↓ ↑↓ п=3 ↑↓ ↑↓ ↑ ↑ ↑ п=4 ↑↓ тl 0 +1 0 -1 +2 +1 0 -1 -2 d-электроны f-электроны


