Презентация на тему Строение атома(97-2003).ppt
- Количество слайдов: 36
 СТРОЕНИЕ АТОМА .
СТРОЕНИЕ АТОМА .
 Квантовая механика – система понятий и уравнений, которые применяются для описания элементарных частиц, ядер, атомов, молекул. Составными частями квантовой механики являются: 1) корпускулярно-волновой дуализм; 2) принцип неопределенности; 3) волновое управление.
Квантовая механика – система понятий и уравнений, которые применяются для описания элементарных частиц, ядер, атомов, молекул. Составными частями квантовой механики являются: 1) корпускулярно-волновой дуализм; 2) принцип неопределенности; 3) волновое управление.
 Корпускулярно-волновой дуализм В 1924 г. французский физик Луи де Бройль высказал предположение: «Любая движущаяся частица одновременно обладает и механическими и волновыми свойствами» . Предположение де Бройля подтвердилось экспериментально на явлении дифракции электронов и нашло применение в электронных микроскопах.
Корпускулярно-волновой дуализм В 1924 г. французский физик Луи де Бройль высказал предположение: «Любая движущаяся частица одновременно обладает и механическими и волновыми свойствами» . Предположение де Бройля подтвердилось экспериментально на явлении дифракции электронов и нашло применение в электронных микроскопах.
 Корпускулярно-волновой дуализм Эта зависимость выражается уравнением: , где – длина волны; h – постоянная Планка, 6, 6· 10 -34 Дж·с; m – масса частицы (электрона); ν – скорость частицы.
Корпускулярно-волновой дуализм Эта зависимость выражается уравнением: , где – длина волны; h – постоянная Планка, 6, 6· 10 -34 Дж·с; m – масса частицы (электрона); ν – скорость частицы.
 Принцип неопределенности В 1925 г. немецкий физик В. Гейзенберг высказал положение: «Для микрочастицы атомного масштаба невозможно одновременно и точно указать координату и скорость ее движения» .
Принцип неопределенности В 1925 г. немецкий физик В. Гейзенберг высказал положение: «Для микрочастицы атомного масштаба невозможно одновременно и точно указать координату и скорость ее движения» .
 Принцип неопределенности Математическое выражение этого положения: , где ∆q – неопределенность координат, или положения в пространстве; ∆p – неопределенность импульса, p = m·V, где m – масса, V – скорость; h – постоянная Планка, ћ – приведенная постоянная Планка.
Принцип неопределенности Математическое выражение этого положения: , где ∆q – неопределенность координат, или положения в пространстве; ∆p – неопределенность импульса, p = m·V, где m – масса, V – скорость; h – постоянная Планка, ћ – приведенная постоянная Планка.
 Принцип неопределенности Из принципа неопределенности следует два вывода: 1) Невозможно точно представить траекторию движения электрона в атоме; 2) Электрон в атоме нельзя рассматривать с математической точностью. Можно лишь вычислить вероятность пребывания электрона в околоядерном пространстве.
Принцип неопределенности Из принципа неопределенности следует два вывода: 1) Невозможно точно представить траекторию движения электрона в атоме; 2) Электрон в атоме нельзя рассматривать с математической точностью. Можно лишь вычислить вероятность пребывания электрона в околоядерном пространстве.
 Волновое уравнение В 1926 г. австрийский ученый Э. Шредингер предложил уравнение с помощью которого вычисляют вероятность нахождения электрона в атоме: ,
Волновое уравнение В 1926 г. австрийский ученый Э. Шредингер предложил уравнение с помощью которого вычисляют вероятность нахождения электрона в атоме: ,
 Волновое уравнение где сумма вторых производных волновой функции (пси) ; m – масса электрона; h – постоянная Планка; E – полная энергия электрона; U – потенциальная энергия электрона – функция координат x, y, z, называемая волновой функцией (орбиталью) и является основной характеристикой электрона в атоме.
Волновое уравнение где сумма вторых производных волновой функции (пси) ; m – масса электрона; h – постоянная Планка; E – полная энергия электрона; U – потенциальная энергия электрона – функция координат x, y, z, называемая волновой функцией (орбиталью) и является основной характеристикой электрона в атоме.
 Квантово-механическая модель атома • Квантово-механическая модель атома – это воображаемый вид атома, созданный на основе положений квантовой механики. • Электронное облако – это околоядерное пространство, в котором вероятность пребывания электрона максимальна.
Квантово-механическая модель атома • Квантово-механическая модель атома – это воображаемый вид атома, созданный на основе положений квантовой механики. • Электронное облако – это околоядерное пространство, в котором вероятность пребывания электрона максимальна.
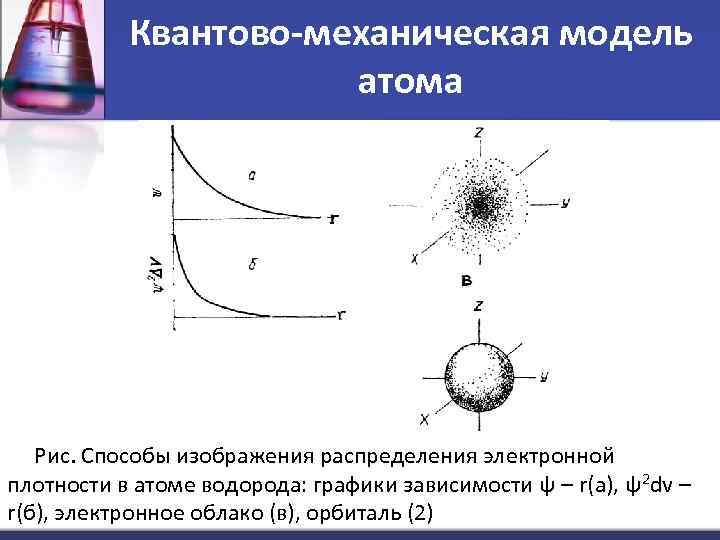 Квантово-механическая модель атома Рис. Способы изображения распределения электронной плотности в атоме водорода: графики зависимости ψ – r(a), ψ2 dv – r(б), электронное облако (в), орбиталь (2)
Квантово-механическая модель атома Рис. Способы изображения распределения электронной плотности в атоме водорода: графики зависимости ψ – r(a), ψ2 dv – r(б), электронное облако (в), орбиталь (2)
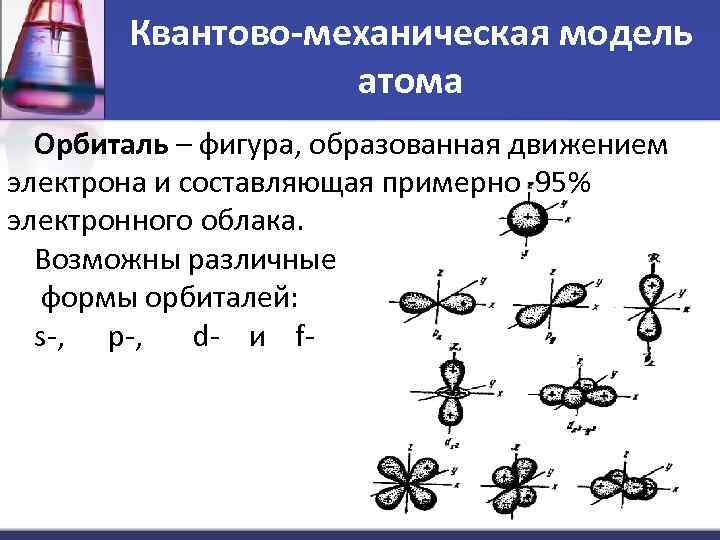 Квантово-механическая модель атома Орбиталь – фигура, образованная движением электрона и составляющая примерно 95% электронного облака. Возможны различные формы орбиталей: s-, p-, d- и f-
Квантово-механическая модель атома Орбиталь – фигура, образованная движением электрона и составляющая примерно 95% электронного облака. Возможны различные формы орбиталей: s-, p-, d- и f-
 Квантовые числа Нахождение электрона в атоме характеризуется четырьмя квантовыми числами; n – главное, ℓ - орбитальное, m – магнитное, s – спиновое. Все эти числа характеризуют определенную энергию электрона.
Квантовые числа Нахождение электрона в атоме характеризуется четырьмя квантовыми числами; n – главное, ℓ - орбитальное, m – магнитное, s – спиновое. Все эти числа характеризуют определенную энергию электрона.
 Квантовые числа n определяет размер электронного облака и принимает значение [1; ). Электроны с одинаковым значением n образуют уровень в атоме.
Квантовые числа n определяет размер электронного облака и принимает значение [1; ). Электроны с одинаковым значением n образуют уровень в атоме.
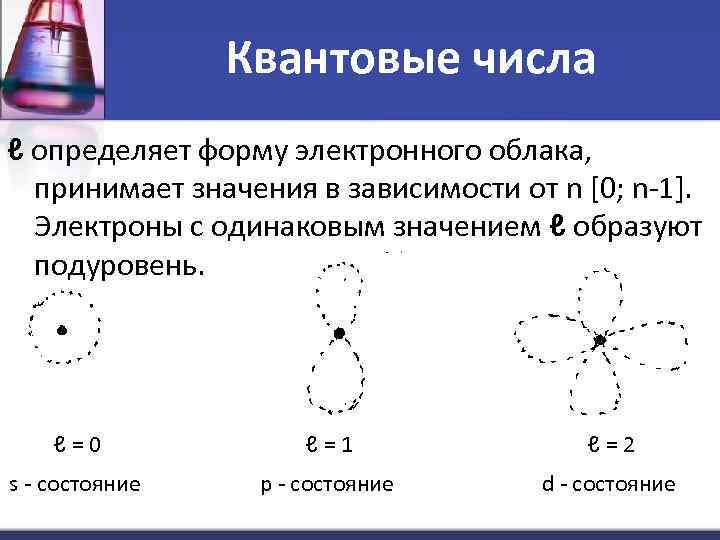 Квантовые числа ℓ определяет форму электронного облака, принимает значения в зависимости от n [0; n-1]. Электроны с одинаковым значением ℓ образуют подуровень. ℓ = 0 ℓ = 1 ℓ = 2 s - состояние p - состояние d - состояние
Квантовые числа ℓ определяет форму электронного облака, принимает значения в зависимости от n [0; n-1]. Электроны с одинаковым значением ℓ образуют подуровень. ℓ = 0 ℓ = 1 ℓ = 2 s - состояние p - состояние d - состояние
 Квантовые числа m определяет ориентацию электронного облака, принимает значения в зависимости от ℓ [-ℓ; 0; +ℓ]. Состояние электрона в атоме определяемое значением n, ℓ, m называется атомной орбиталью (АО). Обозначается или сокращено –.
Квантовые числа m определяет ориентацию электронного облака, принимает значения в зависимости от ℓ [-ℓ; 0; +ℓ]. Состояние электрона в атоме определяемое значением n, ℓ, m называется атомной орбиталью (АО). Обозначается или сокращено –.
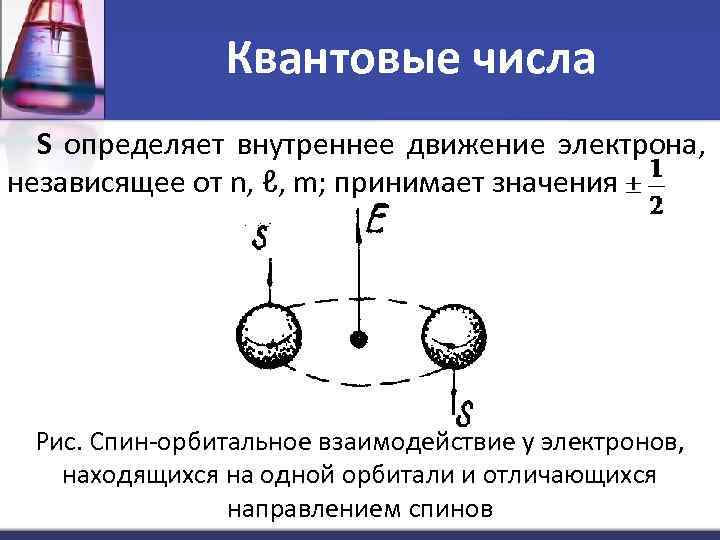 : Квантовые числа S определяет внутреннее движение электрона, независящее от n, ℓ, m; принимает значения Рис. Спин-орбитальное взаимодействие у электронов, находящихся на одной орбитали и отличающихся направлением спинов
: Квантовые числа S определяет внутреннее движение электрона, независящее от n, ℓ, m; принимает значения Рис. Спин-орбитальное взаимодействие у электронов, находящихся на одной орбитали и отличающихся направлением спинов
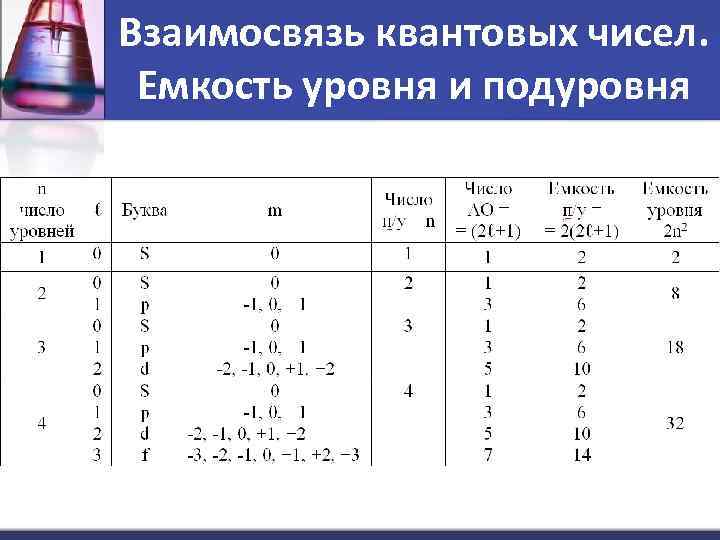 Взаимосвязь квантовых чисел. Емкость уровня и подуровня
Взаимосвязь квантовых чисел. Емкость уровня и подуровня
 Правила заполнения электронами атомных орбиталей (АО) 1) Принцип минимальной энергии(В. Клечковский): «АО заполняются электронами в порядке повышения энергии (Е) их уровней. Или при переходе от одного элемента к другому электроны размещаются последовательно на орбиталях, расположенных в порядке возрастания суммы главного и орбитального квантовых чисел (n+ℓ). При одинаковых энергиях этой суммы первой заполняется орбиталь с меньшим значением главного квантового числа» .
Правила заполнения электронами атомных орбиталей (АО) 1) Принцип минимальной энергии(В. Клечковский): «АО заполняются электронами в порядке повышения энергии (Е) их уровней. Или при переходе от одного элемента к другому электроны размещаются последовательно на орбиталях, расположенных в порядке возрастания суммы главного и орбитального квантовых чисел (n+ℓ). При одинаковых энергиях этой суммы первой заполняется орбиталь с меньшим значением главного квантового числа» .
 Правила заполнения электронами атомных орбиталей (АО) Например, для 3 d подуровня (n+ℓ) = 3+2 = 5 и для 4 р подуровня (n+ℓ) = 4+1 = 5. E 3 d < E 4 p, так как главные квантовые числа 3 d = 3; 4 р = 4, то первым заполняет подуровень 3 d.
Правила заполнения электронами атомных орбиталей (АО) Например, для 3 d подуровня (n+ℓ) = 3+2 = 5 и для 4 р подуровня (n+ℓ) = 4+1 = 5. E 3 d < E 4 p, так как главные квантовые числа 3 d = 3; 4 р = 4, то первым заполняет подуровень 3 d.
 Правила заполнения электронами атомных орбиталей (АО) Согласно принципу минимальной энергии имеем такой порядок заполнения АО:
Правила заполнения электронами атомных орбиталей (АО) Согласно принципу минимальной энергии имеем такой порядок заполнения АО:
 Правила заполнения электронами атомных орбиталей (АО) 2) Принцип В. Паули: «В атоме не может быть даже двух электронов, у которых все четыре квантовых числа одинаковы» . Следствие: «В одной АО может максимально находиться только два электрона с противоположными спинами» .
Правила заполнения электронами атомных орбиталей (АО) 2) Принцип В. Паули: «В атоме не может быть даже двух электронов, у которых все четыре квантовых числа одинаковы» . Следствие: «В одной АО может максимально находиться только два электрона с противоположными спинами» .
 Правила заполнения электронами атомных орбиталей (АО) 3) Правило Ф. Хунда: «Суммарный спин электрона в подуровне должен быть максимальным, т. е. АО подуровня сначала заполняются по одному электрону, а затем спариваются» .
Правила заполнения электронами атомных орбиталей (АО) 3) Правило Ф. Хунда: «Суммарный спин электрона в подуровне должен быть максимальным, т. е. АО подуровня сначала заполняются по одному электрону, а затем спариваются» .
 Периодическая система Д. И. Менделеева и электронная структура атомов В 1869 г. Д. И. Менделеев сообщил об открытии периодического закона, современная формулировка которого такова: «Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от заряда ядер их атомов» . Физический смысл периодического закона: повторение свойств элементов связано с повторением электронного строения внешнего энергетического уровня.
Периодическая система Д. И. Менделеева и электронная структура атомов В 1869 г. Д. И. Менделеев сообщил об открытии периодического закона, современная формулировка которого такова: «Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от заряда ядер их атомов» . Физический смысл периодического закона: повторение свойств элементов связано с повторением электронного строения внешнего энергетического уровня.
 Периодическая система Д. И. Менделеева и электронная структура атомов Первый период состоит из двух элементов: Н и Не. Атом гелия заканчивает формирование К-оболочки атома, обозначим ее [K] или [He]. Оба элемента имеют формирующие s-электроны и соответственно называются s-элементами.
Периодическая система Д. И. Менделеева и электронная структура атомов Первый период состоит из двух элементов: Н и Не. Атом гелия заканчивает формирование К-оболочки атома, обозначим ее [K] или [He]. Оба элемента имеют формирующие s-электроны и соответственно называются s-элементами.
 Периодическая система Д. И. Менделеева и электронная структура атомов У элементов второго периода формируется Lоболочка, заполняются s- и р- подоболочки (подуровни). Формирующими электронами у первых двух элементов являются s-электроны, поэтому Li и Be относятся к s-элементам. Остальные шесть элементов этого периода входят в число р- элементов, т. к. формирование их орбиталей заканчивается р- электроном. У элемента Ne полностью заполняется 2 р подоболочка, обозначается она как [Ne].
Периодическая система Д. И. Менделеева и электронная структура атомов У элементов второго периода формируется Lоболочка, заполняются s- и р- подоболочки (подуровни). Формирующими электронами у первых двух элементов являются s-электроны, поэтому Li и Be относятся к s-элементам. Остальные шесть элементов этого периода входят в число р- элементов, т. к. формирование их орбиталей заканчивается р- электроном. У элемента Ne полностью заполняется 2 р подоболочка, обозначается она как [Ne].
 Периодическая система Д. И. Менделеева и электронная структура атомов Третий период начинается с атома Na, электронная конфигурация которого 1 S 22 p 63 S 1 и заканчивается аргоном Ar с электронной конфигурацией 1 S 22 p 63 S 23 p 6, обозначаемой [Ar]. Подоболочка 3 d остается незаполненной.
Периодическая система Д. И. Менделеева и электронная структура атомов Третий период начинается с атома Na, электронная конфигурация которого 1 S 22 p 63 S 1 и заканчивается аргоном Ar с электронной конфигурацией 1 S 22 p 63 S 23 p 6, обозначаемой [Ar]. Подоболочка 3 d остается незаполненной.
 Периодическая система Д. И. Менделеева и электронная структура атомов В четвертом периоде начинается формирование Nуровня (n=4) и период начинается с s-элемента калия [Ar] 4 S 1 Элементы от Sc до Zn, имеющие формирующие dэлектроны, относятся к d-элементами. У атома Сr более устойчивой является конфигурация 3 d 54 S 1, чем 3 d 44 S 2. Такое явление получило название «провала» электрона. Провал электронов имеется также у атомов Cu, Nb, Mo, Pt, Pd. Четвертый период завершается формированием 4 р подоболочки криптона Kr и обозначается [Ar] 3 d 104 S 24 p 6 или [Kr]. В этом периоде находится 18 элементов.
Периодическая система Д. И. Менделеева и электронная структура атомов В четвертом периоде начинается формирование Nуровня (n=4) и период начинается с s-элемента калия [Ar] 4 S 1 Элементы от Sc до Zn, имеющие формирующие dэлектроны, относятся к d-элементами. У атома Сr более устойчивой является конфигурация 3 d 54 S 1, чем 3 d 44 S 2. Такое явление получило название «провала» электрона. Провал электронов имеется также у атомов Cu, Nb, Mo, Pt, Pd. Четвертый период завершается формированием 4 р подоболочки криптона Kr и обозначается [Ar] 3 d 104 S 24 p 6 или [Kr]. В этом периоде находится 18 элементов.
 Периодическая система Д. И. Менделеева и электронная структура атомов Пятый период аналогичен 4 -ому и заканчивается рэлементом Хе; обозначается [Kr] 4 d 105 S 25 p 6 или [Хе].
Периодическая система Д. И. Менделеева и электронная структура атомов Пятый период аналогичен 4 -ому и заканчивается рэлементом Хе; обозначается [Kr] 4 d 105 S 25 p 6 или [Хе].
 Периодическая система Д. И. Менделеева и электронная структура атомов В шестом периоде, как и в пятом, после завершения sподоболочки начинается формирование dподоболочки предвнешнего уровня у лантана La. Однако, у следующего элемента энергетически выгоднее формирование 4 f-подоболочки по сравнению с 5 d-подоболочкой. Поэтому после La следует 14 лантаноидов с формирующим fэлектронами, т. е. f-элементов от церия Ce [Xe] 4 f 145 d 16 S 2 и до лютеция Lu [Хе] 4 f 145 d 16 S 2. Затем продолжается заполнение оставшихся орбиталей в 5 dподоболочке и 6 р-подоболочке. Период завершает радон Rn [Xe] 4 f 145 d 106 S 26 р6, или [Rn]. Таким образом, период имеет 32 элемента.
Периодическая система Д. И. Менделеева и электронная структура атомов В шестом периоде, как и в пятом, после завершения sподоболочки начинается формирование dподоболочки предвнешнего уровня у лантана La. Однако, у следующего элемента энергетически выгоднее формирование 4 f-подоболочки по сравнению с 5 d-подоболочкой. Поэтому после La следует 14 лантаноидов с формирующим fэлектронами, т. е. f-элементов от церия Ce [Xe] 4 f 145 d 16 S 2 и до лютеция Lu [Хе] 4 f 145 d 16 S 2. Затем продолжается заполнение оставшихся орбиталей в 5 dподоболочке и 6 р-подоболочке. Период завершает радон Rn [Xe] 4 f 145 d 106 S 26 р6, или [Rn]. Таким образом, период имеет 32 элемента.
 Периодическая система Д. И. Менделеева и электронная структура атомов Седьмой период начинается и продолжается аналогично шестому периоду. Однако формирование его еще незавершено.
Периодическая система Д. И. Менделеева и электронная структура атомов Седьмой период начинается и продолжается аналогично шестому периоду. Однако формирование его еще незавершено.
 Периодические свойства элементов Поскольку электронное строение атомов изменяется периодически, соответственно периодически изменяются и свойства элементов: атомный радиус, энергия ионизации, средство к электрону, электроотрицательность (ЭО).
Периодические свойства элементов Поскольку электронное строение атомов изменяется периодически, соответственно периодически изменяются и свойства элементов: атомный радиус, энергия ионизации, средство к электрону, электроотрицательность (ЭО).
 Периодические свойства элементов Радиус атома (ra) - это теоретически рассчитанное расстояние от ядра до наиболее удаленного от него электрона (орбитальный радиус) или половина расстояния между центрами двух смежных атомов в кристалле (эффективный радиус). Энергия ионизации (Еu) – это энергия, необходимая для отрыва электрона от невозбужденного атома.
Периодические свойства элементов Радиус атома (ra) - это теоретически рассчитанное расстояние от ядра до наиболее удаленного от него электрона (орбитальный радиус) или половина расстояния между центрами двух смежных атомов в кристалле (эффективный радиус). Энергия ионизации (Еu) – это энергия, необходимая для отрыва электрона от невозбужденного атома.
 Периодические свойства элементов Сродство к электрону (Е ) – это энергия, поглощаемая или выделяемая присоединении электрона к частице (атому, иону, молекуле). Электроотрицательность – (ЭО) – это способность атома в ковалентной молекуле смещать к себе электроны химической связи).
Периодические свойства элементов Сродство к электрону (Е ) – это энергия, поглощаемая или выделяемая присоединении электрона к частице (атому, иону, молекуле). Электроотрицательность – (ЭО) – это способность атома в ковалентной молекуле смещать к себе электроны химической связи).
 Периодические свойства элементов Л. Полинг (американский ученый) предложил относительную шкалу ЭО, приняв ЭО Li за единицу:
Периодические свойства элементов Л. Полинг (американский ученый) предложил относительную шкалу ЭО, приняв ЭО Li за единицу:
 Периодические свойства элементов Общий характер изменения периодических свойств в периодической системе можно представить схемой:
Периодические свойства элементов Общий характер изменения периодических свойств в периодической системе можно представить схемой:


