Строение атома.pptx
- Количество слайдов: 29
 Строение атома • Историческаясправка. Основные представления о строении атома. • Современная квантово-механическая теория строения атома. а) корпускулярно – волновой дуализм б) принцип неопределенности в) волновая функция. Понятие орбитали • Квантовые числа. • Правила заполнения электронных оболочек атомов.
Строение атома • Историческаясправка. Основные представления о строении атома. • Современная квантово-механическая теория строения атома. а) корпускулярно – волновой дуализм б) принцип неопределенности в) волновая функция. Понятие орбитали • Квантовые числа. • Правила заполнения электронных оболочек атомов.
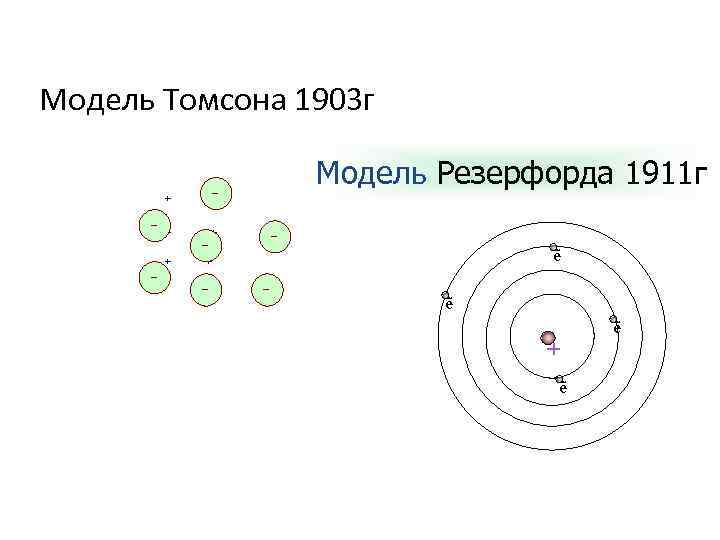 Модель Томсона 1903 г + – – + + – Модель Резерфорда 1911 г – – + – ẽ + ẽ ẽ
Модель Томсона 1903 г + – – + + – Модель Резерфорда 1911 г – – + – ẽ + ẽ ẽ
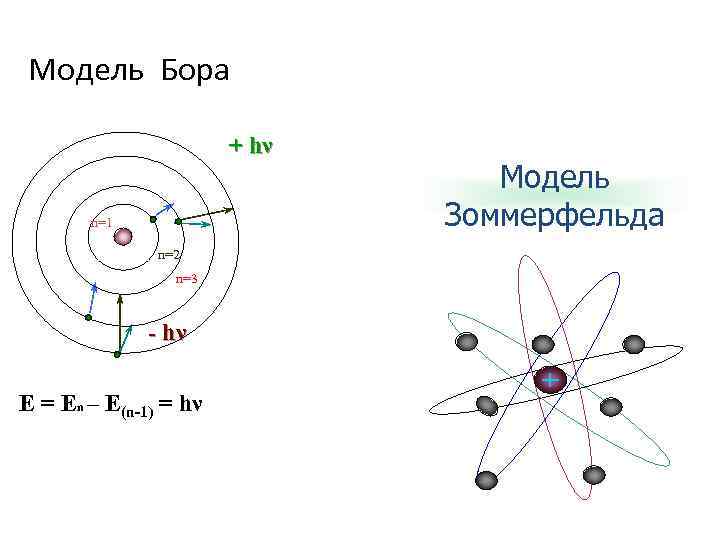 Модель Бора + hν n=1 n=2 n=3 - hν E = En – E(n-1) = hν Модель Зоммерфельда
Модель Бора + hν n=1 n=2 n=3 - hν E = En – E(n-1) = hν Модель Зоммерфельда
 ядра атомов состоят • из положительно заряженных частиц – протонов • нейтральных частиц – нейтронов. • Сумма числа протонов (Z) и нейтронов (N) называется массовым числом атома: А = Z + N Заряд ядра (Z) = порядковому номеру = числу протонов = числу электронов в атоме элемента в таблице Менделеева
ядра атомов состоят • из положительно заряженных частиц – протонов • нейтральных частиц – нейтронов. • Сумма числа протонов (Z) и нейтронов (N) называется массовым числом атома: А = Z + N Заряд ядра (Z) = порядковому номеру = числу протонов = числу электронов в атоме элемента в таблице Менделеева
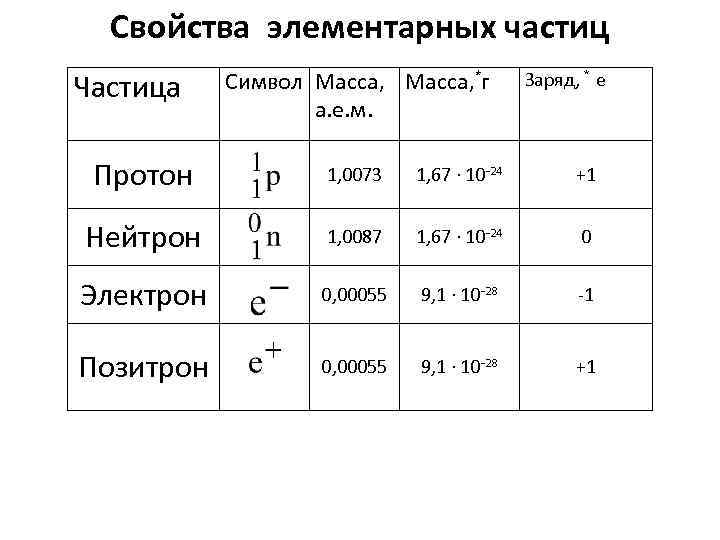 Свойства элементарных частиц Частица Символ Масса, *г а. е. м. Заряд, * e Протон 1, 0073 1, 67 ∙ 10 -24 +1 Нейтрон 1, 0087 1, 67 ∙ 10 -24 0 Электрон 0, 00055 9, 1 ∙ 10 -28 -1 Позитрон 0, 00055 9, 1 ∙ 10 -28 +1
Свойства элементарных частиц Частица Символ Масса, *г а. е. м. Заряд, * e Протон 1, 0073 1, 67 ∙ 10 -24 +1 Нейтрон 1, 0087 1, 67 ∙ 10 -24 0 Электрон 0, 00055 9, 1 ∙ 10 -28 -1 Позитрон 0, 00055 9, 1 ∙ 10 -28 +1
 АТОМ ЯДРО (протоны и нейтроны) Определяют массу атома и заряд ядра, радиоактивные свойства ЭЛЕКТРОНЫ Определяют химические свойства
АТОМ ЯДРО (протоны и нейтроны) Определяют массу атома и заряд ядра, радиоактивные свойства ЭЛЕКТРОНЫ Определяют химические свойства
 • Атомы с одинаковым числом протонов, отличающиеся друг от друга числом нейтронов называют – изотопами.
• Атомы с одинаковым числом протонов, отличающиеся друг от друга числом нейтронов называют – изотопами.
 Корпускулярно – волновой дуализм наличие у электрона свойств и частицы, и волны Уравнение Луи де Бройля h/mv Принцип неопределенности Гейзенберга (1925 ) невозможно одновременно с одинаковой точностью определить скорость движения электрона и его положение в пространстве рx∙Δx ħ ħ = h/2π
Корпускулярно – волновой дуализм наличие у электрона свойств и частицы, и волны Уравнение Луи де Бройля h/mv Принцип неопределенности Гейзенберга (1925 ) невозможно одновременно с одинаковой точностью определить скорость движения электрона и его положение в пространстве рx∙Δx ħ ħ = h/2π
 Уравнение Шрёдингера Волновая функция Ψ – характеризует вероятность нахождения электрона в данной части пространства. Пространство вокруг ядра, в котором наиболее вероятно нахождение электрона, называется электронным облаком или орбиталью
Уравнение Шрёдингера Волновая функция Ψ – характеризует вероятность нахождения электрона в данной части пространства. Пространство вокруг ядра, в котором наиболее вероятно нахождение электрона, называется электронным облаком или орбиталью
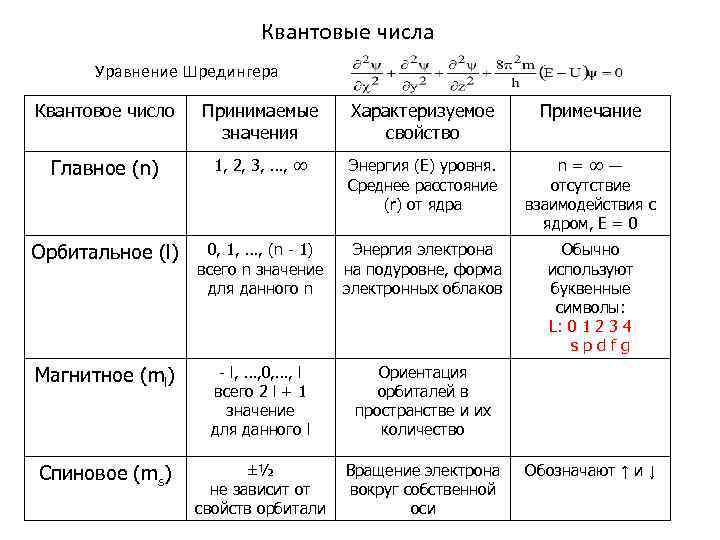 Квантовые числа Уравнение Шредингера Квантовое число Принимаемые значения Характеризуемое свойство Примечание Главное (n) 1, 2, 3, …, ∞ Энергия (Е) уровня. Среднее расстояние (r) от ядра n=∞― отсутствие взаимодействия с ядром, Е = 0 Орбитальное (l) 0, 1, …, (n - 1) всего n значение для данного n Энергия электрона на подуровне, форма электронных облаков Обычно используют буквенные символы: L: 0 1 2 3 4 spdfg Магнитное (ml) - l, …, 0, …, l всего 2 l + 1 значение для данного l Ориентация орбиталей в пространстве и их количество Спиновое (ms) ±½ не зависит от свойств орбитали Вращение электрона вокруг собственной оси Обозначают ↑ и ↓
Квантовые числа Уравнение Шредингера Квантовое число Принимаемые значения Характеризуемое свойство Примечание Главное (n) 1, 2, 3, …, ∞ Энергия (Е) уровня. Среднее расстояние (r) от ядра n=∞― отсутствие взаимодействия с ядром, Е = 0 Орбитальное (l) 0, 1, …, (n - 1) всего n значение для данного n Энергия электрона на подуровне, форма электронных облаков Обычно используют буквенные символы: L: 0 1 2 3 4 spdfg Магнитное (ml) - l, …, 0, …, l всего 2 l + 1 значение для данного l Ориентация орбиталей в пространстве и их количество Спиновое (ms) ±½ не зависит от свойств орбитали Вращение электрона вокруг собственной оси Обозначают ↑ и ↓
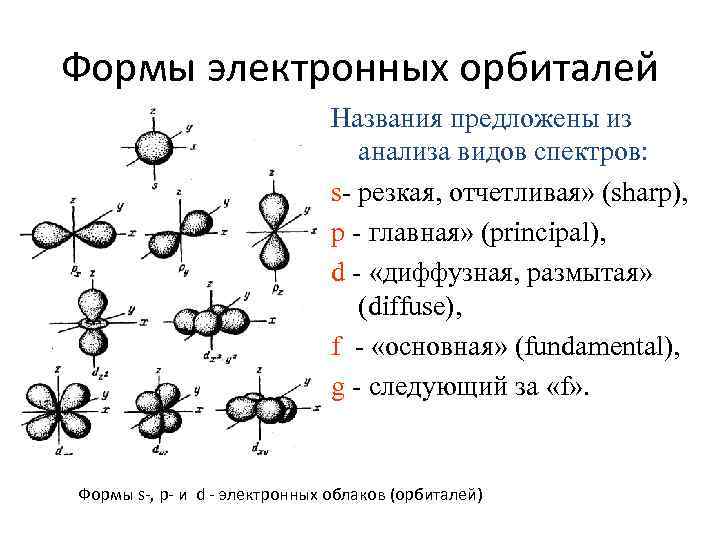 Формы электронных орбиталей Названия предложены из анализа видов спектров: s- резкая, отчетливая» (sharp), p - главная» (principal), d - «диффузная, размытая» (diffuse), f - «основная» (fundamental), g - следующий за «f» . Формы s-, р- и d - электронных облаков (орбиталей)
Формы электронных орбиталей Названия предложены из анализа видов спектров: s- резкая, отчетливая» (sharp), p - главная» (principal), d - «диффузная, размытая» (diffuse), f - «основная» (fundamental), g - следующий за «f» . Формы s-, р- и d - электронных облаков (орбиталей)
 Правила заполнения атомных орбиталей(АО) Принцип Паули: Никакие два электрона в одном атоме не могут характеризоваться одинаковым набором значений всех четырех квантовых чисел n, l, m, s. По правилу Гунда АО заполняются электронами так, чтобы их суммарный «спин» был максимален. Правило Клечковского: Энергия уровней и подуровней возрастает в порядке увеличения суммы n + l, а при одном и том же значении этой суммы ниже располагаются уровни с меньшим n.
Правила заполнения атомных орбиталей(АО) Принцип Паули: Никакие два электрона в одном атоме не могут характеризоваться одинаковым набором значений всех четырех квантовых чисел n, l, m, s. По правилу Гунда АО заполняются электронами так, чтобы их суммарный «спин» был максимален. Правило Клечковского: Энергия уровней и подуровней возрастает в порядке увеличения суммы n + l, а при одном и том же значении этой суммы ниже располагаются уровни с меньшим n.

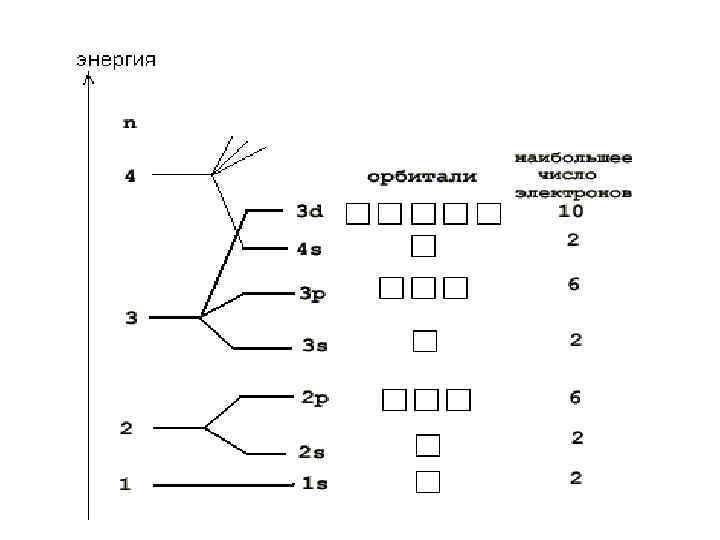
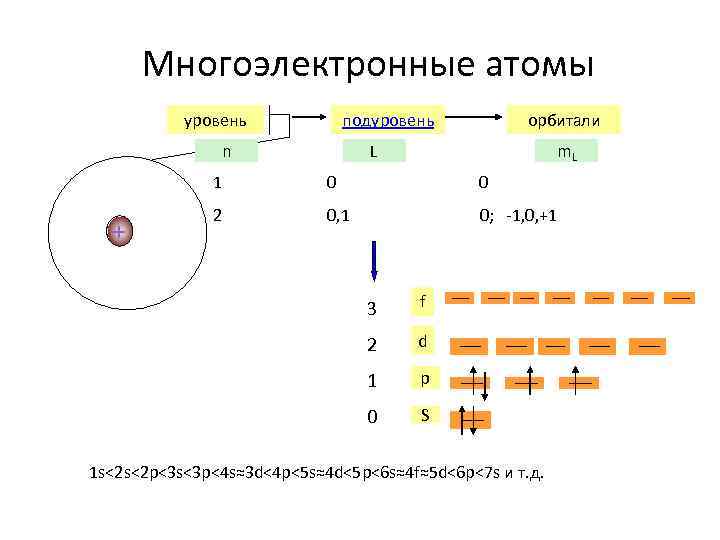 Многоэлектронные атомы уровень n подуровень орбитали L m. L 1 0 + 2 0, 1 0; -1, 0, +1 3 f 2 d 1 p 0 S 1 s<2 s<2 p<3 s<3 p<4 s≈3 d<4 p<5 s≈4 d<5 p<6 s≈4 f≈5 d<6 p<7 s и т. д.
Многоэлектронные атомы уровень n подуровень орбитали L m. L 1 0 + 2 0, 1 0; -1, 0, +1 3 f 2 d 1 p 0 S 1 s<2 s<2 p<3 s<3 p<4 s≈3 d<4 p<5 s≈4 d<5 p<6 s≈4 f≈5 d<6 p<7 s и т. д.
 Максимальное число электронов на первых 4 -х электронных уровнях. Электронный уровень Максимальное количество электронов на уровне (n) (2 n 2) 1 2 2 8 3 18 4 32
Максимальное число электронов на первых 4 -х электронных уровнях. Электронный уровень Максимальное количество электронов на уровне (n) (2 n 2) 1 2 2 8 3 18 4 32

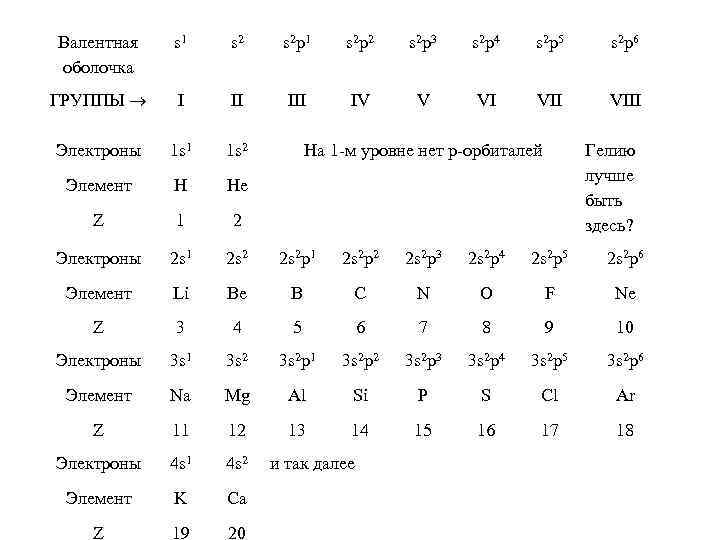 Валентная оболочка s 1 s 2 p 2 s 2 p 3 s 2 p 4 s 2 p 5 s 2 p 6 ГРУППЫ ® I II IV V VI VIII Электроны 1 s 1 1 s 2 Элемент H He Z 1 2 Электроны 2 s 1 2 s 2 p 2 2 s 2 p 3 2 s 2 p 4 2 s 2 p 5 2 s 2 p 6 Элемент Li Be B C N O F Ne Z 3 4 5 6 7 8 9 10 Электроны 3 s 1 3 s 2 p 2 3 s 2 p 3 3 s 2 p 4 3 s 2 p 5 3 s 2 p 6 Элемент Na Mg Al Si P S Cl Ar Z 11 12 13 14 15 16 17 18 Электроны 4 s 1 4 s 2 Элемент K Ca Z 19 20 На 1 -м уровне нет p-орбиталей и так далее Гелию лучше быть здесь?
Валентная оболочка s 1 s 2 p 2 s 2 p 3 s 2 p 4 s 2 p 5 s 2 p 6 ГРУППЫ ® I II IV V VI VIII Электроны 1 s 1 1 s 2 Элемент H He Z 1 2 Электроны 2 s 1 2 s 2 p 2 2 s 2 p 3 2 s 2 p 4 2 s 2 p 5 2 s 2 p 6 Элемент Li Be B C N O F Ne Z 3 4 5 6 7 8 9 10 Электроны 3 s 1 3 s 2 p 2 3 s 2 p 3 3 s 2 p 4 3 s 2 p 5 3 s 2 p 6 Элемент Na Mg Al Si P S Cl Ar Z 11 12 13 14 15 16 17 18 Электроны 4 s 1 4 s 2 Элемент K Ca Z 19 20 На 1 -м уровне нет p-орбиталей и так далее Гелию лучше быть здесь?
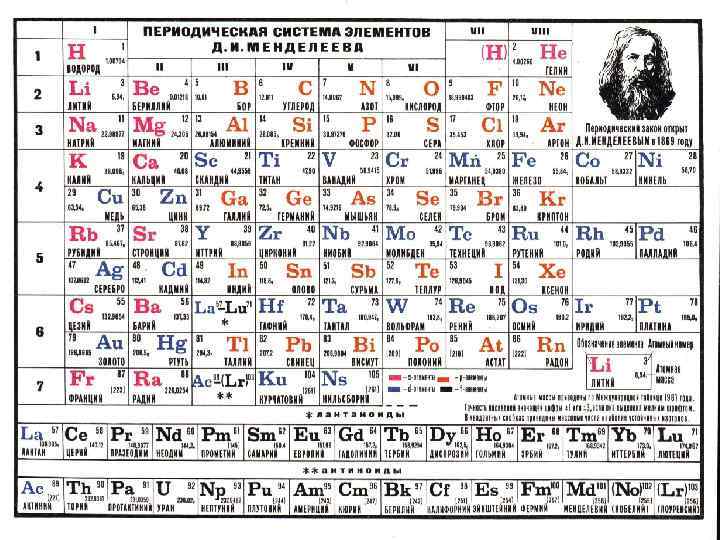
 ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА Свойства элементов периодически изменяются в соответствии с их атомным весом. 18 Ar(39, 948) – 19 K (39, 098); 52 Te(127, 60) – 53 I(126, 904); 27 Co(58, 933) – 28 Ni(58, 69); 90 Th(232, 038) – 91 Pa(231, 0359). Периодический закон в современной трактовке: Свойства элементов периодически изменяются в соответствии с зарядом ядер их атомов. Периодическая таблица элементов является графическим выражением Периодического закона.
ПЕРИОДИЧЕСКАЯ СИСТЕМА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА Свойства элементов периодически изменяются в соответствии с их атомным весом. 18 Ar(39, 948) – 19 K (39, 098); 52 Te(127, 60) – 53 I(126, 904); 27 Co(58, 933) – 28 Ni(58, 69); 90 Th(232, 038) – 91 Pa(231, 0359). Периодический закон в современной трактовке: Свойства элементов периодически изменяются в соответствии с зарядом ядер их атомов. Периодическая таблица элементов является графическим выражением Периодического закона.

 Структура периодической таблицы В периодической таблице все элементы расположены по возрастающим атомным номерам в ряд, внутри которого периодически повторяются элементы со сходными свойствами. • Горизонтальные строчки Периодической таблицы называются ПЕРИОДАМИ, а вертикальные - ГРУППАМИ. • В группах собраны элементы с похожими химическими свойствами, а в периодах химические свойства постепенно изменяются. • Если сравнить между собой элементы разных периодов, то можно отметить важную особенность: • Номер ПЕРИОДА, в котором находится элемент, совпадает с номером его валентной оболочки. Эта валентная оболочка постепенно заполняется от начала к концу периода.
Структура периодической таблицы В периодической таблице все элементы расположены по возрастающим атомным номерам в ряд, внутри которого периодически повторяются элементы со сходными свойствами. • Горизонтальные строчки Периодической таблицы называются ПЕРИОДАМИ, а вертикальные - ГРУППАМИ. • В группах собраны элементы с похожими химическими свойствами, а в периодах химические свойства постепенно изменяются. • Если сравнить между собой элементы разных периодов, то можно отметить важную особенность: • Номер ПЕРИОДА, в котором находится элемент, совпадает с номером его валентной оболочки. Эта валентная оболочка постепенно заполняется от начала к концу периода.
 Изменение свойств элементов одного периода • Каждый период Периодической таблицы начинается активным металлом и заканчивается инертным газом. В больших периодах с ростом заряда ядра происходит заполнение внешней e-ной оболочки с номером n , а также незаполненной предвнешней с номером (n-1) и (n-2). В четных рядах больших периодов свойства изменяются, как в малых. Число заполненных оболочек=номеру внешней оболочки=номеру периода Группы – вертикальные колонки в периодической системе. Каждая разделена на главную А и побочную В.
Изменение свойств элементов одного периода • Каждый период Периодической таблицы начинается активным металлом и заканчивается инертным газом. В больших периодах с ростом заряда ядра происходит заполнение внешней e-ной оболочки с номером n , а также незаполненной предвнешней с номером (n-1) и (n-2). В четных рядах больших периодов свойства изменяются, как в малых. Число заполненных оболочек=номеру внешней оболочки=номеру периода Группы – вертикальные колонки в периодической системе. Каждая разделена на главную А и побочную В.
 Типы элементов: Если заполняются S- АО внешней оболочки - S – элементы P-АО внешней оболочки - P- элементы d-АО незаполненной предвнешней оболочки- d-элементы f- АО незаполненной третьей снаружи- f-элементы Главная А подгруппа Побочная В подгруппа Содержит s- или p- элементы Содержит d- или f- элементы n. S 1 -2 n. S 2 n. P 1 -6 2(n-1)d 1 -10 n. S 2(n-2)d 1 -14 n. S
Типы элементов: Если заполняются S- АО внешней оболочки - S – элементы P-АО внешней оболочки - P- элементы d-АО незаполненной предвнешней оболочки- d-элементы f- АО незаполненной третьей снаружи- f-элементы Главная А подгруппа Побочная В подгруппа Содержит s- или p- элементы Содержит d- или f- элементы n. S 1 -2 n. S 2 n. P 1 -6 2(n-1)d 1 -10 n. S 2(n-2)d 1 -14 n. S
 Периодичность в изменении свойств химических элементов 1. Атомный радиус 2. Энергия или потенциал ионизации. I. Это энергия, необходимая для отрыва внешнего электрона от нейтрального атома и превращения последнего в катион. Э – ē = Э+ - I (эндо процесс). Единицы измерения КДж/моль или Э. В/атом. На практике чаще используют термин « потенциал ионизации» I в вольтах (в). 3. Сродство к электрону Е. Это количество энергии, которое выделяется присоединении электрона к нейтральному атому и превращения последнего в анион. Э + ē = Э+ + Е (экзотермический процесс). Единицы измерения как и у потенциала ионизации.
Периодичность в изменении свойств химических элементов 1. Атомный радиус 2. Энергия или потенциал ионизации. I. Это энергия, необходимая для отрыва внешнего электрона от нейтрального атома и превращения последнего в катион. Э – ē = Э+ - I (эндо процесс). Единицы измерения КДж/моль или Э. В/атом. На практике чаще используют термин « потенциал ионизации» I в вольтах (в). 3. Сродство к электрону Е. Это количество энергии, которое выделяется присоединении электрона к нейтральному атому и превращения последнего в анион. Э + ē = Э+ + Е (экзотермический процесс). Единицы измерения как и у потенциала ионизации.
 4. Электроотрицательность. χ. По Малликену эта величина пропорциональна потенциалу ионизации и сродству к электрону: χ=
4. Электроотрицательность. χ. По Малликену эта величина пропорциональна потенциалу ионизации и сродству к электрону: χ=
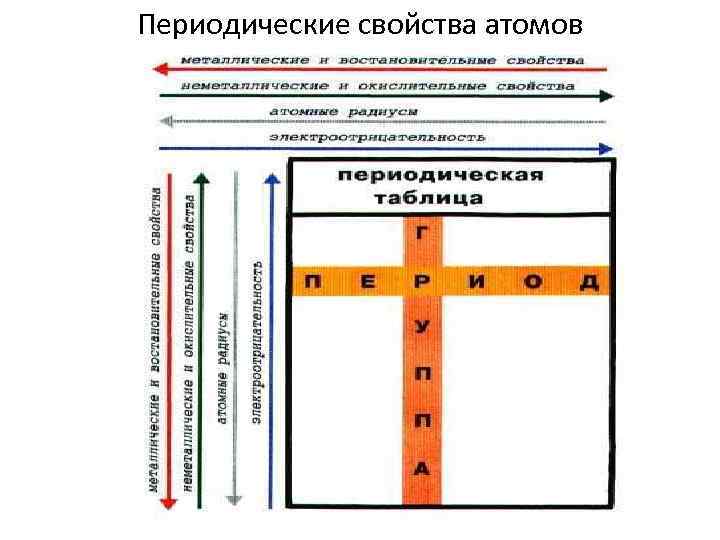 Периодические свойства атомов
Периодические свойства атомов
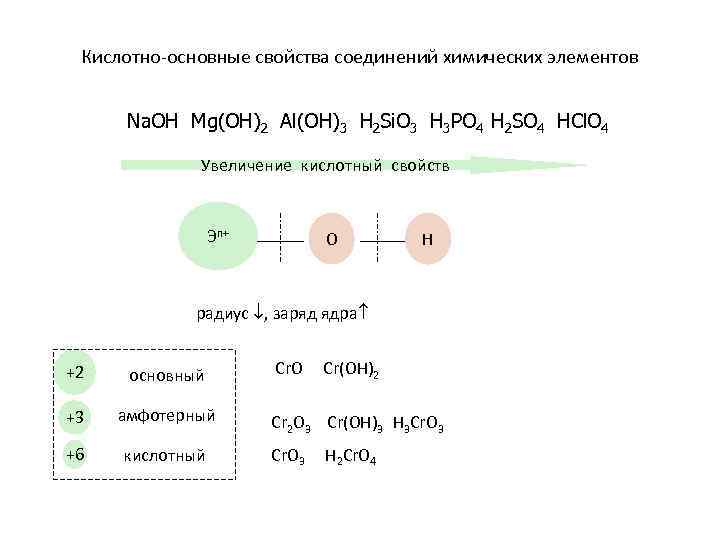 Кислотно-основные свойства соединений химических элементов Na. OН Mg(OH)2 Al(OH)3 H 2 Si. O 3 H 3 PO 4 H 2 SO 4 HСl. O 4 Увеличение кислотный свойств Эn+ О Н радиус , заряд ядра +2 основный +3 амфотерный +6 кислотный Cr. O Cr(OH)2 Cr 2 O 3 Cr(OH)3 H 3 Cr. O 3 H 2 Cr. O 4
Кислотно-основные свойства соединений химических элементов Na. OН Mg(OH)2 Al(OH)3 H 2 Si. O 3 H 3 PO 4 H 2 SO 4 HСl. O 4 Увеличение кислотный свойств Эn+ О Н радиус , заряд ядра +2 основный +3 амфотерный +6 кислотный Cr. O Cr(OH)2 Cr 2 O 3 Cr(OH)3 H 3 Cr. O 3 H 2 Cr. O 4
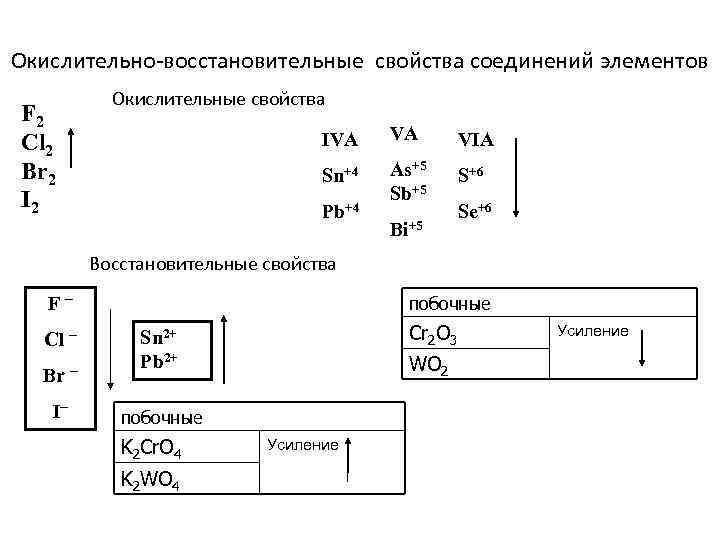 Окислительно-восстановительные свойства соединений элементов F 2 Cl 2 Br 2 I 2 Окислительные свойства IVA VA VIA Sn+4 As+5 Sb+5 S+6 Pb+4 Bi+5 Se+6 Восстановительные свойства F Cl Br I побочные Cr 2 O 3 Sn 2+ Pb 2+ WO 2 побочные K 2 Cr. O 4 K 2 WO 4 Усиление
Окислительно-восстановительные свойства соединений элементов F 2 Cl 2 Br 2 I 2 Окислительные свойства IVA VA VIA Sn+4 As+5 Sb+5 S+6 Pb+4 Bi+5 Se+6 Восстановительные свойства F Cl Br I побочные Cr 2 O 3 Sn 2+ Pb 2+ WO 2 побочные K 2 Cr. O 4 K 2 WO 4 Усиление


