АРОМАТИЧЕСКИЕ углеводороды.ppt
- Количество слайдов: 40
 «Строение ароматических углеводородов. Ароматическая связь»
«Строение ароматических углеводородов. Ароматическая связь»
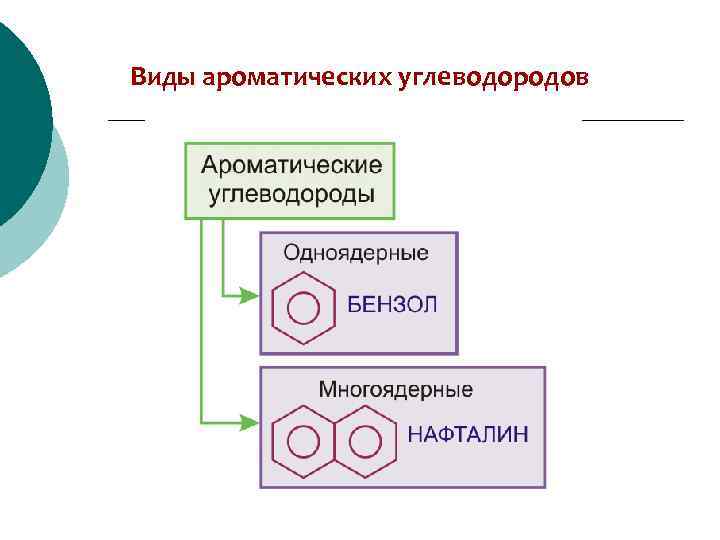 Виды ароматических углеводородов
Виды ароматических углеводородов
 С 6 Н 6
С 6 Н 6
 Арены ¡ ¡ Ароматическими углеводородами (аренами) называются вещества, в молекулах которых содержится одно или несколько бензольных колец — циклических групп атомов углерода с особым характером связей. Понятие “бензольное кольцо” требует расшифровки. Для этого необходимо рассмотреть строение молекулы бензола. Первая структура бензола была предложена в 1865 г. немецким ученым А. Кекуле:
Арены ¡ ¡ Ароматическими углеводородами (аренами) называются вещества, в молекулах которых содержится одно или несколько бензольных колец — циклических групп атомов углерода с особым характером связей. Понятие “бензольное кольцо” требует расшифровки. Для этого необходимо рассмотреть строение молекулы бензола. Первая структура бензола была предложена в 1865 г. немецким ученым А. Кекуле:
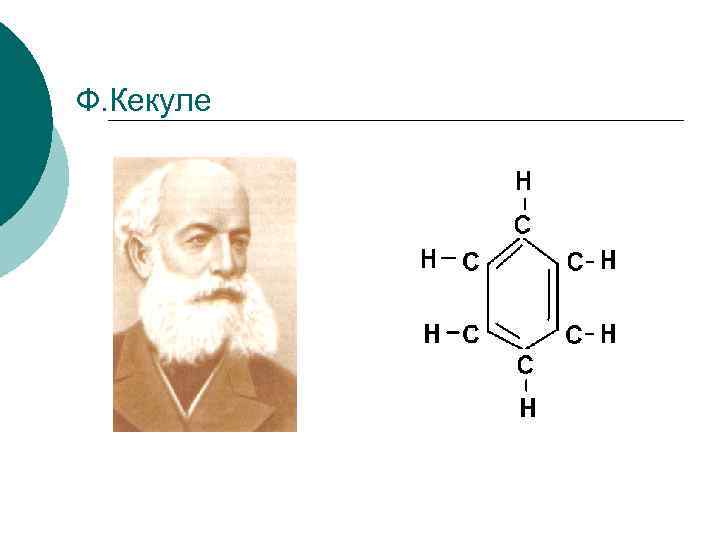 Ф. Кекуле
Ф. Кекуле
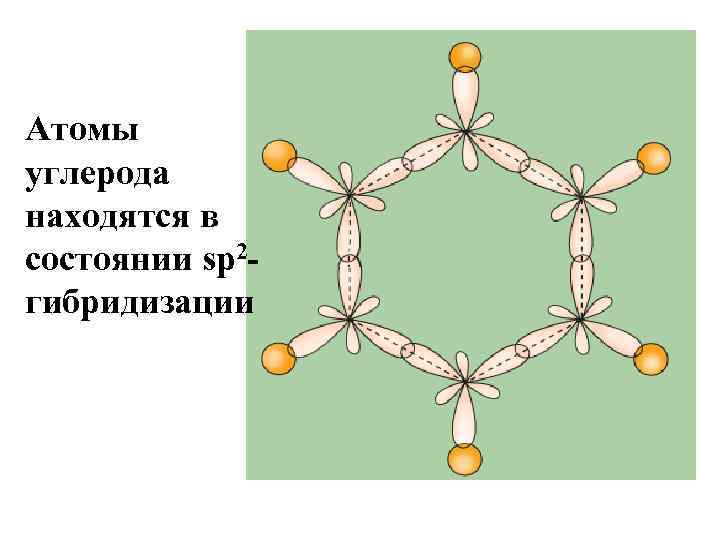 Атомы углерода находятся в состоянии sp 2 гибридизации
Атомы углерода находятся в состоянии sp 2 гибридизации
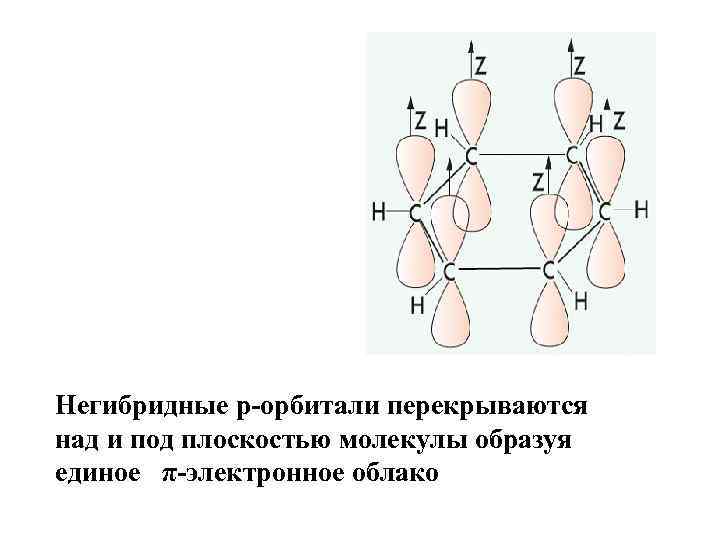 Негибридные р-орбитали перекрываются над и под плоскостью молекулы образуя единое π-электронное облако
Негибридные р-орбитали перекрываются над и под плоскостью молекулы образуя единое π-электронное облако
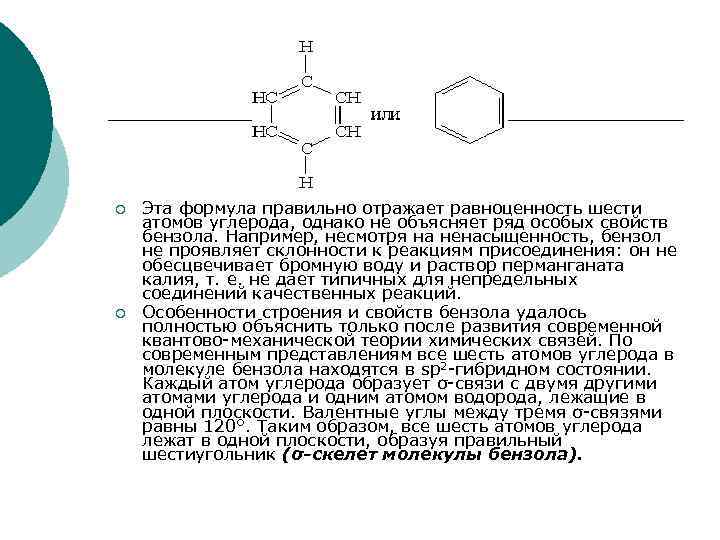 ¡ ¡ Эта формула правильно отражает равноценность шести атомов углерода, однако не объясняет ряд особых свойств бензола. Например, несмотря на ненасыщенность, бензол не проявляет склонности к реакциям присоединения: он не обесцвечивает бромную воду и раствор перманганата калия, т. е. не дает типичных для непредельных соединений качественных реакций. Особенности строения и свойств бензола удалось полностью объяснить только после развития современной квантово-механической теории химических связей. По современным представлениям все шесть атомов углерода в молекуле бензола находятся в sp 2 -гибридном состоянии. Каждый атом углерода образует σ-связи с двумя другими атомами углерода и одним атомом водорода, лежащие в одной плоскости. Валентные углы между тремя σ-связями равны 120°. Таким образом, все шесть атомов углерода лежат в одной плоскости, образуя правильный шестиугольник (σ-скелет молекулы бензола).
¡ ¡ Эта формула правильно отражает равноценность шести атомов углерода, однако не объясняет ряд особых свойств бензола. Например, несмотря на ненасыщенность, бензол не проявляет склонности к реакциям присоединения: он не обесцвечивает бромную воду и раствор перманганата калия, т. е. не дает типичных для непредельных соединений качественных реакций. Особенности строения и свойств бензола удалось полностью объяснить только после развития современной квантово-механической теории химических связей. По современным представлениям все шесть атомов углерода в молекуле бензола находятся в sp 2 -гибридном состоянии. Каждый атом углерода образует σ-связи с двумя другими атомами углерода и одним атомом водорода, лежащие в одной плоскости. Валентные углы между тремя σ-связями равны 120°. Таким образом, все шесть атомов углерода лежат в одной плоскости, образуя правильный шестиугольник (σ-скелет молекулы бензола).
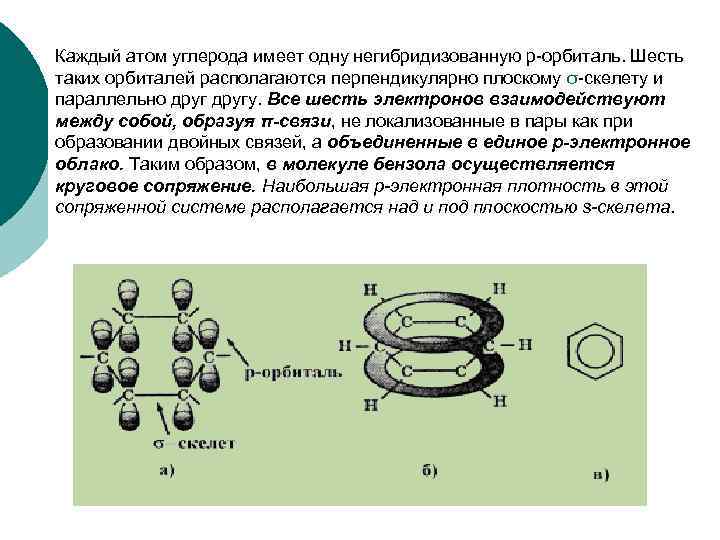 Каждый атом углерода имеет одну негибридизованную р-орбиталь. Шесть таких орбиталей располагаются перпендикулярно плоскому σ-скелету и параллельно другу. Все шесть электронов взаимодействуют между собой, образуя π-связи, не локализованные в пары как при образовании двойных связей, а объединенные в единое p-электронное облако. Таким образом, в молекуле бензола осуществляется круговое сопряжение. Наибольшая p-электронная плотность в этой сопряженной системе располагается над и под плоскостью s-скелета.
Каждый атом углерода имеет одну негибридизованную р-орбиталь. Шесть таких орбиталей располагаются перпендикулярно плоскому σ-скелету и параллельно другу. Все шесть электронов взаимодействуют между собой, образуя π-связи, не локализованные в пары как при образовании двойных связей, а объединенные в единое p-электронное облако. Таким образом, в молекуле бензола осуществляется круговое сопряжение. Наибольшая p-электронная плотность в этой сопряженной системе располагается над и под плоскостью s-скелета.
 Общая формула углеводородов ряда бензола: Cn. H 2 n-6 где n=6, 7, 8, 9, 10…. т. е. n ≥ 6
Общая формула углеводородов ряда бензола: Cn. H 2 n-6 где n=6, 7, 8, 9, 10…. т. е. n ≥ 6
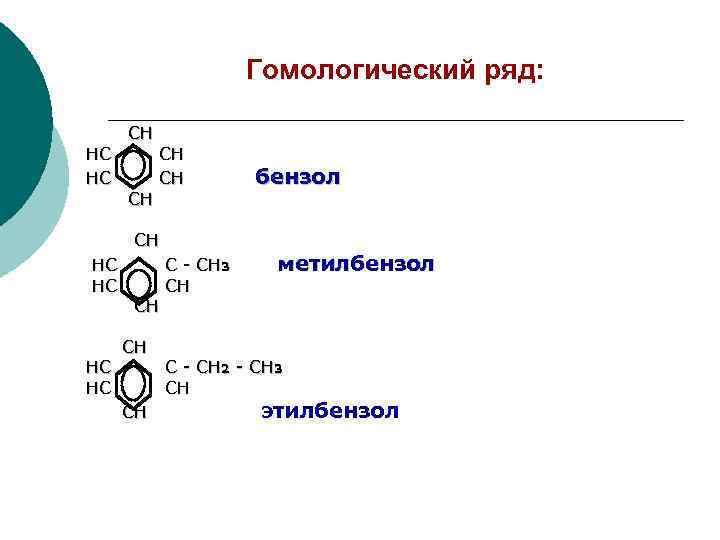 Гомологический ряд: HC HC CH CH CH C - С H 3 CH бензол метилбензол C - CH 2 - CH 3 CH этилбензол
Гомологический ряд: HC HC CH CH CH C - С H 3 CH бензол метилбензол C - CH 2 - CH 3 CH этилбензол
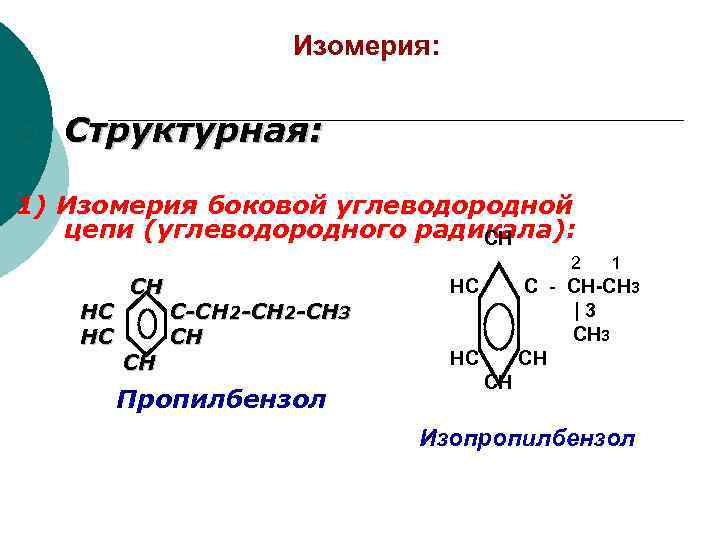 Изомерия: ¡ Структурная: 1) Изомерия боковой углеводородной цепи (углеводородного радикала): CH HC HC CH CH 2 HC C-CH 2 -CH 3 CH Пропилбензол 1 C - CH-CH 3 |3 CH HC CH Изопропилбензол
Изомерия: ¡ Структурная: 1) Изомерия боковой углеводородной цепи (углеводородного радикала): CH HC HC CH CH 2 HC C-CH 2 -CH 3 CH Пропилбензол 1 C - CH-CH 3 |3 CH HC CH Изопропилбензол
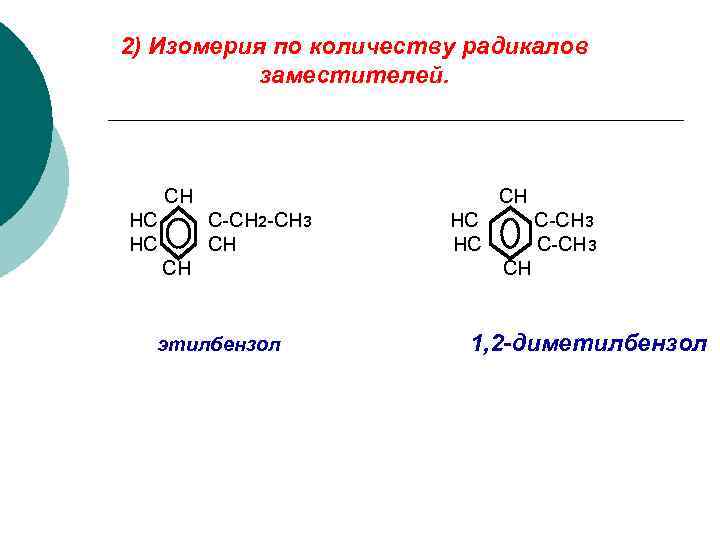 2) Изомерия по количеству радикалов заместителей. CH HC HC CH C-СH 2 -CH 3 CH CH этилбензол HC HC C-CH 3 CH 1, 2 -диметилбензол
2) Изомерия по количеству радикалов заместителей. CH HC HC CH C-СH 2 -CH 3 CH CH этилбензол HC HC C-CH 3 CH 1, 2 -диметилбензол
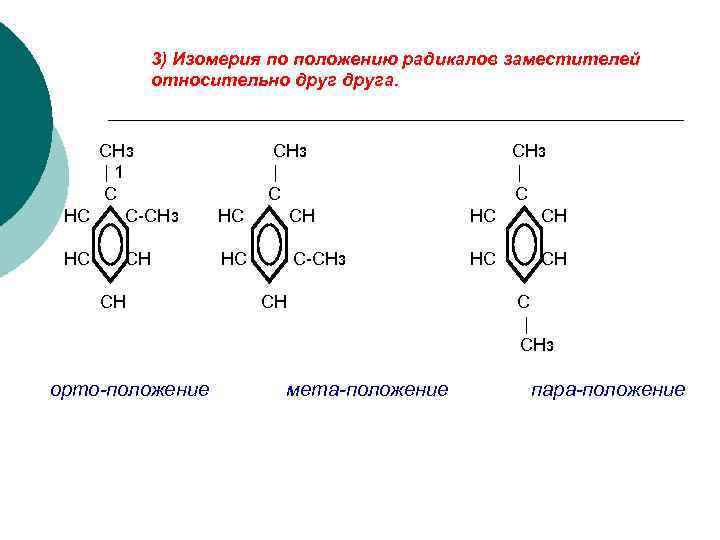 3) Изомерия по положению радикалов заместителей относительно друга. CH 3 |1 C HC C-CH 3 HC HC HC CH CH орто-положение CH 3 | C CH C-CH 3 CH мета-положение CH 3 | C HC CH C | CH 3 пара-положение
3) Изомерия по положению радикалов заместителей относительно друга. CH 3 |1 C HC C-CH 3 HC HC HC CH CH орто-положение CH 3 | C CH C-CH 3 CH мета-положение CH 3 | C HC CH C | CH 3 пара-положение
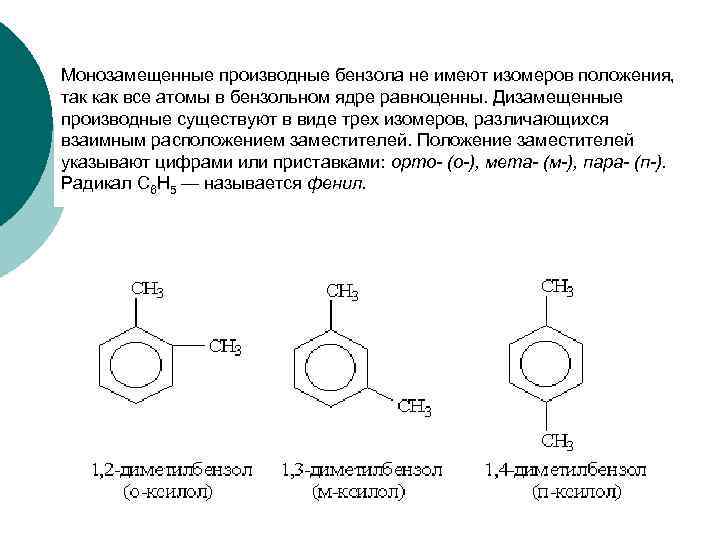 Монозамещенные производные бензола не имеют изомеров положения, так как все атомы в бензольном ядре равноценны. Дизамещенные производные существуют в виде трех изомеров, различающихся взаимным расположением заместителей. Положение заместителей указывают цифрами или приставками: орто- (о-), мета- (м-), пара- (п-). Радикал С 6 Н 5 — называется фенил.
Монозамещенные производные бензола не имеют изомеров положения, так как все атомы в бензольном ядре равноценны. Дизамещенные производные существуют в виде трех изомеров, различающихся взаимным расположением заместителей. Положение заместителей указывают цифрами или приставками: орто- (о-), мета- (м-), пара- (п-). Радикал С 6 Н 5 — называется фенил.
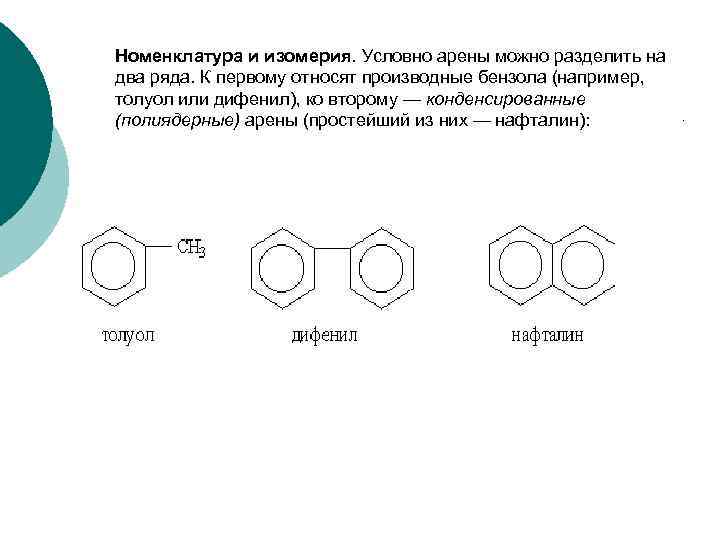 Номенклатура и изомерия. Условно арены можно разделить на два ряда. К первому относят производные бензола (например, толуол или дифенил), ко второму — конденсированные (полиядерные) арены (простейший из них — нафталин):
Номенклатура и изомерия. Условно арены можно разделить на два ряда. К первому относят производные бензола (например, толуол или дифенил), ко второму — конденсированные (полиядерные) арены (простейший из них — нафталин):
 Получение ароматических углеводородов и бензола: 1. 2. В промышленных масштабах бензол и его гомологи получают из нефти и каменного угля, поэтому их часто называют нафтены. Реакция тримеризации или реакция Зелинского: Cакт, 500˚С 3 СH≡CH CH HC HC CH CH CH Сакт- раскаленный активированный уголь
Получение ароматических углеводородов и бензола: 1. 2. В промышленных масштабах бензол и его гомологи получают из нефти и каменного угля, поэтому их часто называют нафтены. Реакция тримеризации или реакция Зелинского: Cакт, 500˚С 3 СH≡CH CH HC HC CH CH CH Сакт- раскаленный активированный уголь
 Способы получения 1. Получение из алифатических углеводородов. При пропускании алканов с неразветвленной цепью, имеющих не менее шести атомов углерода в молекуле, над нагретой платиной или оксидом хрома происходит дегидроциклизация — образование арена с выделением водорода:
Способы получения 1. Получение из алифатических углеводородов. При пропускании алканов с неразветвленной цепью, имеющих не менее шести атомов углерода в молекуле, над нагретой платиной или оксидом хрома происходит дегидроциклизация — образование арена с выделением водорода:
 2. Дегидрирование циклоалканов. Реакция происходит при пропускании паров циклогексана и его гомологов над нагретой платиной: 3. Получение гомологов бензола по реакции Фриделя -Крафтса (см. далее). 4. Сплавление солей ароматических кислот со щелочью:
2. Дегидрирование циклоалканов. Реакция происходит при пропускании паров циклогексана и его гомологов над нагретой платиной: 3. Получение гомологов бензола по реакции Фриделя -Крафтса (см. далее). 4. Сплавление солей ароматических кислот со щелочью:
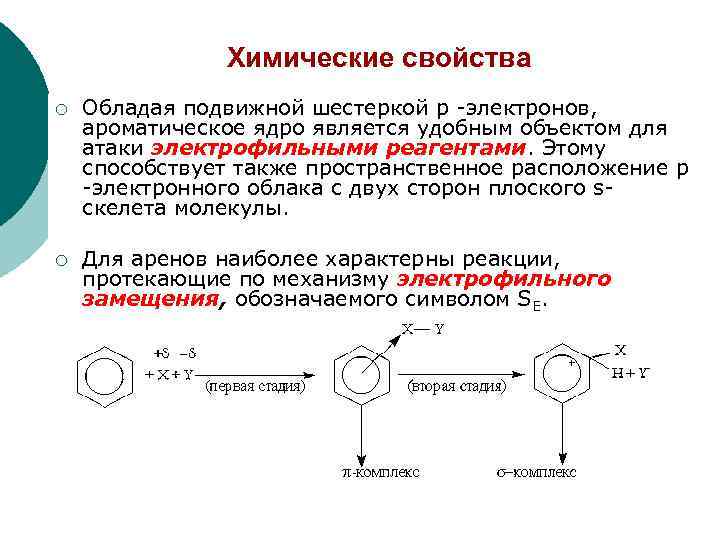 Химические свойства ¡ Обладая подвижной шестеркой p -электронов, ароматическое ядро является удобным объектом для атаки электрофильными реагентами. Этому способствует также пространственное расположение p -электронного облака с двух сторон плоского sскелета молекулы. ¡ Для аренов наиболее характерны реакции, протекающие по механизму электрофильного замещения, обозначаемого символом SE.
Химические свойства ¡ Обладая подвижной шестеркой p -электронов, ароматическое ядро является удобным объектом для атаки электрофильными реагентами. Этому способствует также пространственное расположение p -электронного облака с двух сторон плоского sскелета молекулы. ¡ Для аренов наиболее характерны реакции, протекающие по механизму электрофильного замещения, обозначаемого символом SE.
 Галогенирование Бензол не взаимодействует с хлором или бромом в обычных условиях. Реакция может протекать только в присутствии катализаторов — безводных Аl. Сl 3, Fe. Сl 3, Аl. Вr 3. В результате реакции образуются галогенозамещенные арены: Роль катализатора заключается в поляризации нейтральной молекулы галогена с образованием из нее электрофильной частицы:
Галогенирование Бензол не взаимодействует с хлором или бромом в обычных условиях. Реакция может протекать только в присутствии катализаторов — безводных Аl. Сl 3, Fe. Сl 3, Аl. Вr 3. В результате реакции образуются галогенозамещенные арены: Роль катализатора заключается в поляризации нейтральной молекулы галогена с образованием из нее электрофильной частицы:
 Нитрование Бензол очень медленно реагирует с концентрированной азотной кислотой даже при сильном нагревании. Однако при действии так называемой нитрующей смеси (смесь концентрированных азотной и серной кислот) реакция нитрования проходит достаточно легко:
Нитрование Бензол очень медленно реагирует с концентрированной азотной кислотой даже при сильном нагревании. Однако при действии так называемой нитрующей смеси (смесь концентрированных азотной и серной кислот) реакция нитрования проходит достаточно легко:
 Сулъфирование Реакция легко проходит под действием “дымящей” серной кислоты (олеума):
Сулъфирование Реакция легко проходит под действием “дымящей” серной кислоты (олеума):
 Алкилирование по Фриделю-Крафтсу В результате реакции происходит введение в бензольное ядро алкильной группы с получением гомологов бензола. Реакция протекает при действии на бензол галогеналканов RСl в присутствии катализаторов — галогенидов алюминия. Роль катализатора сводится к поляризации молекулы RСl с образованием электрофильной частицы, и в зависимости от строения радикала в галогеналкане можно получить разные гомологи бензола:
Алкилирование по Фриделю-Крафтсу В результате реакции происходит введение в бензольное ядро алкильной группы с получением гомологов бензола. Реакция протекает при действии на бензол галогеналканов RСl в присутствии катализаторов — галогенидов алюминия. Роль катализатора сводится к поляризации молекулы RСl с образованием электрофильной частицы, и в зависимости от строения радикала в галогеналкане можно получить разные гомологи бензола:
 • Алкилирование алкенами. Эти реакции широко используются в промышленности для получения этилбензола и изопропилбензола (кумола). Алкилирование проводят в присутствии катализатора Аl. Сl 3. Механизм реакции сходен с механизмом предыдущей реакции:
• Алкилирование алкенами. Эти реакции широко используются в промышленности для получения этилбензола и изопропилбензола (кумола). Алкилирование проводят в присутствии катализатора Аl. Сl 3. Механизм реакции сходен с механизмом предыдущей реакции:
 Все рассмотренные выше реакции протекают по механизму электрофильного замещения SE.
Все рассмотренные выше реакции протекают по механизму электрофильного замещения SE.
 Реакции присоединения к аренам приводят к разрушению ароматической системы и требуют больших затрат энергии, поэтому протекают только в жестких условиях.
Реакции присоединения к аренам приводят к разрушению ароматической системы и требуют больших затрат энергии, поэтому протекают только в жестких условиях.
 Гидрирование Реакция присоединения водорода к аренам идет при нагревании и высоком давлении в присутствии металлических катализаторов (Ni, Pt, Pd). Бензол превращается в циклогексан, а гомологи бензола — в производные циклогексана:
Гидрирование Реакция присоединения водорода к аренам идет при нагревании и высоком давлении в присутствии металлических катализаторов (Ni, Pt, Pd). Бензол превращается в циклогексан, а гомологи бензола — в производные циклогексана:
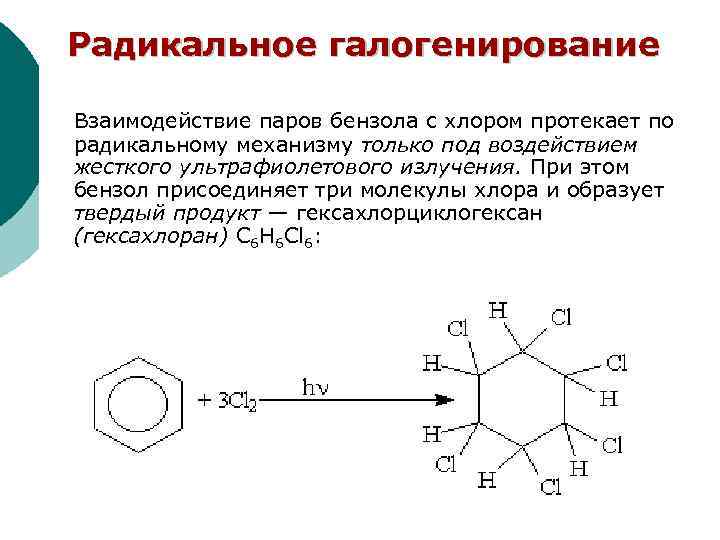 Радикальное галогенирование Взаимодействие паров бензола с хлором протекает по радикальному механизму только под воздействием жесткого ультрафиолетового излучения. При этом бензол присоединяет три молекулы хлора и образует твердый продукт — гексахлорциклогексан (гексахлоран) С 6 Н 6 Сl 6:
Радикальное галогенирование Взаимодействие паров бензола с хлором протекает по радикальному механизму только под воздействием жесткого ультрафиолетового излучения. При этом бензол присоединяет три молекулы хлора и образует твердый продукт — гексахлорциклогексан (гексахлоран) С 6 Н 6 Сl 6:
 Химические свойства гомологов бензола Гомологи бензола имеют целый ряд особых химических свойств, связанных со взаимным влиянием алкильного радикала на бензольное кольцо, и наоборот.
Химические свойства гомологов бензола Гомологи бензола имеют целый ряд особых химических свойств, связанных со взаимным влиянием алкильного радикала на бензольное кольцо, и наоборот.
 Правила ориентации (замещения) в бензольном кольце Ø Ø Ø Важнейшим фактором, определяющим химические свойства молекулы, является распределение в ней электронной плотности. Характер распределения зависит от взаимного влияния атомов. В молекулах, имеющих только s-связи, взаимное влияние атомов осуществляется через индуктивный эффект. В молекулах, представляющих собой сопряженные системы, проявляется действие мезомерного эффекта. Влияние заместителей, передающееся по сопряженной системе pсвязей, называется мезомерным (М) эффектом.
Правила ориентации (замещения) в бензольном кольце Ø Ø Ø Важнейшим фактором, определяющим химические свойства молекулы, является распределение в ней электронной плотности. Характер распределения зависит от взаимного влияния атомов. В молекулах, имеющих только s-связи, взаимное влияние атомов осуществляется через индуктивный эффект. В молекулах, представляющих собой сопряженные системы, проявляется действие мезомерного эффекта. Влияние заместителей, передающееся по сопряженной системе pсвязей, называется мезомерным (М) эффектом.
 Ø В молекуле бензола p -электронное облако распределено равномерно по всем атомам углерода за счет сопряжения. Если же в бензольное кольцо ввести какой-нибудь заместитель, это равномерное распределение нарушается и происходит перераспределение электронной плотности в кольце. Место вступления второго заместителя в бензольное кольцо определяется природой уже имеющегося заместителя.
Ø В молекуле бензола p -электронное облако распределено равномерно по всем атомам углерода за счет сопряжения. Если же в бензольное кольцо ввести какой-нибудь заместитель, это равномерное распределение нарушается и происходит перераспределение электронной плотности в кольце. Место вступления второго заместителя в бензольное кольцо определяется природой уже имеющегося заместителя.
 Заместители подразделяют на две группы в зависимости от проявляемого ими эффекта (мезомерного или индуктивного): 1. электронодонорные 2. электроноакцепторные
Заместители подразделяют на две группы в зависимости от проявляемого ими эффекта (мезомерного или индуктивного): 1. электронодонорные 2. электроноакцепторные
 Электронодонорные заместители проявляют +Ми +I-эффект и повышают электронную плотность в сопряженной системе. К ним относятся гидроксильная группа —ОН и аминогруппа —NН 2. Неподеленная пара электронов в этих группах вступает в общее сопряжение с p -электронной системой бензольного кольца и увеличивает длину сопряженной системы. В результате электронная плотность сосредоточивается в орто- и параположениях:
Электронодонорные заместители проявляют +Ми +I-эффект и повышают электронную плотность в сопряженной системе. К ним относятся гидроксильная группа —ОН и аминогруппа —NН 2. Неподеленная пара электронов в этих группах вступает в общее сопряжение с p -электронной системой бензольного кольца и увеличивает длину сопряженной системы. В результате электронная плотность сосредоточивается в орто- и параположениях:
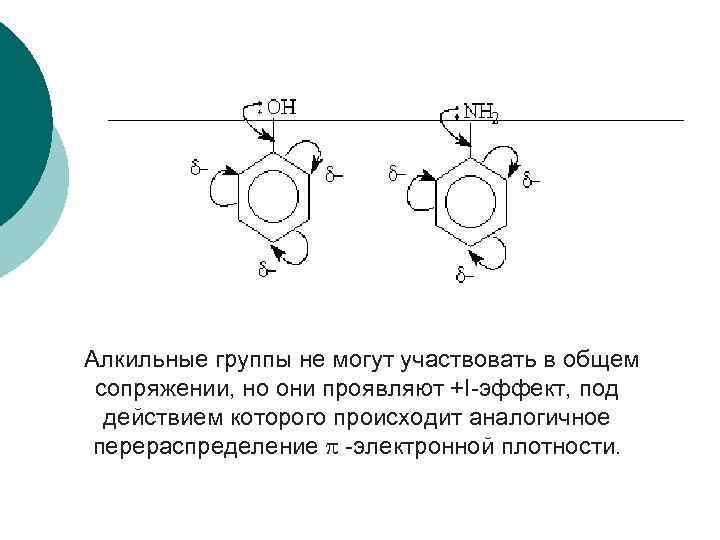 Алкильные группы не могут участвовать в общем сопряжении, но они проявляют +I-эффект, под действием которого происходит аналогичное перераспределение p -электронной плотности.
Алкильные группы не могут участвовать в общем сопряжении, но они проявляют +I-эффект, под действием которого происходит аналогичное перераспределение p -электронной плотности.
 Электроноакцепторные заместители проявляют -Мэффект и снижают электронную плотность в сопряженной системе. К ним относятся нитрогруппа —NO 2, сульфогруппа — SO 3 Н, альдегидная —СНО и карбоксильная —СООН группы. Полностью галогенизированные алкильные радикалы (например, —ССl 3) проявляют -I-эффект и также способствуют понижению электронной плотности кольца.
Электроноакцепторные заместители проявляют -Мэффект и снижают электронную плотность в сопряженной системе. К ним относятся нитрогруппа —NO 2, сульфогруппа — SO 3 Н, альдегидная —СНО и карбоксильная —СООН группы. Полностью галогенизированные алкильные радикалы (например, —ССl 3) проявляют -I-эффект и также способствуют понижению электронной плотности кольца.
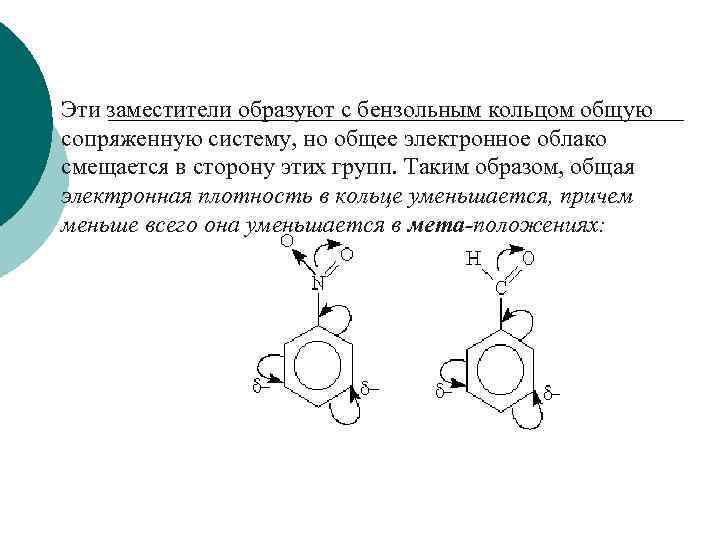 Эти заместители образуют с бензольным кольцом общую сопряженную систему, но общее электронное облако смещается в сторону этих групп. Таким образом, общая электронная плотность в кольце уменьшается, причем меньше всего она уменьшается в мета-положениях:
Эти заместители образуют с бензольным кольцом общую сопряженную систему, но общее электронное облако смещается в сторону этих групп. Таким образом, общая электронная плотность в кольце уменьшается, причем меньше всего она уменьшается в мета-положениях:
 Заместители, обладающие +I-эффектом или +М-эффектом, способствуют электрофильному замещению в орто- и параположениях бензольного кольца и называются заместителями (ориентантами) первого рода:
Заместители, обладающие +I-эффектом или +М-эффектом, способствуют электрофильному замещению в орто- и параположениях бензольного кольца и называются заместителями (ориентантами) первого рода:
 Заместители, обладающие -I-эффектом или -Мэффектом, направляют электрофильное замещение в мета-положения бензольного кольца и называются заместителями (ориентантами) второго рода:
Заместители, обладающие -I-эффектом или -Мэффектом, направляют электрофильное замещение в мета-положения бензольного кольца и называются заместителями (ориентантами) второго рода:
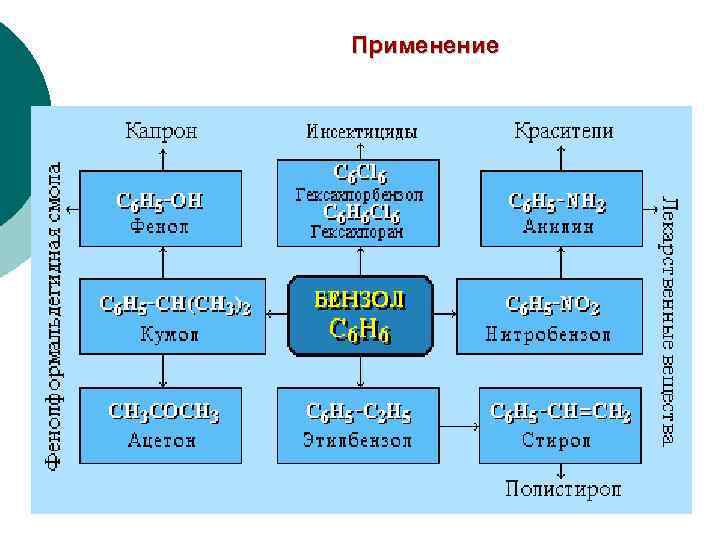 Применение
Применение


