 Степень окисления - это условный заряд, возникающий на атоме при смещении электронов от атома к атому
Степень окисления - это условный заряд, возникающий на атоме при смещении электронов от атома к атому
 Степень окисления простых веществ равна О Атомное строение: S 0, P 0, Si 0 Молекулярное строение: 0, Cl 2 0, O 2 0 N 2
Степень окисления простых веществ равна О Атомное строение: S 0, P 0, Si 0 Молекулярное строение: 0, Cl 2 0, O 2 0 N 2
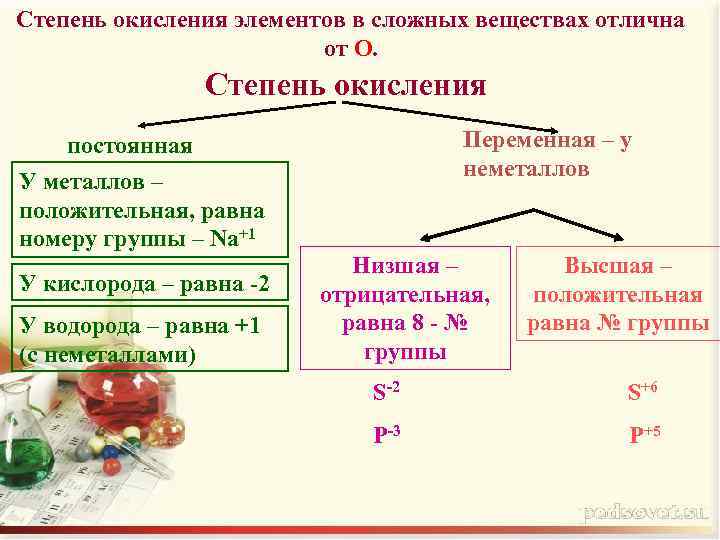 Степень окисления элементов в сложных веществах отлична от О. Степень окисления постоянная У металлов – положительная, равна номеру группы – Na+1 У кислорода – равна -2 У водорода – равна +1 (с неметаллами) Переменная – у неметаллов Низшая – отрицательная, равна 8 - № группы Высшая – положительная равна № группы S-2 S+6 P-3 P+5
Степень окисления элементов в сложных веществах отлична от О. Степень окисления постоянная У металлов – положительная, равна номеру группы – Na+1 У кислорода – равна -2 У водорода – равна +1 (с неметаллами) Переменная – у неметаллов Низшая – отрицательная, равна 8 - № группы Высшая – положительная равна № группы S-2 S+6 P-3 P+5
 Атомы металлов отдают электроны с внешнего слоя и превращаются в положительно заряженные ионы Ca 0 атом -2 электрона +2 Ca ион
Атомы металлов отдают электроны с внешнего слоя и превращаются в положительно заряженные ионы Ca 0 атом -2 электрона +2 Ca ион
 Атомы неметаллов принимают электроны на внешний слой до его завершения и превращаются в отрицательно заряженные ионы. Cl 02 атом +2 электрона -1 2 Cl ион
Атомы неметаллов принимают электроны на внешний слой до его завершения и превращаются в отрицательно заряженные ионы. Cl 02 атом +2 электрона -1 2 Cl ион
 Атомы неметаллов смещают электроны внешнего слоя к более электроотрицательным элементами и становятся положительно заряженны. C -4 электрона C +4
Атомы неметаллов смещают электроны внешнего слоя к более электроотрицательным элементами и становятся положительно заряженны. C -4 электрона C +4
 Сумма степеней окисления в молекуле равна (-2) х 3 = - 6 0 Al 2 S 3 S-2 Al+3 (+6) + (- 6) = 0 (+3) х 2 = +6
Сумма степеней окисления в молекуле равна (-2) х 3 = - 6 0 Al 2 S 3 S-2 Al+3 (+6) + (- 6) = 0 (+3) х 2 = +6
 Алгоритм определения степени окисления по формуле Наименьшее общее кратное 3 х2= 6 +3 - Al 2 S 3 Металл – положительная СО Находится в III А группе - +3 6: 3= 2 Неметалл – переменная СО Отрицательная Сумма степеней окисления в молекуле равна 0
Алгоритм определения степени окисления по формуле Наименьшее общее кратное 3 х2= 6 +3 - Al 2 S 3 Металл – положительная СО Находится в III А группе - +3 6: 3= 2 Неметалл – переменная СО Отрицательная Сумма степеней окисления в молекуле равна 0
 Проверка +6 -6 +3 -2 Al 2 S 3
Проверка +6 -6 +3 -2 Al 2 S 3
 Определите С. О. по формулам Cl 2 O 7, Na. Сl, Na 2 S, Mg. O, H 3 N, N 2, Al 2 S 3, Cu 2 O
Определите С. О. по формулам Cl 2 O 7, Na. Сl, Na 2 S, Mg. O, H 3 N, N 2, Al 2 S 3, Cu 2 O
 NO, N 2 O 3, PCl 5, Cu. Cl 2
NO, N 2 O 3, PCl 5, Cu. Cl 2
 Определите степени окисления, валентность элементов, химическую связь, в веществах формулы которых: а) Cl 2 O 7, Cl 2 O, Cl. O 2; б) Fe. Cl 2, Fe. Cl 3; в) Mn. S, Mn. O 2, Mn. F 4, Mn. O, Mn. Cl 4; r) Cu 2 O, Mg 2 Si, Si. Cl 4, Na 3 N, Fe. S.
Определите степени окисления, валентность элементов, химическую связь, в веществах формулы которых: а) Cl 2 O 7, Cl 2 O, Cl. O 2; б) Fe. Cl 2, Fe. Cl 3; в) Mn. S, Mn. O 2, Mn. F 4, Mn. O, Mn. Cl 4; r) Cu 2 O, Mg 2 Si, Si. Cl 4, Na 3 N, Fe. S.