 Степень окисления – это условный заряд атома в молекуле, вычисленный из предположения, что молекула состоит только из ионов.
Степень окисления – это условный заряд атома в молекуле, вычисленный из предположения, что молекула состоит только из ионов.
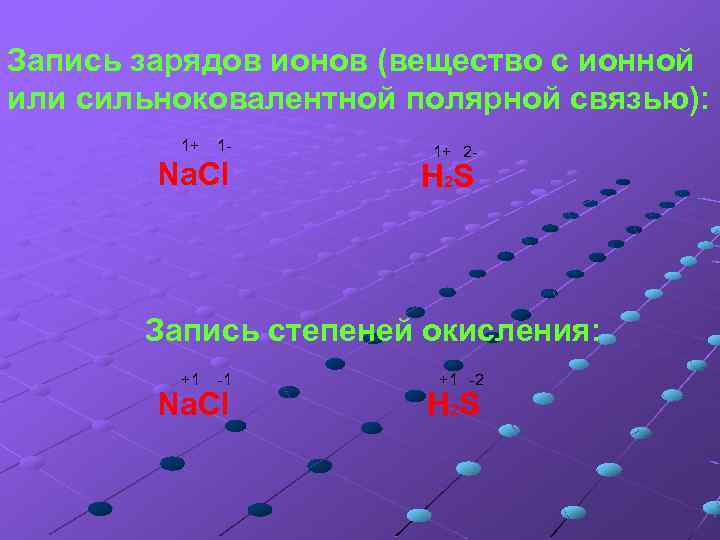 Запись зарядов ионов (вещество с ионной или сильноковалентной полярной связью): 1+ 1 - Na. Cl 1+ 2 - H 2 S Запись степеней окисления: +1 -1 Na. Cl +1 -2 H 2 S
Запись зарядов ионов (вещество с ионной или сильноковалентной полярной связью): 1+ 1 - Na. Cl 1+ 2 - H 2 S Запись степеней окисления: +1 -1 Na. Cl +1 -2 H 2 S
 (Э. О. ) - это свойство атома химического элемента притягивать к себе электроны из общих электронных пар. F – самый э. о. элемент.
(Э. О. ) - это свойство атома химического элемента притягивать к себе электроны из общих электронных пар. F – самый э. о. элемент.
 Основные положения для расчёта степеней окисления элементов в соединениях: -1 F Щелочные металлы ( I группа главная подгруппа ): +1 Li +1 Na +1 K
Основные положения для расчёта степеней окисления элементов в соединениях: -1 F Щелочные металлы ( I группа главная подгруппа ): +1 Li +1 Na +1 K
 Щелочноземельные металлы ( II группа главная подгруппа ): +2 Ba +2 +2 Ca Mg
Щелочноземельные металлы ( II группа главная подгруппа ): +2 Ba +2 +2 Ca Mg
 +1 Н с элементами с большим значением Э. О. : +1 -1 HCl +1 -2 H 2 S -1 Н с элементами с меньшим значением Э. О. (гидриды): +1 -1 +2 -1 Na. H - гидрид натрия Ca. H 2 - гидрид кальция
+1 Н с элементами с большим значением Э. О. : +1 -1 HCl +1 -2 H 2 S -1 Н с элементами с меньшим значением Э. О. (гидриды): +1 -1 +2 -1 Na. H - гидрид натрия Ca. H 2 - гидрид кальция
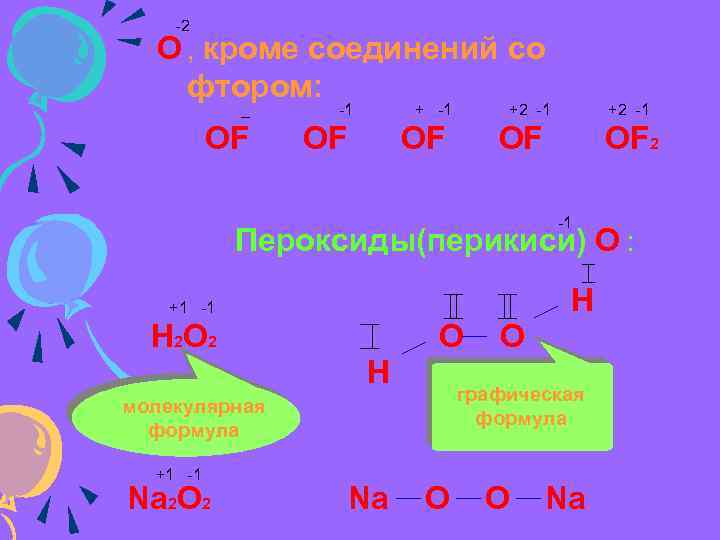 -2 О , кроме соединений со фтором: _ OF -1 + -1 OF +2 -1 OF OF 2 -1 Пероксиды(перикиси) О : Н +1 -1 Н 2 О 2 O H графическая формула молекулярная формула +1 -1 Na 2 O 2 Na O O O Na
-2 О , кроме соединений со фтором: _ OF -1 + -1 OF +2 -1 OF OF 2 -1 Пероксиды(перикиси) О : Н +1 -1 Н 2 О 2 O H графическая формула молекулярная формула +1 -1 Na 2 O 2 Na O O O Na
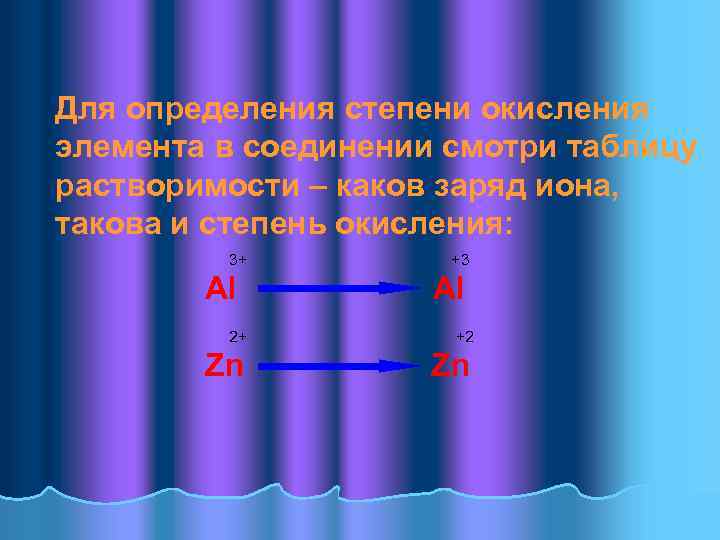 Для определения степени окисления элемента в соединении смотри таблицу растворимости – каков заряд иона, такова и степень окисления: 3+ Al +3 Al 2+ +2 Zn Zn
Для определения степени окисления элемента в соединении смотри таблицу растворимости – каков заряд иона, такова и степень окисления: 3+ Al +3 Al 2+ +2 Zn Zn
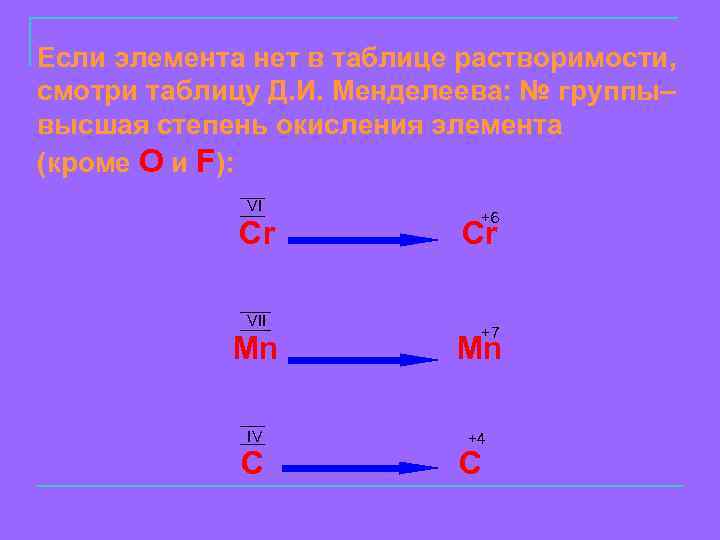 Если элемента нет в таблице растворимости, смотри таблицу Д. И. Менделеева: № группы– высшая степень окисления элемента (кроме О и F): VI Cr VII +6 Cr +7 Mn Mn IV +4 C C
Если элемента нет в таблице растворимости, смотри таблицу Д. И. Менделеева: № группы– высшая степень окисления элемента (кроме О и F): VI Cr VII +6 Cr +7 Mn Mn IV +4 C C
 это сложные вещества, состоящие из двух элементов. это сложные вещества, состоящие из двух элементов, один из которых кислород со степенью окисления -2.
это сложные вещества, состоящие из двух элементов. это сложные вещества, состоящие из двух элементов, один из которых кислород со степенью окисления -2.