АРО Методы разделения.ppt
- Количество слайдов: 41

Стадии пробоподготовки • Высушивание (определение влаги) • Разложение • Устранение влияния мешающих компонентов • Разделение и концентрирование.

Способы устранения мешающих компонентов • Маскирование • разделение веществ (концентрирование). Маскирование – это перевод мешающих компонентов в такую форму, которая уже не оказывает влияние на определение

Методы маскирования • Связывание мешающего иона в прочный комплекс; • Создание благоприятных условий протекания реакции регулированием р. Н; • Изменение степени окисления мешающего иона; • Осаждение мешающих ионов без отделения осадка; • Другие (изменение экстрагента, температуры и т. д. ).

Связывание мешающего иона в прочный комплекс. Условие: ßMR >> ßXR М – мешающий ион, Х – определяемый. При определении Со 2+ в виде [Co(SCN)4]2 - cинего цвета мешающее влияние Fe 3+ (образует [Fe(SCN)n]3 -n красного цвета) устраняют добавлением F - иона. Образуется бесцветный комплекс Fe. F 63 -. Фторид – маскирователь ионов Fe(III).
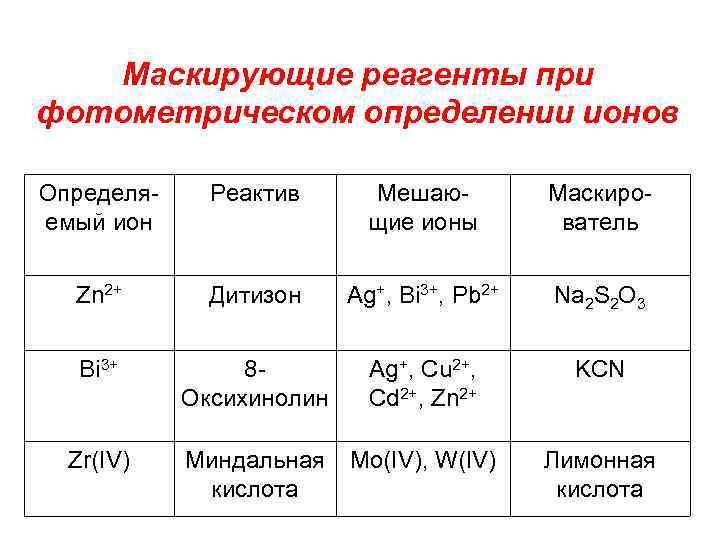
Маскирующие реагенты при фотометрическом определении ионов Определяемый ион Реактив Мешающие ионы Маскирователь Zn 2+ Дитизон Ag+, Bi 3+, Pb 2+ Na 2 S 2 O 3 Bi 3+ 8 Оксихинолин Ag+, Cu 2+, Cd 2+, Zn 2+ KCN Zr(IV) Миндальная Mo(IV), W(IV) кислота Лимонная кислота

2. Регулирование р. Н раствора, в котором проводят реакцию. Пример: Анионы VO 3 - и WO 42 - в нейтральной среде образуют с хромотроповой кислотой комплексы жёлтого цвета. При р. Н = 2 комплекс образует только VO 3 -
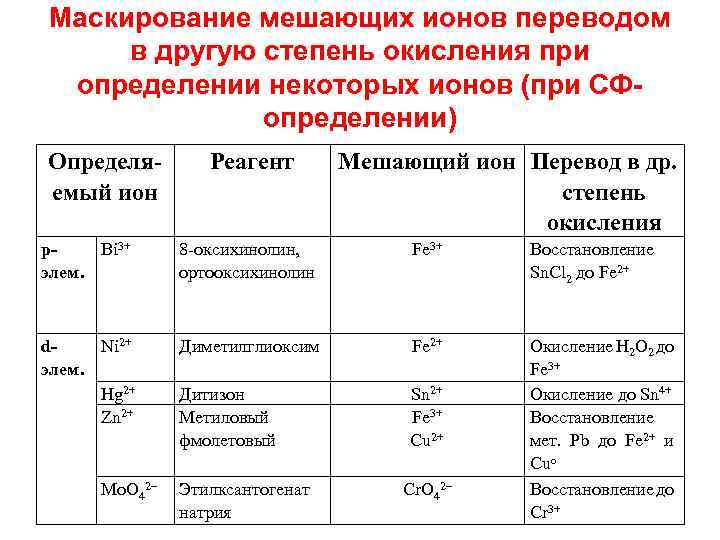
Маскирование мешающих ионов переводом в другую степень окисления при определении некоторых ионов (при СФопределении) Определяемый ион Реагент Мешающий ион Перевод в др. степень окисления р. Bi 3+ элем. 8 -оксихинолин, ортооксихинолин Fe 3+ Восстановление Sn. Cl 2 до Fe 2+ d. Ni 2+ элем. Hg 2+ Zn 2+ Диметилглиоксим Fe 2+ Дитизон Метиловый фмолетовый Sn 2+ Fe 3+ Cu 2+ Окисление H 2 O 2 до Fe 3+ Окисление до Sn 4+ Восстановление мет. Pb до Fe 2+ и Сuo Восстановление до Cr 3+ Mo. O 42– Этилксантогенат натрия Cr. O 42–

4. Осаждение мешающих ионов без отделения осадка. Пример: Комплексонометрическое определение ионов кальция в присутствии магния, который осаждают в виде гидроксида. Кs Mg(OH)2=6· 10 -10 Ks Ca(OH)2=6, 5· 10 -6
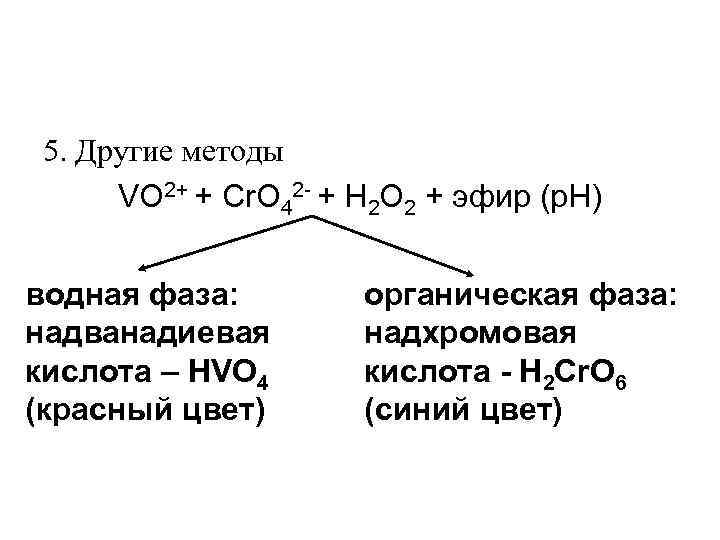
5. Другие методы VO 2+ + Cr. O 42 - + H 2 O 2 + эфир (p. H) водная фаза: надванадиевая кислота – HVO 4 (красный цвет) органическая фаза: надхромовая кислота - H 2 Cr. O 6 (синий цвет)

Оценка эффективности маскирования Индекс маскирования • логарифм отношения общей концентрации мешающего вещества к его концентрации, оставшейся не связанной.

Методы разделения и концентрирования • Разделение –это операция (процесс), в результате которой компоненты, составляющие исходную смесь, отделяются один от другого. • Концентрирование – это операция (процесс), в результате которой повышается отношение концентрации микрокомпонентов к концентрации макрокомпонента.

• Абсолютное концентрирование – это операция, в результате которой микрокомпоненты переходят из большой массы образца в малую. • Относительное концентрирование – это операция, в результате которой увеличивается соотношение между микрокомпонентом и главными мешающими макрокомпонентами

Количественные характеристики методов • Степень извлечения • Коэффициент концентрирования • Коэффициент разделения

Количественные характеристики R – cтепень извлечения qk – количество элемента в концентрате, qпр – количество элемента в пробе

K - коэффициент концентрирования При R=100 % Пример: При анализе воды 500 мл упаривается до 50 мл. К=10

Коэффициент разделения S D – коэффициент распределения

Классификация методов разделения (по фазовому признаку) • 1. Методы, основанные на образовании выделяемым веществом новой фазы • 2. Методы межфазного распределения. Основаны на различиях в распределении веществ между фазами • 3. Мембранные методы. Основаны на различиях в массопереносе через мембрану. • 4. Методы внутрифазного разделения. Основаны на механизмах разделения внутри одной фазы
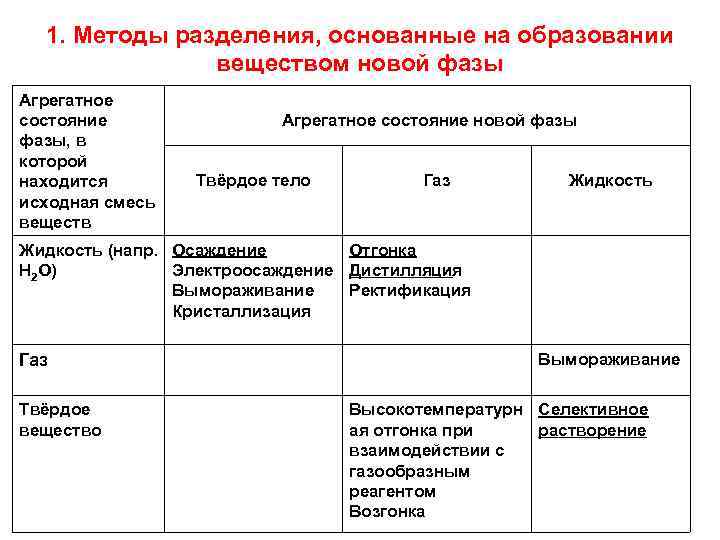
1. Методы разделения, основанные на образовании веществом новой фазы Агрегатное состояние Агрегатное состояние новой фазы, в которой Твёрдое тело Газ Жидкость находится исходная смесь веществ Жидкость (напр. Осаждение Отгонка Н 2 О) Электроосаждение Дистилляция Вымораживание Ректификация Кристаллизация Газ Твёрдое вещество Вымораживание Высокотемпературн Селективное ая отгонка при растворение взаимодействии с газообразным реагентом Возгонка
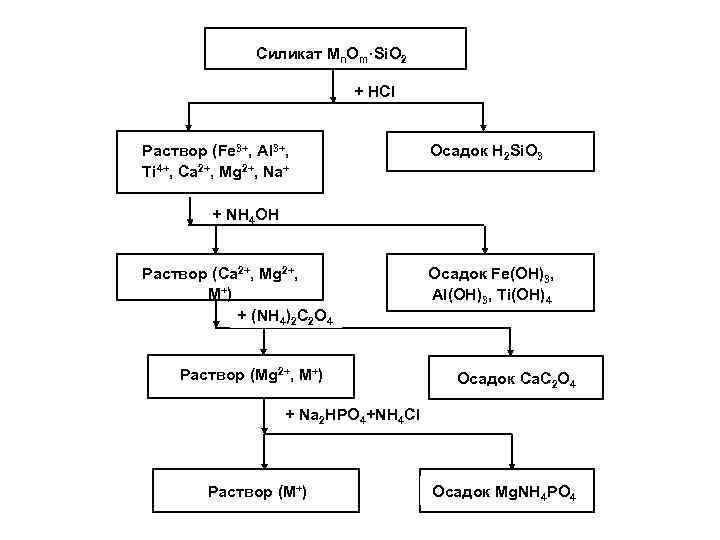
Силикат Mn. Om·Si. O 2 + HCl Раствор (Fe 3+, Al 3+, Ti 4+, Ca 2+, Mg 2+, Na+ Осадок H 2 Si. O 3 + NH 4 OH Раствор (Ca 2+, Mg 2+, M+) + (NH 4)2 C 2 O 4 Раствор (Mg 2+, M+) Осадок Fe(OH)3, Al(OH)3, Ti(OH)4 Осадок Ca. C 2 O 4 + Na 2 HPO 4+NH 4 Cl Раствор (M+) Осадок Mg. NH 4 PO 4

Электроосаждение – осаждение вещества из жидкой фазы на электроде за счет окислительновосстановительной реакции с гетерогенным переносом электронов.

Способы осуществления • Электроосаждение с внешним источником тока (для выделения катионных форм элементов). По уравнению Нернста вычисляют потенциалы выделения для конкретных условий проведения процесса разделения (разделение элементов возможно, если значения потенциалов выделения существенно отличаются). • Электрохимическое осаждение продуктов окислительно-восстановительных реакций, происходящих на электродах под воздействием приложенной разности потенциалов.

Способы осуществления • Внутренний электролиз – электролитическое выделение на одном из электродов гальванического элемента. • Самопроизвольное осаждение на поверхности электроотрицательного металла (цементация). Теоретически: чем больше разность потенциалов между осаждаемым и осаждающим металлами, тем более полное должно быть выделение. Практически: цементация зависит от ряда факторов: кислотности раствора, природы находящихся в растворе ионов, присутствия комплексообразующих лигандов и т. д.

Достоинства электроосаждения: • Не вводятся дополнительные реактивы в разновидностях 1, 3, 4. • Экономически выгодны, т. к. электроэнергия дешевле многих реактивов.

• Вымораживание – (метод разделения и концентрирования) применяется при анализе газов для отделения влаги, а так же для криогенного концентрирования более высококипящих примесей. • Отгонка – более эффективно выделение из раствора матричных компонентов. Процесс отгонки часто совмещают с процессом растворения твердой матрицы (например, при анализе В, Si. O 2, Ge, As и др. на содержание примесей). Обычно отгоняют летучие фториды, хлориды и пр.

• Дистилляция и ректификация – эти методы применяются в основном в препаративных целях. • Перегонку применяют для очистки воды, растворов кислот, органических растворителей. • Дистилляционные методы применяются и для концентрирования нелетучих примесей (упаривание растворов). • Ректификацию используют для получения чистых препаратов и для выделения определенных фракций при соответствующих значениях температуры.

• Высокотемпературная отгонка при взаимодействии с газообразным реагентом – применяется при определении S, С в металлах и сплавах. Их превращают в оксиды при сжигании в потоке кислорода. Газообразным реагентом является O 2. Кроме кислорода используют HCl, Cl 2, CCl 4 и др. • Селективное растворение – применяют • При определении неметаллических включений (оксидов, карбидов, нитридов) в сталях, сплавах. Образцы сталей, сплавов растворяют в HCl, H 3 PO 4 (кислоты-окислители не используют). • При определении меди или примесей в медных сплавах. Сплав растворяют в HCl, медь остается в осадке в виде Cu. O. • При анализе минералов, горных пород: силикат + HCl (получается раствор и осадок H 2 Si. O 3).

2. Методы межфазного распределения. Основаны на различиях в распределении вещества между фазами Экстракция, сорбция, хроматографические методы (газовая, газожидкостная, ионообменная и другие виды хроматографии), соосаждение, зонная плавка и др.

Количественная характеристика процессов, лежащих в основе методов разделения этой группы: Коэффициент распределения где сi’, сi’’ – концентрации вещества в двух фазах: исходной и ’ извлекаемой. где сi , сi’’ – концентрации вещества в двух фазах: исходной и извле Селективность извлечения характеризуется коэффициентом:

Способы осуществления процесса межфазного распределения Однократное равновесное распределение Многократное повторение процесса распределения Коэффициенты распределения KDi и KDj существенно KDi и KDj мало различаются 1. Выбор новых селективных 1. Обработка раствора свежими экстрагентов порциями экстрагента (n раз) 2. Прокачка раствора через 1. Синтез селективных сорбентов сорбент (перистальтический насос)

3. Мембранные методы разделения Мембрана - это разделительная перегородка, способная реагировать на изменение физико-химических параметров сред, находящихся по обе стороны от неё. Движущая сила процессаградиент концентрации, давления, температуры, электрического потенциала
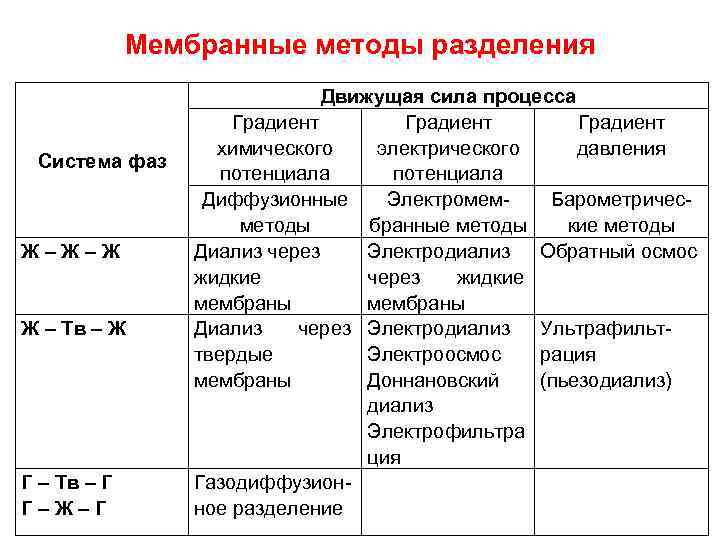
Мембранные методы разделения Система фаз Ж – Ж Ж – Тв – Ж Г – Тв – Г Г – Ж – Г Движущая сила процесса Градиент химического электрического давления потенциала Диффузионные Электромем. Барометричесметоды бранные методы кие методы Диализ через Электродиализ Обратный осмос жидкие через жидкие мембраны Диализ через Электродиализ Ультрафильттвердые Электроосмос рация мембраны Доннановский (пьезодиализ) диализ Электрофильтра ция Газодиффузион- ное разделение

Диализ – процесс массопереноса через твердые и жидкие мембраны В соответствие с уравнением Фика, скорость массопереноса пропорциональна коэффициенту диффузии (D): где Di – коэффициент диффузии i-того вещества в фазе мембраны; Δс – градиент его концентрации в мембране.

• Электродиализ – если к мембране приложить ЭДС, то основным типом массопереноса для заряженных частиц становится электромиграция. • Доннановский диализ –движущую силу процесса определяет разность доннановских потенциалов, возникающих на границах раздела фаз со стороны отдающего и принимающего растворов при наличии между ними концентрационных градиентов ионов.

• Газодиффузионное разделение – это процесс разделения газов при переносе через твердые или жидкие мембраны. Движущей силой процесса является градиент концентраций переносимого газового компонента, обусловленный разницей парциальных давлений газа по обе стороны мембраны. Коэффициенты разделения газов определяются различием их растворимости в фазе мембраны.

• Электроосмос – метод выделения одноименно заряженных ионов, основанный на движении жидкости вдоль заряженной поверхности (мембраны) под влиянием внешнего электрического поля. • Электрофильтрация – метод выделения одноименно заряженных ионов, основанный на прохождении ионов через пористые мембраны (под влиянием внешнего электрического поля).

Баромембранные методы (обратный осмос, ультрафильтрация). • Обратный осмос – это движение растворителя через пористую мембрану из концентрированного раствора в более разбавленный. Проявляется при перепаде давления р на мембране, превышающем осмотическое давление – π. Движущей силой процесса является градиент давления Δр = р – π. • Ультрафильтрация – отделение (разделение) частиц и молекул, существенно отличающихся по размерам от молекул растворителя.

Преимущества мембранных методов: • Простота и компактность аппаратурного оформления • Экологическая чистота • Непрерывность процесса • Возможность автоматизации. Применение - опреснение природных вод (электродиализ) – очистка и концентрирование примесей из сточных вод (электродиализ) – разделение газовых смесей (газодиффузионное разделение) – ультрафильтрационное разделение ферментов и т. д.
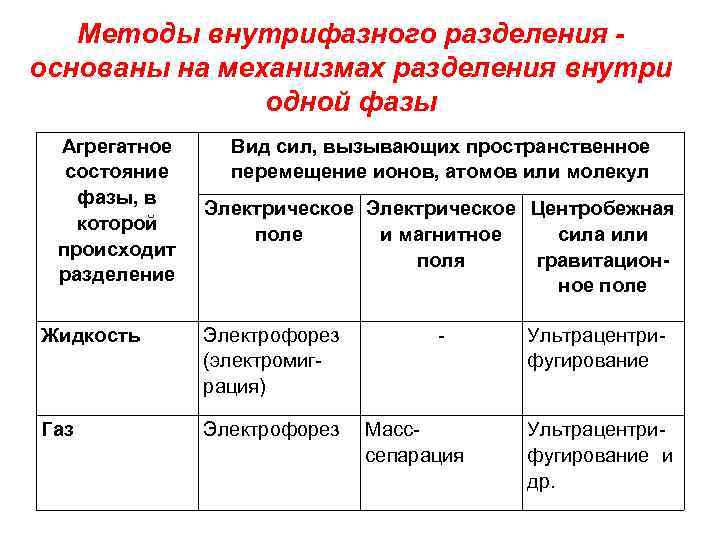
Методы внутрифазного разделения основаны на механизмах разделения внутри одной фазы Агрегатное состояние фазы, в которой происходит разделение Вид сил, вызывающих пространственное перемещение ионов, атомов или молекул Электрическое Центробежная поле и магнитное сила или поля гравитационное поле Жидкость Электрофорез (электромиграция) Газ Электрофорез - Масссепарация Ультрацентрифугирование и др.

• Электрофорез (электромиграция) разделение ионов в растворах за счет различных скоростей их движения в электрическом поле. • Масс-сепарация - воздействие на систему ускоряющего электрического и отклоняющего магнитного полей. При двойном воздействии на ионы в растворе различия в массе и заряде проявляются в наибольшей степени.

Процесс масс-сепарации включает 3 этапа: • Получение ионов из молекул (атомов) исследуемого вещества и формирование ионного пучка; • Пространственное разделение пучка по массам ионов в магнитном и/или электрическом полях; • Улавливание и (в случае массспектрометрии) регистрация ионов соответствующих масс.
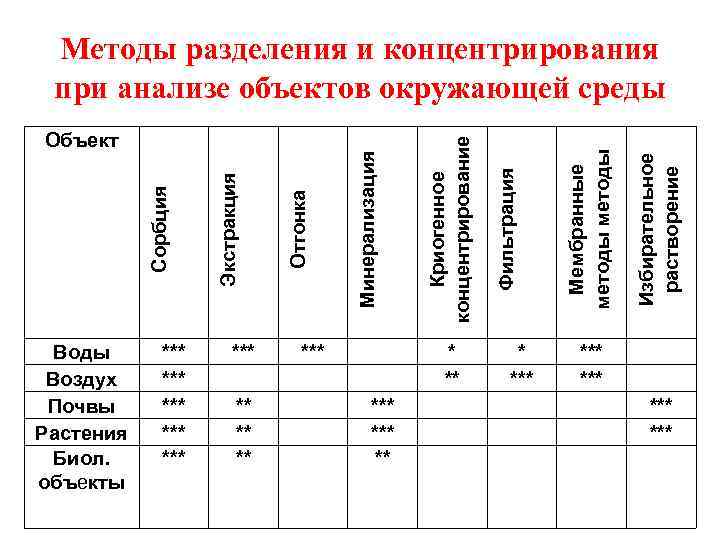
*** ** *** ** Фильтрация Криогенное концентрирование Отгонка *** * *** Избирательное растворение *** *** *** Мембранные методы Воды Воздух Почвы Растения Биол. объекты Экстракция Сорбция Объект Минерализация Методы разделения и концентрирования при анализе объектов окружающей среды ***
АРО Методы разделения.ppt