Способы выражения содержания растворенного вещества. Коллигативные свойства


Способы выражения содержания растворенного вещества. Коллигативные свойства растворов Лекция 9 по курсу «Общая химия»
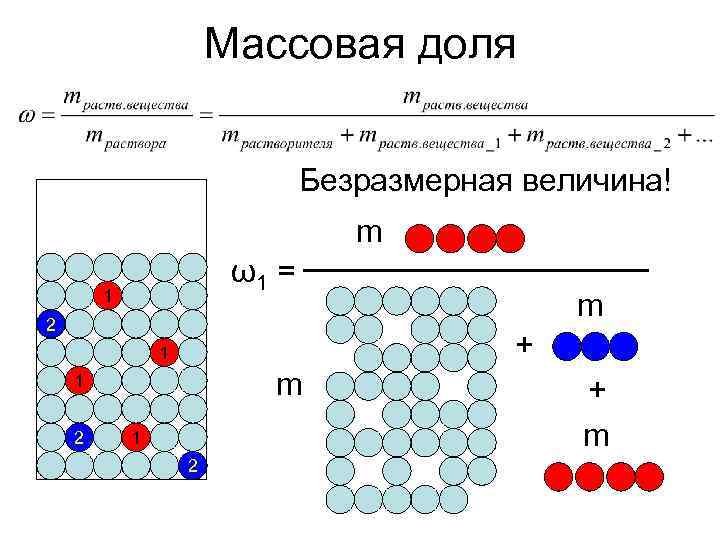
Массовая доля Безразмерная величина! m ω1 = 1 2 m 1 + 1 m + 2 1 m 2
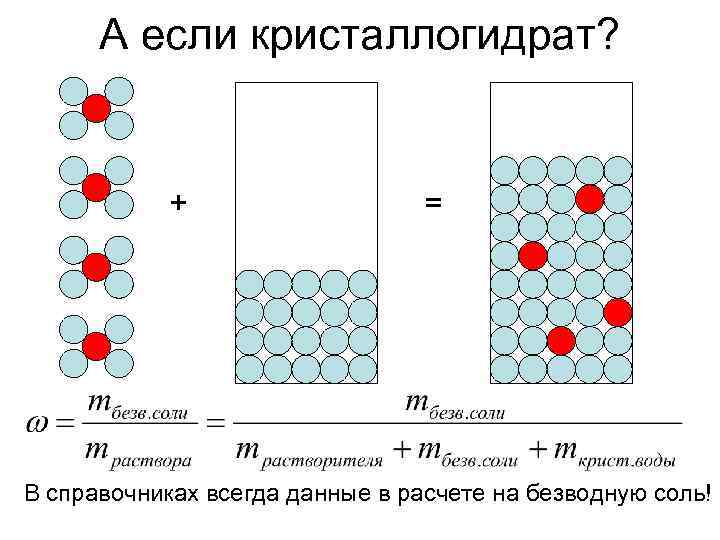
А если кристаллогидрат? + = В справочниках всегда данные в расчете на безводную соль!
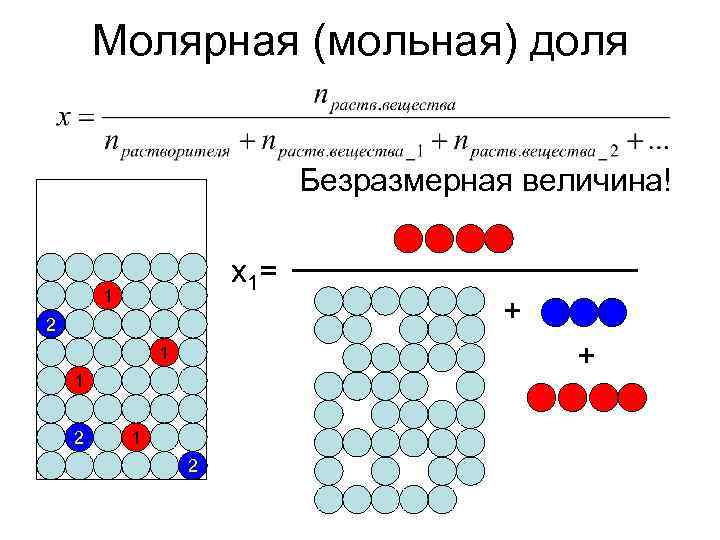
Молярная (мольная) доля Безразмерная величина! x 1= 1 2 + 1 + 1 2 1 2

Молярная концентрация Размерность: моль/дм 3 Пересчет массовой доли в молярную концентрацию: Отсюда:
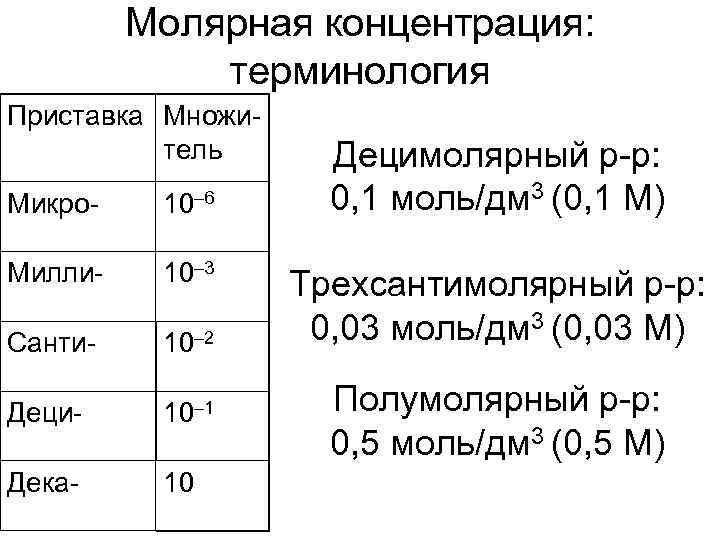
Молярная концентрация: терминология Приставка Множи- тель Децимолярный р-р: Микро- 10– 6 0, 1 моль/дм 3 (0, 1 М) Милли- 10– 3 Трехсантимолярный р-р: Санти- 10– 2 0, 03 моль/дм 3 (0, 03 М) Деци- 10– 1 Полумолярный р-р: 0, 5 моль/дм 3 (0, 5 М) Дека- 10

Массовая концентрация и моляльность Массовая концентрация Размерность: г/дм 3 Моляльность Размерность: моль/кг Относится к единице массы растворителя, а не раствора!
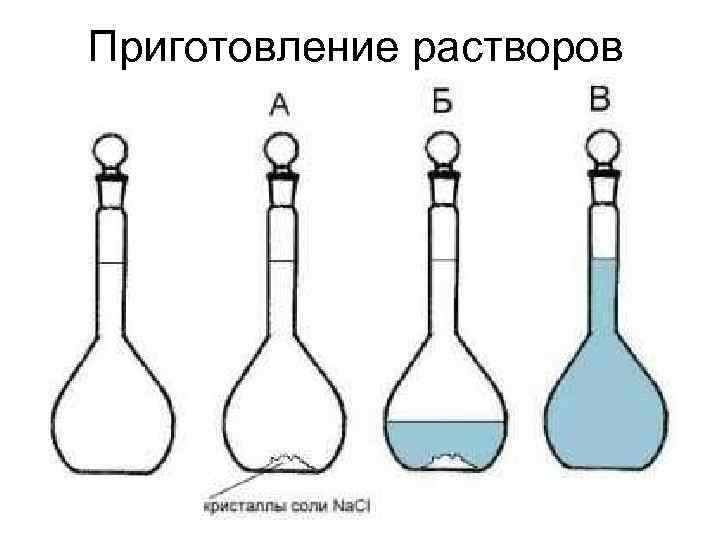
Приготовление растворов

Приготовление растворов: нюансы Эта мерная колба – грязная! (Капли воды остаются на горлышке) Правильно доведенный до метки раствор (нижний край мениска касается метки)

Приготовление растворов: нюансы Сначала растворяйте, а потом разбавляйте! Иначе может случиться, как в этом фильме… Лучший способ испортить ваш раствор Пробкой, а не пальцем!!!
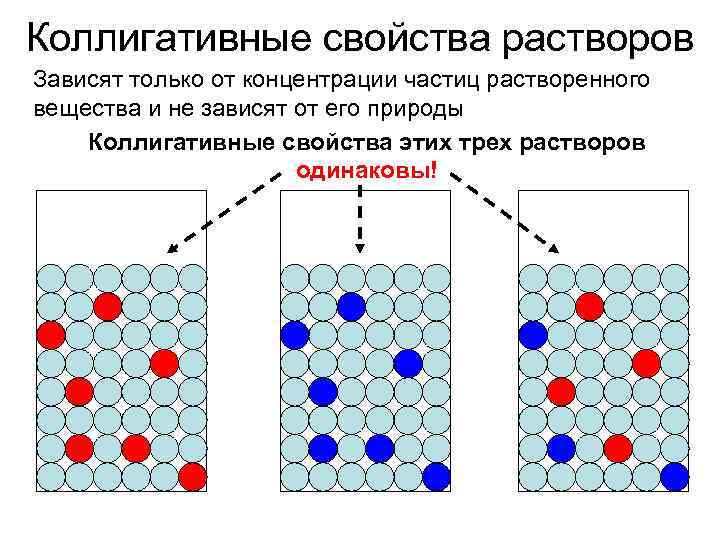
Коллигативные свойства растворов Зависят только от концентрации частиц растворенного вещества и не зависят от его природы Коллигативные свойства этих трех растворов одинаковы!
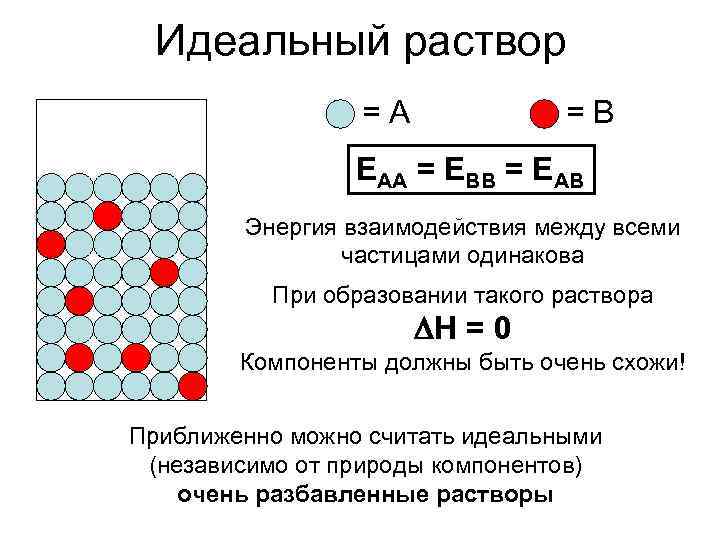
Идеальный раствор =A =B EAA = EBB = EAB Энергия взаимодействия между всеми частицами одинакова При образовании такого раствора H = 0 Компоненты должны быть очень схожи! Приближенно можно считать идеальными (независимо от природы компонентов) очень разбавленные растворы

Закон Рауля Над раствором парциальное давление насыщенного пара компонента B пропорционально его молярной доле x. B, причем коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом B: PB = PB 0 x. B В другой формулировке: относительное понижение давления насыщенного пара растворителя А над раствором вещества В Ф. М. Рауль равно молярной доле растворенного вещества: (PA 0 – PА)/PA 0 = x. B Применим только к идеальным растворам!

Два следствия закона Рауля Понижение температуры замерзания раствора по сравнению с чистым растворителем пропорционально моляльности раствора: Tзам = KCm (K – криоскопическая константа) Повышение температуры кипения раствора по сравнению с чистым растворителем пропорционально моляльности раствора: Tкип = ЕCm (Е – эбулиоскопическая константа) Е и K зависят от природы растворителя, обычно значение К больше

Определение молярной массы (эбулиоскопия и криоскопия) Если вещество В растворено в жидкости А, то: Tзам = KCm; где Cm = n. B/m. A = m. B/m. AMB, отсюда: MB = Km. B/m. A Tзам Аналогично для эбулиоскопии
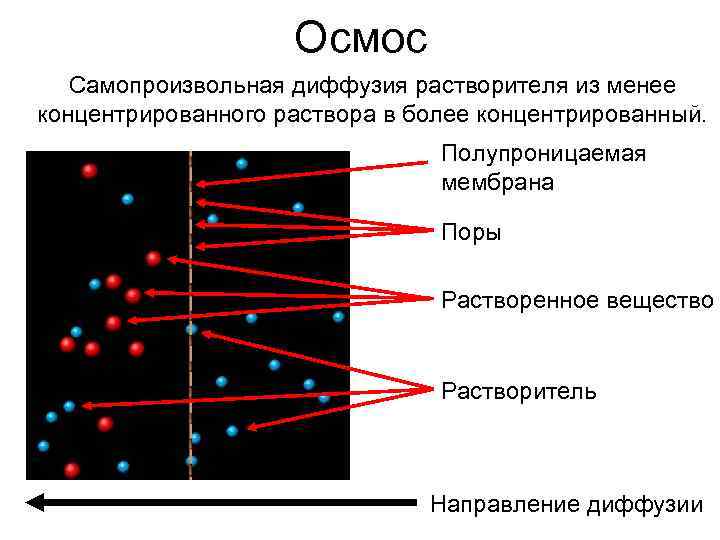
Осмос Самопроизвольная диффузия растворителя из менее концентрированного раствора в более концентрированный. Полупроницаемая мембрана Поры Растворенное вещество Растворитель Направление диффузии

Осмотическое давление Уравнение Вант-Гоффа = CRT где – осмотическое давление, C – концентрация, R – универсальная газовая постоянная, T – температура Я. Х. Вант-Гофф Растворы с одинаковым осмотическим давлением – изотонические
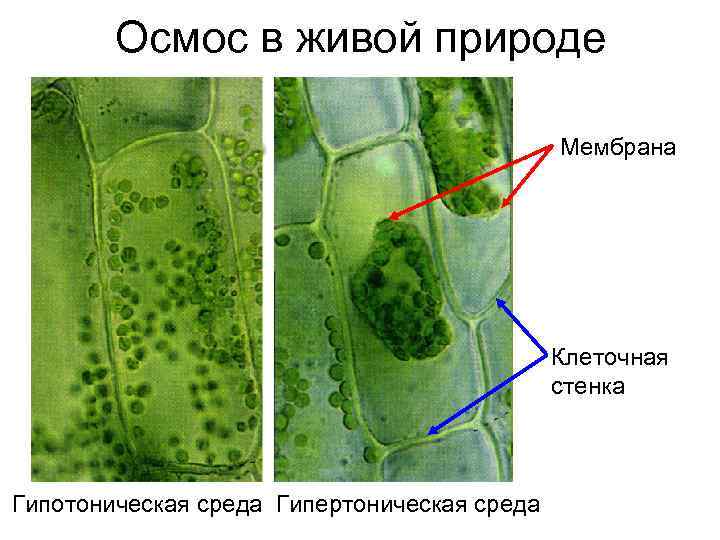
Осмос в живой природе Мембрана Клеточная стенка Гипотоническая среда Гипертоническая среда
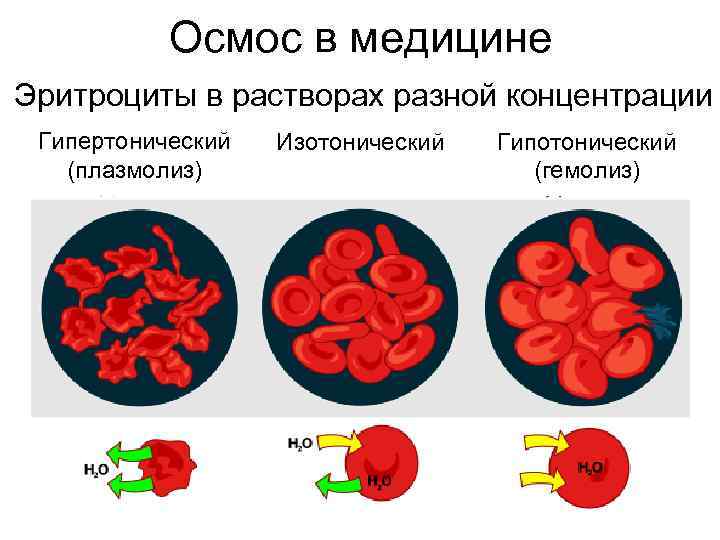
Осмос в медицине Эритроциты в растворах разной концентрации Гипертонический Изотонический Гипотонический (плазмолиз) (гемолиз)

Изотонический коэффициент Поправка к уравнению Вант-Гоффа для растворов электролитов = i. CRT (i – изотонический коэффициент) i = 1+ α (n – 1) Степень диссоциации Число частиц, образующихся при диссоциации из одной молекулы или формульной единицы Для сильных электролитов α = 1 i = n
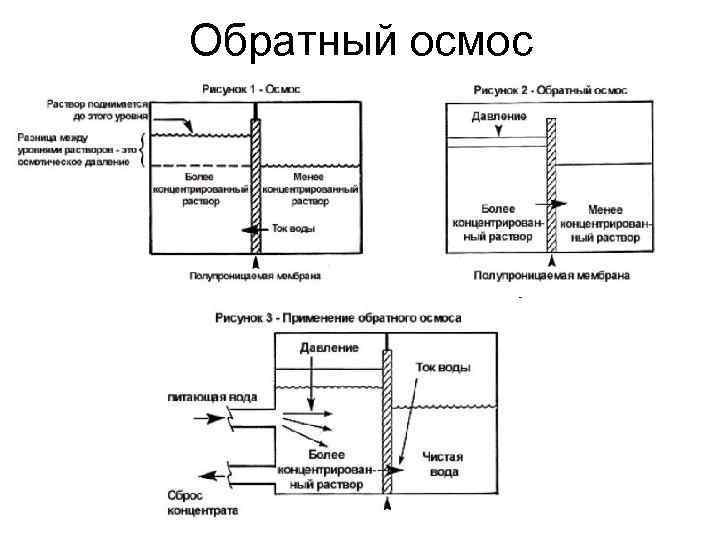
Обратный осмос

Осмос: вопрос на засыпку Диаметры частиц: H 2 O Na+ F– 0, 28 нм 0, 19 нм 0, 27 нм Почему вода проходит, а растворенный Na. F не проходит через полупроницаемую мембрану?
9_Способы выражения_Коллигативные свойства.ppt
- Количество слайдов: 22

