культивирование МО.ppt
- Количество слайдов: 54

Способы и системы культивирования микроорганизмов Работу выполнил Студент 4 курса гр. 01 -204 Жарников Евгений

Основные источники получения микроорганизмов, используемых для культивирования. 1. Классический путь – проводится выделение микроорганизмов из мест, где обитание того или иного вида наиболее вероятно. В элективных средах путем варьирования различных факторов создаются избирательные условия для преимущественного развития определенного микроорганизма. Таким образом получают накопительные культуры микроорганизмов. Следующий этап – выделение чистых культур. Для этого используют плотные питательные среды, на которые засевают образцы проб из накопительных культур. Отдельные клетки микроорганизмов на плотных питательных средах образуют изолированные колонии, при их последующем пересеве получаются чистые культуры продуцента. 2. Другой путь подбора микроорганизмов – из имеющихся коллекций микроорганизмов.

Получение накопительных и чистых культур Получение накопительных культур – основной этап Получение накопительных культур процесса получения чистых культур. К физическим методам относят: - регуляцию роста температурой - тепловую и ультразвуковую обработку - УФ-облучение К химическим методам относят: - использование токсичных веществ К биологическим методам относят: - использование специфических хозяев для выделяемого организма

Получение накопительных культур Выделение чистой культуры данного микроорганизма будет успешным, если он присутствует в смешанной популяции в достаточно высокой концентрации, т. е. количественно преобладает. Разработанные методы накопления имеют целью добиться увеличения относительного количества данного организма благодаря созданию лучших условий для его роста и выживания по сравнению с другими или путем пространственного отделения его от других членов популяции. Как правило, накопительные культуры получают в закрытых системах, т. е. микроорганизмы выращивают в обычных периодических (стационарных) условиях на чашках Петри, в колбах или пробирках, где в среде культивирования концентрация питательных веществ и продуктов метаболизма постоянно изменяется в процессе роста клеток.

Получение чистых культур • Из накопительных культур микроорганизмы обычно выделяют путем их пространственного отделения от других форм на твердой среде, где они растут в виде колоний. Для микроорганизмов, не растущих на твердых средах, можно использовать метод предельного разведения, последовательно перенося клетки в отдельные пробирки с жидкой средой. • Для выделения микроорганизмов в виде чистых культур известно сравнительно мало методов. Чаще всего используют способ изолирования отдельных клеток на твердой питательной среде или метод предельных разведений. • Однако получение отдельной колонии не всегда гарантирует чистоту культуры, поскольку колонии могут вырасти не только из отдельных клеток, но из их скоплений. • Для выделения предпочтительнее использовать неселективную среду, поскольку на ней лучше растут контаминирующие микроорганизмы и их легче обнаружить. Не следует очень быстро отбирать колонии, поскольку за данный отрезок времени могут не вырасти медленно растущие контаминирующие организмы.

Чистые культуры Из чистой культуры обычно вырастают одинаковые колонии, и при микроскопировании выявляются схожие клетки, в частности, по морфологии и результатам окраски по методу К. Грама. Однако возможны исключения, например, колонии, вырастающие из чистой культуры, могут быть гладкие (S) и шероховатые (Р). Кроме того, в чистых культурах различных микроорганизмов могут появиться морфологически различные клетки (полиморфизм), цисты и споры. Наконец, некоторые микроорганизмы проявляют грамвариабельность. Тем не менее, указанные критерии широко используются при определении чистоты культур.

Определение чистоты культуры • При определении чистоты культуры учитывают морфологию колоний, формирующихся на плотных питательных средах, оценивая следующие признаки: • • профиль – плоский, выпуклый, кратерообразный, конусовидный и т. д. ; • • форму – округлая, амебовидная, неправильная, ризоидная и т. д. ; • • размер (диаметр) – измеряют в миллиметрах; если размеры колонии не превышают 1 мм, то их называют точечными; • • поверхность – гладкая, шероховатая, бороздчатая, складчатая, морщинистая, с концентрическими кругами или радиально исчерченная; • • блеск и прозрачность – колония блестящая, матовая, тусклая, мучнистая, прозрачная; • • цвет – бесцветная (грязно-белые колонии относят к бесцветным) или пигментированная; особо отмечают выделение в субстрат пигмента; •

• край – ровный, волнистый, зубчатый, лопастной, ризоидный, бахромчатый и т. д. ; • структуру – однородная, мелко- или крупнозернистая, струйчатая и т. д. ; • консистенцию: колония может легко сниматься с агара, быть плотной, мягкой или врастающей в агар, маслянистой, слизистой (прилипает к петле), вязкой, пленчатой (снимается целиком), быть хрупкой (легко ломается прикосновении петлей). • Размеры и многие другие особенности колонии могут изменяться с возрастом и зависят от состава среды. Поэтому при их описании указывают возраст культуры, состав среды и температуру культивирования.
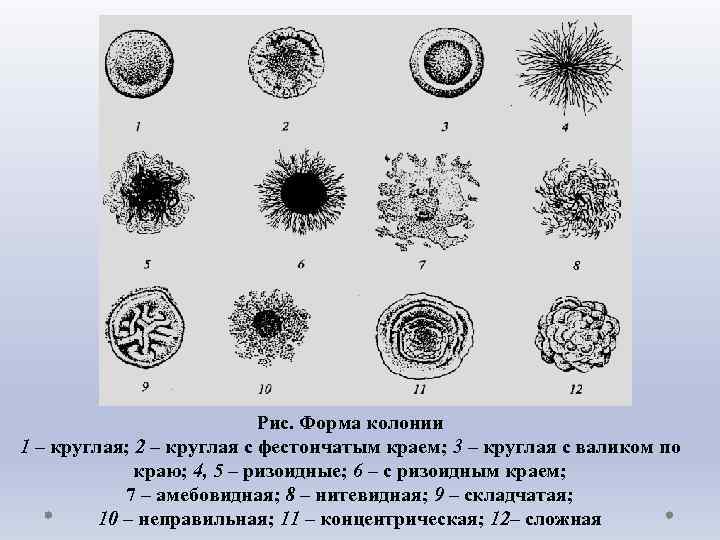
Рис. Форма колонии 1 – круглая; 2 – круглая с фестончатым краем; 3 – круглая с валиком по краю; 4, 5 – ризоидные; 6 – с ризоидным краем; 7 – амебовидная; 8 – нитевидная; 9 – складчатая; 10 – неправильная; 11 – концентрическая; 12– сложная

Рис. Профиль колонии 1 – изогнутый; 2 – кратерообразный; 3 – бугристый; 4 – врастающий в субстрат; 5 – плоский; 6 – выпуклый; 7 – каплевидный; 8 – конусовидный
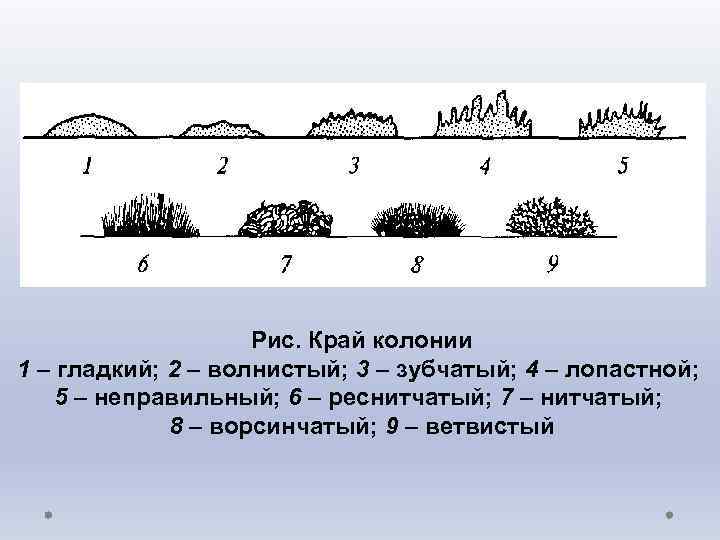
Рис. Край колонии 1 – гладкий; 2 – волнистый; 3 – зубчатый; 4 – лопастной; 5 – неправильный; 6 – реснитчатый; 7 – нитчатый; 8 – ворсинчатый; 9 – ветвистый
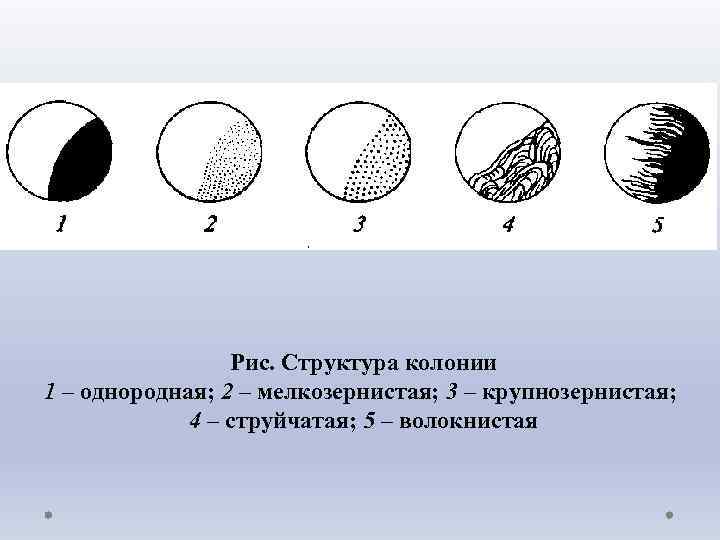
Рис. Структура колонии 1 – однородная; 2 – мелкозернистая; 3 – крупнозернистая; 4 – струйчатая; 5 – волокнистая
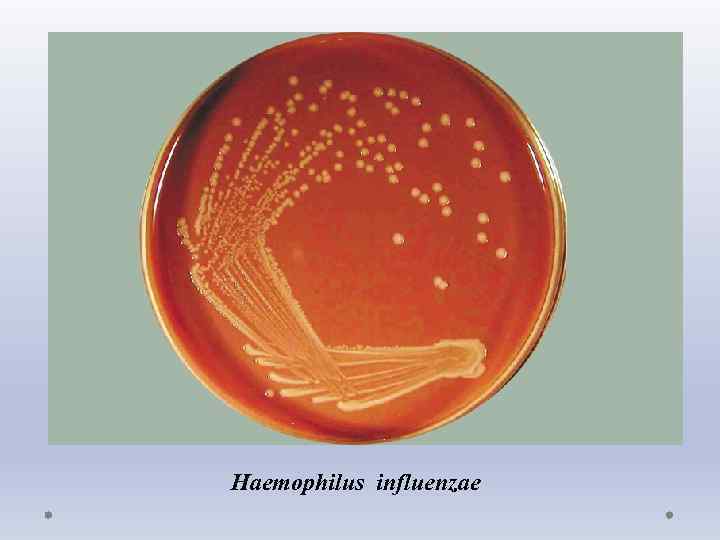
Haemophilus influenzae

• Рис. Культура дрожжевого гриба Candida albicans
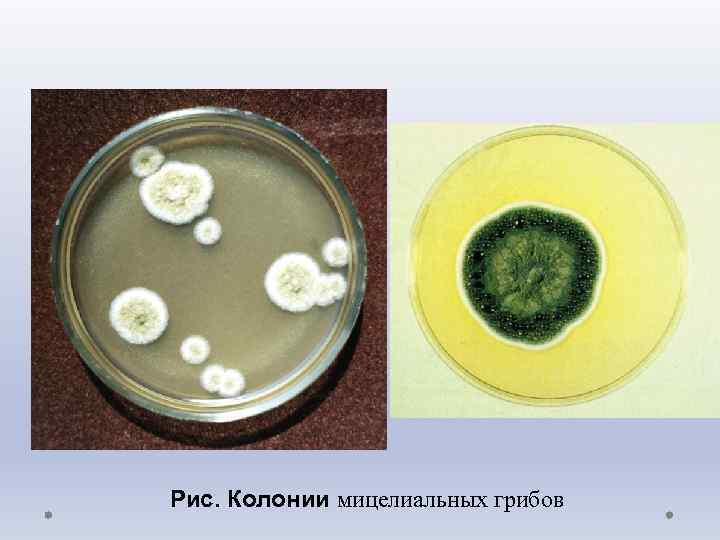
Рис. Колонии мицелиальных грибов

Классификация процессов культивирования • Выбор процесса культивирования зависит не только от потребностей организма, но и от того, для чего будет использована культура, то есть, от конечной цели эксперимента. • 1) по состоянию питательной среды или по основной фазе (поверхностные и глубинные); • 2) по наличию или отсутствию перемешивания (динамические или статические); • 3) по содержанию кислорода (на аэробные или анаэробные); • 4) по способу действия (закрытые, чаще периодические, и открытые, чаще непрерывные); • 5) по количеству ферментеров (одно-, дву- и многостадийные); • 6) по способу управления (хемостатные, турбидостатные, оксистатные, р. Н-статные и другие); • 7) по степени защищенности от посторонней микрофлоры; • 8) по числу видов микроорганизмов.
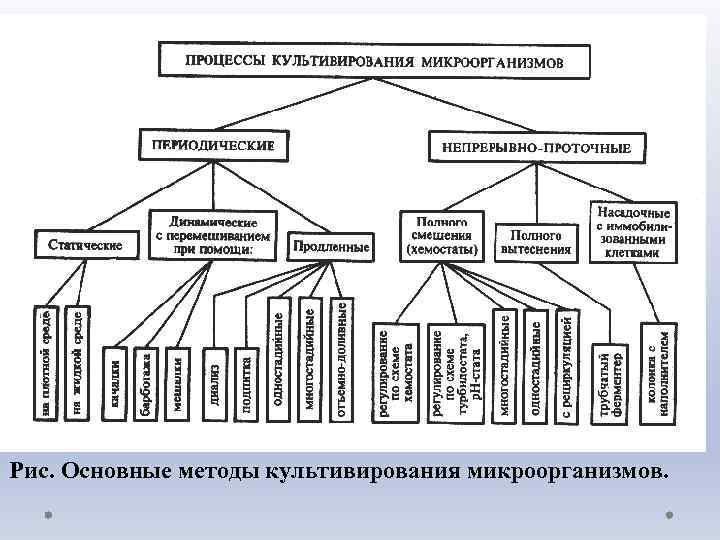
Рис. Основные методы культивирования микроорганизмов.

Метод посева штрихом Грамположительная Bacillus anthracis (фиолетовые палочки) в образце спинномозговой жидкости. (Другие клетки — На питательных средах Окраска по Граму Staphylococcus aureus (грамположительные кокки) и. Escherichia coli (грамотрицательные

Методы культивирования на твердых средах • 1. В случае культур, выращенных на твердой среде, нет необходимости использовать центрифугу или другие средства для сбора клеток, поскольку в этих культурах клетки находятся уже в сконцентрированном состоянии. • 2. Твердые культуры относительно свободны от макромолекулярных компонентов и полностью свободны от частиц питательной среды, так как последние обычно находятся внутри агарового геля. • 3. На твердых средах можно получать результаты, которые невозможно достичь другим путем. 1. Твердая культура имеет ограничения при выращивании больших количеств биомассы. 2. Твердые культуры не обеспечивают однородность популяции клеток, т. е. культура гетерогенна в физиологическом отношении. 3. Твердые культуры характеризуются небольшим числом клеток в пересчете на данное количество среды.

Жидкофазное поверхностное культивирование • Поверхностные жидкофазные процессы в биотехнологических производствах используют для культивирования мицелиальных грибов при получении органических кислот, ферментных препаратов, кормовой биомассы. Для этих целей применяется кюветный способ культивирования. Среда загружается в стерильные кюветы, размещаемые на открытых стеллажах в растильных камерах с регулируемым температурно-влажностным режимом. Вентиляцию помещений осуществляют очищенным и стерильным воздухом, который одновременно выполняет функцию теплового агента. • Микроорганизмы растут в виде пленки биомассы на поверхности жидкой питательной среды. • После завершения процесса культуральная жидкость сливается из кювет через вмонтированные в днища штуцеры и поступает на обработку.

Глубинное периодическое культивирование Ферментер

Процессы суспензионного или глубинного культивирования Простейшая классификация процессов суспензионного или глубинного культивирования: • 1)периодическое культивирование; • 2)продленное оптимизированное периодическое культивирование с подпиткой или без нее; • 3)многоциклическое культивирование; • 4)полунепрерывное культивирование; • 5)непрерывно-синхронное культивирование; • 6) непрерывное культивирование.

Периодическое культивирование Периодический метод культивирования предусматривает внесение посевного материала в питательную среду (инокуляция клетками среды) в начале процесса и получение культуры по достижении заданной фазы развития популяции. Концентрация микроорганизмов в периодической культуре нарастает и останавливается либо из-за лимитирования субстратом, либо из-за ингибирования токсичными продуктами жизнедеятельности. Практически все системы периодического культивирования являются закрытыми, поскольку микроорганизмы в них размножаются и проходят все фазы развития без притока питательной среды и оттока культуральной жидкости.

При изучении динамики роста культур микроорганизмов необходимо строго соблюдать некоторые условия: 1) жизнеспособность засева; 2) наличие в среде культивирования всех необходимых питательных веществ; 3)отсутствие в среде ингибиторов, подавляющих рост клеток; 4) поддержание в среде оптимальными всех физико-химических условий.

Многоциклическое культивирование • называют такие процессы, в которых цикл выращивания культуры повторяется многократно без многократной стерилизации емкости. • Зависимость концентрации микроорганизмов и удельной скорости роста от времени в каждом цикле многоциклического процесса имеет характер, аналогичный таковому в периодическом процессе. • Применяют как для получения биомассы, так и продуктов микробного синтеза – токсинов, антибиотиков, внеклеточных ферментов, аминокислот.

Продленное периодическое оптимизированное культивирование • Продленный периодический процесс культивирования, как и периодический, предусматривает одноразовую загрузку и разгрузку ферментера. Однако цикл развития микроорганизмов в продленном периодическом процессе удлиняется либо за счет подпитки (периодической или непре-рывной), либо за счет длительного удержания клеток в системе (диализ).

Культивирование с подпиткой • Если зависимость удельной скорости роста от количества субстрата имеет насыщение, то исходную концентрацию субстрата можно задать сразу побольше в пределах плато, где влияние субстрата на скорость роста биомассы невелико или вообще отсутствует. В этом случае пока концентрация субстрата не снизится до критического уровня подпитку можно не производить. • Если зависимость удельной скорости роста биомассы от концентрации субстрата имеет экстремум, то подпитка требуется уже с самого начала процесса для поддержания его на оптимальном уровне. • Подпитка может осуществляться импульсно или по каплям на протяжении всего процесса.

Диализные системы • Диализ – исторический первый метод очистки – был предложен Т. Грэхемом в 1861 г. для удаления из системы низкомолекулярных веществ. • Суть этого метода заключается в том, что культура развивается в пространстве, ограниченном полупроницаемой мембраной, а продукты диффундируют во внешний раствор. • Для культивирования с диализом используются мембраны, отличающиеся размером пор. Диализные мембраны задерживают клетки и макромолекулы, но проницаемы для таких мелких молекул, как основные питательные компоненты, требующиеся микроорганизмам для их роста. • Диализные мембраны изготавливают из пергамента, целлофана, ацетатцеллюлозы, полиамида, поликарбо-ната, кремний и др.

• Диализные культуры применяются в основном в трех случаях: • 1) для концентрирования недиффундирующего продукта, • 2) для уменьшения концентрации диффундирующего продукта, ингибирующего рост клеток, и повышения выхода биомассы, • 3) для накопления и отделения от клеток диффундирующего продукта. • Преимущества процесса диализа: 1) работа в мягких условиях температуры и р. Н; 2) отсутствие органических растворителей; 3) возможность высокой степени очистки клеток от примесей низкомолекулярных соединений, солей и металлов. • Недостатки: 1) низкая скорость диализа, определяемая молекулярной диффузией; 2) возможность обрастания диализных мембран и забивания их пор.

Электродиализ Некоторых недостатков диализа удается избежать за счет применения электродиализа (Доре, 1910). В этом случае параллельно мембранам и диализуемой жидкости накладывается электрическое поле, в результате чего анионы и катионы из раствора диффундируют через диализные мембраны к аноду и катоду, а клетки остаются в растворе. В простейшем случае электродиализатор состоит из 3 камер, отделенных друг от друга полупроницаемыми мембранами – центральной для обрабатываемого раствора, а также для пермеата в зоне анода и пермеата в зоне катода по обеим сторонам от центральной камеры. Мембраны при катоде и при аноде могут быть выполнены из разного материала, селективного для катионов и анионов. Недостатком электродиализа является выделение при высоком напряжении большого количества тепла, что может привести к необратимым изменениям в системам с биологическими компонентами.

Гомогенные системы идеального смешивания • В этой системе микроорганизмы растут в культуральной среде, постоянной по своему составу и находятся с состоянии установившегося динамического равновесия. • По количеству ферментов могут быть: одностадийные; двухстадийные; многостадийные; • Основной аппарат для выращивания непрерывной гомогенной культуры – ферментер.

Культивирование полного вытеснения Этот способ культивирования используется для анаэробных условий. Открытая система полного вытеснения отличается от системы идеального смешения тем, что культура в ней не перемешивается и представляет собой поток жидкости через трубку. Наиболее распространенным аппаратом является трубчатый реактор S 0 xs x 0 Трубчатый ферментер полного вытеснения: S 0 – концентрация субстрата в поступающей среде; Х 0 – начальная концентрация биомассы;

Синхронно делящиеся культуры • Сущность метода синхронизации заключается в том, что путем различных воздействий микробная популяция искусственно приводится в однородное физиологическое состояние. Наиболее легко определяемым показателем такого состояния популяции является одновременное (синхронное) деление почти всех клеток культуры. • Среди бактерий синхронное размножение изучалось главным образом на популяциях Escherichia coli, Salmonella typhimurium, Corynebacterium diphtheriae и других.
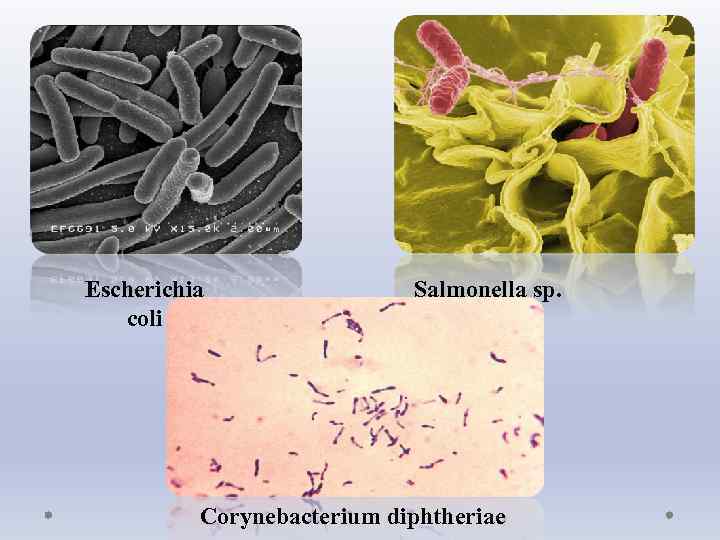
Escherichia coli Salmonella sp. Corynebacterium diphtheriae

В зависимости от характера воздействия механический отбор (селективные методы) действие физических факторов химико-биологические воздействия.

Непрерывно- синхронное культивирование • Этот способ известен как непрерывно синхронный, или фазовый, метод культивирования, гарантирующий поддержание синхронного деления клеток неограниченно долгое время. Метод основан на периодическом сливе из ферментера половины объема выросшей культуры через промежутки времени, равные одной генерации, и одновременном добавлении такого же количества свежей питательной среды, что обеспечивает импульсную подачу источников питания.

КУЛЬТИВИРОВАНИЕ АНАЭРОБНЫХ МИКРООРГАНИЗМОВ • Выращивание анаэробных микроорганизмов более сложно, чем культивирование аэробов, так контакт их клеток с кислородом воздуха должен быть сведен к минимуму или даже полностью исключен. Для этого используют разные приемы, нередко комбинируя их друг с другом.

Выращивание в высоком слое среды • Это наиболее простой способ ограничения доступа воздуха к клеткам микроорганизмов. Жидкую среду наливают в сосуды для культивирования высоким слоем. Так как нельзя стерилизовать среды, если они занимают более половины высоты сосуда, часть среды стерилизуют отдельно и стерильно доливают ее сосуд для культивирования сразу же после посева. Непосредственно перед посевом среду кипятят или прогревают на кипящей водяной бане 30 -40 мин, затем быстро охлаждают, чтобы в ней не успел раствориться кислород воздуха, и вносят на дно посевной материал.

Культивирование в вязких средах • Диффузия кислорода в жидкость уменьшается с увеличением ее вязкости. Поэтому в вязких средах, таких как картофельная или среды с кукурузной либо другой мукой, хорошо развиваются некоторые облигатные анаэробы, например, возбудители маслянокислого или ацетонобутилового брожения. Вязкость жидких сред легко увеличить, если добавить к ним 0, 2 -0, 3 % агара.

Выращивание в толще плотной среды • Этим приемом пользуются для получения изолированных колоний при выделении чистых культур или определении численности анаэробных микроорганизмов. • Посевной материал вносят в расплавленную и остуженную до 48 -50 0 С агаризованную, желательно осветленную среду, тщательно перемешивают и оставляют в пробирках или переносят стерильной пипеткой в заранее простерилизованные обычные пробирки, трубки Бури или чашки Петри.

Выращивание в анаэростатах • Анаэробные микроорганизмы можно выращивать в анаэростатах – вакуумных металлических камерах, снабженных манометром. Анаэростатом может служить обычный вакуумный стеклянный эксикатор. Из анаэростата откачивают воздух, а затем, как правило, заполняют его газовой смесью, состоящей из азота (9080%) и углекислоты (10 -20%), до достижения избыточного давления, которое исключает возможность диффузии кислорода воздуха.

• Анаэростат АЭ-01 • предназначен для культивирования в чашках Петри микроорганизмов группы облигатных анаэробов (бактероидов) и микроаэрофилов

• Для культивирования строгих анаэробов предложены специальные камеры, заполненные газовыми смесями (чаще всего 90% N 2, 5% СО 2 и 5% Н 2), которые содержат внутри все необходимое для выполнения микробиологических работ, включая термостат. • Это оборудование сложно и дорого, но оно имеет неоспоримое преимущество – контакт клеток с кислородом воздуха остается минимальным на всех этапах работы.

• Одновременная загрузка 36 чашек Петри

• В качестве поглотителя кислорода в лабораторной практике используют щелочные растворы пирогаллола, дитионита (гидросульфита) натрия, металлическое железо и некоторые другие реактивы. Полноту поглощения кислорода контролируют раствором, содержащим окислительно-восстановительный индикатор. В качестве восстановителя чаще всего используют сульфид и тиогликолат натрия.

ХРАНЕНИЕ МИКРООРГАНИЗМОВ • К числу наиболее распространенных способов хранения микроорганизмов относятся периодические посевы на свежие питательные среды, сохранение культур на питательных средах под слоем вазелинового масла, хранение клеток в лиофилизированном состоянии. • Реже микроорганизмы сохраняют при низких или сверхнизких температурах, в дистиллированной воде или 1%-ном растворе хлористого натрия, на адсорбентах в высушенном состоянии. • Выбор метода хранения во многом зависит от целей, для которых используются микроорганизмы, а также от имеющегося в распоряжении исследователя оборудования.

Периодические посевы на питательные среды • Этот способ был одним из первых приемов длительного сохранения микроорганизмов в лабораторных условиях и до настоящего времени широко используется в практике микробиологических работ. • Аэробные микроорганизмы пересевают чаще всего на поверхности скошенной агаризованной среды, микроаэрофилы – в полужидкую среду, содержащую 0, 20, 3% агара, анаэробы – в толщу плотной среды или в жидкую среду. • Культуры пересевают на свежие среды в 2 пробирки (колбы). В дальнейшем из одной пробирки микроорганизмы используют для работы, культуру во второй пробирке оставляют для сохранения и последующего пересева.

Хранение под минеральным маслом • Хранение под минеральным маслом широко используется для бактерий и микроскопических грибов. Это метод обеспечивает довольно длительное сохранение жизнеспособности и стабильности микроорганизмов. Масло предотвращает высыхание среды, замедляет процессы метаболизма и позволяет увеличить время между пересевами. • Микроорганизмы выращивают на оптимизированной агаризованной питательной среде: • аэробные микроорганизмы – на поверхности коротко скошенной (под углом 45 °) среды, • анаэробы – в толще среды (посев уколом или в расплавленную среду с перемешиванием). •

Хранение при низких и сверхнизких температурах • Криоконсервация. Хранение микроорганизмов в замороженном состоянии при низких и сверхнизких температурах по сравнению с другими методами характеризуется наибольшей универсальностью. Однако этот метод требует специального оборудования и большой осторожности в работе с жидким азотом, поэтому используется лишь для сохранения микроорганизмов, не выдерживающих лиофилизацию.

Хранение в глицероле • Одним из самых удобных методов хранения микроорганизмов является их содержание при низких и сверхнизких температурах в растворах глицерола, который служит криопротектором. Данный способ широко распространен, однако не все микроорганизмы выдерживают такую обработку. Поэтому считается, что для клеток, подвергаемых замораживанию в глицероле, необходимы предварительные эксперименты по определению степени выживаемости. • Наибольшее распространение это способ консервации микроорганизмов получил при хранении суспензий различных спор.

Хранение в дистиллированной воде или 1%-ном растворе хлорида натрия • Хранение микроорганизмов в дистиллированной воде или 1%-ном растворе хлорида натрия не требует специального оборудования и доступно любому экспериментатору. Микроорганизмы предварительно выращивают в оптимальных условиях, после чего клетки суспендируют в дистиллированной воде или 1%-ном растворе хлорида натрия. Успешному сохранению клеток способствует высокая плотность суспензии – не менее 108 -109 клеток в 1 мл. • Суспензию разливают в стерильные пробирки или флаконы и сохраняют в холодильнике или при комнатной температуре. Оставлять на хранение рекомендуется клетки начала стационарной фазы роста культуры или сформировавшиеся покоящиеся формы – споры, цисты.

Хранение в высушенном состоянии на адсорбентах • Этот метод применяют главным образом для актиномицетов, микроскопических грибов и анаэробных бактерий, образующих споры. В качестве адсорбентов используют почву, кварцевый песок, силикагель, вату, фильтровальную бумагу. • Разработанной стандартной техники это способ не имеет. В самом общем виде все сводится к тому, что стерильный адсорбент, помещенный в ампулы, смешивают с густой суспензией клеток и высушивают под вакуумом или при комнатной температуре. Затем ампулы запаивают и хранят при комнатной температуре или в холодильнике. Имеются данные, что у актиномицетов после хранения в почве или в кварцевом песке восстанавливаются некоторые таксономические признаки (окраска воздушного и субстратного мицелия), которые были утрачены в процессе длительного культивирования в лаборатории.

Оценка жизнеспособности микроорганизмов после длительного хранения • Жизнеспособность микроорганизмов после различных сроков хранения определяют путем высева их на богатые питательные среды с последующим подсчетом выросших колоний. Процент выживаемости микроорганизмов определяют по отношению числа сохранившихся клеток к первоначальному числу жизнеспособных клеток (до начала хранения), принятому за 100%.

Спасибо за внимание!
культивирование МО.ppt