урок-обобщ Углеводороды.ppt
- Количество слайдов: 19


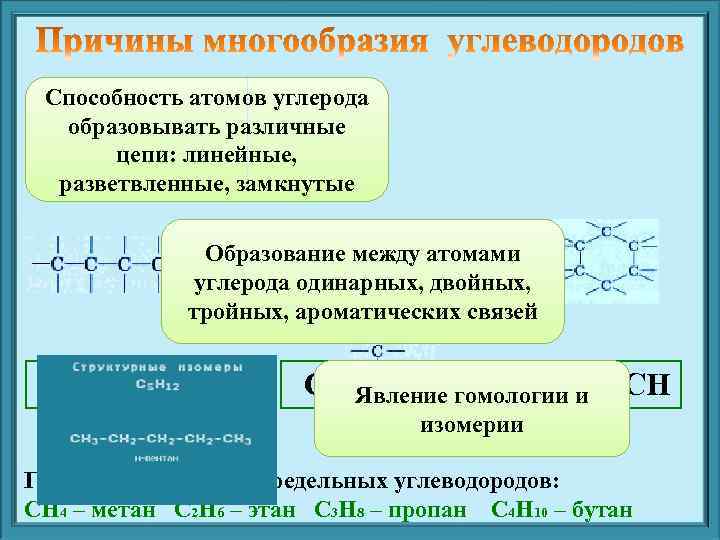
Способность атомов углерода образовывать различные цепи: линейные, разветвленные, замкнутые Образование между атомами углерода одинарных, двойных, тройных, ароматических связей СН 3 – СН 3 СН 2 ═ СН 2 гомологии и ≡ СН СН Явление изомерии Гомологический ряд предельных углеводородов: СН 4 – метан С 2 Н 6 – этан С 3 Н 8 – пропан С 4 Н 10 – бутан

Признаки сравнения Класс углеводородов Алканы Алкены Алкадиены Cn. H 2 n + 2 Cn. H 2 n Незам. ц. С-С Незам. ц 1 С=С Структур. , полож. кратной св. Номенкла- -ан тура -ен -ин Формула СН 2 = СН 2 этен Общая формула Строение Типы изомерии СН 3 – СН 3 этан Алкины Арены Cn. H 2 n - 2 Cn. H 2 n - 6 Незам. ц. 2 С=С Незам. ц. 1 С≡С Зам. ц. из 6 С; особая св. -диен СН 2=С=СН 2 пропадиен СН≡СН этин

Даны формулы углеводородов: а) CH 3 -CH 2 - CH 3 бутан б) CH 3 -CH(CH 3)-CH 3 2, 3 диметилбутан в) CH 3 -CH 2 -CH 3 пропан г) CH 2=C(CH 3)-C(CH 3)2 -CH 3 2, 3, 3 триметилбутен-1 д) CH 2=C(CH 3)- CH 3 2 метилпропен е) CH 3 -C≡C- CH 3 бутин-2 ж) CH 3 -CH(CH 3)-CH 3 2 метилпропан з) CH≡C- CH 2 - CH 3 бутин-1 и) бензол к) CH 2=CH-CH= CH 2 бутандиен-1, 3

Даны формулы углеводородов: а) CH 3 -CH 2 - CH 3 б) CH 3 -CH(CH 3)-CH 3 в) CH 3 -CH 2 -CH 3 г) CH 2=C(CH 3)-C(CH 3)2 -CH 3 д) CH 2=C(CH 3)-CH 3 е) CH 3 -C≡C- CH 3 ж) CH 3 -CH(CH 3)-CH 3 з) CH≡C- CH 2 - CH 3 и) к) CH 2=CH-CH= CH 2 1. Непредельные соединения г) д) е) з) к) 2. а) алкан а)б)в)ж) б) алкен г)д) в) алкадиен г) алкин к) е)з) 3. Вещество (вещества), состав которого соответствует формуле: а) Cn H 2 n + 2 а)б)в)ж) б) Cn H 2 n - 6 и) в) Cn H 2 n г)д) г) Cn H 2 n - 2 е) з) к)

Даны формулы углеводородов: а) CH 3 -CH 2 -CH 3 б) CH 3 -CH(CH 3)-CH 3 в) CH 3 -CH 2 -CH 3 г) CH 2=C(CH 3)-C(CH 3)2 -CH 3 д) CH 2=C(CH 3)-CH 3 е) CH 3 -C≡C- CH 3 ж) CH 3 -CH(CH 3)-CH 3 з) CH≡C- CH 2 - CH 3 и) к) CH 2=CH-CH= CH 2 4. Гомолог вещества с формулой в) а) 5. Изомер вещества с формулой ж) а) 6. Изомеры вещества с формулой з) е) к)
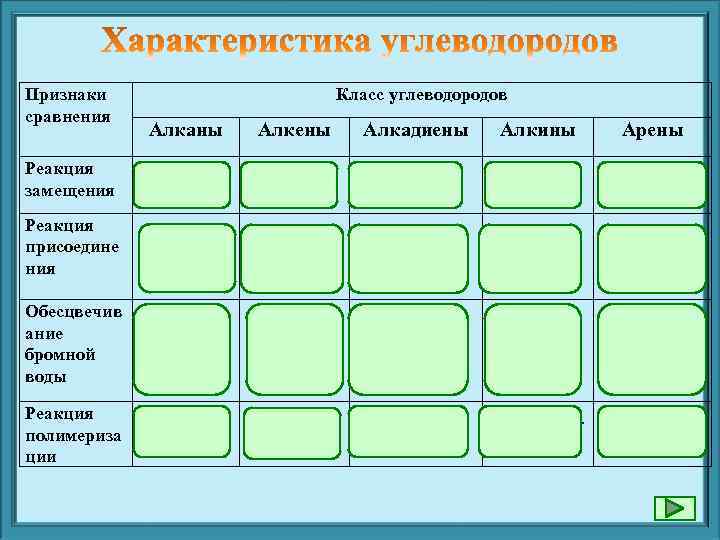
Признаки сравнения Класс углеводородов Алканы Алкены Алкадиены Алкины Арены Реакция замещения + ─ ─ ─ + Реакция присоедине ния ─ + + Обесцвечив ание бромной воды ─ + + + ─ тримериза ция ─ Реакция полимериза ции ─ + +

Тип реакций - замещение свет СН 4 + Br 2 → СН 3 Br + HBr бромметан
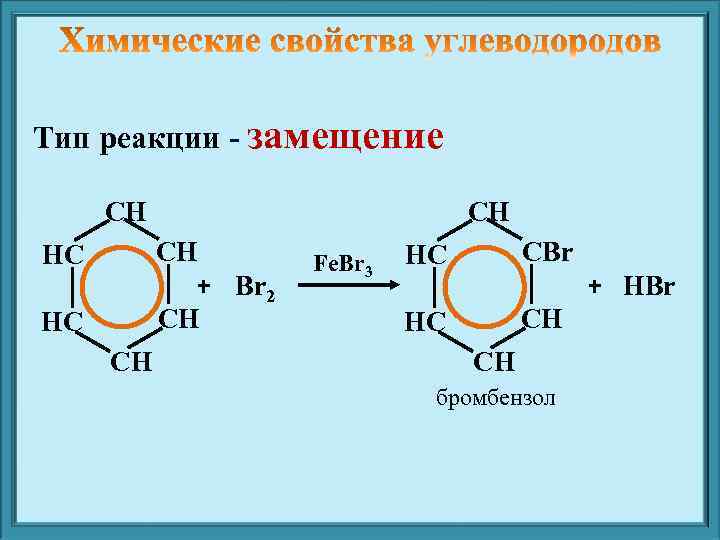
Тип реакции - замещение СН СН СН + Br 2 СН НС НС СН Fe. Br 3 НС СBr НС СН + HBr СН бромбензол
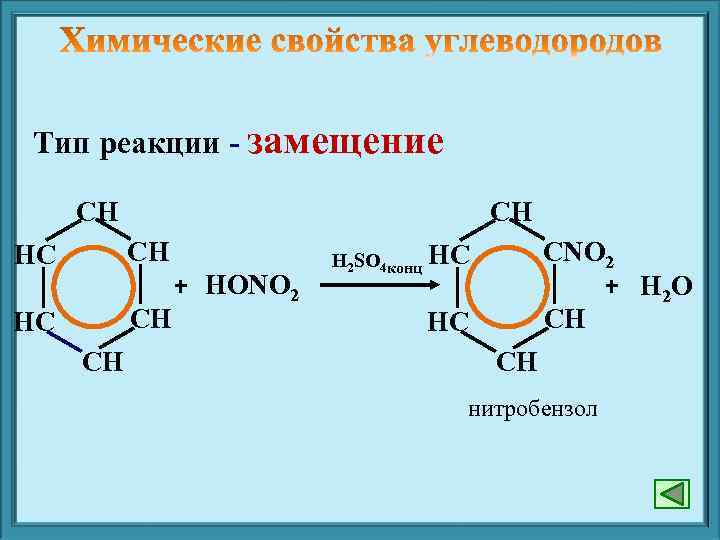
Тип реакции - замещение СН СН НС СН СН + HONO 2 СNO 2 + H 2 O СН H 2 SO 4 конц НС НС СН нитробензол
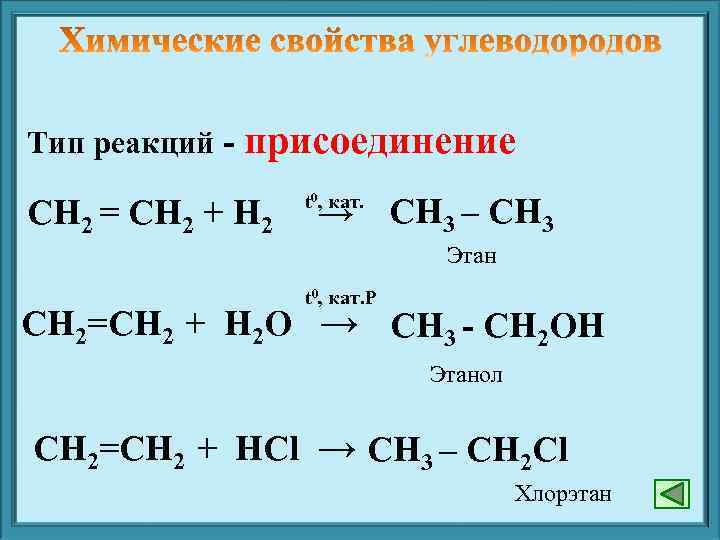
Тип реакций - присоединение СН 2 = СН 2 + Н 2 t 0, кат. → СН 3 – СН 3 Этан t 0, кат. Р СН 2=СН 2 + H 2 O → СН 3 - СН 2 OH Этанол СН 2=СН 2 + HCl → СН 3 – СH 2 Cl Хлорэтан

Тип реакций - присоединение СН ≡ СН + 2 Н 2 t 0, кат. → СН 3 – СН 3 Этан СН ≡ СН + H 2 O Hg 2+ → СН 3 - СOH Этаналь СН ≡ СН + HCl → СН 2 = СHCl Винилхлорид

Обесцвечивание бромной воды качественная реакция на кратную связь СН 2═СН-СН=СН 2 + Br 2→ СН 2 Br–CH=CH–СН 2 Br 1, 4 дибромбутeн-2 СН 2 = СН 2 + Br-Br → СН 2 Br - СН 2 Br СН ≡ СН + 2 Br-Br → СНBr 1, 2 -СНBr 2 2 - дибромэтан СН 2 Br–CH=CH- СН 2 Br + Br 2 → СН 2–CH–CH–СН 2 1, 1, 2, 2 - тетрабромэтан │ │ Br Br 1, 2, 3, 4 тетрабромбутан
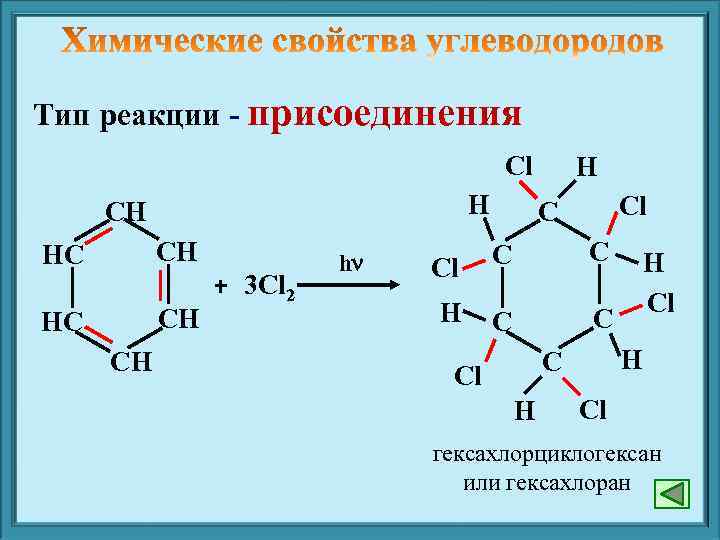
Тип реакции - присоединения Cl H СН НС СН СН + 3 Cl 2 h H Cl С С H С Cl H H Cl Cl гексахлорциклогексан или гексахлоран
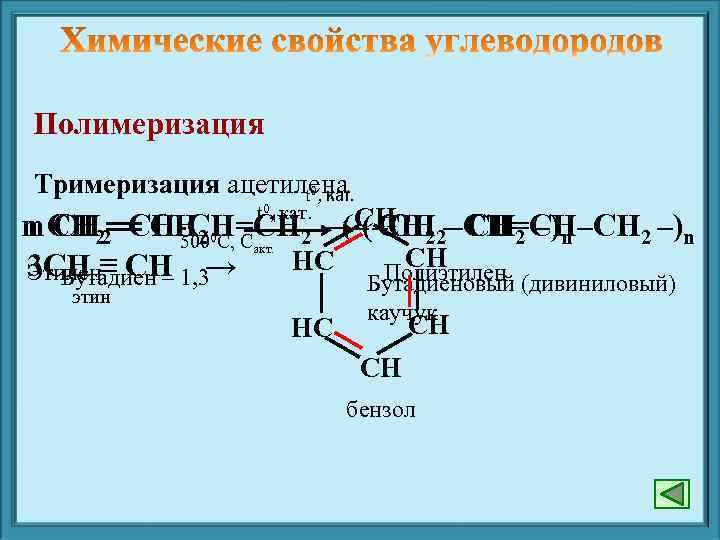
Полимеризация Тримеризация ацетилена t 0, кат. n СН ═ СН 2 0 C, C (– СН –СН=СН–СН 2 –)n (–СН n СН 22═СН-СН=СН 2 → СН 22– СН 2 –)n 500 акт. СН НС 3 СН ≡ СН → Этилен Полиэтилен Бутадиен – 1, 3 этин НС Бутадиеновый (дивиниловый) каучук СН СН бензол

Даны формулы углеводородов: а) CH 3 -CH 2 -CH 3 б) CH 3 -CH(CH 3)-CH 3 в) CH 3 -CH 2 -CH 3 г) CH 2=C(CH 3)-C(CH 3)2 -CH 3 д) CH 2=C(CH 3)-CH 3 е) CH 3 -C≡C- CH 3 ж) CH 3 -CH(CH 3)-CH 3 з) CH≡C- CH 2 - CH 3 и) к) CH 2=CH-CH=CH 2 7. Вещества, вступающие в реакцию замещения с хлором, а) б) в) и) ж) 8. Вещества, обесцвечивающие бромную воду, г) д) е) з) к) 9. Вещества, вступающие в реакции присоединения, г) д) е) з) к) и)
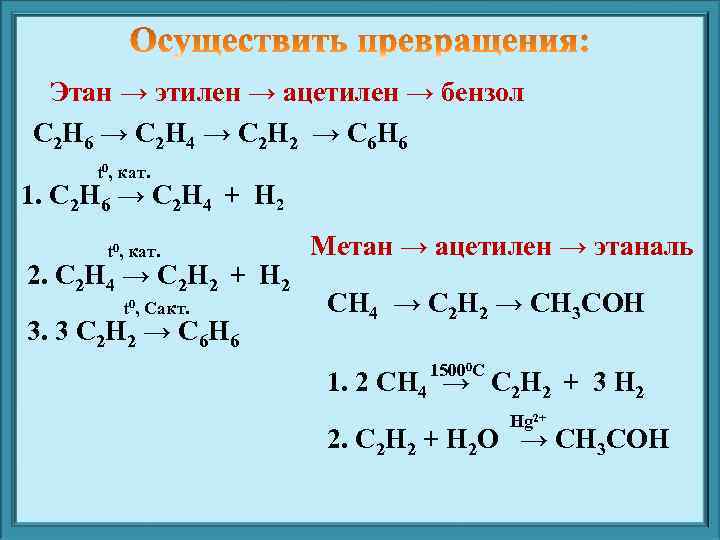
Этан → этилен → ацетилен → бензол С 2 Н 6 → С 2 Н 4 → С 2 Н 2 → С 6 Н 6 t 0, кат. 1. С 2 Н 6 → С 2 Н 4 + Н 2 t 0, кат. 2. С 2 Н 4 → С 2 Н 2 + Н 2 t 0, Cакт. 3. 3 С 2 Н 2 → С 6 Н 6 Метан → ацетилен → этаналь СН 4 → С 2 Н 2 → СН 3 СОН 15000 С 1. 2 СН 4 → С 2 Н 2 + 3 Н 2 Hg 2+ 2. С 2 Н 2 + Н 2 O → СН 3 COH

Этиловый спирт → этилен → полиэтилен ↓ 1, 2 - дибромэтан С 2 Н 5 ОН → СН 2 = СН 2 → ↓ (-СН 2 -)n СН 2 Br - СН 2 Br t 0 , H 2 SO 4(к) 1. С 2 Н 5 ОН → С 2 Н 4 + Н 2 О 2. n СН 2 = СН 2 → (-СН 2 -)n 3. СН 2 = СН 2 + Br 2 → СН 2 Br - СН 2 Br
урок-обобщ Углеводороды.ppt