Метали 14.ppt
- Количество слайдов: 23

Способи добування металів Металургія — це галузь промисловості, яка займається видобуванням металів із руд. Електроліз — окисно-відновний процес, що відбувається на електродах під час проходження електричного струму через розплав або розчин електроліту.

Електроліз розчинів Якщо налити в U-подібну трубку розчин Cu. Cl 2, занурити у кожне коліно вугляні електроди і з’єднати їх металевими провідниками з джерелом постійного струму, то катод вкриватиметься шар за шаром червоним нальотом металічної міді, а на аноді виділятиметься вільний хлор Cu. Cl 2 = Cu 2+ + 2 Cl. Йони хаотично рухаються у розчині. Після вмикання струму безладний рух йонів стає спрямованим. Йони Купруму рухаються до катоду, а йони Хлору – до аноду і там розряджаються. На катоді відбувається процес відновлення, а на аноді – процес окиснення.
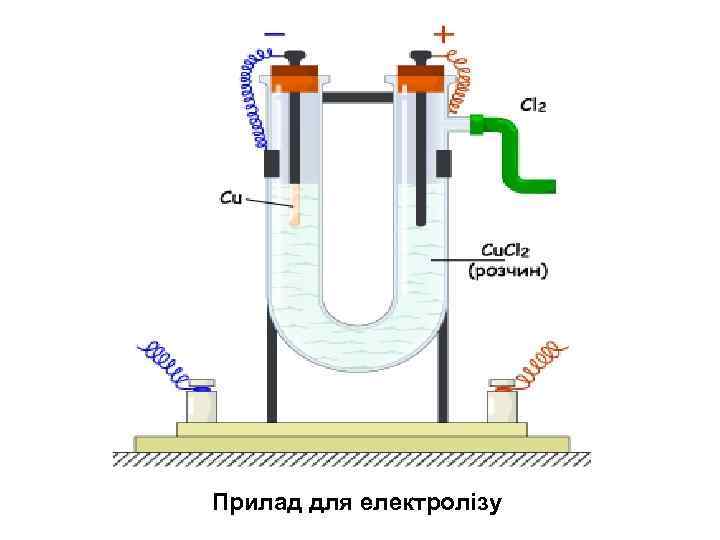
Прилад для електролізу


Золото і платину добувають механічним відділенням їх від гірських порід РУДИ – мінерали та гірські породи , що містять сполуки металів, з яких можна та економічно вигідно добувати метали.

Класифікація металічних руд За видом металу v Руди чорних і легуючих металів ( Fe, Mn, Cr, Ti, V, Ni, Co, W, Mo, Zr, Ta, Nb). v. Руди кольорових металів (Cu, Pb, Zn, Sn, Hg, Sb, As і ін. ). v. Руди легких металів (Al, Mg, Li, Be). v. Руди благородних металів (Au, Ag, Pt). v. Руди рідкісних і розсіяних металів (In, Cd, Se, Te, Ga, Tl, Sc, Cs, Ge, Rb і ін. ). v. Руди радіоактивних металів (Ra, Th, U) За типом металовмісної сполуки v. Оксидні Fe 2 O 3 - Гематит Al 2 O 3 • n. H 2 O - Боксит Mn. O 2 - Піролюзит Ti. O 2 - Рутил v. Сульфідні Pb. S – Галеніт Zn. S - Сфалерит Cu 2 S - Халькозин Mo. S - Молібденіт v. Карбонатні Ca. CO 3 - Кальцит Ca. Mg(CO 3)2 - Доломіт Fe. CO 3 - Сидерит Mg. CO 3 - Магнезит
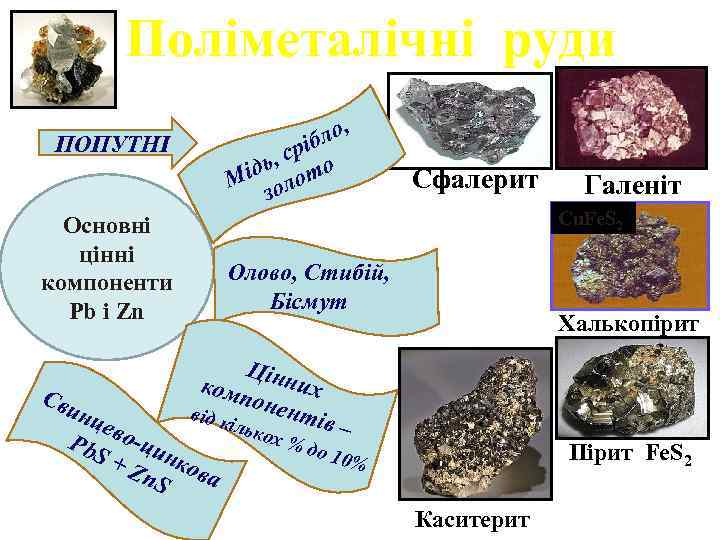
Поліметалічні руди ло, б срі , ідь ото М ол з ПОПУТНІ Галеніт Cu. Fe. S 2 Основні цінні компоненти Pb i Zn Сви н Сфалерит Олово, Стибій, Бісмут Халькопірит Цінн их комп онен від к тів ільк – цев Pb. S о-ци + Z нков а n. S ох % до 1 Пірит Fe. S 2 0% Каситерит

Сплави — це суміші, що складаються з двох або більше металів, а також металів і неметалів. Хімічний зв’язок у сплавах — металічний. Тому вони мають усі властивості металів. Властивості сплавів відрізняються від властивостей вихідних металів. Сплави добувають, змішуючи розплавлені метали, які потім охолоджуються й тверднуть. Повністю однорідні сплави— тверді розчини. Вони утворюються в тому випадку, коли розплавлені метали кристалізуються в однотипних ґратках і мають близькі за розмірами атоми. Відповідно вони змішуються між собою в будь-яких співвідношеннях, наприклад: Ag — Cu, Cu — Ni, Ag — Au та ін. Сполуки-інтерметаліди. Розплавлені метали під час змішування реагують один з одним. Наприклад, Cu. Zn, та ін.

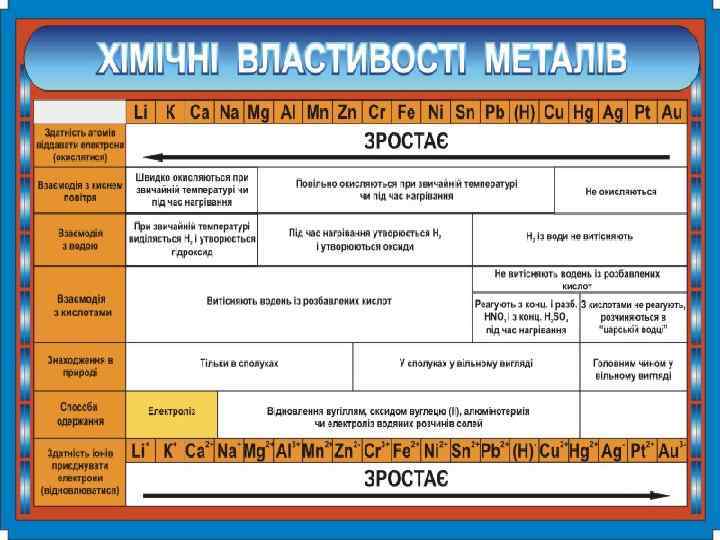
Хімічні властивості металів • Хімічна активність металів визначається здатністю їх атомів віддавати валентні електрони, тобто окиснюватись і перетворюватись на катіони (позитивно заряджені йони). • За активністю метали розташовано у певний ряд (ряд Бекетова, витискувальний ряд, ряд активності, електрохімічний ряд металів). • Чим лівіше стоїть у ряду метал, тим він сильніший відновник і тим важче відновити його. послаблення відновних властивостей, активності

• кожний метал цього ряду може витіснити з водного розчину сполуки будь-який з металічних елементів, що стоїть праворуч від нього, і може бути витіснений будь-яким з металів, що стоять ліворуч; • усі метали, що стоять ліворуч від водню, можуть витісняти Гідроген з кислот, а ті, що стоять праворуч, - не можуть
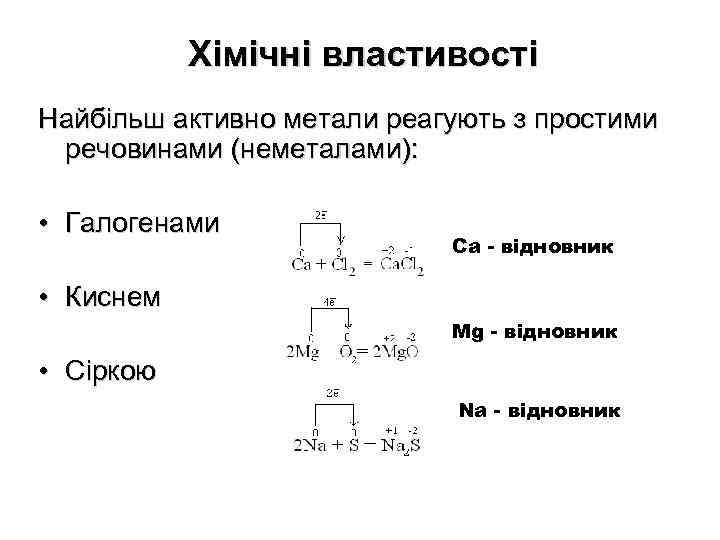
Хімічні властивості Найбільш активно метали реагують з простими речовинами (неметалами): • Галогенами Ca - відновник • Киснем Mg - відновник • Сіркою Na - відновник

Взаємодія з солями Реакція відбувається тільки у водному розчині: активніші метали витісняють менш активні.

Взаємодія з кислотами

Взаємодія з водою • Лужні й лужноземельні метали взаємодіють з водою за стандартних умов з утворенням лугів • Менш активні метали реагують з водою при нагріванні:

Взаємодія з оксидами Активні метали відновлюють менш активні з оксидів під час нагрівання – металотермія Взаємодія с лугами Метали, яким відповідають амфотерні гідроксиди, реагують з лугами

Хімічні властивості Метали можуть утворювати хімічні сполуки між собою – інтерметалічні сполуки або інтерметаліди. Прикладом є сполуки деяких металів з сурмою: Na 2 Sb, Ca 3 Sb, Ni 4 Sb. В них найчастіше всього не зберігаються ступені окиснення, характерні в сполуках з неметалами.

Корозія металів Корозія – це хімічне і електрохімічне руйнування металів та їх сплавів в результаті взаємодії на них зовнішнього середовища. Існує два види корозії: хімічна і електрохімічна. Електрохімічна корозія Корозію Ме та їх сплавів викликають такі компоненти зовнішнього середовища , як вода, кисень, оксиди карбону і сульфуру , водні розчини солей. Більш активний Ме при електрохімічній корозії руйнується, переходячи в воду, тим самим захищає менш активний від руйнування.

Корозія металів Корозія — руйнування металу під дією навколишнього середовища. Це окисновідновний процес. Хімічна корозія — руйнування металу під час його окиснення без виникнення електричного струму в системі. При цьому метал взаємодіє з газами (газова корозія) і рідкими неелектролітами (бензин, нафта, толуол та ін. ). Наприклад, сполука металів із киснем повітря. Електрохімічна корозія — руйнування металу, який знаходиться у контакті з іншим металом у розчині електроліту. При цьому активніший метал віддає електрони, а менш активний їх приймає, тобто в системі виникає електричний струм. Пара таких металів називається гальванічною парою.
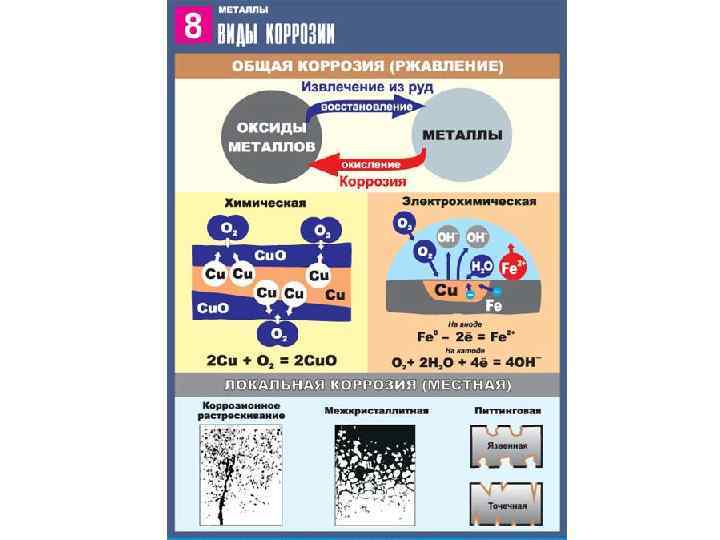

Чинники, що впливають на швидкість корозії 1) Положення контактуючих металів у ряду стандартних електродних потенціалів. Чим далі метали розташовані один від одного, тим вища швидкість корозії. 2) Характер розчину електроліту. Чим вища кислотність розчину і чим більше в ньому окисників, тим швидше відбувається корозія. 3) Температура. За високих температур швидкість корозії зростає.

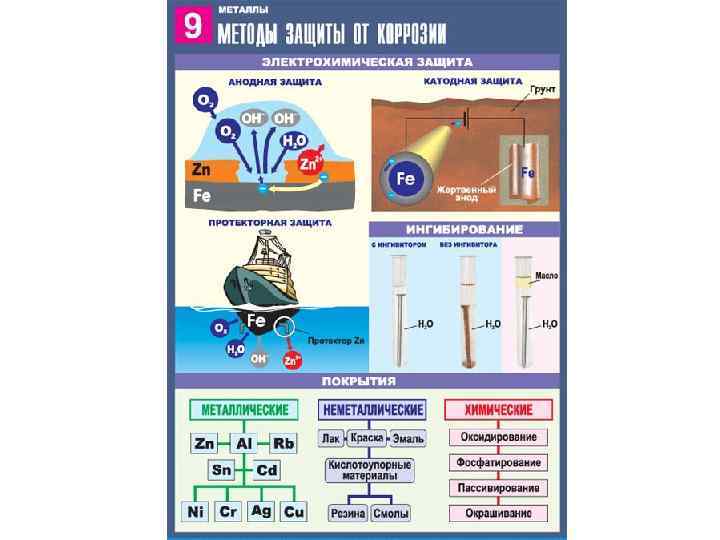
Захист від корозії 1) Захисні поверхневі покриття. Ізолюють метал від контакту з навколишнім середовищем. — Металеві покриття. Метал, який наноситься для запобігання корозії, сам стійкий до неї. Наприклад, покриття заліза цинком (оцинковане залізо). — Неметалеві покриття. Це лаки, фарби, емалі, мастила та ін. 2) Створення антикорозійних сплавів. Наприклад, додаванням хрому (до 12 %) до сталі одержують нержавіючу сталь. 3) Протекторний захист. Застосовується у випадках, коли металева конструкція, що захищається (труби, корпус корабля), знаходиться в активному середовищі електроліту (ґрунтові води, морська вода). Із конструкцією з’єднується активніший метал-протектор. У процесі корозії активніший метал-протектор руйнується, а метал конструкції не кородує. 4) Зміна складу середовища. В електроліт додають речовини, які уповільнюють корозію, — інгібітори.
Метали 14.ppt