Спирты2234345.pptx
- Количество слайдов: 16
 СПИРТЫ
СПИРТЫ
 Историческая справка v Этиловый спирт, вернее хмельной растительный напиток его содержащий, был известен человечеству с глубокой древности. Считается, что не менее чем за 8000 лет до новой эры люди изготавливали легкие спиртные напитки из фруктов и мёда. Впервые спирт из вина получили в 6 -7 веках арабские химики, а первую бутылку крепкого алкоголя (прообраза современной водки) изготовил персидский алхимик Ар-Рази в 860 году. В Европе этиловый спирт был получен из продуктов брожения в 11 -12 веке, в Италии. В Россию спирт впервые попал в 1386 году, когда генуэзское посольство привезло его с собой под названием «Аква вита» и презентовала царскому двору. В 1660 году английский химик и богослов Роберт Бойль впервые получил обезвоженный этиловый спирт, а также открыл его некоторые физические и химические свойства, в частности обнаружив способность этанола выступать в качестве высокотемпературного горючего для горелок. Абсолютированный спирт был получен в 1796 году русским химиком Т. Е. Ловицем.
Историческая справка v Этиловый спирт, вернее хмельной растительный напиток его содержащий, был известен человечеству с глубокой древности. Считается, что не менее чем за 8000 лет до новой эры люди изготавливали легкие спиртные напитки из фруктов и мёда. Впервые спирт из вина получили в 6 -7 веках арабские химики, а первую бутылку крепкого алкоголя (прообраза современной водки) изготовил персидский алхимик Ар-Рази в 860 году. В Европе этиловый спирт был получен из продуктов брожения в 11 -12 веке, в Италии. В Россию спирт впервые попал в 1386 году, когда генуэзское посольство привезло его с собой под названием «Аква вита» и презентовала царскому двору. В 1660 году английский химик и богослов Роберт Бойль впервые получил обезвоженный этиловый спирт, а также открыл его некоторые физические и химические свойства, в частности обнаружив способность этанола выступать в качестве высокотемпературного горючего для горелок. Абсолютированный спирт был получен в 1796 году русским химиком Т. Е. Ловицем.
 Спирты и Фенолы v Спирты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильные группы -ОН. v Этиловый спирт – одноатомный спирт. v Фенолы-органические соединения ароматического ряда, в молекулах которых гидроксильные группы связаны с атомами углерода ароматического кольца. По числу ОН-групп различают: v одноатомные фенолы (аренолы): фенол (C 6 H 5 OH) и его гомологи; v двухатомные фенолы (арендиолы): гидрохинон, пирокатехин, резорцин; v трёхатомные фенолы (арентриолы): пирогаллол, флороглюцин, гидроксигидрохинон и т. д.
Спирты и Фенолы v Спирты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильные группы -ОН. v Этиловый спирт – одноатомный спирт. v Фенолы-органические соединения ароматического ряда, в молекулах которых гидроксильные группы связаны с атомами углерода ароматического кольца. По числу ОН-групп различают: v одноатомные фенолы (аренолы): фенол (C 6 H 5 OH) и его гомологи; v двухатомные фенолы (арендиолы): гидрохинон, пирокатехин, резорцин; v трёхатомные фенолы (арентриолы): пирогаллол, флороглюцин, гидроксигидрохинон и т. д.
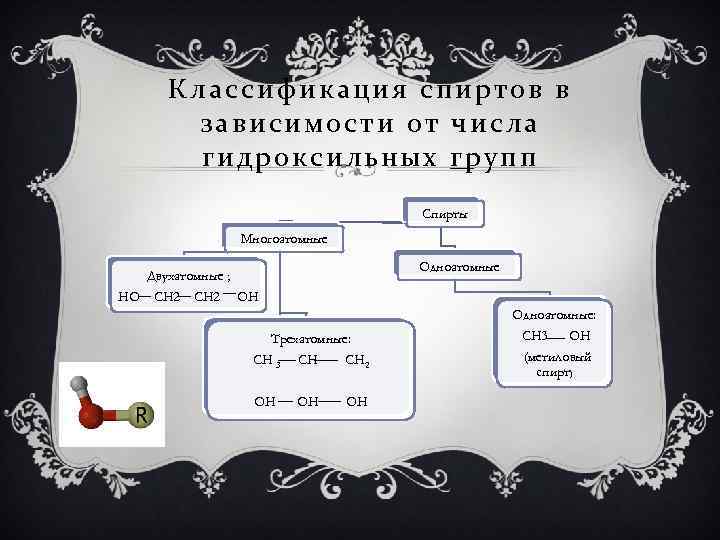 Классификация спиртов в зависимости от числа гидроксильных групп Спирты Многоатомные Одноатомные Двухатомные ; HO CH 2 OH Трехатомные: CH 3 CH CH 2 OH OH OH Одноатомные: CH 3 OH (метиловый спирт)
Классификация спиртов в зависимости от числа гидроксильных групп Спирты Многоатомные Одноатомные Двухатомные ; HO CH 2 OH Трехатомные: CH 3 CH CH 2 OH OH OH Одноатомные: CH 3 OH (метиловый спирт)
 Одноатомные спирты Метанол (метиловый спирт, древесный спирт) - прозрачная, бесцветная жидкость, легко смешиваемая с водой, спиртом и эфиром. Это крайне ядовитое вещество в косметике не применяется. v Этанол (этиловый спирт, винный спирт, спирт пищевой) - прозрачная, бесцветная, летучая жидкость, может смешиваться с водой и органическими растворителями, значительно менее ядовит, чем метанол, широко применяется в медицине и косметике в качестве растворителя для биологически активных веществ (эфирных масел, смол, йода и т. д. ). Получают этанол в результате брожения веществ, содержащих сахар и крахмал. Процесс брожения происходит за счет ферментов дрожжей. После брожения спирт выделяют путем перегонки. Затем производится очистка от нежелательных веществ-примесей (ректификация). Этанол поступает в аптеки в основном крепостью 96°. Другие смеси этанола с водой содержат 90, 80, 70, 40% спирта. Почти чистый спирт (с очень незначительными примесями воды) называют абсолютным спиртом. v В зависимости от цели применения спирта его ароматизируют различными добавками (эфирными маслами, камфорой). Этанол способствует расширению подкожных капилляров, обладает дезинфицирующим действием.
Одноатомные спирты Метанол (метиловый спирт, древесный спирт) - прозрачная, бесцветная жидкость, легко смешиваемая с водой, спиртом и эфиром. Это крайне ядовитое вещество в косметике не применяется. v Этанол (этиловый спирт, винный спирт, спирт пищевой) - прозрачная, бесцветная, летучая жидкость, может смешиваться с водой и органическими растворителями, значительно менее ядовит, чем метанол, широко применяется в медицине и косметике в качестве растворителя для биологически активных веществ (эфирных масел, смол, йода и т. д. ). Получают этанол в результате брожения веществ, содержащих сахар и крахмал. Процесс брожения происходит за счет ферментов дрожжей. После брожения спирт выделяют путем перегонки. Затем производится очистка от нежелательных веществ-примесей (ректификация). Этанол поступает в аптеки в основном крепостью 96°. Другие смеси этанола с водой содержат 90, 80, 70, 40% спирта. Почти чистый спирт (с очень незначительными примесями воды) называют абсолютным спиртом. v В зависимости от цели применения спирта его ароматизируют различными добавками (эфирными маслами, камфорой). Этанол способствует расширению подкожных капилляров, обладает дезинфицирующим действием.
 Многоатомные спирты Двухатомные спирты имеют стандартное окончание названия - гликоль. В косметических препаратах в качестве растворителя и увлажнителя применяют пропиленгликоль, обладающий невысокой токсичностью. Двухатомные спирты, или гликоли, по заместительной номенклатуре называют диолами. Трехатомный спирт - глицерин - широко используется в медицине и фармацее. По консистенции глицерин похож на сироп, почти без запаха, гигроскопичен, имеет сладкий привкус, растворим во всех других веществах, содержащих ОН-группу, нерастворим в эфире, бензине, хлороформе, в жирных и эфирных маслах. В торговлю поступает 86 - 88%-ный глицерин и обезвоженный 98%-ный глицерин. В разбавленном виде глицерин входит в состав кремов для кожи, туалетной воды для лица, зубных паст, мыла для бритья, геля для рук. Разбавленный в соответствующей пропорции, он смягчает кожу, делает ее эластичной, заменяя естественный фактор влажности кожи. В чистом виде в препаратах для ухода за кожей не применяется, поскольку пересушивает ее. v Сорбит- разновидность виноградного сахара, в соединении с водой образует сладковатую вязкую жидкость, которая может быть использовано как заменитель глицерина. Сорбит обладает способностью сохранять влажность кожи, поэтому входит в состав увлажняющих кремов, кремов для бритья, зубных пост и других косметических препаратов.
Многоатомные спирты Двухатомные спирты имеют стандартное окончание названия - гликоль. В косметических препаратах в качестве растворителя и увлажнителя применяют пропиленгликоль, обладающий невысокой токсичностью. Двухатомные спирты, или гликоли, по заместительной номенклатуре называют диолами. Трехатомный спирт - глицерин - широко используется в медицине и фармацее. По консистенции глицерин похож на сироп, почти без запаха, гигроскопичен, имеет сладкий привкус, растворим во всех других веществах, содержащих ОН-группу, нерастворим в эфире, бензине, хлороформе, в жирных и эфирных маслах. В торговлю поступает 86 - 88%-ный глицерин и обезвоженный 98%-ный глицерин. В разбавленном виде глицерин входит в состав кремов для кожи, туалетной воды для лица, зубных паст, мыла для бритья, геля для рук. Разбавленный в соответствующей пропорции, он смягчает кожу, делает ее эластичной, заменяя естественный фактор влажности кожи. В чистом виде в препаратах для ухода за кожей не применяется, поскольку пересушивает ее. v Сорбит- разновидность виноградного сахара, в соединении с водой образует сладковатую вязкую жидкость, которая может быть использовано как заменитель глицерина. Сорбит обладает способностью сохранять влажность кожи, поэтому входит в состав увлажняющих кремов, кремов для бритья, зубных пост и других косметических препаратов.
 По характеру атома углерода, с которым связана гидроксильная группа, спирты делятся на: Первичные, в молекулах которых гидроксильная CH CH CH группа связана с первичным атомом углерода v Вторичные, связана с CH CH вторичным атомом угле OH рода v Третичные, связана с третичным атомом углерода CH CH CH C OH OH OH
По характеру атома углерода, с которым связана гидроксильная группа, спирты делятся на: Первичные, в молекулах которых гидроксильная CH CH CH группа связана с первичным атомом углерода v Вторичные, связана с CH CH вторичным атомом угле OH рода v Третичные, связана с третичным атомом углерода CH CH CH C OH OH OH
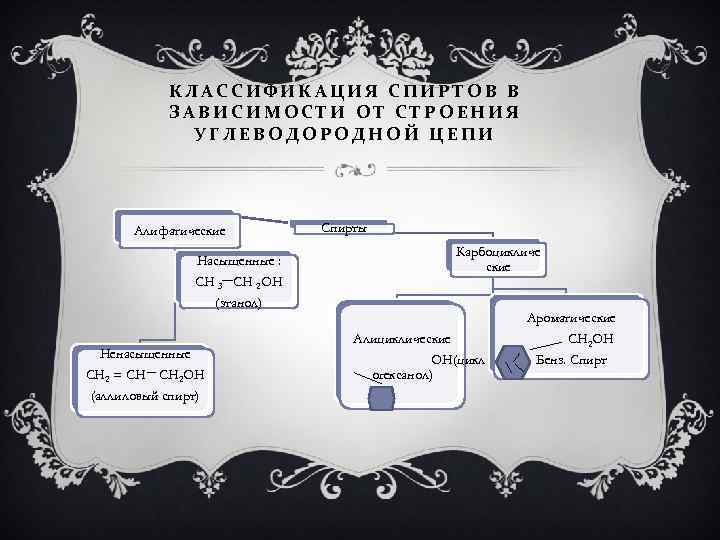 КЛАССИФИКАЦИЯ СПИРТОВ В ЗАВИСИМОСТИ ОТ СТРОЕНИЯ УГЛЕВОДОРОДНОЙ ЦЕПИ Алифатические Насыщенные : CH 3 CH 2 OH Спирты Карбоцикличе ские (этанол) Ненасыщенные CH 2 = CH CH 2 OH (аллиловый спирт) Ароматические Алициклические OH(цикл огексанол) CH 2 OH Бенз. Спирт
КЛАССИФИКАЦИЯ СПИРТОВ В ЗАВИСИМОСТИ ОТ СТРОЕНИЯ УГЛЕВОДОРОДНОЙ ЦЕПИ Алифатические Насыщенные : CH 3 CH 2 OH Спирты Карбоцикличе ские (этанол) Ненасыщенные CH 2 = CH CH 2 OH (аллиловый спирт) Ароматические Алициклические OH(цикл огексанол) CH 2 OH Бенз. Спирт
 Физические свойства спиртов. v Высшие спирты при комнатной температуре – твердые вещества. v Низшие спирты имеют характерный алкогольный запах и жгучий вкус, они хорошо растворимы в воде. По мере увеличения углеводородов радикала растворимость спиртов в воде. v Спирты геометрически подобны молекуле воды. Угол R−O−H в молекуле метанола равен 109°[52]. Гидроксильный кислород находится в состоянии sp³ гибридизации. v Подобно воде, спирты имеют существенно более высокие температуры плавления и кипения, чем можно было бы предполагать на основании физических свойств родственных соединений.
Физические свойства спиртов. v Высшие спирты при комнатной температуре – твердые вещества. v Низшие спирты имеют характерный алкогольный запах и жгучий вкус, они хорошо растворимы в воде. По мере увеличения углеводородов радикала растворимость спиртов в воде. v Спирты геометрически подобны молекуле воды. Угол R−O−H в молекуле метанола равен 109°[52]. Гидроксильный кислород находится в состоянии sp³ гибридизации. v Подобно воде, спирты имеют существенно более высокие температуры плавления и кипения, чем можно было бы предполагать на основании физических свойств родственных соединений.
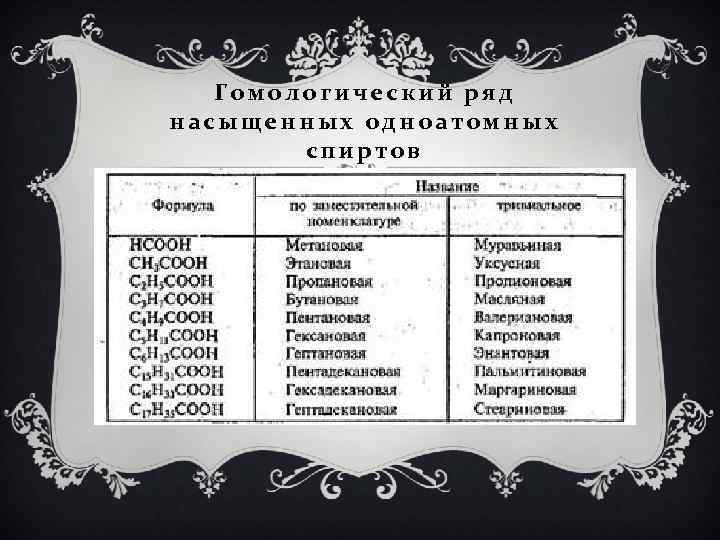 Гомологический ряд насыщенных одноатомных спиртов
Гомологический ряд насыщенных одноатомных спиртов
 Номенклатура спиртов v По номенклатуре ИЮПАК названия простых спиртов образуются от названий соответствующих алканов с добавлением суффикса «-ол» , положение которого указывается арабской цифрой. Правила построения названия спиртов (функциональная группа −OH)[ 1. Выбирается родительский углеводород по самой длинной непрерывной углеводородной цепи, содержащей функциональную группу. Он формирует базовое название (по числу атомов углерода). 2. Родительский углеводород нумеруется в направлении, которое дает суффиксу функциональной группы самое низкое число. 3. Если в соединении помимо функциональной группы имеется другой заместитель, суффикс функциональной группы получает самое низкое число. 4. Если для суффикса функциональной группы получено одно и то же число в обоих направлениях, цепь нумеруется в направлении, которое дает другому заместителю самое низкое число. 5. Если имеется несколько заместителей, они перечисляются в алфавитном порядке. v Имена заместителей ставятся перед именем родительского углеводорода, а суффикс функциональной группы — после. ИЮПАК рекомендует цифру, характеризующую положение функциональной группы, писать сразу после имени углеводородного заместителя перед суффиксом функциональной группы. v Для многоатомных спиртов перед суффиксом -ол по-гречески (-ди-, -три-, …) указывается количество гидроксильных групп (например: пропан-1, 2, 3 -триол).
Номенклатура спиртов v По номенклатуре ИЮПАК названия простых спиртов образуются от названий соответствующих алканов с добавлением суффикса «-ол» , положение которого указывается арабской цифрой. Правила построения названия спиртов (функциональная группа −OH)[ 1. Выбирается родительский углеводород по самой длинной непрерывной углеводородной цепи, содержащей функциональную группу. Он формирует базовое название (по числу атомов углерода). 2. Родительский углеводород нумеруется в направлении, которое дает суффиксу функциональной группы самое низкое число. 3. Если в соединении помимо функциональной группы имеется другой заместитель, суффикс функциональной группы получает самое низкое число. 4. Если для суффикса функциональной группы получено одно и то же число в обоих направлениях, цепь нумеруется в направлении, которое дает другому заместителю самое низкое число. 5. Если имеется несколько заместителей, они перечисляются в алфавитном порядке. v Имена заместителей ставятся перед именем родительского углеводорода, а суффикс функциональной группы — после. ИЮПАК рекомендует цифру, характеризующую положение функциональной группы, писать сразу после имени углеводородного заместителя перед суффиксом функциональной группы. v Для многоатомных спиртов перед суффиксом -ол по-гречески (-ди-, -три-, …) указывается количество гидроксильных групп (например: пропан-1, 2, 3 -триол).
 Изомерия v Спиртам, как и насыщенным углеводородам, свойственна изомерия цепи. На примере спирта состава С 4 Н 10 О можно проиллюстрировать изомеры, отличающиеся строением углеродной цепи, возникающие в результате различного порядка соединения атомов углерода в молекулах. v v v
Изомерия v Спиртам, как и насыщенным углеводородам, свойственна изомерия цепи. На примере спирта состава С 4 Н 10 О можно проиллюстрировать изомеры, отличающиеся строением углеродной цепи, возникающие в результате различного порядка соединения атомов углерода в молекулах. v v v
 Образование водородных связей В молекуле спирта R-O-H химическая связь между атомом водорода и более электроотрицательным атомом кислорода весьма полярна. Водород имеет частичный положительный заряд (d+), а кислород - частичный отрицательный (d-): R - углеводородный радикал (CH 3, C 2 H 5 и т. п. ) Следовательно, возможно образование водородных связей между молекулами спирта: Это приводит к ассоциации молекул и объясняет относительно высокую т. кип. спиртов. В присутствии воды возникают водородные связи между молекулами спирта и воды: Поэтому низшие спирты хорошо растворимы в воде.
Образование водородных связей В молекуле спирта R-O-H химическая связь между атомом водорода и более электроотрицательным атомом кислорода весьма полярна. Водород имеет частичный положительный заряд (d+), а кислород - частичный отрицательный (d-): R - углеводородный радикал (CH 3, C 2 H 5 и т. п. ) Следовательно, возможно образование водородных связей между молекулами спирта: Это приводит к ассоциации молекул и объясняет относительно высокую т. кип. спиртов. В присутствии воды возникают водородные связи между молекулами спирта и воды: Поэтому низшие спирты хорошо растворимы в воде.
 Химические свойства спиртов v Физико-химические свойства спиртов определяются в основном строением углеводородной цепи и функциональной группы −OH, а также их взаимным влиянием: v 1) Чем больше заместитель, тем сильнее он влияет на функциональную группу, снижая полярность связи O—Н. Реакции, основанные на разрыве этой связи, протекают более медленно. v 2) Гидроксильная группа −ОН уменьшает электронную плотность вдоль прилегающих σ-связей углеродной цепи (отрицательный индуктивный эффект). v Все химические реакции спиртов можно разделить на три условных группы, связанных с определёнными реакционными центрами и химическими связями: v Разрыв связи O−H (реакционный центр — водород); v Разрыв или присоединение по связи С−OH (реакционный центр — кислород); v Разрыв связи −СOH (реакционный центр — углерод). v Реакции с участием гидроксильной группы связи С−O и О−H) v Кислотно-основные реакции спиртов v Со щелочными и щелочноземельными металлами, алюминием, галлием, таллием, и некоторыми другими металлами, а также сильными основаниями (например: амидами или гидридами) спирты способны реагировать с образованием алкоголятов.
Химические свойства спиртов v Физико-химические свойства спиртов определяются в основном строением углеводородной цепи и функциональной группы −OH, а также их взаимным влиянием: v 1) Чем больше заместитель, тем сильнее он влияет на функциональную группу, снижая полярность связи O—Н. Реакции, основанные на разрыве этой связи, протекают более медленно. v 2) Гидроксильная группа −ОН уменьшает электронную плотность вдоль прилегающих σ-связей углеродной цепи (отрицательный индуктивный эффект). v Все химические реакции спиртов можно разделить на три условных группы, связанных с определёнными реакционными центрами и химическими связями: v Разрыв связи O−H (реакционный центр — водород); v Разрыв или присоединение по связи С−OH (реакционный центр — кислород); v Разрыв связи −СOH (реакционный центр — углерод). v Реакции с участием гидроксильной группы связи С−O и О−H) v Кислотно-основные реакции спиртов v Со щелочными и щелочноземельными металлами, алюминием, галлием, таллием, и некоторыми другими металлами, а также сильными основаниями (например: амидами или гидридами) спирты способны реагировать с образованием алкоголятов.
 Получение спиртов v Спирты являются обширным и очень разнообразным классом органических соединений: они широко распространены в природе, имеют важнейшее промышленное значение и обладают исключительными химическими свойствами. v Существует огромное количество методов получения спиртов, при этом их можно разбить на две условных группы: v химические способы получения спиртов — синтетические спирты; v биохимические способы получения спиртов — биоспирты.
Получение спиртов v Спирты являются обширным и очень разнообразным классом органических соединений: они широко распространены в природе, имеют важнейшее промышленное значение и обладают исключительными химическими свойствами. v Существует огромное количество методов получения спиртов, при этом их можно разбить на две условных группы: v химические способы получения спиртов — синтетические спирты; v биохимические способы получения спиртов — биоспирты.
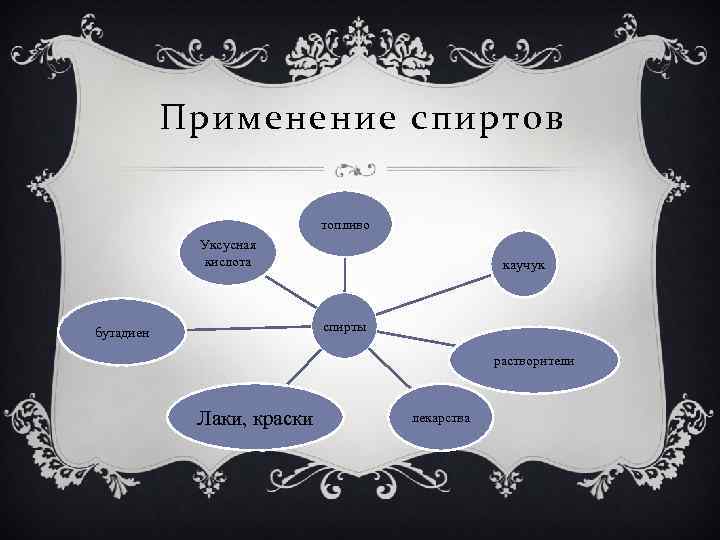 Применение спиртов топливо Уксусная кислота каучук спирты бутадиен растворители Лаки, краски лекарства
Применение спиртов топливо Уксусная кислота каучук спирты бутадиен растворители Лаки, краски лекарства


