СПИРТЫ, АЛЬДЕГИДЫ, КИСЛОТЫ_лекция-1.ppt
- Количество слайдов: 59
 СПИРТЫ, АЛЬДЕГИДЫ, КИСЛОТЫ
СПИРТЫ, АЛЬДЕГИДЫ, КИСЛОТЫ
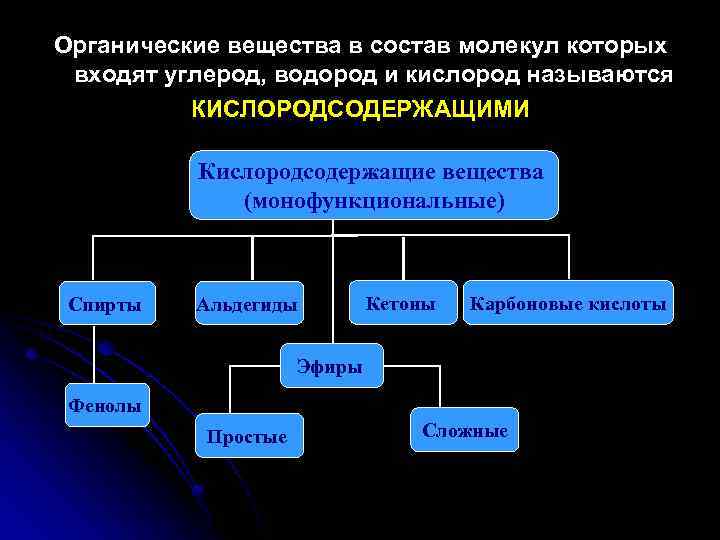 Органические вещества в состав молекул которых входят углерод, водород и кислород называются КИСЛОРОДСОДЕРЖАЩИМИ Кислородсодержащие вещества (монофункциональные) Спирты Альдегиды Кетоны Карбоновые кислоты Эфиры Фенолы Простые Сложные
Органические вещества в состав молекул которых входят углерод, водород и кислород называются КИСЛОРОДСОДЕРЖАЩИМИ Кислородсодержащие вещества (монофункциональные) Спирты Альдегиды Кетоны Карбоновые кислоты Эфиры Фенолы Простые Сложные
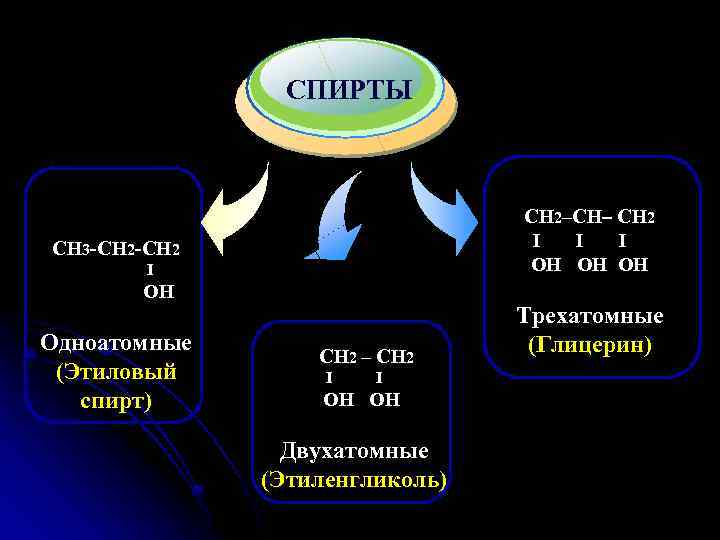 Title Add your text СПИРТЫ CH 2‒CH‒ CH 2 I I I OH OH CH 3 -CH 2 I OH Одноатомные (Этиловый спирт) CH 2 ‒ CH 2 I I OH Двухатомные (Этиленгликоль) Трехатомные (Глицерин)
Title Add your text СПИРТЫ CH 2‒CH‒ CH 2 I I I OH OH CH 3 -CH 2 I OH Одноатомные (Этиловый спирт) CH 2 ‒ CH 2 I I OH Двухатомные (Этиленгликоль) Трехатомные (Глицерин)
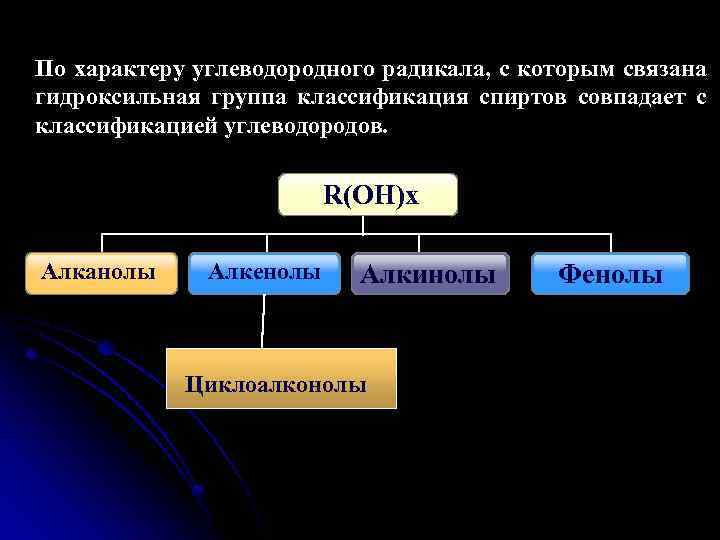 По характеру углеводородного радикала, с которым связана гидроксильная группа классификация спиртов совпадает с классификацией углеводородов. R(OH)x Алканолы Алкенолы Алкинолы Циклоалконолы Фенолы
По характеру углеводородного радикала, с которым связана гидроксильная группа классификация спиртов совпадает с классификацией углеводородов. R(OH)x Алканолы Алкенолы Алкинолы Циклоалконолы Фенолы
 Номенклатура спиртов Алканолы образуют гомологический ряд общей формулы Cn. H 2 n+1 OH (n=1, 2, 3, : N). Названия алканолов по систематической номенклатуре строятся из названий соответствующих алканов путём добавления суффикса «ол» Метиловый спирт Этиловый спирт CH 3 -OH - метанол C 2 H 5 -OH - этанол Пропиловый спирт СН 3 -СН 2 -ОН - пропанол -ОН - Бутиловый спирт СН 3 -СН 2 -СН 2 -ОН - бутанол
Номенклатура спиртов Алканолы образуют гомологический ряд общей формулы Cn. H 2 n+1 OH (n=1, 2, 3, : N). Названия алканолов по систематической номенклатуре строятся из названий соответствующих алканов путём добавления суффикса «ол» Метиловый спирт Этиловый спирт CH 3 -OH - метанол C 2 H 5 -OH - этанол Пропиловый спирт СН 3 -СН 2 -ОН - пропанол -ОН - Бутиловый спирт СН 3 -СН 2 -СН 2 -ОН - бутанол
 Строение молекулы этанола Н Н | | δ δ+ Н – С О Н | | Н Н В молекуле этанола атомы углерода, водорода и кислорода связаны только одинарными связями. Поскольку электроотрицательность кислорода больше электроотрицательности углерода и водорода, общие электронные пары связей С –О и О – Н смещены в сторону атома кислорода. На нём возникает частичный отрицательный, а на атомах углерода и водорода частичные положительные заряды.
Строение молекулы этанола Н Н | | δ δ+ Н – С О Н | | Н Н В молекуле этанола атомы углерода, водорода и кислорода связаны только одинарными связями. Поскольку электроотрицательность кислорода больше электроотрицательности углерода и водорода, общие электронные пары связей С –О и О – Н смещены в сторону атома кислорода. На нём возникает частичный отрицательный, а на атомах углерода и водорода частичные положительные заряды.
 Реакция замещения водорода -ОН группы С 2 Н 5 ОН + Na → C 2 H 5 ONa + H 2 O → C 2 H 5 OH + Na. OH Как слабые кислоты алканолы могут реагировать со щелочными металлами. Образующиеся при этом металлические производные спиртов называются алкоголятами.
Реакция замещения водорода -ОН группы С 2 Н 5 ОН + Na → C 2 H 5 ONa + H 2 O → C 2 H 5 OH + Na. OH Как слабые кислоты алканолы могут реагировать со щелочными металлами. Образующиеся при этом металлические производные спиртов называются алкоголятами.
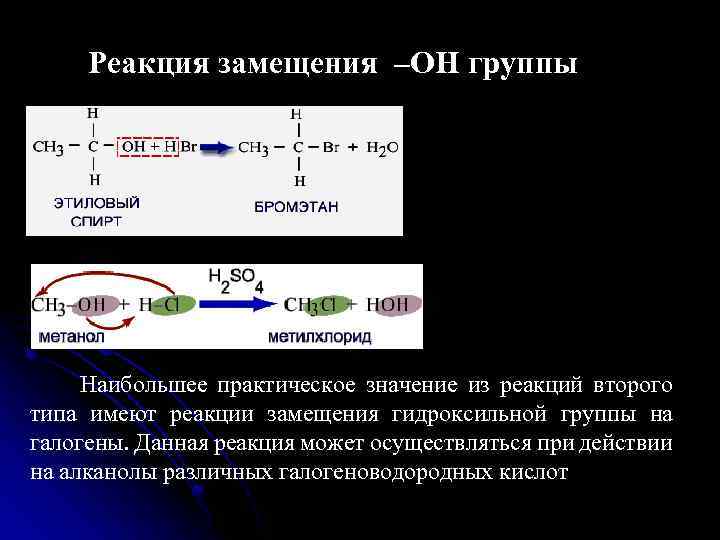 Реакция замещения –ОН группы Наибольшее практическое значение из реакций второго типа имеют реакции замещения гидроксильной группы на галогены. Данная реакция может осуществляться при действии на алканолы различных галогеноводородных кислот
Реакция замещения –ОН группы Наибольшее практическое значение из реакций второго типа имеют реакции замещения гидроксильной группы на галогены. Данная реакция может осуществляться при действии на алканолы различных галогеноводородных кислот
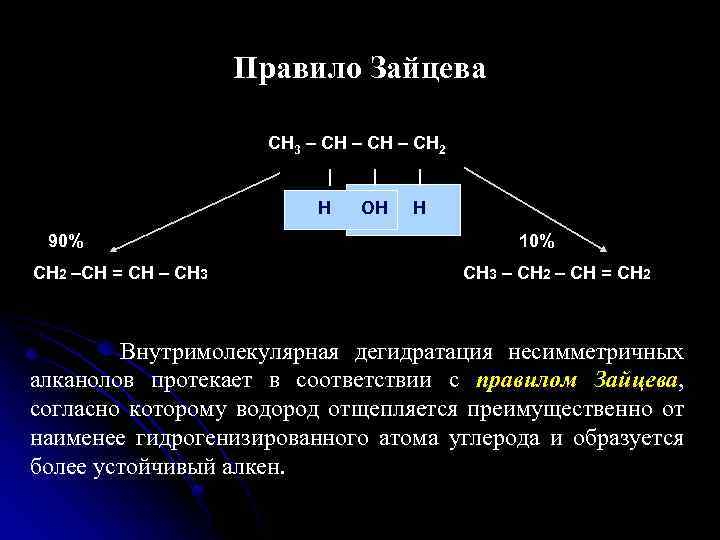 Правило Зайцева СН 3 – СН 2 | | | Н ОН Н 90% 10% СН 2 –СН = СН – СН 3 СН 3 – СН 2 – СН = СН 2 Внутримолекулярная дегидратация несимметричных алканолов протекает в соответствии с правилом Зайцева, согласно которому водород отщепляется преимущественно от наименее гидрогенизированного атома углерода и образуется более устойчивый алкен.
Правило Зайцева СН 3 – СН 2 | | | Н ОН Н 90% 10% СН 2 –СН = СН – СН 3 СН 3 – СН 2 – СН = СН 2 Внутримолекулярная дегидратация несимметричных алканолов протекает в соответствии с правилом Зайцева, согласно которому водород отщепляется преимущественно от наименее гидрогенизированного атома углерода и образуется более устойчивый алкен.
 Дегидратация спиртов При более слабом нагревании этилового спирта с серной кислотой образуется диэтиловый эфир. Это летучая, легко воспламеняющаяся жидкость. Диэтиловый эфир относится к классу простых эфиров – органических веществ, молекулы которых состоят из двух углеводородных радикалов, соединённых посредством атома кислорода. Общая формула R – O - R
Дегидратация спиртов При более слабом нагревании этилового спирта с серной кислотой образуется диэтиловый эфир. Это летучая, легко воспламеняющаяся жидкость. Диэтиловый эфир относится к классу простых эфиров – органических веществ, молекулы которых состоят из двух углеводородных радикалов, соединённых посредством атома кислорода. Общая формула R – O - R
 Третичные спирты могут окисляться только в жёстких условиях, при действии сильных окислителей. Реакции сопровождаются разрывом С – С связей у α углеродных атомов и образованием смеси карбонильных соединений
Третичные спирты могут окисляться только в жёстких условиях, при действии сильных окислителей. Реакции сопровождаются разрывом С – С связей у α углеродных атомов и образованием смеси карбонильных соединений
 Наиболее распространённым методом получения этанола является ферментативное расщепление моносахаридов. С 6 H 10 O 5)n+n. H 2 O зимаза C 6 H 12 O 6 2 С 2 Н 5 OH+2 CO 2
Наиболее распространённым методом получения этанола является ферментативное расщепление моносахаридов. С 6 H 10 O 5)n+n. H 2 O зимаза C 6 H 12 O 6 2 С 2 Н 5 OH+2 CO 2
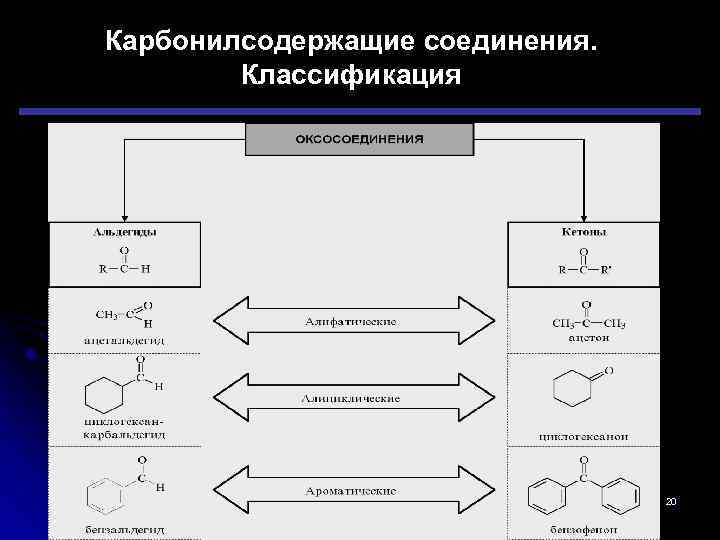 Карбонилсодержащие соединения. Классификация 20
Карбонилсодержащие соединения. Классификация 20
 O // соединения, содержащие карбонильную группу, в которой атом углерода связан с R – C радикалом и одним атомом водорода, то есть общая формула альдегидов: H АЛЬДЕГИДЫ – органические КЕТОНЫ – органические соединения, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами: R 1 – C – R 2 || O 2/17/2018 21
O // соединения, содержащие карбонильную группу, в которой атом углерода связан с R – C радикалом и одним атомом водорода, то есть общая формула альдегидов: H АЛЬДЕГИДЫ – органические КЕТОНЫ – органические соединения, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами: R 1 – C – R 2 || O 2/17/2018 21
 Альдегиды. Номенклатура 1. ВЫБОР ГЛАВНОЙ ЦЕПИ 2. НУМЕРАЦИЯ ГЛАВНОЙ ЦЕПИ (НАЧИНАЕТСЯ С АТОМА УГЛЕРОДА ФУНКЦИОНАЛЬНОЙ ГРУППЫ 3. НАЗЫВАЮТСЯ ЗАМЕСТИТЕЛИ И ИХ ПОЛОЖЕНИЕ В АЛФАВИТНОМ ПОРЯДКЕ 4. НАЗЫВАЕТСЯ УГЛЕВОДОРОД ПО ЧИСЛУ АТОМОВ УГЛЕРОДА В ЦЕПИ С СУФФИКСОМ -АЛЬ
Альдегиды. Номенклатура 1. ВЫБОР ГЛАВНОЙ ЦЕПИ 2. НУМЕРАЦИЯ ГЛАВНОЙ ЦЕПИ (НАЧИНАЕТСЯ С АТОМА УГЛЕРОДА ФУНКЦИОНАЛЬНОЙ ГРУППЫ 3. НАЗЫВАЮТСЯ ЗАМЕСТИТЕЛИ И ИХ ПОЛОЖЕНИЕ В АЛФАВИТНОМ ПОРЯДКЕ 4. НАЗЫВАЕТСЯ УГЛЕВОДОРОД ПО ЧИСЛУ АТОМОВ УГЛЕРОДА В ЦЕПИ С СУФФИКСОМ -АЛЬ
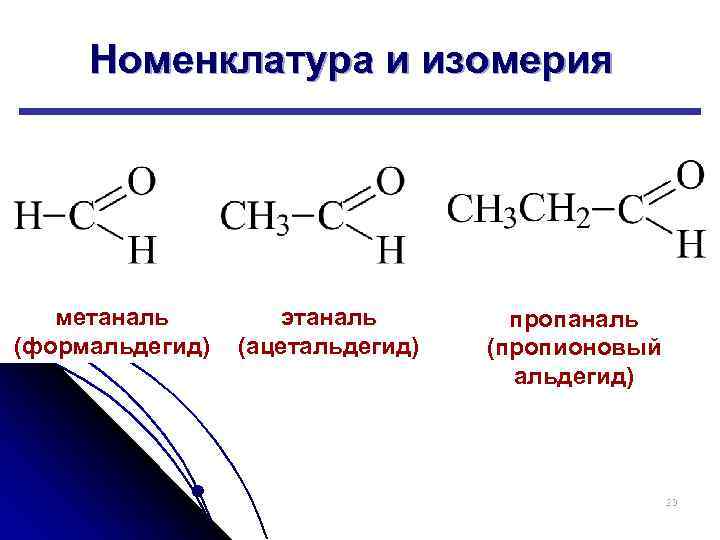 Номенклатура и изомерия метаналь (формальдегид) этаналь (ацетальдегид) пропаналь (пропионовый альдегид) 23
Номенклатура и изомерия метаналь (формальдегид) этаналь (ацетальдегид) пропаналь (пропионовый альдегид) 23
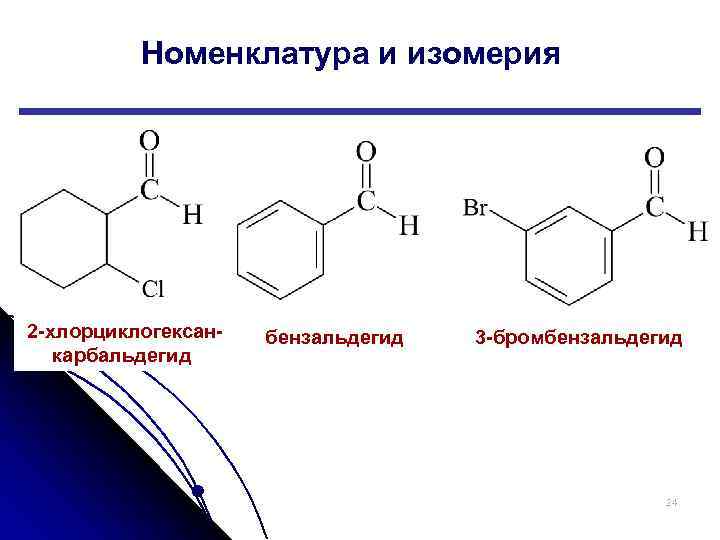 Номенклатура и изомерия 2 хлорциклогексан карбальдегид бензальдегид 3 бромбензальдегид 24
Номенклатура и изомерия 2 хлорциклогексан карбальдегид бензальдегид 3 бромбензальдегид 24
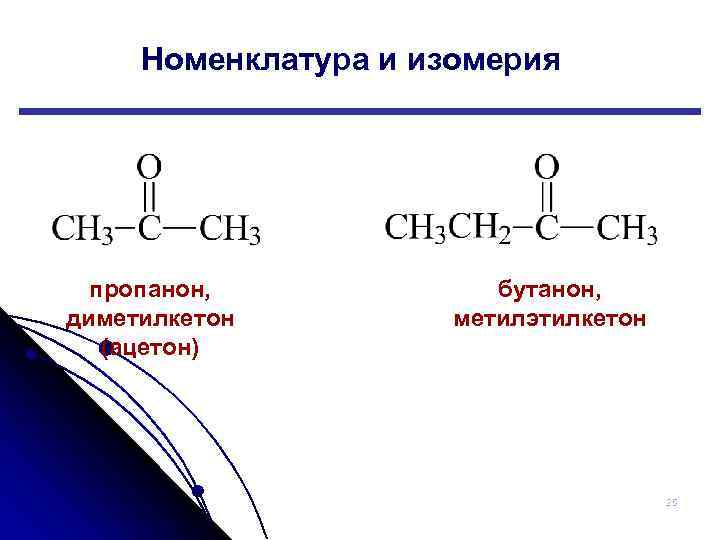 Номенклатура и изомерия пропанон, диметилкетон (ацетон) бутанон, метилэтилкетон 25
Номенклатура и изомерия пропанон, диметилкетон (ацетон) бутанон, метилэтилкетон 25
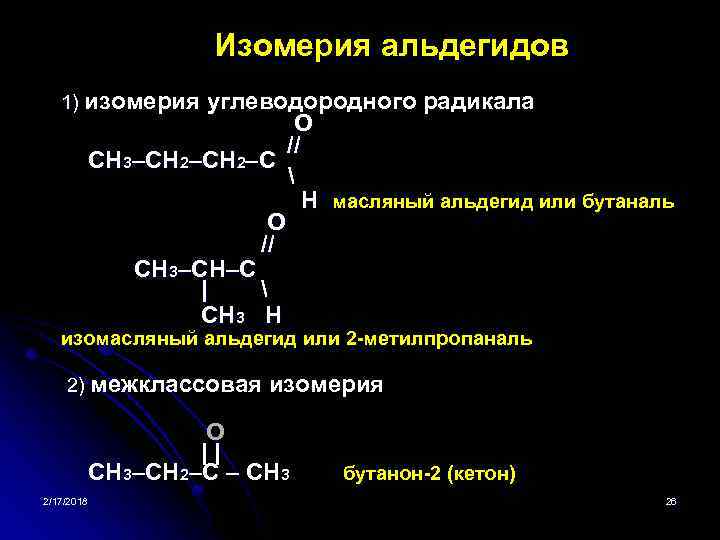 Изомерия альдегидов 1) изомерия углеводородного радикала O // CH 3–CH 2–C H масляный альдегид или бутаналь O // CH 3–CH–C | CH 3 H изомасляный альдегид или 2 метилпропаналь 2) межклассовая изомерия O | | CH 3–CH 2–C – CH 3 бутанон 2 (кетон) 2/17/2018 26
Изомерия альдегидов 1) изомерия углеводородного радикала O // CH 3–CH 2–C H масляный альдегид или бутаналь O // CH 3–CH–C | CH 3 H изомасляный альдегид или 2 метилпропаналь 2) межклассовая изомерия O | | CH 3–CH 2–C – CH 3 бутанон 2 (кетон) 2/17/2018 26
 Способы получения Ацилирование ароматических углеводородов 27
Способы получения Ацилирование ароматических углеводородов 27
 Способы получения Получение из дигалогенпроизводных 28
Способы получения Получение из дигалогенпроизводных 28
 Способы получения Получение из спиртов. Окисление спиртов 29
Способы получения Получение из спиртов. Окисление спиртов 29
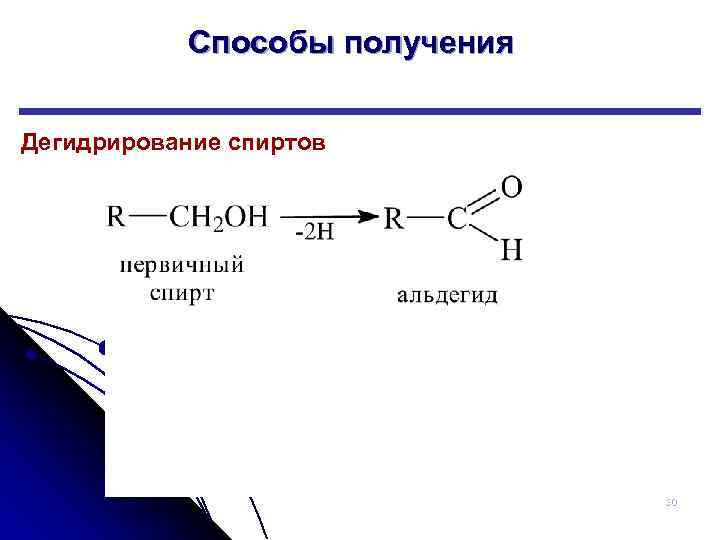 Способы получения Дегидрирование спиртов 30
Способы получения Дегидрирование спиртов 30
 Способы получения Окисление алкенов 31
Способы получения Окисление алкенов 31
 Химические реакции восстановления полимеризации присоединения окисления
Химические реакции восстановления полимеризации присоединения окисления
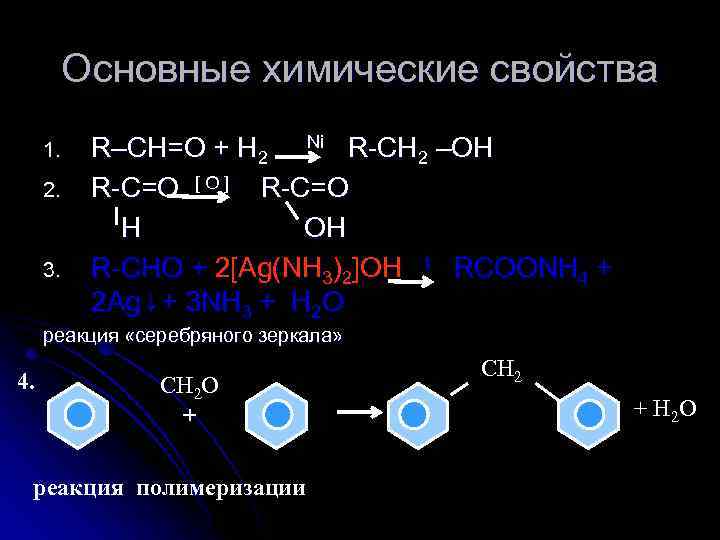 Основные химические свойства R–CH=O + H 2 Ni R-CH 2 –OH 2. R-C=O [ O ] R-C=O H OH 3. R-CHO + 2[Ag(NH 3)2]OH t RCOONH 4 + 2 Ag↓+ 3 NH 3 + H 2 O 1. реакция «серебряного зеркала» 4. СH 2 O + реакция полимеризации СH 2 + H 2 O
Основные химические свойства R–CH=O + H 2 Ni R-CH 2 –OH 2. R-C=O [ O ] R-C=O H OH 3. R-CHO + 2[Ag(NH 3)2]OH t RCOONH 4 + 2 Ag↓+ 3 NH 3 + H 2 O 1. реакция «серебряного зеркала» 4. СH 2 O + реакция полимеризации СH 2 + H 2 O
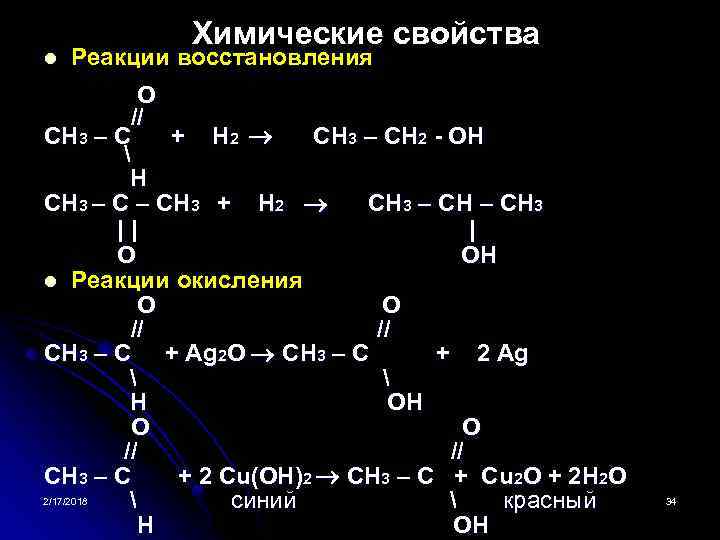 l Химические свойства Реакции восстановления O // CH 3 – C + H 2 CH 3 – CH 2 OH H CH 3 – CH 3 + H 2 CH 3 – CH 3 | | O OH l Реакции окисления O // // CH 3 – C + Ag 2 O CH 3 – C + 2 Ag H O // CH 3 – C + 2 Cu(OH)2 CH 3 – C + Cu 2 O + 2 H 2 O 2/17/2018 34 синий красный H OH
l Химические свойства Реакции восстановления O // CH 3 – C + H 2 CH 3 – CH 2 OH H CH 3 – CH 3 + H 2 CH 3 – CH 3 | | O OH l Реакции окисления O // // CH 3 – C + Ag 2 O CH 3 – C + 2 Ag H O // CH 3 – C + 2 Cu(OH)2 CH 3 – C + Cu 2 O + 2 H 2 O 2/17/2018 34 синий красный H OH
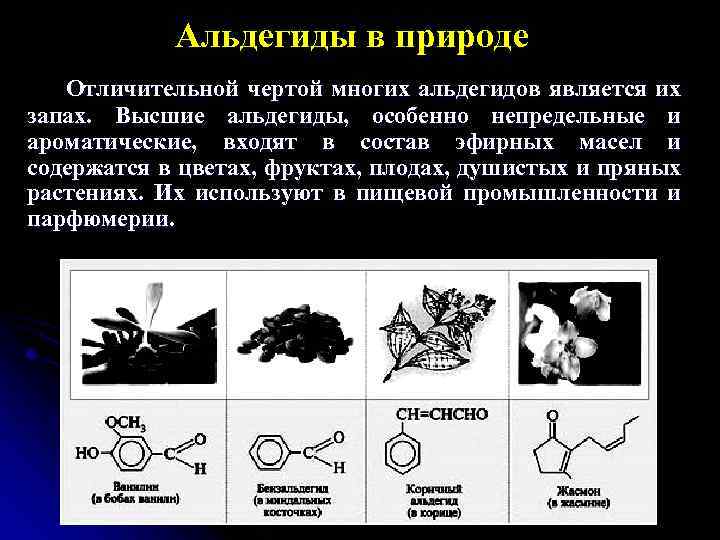 Альдегиды в природе Отличительной чертой многих альдегидов является их запах. Высшие альдегиды, особенно непредельные и ароматические, входят в состав эфирных масел и содержатся в цветах, фруктах, плодах, душистых и пряных растениях. Их используют в пищевой промышленности и парфюмерии.
Альдегиды в природе Отличительной чертой многих альдегидов является их запах. Высшие альдегиды, особенно непредельные и ароматические, входят в состав эфирных масел и содержатся в цветах, фруктах, плодах, душистых и пряных растениях. Их используют в пищевой промышленности и парфюмерии.
 Альдегиды в природе Цитраль Запах цитрусовых обусловлен данным диеновым альдегидом. Его применяют в качестве отдушки средств бытовой химии, косметических и парфюмерных веществ.
Альдегиды в природе Цитраль Запах цитрусовых обусловлен данным диеновым альдегидом. Его применяют в качестве отдушки средств бытовой химии, косметических и парфюмерных веществ.
 Альдегиды в природе Коричный альдегид содержится в масле корицы, его получают перегонкой коры дерева корицы. Применяется в кулинарии в виде палочек или порошка.
Альдегиды в природе Коричный альдегид содержится в масле корицы, его получают перегонкой коры дерева корицы. Применяется в кулинарии в виде палочек или порошка.
 Кетоны в природе Гептанон-2 CH 3―CH 2―CH 2―CO―CH 3 Это соединение представляет собой жидкость с гвоздичным запахом. Гептаноном-2 обусловлен запах многих плодов и молочных продуктов, например, сыра «Рокфор»
Кетоны в природе Гептанон-2 CH 3―CH 2―CH 2―CO―CH 3 Это соединение представляет собой жидкость с гвоздичным запахом. Гептаноном-2 обусловлен запах многих плодов и молочных продуктов, например, сыра «Рокфор»
 Кетоны в природе n-Гидроксифенилбутанон-2 Этот кетон обуславливает в основном запах спелых ягод малины. Его включают в состав синтетических душистых композиций
Кетоны в природе n-Гидроксифенилбутанон-2 Этот кетон обуславливает в основном запах спелых ягод малины. Его включают в состав синтетических душистых композиций
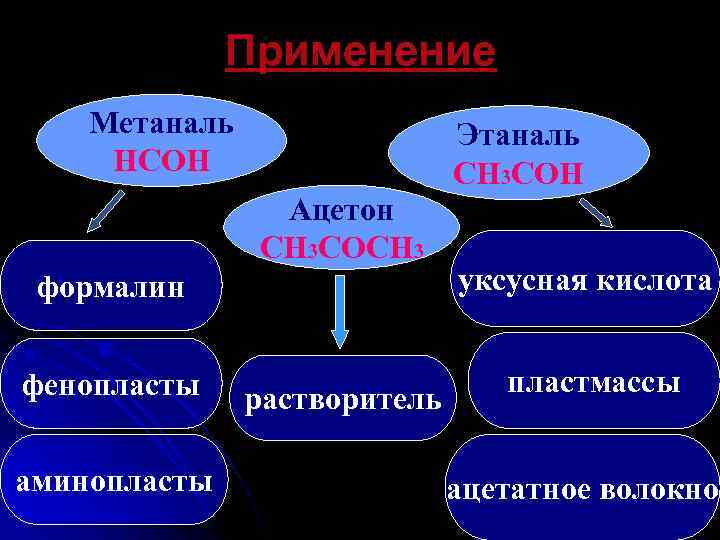 Применение Метаналь HCOH Этаналь CH 3 COH Ацетон CH 3 COCH 3 формалин уксусная кислота фенопласты пластмассы аминопласты растворитель ацетатное волокно
Применение Метаналь HCOH Этаналь CH 3 COH Ацетон CH 3 COCH 3 формалин уксусная кислота фенопласты пластмассы аминопласты растворитель ацетатное волокно
 Карбоновые кислоты — класс органических соединений, молекулы которого содержат карбоксильную группу — COOH. Состав предельных одноосновных карбоновых кислот соответствует общей формуле
Карбоновые кислоты — класс органических соединений, молекулы которого содержат карбоксильную группу — COOH. Состав предельных одноосновных карбоновых кислот соответствует общей формуле
 Классификация По числу карбоксильных групп карбоновые кислоты делятся на: • монокарбоновые или одноосновные (уксусная кислота) • дикарбоновые или двухосновные (щавелевая кислота) В зависимости от строения углеводородного радикала, с которым связана карбоксильная группа, карбоновые кислоты делятся на: • алифатические ( уксусная или акриловая) • алициклические (циклогексанкарбоновая) • ароматические (бензойная, фталевая)
Классификация По числу карбоксильных групп карбоновые кислоты делятся на: • монокарбоновые или одноосновные (уксусная кислота) • дикарбоновые или двухосновные (щавелевая кислота) В зависимости от строения углеводородного радикала, с которым связана карбоксильная группа, карбоновые кислоты делятся на: • алифатические ( уксусная или акриловая) • алициклические (циклогексанкарбоновая) • ароматические (бензойная, фталевая)
 Классификация карбоновых кислот: 1) В зависимости от числа карбоксильных групп ● одноосновные – уксусная ● двухосновные – щавелевая ● многоосновные – лимонная
Классификация карбоновых кислот: 1) В зависимости от числа карбоксильных групп ● одноосновные – уксусная ● двухосновные – щавелевая ● многоосновные – лимонная
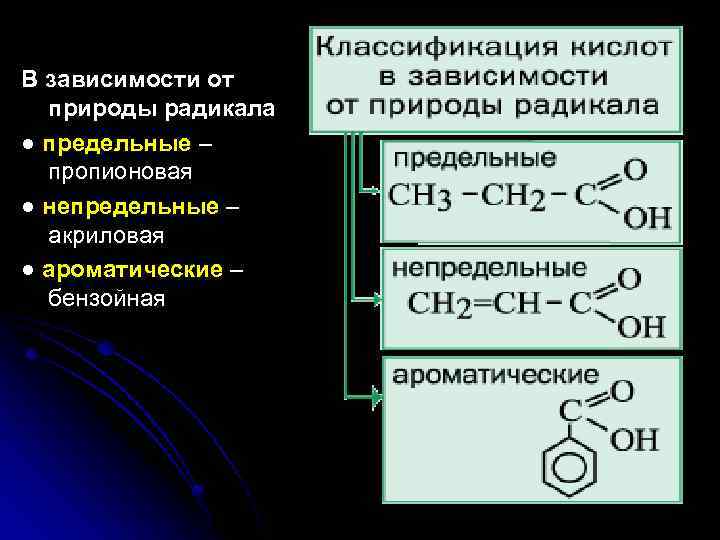 В зависимости от природы радикала ● предельные – пропионовая ● непредельные – акриловая ● ароматические – бензойная
В зависимости от природы радикала ● предельные – пропионовая ● непредельные – акриловая ● ароматические – бензойная
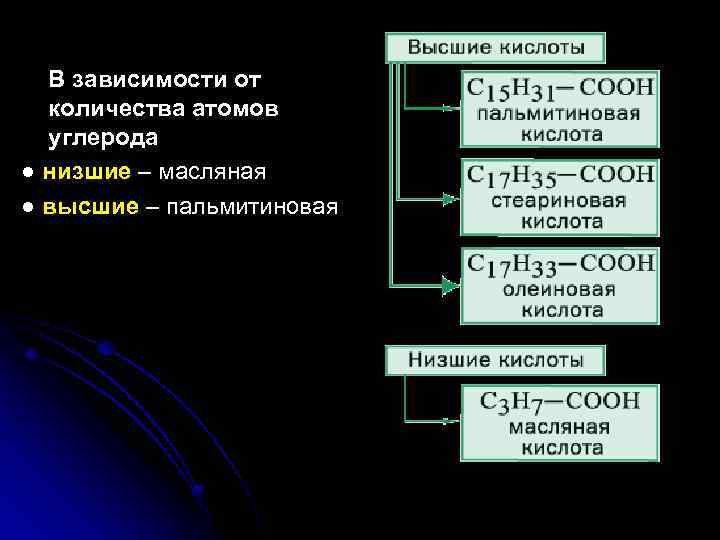 В зависимости от количества атомов углерода ● низшие – масляная ● высшие – пальмитиновая
В зависимости от количества атомов углерода ● низшие – масляная ● высшие – пальмитиновая
 Номенклатура Распространены тривиальные названия. CH 3 COOH – уксусная кислота – По правилам IUPAC к названию углеводорода добавляют "- овая кислота". добавляют "- CH 3 COOH – этановая кислота
Номенклатура Распространены тривиальные названия. CH 3 COOH – уксусная кислота – По правилам IUPAC к названию углеводорода добавляют "- овая кислота". добавляют "- CH 3 COOH – этановая кислота
 Примеры кислот № Формула кислоты Название кислоты Название соли 1 HCOOH Метановая Муравьиная Формиат 2 CH 3 COOH Этановая 3 C 2 H 5 COOH Пропановая Пропионовая Пропионат 4 C 3 H 7 COOH Бутановая Масляная Бутират 5 C 4 H 9 COOH Пентановая Валериановая Валериат 6 C 5 H 11 COOH Гексановая Капроновая Капронат 7 C 6 H 13 COOH Гептановая Энантовая Энтинат 8 C 7 H 15 COOH Октановая Каприловая Каприлат 9 C 8 H 17 COOH Нонановая Пеларгоновая Пеларгонат 10 C 9 H 19 COOH Декановая Каприновая Капринат Уксусная Ацетат
Примеры кислот № Формула кислоты Название кислоты Название соли 1 HCOOH Метановая Муравьиная Формиат 2 CH 3 COOH Этановая 3 C 2 H 5 COOH Пропановая Пропионовая Пропионат 4 C 3 H 7 COOH Бутановая Масляная Бутират 5 C 4 H 9 COOH Пентановая Валериановая Валериат 6 C 5 H 11 COOH Гексановая Капроновая Капронат 7 C 6 H 13 COOH Гептановая Энантовая Энтинат 8 C 7 H 15 COOH Октановая Каприловая Каприлат 9 C 8 H 17 COOH Нонановая Пеларгоновая Пеларгонат 10 C 9 H 19 COOH Декановая Каприновая Капринат Уксусная Ацетат
 Изомерия 1. Изомерия углеродной цепи. 2. Изомерия положения кратной связи, например: СН 2=СН—СН 2—СООН Бутен-3 -овая кислота (винилуксусная кислота) СН 3—СН=СН—СООН Бутен-2 -овая кислота (кротоновая кислота) 3. Цис-, транс-изомерия, например: 4. Межклассовая изомерия: например: С 4 Н 8 О 2 СН 3 — СН 2— СО — СНз метиловый эфир пропановой кислоты СН 3 — СО — CH 2— СН 3 этиловый эфир этановой кислоты С 3 Н 7 – СООН бутановая кислота
Изомерия 1. Изомерия углеродной цепи. 2. Изомерия положения кратной связи, например: СН 2=СН—СН 2—СООН Бутен-3 -овая кислота (винилуксусная кислота) СН 3—СН=СН—СООН Бутен-2 -овая кислота (кротоновая кислота) 3. Цис-, транс-изомерия, например: 4. Межклассовая изомерия: например: С 4 Н 8 О 2 СН 3 — СН 2— СО — СНз метиловый эфир пропановой кислоты СН 3 — СО — CH 2— СН 3 этиловый эфир этановой кислоты С 3 Н 7 – СООН бутановая кислота
 Строение карбоксильной группы l l l Карбоксильная группа СООН состоит из карбонильной группы С=О и гидроксильной группы ОН. В группе СО атом углерода несет частичный положительный заряд и притягивает к себе электронную пару атома кислорода в группе ОН. При этом электронная плотность на атоме кислорода уменьшается, и связь О-Н ослабляется: В свою очередь, группа ОН "гасит" положительный заряд на группе СО.
Строение карбоксильной группы l l l Карбоксильная группа СООН состоит из карбонильной группы С=О и гидроксильной группы ОН. В группе СО атом углерода несет частичный положительный заряд и притягивает к себе электронную пару атома кислорода в группе ОН. При этом электронная плотность на атоме кислорода уменьшается, и связь О-Н ослабляется: В свою очередь, группа ОН "гасит" положительный заряд на группе СО.
 химические свойства Наиболее важные химические свойства, характерные для большинства карбоновых кислот: 1) Взаимодействие с активными металлами: 2 CH 3 COOH + Mg (CH 2 COO)2 Mg + H 2 2) Взаимодействие с оксидами металлов: 2 СН 3 СООН + Са. О (СН 3 СОО)2 Са + Н 2 О
химические свойства Наиболее важные химические свойства, характерные для большинства карбоновых кислот: 1) Взаимодействие с активными металлами: 2 CH 3 COOH + Mg (CH 2 COO)2 Mg + H 2 2) Взаимодействие с оксидами металлов: 2 СН 3 СООН + Са. О (СН 3 СОО)2 Са + Н 2 О
 3) Взаимодействие с основаниями: CH 3 COOH + Na. OH CH 3 COONa + H 2 O 4) Взаимодействие с солями: CH 3 COOH + Na. HCO 3 CH 3 COONa + СО 2 + Н 2 О 5) Взаимодействие со спиртами (реакция этерификации): CH 3 COOH + СН 3 СН 2 ОН CH 3 COOСН 2 СН 3 + H 2 O 6) Взаимодействие с аммиаком: CH 3 COOH + NH 3 CH 3 COONH 4 При нагревании аммонийных солей карбоновых кислот образуются их амиды: CH 3 COONH 4 CH 3 CONH 2 + H 2 O 7) Под действием SОCl 2 карбоновые кислоты превращаются в соответствующие хлорангидриды. CH 3 COOH + SОCl 2 CH 3 COCl + HCl + SO 2
3) Взаимодействие с основаниями: CH 3 COOH + Na. OH CH 3 COONa + H 2 O 4) Взаимодействие с солями: CH 3 COOH + Na. HCO 3 CH 3 COONa + СО 2 + Н 2 О 5) Взаимодействие со спиртами (реакция этерификации): CH 3 COOH + СН 3 СН 2 ОН CH 3 COOСН 2 СН 3 + H 2 O 6) Взаимодействие с аммиаком: CH 3 COOH + NH 3 CH 3 COONH 4 При нагревании аммонийных солей карбоновых кислот образуются их амиды: CH 3 COONH 4 CH 3 CONH 2 + H 2 O 7) Под действием SОCl 2 карбоновые кислоты превращаются в соответствующие хлорангидриды. CH 3 COOH + SОCl 2 CH 3 COCl + HCl + SO 2
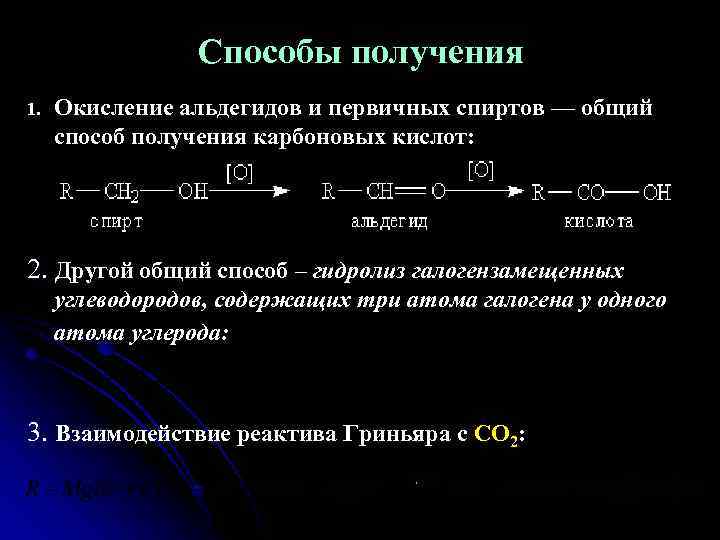 Способы получения 1. Окисление альдегидов и первичных спиртов — общий способ получения карбоновых кислот: 2. Другой общий способ ‒ гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода: -3 Na. Cl 3. Взаимодействие реактива Гриньяра с СО 2:
Способы получения 1. Окисление альдегидов и первичных спиртов — общий способ получения карбоновых кислот: 2. Другой общий способ ‒ гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода: -3 Na. Cl 3. Взаимодействие реактива Гриньяра с СО 2:
 4. Гидролиз сложных эфиров: 5. Гидролиз ангидридов кислот:
4. Гидролиз сложных эфиров: 5. Гидролиз ангидридов кислот:
 Муравьиная кислота – НСООН, жидкость с резким запахом. Содержится в хвое, крапиве, едких выделениях муравьев и пчел. Применяется, как консервант, в медицине для лечения ревматических болей радикулитов.
Муравьиная кислота – НСООН, жидкость с резким запахом. Содержится в хвое, крапиве, едких выделениях муравьев и пчел. Применяется, как консервант, в медицине для лечения ревматических болей радикулитов.
 Уксусная кислота – CH 3 COOH известна с глубокой древности как продукт скисания вина на воздухе или под действием ферментов. Из всех карбоновых кислот уксусная имеет наибольшее применение в промышленности. Используют для получения искусственных волокон и пластмасс на основе целлюлозы, применяют в производстве красителей, медикаментов, ядохимикатов, органического стекла.
Уксусная кислота – CH 3 COOH известна с глубокой древности как продукт скисания вина на воздухе или под действием ферментов. Из всех карбоновых кислот уксусная имеет наибольшее применение в промышленности. Используют для получения искусственных волокон и пластмасс на основе целлюлозы, применяют в производстве красителей, медикаментов, ядохимикатов, органического стекла.
 Масляная кислота СН 3 СН 2 СООН сообщает прогорклому маслу его типичный запах, её эфиры содержатся в коровьем масле и нефти. Эфиры масляной кислоты применяют как душистые вещества, пластификаторы, эмульгаторы.
Масляная кислота СН 3 СН 2 СООН сообщает прогорклому маслу его типичный запах, её эфиры содержатся в коровьем масле и нефти. Эфиры масляной кислоты применяют как душистые вещества, пластификаторы, эмульгаторы.
 Валериановая кислота Среди изомеров валериановой кислоты наибольшее значение имеет 3 метилбутановая кислота (изовалериановая кислота) СН 3 СH(СН 3) СН 2 СООН, которую получают из валерианового корня или синтетически. Она применяется для синтеза лекарственных веществ: валидола, бромурала и др. В пищевой промышленности используют изоамиловый эфир изовалериановой кислоты (яблочная эссенция).
Валериановая кислота Среди изомеров валериановой кислоты наибольшее значение имеет 3 метилбутановая кислота (изовалериановая кислота) СН 3 СH(СН 3) СН 2 СООН, которую получают из валерианового корня или синтетически. Она применяется для синтеза лекарственных веществ: валидола, бромурала и др. В пищевой промышленности используют изоамиловый эфир изовалериановой кислоты (яблочная эссенция).
 Капроновая кислота CH 3(CH 2)4 COOH входит в состав козьего жира (от латинского «caper» ‒ коза). Это бесцветная маслянистая жидкость с неприятным запахом. В природе капроновая кислота находится в различных животных жирах. Многие эфиры капроновой кислоты обладают фруктовым запахом и применяются в качестве эссенций.
Капроновая кислота CH 3(CH 2)4 COOH входит в состав козьего жира (от латинского «caper» ‒ коза). Это бесцветная маслянистая жидкость с неприятным запахом. В природе капроновая кислота находится в различных животных жирах. Многие эфиры капроновой кислоты обладают фруктовым запахом и применяются в качестве эссенций.
 Винная кислота Называется так потому, что была выделена из так называемого винного камня. Помимо винограда виннокаменная кислота содержится во многих фруктах. Также используется при изготовлении лимонадов, печенья, и при окрашивании тканей.
Винная кислота Называется так потому, что была выделена из так называемого винного камня. Помимо винограда виннокаменная кислота содержится во многих фруктах. Также используется при изготовлении лимонадов, печенья, и при окрашивании тканей.
 Щавелевая кислота НООС―СООН Бесцветное вещество в виде кристаллов. Содержится в щавеле, ревене, шпинате, клевере и помидорах. Применяется в текстильной промышленности, органическом синтезе, для отчистки металлов от ржавчины и накипи.
Щавелевая кислота НООС―СООН Бесцветное вещество в виде кристаллов. Содержится в щавеле, ревене, шпинате, клевере и помидорах. Применяется в текстильной промышленности, органическом синтезе, для отчистки металлов от ржавчины и накипи.
 Лимонная кислота Впервые лимонная кислот была выделена в 1784 году из сока недозрелых лимонов шведским аптекарем Карлом Шееле. Лимонная кислота содержится не только в лимонах, но и в землянике, смородине, ананасах и других фруктах. Чаще всего ее используют как вкусовое вещество в кондитерских изделиях и напитках.
Лимонная кислота Впервые лимонная кислот была выделена в 1784 году из сока недозрелых лимонов шведским аптекарем Карлом Шееле. Лимонная кислота содержится не только в лимонах, но и в землянике, смородине, ананасах и других фруктах. Чаще всего ее используют как вкусовое вещество в кондитерских изделиях и напитках.
 Молочная кислота CH 3―CHOH―COOH Содержится в квашеной капусте, соленых огурцах, образуется при созревании сыра. Она есть везде, где есть сахар. Молочную кислоту применяют в текстильном производстве и кожевенной промышленности, ветеринарии, кондитерской промышленности. Молочная кислота – консервант, т. е. ее добавка предохраняет продукты от порчи.
Молочная кислота CH 3―CHOH―COOH Содержится в квашеной капусте, соленых огурцах, образуется при созревании сыра. Она есть везде, где есть сахар. Молочную кислоту применяют в текстильном производстве и кожевенной промышленности, ветеринарии, кондитерской промышленности. Молочная кислота – консервант, т. е. ее добавка предохраняет продукты от порчи.
 Янтарная кислота Впервые получена в XVII веке перегонкой янтаря. Содержится в недозрелых фруктах и буром угле. Используется, как лекарственное средство, для получения пластмасс, смол, в пищевой промышленности используется в качестве пищевой добавки E 363.
Янтарная кислота Впервые получена в XVII веке перегонкой янтаря. Содержится в недозрелых фруктах и буром угле. Используется, как лекарственное средство, для получения пластмасс, смол, в пищевой промышленности используется в качестве пищевой добавки E 363.
 Стеариновая и пальмитиновая кислоты Стеариновая кислота была открыта в свином сале в 1816 году французским химиком Шеврелем. Стеариновая кислота является одной из наиболее распространённых в природе высших жирных кислот. Стеариновая кислота — главная составная часть многих жиров и масел, из которых её выделяют гидролизом. Соли стеариновой кислоты — составная часть мыл. Пальмитиновую кислоту получают омылением жиров или окислением парафинов. Используют в производстве стеарина (смесь со стеариновой кислотой), моющих и косметических средств, смазочных масел и пластификаторов. Пальмитат кальция используют в качестве компонента составов для гидрофобизации тканей, кожи, дерева, эмульгатора в косметических препаратах.
Стеариновая и пальмитиновая кислоты Стеариновая кислота была открыта в свином сале в 1816 году французским химиком Шеврелем. Стеариновая кислота является одной из наиболее распространённых в природе высших жирных кислот. Стеариновая кислота — главная составная часть многих жиров и масел, из которых её выделяют гидролизом. Соли стеариновой кислоты — составная часть мыл. Пальмитиновую кислоту получают омылением жиров или окислением парафинов. Используют в производстве стеарина (смесь со стеариновой кислотой), моющих и косметических средств, смазочных масел и пластификаторов. Пальмитат кальция используют в качестве компонента составов для гидрофобизации тканей, кожи, дерева, эмульгатора в косметических препаратах.
 Бензойная кислота В промышленных масштабах бензойную кислоту получают окислением толуола. Применяют в медицине при кожных заболеваниях как наружное антисептическое и противогрибковое средства, а её натриевую соль – как отхаркивающее средство. Кроме того, бензойную кислоту и её соли используют при консервировании пищевых продуктов (пищевые добавки E 210, E 211, E 212, E 213). Эфиры бензойной кислоты (от метилового до амилового) обладают сильным запахом и применяются в парфюмерной промышленности. Некоторые другие производные бензойной кислоты, широко применяются для синтеза красителей.
Бензойная кислота В промышленных масштабах бензойную кислоту получают окислением толуола. Применяют в медицине при кожных заболеваниях как наружное антисептическое и противогрибковое средства, а её натриевую соль – как отхаркивающее средство. Кроме того, бензойную кислоту и её соли используют при консервировании пищевых продуктов (пищевые добавки E 210, E 211, E 212, E 213). Эфиры бензойной кислоты (от метилового до амилового) обладают сильным запахом и применяются в парфюмерной промышленности. Некоторые другие производные бензойной кислоты, широко применяются для синтеза красителей.
 Аскорбиновая кислота является одним из самых ценных веществ, содержащихся в плодах. Одним из наиболее необходимых веществ для устойчивости организма к простудным заболеваниям. Аскорбиновая кислота влияет на образование соединительной ткани, красных кровяных телец, она ускоряет всасывание железа и предохраняет другие витамины от окисления.
Аскорбиновая кислота является одним из самых ценных веществ, содержащихся в плодах. Одним из наиболее необходимых веществ для устойчивости организма к простудным заболеваниям. Аскорбиновая кислота влияет на образование соединительной ткани, красных кровяных телец, она ускоряет всасывание железа и предохраняет другие витамины от окисления.


