СПИРТИ.pptx
- Количество слайдов: 56
 Спирти. Хімічні властивості спиртів. Використання спиртів. Отруйність спиртів, їх шкідливий вплив на організм людини.
Спирти. Хімічні властивості спиртів. Використання спиртів. Отруйність спиртів, їх шкідливий вплив на організм людини.
 Мета: Вивчити хімічні властивості одноатомних та багатоатомних спиртів; § Порівняти хімічні властивості одноатомних та багатоатомних спиртів; § Застосування спиртів у н/г; § Згубний вплив метанолу та етанолу на організм людини. §
Мета: Вивчити хімічні властивості одноатомних та багатоатомних спиртів; § Порівняти хімічні властивості одноатомних та багатоатомних спиртів; § Застосування спиртів у н/г; § Згубний вплив метанолу та етанолу на організм людини. §
 Оксигеновмісні органічні сполуки Органічні сполуки, що містять у своєму складі атоми Оксигену, називаються оксигеновмісними. Функціональні групи — це групи атомів, що визначають хімічні й фізичні властивості речовин. Наприклад: −OH — гідроксильна група; −COH — карбонільна; −COOH — карбоксильна.
Оксигеновмісні органічні сполуки Органічні сполуки, що містять у своєму складі атоми Оксигену, називаються оксигеновмісними. Функціональні групи — це групи атомів, що визначають хімічні й фізичні властивості речовин. Наприклад: −OH — гідроксильна група; −COH — карбонільна; −COOH — карбоксильна.
 Органічні речовини, молекули яких містять одну або кілька функціональних гідроксильних груп, з’єднаних з вуглеводнями, називаються спиртами. Загальна формула спиртів: R –(OH)n
Органічні речовини, молекули яких містять одну або кілька функціональних гідроксильних груп, з’єднаних з вуглеводнями, називаються спиртами. Загальна формула спиртів: R –(OH)n
 Класифікація спиртів За природою вуглеводневого радикала: • насичені; • ненасичені; • ароматичні. За кількістю гідроксильних груп: • одноатомні; • багатоатомні.
Класифікація спиртів За природою вуглеводневого радикала: • насичені; • ненасичені; • ароматичні. За кількістю гідроксильних груп: • одноатомні; • багатоатомні.
 Номенклатура спиртів Назви спиртів походять від назв відповідних вуглеводнів з додаванням суфікса -ол. Нумерацію карбонового скелета починають із того краю, ближче до якого знаходиться гідроксильна група. CH 3 − OH — метанол (метиловий спирт, мурашиний спирт); C 2 H 5 − OH — етанол (етиловий спирт); C 3 H 7 − OH — пропанол (пропіловий спирт)
Номенклатура спиртів Назви спиртів походять від назв відповідних вуглеводнів з додаванням суфікса -ол. Нумерацію карбонового скелета починають із того краю, ближче до якого знаходиться гідроксильна група. CH 3 − OH — метанол (метиловий спирт, мурашиний спирт); C 2 H 5 − OH — етанол (етиловий спирт); C 3 H 7 − OH — пропанол (пропіловий спирт)
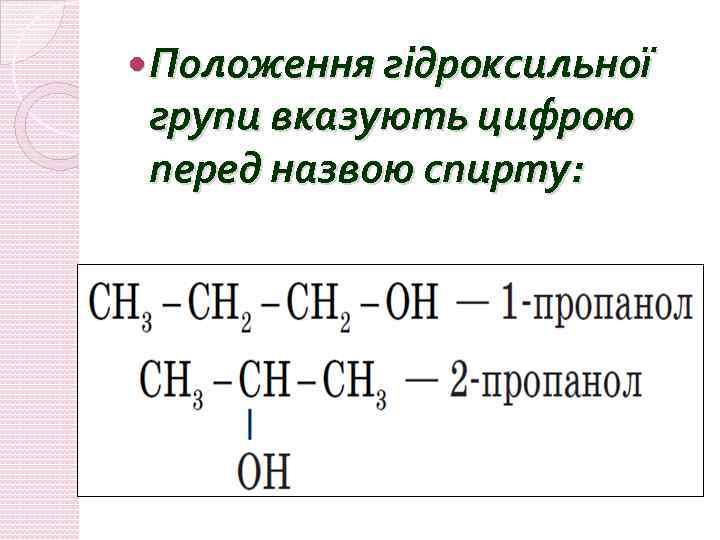 Положення гідроксильної групи вказують цифрою перед назвою спирту:
Положення гідроксильної групи вказують цифрою перед назвою спирту:
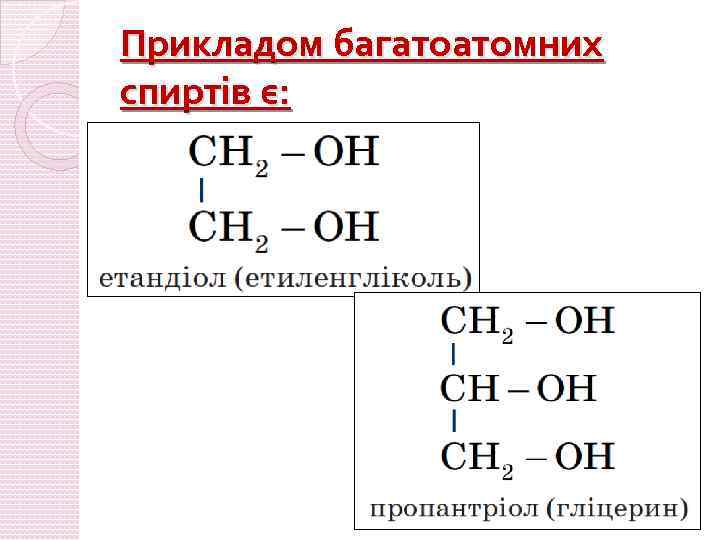 Прикладом багатоатомних спиртів є:
Прикладом багатоатомних спиртів є:
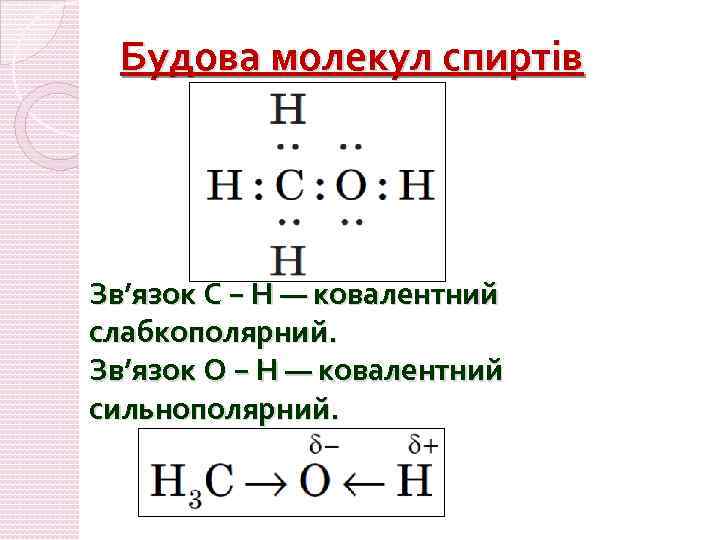 Будова молекул спиртів Зв’язок C − H — ковалентний слабкополярний. Зв’язок O − H — ковалентний сильнополярний.
Будова молекул спиртів Зв’язок C − H — ковалентний слабкополярний. Зв’язок O − H — ковалентний сильнополярний.
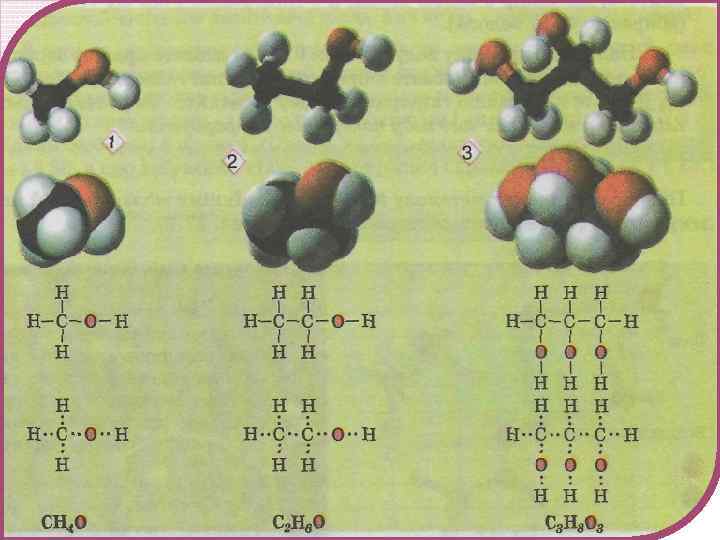
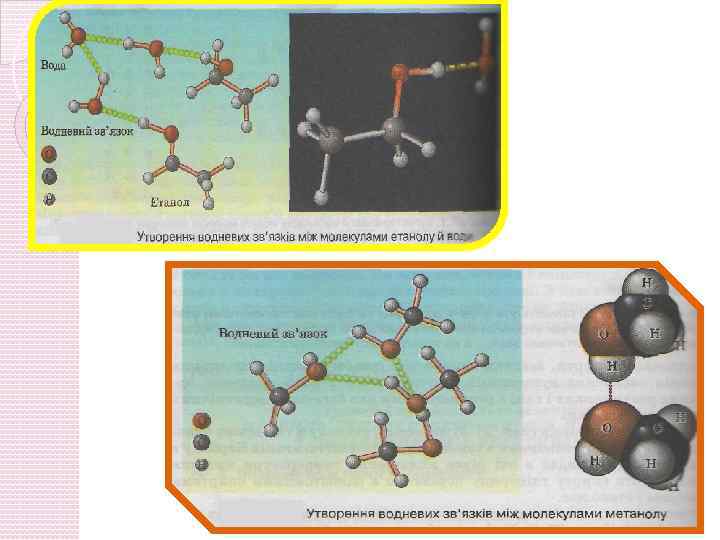
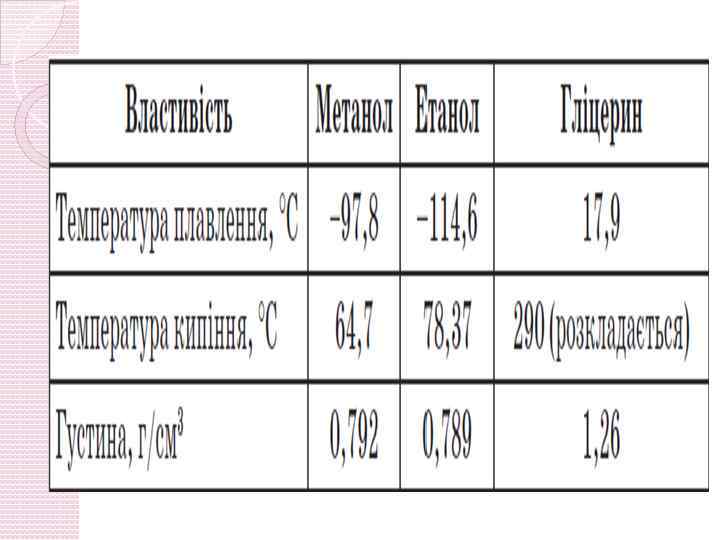
 Фізичні властивості спиртів Метанол — рідина без кольору, з різким запахом, добре розчинна у воді в будь-яких співвідношеннях, отруйна. Етанол — рідина без кольору, з різким запахом, добре розчинна у воді в будьяких співвідношеннях, отруйна. Гліцерин — грузла рідина без кольору й запаху, солодка на смак, добре розчинна у воді.
Фізичні властивості спиртів Метанол — рідина без кольору, з різким запахом, добре розчинна у воді в будь-яких співвідношеннях, отруйна. Етанол — рідина без кольору, з різким запахом, добре розчинна у воді в будьяких співвідношеннях, отруйна. Гліцерин — грузла рідина без кольору й запаху, солодка на смак, добре розчинна у воді.
 Хімічні властивості спиртів Спирти — нейтральні речовини, незважаючи на наявність гідроксильної групи, спирти не змінюють забарвлення індикаторів, не вступають у хімічні реакції з водними розчинами лугів і розведених кислот. Лабораторні спиртівки заповнюють 98%-м спиртом. Який висновок можна зробити про горючість спиртів?
Хімічні властивості спиртів Спирти — нейтральні речовини, незважаючи на наявність гідроксильної групи, спирти не змінюють забарвлення індикаторів, не вступають у хімічні реакції з водними розчинами лугів і розведених кислот. Лабораторні спиртівки заповнюють 98%-м спиртом. Який висновок можна зробити про горючість спиртів?
 1. Реакції горіння. 2 СН 3 ОН + 3 О 2 → 2 СО 2 ↑+ 4 Н 2 О 2 С 2 Н 5 ОН + 6 О 2 → 4 СО 2 ↑ + 6 Н 2 О С 4 Н 9 ОН + 4 О 2 → 4 СО↑ + 5 Н 2 О С 6 Н 13 ОН + 3 О 2 → 6 С + 7 Н 2 О
1. Реакції горіння. 2 СН 3 ОН + 3 О 2 → 2 СО 2 ↑+ 4 Н 2 О 2 С 2 Н 5 ОН + 6 О 2 → 4 СО 2 ↑ + 6 Н 2 О С 4 Н 9 ОН + 4 О 2 → 4 СО↑ + 5 Н 2 О С 6 Н 13 ОН + 3 О 2 → 6 С + 7 Н 2 О
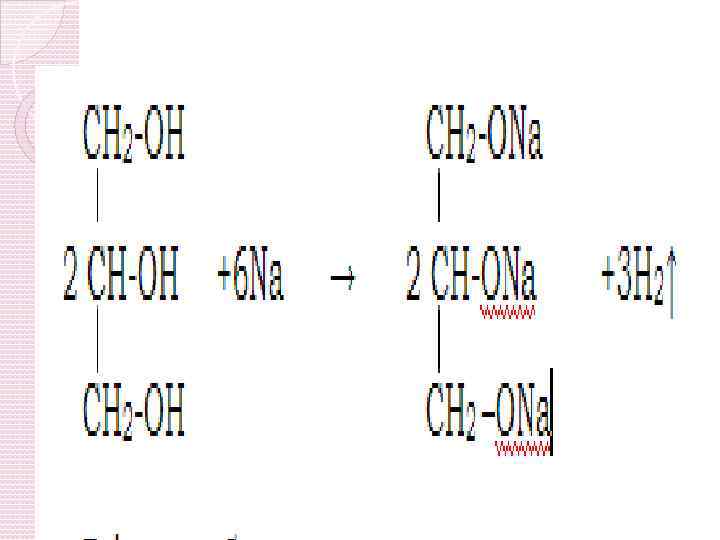
 2. Взаємодія спиртів з лужними металами Зсув електронної густини в молекулі спирту спричиняє рухливість атома Гідрогену в гідроксильній групі, тому цей атом Гідрогену може заміщатися металевим натрієм. Складаємо рівняння хімічних реакцій. 2 СН 3 ОН + 2 Na → 2 СН 3 ОNa + Н 2↑ 2 С 2 Н 5 ОН + 2 Na → 2 С 2 Н 5 ОNa+ Н 2↑ 2 С 4 Н 9 ОН + 2 Na → 2 С 4 Н 9 ОNa + Н 2↑ С 2 Н 5 ONа+ Н 2 О → С 2 Н 5 ОН+Nа. ОН
2. Взаємодія спиртів з лужними металами Зсув електронної густини в молекулі спирту спричиняє рухливість атома Гідрогену в гідроксильній групі, тому цей атом Гідрогену може заміщатися металевим натрієм. Складаємо рівняння хімічних реакцій. 2 СН 3 ОН + 2 Na → 2 СН 3 ОNa + Н 2↑ 2 С 2 Н 5 ОН + 2 Na → 2 С 2 Н 5 ОNa+ Н 2↑ 2 С 4 Н 9 ОН + 2 Na → 2 С 4 Н 9 ОNa + Н 2↑ С 2 Н 5 ONа+ Н 2 О → С 2 Н 5 ОН+Nа. ОН
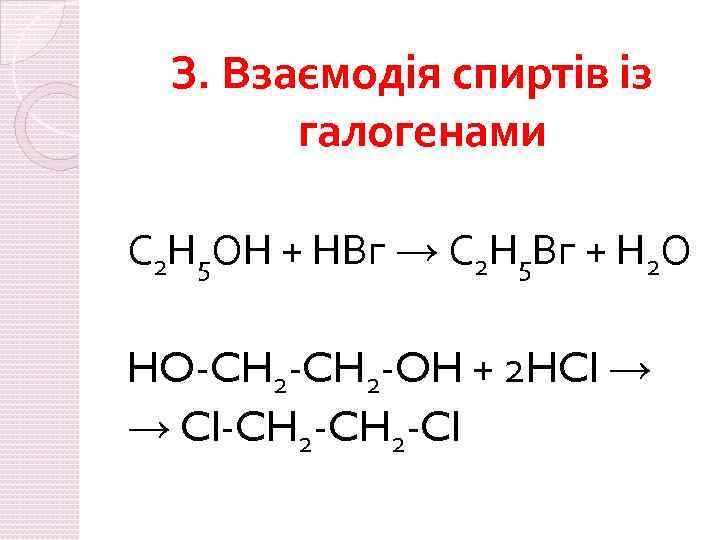 З. Взаємодія спиртів із галогенами С 2 Н 5 ОН + НВг → С 2 Н 5 Вг + Н 2 О HO-CH 2 -OH + 2 HCl → → Cl-CH 2 -Cl
З. Взаємодія спиртів із галогенами С 2 Н 5 ОН + НВг → С 2 Н 5 Вг + Н 2 О HO-CH 2 -OH + 2 HCl → → Cl-CH 2 -Cl
 3. Дегідратація спиртів Дегідратація — відщеплення води, відбувається під дією концентрованої сульфатної кислоти. 3. 1. За температури понад 140°С протікає внутрішньомолекулярна дегідратація з утворенням подвійного зв’язку: С 2 Н 5 ОН → СН 2 = СН 2 + Н 2 О етен
3. Дегідратація спиртів Дегідратація — відщеплення води, відбувається під дією концентрованої сульфатної кислоти. 3. 1. За температури понад 140°С протікає внутрішньомолекулярна дегідратація з утворенням подвійного зв’язку: С 2 Н 5 ОН → СН 2 = СН 2 + Н 2 О етен
 3. 2. За температури менш ніж 140°С протікає міжмолекулярна дегідратація з утворенням етерів: С 2 Н 5 ОН + С 2 Н 5 ОН → С 2 Н 5 -О-С 2 Н 5 + Н 2 О диметиловий етер 3. 3. Дегідратація за методом Лебедєва. 2 С 2 Н 5 ОН → СН 2 = СН - СН = СН 2 + 2 Н 2 О + Н 2 бутадієн
3. 2. За температури менш ніж 140°С протікає міжмолекулярна дегідратація з утворенням етерів: С 2 Н 5 ОН + С 2 Н 5 ОН → С 2 Н 5 -О-С 2 Н 5 + Н 2 О диметиловий етер 3. 3. Дегідратація за методом Лебедєва. 2 С 2 Н 5 ОН → СН 2 = СН - СН = СН 2 + 2 Н 2 О + Н 2 бутадієн
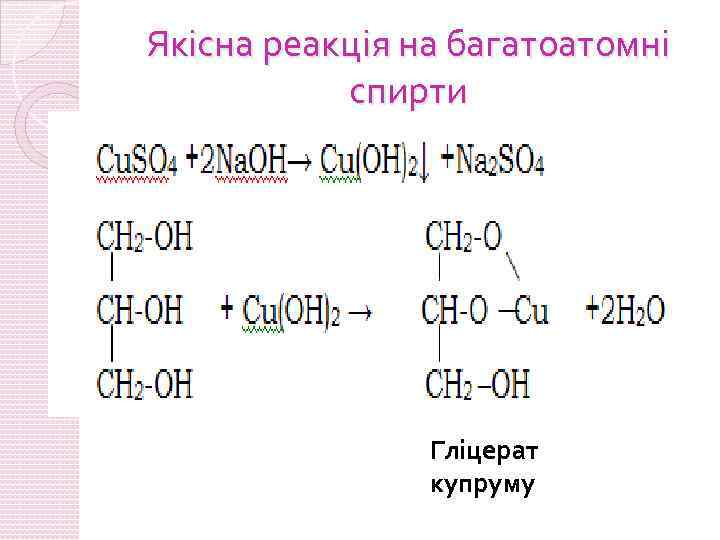 Якісна реакція на багатоатомні спирти Гліцерат купруму
Якісна реакція на багатоатомні спирти Гліцерат купруму
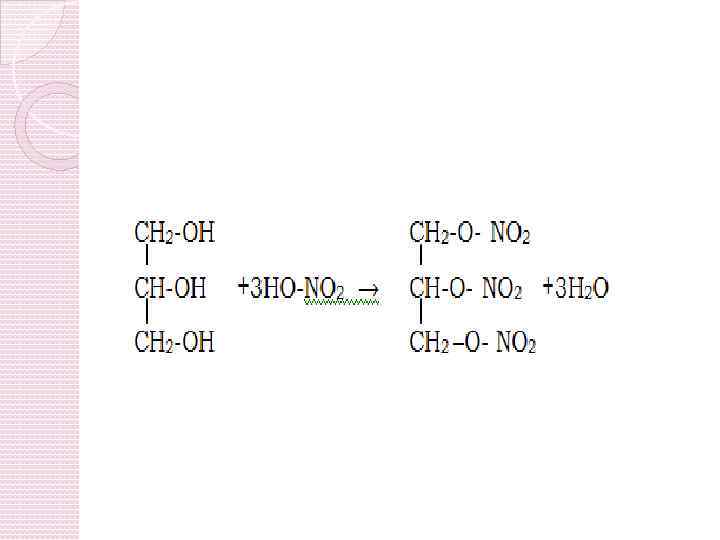
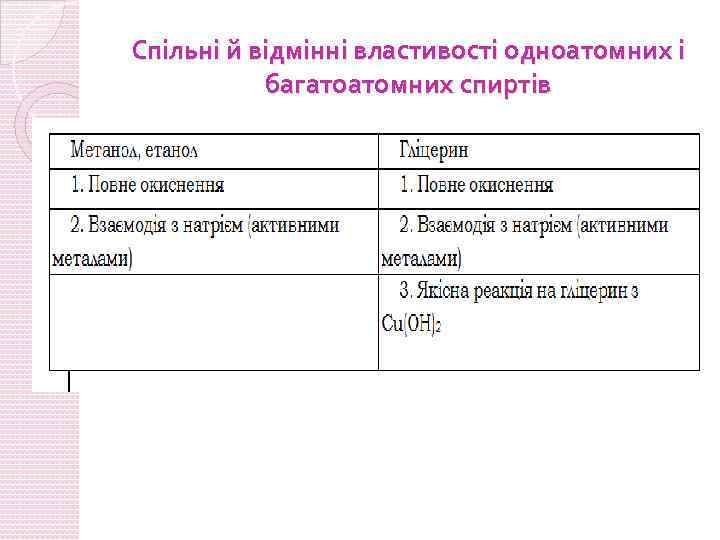 Спільні й відмінні властивості одноатомних і багатоатомних спиртів
Спільні й відмінні властивості одноатомних і багатоатомних спиртів
 Самостійна робота. ВаріантІ Спиртами називають органічні речовини, які мають у своєму складі группу –… Функціональна група, це група атомів, які … Якщо алкан називається етаном, то відповідний йому спирт називається … За числом гідроксильних груп спирти діляться на … За нормальних умов найпростіший спирт перебуває в … агрегатному стані. Одноатомний спирт з одним атомом карбону називається … За числом гідроксильних груп гліцерил належить до … Температура кипіння гліцерилу порівняно з метанолом набагато … При взаємодії етанолу з натрієм утворюється … Варіант ІІ Функціональна група спиртів – це … Якщо алкан називається метаном, то відповідний йому спирт називається … Етиловий спирт за числом гідроксильних груп належить до … Загальна формула одноатомних спиртів … Метанол, на відміну від метану, є рідиною завдяки утворенню … За звичайних умов етанол перебуває в … агрегатному стані. До трьохатомних спиртів належить … В’язкість гліцерину порівняно з етанолом набагато … При взаємодії гліцерину з натрієм утворюється …
Самостійна робота. ВаріантІ Спиртами називають органічні речовини, які мають у своєму складі группу –… Функціональна група, це група атомів, які … Якщо алкан називається етаном, то відповідний йому спирт називається … За числом гідроксильних груп спирти діляться на … За нормальних умов найпростіший спирт перебуває в … агрегатному стані. Одноатомний спирт з одним атомом карбону називається … За числом гідроксильних груп гліцерил належить до … Температура кипіння гліцерилу порівняно з метанолом набагато … При взаємодії етанолу з натрієм утворюється … Варіант ІІ Функціональна група спиртів – це … Якщо алкан називається метаном, то відповідний йому спирт називається … Етиловий спирт за числом гідроксильних груп належить до … Загальна формула одноатомних спиртів … Метанол, на відміну від метану, є рідиною завдяки утворенню … За звичайних умов етанол перебуває в … агрегатному стані. До трьохатомних спиртів належить … В’язкість гліцерину порівняно з етанолом набагато … При взаємодії гліцерину з натрієм утворюється …
 Застосування метанолу, глiцерину. Отруйність спиртів, їх згубна дія на організм людини.
Застосування метанолу, глiцерину. Отруйність спиртів, їх згубна дія на організм людини.
 Де застосовують етанол? Дезинфікуючий засіб .
Де застосовують етанол? Дезинфікуючий засіб .
 Для виготовлення екстрактів рослин, спиртових настоянок.
Для виготовлення екстрактів рослин, спиртових настоянок.
 Як пальне для міського транспорту ( у Бразилії)
Як пальне для міського транспорту ( у Бразилії)
 Як антифриз.
Як антифриз.
 Пальне для камінів
Пальне для камінів
 В лікеро-горілчаній промисловості
В лікеро-горілчаній промисловості
 Де застосовують гліцерин? Як консервант біо препаратів
Де застосовують гліцерин? Як консервант біо препаратів
 Додають в мило (добре зволожує шкіру)
Додають в мило (добре зволожує шкіру)
 Додають в зубні пасти, мазі, креми, гелі, засоби для миття посуду (запобігає висиханню шкіри).
Додають в зубні пасти, мазі, креми, гелі, засоби для миття посуду (запобігає висиханню шкіри).
 Нітрогліцерин – засіб від стенокардії
Нітрогліцерин – засіб від стенокардії
 Нітрогліцерин як вибухівка.
Нітрогліцерин як вибухівка.
 Використовують гліцерин у виробництві лікерів, шоколаду, морозива, желе.
Використовують гліцерин у виробництві лікерів, шоколаду, морозива, желе.
 Метанол – отруйна сполука !
Метанол – отруйна сполука !
 ВПЛИВ МЕТАНОЛУ Й ЕТАНОЛУ НА ОРГАНІЗМ ЛЮДИНИ
ВПЛИВ МЕТАНОЛУ Й ЕТАНОЛУ НА ОРГАНІЗМ ЛЮДИНИ
 Фізіологічна дія спиртів на організм людини негативна. Метиловий спирт СН 3 ОН – сильна отрута! У малих кількостях викликає сліпоту, у великих – спричиняє смерть. Етиловий спирт – наркотик. Під впливом етанолу у людини послаблюється увага, загальмовується реакція, порушується кореляція рухів. При тривалому вживанні викликає глибокі порушення нервової системи, захворювання серцево-судинної системи, травного тракту і зрештою настає важка хвороба – алкоголізм.
Фізіологічна дія спиртів на організм людини негативна. Метиловий спирт СН 3 ОН – сильна отрута! У малих кількостях викликає сліпоту, у великих – спричиняє смерть. Етиловий спирт – наркотик. Під впливом етанолу у людини послаблюється увага, загальмовується реакція, порушується кореляція рухів. При тривалому вживанні викликає глибокі порушення нервової системи, захворювання серцево-судинної системи, травного тракту і зрештою настає важка хвороба – алкоголізм.
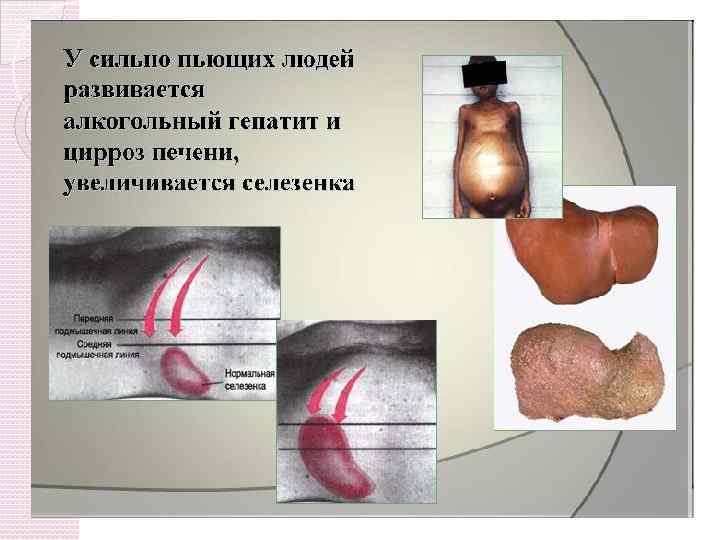
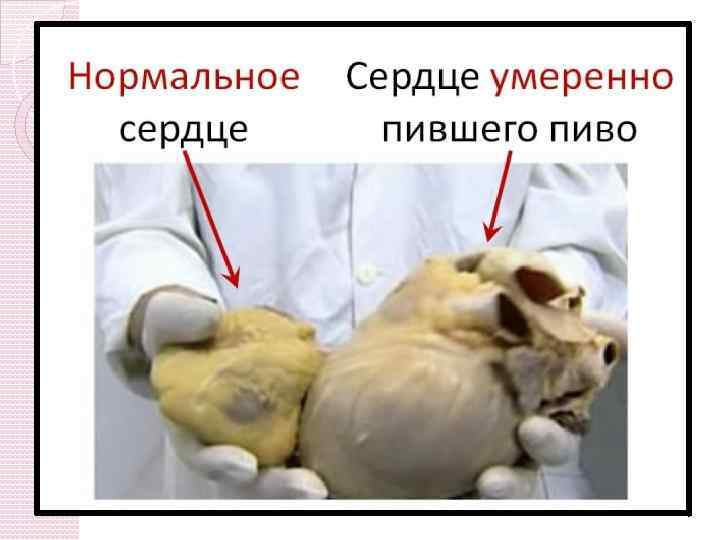
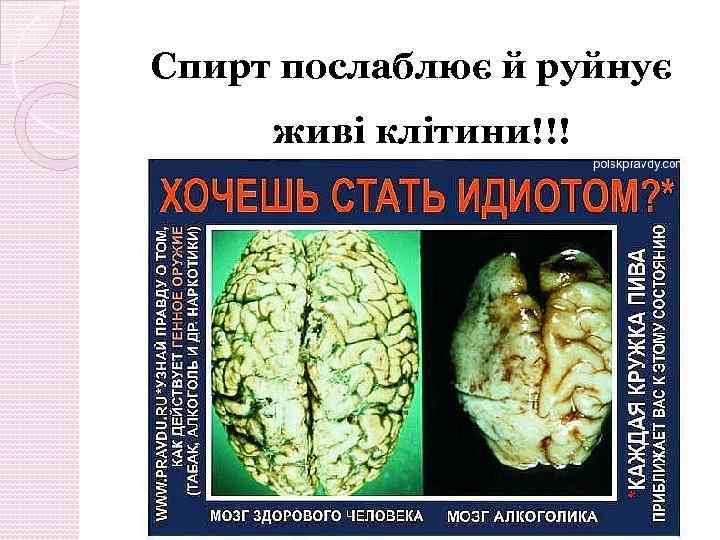 Спирт послаблює й руйнує живі клітини!!!
Спирт послаблює й руйнує живі клітини!!!
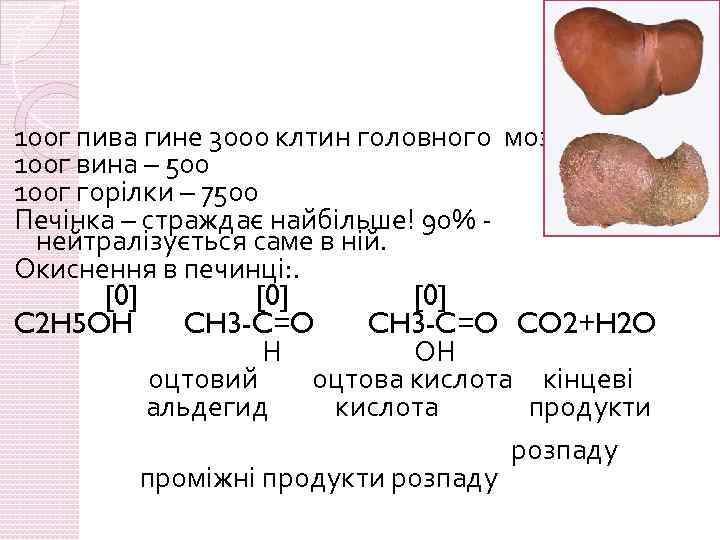 100 г пива гине 3000 клтин головного мозгу 100 г вина – 500 100 г горілки – 7500 Печінка – страждає найбільше! 90% - нейтралізується саме в ній. Окиснення в печинці: . [0] C 2 H 5 OH CH 3 -C=O CO 2+H 2 O Н ОН оцтовий оцтова кислота кінцеві альдегид кислота продукти розпаду проміжні продукти розпаду
100 г пива гине 3000 клтин головного мозгу 100 г вина – 500 100 г горілки – 7500 Печінка – страждає найбільше! 90% - нейтралізується саме в ній. Окиснення в печинці: . [0] C 2 H 5 OH CH 3 -C=O CO 2+H 2 O Н ОН оцтовий оцтова кислота кінцеві альдегид кислота продукти розпаду проміжні продукти розпаду
 З історії алкоголю: Про п'янкі властивості спиртних напоїв люди дізналися не менше ніж за 8000 років до н. е.
З історії алкоголю: Про п'янкі властивості спиртних напоїв люди дізналися не менше ніж за 8000 років до н. е.
 Чистий спирт почали одержувати у VI—VII століттях араби і назвали його «аль коголь» , що означає «одурманюючий» .
Чистий спирт почали одержувати у VI—VII століттях араби і назвали його «аль коголь» , що означає «одурманюючий» .
 У 1913 році в Україні продавалося 3, 4 літра спиртного на людину, а на прикінці 90 -х XXст. ця цифра зросла до 13, 2 літра.
У 1913 році в Україні продавалося 3, 4 літра спиртного на людину, а на прикінці 90 -х XXст. ця цифра зросла до 13, 2 літра.
 У стародавній Греції пити нерозведене водою вино вважалося негідним вільного громадянина.
У стародавній Греції пити нерозведене водою вино вважалося негідним вільного громадянина.
 За часів Петра І п’яницям , які потрапляли в тюрму, вішали важку чавунну медаль з надписом «За пияцтво!»
За часів Петра І п’яницям , які потрапляли в тюрму, вішали важку чавунну медаль з надписом «За пияцтво!»
 У 20 -х роках минулого століття в США було введено сухий закон, який відмінили в 1933 році. У 1985 році війну пияцтву було проголошено і в СРСР.
У 20 -х роках минулого століття в США було введено сухий закон, який відмінили в 1933 році. У 1985 році війну пияцтву було проголошено і в СРСР.
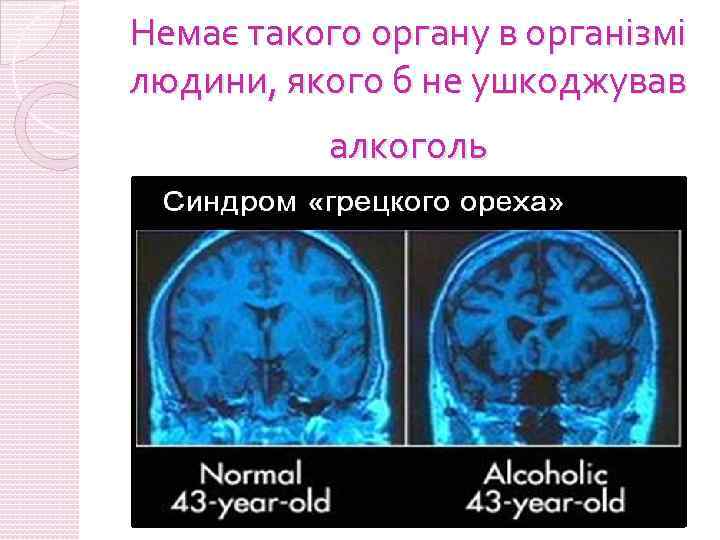 Немає такого органу в організмі людини, якого б не ушкоджував алкоголь
Немає такого органу в організмі людини, якого б не ушкоджував алкоголь

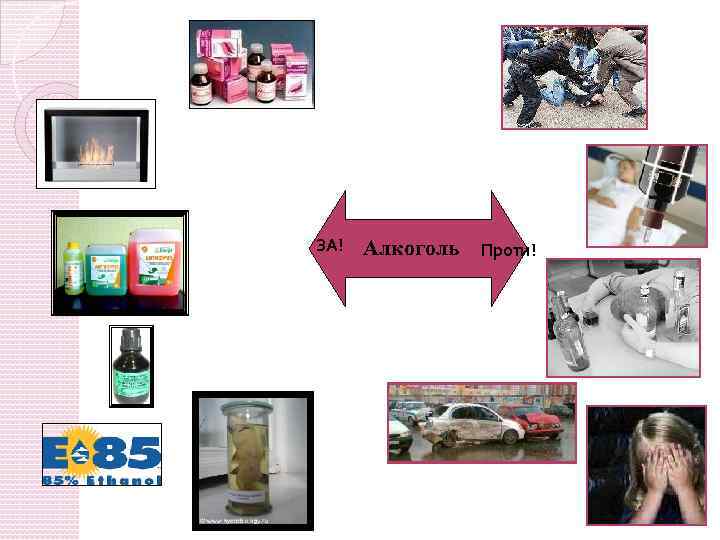 ЗА! Алкоголь Проти!
ЗА! Алкоголь Проти!

 Домашнє завдання: 1. Зобразіть структурні формули а) 1 -бутанолу, б) 2 -метил-1 -пропанолу. 2. Напишіть реакцію внутрішньомолекулярної дегідратації 1 -пропанолу. 3. Обчисліть масу етанолу, що повністю прореагувала з 5 моль металевого натрію. Читати & 27.
Домашнє завдання: 1. Зобразіть структурні формули а) 1 -бутанолу, б) 2 -метил-1 -пропанолу. 2. Напишіть реакцію внутрішньомолекулярної дегідратації 1 -пропанолу. 3. Обчисліть масу етанолу, що повністю прореагувала з 5 моль металевого натрію. Читати & 27.
 Задача Обчисліть об'єм водню, який виділиться в результаті взаємодії 46 г етанолу з надлишком металічного натрію. (11, 2 л)
Задача Обчисліть об'єм водню, який виділиться в результаті взаємодії 46 г етанолу з надлишком металічного натрію. (11, 2 л)


