спид Выполнили группа акушер-гинекологов КЛАССИФИКАЦИЯ ВИЧ-ИНФЕКЦИИ ПРЕДИСЛОВИЕ




































































































































































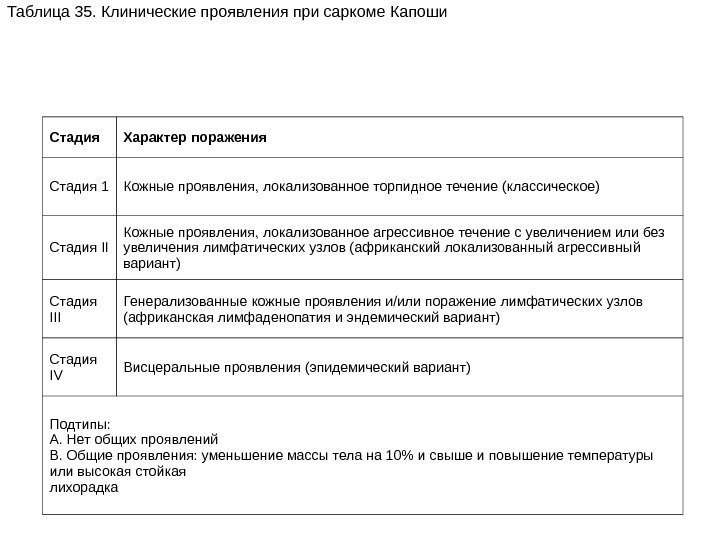

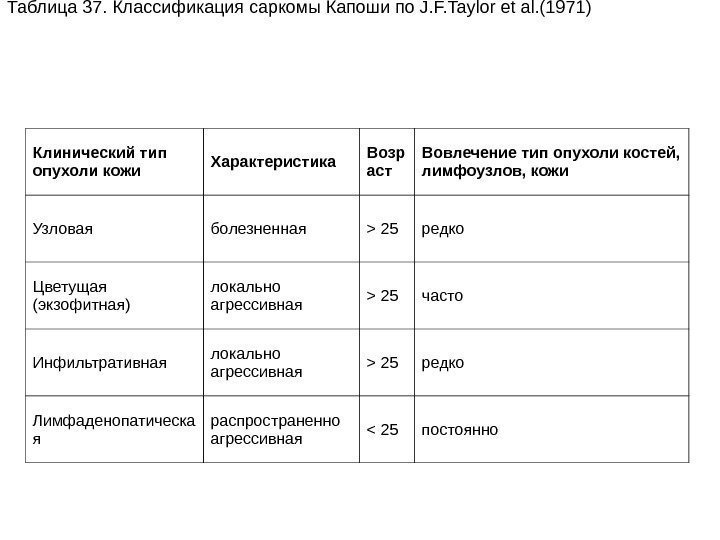



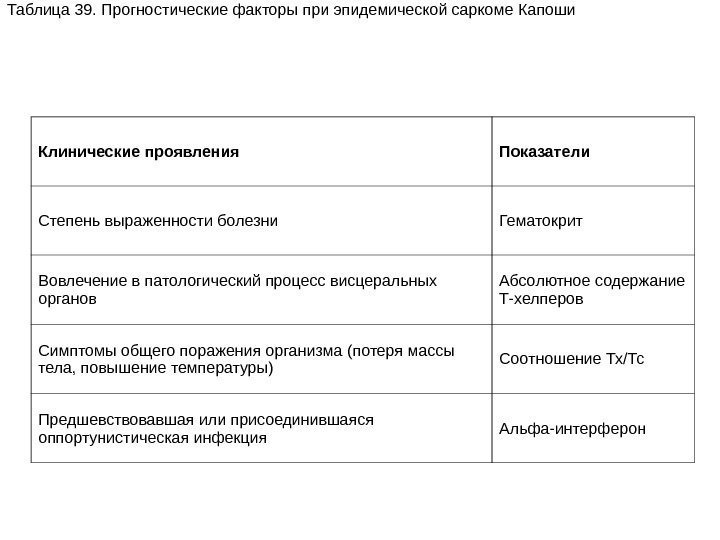
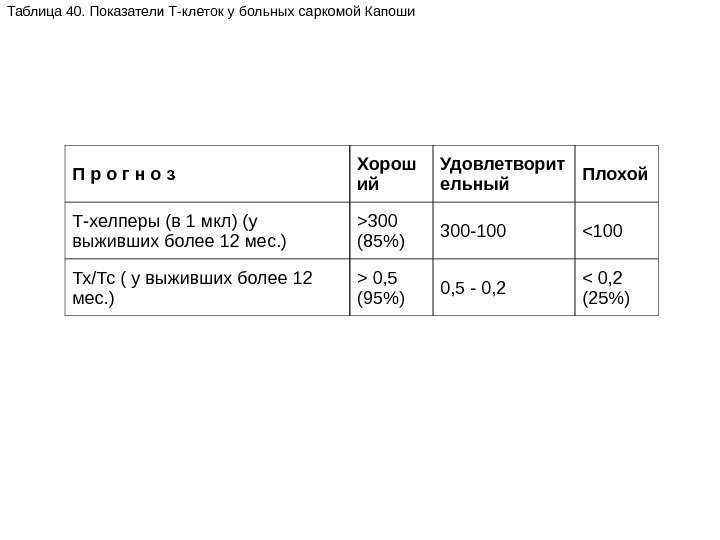

















































































































klassifikaciya_vich-infekcii.ppt
- Размер: 3.4 Мб
- Автор:
- Количество слайдов: 326
Описание презентации спид Выполнили группа акушер-гинекологов КЛАССИФИКАЦИЯ ВИЧ-ИНФЕКЦИИ ПРЕДИСЛОВИЕ по слайдам
 спид Выполнили группа акушер-гинекологов
спид Выполнили группа акушер-гинекологов
 КЛАССИФИКАЦИЯ ВИЧ-ИНФЕКЦИИ ПРЕДИСЛОВИЕ В 1982 году М. S. Gottlib ввел понятие Aquired Immune Deficienci Syndrom (AIDS) — синдром приобретенного иммунодефицита (СПИД), за год до того впервые с соавторами описавший новое заболевание. В этом же 1982 году определил группу СПИД-ассоциируемых оппортунистических инфекций, наличие которых позволяет диагностировать новую нозологическую форму патологии человека — СПИД. Тогда же СПИД окрестили болезнью четырех “Н” — по заглавным буквам английских слов — гомосексуалисты, больные гемофилией, гаитяне и героин, выделив этим самым группы риска для новой болезни.
КЛАССИФИКАЦИЯ ВИЧ-ИНФЕКЦИИ ПРЕДИСЛОВИЕ В 1982 году М. S. Gottlib ввел понятие Aquired Immune Deficienci Syndrom (AIDS) — синдром приобретенного иммунодефицита (СПИД), за год до того впервые с соавторами описавший новое заболевание. В этом же 1982 году определил группу СПИД-ассоциируемых оппортунистических инфекций, наличие которых позволяет диагностировать новую нозологическую форму патологии человека — СПИД. Тогда же СПИД окрестили болезнью четырех “Н” — по заглавным буквам английских слов — гомосексуалисты, больные гемофилией, гаитяне и героин, выделив этим самым группы риска для новой болезни.
 Пандемия ВИЧ-инфекции далеко вышла за рамки проблемы одной страны, одной специальности, одной медицины. В новый век мир войдет с проблемой ВИЧ-инфекции, инфекций, передающихся половым путем, нарастающего экологического стресса, обусловливающего иммуносупрессию и связанной с этим проблемами патологий, вызванных условнопатогенными возбудителями. Все большую роль будут играть заболевания, вызванные вирусами и прионами, мир будет вновь встречаться с возвращающимися инфекциями, а также инфекциями ранее неизвестными, но ВИЧ-инфекция будет довлеть как по объему поражения популяций, так и постепенно занимать лидирующее положение в причинах смерти, особенно людей молодого возраста. По самым оптимистическим прогнозам в период с 2002 по 2010 годы еще 45 млн. человек в 126 странах с низким и средним уровнем доходов будет инфицировано ВИЧ, если только мир не сможет осуществить кардинальные, широкомасштабные, глобальные профилактические мероприятия. Более 40% случаев инфицирования произойдет в Азии и странах Тихоокеанского региона (в котором уже сейчас отмечается около 20% всех новых случаев инфицирования в год).
Пандемия ВИЧ-инфекции далеко вышла за рамки проблемы одной страны, одной специальности, одной медицины. В новый век мир войдет с проблемой ВИЧ-инфекции, инфекций, передающихся половым путем, нарастающего экологического стресса, обусловливающего иммуносупрессию и связанной с этим проблемами патологий, вызванных условнопатогенными возбудителями. Все большую роль будут играть заболевания, вызванные вирусами и прионами, мир будет вновь встречаться с возвращающимися инфекциями, а также инфекциями ранее неизвестными, но ВИЧ-инфекция будет довлеть как по объему поражения популяций, так и постепенно занимать лидирующее положение в причинах смерти, особенно людей молодого возраста. По самым оптимистическим прогнозам в период с 2002 по 2010 годы еще 45 млн. человек в 126 странах с низким и средним уровнем доходов будет инфицировано ВИЧ, если только мир не сможет осуществить кардинальные, широкомасштабные, глобальные профилактические мероприятия. Более 40% случаев инфицирования произойдет в Азии и странах Тихоокеанского региона (в котором уже сейчас отмечается около 20% всех новых случаев инфицирования в год).
 По оценкам ВОЗ в 2003 г. зарегистрировано самое большое число зараженных ВИЧ и смертей от СПИДа по всему миру: за год зарегистрировано пять миллионов зараженных и три миллиона смертей. Болезнь по-прежнему наиболее распространена в Африке южнее Сахары, на этот регион приходятся три миллиона вновь нфицированных и 2, 3 миллиона смертей в 2003 году. Вызывает у ООН опасение новый пояс распространения болезни – Китай, Индонезия, Россия и восточно-европейские государства. Около 40 миллионов человек сейчас живут с ВИЧ, из которых 26, 6 миллионов живут в южной части африканского континента. В Китае, где эпидемия находится в самом начале, 1, 5 миллиона инфицированных, число инфицированных последние три года увеличивается на 30% в год. В некоторых частях Африки ситуация стабилизируется, но специалисты отмечают, что видимость стабилизации вызвана тем, что число новозараженных уравновешивается большим количеством умирающих.
По оценкам ВОЗ в 2003 г. зарегистрировано самое большое число зараженных ВИЧ и смертей от СПИДа по всему миру: за год зарегистрировано пять миллионов зараженных и три миллиона смертей. Болезнь по-прежнему наиболее распространена в Африке южнее Сахары, на этот регион приходятся три миллиона вновь нфицированных и 2, 3 миллиона смертей в 2003 году. Вызывает у ООН опасение новый пояс распространения болезни – Китай, Индонезия, Россия и восточно-европейские государства. Около 40 миллионов человек сейчас живут с ВИЧ, из которых 26, 6 миллионов живут в южной части африканского континента. В Китае, где эпидемия находится в самом начале, 1, 5 миллиона инфицированных, число инфицированных последние три года увеличивается на 30% в год. В некоторых частях Африки ситуация стабилизируется, но специалисты отмечают, что видимость стабилизации вызвана тем, что число новозараженных уравновешивается большим количеством умирающих.
 ЭТИОЛОГИЯ, ЭПИДЕМИОЛОГИЯ, ПАТИОГЕНЕЗ И КЛИНИКА ВИЧ-ИНФЕКЦИИ • Возбудители инфекционных болезней человека представлены прионами, вирусами, риккетсиями, бактериями, простейшими и гельминтами (табл. 1), причем все больший удельный вес в патологии человека занимают вирусы. Последние могут вызвать клинику острой инфекции, но процесс может завершиться и персистенцией вируса. Персистенция – вид инфекционного процесса, когда возбудитель пребывает в организме больше времени, чем срок инкубации в сумме с длительностью неосложненной клиники. Этот вид инфекционного процесса имеет следующие варианты клинического проявления: а) бессимптомная (латентная инфекция), б) с симптомами (хроническая инфекция), в) своеобразный нестандартный процесс (медленная инфекция). Именно медленная инфекция со средины ХХ века все больше привлекает внимание, а к концу века один из вирусов, представителей медленных вирусов — вирус иммунодефицита человека — обусловил пандемию с самой высокой летальностью.
ЭТИОЛОГИЯ, ЭПИДЕМИОЛОГИЯ, ПАТИОГЕНЕЗ И КЛИНИКА ВИЧ-ИНФЕКЦИИ • Возбудители инфекционных болезней человека представлены прионами, вирусами, риккетсиями, бактериями, простейшими и гельминтами (табл. 1), причем все больший удельный вес в патологии человека занимают вирусы. Последние могут вызвать клинику острой инфекции, но процесс может завершиться и персистенцией вируса. Персистенция – вид инфекционного процесса, когда возбудитель пребывает в организме больше времени, чем срок инкубации в сумме с длительностью неосложненной клиники. Этот вид инфекционного процесса имеет следующие варианты клинического проявления: а) бессимптомная (латентная инфекция), б) с симптомами (хроническая инфекция), в) своеобразный нестандартный процесс (медленная инфекция). Именно медленная инфекция со средины ХХ века все больше привлекает внимание, а к концу века один из вирусов, представителей медленных вирусов — вирус иммунодефицита человека — обусловил пандемию с самой высокой летальностью.
 Таблица 1. Возбудители инфекционных болезней человека Класс возбудителей Число Бактерии и риккетсии 1000 Вирусы 500 Грибы 500 Простейшие и гельминты 200 Прионы
Таблица 1. Возбудители инфекционных болезней человека Класс возбудителей Число Бактерии и риккетсии 1000 Вирусы 500 Грибы 500 Простейшие и гельминты 200 Прионы
 В 1954 году Сигурсон сообщил о болезнях овец в Исландии, особенностью которых были: необычайная длительность инкубационного периода, медленно прогрессирующее течение, своеобразное поражение органов и систем, обязательный смертельный исход. Через 3 года он описывает подобное заболевание среди папуасов острова Новая Гвинея. Так появилось понятие о медленных вирусных инфекциях. В эту группу включены заболевания, вызванные вирионами: подострый склерозирующий панэнцефалит — вирус кори, подострый послекоревой лейкоэнцефалит — вирус кори, прогрессирующая врожденная краснуха, энцефалит прогрессирующий краснушный панэнцефалит, подострый герпетический панэнцефалит, подострый аденовирусный, хронический инфекционный мононуклеоз — вирус Эпштейна-Барр (вирус весьма загадочный по своим свойствам – в умеренном климате земли вызывает инфекционный мононуклеоз, а на африканском континенте тяжелое опухолевое заболевание – саркому Беркитта), цитомегаловирусное поражение мозга, ВИЧ-инфекция, лимфоцитарный хореоменингит новорожденных. В группу медленных инфекций входят также заболевания, вызванные прионами: Куру, болезнь Крейцфельда-Якоби, амиотрофический лейкоспонгиоз, Висна.
В 1954 году Сигурсон сообщил о болезнях овец в Исландии, особенностью которых были: необычайная длительность инкубационного периода, медленно прогрессирующее течение, своеобразное поражение органов и систем, обязательный смертельный исход. Через 3 года он описывает подобное заболевание среди папуасов острова Новая Гвинея. Так появилось понятие о медленных вирусных инфекциях. В эту группу включены заболевания, вызванные вирионами: подострый склерозирующий панэнцефалит — вирус кори, подострый послекоревой лейкоэнцефалит — вирус кори, прогрессирующая врожденная краснуха, энцефалит прогрессирующий краснушный панэнцефалит, подострый герпетический панэнцефалит, подострый аденовирусный, хронический инфекционный мононуклеоз — вирус Эпштейна-Барр (вирус весьма загадочный по своим свойствам – в умеренном климате земли вызывает инфекционный мононуклеоз, а на африканском континенте тяжелое опухолевое заболевание – саркому Беркитта), цитомегаловирусное поражение мозга, ВИЧ-инфекция, лимфоцитарный хореоменингит новорожденных. В группу медленных инфекций входят также заболевания, вызванные прионами: Куру, болезнь Крейцфельда-Якоби, амиотрофический лейкоспонгиоз, Висна.
 Медленная инфекция – своеобразный инфекционный процесс с длительным инкубационным периодом (месяцы, годы), прогрессирующим течением болезни со смертельным исходом. На сегодня нет общепринятой классификации инфекционных болезней, удовлетворяющей врача-инфекциониста. Отсутствует классификация медленных инфекций. Нам представляется, что наиболее логичным классифицировать медленные инфекции по этиологическому принципу (табл. 2)
Медленная инфекция – своеобразный инфекционный процесс с длительным инкубационным периодом (месяцы, годы), прогрессирующим течением болезни со смертельным исходом. На сегодня нет общепринятой классификации инфекционных болезней, удовлетворяющей врача-инфекциониста. Отсутствует классификация медленных инфекций. Нам представляется, что наиболее логичным классифицировать медленные инфекции по этиологическому принципу (табл. 2)
 Таблица 2 Этиологическая классификация медленных инфекций Этиология Нозологические формы Объект пораже ния Прионные Куру Болезнь Крейтцфельдта-Якоба Синдром Герстманна-Штреусслера-Шейнкера Хроническая семейная бессонница Скрепи Трансмиссивная энцефалопатия норок Губкообразная энцефалопатия крупного рогатого скота Губкообразная энцефалопатия кошек Губкообразная энцефалопатия экзотических животных человек овцы и козы норки коровы, быки кошки антилопы и др.
Таблица 2 Этиологическая классификация медленных инфекций Этиология Нозологические формы Объект пораже ния Прионные Куру Болезнь Крейтцфельдта-Якоба Синдром Герстманна-Штреусслера-Шейнкера Хроническая семейная бессонница Скрепи Трансмиссивная энцефалопатия норок Губкообразная энцефалопатия крупного рогатого скота Губкообразная энцефалопатия кошек Губкообразная энцефалопатия экзотических животных человек овцы и козы норки коровы, быки кошки антилопы и др.
 Вирусные Медленные инфекции группы ретровирусов: —ВИЧ-инфекция —Т-клеточная лимфома и лейкемия — ретровирусы HTLV-I и II Медленные инфекции герпесвирусной группы: —Подострый герпетический энце фалит —Лимфома Беркитта — вирус Эпштейна—Барр + возбудитель тропической малярии —Хронический инфекционный мононуклеоз —Цитомегаловирусное пораже ние мозга —Саркома Капоши — вирус герпеса HHV-8 Медленные инфекции группы вирусных гепатитов: —Первичная карцинома печени — вирус гепатита В —Цирроз печени — вирус гепатита С —Вирусный гепатит TTV Подострый склерозирующий панэнцефалит Прогрессирующий краснушный панэнцефалит Рак шейки матки — папилломавирус Некоторые психозы — вирусы Борна Прогрессирующая врожденная краснуха Подострый аденовирусный эн цефалит Прогрессирующая многоочаго вая лейкоэнцефалопатия Кожевниковская эпилепсия и прогрессирующий бульбарный паралич Хронический менингоэнцефалит при иммунодефиците Т-клеточная лимфома Балканская эндемическая нефропатия Бешенство абортивное Лимфоцитарный хориоменингит
Вирусные Медленные инфекции группы ретровирусов: —ВИЧ-инфекция —Т-клеточная лимфома и лейкемия — ретровирусы HTLV-I и II Медленные инфекции герпесвирусной группы: —Подострый герпетический энце фалит —Лимфома Беркитта — вирус Эпштейна—Барр + возбудитель тропической малярии —Хронический инфекционный мононуклеоз —Цитомегаловирусное пораже ние мозга —Саркома Капоши — вирус герпеса HHV-8 Медленные инфекции группы вирусных гепатитов: —Первичная карцинома печени — вирус гепатита В —Цирроз печени — вирус гепатита С —Вирусный гепатит TTV Подострый склерозирующий панэнцефалит Прогрессирующий краснушный панэнцефалит Рак шейки матки — папилломавирус Некоторые психозы — вирусы Борна Прогрессирующая врожденная краснуха Подострый аденовирусный эн цефалит Прогрессирующая многоочаго вая лейкоэнцефалопатия Кожевниковская эпилепсия и прогрессирующий бульбарный паралич Хронический менингоэнцефалит при иммунодефиците Т-клеточная лимфома Балканская эндемическая нефропатия Бешенство абортивное Лимфоцитарный хориоменингит
 Бактер и-альн ые Язва двенадцатиперстной кишки — Helicobacter pilori Некоторые виды артритов — боррелии, иерсинии Атеросклероз и ИБС — Chlamidia pulmonalis человек
Бактер и-альн ые Язва двенадцатиперстной кишки — Helicobacter pilori Некоторые виды артритов — боррелии, иерсинии Атеросклероз и ИБС — Chlamidia pulmonalis человек
 Нет сомнения, список медленных вирусных инфекций будет расти по мере расширения знаний об этиологии многих, пока считающихся соматическими заболеваний. Медленная вирусная инфекция чаще развивается, если заражение произошло внутриутробно (вирусы краснухи, кори, герпеса, аденовирусы, цитомегаловирусы) или ребенок заразился на первом году жизни (корь), когда остаточный материнский иммунитет снижает ответную реакцию иммунной системы и вирус гнездится в ЦНС, где в дальнейшем защищен от иммунного надзора, обусловливая хронический прогрессирующий инфекционный процесс. Особую группу медленных вирусных инфекций составляют заболевания, обусловленные ретровирусами. Свое название ретровирусы получили по отличительной особенности процесса репликации. Если создание новых вирионов в обычном варианте вирусов идет в направлении переноса генетической информации ДНК-РНК-белок, то у ретровирусов вирусная РНК служит основой для формирования ДНК-провируса (retro — назад) с последующим синтезом вирусной РНК.
Нет сомнения, список медленных вирусных инфекций будет расти по мере расширения знаний об этиологии многих, пока считающихся соматическими заболеваний. Медленная вирусная инфекция чаще развивается, если заражение произошло внутриутробно (вирусы краснухи, кори, герпеса, аденовирусы, цитомегаловирусы) или ребенок заразился на первом году жизни (корь), когда остаточный материнский иммунитет снижает ответную реакцию иммунной системы и вирус гнездится в ЦНС, где в дальнейшем защищен от иммунного надзора, обусловливая хронический прогрессирующий инфекционный процесс. Особую группу медленных вирусных инфекций составляют заболевания, обусловленные ретровирусами. Свое название ретровирусы получили по отличительной особенности процесса репликации. Если создание новых вирионов в обычном варианте вирусов идет в направлении переноса генетической информации ДНК-РНК-белок, то у ретровирусов вирусная РНК служит основой для формирования ДНК-провируса (retro — назад) с последующим синтезом вирусной РНК.
 Генетическим материалом ретровирусов является РНК, которая встраивается в геном инфицированной вирусом клетки с помощью особого фермента обратной транскриптазы (ревертазы), превращающей РНК ретровируса в ДНК. В группу вирусов — этиологических факторов медленных инфекций входят: вирус инфекционной анемии лошадей вирус меди-висны овец вирус артрита-энцефалита коз овец вирус иммунодефицита крупного рогатого скота вирус иммунодефицита кошек вирус иммунодефицита обезьян (SIV) вирус иммунодефицита человека (HIV, в русской транскрипции — ВИЧ).
Генетическим материалом ретровирусов является РНК, которая встраивается в геном инфицированной вирусом клетки с помощью особого фермента обратной транскриптазы (ревертазы), превращающей РНК ретровируса в ДНК. В группу вирусов — этиологических факторов медленных инфекций входят: вирус инфекционной анемии лошадей вирус меди-висны овец вирус артрита-энцефалита коз овец вирус иммунодефицита крупного рогатого скота вирус иммунодефицита кошек вирус иммунодефицита обезьян (SIV) вирус иммунодефицита человека (HIV, в русской транскрипции — ВИЧ).
 В конце 70 -х годов описано новое заболевание, названное Т-клеточным лейкозом/лимфомой, а выделенный вирус получил название Human T-leukemia/lymphoma viruses (HTLV). У больных с Т- клеточной лейкемией/лимфомой в 70% выявлялись антитела к этому вирусу, которого стали называть HTLV-I. У здоровых лиц он выявляется в 2 -10%. Так был открыт первый из группы лимфотропных ретровирусов человека, именно с HTLV-I этиологически связан Т-лейкоз взрослых людей. Причем было установлено, что HTLV-I может быть передан половым путем или внесен в организм при переливании крови, а также при близком контакте, т. к. в семьях больных у других членов появляются антитела. Чаще в семьях передается от мужа жене, от матери ребенку. Антитела к HTLV-I обнаружены у больных гемофилией, у наркоманов. Но нет антител к этому вирусу у больных В-клеточными и другими лейкозами.
В конце 70 -х годов описано новое заболевание, названное Т-клеточным лейкозом/лимфомой, а выделенный вирус получил название Human T-leukemia/lymphoma viruses (HTLV). У больных с Т- клеточной лейкемией/лимфомой в 70% выявлялись антитела к этому вирусу, которого стали называть HTLV-I. У здоровых лиц он выявляется в 2 -10%. Так был открыт первый из группы лимфотропных ретровирусов человека, именно с HTLV-I этиологически связан Т-лейкоз взрослых людей. Причем было установлено, что HTLV-I может быть передан половым путем или внесен в организм при переливании крови, а также при близком контакте, т. к. в семьях больных у других членов появляются антитела. Чаще в семьях передается от мужа жене, от матери ребенку. Антитела к HTLV-I обнаружены у больных гемофилией, у наркоманов. Но нет антител к этому вирусу у больных В-клеточными и другими лейкозами.
 Вирус иммунодефицита человека был выделен в 1983 году группой профессора Люка Монтанье (Montaner L. ) из лимфатического узла больного СПИДом в Парижском институте Пастера. В том же году в США группа профессора Роберта Галло (Gallo R. ) выделила вирус из лимфоцитов периферической крови больных СПИДом. Оба выделенные вируса оказались идентичными и ВОЗ в 1987 году приняла единое название — “вирус иммунодефицита человека” (ВИЧ, или в английской аббревиатуре — HIV). По мнению некоторых специалистов, ВИЧ произошел от SIV- инфицированного человека где-то в 30 — 90 годы в Центральной Африке. ВИЧ-2 более сходен с SIV, нежели с ВИЧ-1 распространен во всем мире, первая группа эпидемий прошла в Африке, вторая и третья — в Америке и Западной Европе, четвертая сейчас имеет место в Азии. Глобальное и интенсивное распространение болезни обусловлено образованием новых штаммов ВИЧ.
Вирус иммунодефицита человека был выделен в 1983 году группой профессора Люка Монтанье (Montaner L. ) из лимфатического узла больного СПИДом в Парижском институте Пастера. В том же году в США группа профессора Роберта Галло (Gallo R. ) выделила вирус из лимфоцитов периферической крови больных СПИДом. Оба выделенные вируса оказались идентичными и ВОЗ в 1987 году приняла единое название — “вирус иммунодефицита человека” (ВИЧ, или в английской аббревиатуре — HIV). По мнению некоторых специалистов, ВИЧ произошел от SIV- инфицированного человека где-то в 30 — 90 годы в Центральной Африке. ВИЧ-2 более сходен с SIV, нежели с ВИЧ-1 распространен во всем мире, первая группа эпидемий прошла в Африке, вторая и третья — в Америке и Западной Европе, четвертая сейчас имеет место в Азии. Глобальное и интенсивное распространение болезни обусловлено образованием новых штаммов ВИЧ.
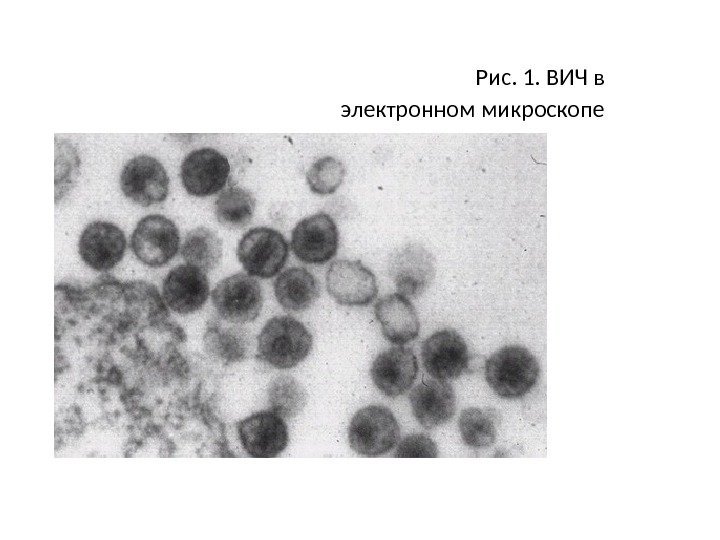
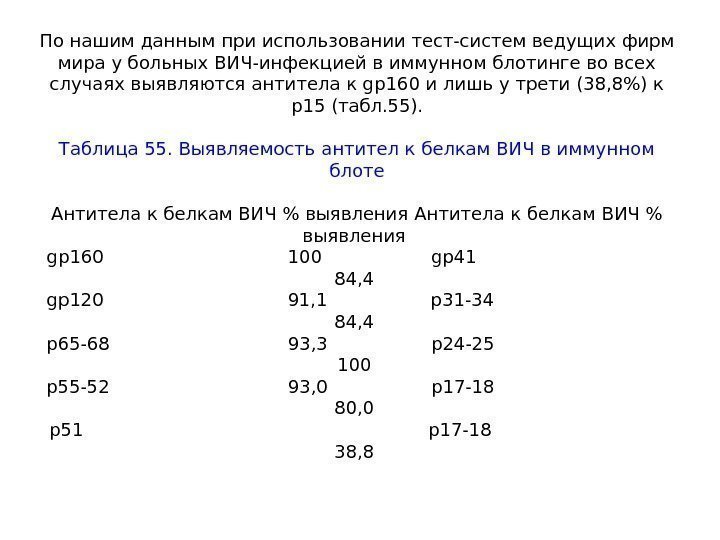
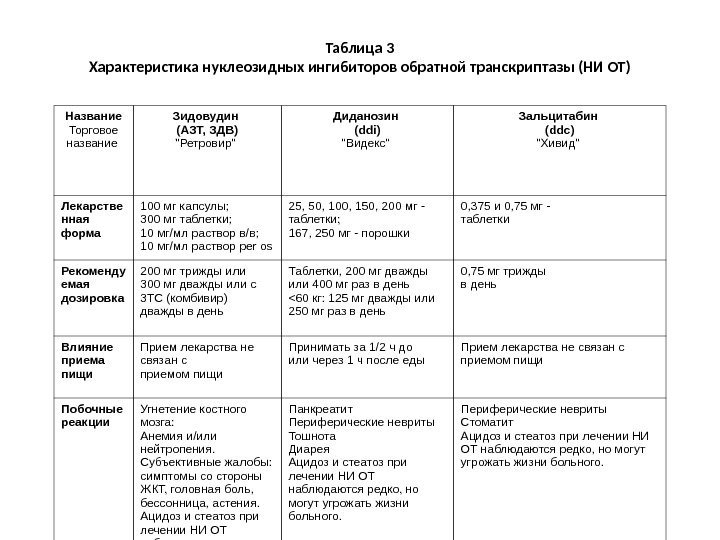
 ВИЧ- представитель семейства ретровирусов, относится к подсемейству лентивирусов (медленных вирусов). Зрелый вирион имеет диаметр около 100 нм. ВИЧ-1 представлен оболочкой, матриксным слоем, оболочкой нуклеотида, геномной РНК, в которую включены фрагмент комплекса интеграции и нуклеопротеиды, а также латеральные тельца. При среднем увеличении в электронном микроскопе видны ядро и оболочка вируса (рис. 1). Наружная мембрана вируса пронизана собственными белками (оболочечные белки) gp 41 и gp 120, получившими название от слова “glicоprotein” c молекулярной массой 41 и 120 k. D. Эти белки образуют 72 отростка на поверхности мембраны вируса, каждый состоит из 3 молекул gp 120. Молекулы gp 120 могут отрываться от вирусной частицы и с током крови поступать в ткани, что имеет существенное значение в патогенезе ВИЧ-инфекции.
ВИЧ- представитель семейства ретровирусов, относится к подсемейству лентивирусов (медленных вирусов). Зрелый вирион имеет диаметр около 100 нм. ВИЧ-1 представлен оболочкой, матриксным слоем, оболочкой нуклеотида, геномной РНК, в которую включены фрагмент комплекса интеграции и нуклеопротеиды, а также латеральные тельца. При среднем увеличении в электронном микроскопе видны ядро и оболочка вируса (рис. 1). Наружная мембрана вируса пронизана собственными белками (оболочечные белки) gp 41 и gp 120, получившими название от слова “glicоprotein” c молекулярной массой 41 и 120 k. D. Эти белки образуют 72 отростка на поверхности мембраны вируса, каждый состоит из 3 молекул gp 120. Молекулы gp 120 могут отрываться от вирусной частицы и с током крови поступать в ткани, что имеет существенное значение в патогенезе ВИЧ-инфекции.
 Оболочка нуклеотида построена из молекул белка (р24) с молекулярной массой 24 k. D. Внутри нуклеоида заключены геном вируса (две молекулы РНК), белок с молекулярной массой 7 k. D и комплекс ферментов: обратная транскриптаза, РНКаза, протеаза. Геном ВИЧ состоит из 9 генов, которые представлены 3 структурными (gag- group-specific antigens, pol -polymerasae, env — envelope), характерными для всех ретровирусов и 6 регуляторными ( tat — transactivator of transcription, rev — regulator of expression of virus proteins, vif — virion infectivity factor, nef — negative regulatory factor, а также vpr, vpu для ВИЧ-1, vpx для ВИЧ-2 с малоизученной функцией). Ген tat наиболее активный регулятор, обеспечивающий усиление в 1000 раз репликацию вируса. Он также регулирует экспрессию клеточных генов. Ген rev избирательно активирует синтез структурных белков вируса. На поздних стадиях ВИЧ-инфекции ген rev замедляет синтез регуляторных белков. Ген nef при взаимодействии с LTR замедляет транскрипцию вирусных геномов, обеспечивая равновесие между вирусом и организмом. Синхронная функция tat и nef обусловливает взвешенную репликацию вируса, не приводящую к гибели инфицированной вирусом клетки.
Оболочка нуклеотида построена из молекул белка (р24) с молекулярной массой 24 k. D. Внутри нуклеоида заключены геном вируса (две молекулы РНК), белок с молекулярной массой 7 k. D и комплекс ферментов: обратная транскриптаза, РНКаза, протеаза. Геном ВИЧ состоит из 9 генов, которые представлены 3 структурными (gag- group-specific antigens, pol -polymerasae, env — envelope), характерными для всех ретровирусов и 6 регуляторными ( tat — transactivator of transcription, rev — regulator of expression of virus proteins, vif — virion infectivity factor, nef — negative regulatory factor, а также vpr, vpu для ВИЧ-1, vpx для ВИЧ-2 с малоизученной функцией). Ген tat наиболее активный регулятор, обеспечивающий усиление в 1000 раз репликацию вируса. Он также регулирует экспрессию клеточных генов. Ген rev избирательно активирует синтез структурных белков вируса. На поздних стадиях ВИЧ-инфекции ген rev замедляет синтез регуляторных белков. Ген nef при взаимодействии с LTR замедляет транскрипцию вирусных геномов, обеспечивая равновесие между вирусом и организмом. Синхронная функция tat и nef обусловливает взвешенную репликацию вируса, не приводящую к гибели инфицированной вирусом клетки.
 Рис. 1. ВИЧ в электронном микроскопе
Рис. 1. ВИЧ в электронном микроскопе
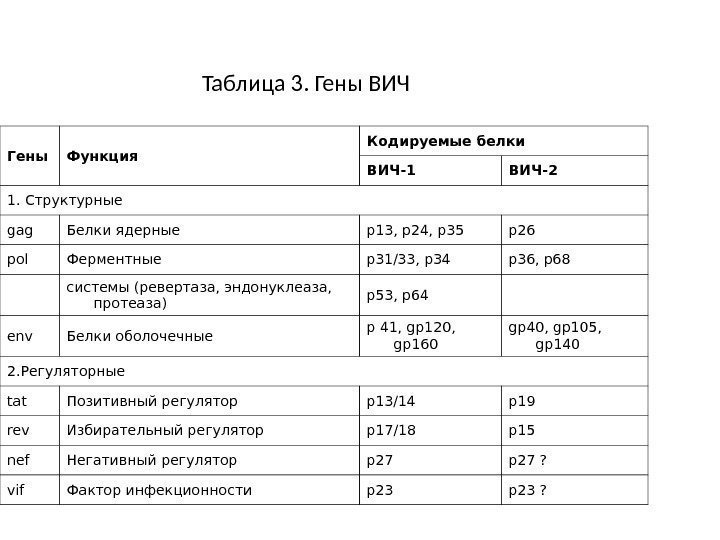
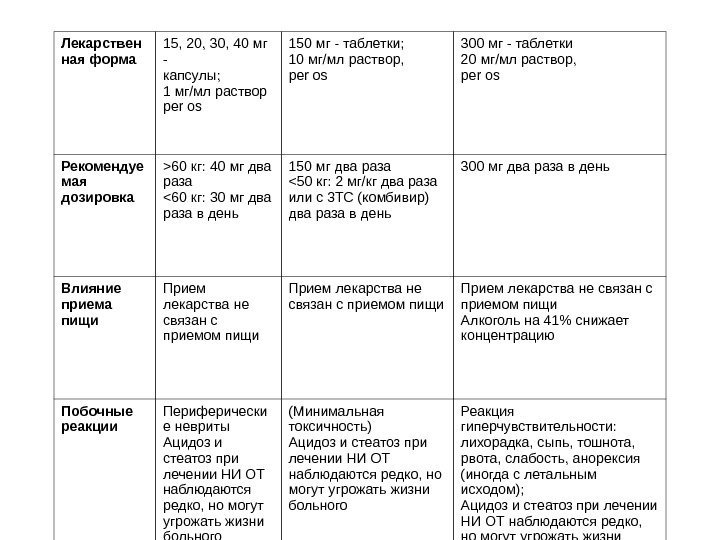
 Структурные гены gag, pol и env обеспечивают синтез белков вириона: 1. Гены оболочки (env) — кодируют трансляцию белка-предшественника оболочки вируса gp 160, в дальнейшем расщепляющегося на gp 120 и gp 41. 2. Группоспецифические гены (gag) — кодируют трансляцию белка — предшественника внутренней части вируса (нуклеотида и матриксный) с молекулярным весом 55 к. D, расщепляющегося на р24/25, р7/9, р13, р15, р17/18. 3. Ген pol — кодирует ферментные системы вируса, обратную транскриптазу (р66/51), интегразу (р31/33), рибонуклеазу Н (р15). Белки вириона в организме инфицированного человека определяют иммунный ответ с синтезом иммуноглобулинов (табл. 3).
Структурные гены gag, pol и env обеспечивают синтез белков вириона: 1. Гены оболочки (env) — кодируют трансляцию белка-предшественника оболочки вируса gp 160, в дальнейшем расщепляющегося на gp 120 и gp 41. 2. Группоспецифические гены (gag) — кодируют трансляцию белка — предшественника внутренней части вируса (нуклеотида и матриксный) с молекулярным весом 55 к. D, расщепляющегося на р24/25, р7/9, р13, р15, р17/18. 3. Ген pol — кодирует ферментные системы вируса, обратную транскриптазу (р66/51), интегразу (р31/33), рибонуклеазу Н (р15). Белки вириона в организме инфицированного человека определяют иммунный ответ с синтезом иммуноглобулинов (табл. 3).
 Таблица 3. Гены ВИЧ Гены Функция Кодируемые белки ВИЧ-1 ВИЧ-2 1. Структурные gag Белки ядерные р13, р24, р35 р26 pol Ферментные р31/33, р34 р36, р68 системы (ревертаза, эндонуклеаза, протеаза) р53, р64 env Белки оболочечные р 41, gp 120, gp 160 gp 40, gp 105, gp 140 2. Регуляторные tat Позитивный регулятор р13/14 р19 rev Избирательный регулятор р17/18 р15 nef Негативный регулятор р27 ? vif Фактор инфекционности р23 ?
Таблица 3. Гены ВИЧ Гены Функция Кодируемые белки ВИЧ-1 ВИЧ-2 1. Структурные gag Белки ядерные р13, р24, р35 р26 pol Ферментные р31/33, р34 р36, р68 системы (ревертаза, эндонуклеаза, протеаза) р53, р64 env Белки оболочечные р 41, gp 120, gp 160 gp 40, gp 105, gp 140 2. Регуляторные tat Позитивный регулятор р13/14 р19 rev Избирательный регулятор р17/18 р15 nef Негативный регулятор р27 ? vif Фактор инфекционности р23 ?
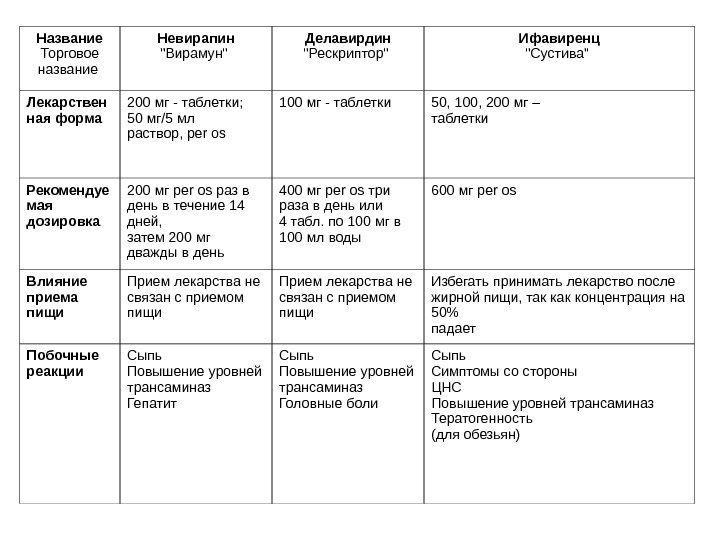
 Помимо структурных и регуляторных генов в состав вириона ВИЧ-1 входят длинные концевые повторы (LTR), а в состав ВИЧ-2 дополнительный ген Х. В мире циркулирует два типа вирусов: ВИЧ-1 и ВИЧ-2, которые отличают структура, антигенный состав и эпидемиологическая характеристика. По мнению некоторых специалистов, ВИЧ произошел от SIV- инфицированного человека где-то в 30 — 90 годы в центральной Африке. ВИЧ-2 более сходен с SIV, нежели с ВИЧ-1 распространен во всем мире, первая группа эпидемий прошла в Африке, вторая — в Америке и Западной Европе, четвертая сейчас имеет место в Азии. Колоссальное распространение болезни обусловлено образованием все новых штаммов ВИЧ. Тип ВИЧ-1 в зависимости от строения фрагментов гена env имеет субтипы (клайды) А, В, С, D, Е, F, G, H, J и др. а также О (от outlier — в стороне). Субтипы А-Н составляют группу М (major), на сегодня доминирующую на земле, причем почти половину составляет субтип С. С 1990 года идет рост распространенности субтипа Е. Прослеживается определенная географическая зависимость распространения отдельных субтипов ВИЧ (табл. 4).
Помимо структурных и регуляторных генов в состав вириона ВИЧ-1 входят длинные концевые повторы (LTR), а в состав ВИЧ-2 дополнительный ген Х. В мире циркулирует два типа вирусов: ВИЧ-1 и ВИЧ-2, которые отличают структура, антигенный состав и эпидемиологическая характеристика. По мнению некоторых специалистов, ВИЧ произошел от SIV- инфицированного человека где-то в 30 — 90 годы в центральной Африке. ВИЧ-2 более сходен с SIV, нежели с ВИЧ-1 распространен во всем мире, первая группа эпидемий прошла в Африке, вторая — в Америке и Западной Европе, четвертая сейчас имеет место в Азии. Колоссальное распространение болезни обусловлено образованием все новых штаммов ВИЧ. Тип ВИЧ-1 в зависимости от строения фрагментов гена env имеет субтипы (клайды) А, В, С, D, Е, F, G, H, J и др. а также О (от outlier — в стороне). Субтипы А-Н составляют группу М (major), на сегодня доминирующую на земле, причем почти половину составляет субтип С. С 1990 года идет рост распространенности субтипа Е. Прослеживается определенная географическая зависимость распространения отдельных субтипов ВИЧ (табл. 4).
 ВИЧ отличает исключительно высокая генетическая изменчивость, частота генетических ошибок при репликации составляет 10 -4 -10 -5 ошибок/на ген/на цикл репликации. Иными словами, ни один ВИЧ, содержащий 104 нуклеотидов в длину, не производит при репликации вирион, в точности повторяющий родительский. Высокая генетическая изменчивость, реализуемая в вариабельности антигенных и биологических свойств изолятов. Это во многом связано с продуктом гена env вируса – gp 120, вариабельность аминоксилотной последовательности которого составляет 5 -20% для изолятов одного субтипа и 25 -35% для разных субтипов. Особенно вариабелен участок gp 120, образующий петлеобразный домен, получивший название V 3 -петли, состоящий из 35 аминокислот и к которому вырабатывается 80 -95% всех нейтрализующих антител. Исключительная генетическая изменчивость позволяет вирусу выжить в инфицированном организме, ибо всегда в огромном пуле найдется вирус, способный к эволюционному отбору. Наряду с генетическими особенностями ВИЧ-1 имеет фенотипические различия. Так, у ВИЧ-инфицированных по репликативной активности выделяют а) rapid/high – высокоинфекционные, эффективно реплицирующие изоляты и б) slow/low – низкоинфекционные, слабо реплицирующие изоляты. По характеру цитопатического действия изоляты классифицируют на а) низко реплицирующиеся, не способные к образованию синцития; б) высоко реплицирующиеся, не образующие синцитий (НСО) и в) высоко реплицирующиеся, образующие синцитий (СО
ВИЧ отличает исключительно высокая генетическая изменчивость, частота генетических ошибок при репликации составляет 10 -4 -10 -5 ошибок/на ген/на цикл репликации. Иными словами, ни один ВИЧ, содержащий 104 нуклеотидов в длину, не производит при репликации вирион, в точности повторяющий родительский. Высокая генетическая изменчивость, реализуемая в вариабельности антигенных и биологических свойств изолятов. Это во многом связано с продуктом гена env вируса – gp 120, вариабельность аминоксилотной последовательности которого составляет 5 -20% для изолятов одного субтипа и 25 -35% для разных субтипов. Особенно вариабелен участок gp 120, образующий петлеобразный домен, получивший название V 3 -петли, состоящий из 35 аминокислот и к которому вырабатывается 80 -95% всех нейтрализующих антител. Исключительная генетическая изменчивость позволяет вирусу выжить в инфицированном организме, ибо всегда в огромном пуле найдется вирус, способный к эволюционному отбору. Наряду с генетическими особенностями ВИЧ-1 имеет фенотипические различия. Так, у ВИЧ-инфицированных по репликативной активности выделяют а) rapid/high – высокоинфекционные, эффективно реплицирующие изоляты и б) slow/low – низкоинфекционные, слабо реплицирующие изоляты. По характеру цитопатического действия изоляты классифицируют на а) низко реплицирующиеся, не способные к образованию синцития; б) высоко реплицирующиеся, не образующие синцитий (НСО) и в) высоко реплицирующиеся, образующие синцитий (СО
 • ). По тропизму классифицируют лимфоцитотропныне изоляты (разгар болезни) и моноцитотропные (начальные этапы болезни). • Прогрессирование ВИЧ-инфекции связано с тропизмом вируса к Т-хелперам, способности индуцировать синцитий и/или с высокой репликативной активность. Мутации в гене env определяют переход изолятов НСО в СО. Переход в СО появляется при снижении CD 4+клеток до 400 -500 в 1 мкл. При появлении СО-вариантов изолятов HIV дальнейшее падение уровня CD 4+ клеток идет прогрессивнее. В стадии СПИД СО-варианты изолятов выявляются у Ң больных, следловательно и НСО могут обусловить формирование терминальной стадии и смерть больного. Мутации в гене pol обеспечивают у HIV формирование резистентности к ингибиторам обратной транскриптазы. Быстрое уменьшение CD 4+ лимфоцитов связано с более высоким уровнем репликативной активности HIV, как образующих, так и не образующих синцитий.
• ). По тропизму классифицируют лимфоцитотропныне изоляты (разгар болезни) и моноцитотропные (начальные этапы болезни). • Прогрессирование ВИЧ-инфекции связано с тропизмом вируса к Т-хелперам, способности индуцировать синцитий и/или с высокой репликативной активность. Мутации в гене env определяют переход изолятов НСО в СО. Переход в СО появляется при снижении CD 4+клеток до 400 -500 в 1 мкл. При появлении СО-вариантов изолятов HIV дальнейшее падение уровня CD 4+ клеток идет прогрессивнее. В стадии СПИД СО-варианты изолятов выявляются у Ң больных, следловательно и НСО могут обусловить формирование терминальной стадии и смерть больного. Мутации в гене pol обеспечивают у HIV формирование резистентности к ингибиторам обратной транскриптазы. Быстрое уменьшение CD 4+ лимфоцитов связано с более высоким уровнем репликативной активности HIV, как образующих, так и не образующих синцитий.
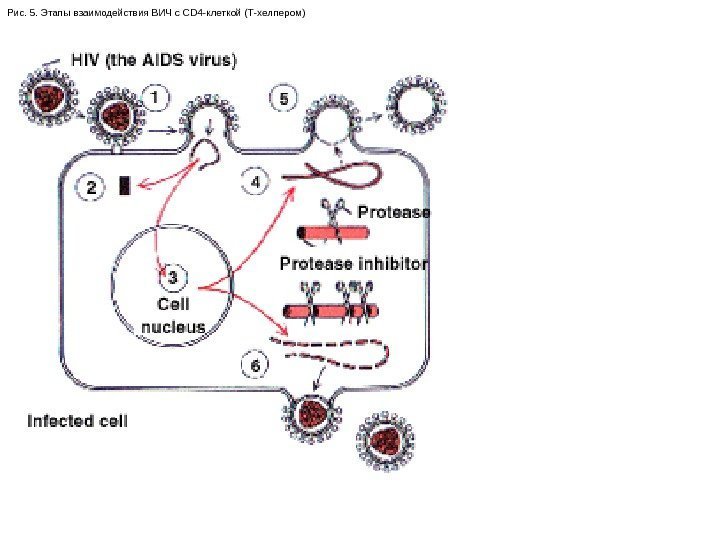
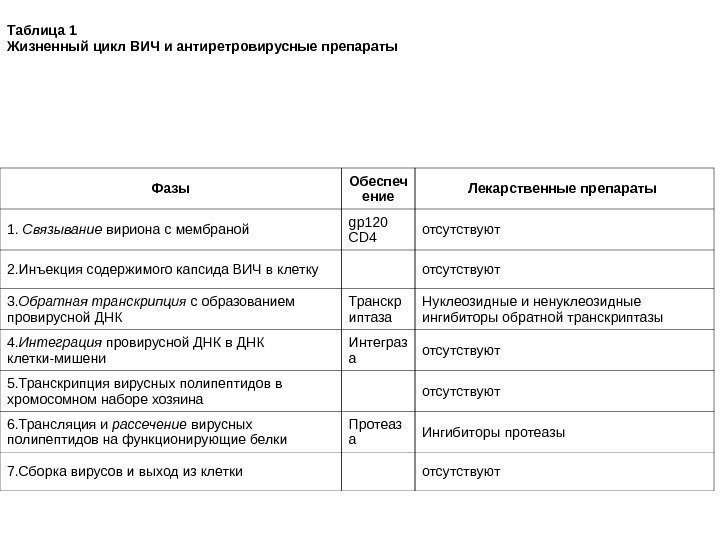
 • Инфекционный процесс при заражении ВИЧ носит последовательный, фазовый характер: проникновение вируса через слизистую оболочку половых путей или непосредственное поступление в кровоток, • связывание вириона с поверхностью клетки, слияние мембраны клетки и вириона, обеспечивающее проникновение вируса внутрь, • высвобождение нуклеоида и геномной РНК вируса, • интеграция генома вируса в геном инфицированной клетки, • латентная фаза, • фаза активации транскрипции с ДНК провируса и последующая трансляция белков вируса, • наработка всех компонентов вируса и формирование новых (дочерних) вирионов, • их высвобождение из клетки, сопровождающееся цитопатическим эффектом для клетки-мишени.
• Инфекционный процесс при заражении ВИЧ носит последовательный, фазовый характер: проникновение вируса через слизистую оболочку половых путей или непосредственное поступление в кровоток, • связывание вириона с поверхностью клетки, слияние мембраны клетки и вириона, обеспечивающее проникновение вируса внутрь, • высвобождение нуклеоида и геномной РНК вируса, • интеграция генома вируса в геном инфицированной клетки, • латентная фаза, • фаза активации транскрипции с ДНК провируса и последующая трансляция белков вируса, • наработка всех компонентов вируса и формирование новых (дочерних) вирионов, • их высвобождение из клетки, сопровождающееся цитопатическим эффектом для клетки-мишени.
 Весь каскад этих превращений начинается со связывания вириона с поверхностью клетки-мишени. Это обеспечивается как специфическими, т. е. через специфический для вириона рецептор (молекула СD 4), так и неспецифическими, т. е. независящими от наличия СD 4 компонентами. Высокая плотность CD 4 на поверхности Т-хелперов определяет их преимущественное поражение при ВИЧ-инфекции. Плотность рецепторов — величина не постоянная, она зависит от функционального состояния клетки и при активации ее возрастает. Поэтому неактивированные CD 4+ лимфоциты более устойчивы к вирусу. Иными словами одни субпопуляции CD 4+ лимфоцитов лучше обеспечивают рецепцию ВИЧ по сравнению с другими.
Весь каскад этих превращений начинается со связывания вириона с поверхностью клетки-мишени. Это обеспечивается как специфическими, т. е. через специфический для вириона рецептор (молекула СD 4), так и неспецифическими, т. е. независящими от наличия СD 4 компонентами. Высокая плотность CD 4 на поверхности Т-хелперов определяет их преимущественное поражение при ВИЧ-инфекции. Плотность рецепторов — величина не постоянная, она зависит от функционального состояния клетки и при активации ее возрастает. Поэтому неактивированные CD 4+ лимфоциты более устойчивы к вирусу. Иными словами одни субпопуляции CD 4+ лимфоцитов лучше обеспечивают рецепцию ВИЧ по сравнению с другими.
 Процесс инфицирования клетки вирусом осуществляется в две фазы: прикрепления и слияния. Прикрепленный через gp 120 к рецептору CD 4 клетки-мишени вирус белком gp 41 оболочки сливается с мембраной клетки. Дальнейшее проникновение вируса в клетку осуществляется, очевидно, и путем эндоцитоза, и через плазматическую мембрану. В процессе инфицирования клетки белок ВИЧ gp 41 обеспечивает не только слияние вирусной мембраны с мембраной клетки, но также определяет слияние мембран соседних инфицированных клеток с образованием одной многоядерной синцитиальной клетки (синцитий), обреченной на гибель, продолжительность жизни сиицитиальных клеток не превышает 3 -7 дней. Вирулентность ВИЧ коррелирует с возможностью образовывать синцитий. В цитоплазме клетки-мишени информация с вирусной РНК переписывается на ДНК с помощью обратной транскриптазы с образованием в конечном итоге промежуточной двухнитевой линейчатой ДНК, которая транспортируется в ядро клетки, там приобретает кольцевую форму и интегрирует с ядром клетки, превращаясь в ДНК-провирус. Интеграция осуществляется под влиянием фермента интегразы, взаимодействующей с концевыми последовательностями LTR. Характерная и отличительная особенность ВИЧ от других ретровирусов — сохранение части ДНК в неинтегрированном состоянии, эта ДНК самостоятельно функционирует как репликон. Таким образом, в организме зараженного ВИЧ находится в двух вариантах. Заражение происходит зрелым вирусом, геном которого представлен РНК. В клетках инфицированного человека на геномной РНК, как на матрице синтезируется провирус с помощью особого вирусного фермента — обратной транскриптазы. ДНК, содержащая провирус, выполняет в свою очередь функцию матрицы для синтеза информационной РНК. С последней транслируются вирусные белки и транскрибируется полноразмерная геномная РНК для новых вирионов. На рис. 12 представлена электронная микрофотография, на которой виден момент выхода нового вириона из клетки.
Процесс инфицирования клетки вирусом осуществляется в две фазы: прикрепления и слияния. Прикрепленный через gp 120 к рецептору CD 4 клетки-мишени вирус белком gp 41 оболочки сливается с мембраной клетки. Дальнейшее проникновение вируса в клетку осуществляется, очевидно, и путем эндоцитоза, и через плазматическую мембрану. В процессе инфицирования клетки белок ВИЧ gp 41 обеспечивает не только слияние вирусной мембраны с мембраной клетки, но также определяет слияние мембран соседних инфицированных клеток с образованием одной многоядерной синцитиальной клетки (синцитий), обреченной на гибель, продолжительность жизни сиицитиальных клеток не превышает 3 -7 дней. Вирулентность ВИЧ коррелирует с возможностью образовывать синцитий. В цитоплазме клетки-мишени информация с вирусной РНК переписывается на ДНК с помощью обратной транскриптазы с образованием в конечном итоге промежуточной двухнитевой линейчатой ДНК, которая транспортируется в ядро клетки, там приобретает кольцевую форму и интегрирует с ядром клетки, превращаясь в ДНК-провирус. Интеграция осуществляется под влиянием фермента интегразы, взаимодействующей с концевыми последовательностями LTR. Характерная и отличительная особенность ВИЧ от других ретровирусов — сохранение части ДНК в неинтегрированном состоянии, эта ДНК самостоятельно функционирует как репликон. Таким образом, в организме зараженного ВИЧ находится в двух вариантах. Заражение происходит зрелым вирусом, геном которого представлен РНК. В клетках инфицированного человека на геномной РНК, как на матрице синтезируется провирус с помощью особого вирусного фермента — обратной транскриптазы. ДНК, содержащая провирус, выполняет в свою очередь функцию матрицы для синтеза информационной РНК. С последней транслируются вирусные белки и транскрибируется полноразмерная геномная РНК для новых вирионов. На рис. 12 представлена электронная микрофотография, на которой виден момент выхода нового вириона из клетки.
 • Заканчивается морфогенез цитопатическим действием ВИЧ, которое может быть выражено: а) прямой деструкцией и цитолизом инфицированной клетки, б) синцитиеобразованием, т. е. слиянием мембран инфицированных и неинфицированных клеток, имеющих СD 4, в силу чего клетки теряют свои физиологические функции, в) хронической инфекцией без выраженного цитолиза (дендритные лимфоциты, моноциты/макрофаги, нейроны), г) патогенных эффектов отдельных белков ВИЧ (около половины гликопротеина gp 120, синтезируемого в клетке, идет не на построение новых вирионов, а проникая во внеклеточную среду, связываются с СD 4, преимущественно неинфицированных ВИЧ клеток, обусловливая этим инактивацию иммунокомпетентных клеток, в частности Т 4 (СD 4+)- лимфоцитов.
• Заканчивается морфогенез цитопатическим действием ВИЧ, которое может быть выражено: а) прямой деструкцией и цитолизом инфицированной клетки, б) синцитиеобразованием, т. е. слиянием мембран инфицированных и неинфицированных клеток, имеющих СD 4, в силу чего клетки теряют свои физиологические функции, в) хронической инфекцией без выраженного цитолиза (дендритные лимфоциты, моноциты/макрофаги, нейроны), г) патогенных эффектов отдельных белков ВИЧ (около половины гликопротеина gp 120, синтезируемого в клетке, идет не на построение новых вирионов, а проникая во внеклеточную среду, связываются с СD 4, преимущественно неинфицированных ВИЧ клеток, обусловливая этим инактивацию иммунокомпетентных клеток, в частности Т 4 (СD 4+)- лимфоцитов.
 Жизненный цикл инфицированной клетки 22 дня Полная ВИЧ-1 продукция 10, 3 х 10 вирионов в день Минимальная продолжителльность жизненного цикла ВИЧ- vitro 1, 2 дня Длительность жизни вируса в плазме 0, 3 дня Внутриклеточная фаза 0, 9 дня Среднее время, необходимое ВИЧ-1 для продукции новой генерации 2, 6 дня D. Ho (1996) приводит следующую динамику жизненного цикла ВИЧ (табл. 4): Таблица 5. Клеточная и вирусная динамика ВИЧ по D. Ho (1996)
Жизненный цикл инфицированной клетки 22 дня Полная ВИЧ-1 продукция 10, 3 х 10 вирионов в день Минимальная продолжителльность жизненного цикла ВИЧ- vitro 1, 2 дня Длительность жизни вируса в плазме 0, 3 дня Внутриклеточная фаза 0, 9 дня Среднее время, необходимое ВИЧ-1 для продукции новой генерации 2, 6 дня D. Ho (1996) приводит следующую динамику жизненного цикла ВИЧ (табл. 4): Таблица 5. Клеточная и вирусная динамика ВИЧ по D. Ho (1996)
 В настоящее время идет интенсивное изучение структуры ВИЧ, патогенеза и морфогенеза, терапии и разработка вакцин. Отрабатываются возможности этих исследований на экспериментальных животных. Проблема вакцины. Генетическая изменчивость ВИЧ-1 реализуется в вариабельности антигенных свойств изолятов. Последние зависят от gp 120 оболочки HIV. Именно gp 120 определяет тропность к клеткам, проникновение вируса внутрь клеток, характер патологического процесса в организме больного. Gp 120 – основная мишень для иммунной системы организма, против этого гликопротеида идет образование нейтрализующих антител. При этом нейтрализация анти-ВИЧ к V 3 -петле носит типоспецифический характер. Следовательно, от превалирования субтипа ВИЧ-1 зависит подход к созданию вакцины. По трудностям создания вакцины против ВИЧ, если оценить характер инфекции, степень антигенной вариабельности, наличия естественного иммунитета, наличия модели на животных, возможности культивирования вируса в баллах от 1 до 5, то по сложности вакцина наиболее трудоемка из всех известных, оценивается в 14 баллов. К примеру, вакцина к герпесу оценивается в 10 баллов, уже созданные вакцины против кори – в 6 и против полиомиелита – в 7 баллов (Козлов А. П. , 1998).
В настоящее время идет интенсивное изучение структуры ВИЧ, патогенеза и морфогенеза, терапии и разработка вакцин. Отрабатываются возможности этих исследований на экспериментальных животных. Проблема вакцины. Генетическая изменчивость ВИЧ-1 реализуется в вариабельности антигенных свойств изолятов. Последние зависят от gp 120 оболочки HIV. Именно gp 120 определяет тропность к клеткам, проникновение вируса внутрь клеток, характер патологического процесса в организме больного. Gp 120 – основная мишень для иммунной системы организма, против этого гликопротеида идет образование нейтрализующих антител. При этом нейтрализация анти-ВИЧ к V 3 -петле носит типоспецифический характер. Следовательно, от превалирования субтипа ВИЧ-1 зависит подход к созданию вакцины. По трудностям создания вакцины против ВИЧ, если оценить характер инфекции, степень антигенной вариабельности, наличия естественного иммунитета, наличия модели на животных, возможности культивирования вируса в баллах от 1 до 5, то по сложности вакцина наиболее трудоемка из всех известных, оценивается в 14 баллов. К примеру, вакцина к герпесу оценивается в 10 баллов, уже созданные вакцины против кори – в 6 и против полиомиелита – в 7 баллов (Козлов А. П. , 1998).
 ЭПИДЕМИОЛОГИЯ Этапы эпидемии ВИЧ-инфекции 1930 -1959 годы – Появление болезни в Африке 1977 год – Появление болезни в США 1981 год – Выявление первых больных в США 1983 год выделен HIV > В 2003 году: в мире живут с ВИЧ – 34 -46 млн. чел. , в том числе —Африка к югу от Сахары – 25 -28, 2 млн. чел. —Восточная Азия – 4, 6 -8, 2 млн. —Латинская Америка – 1, 3 -1, 9 млн. чел. —Восточная Европа и Центральная Азия – 1, 2 -1, 8 млн. чел. —Севреная Америка – 0 Ю 79 -1, 2 млн. чел. —Восточная Азия и Тихоокеанский регион – 0, 7 -1, 3 млн. чел. —Западная Европа – 0, 52 -0, 68 млдн. Чел.
ЭПИДЕМИОЛОГИЯ Этапы эпидемии ВИЧ-инфекции 1930 -1959 годы – Появление болезни в Африке 1977 год – Появление болезни в США 1981 год – Выявление первых больных в США 1983 год выделен HIV > В 2003 году: в мире живут с ВИЧ – 34 -46 млн. чел. , в том числе —Африка к югу от Сахары – 25 -28, 2 млн. чел. —Восточная Азия – 4, 6 -8, 2 млн. —Латинская Америка – 1, 3 -1, 9 млн. чел. —Восточная Европа и Центральная Азия – 1, 2 -1, 8 млн. чел. —Севреная Америка – 0 Ю 79 -1, 2 млн. чел. —Восточная Азия и Тихоокеанский регион – 0, 7 -1, 3 млн. чел. —Западная Европа – 0, 52 -0, 68 млдн. Чел.
 95% инфицированных живут в странах со средним и низким уровнем дохода вновь инфицировано за год – 5 млн. , в т. ч. 0 Ю 7 млн. – дети до 15 лет в день вновь инфицируеьтся около 14 тыс. чел, в т. ч. 50%-женщины, около 2 тыс. – дети в возрасте до 15 лет. умерло за год 3 млн, в т. ч – 0, 5 млн. – дети до 15 лет >В России: 1987 год – первый больной; в первые годы эпидемии чрезвычайная острота внутрибольничного заражения детей; контроль за кровью позволил избежать трагедии США, Германии, Франции, Японии, где тысячи заражены при переливании крови в 90 годы; эпидемия в России прошла первую, начальную стадию; вступила во вторую “концентрированную”, когда будет высокая инфицированность групп риска и рост в целом среди населения; не за горами третья, заключительная стадия – “генерализованной” эпидемии ;
95% инфицированных живут в странах со средним и низким уровнем дохода вновь инфицировано за год – 5 млн. , в т. ч. 0 Ю 7 млн. – дети до 15 лет в день вновь инфицируеьтся около 14 тыс. чел, в т. ч. 50%-женщины, около 2 тыс. – дети в возрасте до 15 лет. умерло за год 3 млн, в т. ч – 0, 5 млн. – дети до 15 лет >В России: 1987 год – первый больной; в первые годы эпидемии чрезвычайная острота внутрибольничного заражения детей; контроль за кровью позволил избежать трагедии США, Германии, Франции, Японии, где тысячи заражены при переливании крови в 90 годы; эпидемия в России прошла первую, начальную стадию; вступила во вторую “концентрированную”, когда будет высокая инфицированность групп риска и рост в целом среди населения; не за горами третья, заключительная стадия – “генерализованной” эпидемии ;
 в на 6. 08. 03. зарегистрировано 248 тыс. больных ВИЧ-инфекцией, в том числе: • —дети – 7, 5 тыс. • —родилось от ВИЧ+ матерей – 6, 2 тыс. • —всего умерло 3454 чел. в том числе 216 детей, • —заболевание перешло в стадию СПИД – 817 чел. , в т. ч. детей – 193. • —Умерло от СПИДа – 609 чел. , в т. ч. 125 детей. Интенсивный рост больных идет в России: вновь выявлено в 1998 г. – 3, 7 тыс. , в 1999 г – 15, 6 тыс. , в 2000 г. – 58 тыс. , за 8, 5 мес. 2001 г. – 56, 2 тыс. Хотя темпы роста ВИЧ-инфекции в стране колоссальны, едва ли правомерны высказывания, в том числе и работников ВОЗ, что Россия является лидером по распространенности ВИЧ-инфекции. Достаточно проанализировать показатели. В мире в 2000 г. в день заражался ВИЧ 1 чел. из 407 тыс. жителей, в России – 1 на 1 млн. , т. е в 2, 4 раза показатель ниже (хотя в Санкт-Петербурге – 1 на 131 тыс. жителей города, т. е в 7, 6 раза тем выше ).
в на 6. 08. 03. зарегистрировано 248 тыс. больных ВИЧ-инфекцией, в том числе: • —дети – 7, 5 тыс. • —родилось от ВИЧ+ матерей – 6, 2 тыс. • —всего умерло 3454 чел. в том числе 216 детей, • —заболевание перешло в стадию СПИД – 817 чел. , в т. ч. детей – 193. • —Умерло от СПИДа – 609 чел. , в т. ч. 125 детей. Интенсивный рост больных идет в России: вновь выявлено в 1998 г. – 3, 7 тыс. , в 1999 г – 15, 6 тыс. , в 2000 г. – 58 тыс. , за 8, 5 мес. 2001 г. – 56, 2 тыс. Хотя темпы роста ВИЧ-инфекции в стране колоссальны, едва ли правомерны высказывания, в том числе и работников ВОЗ, что Россия является лидером по распространенности ВИЧ-инфекции. Достаточно проанализировать показатели. В мире в 2000 г. в день заражался ВИЧ 1 чел. из 407 тыс. жителей, в России – 1 на 1 млн. , т. е в 2, 4 раза показатель ниже (хотя в Санкт-Петербурге – 1 на 131 тыс. жителей города, т. е в 7, 6 раза тем выше ).
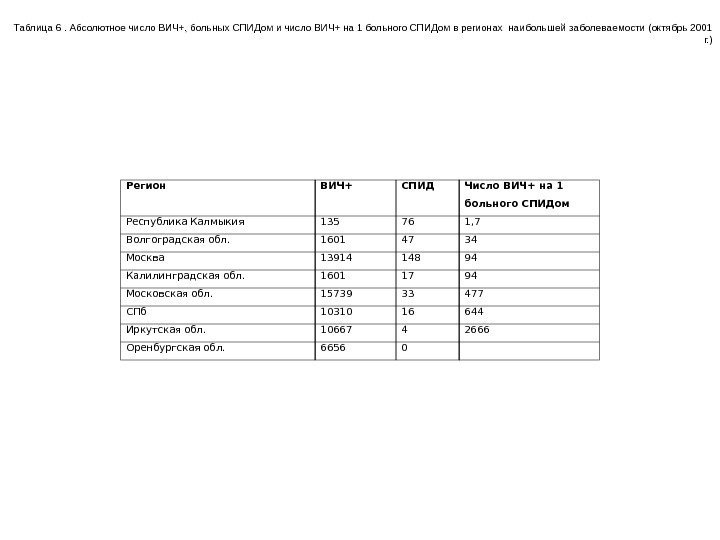
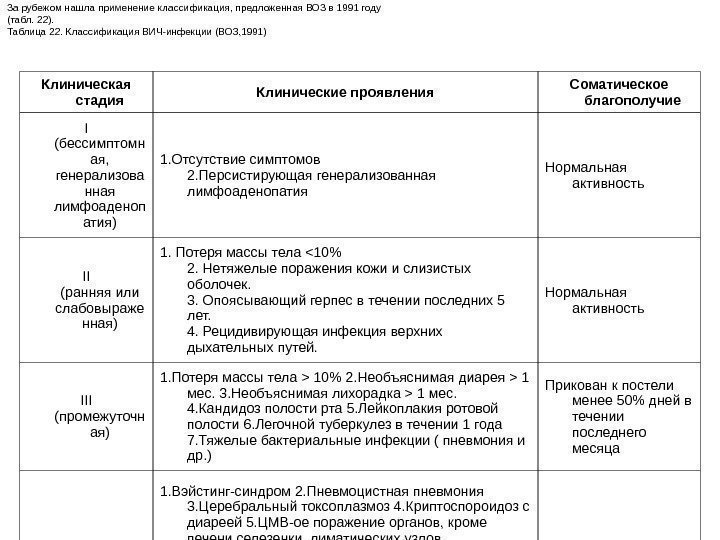
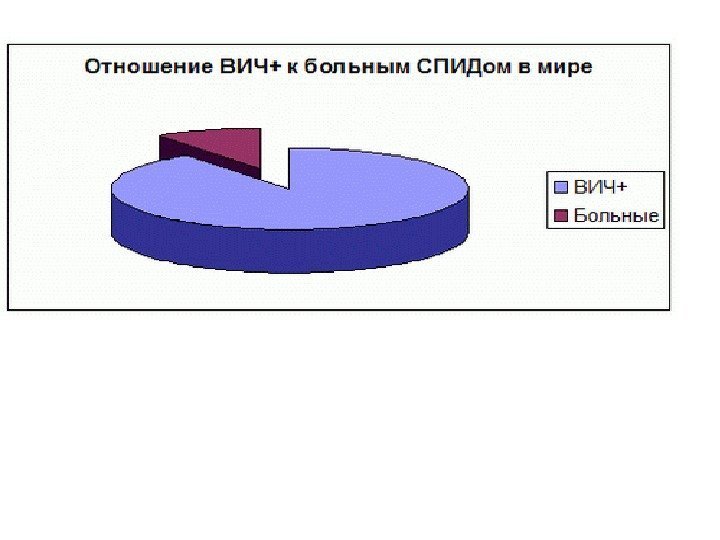
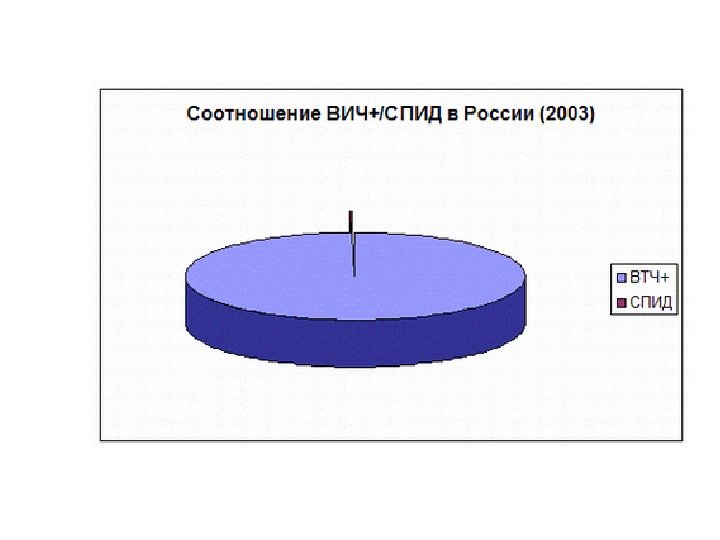
 ВИЧ+ Больные СПИД 141, 3 тыс. 0, 5 тыс } соотношение 1 на 254 (0, 33%)Если в США в 1998 насчитывалось 796 тыс. ВИЧ-инфицированных, 86% в стадия IIIB-IV, то в России: РФ на 1. 01. 2001 Таким образом, в России на сегодня клиника ВИЧ-инфекции находится на начальных этапах, с момента эпидемии, начавшейся в 1996 году, прошло лишь 5 лет. Зато в регионах, где эпидвспышка нозокоминального характера началась в 1989 году (Калмыкия, Волгоградская область), соотношение ВИЧ-инфицированных к больным в стадии СПИД намного ближе в показателям США, нежели в регионах более позднего начала эпидемии (табл. 6).
ВИЧ+ Больные СПИД 141, 3 тыс. 0, 5 тыс } соотношение 1 на 254 (0, 33%)Если в США в 1998 насчитывалось 796 тыс. ВИЧ-инфицированных, 86% в стадия IIIB-IV, то в России: РФ на 1. 01. 2001 Таким образом, в России на сегодня клиника ВИЧ-инфекции находится на начальных этапах, с момента эпидемии, начавшейся в 1996 году, прошло лишь 5 лет. Зато в регионах, где эпидвспышка нозокоминального характера началась в 1989 году (Калмыкия, Волгоградская область), соотношение ВИЧ-инфицированных к больным в стадии СПИД намного ближе в показателям США, нежели в регионах более позднего начала эпидемии (табл. 6).
 Регион ВИЧ+ СПИД Число ВИЧ+ на 1 больного СПИДом Республика Калмыкия 135 76 1, 7 Волгоградская обл. 1601 47 34 Москва 13914 148 94 Калилинградская обл. 1601 17 94 Московская обл. 15739 33 477 СПб 10310 16 644 Иркутская обл. 10667 4 2666 Оренбургская обл. 6656 0 Таблица 6. Абсолютное число ВИЧ+, больных СПИДом и число ВИЧ+ на 1 больного СПИДом в регионах наибольшей заболеваемости (октябрь 2001 г. )
Регион ВИЧ+ СПИД Число ВИЧ+ на 1 больного СПИДом Республика Калмыкия 135 76 1, 7 Волгоградская обл. 1601 47 34 Москва 13914 148 94 Калилинградская обл. 1601 17 94 Московская обл. 15739 33 477 СПб 10310 16 644 Иркутская обл. 10667 4 2666 Оренбургская обл. 6656 0 Таблица 6. Абсолютное число ВИЧ+, больных СПИДом и число ВИЧ+ на 1 больного СПИДом в регионах наибольшей заболеваемости (октябрь 2001 г. )
 Ретроспективные исследования позволяют полагать, что в США впервые СПИД стал регистрироваться в 1979 году, во всяком случае, у 9 больных была клиника СПИД, из них 7 умерли. В 1980 году таких больных насчитывалось уже 46, из которых 42 умерли. Дальнейшее валоподобное нарастание числа инфицированных и больных позволило говорить о пандемии. Причем истинное число ВИЧ-инфицированных и больных СПИДом в мире на много превышает число зарегистрированных (табл. 7). К концу 1998 года ежедневно в мире прибывало примерно 16 000 вновь инфицированных.
Ретроспективные исследования позволяют полагать, что в США впервые СПИД стал регистрироваться в 1979 году, во всяком случае, у 9 больных была клиника СПИД, из них 7 умерли. В 1980 году таких больных насчитывалось уже 46, из которых 42 умерли. Дальнейшее валоподобное нарастание числа инфицированных и больных позволило говорить о пандемии. Причем истинное число ВИЧ-инфицированных и больных СПИДом в мире на много превышает число зарегистрированных (табл. 7). К концу 1998 года ежедневно в мире прибывало примерно 16 000 вновь инфицированных.
 Регион Болезни, предающиеся половым путем Распростране нность ВИЧ-инфекци и Кумулятивны е данные по ВИЧ+ Африка 60 млн. 13, 0 млн. 16, 0 млн Азия 138 млн. 4, 0 млн. 4, 1 млн. Европа 16 млн. 0, 5 млн 0, 65 млн Северная Америка 8 млн. 0, 75 млн. 1, 3 млн. Океания 4 млн. 70 тыс. 75 тыс. Глобальные показатели 250 млн. 24 млн. Таблица 7. Географическое распространение болезней, передающихся половым путем и ВИЧ-инфекции среди взрослых на 1995 г. (по Quin T. C. , 1995)
Регион Болезни, предающиеся половым путем Распростране нность ВИЧ-инфекци и Кумулятивны е данные по ВИЧ+ Африка 60 млн. 13, 0 млн. 16, 0 млн Азия 138 млн. 4, 0 млн. 4, 1 млн. Европа 16 млн. 0, 5 млн 0, 65 млн Северная Америка 8 млн. 0, 75 млн. 1, 3 млн. Океания 4 млн. 70 тыс. 75 тыс. Глобальные показатели 250 млн. 24 млн. Таблица 7. Географическое распространение болезней, передающихся половым путем и ВИЧ-инфекции среди взрослых на 1995 г. (по Quin T. C. , 1995)
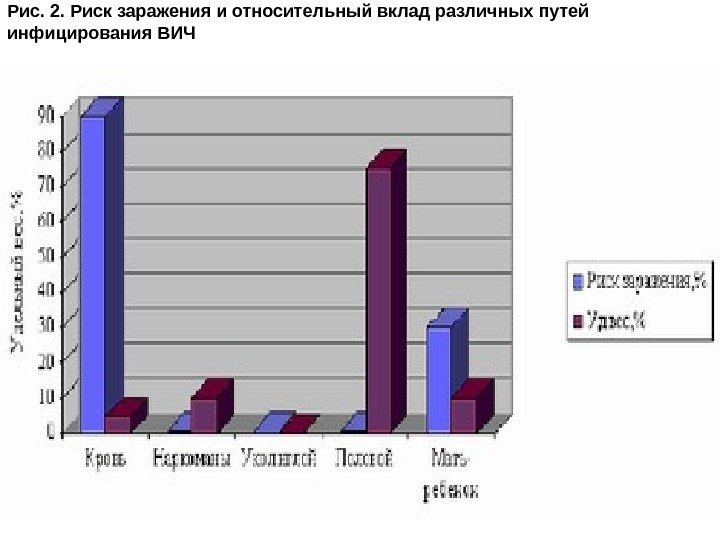
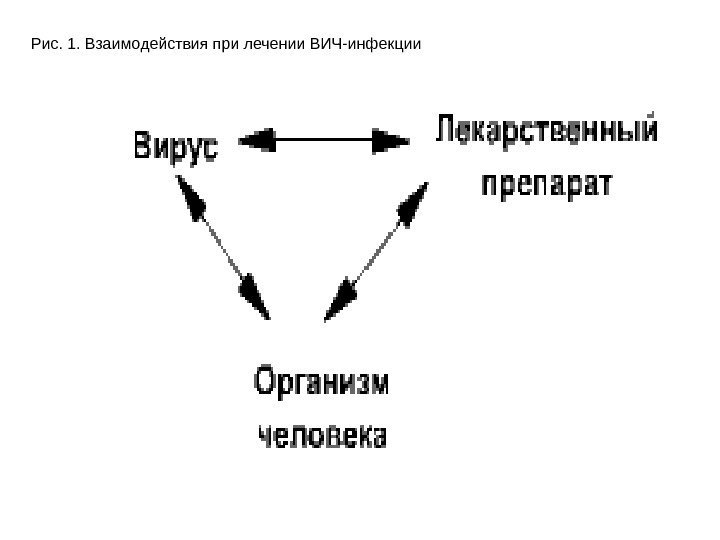
 ВИЧ передается тремя способами: при гетеросексуальных и гомосексуальных сношениях, парентерально с кровью и ее препаратами и вертикально, от инфицированной матери к ребенку внутриутробно, во время родов или вскоре после, при кормлении грудью. Прослеживается несоответствие между риском заражения и реальным вкладом различных путей инфицирования ВИЧ (рис. 2). Доминирование того или иного пути передачи варьирует в зависимости от социальных, культурных, этнических условий, особенности уклада жизни. Так, при введении человеку инфицированной крови почти все заражаются, но среди больных ВИЧ-инфекцией роль передачи с кровью не так уж велика, что и понятно, так как среди населения гемотрансфузии получает незначительная часть людей. Зато половой путь ппри сравнительно низком риске передачи, является сегодня в мире ведущим.
ВИЧ передается тремя способами: при гетеросексуальных и гомосексуальных сношениях, парентерально с кровью и ее препаратами и вертикально, от инфицированной матери к ребенку внутриутробно, во время родов или вскоре после, при кормлении грудью. Прослеживается несоответствие между риском заражения и реальным вкладом различных путей инфицирования ВИЧ (рис. 2). Доминирование того или иного пути передачи варьирует в зависимости от социальных, культурных, этнических условий, особенности уклада жизни. Так, при введении человеку инфицированной крови почти все заражаются, но среди больных ВИЧ-инфекцией роль передачи с кровью не так уж велика, что и понятно, так как среди населения гемотрансфузии получает незначительная часть людей. Зато половой путь ппри сравнительно низком риске передачи, является сегодня в мире ведущим.
 Рис. 2. Риск заражения и относительный вклад различных путей инфицирования ВИЧ
Рис. 2. Риск заражения и относительный вклад различных путей инфицирования ВИЧ
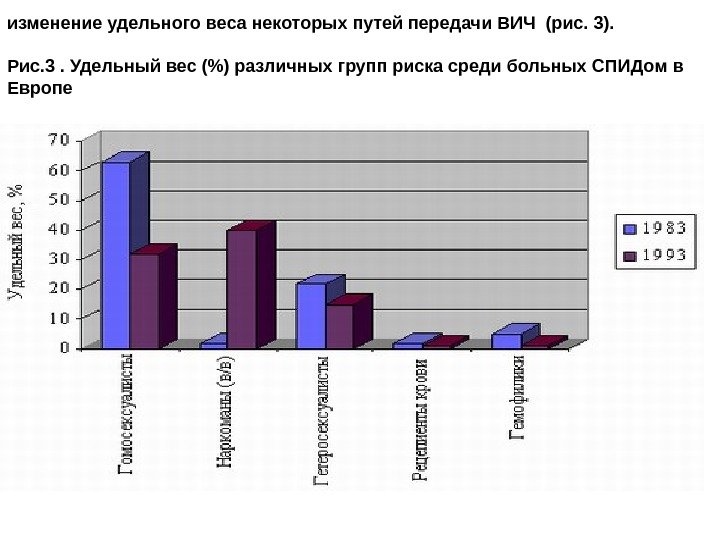
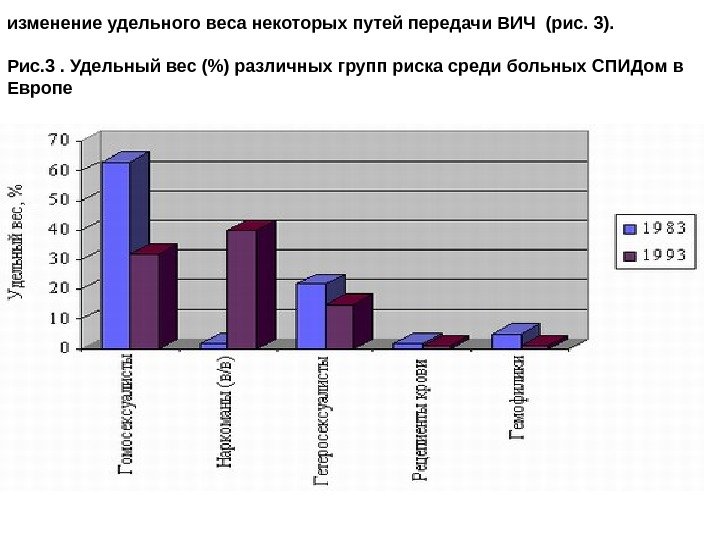
 изменение удельного веса некоторых путей передачи ВИЧ (рис. 3). Рис. 3. Удельный вес (%) различных групп риска среди больных СПИДом в Европе
изменение удельного веса некоторых путей передачи ВИЧ (рис. 3). Рис. 3. Удельный вес (%) различных групп риска среди больных СПИДом в Европе
 Вид передачи ВИЧ Уд. вес, % Сексуальный 70 -80 Перинатальный 5 -10 Инъекционный 5 -10 Через кровь и ее препараты 5 -10 По данным американских исследователей в первое десятилетие пандемии 65% приходилось на половой путь передачи, 17% на парентеральный при внутривенном введении лекарственных препаратов, 10% заражались при введении препаратов крови при гемофилии, 2% — при переливании крови по другим причинам, в 5 -6% причину установить не удавалось. В 1997 год в мире по-прежнему ведущим сохранился сексуальный путь передачи (табл. 8). В Таблица 8 Удельный вес различных путей передачи ВИЧ в мире (по Т. Mertens, P. Piot, 1997)
Вид передачи ВИЧ Уд. вес, % Сексуальный 70 -80 Перинатальный 5 -10 Инъекционный 5 -10 Через кровь и ее препараты 5 -10 По данным американских исследователей в первое десятилетие пандемии 65% приходилось на половой путь передачи, 17% на парентеральный при внутривенном введении лекарственных препаратов, 10% заражались при введении препаратов крови при гемофилии, 2% — при переливании крови по другим причинам, в 5 -6% причину установить не удавалось. В 1997 год в мире по-прежнему ведущим сохранился сексуальный путь передачи (табл. 8). В Таблица 8 Удельный вес различных путей передачи ВИЧ в мире (по Т. Mertens, P. Piot, 1997)
 изменение удельного веса некоторых путей передачи ВИЧ (рис. 3). Рис. 3. Удельный вес (%) различных групп риска среди больных СПИДом в Европе
изменение удельного веса некоторых путей передачи ВИЧ (рис. 3). Рис. 3. Удельный вес (%) различных групп риска среди больных СПИДом в Европе
 Европе гомо- и бисексуалисты среди инфицированных составляли 60 -70 %, наркоманы — 10 -15, больные гемофилией — 1 — 5 % в первые годы пандемии, но с 1985 по 1992 год удельный вес инфицированных, связанный с гомосексуальным путем передами сократился с 62% до 36%, в то время как процент передачи ВИЧ с парентеральными наркотиками увеличился с 16 до 40% (Квинн Т. С. , 1996). Но если в Чехии и Словакии до 70%, в Болгарии до 75% , большинство инфицированных в скандинавских странах заразились при гомо- и бисексуальном контакте, то в 70% в Италии и Испании инфицирование произошло парентеральным путем с приемом наркотических средств. В Африке среди больных гомосексуалисты и наркоманы составляли вместе лишь 5%, в ЮАР — 10 %.
Европе гомо- и бисексуалисты среди инфицированных составляли 60 -70 %, наркоманы — 10 -15, больные гемофилией — 1 — 5 % в первые годы пандемии, но с 1985 по 1992 год удельный вес инфицированных, связанный с гомосексуальным путем передами сократился с 62% до 36%, в то время как процент передачи ВИЧ с парентеральными наркотиками увеличился с 16 до 40% (Квинн Т. С. , 1996). Но если в Чехии и Словакии до 70%, в Болгарии до 75% , большинство инфицированных в скандинавских странах заразились при гомо- и бисексуальном контакте, то в 70% в Италии и Испании инфицирование произошло парентеральным путем с приемом наркотических средств. В Африке среди больных гомосексуалисты и наркоманы составляли вместе лишь 5%, в ЮАР — 10 %.
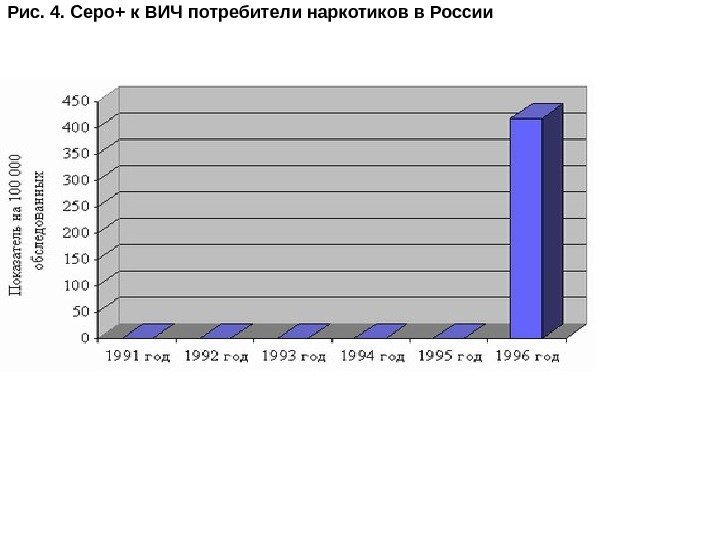
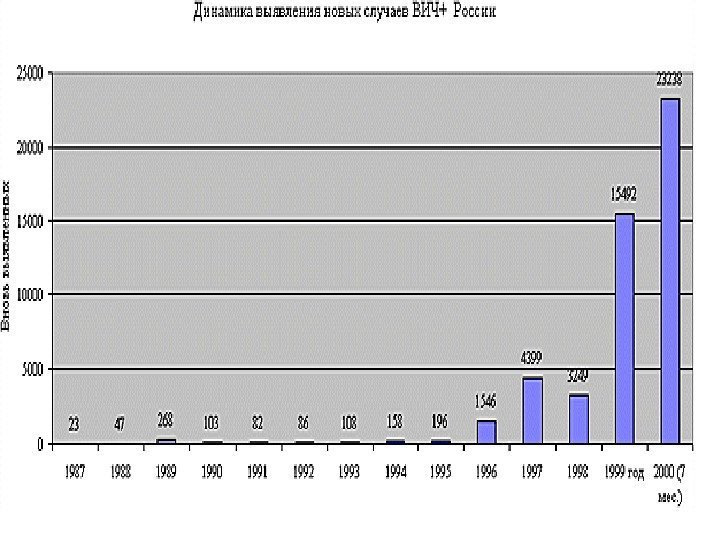
 Если в 1997 году, как в мире, так и в Европе по-прежнему доминировал гомосексуальный путь передачи, то в России — гемоконтактный, обусловленный приемом парентерально наркотических средств, пришедший на смену сексуальному пути передачи, преобладавшему 10 лет назад. Стала стремительно расти инфицированность ВИЧ внутривенных потребителей наркуотических средств (рис. 4) До 1996 года в России среди ВИЧ+ доминировали приезжающие на учебу иностранцы и ведущим был гомосексуальный контакт. С 1996 года в различных регионах страны ситуация стала меняться в связи с начавшейся эпидемией. Поэтому к концу 1997 года на долю инфицированных парентерально с введением наркотических средств по России приходилось свыше 60%, а в некоторых регионах до 80% и более. В Калининграде лишь 5% больных инфицировались половым путем, среди инфицированных 77, 4% мужчины, 55, 4% — лица в возрасте 20 -30 лет
Если в 1997 году, как в мире, так и в Европе по-прежнему доминировал гомосексуальный путь передачи, то в России — гемоконтактный, обусловленный приемом парентерально наркотических средств, пришедший на смену сексуальному пути передачи, преобладавшему 10 лет назад. Стала стремительно расти инфицированность ВИЧ внутривенных потребителей наркуотических средств (рис. 4) До 1996 года в России среди ВИЧ+ доминировали приезжающие на учебу иностранцы и ведущим был гомосексуальный контакт. С 1996 года в различных регионах страны ситуация стала меняться в связи с начавшейся эпидемией. Поэтому к концу 1997 года на долю инфицированных парентерально с введением наркотических средств по России приходилось свыше 60%, а в некоторых регионах до 80% и более. В Калининграде лишь 5% больных инфицировались половым путем, среди инфицированных 77, 4% мужчины, 55, 4% — лица в возрасте 20 -30 лет
 Рис. 4. Серо+ к ВИЧ потребители наркотиков в России
Рис. 4. Серо+ к ВИЧ потребители наркотиков в России
 На рубеже веков можно говорить о двух эпидемиях – ВИЧ-инфекции и наркомании, при этом между ними прослеживается тесная связь. В мире только с 1985 по 1994 год увеличилось производство кока на 200%, опиума — на 300%. Примерно половина потребителей инъекционных наркотиков за 18 мес. становятся ВИЧ-инфицированными. Например, в Банконге увеличился удельный вес ВИЧ-инфицированных среди наркоманов с 1 до 50%. Среди инфицированных обычно преобладают люди молодого возраста, но, учитывая многолетний период инкубации, среди больных СПИДом превалируют лица в возрасте 30 -39 лет. Соотношение мужчин к женщинам по данным ВОЗ составляет 10 -15/1, в США на мужчин приходится 93%. В то же время в Африке в одинаковой степени инфицированы мужчины и женщины, в СНГ на долю мужчин приходится 62, 5%.
На рубеже веков можно говорить о двух эпидемиях – ВИЧ-инфекции и наркомании, при этом между ними прослеживается тесная связь. В мире только с 1985 по 1994 год увеличилось производство кока на 200%, опиума — на 300%. Примерно половина потребителей инъекционных наркотиков за 18 мес. становятся ВИЧ-инфицированными. Например, в Банконге увеличился удельный вес ВИЧ-инфицированных среди наркоманов с 1 до 50%. Среди инфицированных обычно преобладают люди молодого возраста, но, учитывая многолетний период инкубации, среди больных СПИДом превалируют лица в возрасте 30 -39 лет. Соотношение мужчин к женщинам по данным ВОЗ составляет 10 -15/1, в США на мужчин приходится 93%. В то же время в Африке в одинаковой степени инфицированы мужчины и женщины, в СНГ на долю мужчин приходится 62, 5%.
 В первые же годы распространения ВИЧ-инфекции были определены группы риска: гомосексуалисты, наркоманы в случаях введения наркотических средств парентерально, проститутки и лица с заболеваниями, требующими частого повторного введения крови и ее препаратов, в частности больные гемофилией. Преимущественное распространение ВИЧ-инфекции в первые годы пандемии среди гомосексуалистов объяснялись частой травматизацией до крови гениталий при этом виде половой связи и проникновение с кровью возбудителя. Но по мере развития пандемии инфекция все больше захватывает основную часть популяции — гетеросексуалов, так как вирус набрал “критическую массу” и обеспечил достаточную эффективность передачи как от мужчины к женщине, так и наоборот, т. е. на основную популяцию населения.
В первые же годы распространения ВИЧ-инфекции были определены группы риска: гомосексуалисты, наркоманы в случаях введения наркотических средств парентерально, проститутки и лица с заболеваниями, требующими частого повторного введения крови и ее препаратов, в частности больные гемофилией. Преимущественное распространение ВИЧ-инфекции в первые годы пандемии среди гомосексуалистов объяснялись частой травматизацией до крови гениталий при этом виде половой связи и проникновение с кровью возбудителя. Но по мере развития пандемии инфекция все больше захватывает основную часть популяции — гетеросексуалов, так как вирус набрал “критическую массу” и обеспечил достаточную эффективность передачи как от мужчины к женщине, так и наоборот, т. е. на основную популяцию населения.
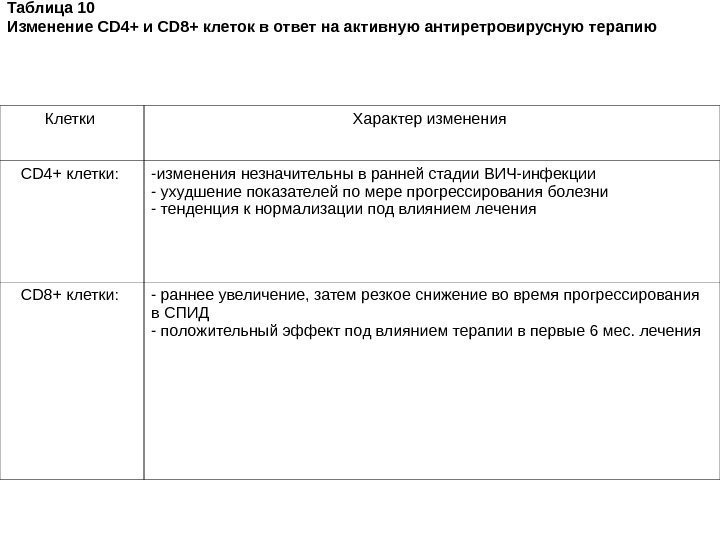
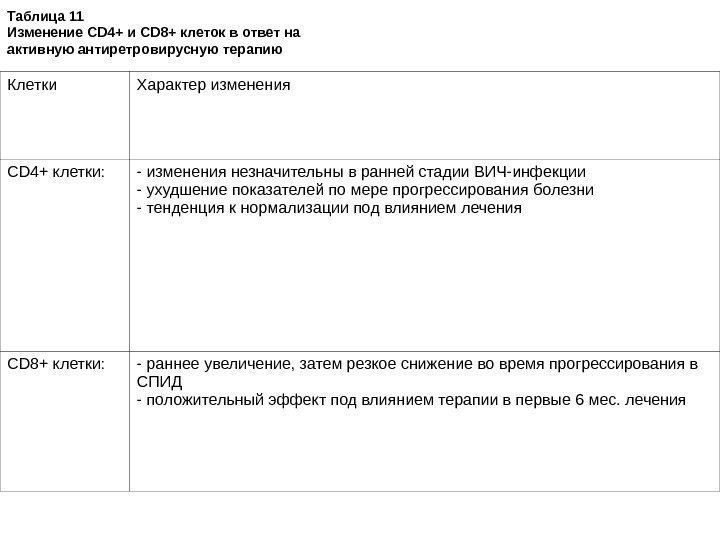
 Путь передачи Риск инфицирования Половые сношения Передача женщины-мужчине 1 из 700 — 3000 Передача мужчины-женщине 1 из 200 — 2000 Передача мужчины-мужчине 1 из 10 — 1600 Фелляция 6 -8 % Иглы Укол иглой 1 из 200 Использование совместной иглы 1 из 150 Переливание инфицированной крови 95 из 100 Передача от матери младенцу Без лечения азидотимидином 1 в 3 -5 случаях При лечении азидотимидином <1 из 10 случаев Комбинированная антиретровирусная терапия 1 из 50 случаев. Таблица 9. Риск передачи ВИЧ (Royce RA, et al. , 1997)
Путь передачи Риск инфицирования Половые сношения Передача женщины-мужчине 1 из 700 — 3000 Передача мужчины-женщине 1 из 200 — 2000 Передача мужчины-мужчине 1 из 10 — 1600 Фелляция 6 -8 % Иглы Укол иглой 1 из 200 Использование совместной иглы 1 из 150 Переливание инфицированной крови 95 из 100 Передача от матери младенцу Без лечения азидотимидином 1 в 3 -5 случаях При лечении азидотимидином <1 из 10 случаев Комбинированная антиретровирусная терапия 1 из 50 случаев. Таблица 9. Риск передачи ВИЧ (Royce RA, et al. , 1997)
 Являются факторами предачи Инфективны х ед. в 1 мл биологическ ой жидкости Не являются факторами передачи Инфективны х ед. в 1 мл биологическ ой жидкости Грудное молоко < 1 Слезы < 1 Вагинальный секрет < 1 Слюна < 1 Семенная жидкость 10 -50 Пот < 1 Кровь до 3000 Таблица 10. Факторы передачи ВИЧ
Являются факторами предачи Инфективны х ед. в 1 мл биологическ ой жидкости Не являются факторами передачи Инфективны х ед. в 1 мл биологическ ой жидкости Грудное молоко < 1 Слезы < 1 Вагинальный секрет < 1 Слюна < 1 Семенная жидкость 10 -50 Пот < 1 Кровь до 3000 Таблица 10. Факторы передачи ВИЧ
 Группа инфицированных Частота инфицироания партнера, % От мужчины к женщине Партнерши серопозитивных больных СПИДом 54 Партнерши серопозитивных бисексуальных мужчин 14 Жены серопозитивных больных гемофилией 7 -9 От женщины к мужчине Партнеры женщин, больных СПИДом 65 Таблица 11. Эффективность передачи ВИЧ при гетеросексуальном контакте
Группа инфицированных Частота инфицироания партнера, % От мужчины к женщине Партнерши серопозитивных больных СПИДом 54 Партнерши серопозитивных бисексуальных мужчин 14 Жены серопозитивных больных гемофилией 7 -9 От женщины к мужчине Партнеры женщин, больных СПИДом 65 Таблица 11. Эффективность передачи ВИЧ при гетеросексуальном контакте
 Четко выявляется и зависимость инфицирования от того, используются ли индивидуальные средства защиты от инфекции во время полового сношения. В целом же в течении одного года в семейных парах вероятность заражения от одного к другому партнеру составляет 90%. Прослеживается взаимосвязь между распространением ВИЧ-инфекции и другими венерическими заболеваниями. Причем скорость распространения ВИЧ через лиц, одновременно страдающих венерическими болезнями, увеличивается до 20 раз. Это обусловлено тем, что при многих венерических заболеваниях имеется язвенное поражение гениталий, которые облегчают проникновение вируса. Кроме того, у больных венерическими заболеваниями формируется иммунодефицит, способствующий в случае инфицирования более высокому риску развития болезни, чем у исходно здорового человека. Следует отметить, что 80% гомосексуалистов болеют различными венерическими заболеваниями.
Четко выявляется и зависимость инфицирования от того, используются ли индивидуальные средства защиты от инфекции во время полового сношения. В целом же в течении одного года в семейных парах вероятность заражения от одного к другому партнеру составляет 90%. Прослеживается взаимосвязь между распространением ВИЧ-инфекции и другими венерическими заболеваниями. Причем скорость распространения ВИЧ через лиц, одновременно страдающих венерическими болезнями, увеличивается до 20 раз. Это обусловлено тем, что при многих венерических заболеваниях имеется язвенное поражение гениталий, которые облегчают проникновение вируса. Кроме того, у больных венерическими заболеваниями формируется иммунодефицит, способствующий в случае инфицирования более высокому риску развития болезни, чем у исходно здорового человека. Следует отметить, что 80% гомосексуалистов болеют различными венерическими заболеваниями.
 Группу риска по ВИЧ-инфицированности составляют не только лица с беспорядочными половыми связями, но, особенно, лица, находящиеся в местах лишения свободы, что вполне объяснимо, ибо нет в мире тюрьмы, где бы не были распространены и наркомания и гомосексуализм. В большинстве стран мира регистрации подлежат только ВИЧ-инфицированные с клиникой СПИДа, основная же часть серопозитивных к ВИЧ остается без учета. Имеется прогноз на ближайшие годы (табл. 12). К концу ХХ века зараженных ожидается около 38 млн. , а по оценкам некоторых эпидемиологов истинное число — около 110 млн. За первые 8 лет изучения ВИЧ-инфекции число больных в мире приблизилось к 200 тысячам, а инфицированных — к 10 -15 млн. человек. Ежемесячно регистрируется свыше 60 тыс. вновь инфицированных, каждые 4 мин. в мире регистрируется новый больной СПИД, каждые 15 сек. — новый зараженный ВИЧ. Примерно 90% ВИЧ-инфицированных живут в развивающихся странах. По данным В. И. Покровского (1989) к 2000 году на территории бывшего СССР ожидается около 30 тыс. больных СПИД и около 1 млн. 45 тыс. инфицированных.
Группу риска по ВИЧ-инфицированности составляют не только лица с беспорядочными половыми связями, но, особенно, лица, находящиеся в местах лишения свободы, что вполне объяснимо, ибо нет в мире тюрьмы, где бы не были распространены и наркомания и гомосексуализм. В большинстве стран мира регистрации подлежат только ВИЧ-инфицированные с клиникой СПИДа, основная же часть серопозитивных к ВИЧ остается без учета. Имеется прогноз на ближайшие годы (табл. 12). К концу ХХ века зараженных ожидается около 38 млн. , а по оценкам некоторых эпидемиологов истинное число — около 110 млн. За первые 8 лет изучения ВИЧ-инфекции число больных в мире приблизилось к 200 тысячам, а инфицированных — к 10 -15 млн. человек. Ежемесячно регистрируется свыше 60 тыс. вновь инфицированных, каждые 4 мин. в мире регистрируется новый больной СПИД, каждые 15 сек. — новый зараженный ВИЧ. Примерно 90% ВИЧ-инфицированных живут в развивающихся странах. По данным В. И. Покровского (1989) к 2000 году на территории бывшего СССР ожидается около 30 тыс. больных СПИД и около 1 млн. 45 тыс. инфицированных.
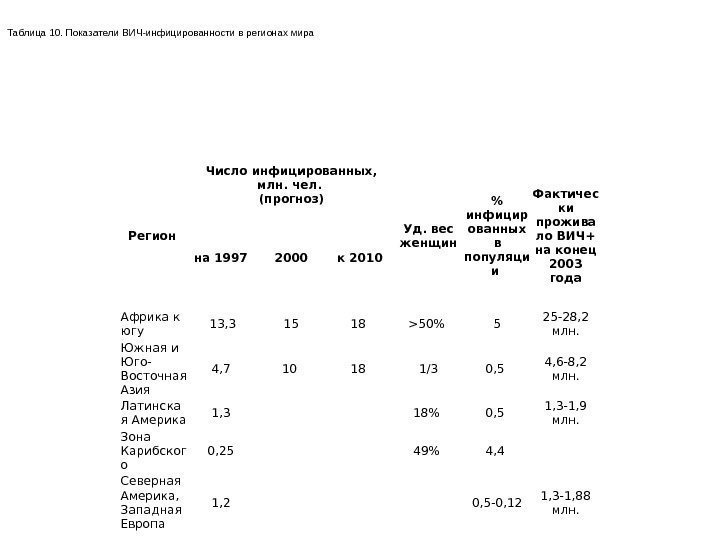
 Регион Число инфицированных, млн. чел. (прогноз) Уд. вес женщин % инфицир ованных в популяци и Фактичес ки прожива ло ВИЧ+ на конец 2003 годана 1997 2000 к 2010 Африка к югу 13, 3 15 18 >50% 5 25 -28, 2 млн. Южная и Юго- Восточная Азия 4, 7 10 18 1/3 0, 5 4, 6 -8, 2 млн. Латинска я Америка 1, 3 18% 0, 5 1, 3 -1, 9 млн. Зона Карибског о 0, 25 49% 4, 4 Северная Америка, Западная Европа 1, 2 0, 5 -0, 12 1, 3 -1, 88 млн. Таблица 10. Показатели ВИЧ-инфицированности в регионах мира
Регион Число инфицированных, млн. чел. (прогноз) Уд. вес женщин % инфицир ованных в популяци и Фактичес ки прожива ло ВИЧ+ на конец 2003 годана 1997 2000 к 2010 Африка к югу 13, 3 15 18 >50% 5 25 -28, 2 млн. Южная и Юго- Восточная Азия 4, 7 10 18 1/3 0, 5 4, 6 -8, 2 млн. Латинска я Америка 1, 3 18% 0, 5 1, 3 -1, 9 млн. Зона Карибског о 0, 25 49% 4, 4 Северная Америка, Западная Европа 1, 2 0, 5 -0, 12 1, 3 -1, 88 млн. Таблица 10. Показатели ВИЧ-инфицированности в регионах мира
 Если первоначально считали, что женщин СПИД не поражает, то на сегодня увеличивается число случаев ВИЧ-инфекции среди женщин. Среди них группу риска составляют лица, представляющие сексуальные услуги на коммерческой основе (табл. 13). При этом, степень инфицирования в значительной мере зависит от использования индивидуальных средств защиты, как среди женщин, так и мужчин (табл. 14). Среди гомосексуалистов (исключая наркоманов) темп роста начал уменьшаться с 1987 года. Эпидемиологические исследования показали, что частота заражения женщин от мужчин при половом контакте в 3 раза выше, чем мужчин от инфицированных женщин (Покровский В. И. , 1996). Однако, наблюдения в Тайланде показали, что передача ВИЧ от женщин к мужчинам в 30 -50 раз выше, чем полагали ранее.
Если первоначально считали, что женщин СПИД не поражает, то на сегодня увеличивается число случаев ВИЧ-инфекции среди женщин. Среди них группу риска составляют лица, представляющие сексуальные услуги на коммерческой основе (табл. 13). При этом, степень инфицирования в значительной мере зависит от использования индивидуальных средств защиты, как среди женщин, так и мужчин (табл. 14). Среди гомосексуалистов (исключая наркоманов) темп роста начал уменьшаться с 1987 года. Эпидемиологические исследования показали, что частота заражения женщин от мужчин при половом контакте в 3 раза выше, чем мужчин от инфицированных женщин (Покровский В. И. , 1996). Однако, наблюдения в Тайланде показали, что передача ВИЧ от женщин к мужчинам в 30 -50 раз выше, чем полагали ранее.
 Страна ВИЧ-инфицированные проститутки, % Камерун, Доула, . 10, 9 Центральноафриканская республика, Банги, . 17, 0 Конго, Пуэнт-Наур, . 64, 1 Эфиопия, Аддис-Абеба, . 18, 2 Кения, Найроби, . 87, 8 Малави, . 55, 9 Танзания, Аруша, . 75, 0 Буркина-Фасо 44, 7 Джибути 41, 4 Гаити, Порт-0 Пренс, . 41, 0 Гондурас, . 35, 0 Индия, Нью-Дели, . 30, 1 Тайланд, Ранонг, . 52, 2 Таблица 13. Частота ВИЧ-инфекции у лиц, представляющи сексуальные услуги на коммерческой основе (по Абоаги-Квартенг Т. и Муди Р. , 1997)
Страна ВИЧ-инфицированные проститутки, % Камерун, Доула, . 10, 9 Центральноафриканская республика, Банги, . 17, 0 Конго, Пуэнт-Наур, . 64, 1 Эфиопия, Аддис-Абеба, . 18, 2 Кения, Найроби, . 87, 8 Малави, . 55, 9 Танзания, Аруша, . 75, 0 Буркина-Фасо 44, 7 Джибути 41, 4 Гаити, Порт-0 Пренс, . 41, 0 Гондурас, . 35, 0 Индия, Нью-Дели, . 30, 1 Тайланд, Ранонг, . 52, 2 Таблица 13. Частота ВИЧ-инфекции у лиц, представляющи сексуальные услуги на коммерческой основе (по Абоаги-Квартенг Т. и Муди Р. , 1997)
 Восприимчивость к вирусу здоровых людей определяется стадией болезни зараженного партнера: при интенсивной виремии выше риск. Иными словами, в динамике развития болезни растет концентрация вируса в биологических субстратах, что увеличивает риск заражения партнера. У детей в 80 -90% заражение связано с инфицированием во время беременности, родов или вскармливания грудным молоком. Последнее обусловлено тем, что у 70% ВИЧ-позитивных матерей вирус выявляется в молоке сразу после родов и в 53% через год. Поэтому примерно треть ВИЧ-инфицированных от матерей детей заражаются через молоко. И только 5 -10% детей инфицируются инъекционным путем, в 3 -5% через кровь и ее препараты.
Восприимчивость к вирусу здоровых людей определяется стадией болезни зараженного партнера: при интенсивной виремии выше риск. Иными словами, в динамике развития болезни растет концентрация вируса в биологических субстратах, что увеличивает риск заражения партнера. У детей в 80 -90% заражение связано с инфицированием во время беременности, родов или вскармливания грудным молоком. Последнее обусловлено тем, что у 70% ВИЧ-позитивных матерей вирус выявляется в молоке сразу после родов и в 53% через год. Поэтому примерно треть ВИЧ-инфицированных от матерей детей заражаются через молоко. И только 5 -10% детей инфицируются инъекционным путем, в 3 -5% через кровь и ее препараты.
 Если первоначально считали, что женщин СПИД не поражает, то на сегодня увеличивается число случаев ВИЧ-инфекции среди женщин. Среди них группу риска составляют лица, представляющие сексуальные услуги на коммерческой основе (табл. 13). При этом, степень инфицирования в значительной мере зависит от использования индивидуальных средств защиты, как среди женщин, так и мужчин (табл. 14). Среди гомосексуалистов (исключая наркоманов) темп роста начал уменьшаться с 1987 года. Эпидемиологические исследования показали, что частота заражения женщин от мужчин при половом контакте в 3 раза выше, чем мужчин от инфицированных женщин (Покровский В. И. , 1996). Однако, наблюдения в Тайланде показали, что передача ВИЧ от женщин к мужчинам в 30 -50 раз выше, чем полагали ранее.
Если первоначально считали, что женщин СПИД не поражает, то на сегодня увеличивается число случаев ВИЧ-инфекции среди женщин. Среди них группу риска составляют лица, представляющие сексуальные услуги на коммерческой основе (табл. 13). При этом, степень инфицирования в значительной мере зависит от использования индивидуальных средств защиты, как среди женщин, так и мужчин (табл. 14). Среди гомосексуалистов (исключая наркоманов) темп роста начал уменьшаться с 1987 года. Эпидемиологические исследования показали, что частота заражения женщин от мужчин при половом контакте в 3 раза выше, чем мужчин от инфицированных женщин (Покровский В. И. , 1996). Однако, наблюдения в Тайланде показали, что передача ВИЧ от женщин к мужчинам в 30 -50 раз выше, чем полагали ранее.
 По данным различных авторов ВИЧ-инфицированные матери в развитых странах в 1/4 -1/3 заражают детей, а в развивающихся странах и того выше — в 40 -50%. Прослеживается тесная связь между уровнем вирусной нагрузки на плазму матери в последние месяцы беременности и способностью ее заразить ребенка. Но если CD 4+ лимфоцитов менее 200 в 1 мкл, способность матери заразить ребенка уже не зависит от вирусной нагрузки на плазму. Лечение матери зидовудином в последний месяц и дача препарата ребенку снижают риск его инфицирования с 26 до 8%, т. е. в 3 раза. Самый высокий показатель инфицирования ВИЧ приходится на Африку, регионы Карибского моря и Южной Азии. Распространенность инфекции тесно связана с социальным фактором — на индустриально развитые страны приходится 6% от всех инфицированных и 94% на развивающиеся страны. К примеру, в 1994 году при ежедневном инфицировании примерно 6 -10 тыс. человек половина приходилось на жителей Африканского континента и 40% — жителей Юга Азии. Из числа имевших развернутую клинику СПИД в 1994 году 85% были жителями Африки, 7% — Западной Европы и Океании.
По данным различных авторов ВИЧ-инфицированные матери в развитых странах в 1/4 -1/3 заражают детей, а в развивающихся странах и того выше — в 40 -50%. Прослеживается тесная связь между уровнем вирусной нагрузки на плазму матери в последние месяцы беременности и способностью ее заразить ребенка. Но если CD 4+ лимфоцитов менее 200 в 1 мкл, способность матери заразить ребенка уже не зависит от вирусной нагрузки на плазму. Лечение матери зидовудином в последний месяц и дача препарата ребенку снижают риск его инфицирования с 26 до 8%, т. е. в 3 раза. Самый высокий показатель инфицирования ВИЧ приходится на Африку, регионы Карибского моря и Южной Азии. Распространенность инфекции тесно связана с социальным фактором — на индустриально развитые страны приходится 6% от всех инфицированных и 94% на развивающиеся страны. К примеру, в 1994 году при ежедневном инфицировании примерно 6 -10 тыс. человек половина приходилось на жителей Африканского континента и 40% — жителей Юга Азии. Из числа имевших развернутую клинику СПИД в 1994 году 85% были жителями Африки, 7% — Западной Европы и Океании.
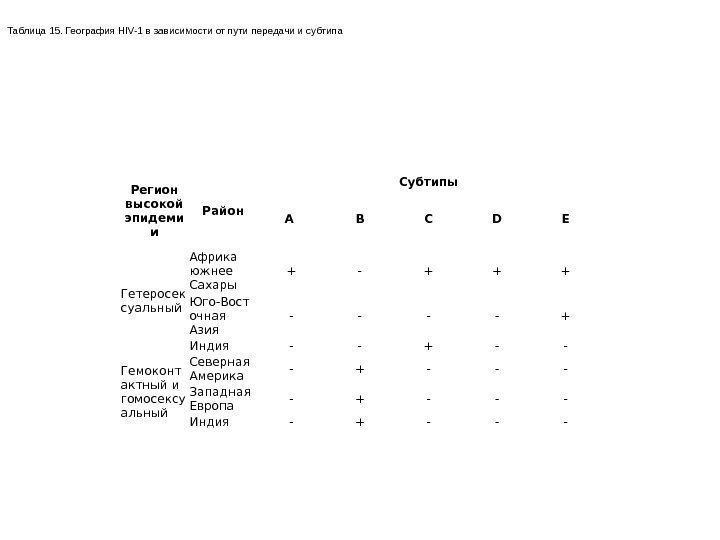
 Неравномерно распространены в мире и типы ВИЧ, в частности ВИЧ-2 в одних регионах не встречается, в других 1/4 проституток инфицирована этим типом вируса. Распространенность различных субтипов ВИЧ-1 зависит во многом от пути инфицирования (табл. 15).
Неравномерно распространены в мире и типы ВИЧ, в частности ВИЧ-2 в одних регионах не встречается, в других 1/4 проституток инфицирована этим типом вируса. Распространенность различных субтипов ВИЧ-1 зависит во многом от пути инфицирования (табл. 15).
 Регион высокой эпидеми и Район Субтипы А В С D E Гетеросек суальный Африка южнее Сахары + — + + + Юго-Вост очная Азия — — + Индия — — + — — Гемоконт актный и гомосексу альный Северная Америка — + — — — Западная Европа — + — — — Индия — + — — -Таблица 15. География HIV-1 в зависимости от пути передачи и субтипа
Регион высокой эпидеми и Район Субтипы А В С D E Гетеросек суальный Африка южнее Сахары + — + + + Юго-Вост очная Азия — — + Индия — — + — — Гемоконт актный и гомосексу альный Северная Америка — + — — — Западная Европа — + — — — Индия — + — — -Таблица 15. География HIV-1 в зависимости от пути передачи и субтипа
 Глобальное распространение ВИЧ-инфекции проявляется многочисленными эпидемиями в различных регионах со своей динамикой развития, особенностями путей передачи, численностью инфицированных. , уровнем смертности среди инфицированных и дальнейшего характера эпидемии. Т. С. Квинн (1996) представляет характеристику тенденций эпидемий ВИЧ-инфекции в различных регионах мира. Если в странах Северной Америки, Карибского бассейна Латинской Америки, Океании наметилась тенденция к снижению эпидемий, в Европе стабилизация, то в регионах Северо-Восточной и Юго-Восточной Азии эпидемии только на подъеме. Наиболее взрывоопасная обстановка в Индии, Тайланде, Бирме. В регионе стран Азии и Африки (южнее Сахары) при сохранившемся масштабе инфицирования к 2000 году окажется около 90% всех инфицированных в мире. Уже в 1994 году в Уганде уровень смертности среди ВИЧ-инфицированных взрослых мужчин составил более 100 на 1000 человеко-лет наблюдений, что на порядок выше аналогичного показателя среди неинфицированных взрослых (Mulder D. W. et al. , 1994).
Глобальное распространение ВИЧ-инфекции проявляется многочисленными эпидемиями в различных регионах со своей динамикой развития, особенностями путей передачи, численностью инфицированных. , уровнем смертности среди инфицированных и дальнейшего характера эпидемии. Т. С. Квинн (1996) представляет характеристику тенденций эпидемий ВИЧ-инфекции в различных регионах мира. Если в странах Северной Америки, Карибского бассейна Латинской Америки, Океании наметилась тенденция к снижению эпидемий, в Европе стабилизация, то в регионах Северо-Восточной и Юго-Восточной Азии эпидемии только на подъеме. Наиболее взрывоопасная обстановка в Индии, Тайланде, Бирме. В регионе стран Азии и Африки (южнее Сахары) при сохранившемся масштабе инфицирования к 2000 году окажется около 90% всех инфицированных в мире. Уже в 1994 году в Уганде уровень смертности среди ВИЧ-инфицированных взрослых мужчин составил более 100 на 1000 человеко-лет наблюдений, что на порядок выше аналогичного показателя среди неинфицированных взрослых (Mulder D. W. et al. , 1994).
 К особенностям пандемии ВИЧ-инфекции также следует отнести изменение удельного веса различных субтипов (клайдов) ВИЧ-1 в динамике. К 2000 году на первое место выходят субтипы Е и С и намечается тенденция к снижению распространения субтипов D и В. Особенности эпидемиологии ВИЧ-инфекции определяют и тактику предупреждения в каждом конкретном регионе мира. Так, например, преобладающее заражение при гомо- и гетеросексуальном контакте в Европе определило распределение финансовых средств на лечение и профилактику. Среди наркоманов нужен иной подход к предупреждению инфекции. Так, проведенные в Великобритании исследования наглядно демонстрируют эффективность одних и безрезультатность других подходов. В Глазго в целях снижения риска инфицирования наркоманов вели свободную продажу шприцев, бесплатный обмен их для наркоманов, за 18 месяцев наблюдения уровень ВИЧ-инфицированности до начала исследований составлял 1% и не изменился к концу наблюдения, а в Эдинбурге, где ввели методы запрета и полицейского контроля, уровень ВИЧ-инфицирования среди внутривенных наркоманов возрос за этот же период с 1 до 50%.
К особенностям пандемии ВИЧ-инфекции также следует отнести изменение удельного веса различных субтипов (клайдов) ВИЧ-1 в динамике. К 2000 году на первое место выходят субтипы Е и С и намечается тенденция к снижению распространения субтипов D и В. Особенности эпидемиологии ВИЧ-инфекции определяют и тактику предупреждения в каждом конкретном регионе мира. Так, например, преобладающее заражение при гомо- и гетеросексуальном контакте в Европе определило распределение финансовых средств на лечение и профилактику. Среди наркоманов нужен иной подход к предупреждению инфекции. Так, проведенные в Великобритании исследования наглядно демонстрируют эффективность одних и безрезультатность других подходов. В Глазго в целях снижения риска инфицирования наркоманов вели свободную продажу шприцев, бесплатный обмен их для наркоманов, за 18 месяцев наблюдения уровень ВИЧ-инфицированности до начала исследований составлял 1% и не изменился к концу наблюдения, а в Эдинбурге, где ввели методы запрета и полицейского контроля, уровень ВИЧ-инфицирования среди внутривенных наркоманов возрос за этот же период с 1 до 50%.
 ПАТОГЕНЕЗ В связи с тем, что вирусы являются патогенами внутриклеточными, каждый представитель мира вирусов имеет тропность к определенному типу клеток. Тропизм вируса определяется наличием на клетке — мишени рецептора для данного вируса, а также возможность генома вируса встроиться в геном клетки. Рецепция в свою очередь определяет: а) конкретный вирус взаимодействует только с определенными рецепторами, б) на клетке могут быть рецепторы для различных типов вирусов и в) рецепторы для определенного вируса могут быть на клетках различных типов. Рецепторную функцию выполняют различные структуры (лиганды): белки, липиды, углеводные компоненты белков и липидов. Эти лиганды локализованы на плазматической мембране выполняют важнейшие функции жизнеобеспечения клетки — проникновение в нее гормонов, питательных веществ, факторов роста и регуляции и т. п. Вирус использует эти рецепторы в своих целях.
ПАТОГЕНЕЗ В связи с тем, что вирусы являются патогенами внутриклеточными, каждый представитель мира вирусов имеет тропность к определенному типу клеток. Тропизм вируса определяется наличием на клетке — мишени рецептора для данного вируса, а также возможность генома вируса встроиться в геном клетки. Рецепция в свою очередь определяет: а) конкретный вирус взаимодействует только с определенными рецепторами, б) на клетке могут быть рецепторы для различных типов вирусов и в) рецепторы для определенного вируса могут быть на клетках различных типов. Рецепторную функцию выполняют различные структуры (лиганды): белки, липиды, углеводные компоненты белков и липидов. Эти лиганды локализованы на плазматической мембране выполняют важнейшие функции жизнеобеспечения клетки — проникновение в нее гормонов, питательных веществ, факторов роста и регуляции и т. п. Вирус использует эти рецепторы в своих целях.
 Рецепторы, независимо от их биохимического строения, имеют общую структурную характеристику, а именно состоят из участка, расположенного вне клетки, участка, локализованного внутримембранно и участка, погруженного в цитоплазму. Рецептором для ВИЧ является дифференцировочный антиген CD 4 — (СD — аббревиатура от Сell Differention antigen), а также неспецифические, независящие от наличия CD 4 компоненты. CD 4 -гликопротеид с молекулярной массой 55 000, по своему строению имеющий гомологии с определенными участками иммуноглобулинов. Аналогичные гомологии имеет и белок вируса gp 120, что и определяет тропность ВИЧ. Расположенный на мембране иммунокомпетентных клеток Т-хелперов и Т- индукторов, рецептор CD 4 выполняет функцию распознавания (в комплексе с белками HLA II класса) антигенов. Фиксация вируса через gp 120 ВИЧ-1 (или gp 105 в случае инфицирования ВИЧ-2) с мембранным рецептором CD 4 клетки хозяина (рис. 5) блокирует основную функцию этих иммунокомпетентных клеток — восприятие сигналов от антигенпрезентирующих клеток. Последующая за рецепцией репликация вируса ведет к гибели клеток, выпадению функции, ими выполняемой — развитие иммунодефицита.
Рецепторы, независимо от их биохимического строения, имеют общую структурную характеристику, а именно состоят из участка, расположенного вне клетки, участка, локализованного внутримембранно и участка, погруженного в цитоплазму. Рецептором для ВИЧ является дифференцировочный антиген CD 4 — (СD — аббревиатура от Сell Differention antigen), а также неспецифические, независящие от наличия CD 4 компоненты. CD 4 -гликопротеид с молекулярной массой 55 000, по своему строению имеющий гомологии с определенными участками иммуноглобулинов. Аналогичные гомологии имеет и белок вируса gp 120, что и определяет тропность ВИЧ. Расположенный на мембране иммунокомпетентных клеток Т-хелперов и Т- индукторов, рецептор CD 4 выполняет функцию распознавания (в комплексе с белками HLA II класса) антигенов. Фиксация вируса через gp 120 ВИЧ-1 (или gp 105 в случае инфицирования ВИЧ-2) с мембранным рецептором CD 4 клетки хозяина (рис. 5) блокирует основную функцию этих иммунокомпетентных клеток — восприятие сигналов от антигенпрезентирующих клеток. Последующая за рецепцией репликация вируса ведет к гибели клеток, выпадению функции, ими выполняемой — развитие иммунодефицита.
 Рис. 5. Этапы взаимодействия ВИЧ с CD 4 -клеткой (Т-хелпером)
Рис. 5. Этапы взаимодействия ВИЧ с CD 4 -клеткой (Т-хелпером)
 Обозначения: • Связывание ВИЧ с рецептором CD 4 • РНК ВИЧ переписывается на ДНК с помощью обратной транскриптазы с превращением в ДНК-провирус • Интеграция провируса с помощью интегразы в ядро CD 4 -клетки, синтез геномной РНК для новых вирионов • Трансляция вирусных белков и расщепление протеазой вирусных полипептидов • Сборка новых вирионов • Выход новых вирионов из клетки-мишени
Обозначения: • Связывание ВИЧ с рецептором CD 4 • РНК ВИЧ переписывается на ДНК с помощью обратной транскриптазы с превращением в ДНК-провирус • Интеграция провируса с помощью интегразы в ядро CD 4 -клетки, синтез геномной РНК для новых вирионов • Трансляция вирусных белков и расщепление протеазой вирусных полипептидов • Сборка новых вирионов • Выход новых вирионов из клетки-мишени
 В организме человека имеется целый ряд иммунокомпетентных, соматических и ряда других клеток, имеющих рецепторы для ВИЧ (табл. 16) и наблюдается цитопатический эффект во многих из них в случае проникновения вируса.
В организме человека имеется целый ряд иммунокомпетентных, соматических и ряда других клеток, имеющих рецепторы для ВИЧ (табл. 16) и наблюдается цитопатический эффект во многих из них в случае проникновения вируса.
 Тип клеток Наличие CD 4 Цитопатический эффект вируса Система крови- — CD 4+ лимфоциты + + — CD 8+ лимфоциты + + — Дендритные клетки + — — Моноциты/макрофаги + — — Эозинофилы + ? — Мегакариоциты + + — Тимоциты-предшественники CD 4+ и CD 8+ клеток + + — В-лимфоциты на некоторых некоторые линии Нервная система: — Нейроны + — Микроглия + — Астроциты ? ? Клетки хорионтрофобласта плаценты + Спетрматозоиды + -Таблица 16. Клетки-мишени для ВИЧ
Тип клеток Наличие CD 4 Цитопатический эффект вируса Система крови- — CD 4+ лимфоциты + + — CD 8+ лимфоциты + + — Дендритные клетки + — — Моноциты/макрофаги + — — Эозинофилы + ? — Мегакариоциты + + — Тимоциты-предшественники CD 4+ и CD 8+ клеток + + — В-лимфоциты на некоторых некоторые линии Нервная система: — Нейроны + — Микроглия + — Астроциты ? ? Клетки хорионтрофобласта плаценты + Спетрматозоиды + -Таблица 16. Клетки-мишени для ВИЧ
 Помимо основного рецептора для ВИЧ-1 – CD 4 имеется еще ряд корецепторов, в частности, хемокиновые рецепторы, необходимые для проникновения ВИЧ в клетку. Хемокины – полипептиды, вызывающие движение клеток в определенной направленности. У человека выделено около 40 отдельных подобных белков, их подразделили на альфа- и бета-хемокины. В лаборатории Галло в 1995 году был выделен хемокин из CD 8 -лимфоцитов и два белка из макрофагов. Эти три хемокина блокируют инфицирование CD+ мононуклеаров макрофаготропными, но не лимфотропными вариантами ВИЧ-1. В 1996 году Бергер открыл корецептор для ВИЧ, сегодня получивший название СХСR 4. Этот рецептор вместе с CD 4 опосредует инфицирование СО-вариантами ВИЧ 1, адаптированных к росту в Т-хелперах, но не в макрофагах. В 1996 году открыт еще один корецептор для ВИЧ 1 – ССR 5. На сегодня известен ряд хемокиновых рецепторов (табл. 17).
Помимо основного рецептора для ВИЧ-1 – CD 4 имеется еще ряд корецепторов, в частности, хемокиновые рецепторы, необходимые для проникновения ВИЧ в клетку. Хемокины – полипептиды, вызывающие движение клеток в определенной направленности. У человека выделено около 40 отдельных подобных белков, их подразделили на альфа- и бета-хемокины. В лаборатории Галло в 1995 году был выделен хемокин из CD 8 -лимфоцитов и два белка из макрофагов. Эти три хемокина блокируют инфицирование CD+ мононуклеаров макрофаготропными, но не лимфотропными вариантами ВИЧ-1. В 1996 году Бергер открыл корецептор для ВИЧ, сегодня получивший название СХСR 4. Этот рецептор вместе с CD 4 опосредует инфицирование СО-вариантами ВИЧ 1, адаптированных к росту в Т-хелперах, но не в макрофагах. В 1996 году открыт еще один корецептор для ВИЧ 1 – ССR 5. На сегодня известен ряд хемокиновых рецепторов (табл. 17).
 Клетки Рецепторы Хемокиновые лиганды Нейтрофилы, моноциты CXCR 1 ИЛ-8 Нейтрофилы, моноциты, базофилы СХСR 2 ИЛ-8, белок, активирующий нейтрофилы Нормальные и активированные Т- CXCR 3 ИФ-10 клетки, В-клетки, моноциты, макро- фаги, гранулоциты, дендритные клетки CXCR 4 Фактор-1 стромальных клеток Моноциты, базофилы, активи рованные Т- клетки CCR 1 Регулятор и активатор нормальных Т-клеток и др. Моноциты, базофилы, активированные Т- клетки CCR 1 Регулятор и активатор нормальных Т-клеток и др. — II — ССR 2 Белок, вызывающий хемотаксис моноцитов 1, 2, 3, 4 Эозинофилы ССR 3 Белок, вызывающий хемотаксис эоинофилов, белок, вызывающий хемотаксис моноцитов-3, 4, регу- лятор и активатор нормальных Т-клеток Моноциты, активированные Т-клетки ССR 4 Регулятор и активатор нормальных Т-клеток и др. Активированные моноциты и Т-клетки, дендритные клетки CCR 5 — II — Таблица 17. Хемокиновые рецепторы человека
Клетки Рецепторы Хемокиновые лиганды Нейтрофилы, моноциты CXCR 1 ИЛ-8 Нейтрофилы, моноциты, базофилы СХСR 2 ИЛ-8, белок, активирующий нейтрофилы Нормальные и активированные Т- CXCR 3 ИФ-10 клетки, В-клетки, моноциты, макро- фаги, гранулоциты, дендритные клетки CXCR 4 Фактор-1 стромальных клеток Моноциты, базофилы, активи рованные Т- клетки CCR 1 Регулятор и активатор нормальных Т-клеток и др. Моноциты, базофилы, активированные Т- клетки CCR 1 Регулятор и активатор нормальных Т-клеток и др. — II — ССR 2 Белок, вызывающий хемотаксис моноцитов 1, 2, 3, 4 Эозинофилы ССR 3 Белок, вызывающий хемотаксис эоинофилов, белок, вызывающий хемотаксис моноцитов-3, 4, регу- лятор и активатор нормальных Т-клеток Моноциты, активированные Т-клетки ССR 4 Регулятор и активатор нормальных Т-клеток и др. Активированные моноциты и Т-клетки, дендритные клетки CCR 5 — II — Таблица 17. Хемокиновые рецепторы человека
 Таким образом, выделены белки — хемокины, блокирующие проникновение ВИЧ в макрофаги с антигеном CD 4 и белки — корецепторы, способствующие инфицированию. При этом корецепторы – это рецепторы для хемокинов, но их использует ВИЧ в качестве рецептора, с помощью которого проникает внутрь клетки. Некоторые хемокиновые рецепторы необходимы для проникновения ВИЧ в клетку. Было установлено, что длительно контактирующие с ВИЧ-инфицированными и при этом не заражающиеся имеют мутации в рецепторе CCR 5, поэтому мононуклеары у них оказались высокорезистентными к ВИЧ. Проникнув в СD 4+ клетки ВИЧ сразу же начинает репликацию, при этом, чем активнее CD 4+ клетки, тем выше процесс репродукции вируса. А отсюда вытекает, что все регуляторы, активирующие СD 4+клетки, обеспечивают увеличение репликации вируса. К подобным регуляторам относятся фактор некроза опухолей (ФНО), фактор, стимулирующий колонии гранулоцитов/макрофагов, интерлейкин-6 (ИЛ-6). К негативным регуляторам, тормозящим репликацию вируса, относятся интерферон (ИФ), трансформирующий фактор роста. Так, установлено, что ФНО-a активирует транскрипцию провирусной ДНК ВИЧ 1 в хронически инфицированных Т-клетках и макрофагах. Моноциты продуцируют ФНО-a , они не только индуцируют экспрессию ВИЧ-инфицированными клетками, но они также стимулируют активацию латентного провируса ВИЧ. Синхронно с ФНО-a действуют ИЛ-6 и фактор, стимулирующий колонии гранулоцитов/макрофагов.
Таким образом, выделены белки — хемокины, блокирующие проникновение ВИЧ в макрофаги с антигеном CD 4 и белки — корецепторы, способствующие инфицированию. При этом корецепторы – это рецепторы для хемокинов, но их использует ВИЧ в качестве рецептора, с помощью которого проникает внутрь клетки. Некоторые хемокиновые рецепторы необходимы для проникновения ВИЧ в клетку. Было установлено, что длительно контактирующие с ВИЧ-инфицированными и при этом не заражающиеся имеют мутации в рецепторе CCR 5, поэтому мононуклеары у них оказались высокорезистентными к ВИЧ. Проникнув в СD 4+ клетки ВИЧ сразу же начинает репликацию, при этом, чем активнее CD 4+ клетки, тем выше процесс репродукции вируса. А отсюда вытекает, что все регуляторы, активирующие СD 4+клетки, обеспечивают увеличение репликации вируса. К подобным регуляторам относятся фактор некроза опухолей (ФНО), фактор, стимулирующий колонии гранулоцитов/макрофагов, интерлейкин-6 (ИЛ-6). К негативным регуляторам, тормозящим репликацию вируса, относятся интерферон (ИФ), трансформирующий фактор роста. Так, установлено, что ФНО-a активирует транскрипцию провирусной ДНК ВИЧ 1 в хронически инфицированных Т-клетках и макрофагах. Моноциты продуцируют ФНО-a , они не только индуцируют экспрессию ВИЧ-инфицированными клетками, но они также стимулируют активацию латентного провируса ВИЧ. Синхронно с ФНО-a действуют ИЛ-6 и фактор, стимулирующий колонии гранулоцитов/макрофагов.
 Морфо-функциональные изменения в моноцитах/макрофагах оказывают разнонаправленное действие не только на Т-лимфоциты, но и естественные киллеры — главные клетки противоопухолевой защиты. Активность последних по мере прогрессирования заболевания неуклонно снижается. Уже дефицит ИЛ-2 и гамма-интерферона даже при нормальном количестве NK-клеток ведет к снижению функциональной активности их у больных ВИЧ-инфекцией (Ковальчук Л. В. , Чередеев А. Н. , 1991), тем более при дефиците. Хотя NK-клетки принимают участие в противоопухолевой защите, при ВИЧ-инфекции ведущим рассматривается иной механизм развития онкопатологии (рис. 6).
Морфо-функциональные изменения в моноцитах/макрофагах оказывают разнонаправленное действие не только на Т-лимфоциты, но и естественные киллеры — главные клетки противоопухолевой защиты. Активность последних по мере прогрессирования заболевания неуклонно снижается. Уже дефицит ИЛ-2 и гамма-интерферона даже при нормальном количестве NK-клеток ведет к снижению функциональной активности их у больных ВИЧ-инфекцией (Ковальчук Л. В. , Чередеев А. Н. , 1991), тем более при дефиците. Хотя NK-клетки принимают участие в противоопухолевой защите, при ВИЧ-инфекции ведущим рассматривается иной механизм развития онкопатологии (рис. 6).
 Рис. 6. Механизм индукции опухолевого роста при ВИЧ-инфекции
Рис. 6. Механизм индукции опухолевого роста при ВИЧ-инфекции
 Выделено два типа CD 4+клеток: Т-хелперы – 1 и Т-хелперы-2. Т-хелперы – 1 продуцируют цитокины, стимулирующие клеточный иммунитет, а Т-хелперы-2 – цитоктины, усиливающие антителогенез. Соотношение Т-хелперы-1 и Т-хелперы-2 взвешенно и конкурентно, суперэкспрессия цитокинов одного типа клеток ведет к супрессии другого. У больных ВИЧ-инфекцией идет угнетение Т-хелперов-1, чем обеспечивается и вирусная патология и онкогенез. Жизненный цикл ВИЧ после проникновения в организм носит последовательный характер: связывание вириона с поверхностью клетки, слияние мембран вириона и клетки, проникновение вируса внутрь клетки, высвобождение нуклеотида и геномной РНК вируса, интеграция генома вируса в геном инфицированной клетки, латентная фаза, фаза активации транскрипции с ДНК провируса и последующая транскрипция белков вируса, наработка всех компонентов вируса с формированием новых вирионов и их высвобождением из клетки, влекущим за собой гибель клетки-мишени.
Выделено два типа CD 4+клеток: Т-хелперы – 1 и Т-хелперы-2. Т-хелперы – 1 продуцируют цитокины, стимулирующие клеточный иммунитет, а Т-хелперы-2 – цитоктины, усиливающие антителогенез. Соотношение Т-хелперы-1 и Т-хелперы-2 взвешенно и конкурентно, суперэкспрессия цитокинов одного типа клеток ведет к супрессии другого. У больных ВИЧ-инфекцией идет угнетение Т-хелперов-1, чем обеспечивается и вирусная патология и онкогенез. Жизненный цикл ВИЧ после проникновения в организм носит последовательный характер: связывание вириона с поверхностью клетки, слияние мембран вириона и клетки, проникновение вируса внутрь клетки, высвобождение нуклеотида и геномной РНК вируса, интеграция генома вируса в геном инфицированной клетки, латентная фаза, фаза активации транскрипции с ДНК провируса и последующая транскрипция белков вируса, наработка всех компонентов вируса с формированием новых вирионов и их высвобождением из клетки, влекущим за собой гибель клетки-мишени.
 Сродство вирусного мембранного гликопротеида gp 120 (gp 105 в случае ВИЧ-2) к клеточному рецептору CD 4 определяет высокую степень избирательного поражения клеточных структур. Поэтому в патологический процесс вовлекаются в первую очередь и в большей степени CD 4+ лимфоциты, моноциты крови, макрофаги тканей, дендритные клетки крови, лимфатических узлов, селезенки, кожи, альвеолярных и интерстициальных макрофагов легких, микроглия и другие клетки нервной системы, имеющие CD 4 — рецепторы. Так же поражаются В- и О-лимфоциты, ретикулярные клетки, эпителиальные клетки кишечника, клетки Лангерганса. Причем последние инфицируются даже легче, чем CD 4+ лимфоциты. Именно клеткам Лангерганса придается большое значение в распространении ВИЧ по организму, ибо в них вирус сохраняется длительное время, иногда годы. Наличие CD 4 рецептора на многих и не только иммунокомпетентных клетках, возможность поражать и клетки, не имеющие этого рецептора, определяют политропность ВИЧ и полиморфизм клинической картины. Степень поражения тех или иных, содержащих СD 4 рецепторы клеток зависит от плотности этих рецепторов на мембране клеток. Наиболее высока плотность на Т-хелперной субпопуляции лимфоцитов, что и определяет во многом патогенез болезни. Но степень поражения клеток-мишеней вирусом зависит также и от возможности репликации вируса в том или ином виде клеток. Очевидно, осуществляется репликация в основном в лимфоцитах с CD 4+ фенотипом и моноцитах/макрофагах.
Сродство вирусного мембранного гликопротеида gp 120 (gp 105 в случае ВИЧ-2) к клеточному рецептору CD 4 определяет высокую степень избирательного поражения клеточных структур. Поэтому в патологический процесс вовлекаются в первую очередь и в большей степени CD 4+ лимфоциты, моноциты крови, макрофаги тканей, дендритные клетки крови, лимфатических узлов, селезенки, кожи, альвеолярных и интерстициальных макрофагов легких, микроглия и другие клетки нервной системы, имеющие CD 4 — рецепторы. Так же поражаются В- и О-лимфоциты, ретикулярные клетки, эпителиальные клетки кишечника, клетки Лангерганса. Причем последние инфицируются даже легче, чем CD 4+ лимфоциты. Именно клеткам Лангерганса придается большое значение в распространении ВИЧ по организму, ибо в них вирус сохраняется длительное время, иногда годы. Наличие CD 4 рецептора на многих и не только иммунокомпетентных клетках, возможность поражать и клетки, не имеющие этого рецептора, определяют политропность ВИЧ и полиморфизм клинической картины. Степень поражения тех или иных, содержащих СD 4 рецепторы клеток зависит от плотности этих рецепторов на мембране клеток. Наиболее высока плотность на Т-хелперной субпопуляции лимфоцитов, что и определяет во многом патогенез болезни. Но степень поражения клеток-мишеней вирусом зависит также и от возможности репликации вируса в том или ином виде клеток. Очевидно, осуществляется репликация в основном в лимфоцитах с CD 4+ фенотипом и моноцитах/макрофагах.
 Если на CD 4+ лимфоциты вирус оказывает цитопатическое действие с лизисом клетки или слиянием в синцитий, то в моноцитах/макрофагах ВИЧ реплицируется с умеренной интенсивностью, вирионы оформляются в округлые частицы еще в цитоплазме клетки и по выходе из нее не оказывают цитонекротического действия. Тем не менее, моноциты/ макрофаги претерпевают значительные ультраструктурные изменения. Проведенное нами изучение динамики сывороточных монокинов подтверждает активное участие в патогенезе ВИЧ-инфекции моноцитов/ макрофагов, основных продуцентов фактора некроза опухолей и интерлейкина-1 b (выполняющих роль передатчика Т-лимфоцитам антигенспецифических сигналов, необходимых для их активации в иммунном ответе). Увеличение продукции некоторых цитокинов способствует экспрессии вируса. Так, исследования Н. М. Калининой (1996) показали резкое увеличение провоспалительных цитокинов ФНО-a (до 428 при норме 38, 9 пг/мл у взрослых и до 1363 у детей при норме 108, 8 пг/мл в стадии IIIB) и ИЛ-1 b. С гиперпродукцией ФНО-a , ИЛ-1 b и ИЛ-6 связывают развитие при ВИЧ-инфекции лихорадки, анемии, диареи, кахексии, патологических изменений на коже и слизистых при саркоме Капоши, церебральных симптомов. ФНО-a при этом оказывает прямое цитопатическое действие на инфицированные ВИЧ Т-хелперы. В то же время было установлено, что ВИЧ ингибирует продукцию ИЛ-2 и ИФ-g , синтезируемым Т-хелперами первого типа и не ингибирует функцию Т-хелперов второго типа. Следовательно, играя важную роль в регуляции синтеза цитокинов, ВИЧ за счет переключения иммунного ответа с Т-хелперов первого типа на Т-хелперы второго типа, стимулирует гуморальное звено иммунитета.
Если на CD 4+ лимфоциты вирус оказывает цитопатическое действие с лизисом клетки или слиянием в синцитий, то в моноцитах/макрофагах ВИЧ реплицируется с умеренной интенсивностью, вирионы оформляются в округлые частицы еще в цитоплазме клетки и по выходе из нее не оказывают цитонекротического действия. Тем не менее, моноциты/ макрофаги претерпевают значительные ультраструктурные изменения. Проведенное нами изучение динамики сывороточных монокинов подтверждает активное участие в патогенезе ВИЧ-инфекции моноцитов/ макрофагов, основных продуцентов фактора некроза опухолей и интерлейкина-1 b (выполняющих роль передатчика Т-лимфоцитам антигенспецифических сигналов, необходимых для их активации в иммунном ответе). Увеличение продукции некоторых цитокинов способствует экспрессии вируса. Так, исследования Н. М. Калининой (1996) показали резкое увеличение провоспалительных цитокинов ФНО-a (до 428 при норме 38, 9 пг/мл у взрослых и до 1363 у детей при норме 108, 8 пг/мл в стадии IIIB) и ИЛ-1 b. С гиперпродукцией ФНО-a , ИЛ-1 b и ИЛ-6 связывают развитие при ВИЧ-инфекции лихорадки, анемии, диареи, кахексии, патологических изменений на коже и слизистых при саркоме Капоши, церебральных симптомов. ФНО-a при этом оказывает прямое цитопатическое действие на инфицированные ВИЧ Т-хелперы. В то же время было установлено, что ВИЧ ингибирует продукцию ИЛ-2 и ИФ-g , синтезируемым Т-хелперами первого типа и не ингибирует функцию Т-хелперов второго типа. Следовательно, играя важную роль в регуляции синтеза цитокинов, ВИЧ за счет переключения иммунного ответа с Т-хелперов первого типа на Т-хелперы второго типа, стимулирует гуморальное звено иммунитета.
 После инфицирования клетки вирусом происходит соединение вирусной оболочки с помощью белка gp 41 с мембраной клетки. Помимо того вирусный белок gp 41 обеспечивает слияние мембран соседних клеток между собой с образованием одной многоядерной клетки — синцития. При этом слияние может быть как зараженных клеток между собой, так и зараженных с незараженными. Но синцитий в основном индуцируют вирусы, выделенные от больных с клиническими проявлениям ВИЧ-инфекции и не образуют выделенные от инфицированных, не имеющих клинических проявлений. С момента интеграции генома вируса в геном клетки начинается стадия латентной инфекции. В этот период вирус находится в клетке в виде интегрированного в геном ДНК — провируса, . Раньше полагали, что в этот период нет процессов транскрипции и трансляции с вирусных генов, а поэтому и экспрессии вирусных белков, нет иммунного ответа на вирус как в виде специфических иммуноглобулинов, так и сенсибилизированных лимфоцитов. Но последние исследования показали, что сразу после проникновения вируса в клетку начинается и трансляция и транскрипция.
После инфицирования клетки вирусом происходит соединение вирусной оболочки с помощью белка gp 41 с мембраной клетки. Помимо того вирусный белок gp 41 обеспечивает слияние мембран соседних клеток между собой с образованием одной многоядерной клетки — синцития. При этом слияние может быть как зараженных клеток между собой, так и зараженных с незараженными. Но синцитий в основном индуцируют вирусы, выделенные от больных с клиническими проявлениям ВИЧ-инфекции и не образуют выделенные от инфицированных, не имеющих клинических проявлений. С момента интеграции генома вируса в геном клетки начинается стадия латентной инфекции. В этот период вирус находится в клетке в виде интегрированного в геном ДНК — провируса, . Раньше полагали, что в этот период нет процессов транскрипции и трансляции с вирусных генов, а поэтому и экспрессии вирусных белков, нет иммунного ответа на вирус как в виде специфических иммуноглобулинов, так и сенсибилизированных лимфоцитов. Но последние исследования показали, что сразу после проникновения вируса в клетку начинается и трансляция и транскрипция.
 В этот период инфекционного процесса, когда возбудитель находится в геноме клетки в виде ДНК-провируса, его можно обнаружить лишь такими методами, как полимеразная цепная реакция (ПЦР), гибридизация нуклеиновых кислот со специфическими зондами. ПЦР позволяет обнаружить вирус при наличии одной инфицированной из 5 тыс. клеток. Сохранение инфекционного процесса в латентной форме обеспечивается посредством элемента негативной регуляции (NRE), идентифицированного в участке длинного концевого повтора ВИЧ. Делеция NRE приводит к усилению экспрессии вирусного генома. К NRE имеет сродство вирусный белок nef. Тем не менее, один из штаммов ВИЧ-1, несмотря на присутствие nef является высоковирулентным, что объясняется наличием двух мутантов nef. Состояние латентной инфекции без клинических признаков болезни может длиться от 2 до 11 лет. Активация длинных концевых повторов и экспрессия генов ВИЧ, кодирующих белки вируса, знаменует собой манифестацию болезни.
В этот период инфекционного процесса, когда возбудитель находится в геноме клетки в виде ДНК-провируса, его можно обнаружить лишь такими методами, как полимеразная цепная реакция (ПЦР), гибридизация нуклеиновых кислот со специфическими зондами. ПЦР позволяет обнаружить вирус при наличии одной инфицированной из 5 тыс. клеток. Сохранение инфекционного процесса в латентной форме обеспечивается посредством элемента негативной регуляции (NRE), идентифицированного в участке длинного концевого повтора ВИЧ. Делеция NRE приводит к усилению экспрессии вирусного генома. К NRE имеет сродство вирусный белок nef. Тем не менее, один из штаммов ВИЧ-1, несмотря на присутствие nef является высоковирулентным, что объясняется наличием двух мутантов nef. Состояние латентной инфекции без клинических признаков болезни может длиться от 2 до 11 лет. Активация длинных концевых повторов и экспрессия генов ВИЧ, кодирующих белки вируса, знаменует собой манифестацию болезни.
 I. Фаза интегрирования — травмы гениталий — болезни, передающиеся половым путем — вирусная инфекция (простой герпес, цитомегаловирусная инфекция и др. ) II. Манифестация острой фазы (у 15 -25% ВИЧ-инфицированных) — вирусная инфекция группы Herpes III. Фаза перехода из латентной в активную — генетические факторы (ассоциация с HLA) — возраст — ультрафиолетовые лучи и др. факторы Таблица 18. Ко-факторы ВИЧ-инфекции
I. Фаза интегрирования — травмы гениталий — болезни, передающиеся половым путем — вирусная инфекция (простой герпес, цитомегаловирусная инфекция и др. ) II. Манифестация острой фазы (у 15 -25% ВИЧ-инфицированных) — вирусная инфекция группы Herpes III. Фаза перехода из латентной в активную — генетические факторы (ассоциация с HLA) — возраст — ультрафиолетовые лучи и др. факторы Таблица 18. Ко-факторы ВИЧ-инфекции
 В расшифровке патогенеза ВИЧ-инфекции многие вопросы решены, установлены основные этапы развития процесса в клетке после инфицирования ее вирусом. Выявлен ряд факторов, активирующих экспрессию генов ВИЧ (табл. 18). К ним относятся факторы, активирующие Т-лимфоциты: специфические антигены (например, вирусы группы Herpes), неспецифические антигены (например, митогены типа фитогемаглютинина), цитокины (например, фактор некроза опухолей, некоторые интерлейкины, гамма-интерферон), бактериальные иммуномодуляторы (например, монофосфат липида из сальмонелл). К активаторам экспрессии ВИЧ относятся глюкокортикостероидные гормоны, в частности дексаметазон и гидрокортизон, ультрафиолетовое облучение, перекись водорода, свободные кислородные радикалы. Активирует инфекционный процесс беременность, более прогрессирующее течение ВИЧ-инфекции имеют психически неуравновешенные лица, дезадаптированные по сравнению с людьми, имеющими уравновешенную психику.
В расшифровке патогенеза ВИЧ-инфекции многие вопросы решены, установлены основные этапы развития процесса в клетке после инфицирования ее вирусом. Выявлен ряд факторов, активирующих экспрессию генов ВИЧ (табл. 18). К ним относятся факторы, активирующие Т-лимфоциты: специфические антигены (например, вирусы группы Herpes), неспецифические антигены (например, митогены типа фитогемаглютинина), цитокины (например, фактор некроза опухолей, некоторые интерлейкины, гамма-интерферон), бактериальные иммуномодуляторы (например, монофосфат липида из сальмонелл). К активаторам экспрессии ВИЧ относятся глюкокортикостероидные гормоны, в частности дексаметазон и гидрокортизон, ультрафиолетовое облучение, перекись водорода, свободные кислородные радикалы. Активирует инфекционный процесс беременность, более прогрессирующее течение ВИЧ-инфекции имеют психически неуравновешенные лица, дезадаптированные по сравнению с людьми, имеющими уравновешенную психику.
 Довольно сложен и до конца не выяснен механизм репликации вируса в инфицированной клетке. Известно, что в цитоплазме информация с вирусной РНК посредством обратной транскриптазы (ревертазы) переписывается на ДНК клетки, первоначально образуется однонитевая структура, затем та же обратная транскриптаза обеспечивает образование второй нити, а линейная промежуточная форма ДНК вируса транспортируется в ядро, где с помощью фермента интегразы интегрирует с ДНК клетки, превращаясь в ДНК-провирус. Исключительно важный этап патогенеза болезни — сборка вирусных частиц и выход нового потомства вируса из инфицированной клетки. Сборка происходит на плазматической мембране лимфоцита, куда поступают все компоненты вирусной частицы, в том числе и белки-предшественники. Завершается процесс почкованием вирусных частиц с клеточной поверхности. Отличительной чертой ВИЧ является взрывной характер процессов активации транскрипции, синтеза белков-предшественников, сборки вирионов и их почкования: за 5 мин одна лимфоцитарная клетка может образовать до 5000 вирусных частиц.
Довольно сложен и до конца не выяснен механизм репликации вируса в инфицированной клетке. Известно, что в цитоплазме информация с вирусной РНК посредством обратной транскриптазы (ревертазы) переписывается на ДНК клетки, первоначально образуется однонитевая структура, затем та же обратная транскриптаза обеспечивает образование второй нити, а линейная промежуточная форма ДНК вируса транспортируется в ядро, где с помощью фермента интегразы интегрирует с ДНК клетки, превращаясь в ДНК-провирус. Исключительно важный этап патогенеза болезни — сборка вирусных частиц и выход нового потомства вируса из инфицированной клетки. Сборка происходит на плазматической мембране лимфоцита, куда поступают все компоненты вирусной частицы, в том числе и белки-предшественники. Завершается процесс почкованием вирусных частиц с клеточной поверхности. Отличительной чертой ВИЧ является взрывной характер процессов активации транскрипции, синтеза белков-предшественников, сборки вирионов и их почкования: за 5 мин одна лимфоцитарная клетка может образовать до 5000 вирусных частиц.
 Ключевой вопрос патогенеза ВИЧ-инфекции — механизм иммунного повреждения. Как установлено, в составе белков gp 120, главного комплекса гистосовместимости (HLA) класса II и CD 4 -рецепторов имеются сходные участки, что определяет перекресное реагирование образующихся к ВИЧ антител с этими структурами. Например, происходит блокада кооперации CD 4+ лимфоцитов и HLA II. Антитела к gp 120 ВИЧ реагируют с CD 4, обусловливая неадекватную стимуляцию CD 4+ клеток. На всех ядросодержащих клетках имеются антигены HLA I, вирус же нарушает синтез этих антигенов, участвующих в распознавании CD 8+ лимфоцитами (Т-супрессорами) зараженных вирусом клеток, что тормозит процесс лизиса инфицированных клеток.
Ключевой вопрос патогенеза ВИЧ-инфекции — механизм иммунного повреждения. Как установлено, в составе белков gp 120, главного комплекса гистосовместимости (HLA) класса II и CD 4 -рецепторов имеются сходные участки, что определяет перекресное реагирование образующихся к ВИЧ антител с этими структурами. Например, происходит блокада кооперации CD 4+ лимфоцитов и HLA II. Антитела к gp 120 ВИЧ реагируют с CD 4, обусловливая неадекватную стимуляцию CD 4+ клеток. На всех ядросодержащих клетках имеются антигены HLA I, вирус же нарушает синтез этих антигенов, участвующих в распознавании CD 8+ лимфоцитами (Т-супрессорами) зараженных вирусом клеток, что тормозит процесс лизиса инфицированных клеток.
 Взаимосвязь жизненного цикла вируса и иммунных сдвигов в начальной фазе ВИЧ-инфекции изучена в эксперименте при заражении SIV обезьян, полученные данные экстраполированы на человека. Как показали исследования, вирус первоначально локализуется в лимфоидной системе, вирусная экспрессия определяет клинику ранней фазы болезни. Пик экспрессии вируса в клетках лимфоидной ткани предшествует накоплению его в плазме. Появление вирусспецифических цитотоксических Т-лимфоцитов (CTL) совпадает со временем окончания экспрессии вируса в лимфатических узлах. Продукция комплемент (С) — связывающих антител облегчает переход вируса в сеть дендритных клеток герминальных центров лимфатических узлов. Повреждающее действие CTL и продукция копмлементсвязывающих антител оказывают основное патогенное действие в результате виремии. Образование нейтрализующих антител обеспечивает переход острой фазы болезни в хроническую.
Взаимосвязь жизненного цикла вируса и иммунных сдвигов в начальной фазе ВИЧ-инфекции изучена в эксперименте при заражении SIV обезьян, полученные данные экстраполированы на человека. Как показали исследования, вирус первоначально локализуется в лимфоидной системе, вирусная экспрессия определяет клинику ранней фазы болезни. Пик экспрессии вируса в клетках лимфоидной ткани предшествует накоплению его в плазме. Появление вирусспецифических цитотоксических Т-лимфоцитов (CTL) совпадает со временем окончания экспрессии вируса в лимфатических узлах. Продукция комплемент (С) — связывающих антител облегчает переход вируса в сеть дендритных клеток герминальных центров лимфатических узлов. Повреждающее действие CTL и продукция копмлементсвязывающих антител оказывают основное патогенное действие в результате виремии. Образование нейтрализующих антител обеспечивает переход острой фазы болезни в хроническую.
 Как показали исследования, проведенные в нашей лаборатории Ю. А. Митиным, в ходе развития инфекционного процесса на всех фазах болезни наблюдаются морфологические изменения лимфоцитов: увеличивается содержание сегментированных лимфоцитов, усиливается деградация нуклеотидов, снижаются биосинтетические процессы и нарушается организация надмолекулярного комплекса ДНК. Острая фаза болезни приводит к усилению митотической и предмитотической активности лимфоцитов, на стадии II B растет митотическая активность моноцитов периферической крови. Патологический процесс сопровождается усилением перекисного окисления липидов в лимфоцитах. Снижается активность ключевого фермента анаэробного окисления — лактатдегидрогеназы, характерно повышение активности сукцинатдегидрогеназы, снижение активности альфа-глицерофосфатдегидро-геназы.
Как показали исследования, проведенные в нашей лаборатории Ю. А. Митиным, в ходе развития инфекционного процесса на всех фазах болезни наблюдаются морфологические изменения лимфоцитов: увеличивается содержание сегментированных лимфоцитов, усиливается деградация нуклеотидов, снижаются биосинтетические процессы и нарушается организация надмолекулярного комплекса ДНК. Острая фаза болезни приводит к усилению митотической и предмитотической активности лимфоцитов, на стадии II B растет митотическая активность моноцитов периферической крови. Патологический процесс сопровождается усилением перекисного окисления липидов в лимфоцитах. Снижается активность ключевого фермента анаэробного окисления — лактатдегидрогеназы, характерно повышение активности сукцинатдегидрогеназы, снижение активности альфа-глицерофосфатдегидро-геназы.
 В моноцитарных клетках больных изменения функциональной активности проявляются повышением напряженности процессов анаэробного окисления на ранних стадиях инфицирования с одновременным снижением интенсивности цикла трикарбоновых кислот. Прогрессирование патологического процесса ведет к стойкому снижению активности сукцинатдегидрогеназы и лактатдегидрогеназы, характеризуя угнетение функциональной активности моноцитов. Активация пентозного цикла, усиление процесса распада пуриновых оснований приводят к активации прооксидантных НАД-систем (НАДФ и ксантиноксидазы), не компенсируемый при прогрессировании патологического процесса усилением функции антиоксидантных систем (супероксиддисмутаза, глутатион) и обусловливая рост активности трипсиноподобных эндонуклеаз с развитием деградации ядерного хроматина. Все это определяет несбалансированный рост и преждевременную гибель клеток.
В моноцитарных клетках больных изменения функциональной активности проявляются повышением напряженности процессов анаэробного окисления на ранних стадиях инфицирования с одновременным снижением интенсивности цикла трикарбоновых кислот. Прогрессирование патологического процесса ведет к стойкому снижению активности сукцинатдегидрогеназы и лактатдегидрогеназы, характеризуя угнетение функциональной активности моноцитов. Активация пентозного цикла, усиление процесса распада пуриновых оснований приводят к активации прооксидантных НАД-систем (НАДФ и ксантиноксидазы), не компенсируемый при прогрессировании патологического процесса усилением функции антиоксидантных систем (супероксиддисмутаза, глутатион) и обусловливая рост активности трипсиноподобных эндонуклеаз с развитием деградации ядерного хроматина. Все это определяет несбалансированный рост и преждевременную гибель клеток.
 Иммунопатогенетически ВИЧ-инфекция проявляется дефицитом Т- и В-звеньев иммунной системы, дефицитом комплемента, фагоцитов, снижением функции неспецифических факторов защиты. В результате идет формирование анергии с проявлениями аллергического, аутоаллергического и иммунокомплексного патологического процесса. Так, наши исследования показали, что уже во II стадии ВИЧ-инфекция характеризуется снижением абсолютного числа лейкоцитов за счет CD 3+, CD 4+, p 24+ и gp 120+ лимфоцитов, повышением уровня естественных киллеров (NК-клетки), нарастанием РТМЛ с конкавалином А и фитогемагглютинином. Изменения гуморального звена иммунитета проявляются нарастанием Ig. G+ В-лимфоцитов и 4 -5 кратным ростом уровня сывороточных Ig. E.
Иммунопатогенетически ВИЧ-инфекция проявляется дефицитом Т- и В-звеньев иммунной системы, дефицитом комплемента, фагоцитов, снижением функции неспецифических факторов защиты. В результате идет формирование анергии с проявлениями аллергического, аутоаллергического и иммунокомплексного патологического процесса. Так, наши исследования показали, что уже во II стадии ВИЧ-инфекция характеризуется снижением абсолютного числа лейкоцитов за счет CD 3+, CD 4+, p 24+ и gp 120+ лимфоцитов, повышением уровня естественных киллеров (NК-клетки), нарастанием РТМЛ с конкавалином А и фитогемагглютинином. Изменения гуморального звена иммунитета проявляются нарастанием Ig. G+ В-лимфоцитов и 4 -5 кратным ростом уровня сывороточных Ig. E.
 Как показали исследования, проведенные в нашей лаборатории, количественные и функциональные сдвиги в показателях иммунной системы индуцируют изменения структурной организации ее с установлением новых и изменением силы и направленности ранее имевшихся коррелятивных связей: уже на стадии II Б возникает положительная коррелятивная связь между содержанием CD 8+ лимфоцитов и числом иммунокомпетентных клеток, имеющих на поверхностных мембранах антиген ВИЧ р24. В стадии III A устанавливается тесная положительная коррелятивная связь между числом NK-клеток, индексом CD 4/ CD 8 и содержанием клеток, экспрессирующих антигены ВИЧ р24 и gp 120. В стадии III Б и III B возрастает число клеток, экспрессирующих антигены p 24 и gp 120, устанавливается высокая отрицательная коррелятивная связь между числом CD 3+ лимфоцитов и содержанием клеток, экспрессирующих антигены р24 и gp 120, между числом NK-клеток и числом клеток, экспрессирующих антиген р24.
Как показали исследования, проведенные в нашей лаборатории, количественные и функциональные сдвиги в показателях иммунной системы индуцируют изменения структурной организации ее с установлением новых и изменением силы и направленности ранее имевшихся коррелятивных связей: уже на стадии II Б возникает положительная коррелятивная связь между содержанием CD 8+ лимфоцитов и числом иммунокомпетентных клеток, имеющих на поверхностных мембранах антиген ВИЧ р24. В стадии III A устанавливается тесная положительная коррелятивная связь между числом NK-клеток, индексом CD 4/ CD 8 и содержанием клеток, экспрессирующих антигены ВИЧ р24 и gp 120. В стадии III Б и III B возрастает число клеток, экспрессирующих антигены p 24 и gp 120, устанавливается высокая отрицательная коррелятивная связь между числом CD 3+ лимфоцитов и содержанием клеток, экспрессирующих антигены р24 и gp 120, между числом NK-клеток и числом клеток, экспрессирующих антиген р24.
 Для изменений В-звена иммунитета характерны активация В-лимфоцитов, изменение их метаболизма сопровождается уменьшением времени полуобмена иммуноглобулиновых рецепторов с повышением в крови концентрации клеточных рецепторов (Р-белки). Суммарная концентрация сывороточных иммуноглобулинов растет, но выявляется диспропорция уровней подклассов иммуноглобулинов. Так, содержание Ig. G 1 и Ig. G 3 у больных увеличивается, а концентрация Ig. G 2 и Ig. G 4 существенно уменьшается. Очевидно, повышение уровня Ig. G 2 связано с высокой восприимчивостью больных к стафилококкам, пневмококкам, палочке инфлюэнцы. Несмотря на гипергаммаглобулинемию, увеличение количества циркулирующих в крови В-лимфоцитов, их функциональная активность на митогены (например, на митоген лаконоса) остается относительно сниженной, что позволяет В-систему иммунитета у ВИЧ-больных расценивать как супрессированную. К тому же, как показывают наши наблюдения и данные литературы, количество В-клеток в периферической крови больных в стадии СПИД может быть снижено в три и более раз.
Для изменений В-звена иммунитета характерны активация В-лимфоцитов, изменение их метаболизма сопровождается уменьшением времени полуобмена иммуноглобулиновых рецепторов с повышением в крови концентрации клеточных рецепторов (Р-белки). Суммарная концентрация сывороточных иммуноглобулинов растет, но выявляется диспропорция уровней подклассов иммуноглобулинов. Так, содержание Ig. G 1 и Ig. G 3 у больных увеличивается, а концентрация Ig. G 2 и Ig. G 4 существенно уменьшается. Очевидно, повышение уровня Ig. G 2 связано с высокой восприимчивостью больных к стафилококкам, пневмококкам, палочке инфлюэнцы. Несмотря на гипергаммаглобулинемию, увеличение количества циркулирующих в крови В-лимфоцитов, их функциональная активность на митогены (например, на митоген лаконоса) остается относительно сниженной, что позволяет В-систему иммунитета у ВИЧ-больных расценивать как супрессированную. К тому же, как показывают наши наблюдения и данные литературы, количество В-клеток в периферической крови больных в стадии СПИД может быть снижено в три и более раз.
 Многочисленными исследованиями показано, что взаимодействие gp 120 ВИЧ-1 с мембраной CD 4+ лимфоцитов определяет не только отрицательные реакции инфицированных клеток, но и приводит к программированной клеточной гибели — апоптозу зрелых CD 4+ лимфоцитов или CD 34+ гемопоэтических клеток-предшественников даже при отсутствии их инфицирования вирусом. Специфический иммунный ответ при ВИЧ-инфекции имеет ряд особенностей. Локализуясь в иммуноците, вирус проникает в органы и ткани, пребывая вне доступности для иммунной системы, чем определяется персистенция в клетках как вируса, так и его компонентов — белков, нуклеокапсидов, нуклеиновой кислоты. Активация инфекционного процесса ведет к гуморальному иммунному ответу с образованием антител. Но в связи с наличием в составе вирусного белка gp 120, HLA класса II и CD 4 -рецептора лимфоцита сходных участков, образующиеся антитела перекресно реагируют с ними, чем обусловливают нарушение кооперативных взаимодействий в функционировании иммунной системы. Все это определяет формирование аутоаллергических реакций.
Многочисленными исследованиями показано, что взаимодействие gp 120 ВИЧ-1 с мембраной CD 4+ лимфоцитов определяет не только отрицательные реакции инфицированных клеток, но и приводит к программированной клеточной гибели — апоптозу зрелых CD 4+ лимфоцитов или CD 34+ гемопоэтических клеток-предшественников даже при отсутствии их инфицирования вирусом. Специфический иммунный ответ при ВИЧ-инфекции имеет ряд особенностей. Локализуясь в иммуноците, вирус проникает в органы и ткани, пребывая вне доступности для иммунной системы, чем определяется персистенция в клетках как вируса, так и его компонентов — белков, нуклеокапсидов, нуклеиновой кислоты. Активация инфекционного процесса ведет к гуморальному иммунному ответу с образованием антител. Но в связи с наличием в составе вирусного белка gp 120, HLA класса II и CD 4 -рецептора лимфоцита сходных участков, образующиеся антитела перекресно реагируют с ними, чем обусловливают нарушение кооперативных взаимодействий в функционировании иммунной системы. Все это определяет формирование аутоаллергических реакций.
 Именно поэтому в ходе развития инфекционного процесса формируется гиперчувствительность замедленного и немедленного типов, преимущественно к антигенам ВИЧ, в частности gр41 и gp 120. Так, Л. Монтанье (1996) считает, что в патогенезе СПИД основное место принадлежит аутоиммунному процессу. В пользу этого говорят исследования характера иммунных реакций у больных: наличие аутоантител и аллоантител к лимфоцитам, формирование аллергических реакций цитотоксического типа, накопление циркулирующих иммунных комплексов, наличие комплементопосредованной цитотоксичности, активация антителозависимой клеточной цитотоксичности. Кроме того, при сильном антительном ответе возможность развития аутоиммунных процессов обусловлена мимикрией структуры gp 120 под структуру иммуноглобулинов (Atlan H. et al. , 1993). В пользу наличия аутоиммунных процессов в патогенезе ВИЧ-инфекции говорят и клинические проявления болезни, в частности, часто сопутствующие болезни такие типичные аутоаллергические варианты патологии, как спондилоартропатии, системные ревматоидные синдромы: волчаночноподобный, синдром Шегрена, полимиозит, некротизирующий васкулит. Возможный вариант развития аутоиммунного синдрома у больных ВИЧ/СПИД представлен на рис. 7.
Именно поэтому в ходе развития инфекционного процесса формируется гиперчувствительность замедленного и немедленного типов, преимущественно к антигенам ВИЧ, в частности gр41 и gp 120. Так, Л. Монтанье (1996) считает, что в патогенезе СПИД основное место принадлежит аутоиммунному процессу. В пользу этого говорят исследования характера иммунных реакций у больных: наличие аутоантител и аллоантител к лимфоцитам, формирование аллергических реакций цитотоксического типа, накопление циркулирующих иммунных комплексов, наличие комплементопосредованной цитотоксичности, активация антителозависимой клеточной цитотоксичности. Кроме того, при сильном антительном ответе возможность развития аутоиммунных процессов обусловлена мимикрией структуры gp 120 под структуру иммуноглобулинов (Atlan H. et al. , 1993). В пользу наличия аутоиммунных процессов в патогенезе ВИЧ-инфекции говорят и клинические проявления болезни, в частности, часто сопутствующие болезни такие типичные аутоаллергические варианты патологии, как спондилоартропатии, системные ревматоидные синдромы: волчаночноподобный, синдром Шегрена, полимиозит, некротизирующий васкулит. Возможный вариант развития аутоиммунного синдрома у больных ВИЧ/СПИД представлен на рис. 7.
 Рис. 7. Возможные механизмы аутоаллергических нарушений при ВИЧ-инфекции
Рис. 7. Возможные механизмы аутоаллергических нарушений при ВИЧ-инфекции
 Исследования, проведенные Ю. А. Митиным (1997) показали, что у половины больных (52, 4%) развиваются манифестные формы аллергии, преимущественно в виде ринита (46, 1%), лекарственной аллергии (31, 0%), крапивницы (17, 2%), атопического дерматита (16, 1%), ангионевротического отека (2, 3%) с повышением у них уровня специфических Ig. E к бытовым, эпидермальным, пыльцевым и пищевым аллергенам с положительной коррелятивной связью между общим уровнем Ig. E и содержанием СD 8+ лимфоцитов. В целом аллергическая настроенность характеризуется ранним началом от момента заболевания, развитием полисенсибилизации. Формирование иммунодефицита при ВИЧ-инфекции не ограничивается только поражением лимфоцитов с CD 4 -фенотипом. Так, нарушение синтеза белков HLA I ведет к ингибированию функции лимфоцитов с CD 8 -фенотипа, т. е. Т-супрессоров. Белок вируса р15 оказывает супрессивное действие на продукцию Т-клетками ИЛ-2 и интерферона-g. Известно, что для дифференцировки Т-эффекторов из Т-предшественников необходимы ИЛ-2, гамма-интерферон и ИЛ-6. А с продукцией ИЛ-2 и других цитокинов тесно связана функция цитотоксических Т-лимфоцитов, ответственных за противовирусную и противоопухолевую защиту организма. Все это патогенетически определяет характерную для ВИЧ-инфекции СПИД-ассоциированную вирусную и онкопатологию.
Исследования, проведенные Ю. А. Митиным (1997) показали, что у половины больных (52, 4%) развиваются манифестные формы аллергии, преимущественно в виде ринита (46, 1%), лекарственной аллергии (31, 0%), крапивницы (17, 2%), атопического дерматита (16, 1%), ангионевротического отека (2, 3%) с повышением у них уровня специфических Ig. E к бытовым, эпидермальным, пыльцевым и пищевым аллергенам с положительной коррелятивной связью между общим уровнем Ig. E и содержанием СD 8+ лимфоцитов. В целом аллергическая настроенность характеризуется ранним началом от момента заболевания, развитием полисенсибилизации. Формирование иммунодефицита при ВИЧ-инфекции не ограничивается только поражением лимфоцитов с CD 4 -фенотипом. Так, нарушение синтеза белков HLA I ведет к ингибированию функции лимфоцитов с CD 8 -фенотипа, т. е. Т-супрессоров. Белок вируса р15 оказывает супрессивное действие на продукцию Т-клетками ИЛ-2 и интерферона-g. Известно, что для дифференцировки Т-эффекторов из Т-предшественников необходимы ИЛ-2, гамма-интерферон и ИЛ-6. А с продукцией ИЛ-2 и других цитокинов тесно связана функция цитотоксических Т-лимфоцитов, ответственных за противовирусную и противоопухолевую защиту организма. Все это патогенетически определяет характерную для ВИЧ-инфекции СПИД-ассоциированную вирусную и онкопатологию.
 Наряду с поражением иммунной системы в патологический процесс вовлекается и кроветворная ткань. Для заболевания характерны лейкопения, анемия, тромбоцитопения. Угнетается функциональная активность гранулоцитов. Экспериментальные исследования с заражением ВИЧ-подобным ретровирусом LP-BM 5 через 3 месяца в костном мозге выявлена значительная цитопения, снижение содержания эрелых клеток, угнетение гранулоцитопоэза (Magnal M. et al. , 1993). У больных ВИЧ-инфекцией в костном мозге резко снижено содержание колониеобразующих единиц гранулоцитов, макрофагов, мегакариоцитов. Однако дисфункция стволовых клеток не связана с их прямым инфицированием, ибо не обнаружено присутствия ВИЧ в кроветворных клетках при изучении методом гибридизации in situ и иммуногистохимическим исследованием гемопоэтических колоний, а также с помощью полимеразной цепной реакции. Пока нет однозначного мнения о причинах ингибиции пролиферативной активности стволовых клеток, хотя и установлено, что различные изоляты ВИЧ, воздействуя на CD 34+ клетки, угнетают их функциональную активность. Также установлено, что подавление кроветворения в результате действия ВИЧ связано с усилением продукции костномозговыми моноцитами/макрофагами фактора некроза опухолей. В целом патогенез ВИЧ-инфекции схематично представлен на рис. 8. Причем, накопленные в последние годы данные позволили изменить имевшееся ранее представление о патогенезе ВИЧ-инфекции.
Наряду с поражением иммунной системы в патологический процесс вовлекается и кроветворная ткань. Для заболевания характерны лейкопения, анемия, тромбоцитопения. Угнетается функциональная активность гранулоцитов. Экспериментальные исследования с заражением ВИЧ-подобным ретровирусом LP-BM 5 через 3 месяца в костном мозге выявлена значительная цитопения, снижение содержания эрелых клеток, угнетение гранулоцитопоэза (Magnal M. et al. , 1993). У больных ВИЧ-инфекцией в костном мозге резко снижено содержание колониеобразующих единиц гранулоцитов, макрофагов, мегакариоцитов. Однако дисфункция стволовых клеток не связана с их прямым инфицированием, ибо не обнаружено присутствия ВИЧ в кроветворных клетках при изучении методом гибридизации in situ и иммуногистохимическим исследованием гемопоэтических колоний, а также с помощью полимеразной цепной реакции. Пока нет однозначного мнения о причинах ингибиции пролиферативной активности стволовых клеток, хотя и установлено, что различные изоляты ВИЧ, воздействуя на CD 34+ клетки, угнетают их функциональную активность. Также установлено, что подавление кроветворения в результате действия ВИЧ связано с усилением продукции костномозговыми моноцитами/макрофагами фактора некроза опухолей. В целом патогенез ВИЧ-инфекции схематично представлен на рис. 8. Причем, накопленные в последние годы данные позволили изменить имевшееся ранее представление о патогенезе ВИЧ-инфекции.
 Таким образом, поражение иммунной системы при ВИЧ-инфекции носит системный характер, проявляясь глубокой супрессией Т- и В-звеньев клеточного иммунитета. В ходе развития ВИЧ-инфекции происходят закономерные изменения гиперчувствительности немедленного и замедленного типа, гуморального иммунитета и факторов неспецифической защиты, функциональной активности лимфоцитов и моноцитов/макрофагов. Нарастает уровень сывороточных иммуноглобулинов, циркулирующих иммунных комплексов, продуктов катаболизма клеточных рецепторов (Р-белки). происходят характерные изменения нуклеиновых кислот иммунокометентных клеток и активности в них ферментов основных обменных циклов. Наряду с дефицитом CD 4+ лимфоцитов в динамике болезни нарастает функциональная недостаточность СD 8+ лимфоцитов, NK-клеток, нейтрофилов. Нарушение иммунного статуса клинически проявляется инфекционным, аллергическим, аутоиммунным и лимфопролиферативным синдромами иммунологической недостаточности, синдромом, свойственным болезни иммунных комплексов. Все это определяет в целом клинику ВИЧ-инфекции.
Таким образом, поражение иммунной системы при ВИЧ-инфекции носит системный характер, проявляясь глубокой супрессией Т- и В-звеньев клеточного иммунитета. В ходе развития ВИЧ-инфекции происходят закономерные изменения гиперчувствительности немедленного и замедленного типа, гуморального иммунитета и факторов неспецифической защиты, функциональной активности лимфоцитов и моноцитов/макрофагов. Нарастает уровень сывороточных иммуноглобулинов, циркулирующих иммунных комплексов, продуктов катаболизма клеточных рецепторов (Р-белки). происходят характерные изменения нуклеиновых кислот иммунокометентных клеток и активности в них ферментов основных обменных циклов. Наряду с дефицитом CD 4+ лимфоцитов в динамике болезни нарастает функциональная недостаточность СD 8+ лимфоцитов, NK-клеток, нейтрофилов. Нарушение иммунного статуса клинически проявляется инфекционным, аллергическим, аутоиммунным и лимфопролиферативным синдромами иммунологической недостаточности, синдромом, свойственным болезни иммунных комплексов. Все это определяет в целом клинику ВИЧ-инфекции.
 Правда, имеется и другое мнение о патогенезе ВИЧ-инфекции. Так, В. Колядин (1998) полагает, что супрессия неспецифической защиты, а не дефицит Т-клеточного иммунитета определяют формирование оппортунистической инфекции. Последняя ведет к дефициту Т-клеточного звена иммунитета, а именно снижению количества Т-хелперов (CD 4+ клетки). Отсюда, по мнению автора, дефицит CD 4+ клеток — не причина, а следствие развития оппортунистической инфекции. При всей привлекательности идеи автора имеются и возражения. Как известно, прослеживается определенная связь между характером иммунодефицита и видом возбудителя оппортунистической инфекции: c клеточным связаны вирусная, грибковая инфекция, с гуморальныым — бактериальная. У больных ВИЧ/СПИД основные виды суперинфекций представлены заболеваниями, обусловленными вирусами, простейшими и грибами.
Правда, имеется и другое мнение о патогенезе ВИЧ-инфекции. Так, В. Колядин (1998) полагает, что супрессия неспецифической защиты, а не дефицит Т-клеточного иммунитета определяют формирование оппортунистической инфекции. Последняя ведет к дефициту Т-клеточного звена иммунитета, а именно снижению количества Т-хелперов (CD 4+ клетки). Отсюда, по мнению автора, дефицит CD 4+ клеток — не причина, а следствие развития оппортунистической инфекции. При всей привлекательности идеи автора имеются и возражения. Как известно, прослеживается определенная связь между характером иммунодефицита и видом возбудителя оппортунистической инфекции: c клеточным связаны вирусная, грибковая инфекция, с гуморальныым — бактериальная. У больных ВИЧ/СПИД основные виды суперинфекций представлены заболеваниями, обусловленными вирусами, простейшими и грибами.
 КЛИНИКА Классификация. • Уже через год после появления заболевания было сформулировано определение болезни, основанное на клинических проявлениях, выявленных у больных гомосексуалистов. • Заболевание включало ряд состояний, вызванных условнопатогенными возбудителями, что указывало на дефект в иммунной системе, лежащий в основе болезни в целом. • В 1985 году определение болезни было пересмотрено в связи с расшифровкой этиологии заболевания. Тогда же эксперты ВОЗ для экономически слаборазвитых стран, не имеющих возможности широко внедрить этиологическую расшифровку болезни, разработали клинические критерии для постановки диагноза. Они включали: • а) большие признаки: потеря массы тела > 10% от исходной, хроническая диарея в течение > 1 месяца, длительная лихорадка в течение > 1 месяца (постоянная или интермиттирующая); • б) малые признаки: упорный кашель > месяца, генерализованный зудящий дерматит, герпес зостер в анамнезе, ротоглоточный кандидоз, хроническая прогрессирующая или диссеминированная, герпетическая инфекция (herpes simplex), генерализованная лимфаденопатия.
КЛИНИКА Классификация. • Уже через год после появления заболевания было сформулировано определение болезни, основанное на клинических проявлениях, выявленных у больных гомосексуалистов. • Заболевание включало ряд состояний, вызванных условнопатогенными возбудителями, что указывало на дефект в иммунной системе, лежащий в основе болезни в целом. • В 1985 году определение болезни было пересмотрено в связи с расшифровкой этиологии заболевания. Тогда же эксперты ВОЗ для экономически слаборазвитых стран, не имеющих возможности широко внедрить этиологическую расшифровку болезни, разработали клинические критерии для постановки диагноза. Они включали: • а) большие признаки: потеря массы тела > 10% от исходной, хроническая диарея в течение > 1 месяца, длительная лихорадка в течение > 1 месяца (постоянная или интермиттирующая); • б) малые признаки: упорный кашель > месяца, генерализованный зудящий дерматит, герпес зостер в анамнезе, ротоглоточный кандидоз, хроническая прогрессирующая или диссеминированная, герпетическая инфекция (herpes simplex), генерализованная лимфаденопатия.
 В 1987 году были внесены очередные изменения, к этому времени уже четко было определено, что заболевания, вызванные условнопатогенными возбудителями, ассоциируются с последней стадией СПИДа. Определение 1987 года включает 23 СПИД-ассоциируемые заболевания. Группа экспертов ВОЗ предложила среди СПИД-индикаторных заболеваний выделять заболевания 1 -й и 2 -й категории (табл. 19). Если СПИД-индикаторные болезни первой категории позволяют диагностировать СПИД без лабораторного подтверждения, то при выявлении заболеваний второй категории СПИД можно лишь предполагать, но окончательно диагноз может быть подтвержден лабораторными тестами.
В 1987 году были внесены очередные изменения, к этому времени уже четко было определено, что заболевания, вызванные условнопатогенными возбудителями, ассоциируются с последней стадией СПИДа. Определение 1987 года включает 23 СПИД-ассоциируемые заболевания. Группа экспертов ВОЗ предложила среди СПИД-индикаторных заболеваний выделять заболевания 1 -й и 2 -й категории (табл. 19). Если СПИД-индикаторные болезни первой категории позволяют диагностировать СПИД без лабораторного подтверждения, то при выявлении заболеваний второй категории СПИД можно лишь предполагать, но окончательно диагноз может быть подтвержден лабораторными тестами.
 Таблица 19. СПИД-индикаторные заболевания Заболевания I группы* 1. Кандидоз пищевода, бронхов или легких 2. Внелегочной криптококкоз (европейский бластомикоз) 3. Криптоспородиоз с диареей, продолжающейся более 1 мес. 4. Цитомегаловирусные поражения каких-либо органов ( за исключением печени, селезенки и лимфатических узлов) у больного старше 1 мес. 5. Инфекция, обусловленная вирусом простого герпеса с язвенным поражением на коже и/или слизистых оболочках, которые персистируют дольше 1 мес. ; герпетические бронхиты, пневмонии, или эзофагиты любой продолжительности у больного старше 1 мес. 6. Саркома Капоши у больного моложе 60 лет 7. Лимфома головного мозга у больного моложе 60 лет 8. Лимфоцитарная интерстициальная пневмония и/или легочная лимфоидная гиперплазия у детей в возрасте до 14 лет 9. Диссеминированная инфекция, вызванная бактериями группы Mycobakterium avium intercellulare или M. kansassii с поражением различных органов (за исключением или помимо легких, кожи, шейных или прикорневых лимфатических узлов) 10. Пневмоцистная пневмония 11. Прогрессирующая многоочаговая лейкоэнцефалопатия 12. Токсоплазмоз ЦНС у больных старше 1 мес.
Таблица 19. СПИД-индикаторные заболевания Заболевания I группы* 1. Кандидоз пищевода, бронхов или легких 2. Внелегочной криптококкоз (европейский бластомикоз) 3. Криптоспородиоз с диареей, продолжающейся более 1 мес. 4. Цитомегаловирусные поражения каких-либо органов ( за исключением печени, селезенки и лимфатических узлов) у больного старше 1 мес. 5. Инфекция, обусловленная вирусом простого герпеса с язвенным поражением на коже и/или слизистых оболочках, которые персистируют дольше 1 мес. ; герпетические бронхиты, пневмонии, или эзофагиты любой продолжительности у больного старше 1 мес. 6. Саркома Капоши у больного моложе 60 лет 7. Лимфома головного мозга у больного моложе 60 лет 8. Лимфоцитарная интерстициальная пневмония и/или легочная лимфоидная гиперплазия у детей в возрасте до 14 лет 9. Диссеминированная инфекция, вызванная бактериями группы Mycobakterium avium intercellulare или M. kansassii с поражением различных органов (за исключением или помимо легких, кожи, шейных или прикорневых лимфатических узлов) 10. Пневмоцистная пневмония 11. Прогрессирующая многоочаговая лейкоэнцефалопатия 12. Токсоплазмоз ЦНС у больных старше 1 мес.
 Заболевания II группы ** 1. Бактериальные инфекции, сочетанные или рецидивирующие у детей до 14 лет (более 2 случаев за 2 года наблюдения): септицемия, пневмония, менингит, поражения костей и суставов 2. Кандидомикоз диссеминированный (внелегочная локализация) 3. ВИЧ-энцефалопатия (“ВИЧ-деменция”, “СПИД-деменция”) 4. Гистоплазмоз диссеминированный с внелегочной локализацией 5. Изоспориоз с диареей, персистирующий более 1 мес. 6. Саркома Капоши у людей старше 60 лет 7. Лимфома головного мозга (первичная) у людей старше 60 лет 8. Другие В-клеточные лимфомы (за исключением болезни Ходжкина) или лимфомы неизвестного иммунофенотипа 9. Микобактериоз диссеминированный (не туберкулез) с поражением помимо легких, кожи, шейных или прикорневых лимфатических узлов 10. Туберкулез внелегочной (с поражением органов помимо легких) 11. Сальмонеллезная септицемия рецидивитрующая, обусловленная не S. thyphi 12. ВИЧ-дистрофия (истощение, резкое похудание)
Заболевания II группы ** 1. Бактериальные инфекции, сочетанные или рецидивирующие у детей до 14 лет (более 2 случаев за 2 года наблюдения): септицемия, пневмония, менингит, поражения костей и суставов 2. Кандидомикоз диссеминированный (внелегочная локализация) 3. ВИЧ-энцефалопатия (“ВИЧ-деменция”, “СПИД-деменция”) 4. Гистоплазмоз диссеминированный с внелегочной локализацией 5. Изоспориоз с диареей, персистирующий более 1 мес. 6. Саркома Капоши у людей старше 60 лет 7. Лимфома головного мозга (первичная) у людей старше 60 лет 8. Другие В-клеточные лимфомы (за исключением болезни Ходжкина) или лимфомы неизвестного иммунофенотипа 9. Микобактериоз диссеминированный (не туберкулез) с поражением помимо легких, кожи, шейных или прикорневых лимфатических узлов 10. Туберкулез внелегочной (с поражением органов помимо легких) 11. Сальмонеллезная септицемия рецидивитрующая, обусловленная не S. thyphi 12. ВИЧ-дистрофия (истощение, резкое похудание)
 Примечания: * для постановки диагноза СПИД не требуется лабораторное подтверждение ** для постановки диагноза требуется лабораторное подтверждение В вопросе клинической классификации, оценке стадии болезни, определении понятий “СПИД-ассоциируемые заболевания”, “СПИД-индикаторные болезни”, “Стадия СПИД” много остается спорного, неоднозначно трактуемого и условного. К примеру, нет единства в определении состояний, расцениваемых как фаза “СПИД” и фаза “Пре-СПИД” или “СПИД-ассоциируемый комплекс”. Так у женщин шеечная дисплазия, тазовые воспалительные процессы и восходящие кандидозные вульвовагиниты, у наркоманов легочной туберкулез, эндокардит, сепсис и бактериальная пневмония обычно у инфицированных ВИЧ ассоциируют с глубоким иммунодефицитом и их правильнее расценивать как больных СПИДом, а не как ВИЧ-связанные состояния и уровень CD 4+ лимфоцитов, превышающий показатель 200 клеток/ мм не должен довлеть в постановке диагноза. CDC (США) выступает против добавления новых ВИЧ-ассоциируемых состояний в определение понятий “СПИД”, так как по мнению специалистов Центра наиболее объективный критерий — количество Т-хелперов, а не клинические критерии, ибо многие из этих состояний часто встречаются у лиц, не инфицированных ВИЧ. В 1991 году Центр предложил расширить список СПИД-ассоциированных заболеваний и определил, что постановка диагноза СПИД может быть в случаях, если: а) у инфицированного имеется одно из 23 СПИД-ассоциированных состояний или б) он ВИЧ-инфицирован и имеет менее 200 СD 4+ клеток/мм.
Примечания: * для постановки диагноза СПИД не требуется лабораторное подтверждение ** для постановки диагноза требуется лабораторное подтверждение В вопросе клинической классификации, оценке стадии болезни, определении понятий “СПИД-ассоциируемые заболевания”, “СПИД-индикаторные болезни”, “Стадия СПИД” много остается спорного, неоднозначно трактуемого и условного. К примеру, нет единства в определении состояний, расцениваемых как фаза “СПИД” и фаза “Пре-СПИД” или “СПИД-ассоциируемый комплекс”. Так у женщин шеечная дисплазия, тазовые воспалительные процессы и восходящие кандидозные вульвовагиниты, у наркоманов легочной туберкулез, эндокардит, сепсис и бактериальная пневмония обычно у инфицированных ВИЧ ассоциируют с глубоким иммунодефицитом и их правильнее расценивать как больных СПИДом, а не как ВИЧ-связанные состояния и уровень CD 4+ лимфоцитов, превышающий показатель 200 клеток/ мм не должен довлеть в постановке диагноза. CDC (США) выступает против добавления новых ВИЧ-ассоциируемых состояний в определение понятий “СПИД”, так как по мнению специалистов Центра наиболее объективный критерий — количество Т-хелперов, а не клинические критерии, ибо многие из этих состояний часто встречаются у лиц, не инфицированных ВИЧ. В 1991 году Центр предложил расширить список СПИД-ассоциированных заболеваний и определил, что постановка диагноза СПИД может быть в случаях, если: а) у инфицированного имеется одно из 23 СПИД-ассоциированных состояний или б) он ВИЧ-инфицирован и имеет менее 200 СD 4+ клеток/мм.
 Одна из первых классификаций, рекомендованных ВОЗ (1988), рассматривала 4 стадии болезни и все классификации более позднего времени, практически модернизируют ее, сохраняя основные положения. Эта классификация выделяла стадии: 1. Начальная (острая) ВИЧ-инфекция; 2. Персистирующая генерализованная лимфаденопатия; 3. СПИД-ассоциированный комплекс – пре. СПИД; 4. Развернутый СПИД. В странах СНГ получила распространение классификация, предложенная В. И. Покровским (1989), переработанная в 2001 г. (табл. 20 и 21). .
Одна из первых классификаций, рекомендованных ВОЗ (1988), рассматривала 4 стадии болезни и все классификации более позднего времени, практически модернизируют ее, сохраняя основные положения. Эта классификация выделяла стадии: 1. Начальная (острая) ВИЧ-инфекция; 2. Персистирующая генерализованная лимфаденопатия; 3. СПИД-ассоциированный комплекс – пре. СПИД; 4. Развернутый СПИД. В странах СНГ получила распространение классификация, предложенная В. И. Покровским (1989), переработанная в 2001 г. (табл. 20 и 21). .
 В I стадии (инкубация) диагноз может носить только предположительный характер, так как основывается исключительно на эпидемиологических данных: половой контакт с инфицированным ВИЧ партнером, переливание крови серопозитивного к ВИЧ донора, использование нестерильных шприцев при групповом введении наркотиков и т. п. Инкубационный период при инфицировании ВИЧ продолжается от 2 -3 недель до нескольких месяцев или даже лет. Клинических проявлений болезни нет, сохраняется нормальная активность, антитела к ВИЧ не определяются. Но уже в этот период возможно выявление вируса методом полимеразной цепной реакции.
В I стадии (инкубация) диагноз может носить только предположительный характер, так как основывается исключительно на эпидемиологических данных: половой контакт с инфицированным ВИЧ партнером, переливание крови серопозитивного к ВИЧ донора, использование нестерильных шприцев при групповом введении наркотиков и т. п. Инкубационный период при инфицировании ВИЧ продолжается от 2 -3 недель до нескольких месяцев или даже лет. Клинических проявлений болезни нет, сохраняется нормальная активность, антитела к ВИЧ не определяются. Но уже в этот период возможно выявление вируса методом полимеразной цепной реакции.
 Таблица 20. Клиническая классификация ВИЧ-инфекции (по В. И. Покровскому, верситя 1989 г. ) I. Стадия инкубации. II. Стадия первичных проявлений: А — острая лихорадочная фаза Б — бессимптомная фаза В — персистирующая генерализованная лимфаденопатия III. Стадия вторичных заболеваний: А — потеря массы тела менее 10%, поверхностные грибковые, бактериальные, вирусные поражения кожи и слизистых оболочек, опоясывающий герпес, повторные фарингиты, синуситы; Б — прогрессирующая потеря массы тела более 10%, необъяснимая диарея или лихорадка более 1 мес. , повторные или стойкие бактериальные, грибковые, протозойные поражения внутренних органов (без диссеминации) или глубокие поражения кожи и слизистых оболочек, повторный или диссеминированный опоясывающий лишай, локализованная саркома Капоши; В — генерализованные бактериальные, грибковые, вирусные, протозойные, паразитарные заболевания, пневмоцистная пневмония, кандидоз пищевода, атипичный микобактериоз, внелегочный туберкулез, кахексия, диссеминированная саркома Капоши, поражения центральной нервной системы различной этиологии. IV. Терминальная стадия
Таблица 20. Клиническая классификация ВИЧ-инфекции (по В. И. Покровскому, верситя 1989 г. ) I. Стадия инкубации. II. Стадия первичных проявлений: А — острая лихорадочная фаза Б — бессимптомная фаза В — персистирующая генерализованная лимфаденопатия III. Стадия вторичных заболеваний: А — потеря массы тела менее 10%, поверхностные грибковые, бактериальные, вирусные поражения кожи и слизистых оболочек, опоясывающий герпес, повторные фарингиты, синуситы; Б — прогрессирующая потеря массы тела более 10%, необъяснимая диарея или лихорадка более 1 мес. , повторные или стойкие бактериальные, грибковые, протозойные поражения внутренних органов (без диссеминации) или глубокие поражения кожи и слизистых оболочек, повторный или диссеминированный опоясывающий лишай, локализованная саркома Капоши; В — генерализованные бактериальные, грибковые, вирусные, протозойные, паразитарные заболевания, пневмоцистная пневмония, кандидоз пищевода, атипичный микобактериоз, внелегочный туберкулез, кахексия, диссеминированная саркома Капоши, поражения центральной нервной системы различной этиологии. IV. Терминальная стадия
 II стадия (первичных проявлений): IIA стадия — острая лихорадочная. Она же начальная (острая) ВИЧ-инфекция. У части зараженных спустя 2 -5 мес. после проникновения вируса в организм может развиться острое заболевание, протекащее нередко с повышением температуры тела, выраженной интоксикации, тонзиллитом и мононуклеозоподобным синдромом. Помимо лихорадки в этой фазе болезни часто встречаются кореподобная или краснухоподобная сыпь на коже, миалгия, артралгия, язвы в горле, реже в ротовой полости. Иногда заболевание протекает по типу острой респираторной инфекции, в этих случаях больных беспокоит кашель. У части больных развивается полиаденопатия с увеличением 2 -3 групп лимфатических узлов. Увеличение поверхностных лимфатических узлов чаще начинается с затылочных и заднешейных, затем уже увеличиваются подчелюстные, подмышечные и паховые. При пальпации лимфатические узлы эластичные, безболезненные, подвижные, не спаяны между собой и окружающей тканью, размерами от 1 до 5 см, чаще 2 -3 см в диаметре. Иногда этим явлениям сопутствуют немотивированные утомляемость, слабость. Кроме того, регистрируются переходящие нарушения деятельности ЦНС — от головных болей до энцефалита.
II стадия (первичных проявлений): IIA стадия — острая лихорадочная. Она же начальная (острая) ВИЧ-инфекция. У части зараженных спустя 2 -5 мес. после проникновения вируса в организм может развиться острое заболевание, протекащее нередко с повышением температуры тела, выраженной интоксикации, тонзиллитом и мононуклеозоподобным синдромом. Помимо лихорадки в этой фазе болезни часто встречаются кореподобная или краснухоподобная сыпь на коже, миалгия, артралгия, язвы в горле, реже в ротовой полости. Иногда заболевание протекает по типу острой респираторной инфекции, в этих случаях больных беспокоит кашель. У части больных развивается полиаденопатия с увеличением 2 -3 групп лимфатических узлов. Увеличение поверхностных лимфатических узлов чаще начинается с затылочных и заднешейных, затем уже увеличиваются подчелюстные, подмышечные и паховые. При пальпации лимфатические узлы эластичные, безболезненные, подвижные, не спаяны между собой и окружающей тканью, размерами от 1 до 5 см, чаще 2 -3 см в диаметре. Иногда этим явлениям сопутствуют немотивированные утомляемость, слабость. Кроме того, регистрируются переходящие нарушения деятельности ЦНС — от головных болей до энцефалита.
 В крови больных в этот период выявляется лимфопения, но количество CD 4+ лимфоцитов более 500 в 1 мкл. К исходу второй недели в сыворотке крови могут быть обнаружены специфические антитела к антигенам ВИЧ. Продолжительность этого лихорадочного состояния — от нескольких дней до 1 -2 мес. , после чего лимфаденопатия может исчезнуть и болезнь переходит в бессимптомную фазу (IIБ). Длительность IIБ фазы от 1 -2 мес. до нескольких лет, но в среднем около 6 мес. Никаких клинических проявлений заболевания не отмечается, хотя вирус остается в организме и размножается. Иммунный статус при этом сохраняется в пределах нормы, количество лимфоцитов, в том числе CD 4+, нормальное. Результаты исследований в ИФА и иммуноблоттинге положительны.
В крови больных в этот период выявляется лимфопения, но количество CD 4+ лимфоцитов более 500 в 1 мкл. К исходу второй недели в сыворотке крови могут быть обнаружены специфические антитела к антигенам ВИЧ. Продолжительность этого лихорадочного состояния — от нескольких дней до 1 -2 мес. , после чего лимфаденопатия может исчезнуть и болезнь переходит в бессимптомную фазу (IIБ). Длительность IIБ фазы от 1 -2 мес. до нескольких лет, но в среднем около 6 мес. Никаких клинических проявлений заболевания не отмечается, хотя вирус остается в организме и размножается. Иммунный статус при этом сохраняется в пределах нормы, количество лимфоцитов, в том числе CD 4+, нормальное. Результаты исследований в ИФА и иммуноблоттинге положительны.
 IIВ фаза — персистирующая генерализованная лимфаденопатия. Единственным клиническим проявлением болезни в этой стадии может быть только увеличение лимфатических узлов, сохраняющееся месяцы и даже годы. Увеличиваются почти все периферические лимфатические узлы, но наиболее характерно увеличение заднешейных, надключичных, подмышечных и локтевых лимфатических узлов. Особенно характерным и настораживающим врача следует считать увеличение подчелюстных лимфатических узлов при отсутствии патологии полости рта. Нередко увеличиваются мезентериальные лимфатические узлы, которые при пальпации болезненны, иногда симулируя картину “острого” живота. Но лимфатические узлы, увеличенные размером до 5 см в диаметре, могут оставаться безболезненными, с тенденцией к слиянию. В 20% у больных выявляются увеличенными печень и селезенка. В этой фазе болезнь необходимо дифференцировать с острым токсоплазмозом, инфекционным мононуклеозом, сифилисом, ревматоидным артритом, системной красной волчанкой, лимфогранулематозом, саркоидозом. При иммунологическом обследовании в этой стадии болезни общее количество лимфоцитов выше 50% региональной и возрастной нормы, количество CD 4+ лимфоцитов более 500 в 1 мкл. Трудовая и половая активность больных сохранена.
IIВ фаза — персистирующая генерализованная лимфаденопатия. Единственным клиническим проявлением болезни в этой стадии может быть только увеличение лимфатических узлов, сохраняющееся месяцы и даже годы. Увеличиваются почти все периферические лимфатические узлы, но наиболее характерно увеличение заднешейных, надключичных, подмышечных и локтевых лимфатических узлов. Особенно характерным и настораживающим врача следует считать увеличение подчелюстных лимфатических узлов при отсутствии патологии полости рта. Нередко увеличиваются мезентериальные лимфатические узлы, которые при пальпации болезненны, иногда симулируя картину “острого” живота. Но лимфатические узлы, увеличенные размером до 5 см в диаметре, могут оставаться безболезненными, с тенденцией к слиянию. В 20% у больных выявляются увеличенными печень и селезенка. В этой фазе болезнь необходимо дифференцировать с острым токсоплазмозом, инфекционным мононуклеозом, сифилисом, ревматоидным артритом, системной красной волчанкой, лимфогранулематозом, саркоидозом. При иммунологическом обследовании в этой стадии болезни общее количество лимфоцитов выше 50% региональной и возрастной нормы, количество CD 4+ лимфоцитов более 500 в 1 мкл. Трудовая и половая активность больных сохранена.
 III стадия (вторичных заболеваний) характеризуется развитием бактериальных, вирусных и протозойных заболеваний и/или опухолевого процесса, чаще лимфомы или саркомы Капоши. IIIA фаза является переходной от персистирующей генерализованной лимфаденопатии к СПИД-ассоциированному комплексу. В этот период иммуносупрессия выражена стойкой и глубоко: в сыворотке крови нарастает содержание гаммаглобулинов (до 20 -27%), растет уровень иммуноглобулинов, преимущественно за счет класса Ig. G, снижена фагоцитарная активность лейкоцитов, снижается РБТЛ на митогены. Количество CD 4+ лимфоцитов падает ниже 500 и на протяжении этой и следующей фаз до 200 клеток в 1 мкл. Клинически выявляются признаки вирусной интоксикации, лихорадка с повышением температуры тела до 38 о С носит постоянный или перемежающий характер, сопровождается ночными потами, слабостью и быстрой утомляемостью, диареей. Потеря массы тела до 10%. В этой фазе еще нет присоединения выраженной оппортунистической инфекции или инвазии, не развиваются еще и саркома Капоши или друге злокачественные опухоли. Но тем не менее СПИД-маркерные инфекции уже налицо в виде инфекции, вызванной вирусом простого герпеса, токсоплазмоза, кандидозного эзофагита. На коже процесс в виде кандидоза, лейкоплакии, кондилом. Так как фаза IIIA по сути неосложненная генерализованной инфекцией или злокачественным опухолевым процессом форма, некоторые клиницисты полагают, что она может под влиянием адекватной терапии завершиться выздоровлением и считают целесообразным выделение ее в самостоятельную форму. Некоторые клиницисты обозначают эту фазу как продромальный период СПИД.
III стадия (вторичных заболеваний) характеризуется развитием бактериальных, вирусных и протозойных заболеваний и/или опухолевого процесса, чаще лимфомы или саркомы Капоши. IIIA фаза является переходной от персистирующей генерализованной лимфаденопатии к СПИД-ассоциированному комплексу. В этот период иммуносупрессия выражена стойкой и глубоко: в сыворотке крови нарастает содержание гаммаглобулинов (до 20 -27%), растет уровень иммуноглобулинов, преимущественно за счет класса Ig. G, снижена фагоцитарная активность лейкоцитов, снижается РБТЛ на митогены. Количество CD 4+ лимфоцитов падает ниже 500 и на протяжении этой и следующей фаз до 200 клеток в 1 мкл. Клинически выявляются признаки вирусной интоксикации, лихорадка с повышением температуры тела до 38 о С носит постоянный или перемежающий характер, сопровождается ночными потами, слабостью и быстрой утомляемостью, диареей. Потеря массы тела до 10%. В этой фазе еще нет присоединения выраженной оппортунистической инфекции или инвазии, не развиваются еще и саркома Капоши или друге злокачественные опухоли. Но тем не менее СПИД-маркерные инфекции уже налицо в виде инфекции, вызванной вирусом простого герпеса, токсоплазмоза, кандидозного эзофагита. На коже процесс в виде кандидоза, лейкоплакии, кондилом. Так как фаза IIIA по сути неосложненная генерализованной инфекцией или злокачественным опухолевым процессом форма, некоторые клиницисты полагают, что она может под влиянием адекватной терапии завершиться выздоровлением и считают целесообразным выделение ее в самостоятельную форму. Некоторые клиницисты обозначают эту фазу как продромальный период СПИД.
 IIIБ фаза по клиническим проявлениям близка к понятию СПИД-ассоциированный комплекс. Именно в этой фазе появляются симптомы выраженного нарушения клеточного иммунитета: отсутствие реакции ГЗТ на три из четырех кожных проб (внутрикожное введение туберкулина, кандидина, трихофитина и др. ). Клиника характеризуется лихорадкой длительностью более 1 мес. , упорной необъяснимой диареей, ночными потами, сопровождается интоксикацией, снижением массы тела свыше 10%. Персистирующая лимфаденопатия приобретает генерализованный характер. Лабораторно выявляется снижение коэффициента CD 4/CD 8, нарастает лейкопения, тромбоцитопения, анемия, в крови растут циркулирующие иммунные комплексы, идет дальнейшее снижение показателей РБТЛ, угнетение ГЗТ. В этой фазе наличие двух из характерных клинических проявлений и двух лабораторных показателей, особенно с учетом эпидемиологии позволяет с высокой степенью достоверности диагностировать ВИЧ-инфекцию.
IIIБ фаза по клиническим проявлениям близка к понятию СПИД-ассоциированный комплекс. Именно в этой фазе появляются симптомы выраженного нарушения клеточного иммунитета: отсутствие реакции ГЗТ на три из четырех кожных проб (внутрикожное введение туберкулина, кандидина, трихофитина и др. ). Клиника характеризуется лихорадкой длительностью более 1 мес. , упорной необъяснимой диареей, ночными потами, сопровождается интоксикацией, снижением массы тела свыше 10%. Персистирующая лимфаденопатия приобретает генерализованный характер. Лабораторно выявляется снижение коэффициента CD 4/CD 8, нарастает лейкопения, тромбоцитопения, анемия, в крови растут циркулирующие иммунные комплексы, идет дальнейшее снижение показателей РБТЛ, угнетение ГЗТ. В этой фазе наличие двух из характерных клинических проявлений и двух лабораторных показателей, особенно с учетом эпидемиологии позволяет с высокой степенью достоверности диагностировать ВИЧ-инфекцию.
 IIIВ фаза клинически представляет развернутую картину СПИДа. За счет глубокого поражения иммунной системы (количество СД 4+ лимфоцитов менее 200 в 1 мм ) оппортунистическая инфекция приобретает генерализованный характер, развиваются или наслаиваются на инфекционный процесс новообразования в виде диссеминированной саркомы и злокачественной лимфомы. Из инфекционных возбудителей чаще всего встречаются пневмоцисты, кандида, вирусы герпетической группы (вирус простого герпеса, герпес зостер, цитомегаловирус, вирус Эпштейна-Барр). Инфекционный процесс также вызывают микобактерии, легионеллы, кандида, сальмонеллы, микоплазмы, а также в южном регионе токсоплазмы, криптоспоридии, стронгилоидии, гистоплазмы, криптококки и ряд других возбудителей. В зависимости от преимущественной локализации очага выделяют ряд клинических форм: а) с преимущественным поражением легких (до 60% случаев), б) с поражением желудочно-кишечного тракта, в) с церебральными поражениями и/или психоневрологическими проявлениями, г) с поражением кожи и слизистых оболочек, д) генерализованные и/или септические формы, е) недифференцированные формы, в основном с астеновегетативным синдромом, длительной лихорадкой и потерей массы тела. В целом заболевание характеризуется развитием гнойных осложнений, астенией, больной более половины времени вынужден находиться в постели. В процессе болезни этиологические факторы могут меняться.
IIIВ фаза клинически представляет развернутую картину СПИДа. За счет глубокого поражения иммунной системы (количество СД 4+ лимфоцитов менее 200 в 1 мм ) оппортунистическая инфекция приобретает генерализованный характер, развиваются или наслаиваются на инфекционный процесс новообразования в виде диссеминированной саркомы и злокачественной лимфомы. Из инфекционных возбудителей чаще всего встречаются пневмоцисты, кандида, вирусы герпетической группы (вирус простого герпеса, герпес зостер, цитомегаловирус, вирус Эпштейна-Барр). Инфекционный процесс также вызывают микобактерии, легионеллы, кандида, сальмонеллы, микоплазмы, а также в южном регионе токсоплазмы, криптоспоридии, стронгилоидии, гистоплазмы, криптококки и ряд других возбудителей. В зависимости от преимущественной локализации очага выделяют ряд клинических форм: а) с преимущественным поражением легких (до 60% случаев), б) с поражением желудочно-кишечного тракта, в) с церебральными поражениями и/или психоневрологическими проявлениями, г) с поражением кожи и слизистых оболочек, д) генерализованные и/или септические формы, е) недифференцированные формы, в основном с астеновегетативным синдромом, длительной лихорадкой и потерей массы тела. В целом заболевание характеризуется развитием гнойных осложнений, астенией, больной более половины времени вынужден находиться в постели. В процессе болезни этиологические факторы могут меняться.
 IV (терминальная) стадия протекает с максимальным развертыванием клиники, развивается кахексия, держится лихорадка, выражена интоксикация, больной все время проводит в кровати. Развивается деменция. Нарастает вирусемия, содержание лимфоцитов достигает критических величин. Болезнь прогрессирует и больной погибает.
IV (терминальная) стадия протекает с максимальным развертыванием клиники, развивается кахексия, держится лихорадка, выражена интоксикация, больной все время проводит в кровати. Развивается деменция. Нарастает вирусемия, содержание лимфоцитов достигает критических величин. Болезнь прогрессирует и больной погибает.
 Таблица 21. Российская классификация ВИЧ-инфекции (Покровский В. И. , 2001) Стадии Характеристика 1. Инкубации 2. Первичных проявлений Варианты течения: А. Бессимптомная Б. Острая ВИЧ-инфекция без вторичных заболеваний В. Острая инфекция с вторичными заболеваниями 3. Латентная стадия 4. Стадия вторичных заболевани й 4 А – Потеря веса менее 10%; грибковые, вирусные, бактериальные поражения кожи и слизистых; опоясывающий лишай; повторные фарингиты, синуситы. Фазы: · Прогрессирование (на фоне отсутствия противоретровирусной терапии; на фоне противоретровирусной терапии); · Ремиссия (спонтанная; после ранее проводимой противоретровирусной терапии; на фоне противоретровирусной терапии). 4 Б – Потеря веса более 10%; необъяснимая диарея или лихорадка более одного месяца; волосистая лейкоплакия; туберкулез легких; повторные или стойкие вирусные, бактериальные, грибковые, протозойные поражения внутренних органов; повторный или диссеминированный опоясывающий лишай; локализованная саркома Капоши. Фазы: · Прогрессирование (на фоне отсутствия противоретровирусной терапии; на фоне противоретровирусной терапии); · Ремиссия (спонтанная; после ранее проводимой противоретровирусной терапии; на фоне противоретровирусной терапии). 4 В — Кахексия; генерализованные бактериальные, вирусные, грибковые, протозойные или паразитарные заболевания; пневмоцистная пневмония; кандидоз пищевода, бронхов, легких; внелегочный туберкулез; атипичные микобактериозы, диссеминированная саркома Капоши, поражения центральной нервной системы различной этиологии. Фазы: · Прогрессирование (на фоне отсутствия противоретровирусной терапии; на фоне противоретровирусной терапии); · Ремиссия (спонтанная; после ранее проводимой противоретровирусной терапии; на фоне противоретровирусной терапии). Терминальная
Таблица 21. Российская классификация ВИЧ-инфекции (Покровский В. И. , 2001) Стадии Характеристика 1. Инкубации 2. Первичных проявлений Варианты течения: А. Бессимптомная Б. Острая ВИЧ-инфекция без вторичных заболеваний В. Острая инфекция с вторичными заболеваниями 3. Латентная стадия 4. Стадия вторичных заболевани й 4 А – Потеря веса менее 10%; грибковые, вирусные, бактериальные поражения кожи и слизистых; опоясывающий лишай; повторные фарингиты, синуситы. Фазы: · Прогрессирование (на фоне отсутствия противоретровирусной терапии; на фоне противоретровирусной терапии); · Ремиссия (спонтанная; после ранее проводимой противоретровирусной терапии; на фоне противоретровирусной терапии). 4 Б – Потеря веса более 10%; необъяснимая диарея или лихорадка более одного месяца; волосистая лейкоплакия; туберкулез легких; повторные или стойкие вирусные, бактериальные, грибковые, протозойные поражения внутренних органов; повторный или диссеминированный опоясывающий лишай; локализованная саркома Капоши. Фазы: · Прогрессирование (на фоне отсутствия противоретровирусной терапии; на фоне противоретровирусной терапии); · Ремиссия (спонтанная; после ранее проводимой противоретровирусной терапии; на фоне противоретровирусной терапии). 4 В — Кахексия; генерализованные бактериальные, вирусные, грибковые, протозойные или паразитарные заболевания; пневмоцистная пневмония; кандидоз пищевода, бронхов, легких; внелегочный туберкулез; атипичные микобактериозы, диссеминированная саркома Капоши, поражения центральной нервной системы различной этиологии. Фазы: · Прогрессирование (на фоне отсутствия противоретровирусной терапии; на фоне противоретровирусной терапии); · Ремиссия (спонтанная; после ранее проводимой противоретровирусной терапии; на фоне противоретровирусной терапии). Терминальная
 За рубежом нашла применение классификация, предложенная ВОЗ в 1991 году (табл. 22). Таблица 22. Классификация ВИЧ-инфекции (ВОЗ, 1991) Клиническая стадия Клинические проявления Соматическое благополучие I (бессимптомн ая, генерализова нная лимфоаденоп атия) 1. Отсутствие симптомов 2. Персистирующая генерализованная лимфоаденопатия Нормальная активность II (ранняя или слабовыраже нная) 1. Потеря массы тела 10% 2. Необъяснимая диарея > 1 мес. 3. Необъяснимая лихорадка > 1 мес. 4. Кандидоз полости рта 5. Лейкоплакия ротовой полости 6. Легочной туберкулез в течении 1 года 7. Тяжелые бактериальные инфекции ( пневмония и др. ) Прикован к постели менее 50% дней в течении последнего месяца IV собственно СПИД (поздняя, выраженная клиника) 1. Вэйстинг-синдром 2. Пневмоцистная пневмония 3. Церебральный токсоплазмоз 4. Криптоспороидоз с диареей 5. ЦМВ-ое поражение органов, кроме печени, селезенки, лиматических узлов 6. Герпетическое поражение кожи, слизистых оболочек > 1 мес или висцеральные герпетические поражения независимо от длительности 7. Прогрессирующая многоочаговая лейкоэнцефалопатия 8. Любой диссеминирующий эндемичный микоз 9. Кандидоз пищевода, трахеи, бронхов и легких 10. Атипичный диссеминированный микобактериоз 11. Нетифозная сальмонеллезная септицемия 12. Экстрапульмональный туберкулез 13. Лимфома 14. Саркома Капоши 15. ВИЧ-энцефалопатия Прикован к постели менее 50% дней в течении последнего месяца
За рубежом нашла применение классификация, предложенная ВОЗ в 1991 году (табл. 22). Таблица 22. Классификация ВИЧ-инфекции (ВОЗ, 1991) Клиническая стадия Клинические проявления Соматическое благополучие I (бессимптомн ая, генерализова нная лимфоаденоп атия) 1. Отсутствие симптомов 2. Персистирующая генерализованная лимфоаденопатия Нормальная активность II (ранняя или слабовыраже нная) 1. Потеря массы тела 10% 2. Необъяснимая диарея > 1 мес. 3. Необъяснимая лихорадка > 1 мес. 4. Кандидоз полости рта 5. Лейкоплакия ротовой полости 6. Легочной туберкулез в течении 1 года 7. Тяжелые бактериальные инфекции ( пневмония и др. ) Прикован к постели менее 50% дней в течении последнего месяца IV собственно СПИД (поздняя, выраженная клиника) 1. Вэйстинг-синдром 2. Пневмоцистная пневмония 3. Церебральный токсоплазмоз 4. Криптоспороидоз с диареей 5. ЦМВ-ое поражение органов, кроме печени, селезенки, лиматических узлов 6. Герпетическое поражение кожи, слизистых оболочек > 1 мес или висцеральные герпетические поражения независимо от длительности 7. Прогрессирующая многоочаговая лейкоэнцефалопатия 8. Любой диссеминирующий эндемичный микоз 9. Кандидоз пищевода, трахеи, бронхов и легких 10. Атипичный диссеминированный микобактериоз 11. Нетифозная сальмонеллезная септицемия 12. Экстрапульмональный туберкулез 13. Лимфома 14. Саркома Капоши 15. ВИЧ-энцефалопатия Прикован к постели менее 50% дней в течении последнего месяца
 В США с 1993 года стала применяться классификация, разработанная CDC на основании вышеприведенной классификации ВОЗ, рассчитанная на взрослых и подростков (табл. 23). Таблица 23. Классификация стадий ВИЧ-инфекции и расширенное определение случая СПИДа у взрослых и подростков. Число (%) CD 4+ Т-лимфоцитов в мкл Клинические категории A Бессимптомная острая (первичная) или ПГЛП B Манифест ная ни A ни C C СПИД — индикаторные заболевания 1. > 500 (>29%) A 1 B 1 C 1* 2. 200 -499 (14 — 28 %) A 2 B 2 C 2* 2. < 200 ( <14%) = индикатор СПИДа A 3* B 3* C 3* Симптомы в подгруппах: А: Острый ретровирусный синдром Генерализованная лимаденопатия (ГЛАП) Бессимптомное течение В: Синдромы СПИД-ассоциированного комплекса Кандидоз полости рта Дисплазия шейки матки Органические поражения Опоясывающий герпес Идиопатическая тромбоцитопения Листериоз Лейкоплакия Периферическая нейропатия С: Собственно СПИД CD 4 < 200 Кандидоз легких или пищевода Рак шейки матки Кокцидиоидоз Криптоспороидоз Цитомегаловирусная инфекция Герпетический эзофагит ВИЧ-энцефалопатия Гистоплазмоз Изоспориоз Саркома Капоши Лимфома Микобактериоз Пневмоцистоз Бактериальная пневмония Прогрессирующая многоочаговая лейкоэнцефалопатия Сальмонеллез
В США с 1993 года стала применяться классификация, разработанная CDC на основании вышеприведенной классификации ВОЗ, рассчитанная на взрослых и подростков (табл. 23). Таблица 23. Классификация стадий ВИЧ-инфекции и расширенное определение случая СПИДа у взрослых и подростков. Число (%) CD 4+ Т-лимфоцитов в мкл Клинические категории A Бессимптомная острая (первичная) или ПГЛП B Манифест ная ни A ни C C СПИД — индикаторные заболевания 1. > 500 (>29%) A 1 B 1 C 1* 2. 200 -499 (14 — 28 %) A 2 B 2 C 2* 2. < 200 ( <14%) = индикатор СПИДа A 3* B 3* C 3* Симптомы в подгруппах: А: Острый ретровирусный синдром Генерализованная лимаденопатия (ГЛАП) Бессимптомное течение В: Синдромы СПИД-ассоциированного комплекса Кандидоз полости рта Дисплазия шейки матки Органические поражения Опоясывающий герпес Идиопатическая тромбоцитопения Листериоз Лейкоплакия Периферическая нейропатия С: Собственно СПИД CD 4 < 200 Кандидоз легких или пищевода Рак шейки матки Кокцидиоидоз Криптоспороидоз Цитомегаловирусная инфекция Герпетический эзофагит ВИЧ-энцефалопатия Гистоплазмоз Изоспориоз Саркома Капоши Лимфома Микобактериоз Пневмоцистоз Бактериальная пневмония Прогрессирующая многоочаговая лейкоэнцефалопатия Сальмонеллез
 * Категории А 3, В 3, С 1, С 2, С 3 являются определяющими для случая СПИД и подлежат в США учету как больные СПИДом Примечание — ГЛАП — генерализованная лимфаденопатия
* Категории А 3, В 3, С 1, С 2, С 3 являются определяющими для случая СПИД и подлежат в США учету как больные СПИДом Примечание — ГЛАП — генерализованная лимфаденопатия
 Последняя классификация вобрала все лучшее, что было накоплено клинической мыслью за десятилетие работы с больными и наиболее адекватно отражает связь патогенеза болезни с клиникой. В категорию А входят бессимптомная ВИЧ-инфекция, острая ВИЧ-инфекция и персистирующая генерализованная лимфаденопатия (ГЛАП) в случаях подтвержденного диагноза лабораторно. Категория В включает все те клинические варианты ВИЧ-инфекции, которые нельзя включить в категории А и С, в классификации В. И. Покровского она соответствует IIIA — стадии болезни, т. е. переходной от ГЛАП к СПИД-ассоциируемому комплексу, не отяжеленному генерализованной инфекцией или опухолевым процессом. Сюда относятся ротоглоточный кандидоз, бациллярный ангиоматоз, диарея или лихорадка длительностью свыше месяца, волосатая лейкоплакия языка, опоясывающий или простой герпес. К категории С подпадают все те случаи, когда хотя бы однократно выявлялось одно из 12 СПИД-индикаторных заболеваний, включенных в официальный перечень.
Последняя классификация вобрала все лучшее, что было накоплено клинической мыслью за десятилетие работы с больными и наиболее адекватно отражает связь патогенеза болезни с клиникой. В категорию А входят бессимптомная ВИЧ-инфекция, острая ВИЧ-инфекция и персистирующая генерализованная лимфаденопатия (ГЛАП) в случаях подтвержденного диагноза лабораторно. Категория В включает все те клинические варианты ВИЧ-инфекции, которые нельзя включить в категории А и С, в классификации В. И. Покровского она соответствует IIIA — стадии болезни, т. е. переходной от ГЛАП к СПИД-ассоциируемому комплексу, не отяжеленному генерализованной инфекцией или опухолевым процессом. Сюда относятся ротоглоточный кандидоз, бациллярный ангиоматоз, диарея или лихорадка длительностью свыше месяца, волосатая лейкоплакия языка, опоясывающий или простой герпес. К категории С подпадают все те случаи, когда хотя бы однократно выявлялось одно из 12 СПИД-индикаторных заболеваний, включенных в официальный перечень.
 Из существующих классификаций нетрудно убедиться, что ВИЧ-инфекция не имеет своего собственного, клинически очерченного статуса, ее клиника в развернутой фазе болезни — это клиника тех, преимущественно оппортунистических инфекций или опухолей, которые наслаиваются на иммунологически дефицитный организм. Поэтому сформировалось понятие “СПИД-ассоциируемые заболевания”, куда входят те наиболее часто развивающиеся инфекционные, паразитарные, грибковые или неопластические процессы, которые чаще всего являются клиническим проявлением ВИЧ индуцированного вторичного иммунодефицита. Разработка клинической классификации позволила с одной стороны унифицировать подходы к клинической оценке болезни, она же определила тот спектр болезней, которые наиболее часто и наиболее характерно отражают манифестную форму ВИЧ-инфекции, представить в едином целом схему фаз течения болезни, классифицировать состояния, наблюдаемые наиболее закономерно (табл. 24).
Из существующих классификаций нетрудно убедиться, что ВИЧ-инфекция не имеет своего собственного, клинически очерченного статуса, ее клиника в развернутой фазе болезни — это клиника тех, преимущественно оппортунистических инфекций или опухолей, которые наслаиваются на иммунологически дефицитный организм. Поэтому сформировалось понятие “СПИД-ассоциируемые заболевания”, куда входят те наиболее часто развивающиеся инфекционные, паразитарные, грибковые или неопластические процессы, которые чаще всего являются клиническим проявлением ВИЧ индуцированного вторичного иммунодефицита. Разработка клинической классификации позволила с одной стороны унифицировать подходы к клинической оценке болезни, она же определила тот спектр болезней, которые наиболее часто и наиболее характерно отражают манифестную форму ВИЧ-инфекции, представить в едином целом схему фаз течения болезни, классифицировать состояния, наблюдаемые наиболее закономерно (табл. 24).
 Таблица 24. Схема фаз течения ВИЧ-инфекции Инкубация, 1 мес — 1 год (до 3 -10 лет) Начальная фаза, 1 мес — 5 лет СПИД, клинически выраженный период до 3 -х лет СПИД- ассоциирова нный комплекс СПИД Нет клиники Симптомы: Генерализованна я лимфаденоп атия Продром Пред-СПИД Лимфаденопатия Потеря массы тела Лихорадка Пневмония Диарея Лейко-лимфо-тром боцитопения Новообразования Множественная инфекция, преимущественно оппортунистическая Поражение ЦНС, психики
Таблица 24. Схема фаз течения ВИЧ-инфекции Инкубация, 1 мес — 1 год (до 3 -10 лет) Начальная фаза, 1 мес — 5 лет СПИД, клинически выраженный период до 3 -х лет СПИД- ассоциирова нный комплекс СПИД Нет клиники Симптомы: Генерализованна я лимфаденоп атия Продром Пред-СПИД Лимфаденопатия Потеря массы тела Лихорадка Пневмония Диарея Лейко-лимфо-тром боцитопения Новообразования Множественная инфекция, преимущественно оппортунистическая Поражение ЦНС, психики
 К Л И Н И К А Инфицированные ВИЧ лица в большинстве случаев в течение длительного времени не имеют каких-либо клинических проявлений болезни, у части инфицированных имеется слабо выраженная клиническая картина и лишь у небольшой части клиника проявляется ВИЧ-зависимыми заболеваниями или СПИДом. Поэтому в начальном периоде эпидемии, в первое десятилетие ее у больных клиника или отсутствует или нпаходится в ранних фазах болезни. Так, в России на конец 2003 г. из 248 тыс. зарегистрированных больных ВИЧ-инфекцией лишь 817 накходятся в стадии СПИДа (рис. 9 и 10).
К Л И Н И К А Инфицированные ВИЧ лица в большинстве случаев в течение длительного времени не имеют каких-либо клинических проявлений болезни, у части инфицированных имеется слабо выраженная клиническая картина и лишь у небольшой части клиника проявляется ВИЧ-зависимыми заболеваниями или СПИДом. Поэтому в начальном периоде эпидемии, в первое десятилетие ее у больных клиника или отсутствует или нпаходится в ранних фазах болезни. Так, в России на конец 2003 г. из 248 тыс. зарегистрированных больных ВИЧ-инфекцией лишь 817 накходятся в стадии СПИДа (рис. 9 и 10).


 Клиническую картину ВИЧ/СПИД определяют в основном группа инфекционных болезней, и в первую очередь ряд оппортунистических инфекций. Описывая клинику ВИЧ-инфекции M. S. Saag (1997) выделяет несколько последовательных фаз и составляющих клинику патологических состояний и нозологических форм. Стадии болезни, основные нозологические формы супенринфекций и органопатологию демонстрирует табл. 25.
Клиническую картину ВИЧ/СПИД определяют в основном группа инфекционных болезней, и в первую очередь ряд оппортунистических инфекций. Описывая клинику ВИЧ-инфекции M. S. Saag (1997) выделяет несколько последовательных фаз и составляющих клинику патологических состояний и нозологических форм. Стадии болезни, основные нозологические формы супенринфекций и органопатологию демонстрирует табл. 25.
 1. Таблица 25. Стадии, СПИД-ассоциированные заболевания и органопатология при ВИЧ-инфекции 1. Стадии болезни — Начальная (синдром острой сероконверсии) — Ранние проявления болезни — Промежуточная стадия — Поздняя — Предтерминальная — Терминальная стадия
1. Таблица 25. Стадии, СПИД-ассоциированные заболевания и органопатология при ВИЧ-инфекции 1. Стадии болезни — Начальная (синдром острой сероконверсии) — Ранние проявления болезни — Промежуточная стадия — Поздняя — Предтерминальная — Терминальная стадия
 2. Основные виды суперинфекции Паразитозы: — Токсоплазмоз — Изоспоридиоз — Криптоспоридиоз — Микроспоридоз — Циклоспороз — Чесотка — Висцеральный лейшманиоз — Стронгилоидоз — Бластомикоз Микозы: — Пневмоцистоз — Кандидоз — Криптококкоз -Гистоплазмоз — Кокцидиоидоз — Аспергиллез Бактериальная инфекция — Туберкулез — Сальмонеллез — Атипический микобактериоз — Бактериальная инфекция респираторного тракта а)стрептококковая пневмония б)Haemophilus influenzae — инфекция в)синегнойная инфекция (Pseudomonas aeroginosa) г)Бартонеллез Герпесвирусная инфекция — HSV-инфекция — CMV-инфекция — HZV-инфекция — EBV-инфекция — HV 6 и HV 7 -инфекция — HV 8 -инфекция Папиллома-вирусная инфекция и вирусный гепатит у больных ВИЧ-инфекцией Эпидемическая саркома Капоши Лимфома и другие злокачественные опухоли
2. Основные виды суперинфекции Паразитозы: — Токсоплазмоз — Изоспоридиоз — Криптоспоридиоз — Микроспоридоз — Циклоспороз — Чесотка — Висцеральный лейшманиоз — Стронгилоидоз — Бластомикоз Микозы: — Пневмоцистоз — Кандидоз — Криптококкоз -Гистоплазмоз — Кокцидиоидоз — Аспергиллез Бактериальная инфекция — Туберкулез — Сальмонеллез — Атипический микобактериоз — Бактериальная инфекция респираторного тракта а)стрептококковая пневмония б)Haemophilus influenzae — инфекция в)синегнойная инфекция (Pseudomonas aeroginosa) г)Бартонеллез Герпесвирусная инфекция — HSV-инфекция — CMV-инфекция — HZV-инфекция — EBV-инфекция — HV 6 и HV 7 -инфекция — HV 8 -инфекция Папиллома-вирусная инфекция и вирусный гепатит у больных ВИЧ-инфекцией Эпидемическая саркома Капоши Лимфома и другие злокачественные опухоли
 3. Органопатология: Поражения центральной и периферической нервной системы Поражение ротовой полости — грибковая инфекция — вирусная инфекция — опухоли Поражение желудочно-кишечного тракта: а) виды поражений — грибковые заболевания — вирусные заболевания — бактериальная инфекция — опухоли б) клинические синдромы — диарея — болезни ано-ректального тракта Неинфекционные органо-специфические заболевания при ВИЧ-инфекции а) болезни кожи — себорея — псориаз — Рейтер-синдром — приобретенный ихтиоз — папулезная и фолликулярная сыпь б)ВИЧ-связанные аутоиммунные и гипериммунные состояния в) эритродермия г) анулярная гранулема
3. Органопатология: Поражения центральной и периферической нервной системы Поражение ротовой полости — грибковая инфекция — вирусная инфекция — опухоли Поражение желудочно-кишечного тракта: а) виды поражений — грибковые заболевания — вирусные заболевания — бактериальная инфекция — опухоли б) клинические синдромы — диарея — болезни ано-ректального тракта Неинфекционные органо-специфические заболевания при ВИЧ-инфекции а) болезни кожи — себорея — псориаз — Рейтер-синдром — приобретенный ихтиоз — папулезная и фолликулярная сыпь б)ВИЧ-связанные аутоиммунные и гипериммунные состояния в) эритродермия г) анулярная гранулема
 Неинфекционные заболевания легких и дыхательных путей: а) опухоли — саркома Капоши — Неходжкинская лимфома — бронхогенная карцинома б) интерстициальная пневмония в) лимфоцитарный бронхиолит г) облитерирующий бронхиолит д) легочная гипертензия Почечные осложнения у больных ВИЧ/СПИД — водно-электролитные нарушения — острая почечная недостаточность — инфекционные поражения мочевыводящих путей и интерстициальный нефрит Гематологические осложнения у больных ВИЧ-инфекцией — специфические цитопении — анемия — нейтропения — тромбоцитопения
Неинфекционные заболевания легких и дыхательных путей: а) опухоли — саркома Капоши — Неходжкинская лимфома — бронхогенная карцинома б) интерстициальная пневмония в) лимфоцитарный бронхиолит г) облитерирующий бронхиолит д) легочная гипертензия Почечные осложнения у больных ВИЧ/СПИД — водно-электролитные нарушения — острая почечная недостаточность — инфекционные поражения мочевыводящих путей и интерстициальный нефрит Гематологические осложнения у больных ВИЧ-инфекцией — специфические цитопении — анемия — нейтропения — тромбоцитопения
 Как видно из данных таблицы 26, ВИЧ-инфекция не имеет своих строго очерченной клинической картины, ибо она представлена рядом СПИД-ассоциируемых и некоторых заболеваний, преимущеcтвенно в виде суперинфекции, вызываемых условно-патогенными возбудителями. Поэтому в связи с развитием пандемии ВИЧ-инфекции значительно выросло число ряда ранее редко встречающихся, заболеваний, таких как пневмоцистная пневмония и саркома Капоши, цитогегаловирувная инфекция и простой герпес, криптококкоз и. атипический микобактериоз. Структура и время появления тех или иных СПИД-ассоциируемых заболеваний в динамике ВИЧ-инфекции в определенной степени зависят от региона (табл. 7).
Как видно из данных таблицы 26, ВИЧ-инфекция не имеет своих строго очерченной клинической картины, ибо она представлена рядом СПИД-ассоциируемых и некоторых заболеваний, преимущеcтвенно в виде суперинфекции, вызываемых условно-патогенными возбудителями. Поэтому в связи с развитием пандемии ВИЧ-инфекции значительно выросло число ряда ранее редко встречающихся, заболеваний, таких как пневмоцистная пневмония и саркома Капоши, цитогегаловирувная инфекция и простой герпес, криптококкоз и. атипический микобактериоз. Структура и время появления тех или иных СПИД-ассоциируемых заболеваний в динамике ВИЧ-инфекции в определенной степени зависят от региона (табл. 7).
 Таблица 26. Профиль и временная последовательность манифестации СПИД-ассоциируемых инфекций в 3 -х регионах мира ( по Лысенко А. Я. и соавт. 1996) Западная Европа, США Южная Америка Африка, Карибская зона Герпетическая инфекция Кандидоз Туберкулез Криптоспоридиоз Туберкулез Токсоплазмоз Изоспориоз Пневмоцистоз Криптоспоридиоз Токсоплазмоз ЦМВ-инфекция Пневмоцистоз ЦМВ-инфекция Атипичные микобактериозы ЦМВ-инфекция Пневмоцистоз
Таблица 26. Профиль и временная последовательность манифестации СПИД-ассоциируемых инфекций в 3 -х регионах мира ( по Лысенко А. Я. и соавт. 1996) Западная Европа, США Южная Америка Африка, Карибская зона Герпетическая инфекция Кандидоз Туберкулез Криптоспоридиоз Туберкулез Токсоплазмоз Изоспориоз Пневмоцистоз Криптоспоридиоз Токсоплазмоз ЦМВ-инфекция Пневмоцистоз ЦМВ-инфекция Атипичные микобактериозы ЦМВ-инфекция Пневмоцистоз
 При всей полиморфности клинической картины ВИЧ-инфекции, характерна определенная, наиболее часто встречающаяся органная патология или нозология: лимфаденопатия (100%), поражение кожи (84%), пневмоцистная пневмония (50%), саркома Капоши (25%), поражение ЦНС (30%). Вместе с тем, за время пандемии в связи с вндрением активной анттиретровирусной терапии и профилактики оппортунистических инфекций прослеживается изменение удельного веса отдельных нозологических форм СПИД-ассоциируемой патологии у больных ВИЧ-инфекцией. Так, в США за период 1981 -1989 гг. частота пневмоцистной пневмонии практически не изменилась, саркома Капоши, встречавшаяся в первые годы пандемии у половины больных, снизилась в 5 раз, с 1986 года начался подъем цитомегаловирусной инфекции, а цитомегаловирусный (CMV) ретинит вырос с 0, 2 до 2, 4%.
При всей полиморфности клинической картины ВИЧ-инфекции, характерна определенная, наиболее часто встречающаяся органная патология или нозология: лимфаденопатия (100%), поражение кожи (84%), пневмоцистная пневмония (50%), саркома Капоши (25%), поражение ЦНС (30%). Вместе с тем, за время пандемии в связи с вндрением активной анттиретровирусной терапии и профилактики оппортунистических инфекций прослеживается изменение удельного веса отдельных нозологических форм СПИД-ассоциируемой патологии у больных ВИЧ-инфекцией. Так, в США за период 1981 -1989 гг. частота пневмоцистной пневмонии практически не изменилась, саркома Капоши, встречавшаяся в первые годы пандемии у половины больных, снизилась в 5 раз, с 1986 года начался подъем цитомегаловирусной инфекции, а цитомегаловирусный (CMV) ретинит вырос с 0, 2 до 2, 4%.
 Синдром острой сероконверсии. Первичная ВИЧ-инфекция (синдром острой сероконверсии, начальная стадия) клинически манифестирует острым ретровирусным синдромом, который традиционно охарактеризован как мононуклеозоподобная болезнь с лихорадкой, фарингитом, лимфаденопатией и сыпью. Позже было установлено, что она имеет ряд других проявлений, включая оппортунистические инфекции. Первичное инфицирование ВИЧ-1 знаменует начало инфекционного процесса, у одних протекающего как асмптомная первичная инфекция, а у других в виде острого ретровирусного синдрома. В дальнейшем у одних больных процесс приобретает характер длительного непрогрессирующего течения, у других быстро развертывается клиника тяжелейшей болезни со смертельным исходом. Первичная ВИЧ-инфекция характеризуется интенсивной вирусной диссеминацией, ВИЧ-специфическим клеточным и гуморальным иммунным ответом и более чем у половины больных характерной клинической картиной – синдромом острой сероконверсии.
Синдром острой сероконверсии. Первичная ВИЧ-инфекция (синдром острой сероконверсии, начальная стадия) клинически манифестирует острым ретровирусным синдромом, который традиционно охарактеризован как мононуклеозоподобная болезнь с лихорадкой, фарингитом, лимфаденопатией и сыпью. Позже было установлено, что она имеет ряд других проявлений, включая оппортунистические инфекции. Первичное инфицирование ВИЧ-1 знаменует начало инфекционного процесса, у одних протекающего как асмптомная первичная инфекция, а у других в виде острого ретровирусного синдрома. В дальнейшем у одних больных процесс приобретает характер длительного непрогрессирующего течения, у других быстро развертывается клиника тяжелейшей болезни со смертельным исходом. Первичная ВИЧ-инфекция характеризуется интенсивной вирусной диссеминацией, ВИЧ-специфическим клеточным и гуморальным иммунным ответом и более чем у половины больных характерной клинической картиной – синдромом острой сероконверсии.
 С тех пор как распозналичие первичной ВИЧ-инфекции, были изучены особенности клинических проявлений, вирусологических, иммунологических и прогностических особенностей синдрома острой сероконверсии, причем выводы обосновывались не только по данным ретроспективого анализа, но и непосредственным наблюдением за больными, выявленными в период первичной ВИЧ-инфекции. Так было установлено, что у больных первичной ВИЧ-инфекцией с клиникой синдрома острой сероконверсии быстрее идет прогрессирование в СПИД. Те больные, у которых в период сероконверсии вывявляется высокая вирусная нагрузка на плазму и низкие показатели CD 4+ лимфоцитов также характеризуются прогрессирующим течением заболевания. Внедрение активной антиретровирусной терапии позволило сформировать идею, что ВИЧ-инфекцию можно перевести в форму хронической вирусной инфекции.
С тех пор как распозналичие первичной ВИЧ-инфекции, были изучены особенности клинических проявлений, вирусологических, иммунологических и прогностических особенностей синдрома острой сероконверсии, причем выводы обосновывались не только по данным ретроспективого анализа, но и непосредственным наблюдением за больными, выявленными в период первичной ВИЧ-инфекции. Так было установлено, что у больных первичной ВИЧ-инфекцией с клиникой синдрома острой сероконверсии быстрее идет прогрессирование в СПИД. Те больные, у которых в период сероконверсии вывявляется высокая вирусная нагрузка на плазму и низкие показатели CD 4+ лимфоцитов также характеризуются прогрессирующим течением заболевания. Внедрение активной антиретровирусной терапии позволило сформировать идею, что ВИЧ-инфекцию можно перевести в форму хронической вирусной инфекции.
 Синдром острой сероконверсии (СОС) по наблюдениям различных авторов развивается у 53 -92% больных. Такой широкий диапозон регистрации частоты СОС обусловлен тем, что используемые для характеристики его подходы весьма варьируют. Более критический подход к оценке клиники в различных группах риска (мужчины-гомосексуалисты, наркоманы, рецепиенты крови и трансплантатов, мдицинские работники, поранившиеся иглой для инъекций, гетеросексуалы), тщательное сопоставление проявлений болезни с контрольной группой серонегативных лиц позволил считать, что СОС имеет место у 34 -53% инфицированных ВИЧ.
Синдром острой сероконверсии (СОС) по наблюдениям различных авторов развивается у 53 -92% больных. Такой широкий диапозон регистрации частоты СОС обусловлен тем, что используемые для характеристики его подходы весьма варьируют. Более критический подход к оценке клиники в различных группах риска (мужчины-гомосексуалисты, наркоманы, рецепиенты крови и трансплантатов, мдицинские работники, поранившиеся иглой для инъекций, гетеросексуалы), тщательное сопоставление проявлений болезни с контрольной группой серонегативных лиц позволил считать, что СОС имеет место у 34 -53% инфицированных ВИЧ.
 Анонимный автор первым в 1984 году в журнале Lancet сообщил о симптомах, ассоциированных с сероконверсией у инфицированных ВИЧ, а D. D. Ho et al. (1985) и D. A. Cooper et al. (1985) описали клинику синдрома острой сероконверсии. Когда Центр поконтролю зха болезнями США (CDC) в 1986 году представил классификацию ВИЧ-инфекции, то острую фазу обознеачил как “мононуклеозиподобный синдром с или без асептического менингита, связанный с сероконверсией на HTLV-III/LAV-антитела” (CDC, 1986). Со временем более тщательное наблюдение за начальной фазой ВИЧ-инфекции позволило заключить. что клинические проявления первичной ВИЧ-инфекции характеризуются многообразием вариантов и могут включать не только реакцию организма на сероконверсию, но и развитием супериринфекции, обусловленной группой условнопатогенных возбудителей. Поэтому понятие “мноноуклеозоподобный синдром” нуждался в расширении и постепенно в практику вошло понятие “синдром острой сероконверсии”. После инфицирования ВИЧ инкубационный период длится примерно 2 -6 недель, после чего у части больных манифестирует клиника первичной инфекции, которую лабораторно позволяет подтвердить в этой фазе методами ИФА или иммунного блота (выявление Ig. G-антител), можно также диагноз уточнить, используя методы выявления специфических Ig. M – антител, р24 -антигена, уровня ВИЧ-1 ДНК и РНК в полимеразной цепной реакции (ПЦР), выделением вируса в культуре клеток. В типичных случаях антитела вывявляются через 1 -2 мес. после инфицирования. Острый синдром сероконверсии обычно длится 1 -6 недель и как правило проходит самостоятельно без специфического лечения.
Анонимный автор первым в 1984 году в журнале Lancet сообщил о симптомах, ассоциированных с сероконверсией у инфицированных ВИЧ, а D. D. Ho et al. (1985) и D. A. Cooper et al. (1985) описали клинику синдрома острой сероконверсии. Когда Центр поконтролю зха болезнями США (CDC) в 1986 году представил классификацию ВИЧ-инфекции, то острую фазу обознеачил как “мононуклеозиподобный синдром с или без асептического менингита, связанный с сероконверсией на HTLV-III/LAV-антитела” (CDC, 1986). Со временем более тщательное наблюдение за начальной фазой ВИЧ-инфекции позволило заключить. что клинические проявления первичной ВИЧ-инфекции характеризуются многообразием вариантов и могут включать не только реакцию организма на сероконверсию, но и развитием супериринфекции, обусловленной группой условнопатогенных возбудителей. Поэтому понятие “мноноуклеозоподобный синдром” нуждался в расширении и постепенно в практику вошло понятие “синдром острой сероконверсии”. После инфицирования ВИЧ инкубационный период длится примерно 2 -6 недель, после чего у части больных манифестирует клиника первичной инфекции, которую лабораторно позволяет подтвердить в этой фазе методами ИФА или иммунного блота (выявление Ig. G-антител), можно также диагноз уточнить, используя методы выявления специфических Ig. M – антител, р24 -антигена, уровня ВИЧ-1 ДНК и РНК в полимеразной цепной реакции (ПЦР), выделением вируса в культуре клеток. В типичных случаях антитела вывявляются через 1 -2 мес. после инфицирования. Острый синдром сероконверсии обычно длится 1 -6 недель и как правило проходит самостоятельно без специфического лечения.
 К наиболее характерным симптомам острой сероконверсии относятся лихорадка, ночной пот, артралгия, недомогание, головная боль, тошнота, рвота, диарея и анорексия, а также фарингит, сыпь, потеря массы тела, лимфаденлопатия, лейкопения, тромбоцитопения, у части больных — менингит, нейропатии и энцефалопатии. Сыпь при СОС выявляется более чем у половины больных и чаще это макулопапулярные высыпания, преимущественно на верхней половине туловища, шее и лице. Она не шелушится и обычно исчезает в течение 2 -3 недель. Реже по характеру сыпь розеолезная или везикулярно-папулезная. Гистологически сыпь идентична высыпаниям, индуцированным другими вирусами или лекарствами. Неврологическая симптоматика СОС включает лимфоцитарный менингит, энцефалопатию. Уже в первые годы наблюдения у больных в стадии СОС описан энцефалит с судорожным синдромом, позже описаны такие неврологические проявления СОС, как синдром Guillain-Barre, неврит плечевого сплетения, ганглионеврит, вызявающий атаксию-нейропати. В период острой сероконверсии клинику могут дополнять суперинфекции, развивающиеся в результате глубокой иммуносупресии, в частности оральный кандидоз и кандидозный эзофагит, пневмоцистная пневмония, цитомегаловирусый колит, церебральный токсоплазмоз и туберкулез. В виде отдельных наблюдений в этой фазе возможно развитие острой пневмококковой пневмонии, лимфоцитарного альвеолита , апластической анемии, васкулита и в виде единичных наблюдений – нефроз, острая почечная недостаточность
К наиболее характерным симптомам острой сероконверсии относятся лихорадка, ночной пот, артралгия, недомогание, головная боль, тошнота, рвота, диарея и анорексия, а также фарингит, сыпь, потеря массы тела, лимфаденлопатия, лейкопения, тромбоцитопения, у части больных — менингит, нейропатии и энцефалопатии. Сыпь при СОС выявляется более чем у половины больных и чаще это макулопапулярные высыпания, преимущественно на верхней половине туловища, шее и лице. Она не шелушится и обычно исчезает в течение 2 -3 недель. Реже по характеру сыпь розеолезная или везикулярно-папулезная. Гистологически сыпь идентична высыпаниям, индуцированным другими вирусами или лекарствами. Неврологическая симптоматика СОС включает лимфоцитарный менингит, энцефалопатию. Уже в первые годы наблюдения у больных в стадии СОС описан энцефалит с судорожным синдромом, позже описаны такие неврологические проявления СОС, как синдром Guillain-Barre, неврит плечевого сплетения, ганглионеврит, вызявающий атаксию-нейропати. В период острой сероконверсии клинику могут дополнять суперинфекции, развивающиеся в результате глубокой иммуносупресии, в частности оральный кандидоз и кандидозный эзофагит, пневмоцистная пневмония, цитомегаловирусый колит, церебральный токсоплазмоз и туберкулез. В виде отдельных наблюдений в этой фазе возможно развитие острой пневмококковой пневмонии, лимфоцитарного альвеолита , апластической анемии, васкулита и в виде единичных наблюдений – нефроз, острая почечная недостаточность
 Kinloch-de Loes et al. (1993) описывая клинику 31 наблюдения за больными в стадии СОС нашли у 43, 3% больных язвы на слизистых ротовой полости или гениталий (очевидно, заразившихся половым путем). Так как в наблюдениях авторов 5 больных ВИЧ-инфекцией наркоманов не имели этих слизисто-кожных изъязвлений, авторы высказывают предположение, что язвы вызваны прямы действием ВИЧ. В пользу этого свидетельствуют данные электронномикроскопического исследования ткани, взятой из эзофагальных язв, проведенного Rabeneck L. et al. (1990) и обнаруживших вирусные частицы в биопрепаратах. M. S. Saag (1997), обобщивший наблюдения многих клиницистов, приводит данные по частоте основных симптомов острого ретровирусного синдрома (табл. 27).
Kinloch-de Loes et al. (1993) описывая клинику 31 наблюдения за больными в стадии СОС нашли у 43, 3% больных язвы на слизистых ротовой полости или гениталий (очевидно, заразившихся половым путем). Так как в наблюдениях авторов 5 больных ВИЧ-инфекцией наркоманов не имели этих слизисто-кожных изъязвлений, авторы высказывают предположение, что язвы вызваны прямы действием ВИЧ. В пользу этого свидетельствуют данные электронномикроскопического исследования ткани, взятой из эзофагальных язв, проведенного Rabeneck L. et al. (1990) и обнаруживших вирусные частицы в биопрепаратах. M. S. Saag (1997), обобщивший наблюдения многих клиницистов, приводит данные по частоте основных симптомов острого ретровирусного синдрома (табл. 27).
 Таблица 27. Симптомы острого ретровирусного синдрома Симптомы Частота, % Лихорадка 57 Фарингит 73 Сыпь 70 Миалгия 58 Артралгия 58 Диарея 33 Головная боль 30 Изменение психического статуса 3 Нарушения чувствительности
Таблица 27. Симптомы острого ретровирусного синдрома Симптомы Частота, % Лихорадка 57 Фарингит 73 Сыпь 70 Миалгия 58 Артралгия 58 Диарея 33 Головная боль 30 Изменение психического статуса 3 Нарушения чувствительности
 При лабораторном обследовании у больных чаще выявляется транзиторная лейкопения, лимфопения, тромбоцитопению, инверсию соотношения хелперы/супрессоры. У части больных повышается активность трансфераз, анализ спинномозговой жидкости выявляет плеоцитоз и повышение уровня белка. Наблюдения большинства авторов показали, что наличие клиники синдрома острой сероконверсии характеризует быстрое прогрессирование болезни с неблагоприятным исходом в ближайшие 2 -3 года. Среди наиболее прогностически неблагоприятных симптомов синдрома острой сероконверсии, ассоциированных с быстирым прогрессированием ВИЧ-инфекции в СПИД различные авторы отмечают лихорадку свыше 38° С, лимфоцитарный менингит, острsй энцефалит, среди последних у 42% СПИД развивался в ближайшие 4 года, а среди не имевших эти проявления СОС – в 18%, у лиц без клиники СОС – в 8% (Boufassa F. et al. , 1995).
При лабораторном обследовании у больных чаще выявляется транзиторная лейкопения, лимфопения, тромбоцитопению, инверсию соотношения хелперы/супрессоры. У части больных повышается активность трансфераз, анализ спинномозговой жидкости выявляет плеоцитоз и повышение уровня белка. Наблюдения большинства авторов показали, что наличие клиники синдрома острой сероконверсии характеризует быстрое прогрессирование болезни с неблагоприятным исходом в ближайшие 2 -3 года. Среди наиболее прогностически неблагоприятных симптомов синдрома острой сероконверсии, ассоциированных с быстирым прогрессированием ВИЧ-инфекции в СПИД различные авторы отмечают лихорадку свыше 38° С, лимфоцитарный менингит, острsй энцефалит, среди последних у 42% СПИД развивался в ближайшие 4 года, а среди не имевших эти проявления СОС – в 18%, у лиц без клиники СОС – в 8% (Boufassa F. et al. , 1995).
 При лабораторном обследовании у больных чаще выявляется транзиторная лейкопения, лимфопения, тромбоцитопению, инверсию соотношения хелперы/супрессоры. У части больных повышается активность трансфераз, анализ спинномозговой жидкости выявляет плеоцитоз и повышение уровня белка. Наблюдения большинства авторов показали, что наличие клиники синдрома острой сероконверсии характеризует быстрое прогрессирование болезни с неблагоприятным исходом в ближайшие 2 -3 года. Среди наиболее прогностически неблагоприятных симптомов синдрома острой сероконверсии, ассоциированных с быстирым прогрессированием ВИЧ-инфекции в СПИД различные авторы отмечают лихорадку свыше 38° С, лимфоцитарный менингит, острsй энцефалит, среди последних у 42% СПИД развивался в ближайшие 4 года, а среди не имевших эти проявления СОС – в 18%, у лиц без клиники СОС – в 8% (Boufassa F. et al. , 1995).
При лабораторном обследовании у больных чаще выявляется транзиторная лейкопения, лимфопения, тромбоцитопению, инверсию соотношения хелперы/супрессоры. У части больных повышается активность трансфераз, анализ спинномозговой жидкости выявляет плеоцитоз и повышение уровня белка. Наблюдения большинства авторов показали, что наличие клиники синдрома острой сероконверсии характеризует быстрое прогрессирование болезни с неблагоприятным исходом в ближайшие 2 -3 года. Среди наиболее прогностически неблагоприятных симптомов синдрома острой сероконверсии, ассоциированных с быстирым прогрессированием ВИЧ-инфекции в СПИД различные авторы отмечают лихорадку свыше 38° С, лимфоцитарный менингит, острsй энцефалит, среди последних у 42% СПИД развивался в ближайшие 4 года, а среди не имевших эти проявления СОС – в 18%, у лиц без клиники СОС – в 8% (Boufassa F. et al. , 1995).
 Характерно для ВИЧ-инфекции, что чем старше возраст к коменту сероконверсии, тем быстрее болезнь прогрессирует в СПИД. Так, при оценке влияния пола, возраста и способа инфицирования на скорость прогрессирования ВИЧ-инфекции G. Rezza et al. (1992) в течение 7 лет наблюдали 780 больных. Авторы показали, что возраст свыше 25 лет к моменту сероконверсии был единственным фактором, влияющим на скорость прогрессирования болезни. Та же закономерность наблюдалась у больных ВИЧ-инфекцией больных гемофилией, гомосексуалов, бисексуалов и гетеросексуалов, во всех этих группах фактор возраста был единственным показателем риска в момент сероконверсии для быстрого прогрессирования болезни. В то же время установлено, что риск манифестации клиники СОС более высок у гомосексуалов по сравнению с гетеросексуалами и у гомосексуалов по сравнению с гемофиликами. СОС чаще наблюдалась у лиц, заразившихся половым путем по сравнению с людьми, заразившимися гематогенно.
Характерно для ВИЧ-инфекции, что чем старше возраст к коменту сероконверсии, тем быстрее болезнь прогрессирует в СПИД. Так, при оценке влияния пола, возраста и способа инфицирования на скорость прогрессирования ВИЧ-инфекции G. Rezza et al. (1992) в течение 7 лет наблюдали 780 больных. Авторы показали, что возраст свыше 25 лет к моменту сероконверсии был единственным фактором, влияющим на скорость прогрессирования болезни. Та же закономерность наблюдалась у больных ВИЧ-инфекцией больных гемофилией, гомосексуалов, бисексуалов и гетеросексуалов, во всех этих группах фактор возраста был единственным показателем риска в момент сероконверсии для быстрого прогрессирования болезни. В то же время установлено, что риск манифестации клиники СОС более высок у гомосексуалов по сравнению с гетеросексуалами и у гомосексуалов по сравнению с гемофиликами. СОС чаще наблюдалась у лиц, заразившихся половым путем по сравнению с людьми, заразившимися гематогенно.
 В период клинических проявлений СОС Ig. M к ВИЧ обнаруживаются методами иммунофлюоресценции в течение первых 5 суток и Ig. G – в течение 11 суток, а антитела в ИФА и иммунном блоте на 20 дней позже. Пик Ig. M приходится на 3 -5 неделю, затем уровень антител снижается к 2 -3 месяцу. В течение первых 2 недель после начала СОС с помощью ИФА выявляются антиген р24, а р24 -антитела могут быть обнаружены в иммунном блоте в период 2 -3 недели, т. е. по мере снижения уровня антигена. D. A. Cooper et al. (1993) выделили 4 фазы изменения клеточного иммунитета при ВИЧ-инфекции в стадии СОС: 1 -я – снижение общего числа лимфоцитов, 2 -я – инверсия соотношения CD 4/CD 8, связанная с повышением числа CED 8+ клеток, 3 -я – максимальное повышение уровня CD 8+ клеток с максимальным пиком к 33 дню, 4 -я – снижение числа CD 4+ и CD 8+ клеток с сохранением показателя CD 4/CD 8.
В период клинических проявлений СОС Ig. M к ВИЧ обнаруживаются методами иммунофлюоресценции в течение первых 5 суток и Ig. G – в течение 11 суток, а антитела в ИФА и иммунном блоте на 20 дней позже. Пик Ig. M приходится на 3 -5 неделю, затем уровень антител снижается к 2 -3 месяцу. В течение первых 2 недель после начала СОС с помощью ИФА выявляются антиген р24, а р24 -антитела могут быть обнаружены в иммунном блоте в период 2 -3 недели, т. е. по мере снижения уровня антигена. D. A. Cooper et al. (1993) выделили 4 фазы изменения клеточного иммунитета при ВИЧ-инфекции в стадии СОС: 1 -я – снижение общего числа лимфоцитов, 2 -я – инверсия соотношения CD 4/CD 8, связанная с повышением числа CED 8+ клеток, 3 -я – максимальное повышение уровня CD 8+ клеток с максимальным пиком к 33 дню, 4 -я – снижение числа CD 4+ и CD 8+ клеток с сохранением показателя CD 4/CD 8.
 Во время сероконверсии высокий антительный ответ на р24 сочетается с более низкой скоростью прогрессирования болезни. Бессимптомное течение сероконверсии характеризуется высоким уровнем анти-ВИЧ-1 антител и низким показателем уровня РНК-ВИЧ-1, что свидетельствует о контроле иммунной системой степени виремии. Более высокие уровни ВИЧ-специфических цитотоксических Т-клеток сочетается с низким уровнем вирусной нагрузки на плазму и более медленным прогрессированием болезни. Более того, при медленно прогрессирующем варианте ВИЧ-инфекции несмотря на отсутствие антивирусной терапии характерно повышение пролиферации ВИЧ-1 -специфических СD 4+ клеток, а лимфоцит-пролиферативный ответ на антиген р24 характеризуется обратной зависимостью от вирусной нагрузки.
Во время сероконверсии высокий антительный ответ на р24 сочетается с более низкой скоростью прогрессирования болезни. Бессимптомное течение сероконверсии характеризуется высоким уровнем анти-ВИЧ-1 антител и низким показателем уровня РНК-ВИЧ-1, что свидетельствует о контроле иммунной системой степени виремии. Более высокие уровни ВИЧ-специфических цитотоксических Т-клеток сочетается с низким уровнем вирусной нагрузки на плазму и более медленным прогрессированием болезни. Более того, при медленно прогрессирующем варианте ВИЧ-инфекции несмотря на отсутствие антивирусной терапии характерно повышение пролиферации ВИЧ-1 -специфических СD 4+ клеток, а лимфоцит-пролиферативный ответ на антиген р24 характеризуется обратной зависимостью от вирусной нагрузки.
 Вирусологический статус в период сероконверсии весьма варьирует. Во время острого СОС вирусная нагрузка на плазму часто довольно высокая, уровень ее выше 200 000 копий/мл и коррелирует с уровнем выявляемых у больных клинических проявлений болезни. С появлением ВИЧ-специфических антител уровень вирусной нагрузки падает и одновременно исчезает клинические проявления СОС. J. Mellors (1995) при обследовании 62 мужчин-гомосексуалистов с клиникой СОС выявил, что при уровне РНК ВИЧ-1 в плазме выше 100 000 копий/мл имеет место более высокий темп прогрессирования болезни в СПИД вне зависимости от уровня CD 4+ лимфоцитов в этот период. T. W. Schacker et al. (1998) также установили, что высокий уровень вирусной нагрузки на плазму между 120 -365 днями после заражения ВИЧ коррелирует с ускоренным снижением CD 4+ клеток, в то время как высокий уровень копий РНК до 120 дня – не коррелирует.
Вирусологический статус в период сероконверсии весьма варьирует. Во время острого СОС вирусная нагрузка на плазму часто довольно высокая, уровень ее выше 200 000 копий/мл и коррелирует с уровнем выявляемых у больных клинических проявлений болезни. С появлением ВИЧ-специфических антител уровень вирусной нагрузки падает и одновременно исчезает клинические проявления СОС. J. Mellors (1995) при обследовании 62 мужчин-гомосексуалистов с клиникой СОС выявил, что при уровне РНК ВИЧ-1 в плазме выше 100 000 копий/мл имеет место более высокий темп прогрессирования болезни в СПИД вне зависимости от уровня CD 4+ лимфоцитов в этот период. T. W. Schacker et al. (1998) также установили, что высокий уровень вирусной нагрузки на плазму между 120 -365 днями после заражения ВИЧ коррелирует с ускоренным снижением CD 4+ клеток, в то время как высокий уровень копий РНК до 120 дня – не коррелирует.
 В период клинически выраженной острой сероконверсии ВИЧ выделяется из плазмы, мононуклеаров периферической крови, спинномозговой жидкости. Очевидно, часть клинических проявлений СОС индуцирована непосредственно ВИЧ, что также зависит от дозы инфекта, вирулентности штамма, его тропизма и лекарственной устойчивости. Так, у реципиентов, получивших ВИЧ-инфицированную кровь от доноров, у которых развился СПИД вскоре после донорства, быстрее развивалась клиника СОС и заболевание в целом быстрее прогрессировало в СПИД. Синцитий-образующие и быстро реплицирующие штаммы определяют более форсированную клинику, у больных слабо выражен начальный иммунный отвеет. C. Nielsen et al. (1993) наблюдали, что у больных в стадии острой сероконверсии, у которых выделены синцитий-образующие щтаммы, имели более длительный лихорадочный период и быстрее развивался иммунодефицит. T. Lee et al. (1994) полагают, что установившаяся концентрация вируса во время сероконверсии в последующем меняется очень мало и коррелирует с течением болезни.
В период клинически выраженной острой сероконверсии ВИЧ выделяется из плазмы, мононуклеаров периферической крови, спинномозговой жидкости. Очевидно, часть клинических проявлений СОС индуцирована непосредственно ВИЧ, что также зависит от дозы инфекта, вирулентности штамма, его тропизма и лекарственной устойчивости. Так, у реципиентов, получивших ВИЧ-инфицированную кровь от доноров, у которых развился СПИД вскоре после донорства, быстрее развивалась клиника СОС и заболевание в целом быстрее прогрессировало в СПИД. Синцитий-образующие и быстро реплицирующие штаммы определяют более форсированную клинику, у больных слабо выражен начальный иммунный отвеет. C. Nielsen et al. (1993) наблюдали, что у больных в стадии острой сероконверсии, у которых выделены синцитий-образующие щтаммы, имели более длительный лихорадочный период и быстрее развивался иммунодефицит. T. Lee et al. (1994) полагают, что установившаяся концентрация вируса во время сероконверсии в последующем меняется очень мало и коррелирует с течением болезни.
 Не однозначен вопрос терапевтической тактики у больных с синдромом острой сероконверсии. Так как высокие уровни виремии в стадии синдрома острой сероконверсии являются предвестниками прогессирующего течения ВИЧ-инфекции, теоретически вроде бы выгодно проводить антиретровирусную терапию в этот период. Однако, N. D. Russell et al. (1998) полагают, что есть аргументы и против использования интенсивной антиретровирусной терапирпии в этой фазе болезни:
Не однозначен вопрос терапевтической тактики у больных с синдромом острой сероконверсии. Так как высокие уровни виремии в стадии синдрома острой сероконверсии являются предвестниками прогессирующего течения ВИЧ-инфекции, теоретически вроде бы выгодно проводить антиретровирусную терапию в этот период. Однако, N. D. Russell et al. (1998) полагают, что есть аргументы и против использования интенсивной антиретровирусной терапирпии в этой фазе болезни:
 • назначение терапии в период формирования организмом первичного иммунного ответа против ВИЧ может привести к угнетению ВИЧ-специфического цитотоксического иммунного ответа; • лечение одновременно несколькими антиретровирусными препаратами во время периода быстрой вирусной репликации может привести к селекции штаммов с множественной лекарственной устойчивостью и в конечном счете резко снизит эффективность будующей антиретровирусной терапии; • побочные токсические эффекты медикаментов могут привести к снижению качества жизни больного в то время, когда у него могут полностью отсутствовать симптомы инфекции (после короткого острого ретровирусного синдрома); • необходимая продолжительностьт лечения неизвестна, но может продлиться более 10 лет, создавая возможность длительных по продолжительности побочных эффектов
• назначение терапии в период формирования организмом первичного иммунного ответа против ВИЧ может привести к угнетению ВИЧ-специфического цитотоксического иммунного ответа; • лечение одновременно несколькими антиретровирусными препаратами во время периода быстрой вирусной репликации может привести к селекции штаммов с множественной лекарственной устойчивостью и в конечном счете резко снизит эффективность будующей антиретровирусной терапии; • побочные токсические эффекты медикаментов могут привести к снижению качества жизни больного в то время, когда у него могут полностью отсутствовать симптомы инфекции (после короткого острого ретровирусного синдрома); • необходимая продолжительностьт лечения неизвестна, но может продлиться более 10 лет, создавая возможность длительных по продолжительности побочных эффектов
 Ранняя стадия болезни. Раннюю фазу ВИЧ-инфекции характеризует содержание CD 4+ клеток свыше 500 в 1 мм 3. Среди клинических проявлений болезни наиболее характерна лимфаденопатия. Выявляются увеличенные затылочные, заднешейные, аксилярные, надключичные, кубитальные лимфоузлы, которые в норме не пальпируются. Увеличиваются периаортальные и медиастинальные лимфатические узлы. Значительное увеличение группы торакальных или абдоминальных лимфоузлов обычно свидетельствует о присоединении оппортунистической инфекции, распространенном туберкулезе, атипическом микобактериозе, гистоплазмозе или лимфоме. Таблица 28 демонстрирует наиболее типичные причины лимфаденопати у человека.
Ранняя стадия болезни. Раннюю фазу ВИЧ-инфекции характеризует содержание CD 4+ клеток свыше 500 в 1 мм 3. Среди клинических проявлений болезни наиболее характерна лимфаденопатия. Выявляются увеличенные затылочные, заднешейные, аксилярные, надключичные, кубитальные лимфоузлы, которые в норме не пальпируются. Увеличиваются периаортальные и медиастинальные лимфатические узлы. Значительное увеличение группы торакальных или абдоминальных лимфоузлов обычно свидетельствует о присоединении оппортунистической инфекции, распространенном туберкулезе, атипическом микобактериозе, гистоплазмозе или лимфоме. Таблица 28 демонстрирует наиболее типичные причины лимфаденопати у человека.
 Таблица 28. Типичные причины генерализованной лимфаденопатии Заболевание Тесты Инфекции Бактериальные сифилис серология бруцеллез серология Вирусные инфекционный мононуклеоз серология, ПЦР ЦМВ-инфекция серология, ПЦР краснуха серология ВИЧ-инфекция серология, ПЦР Протозойные токсоплазмоз серология Опухоли лейкоз гемограмма, миелограмма лимфомы биопсия лимфоузлов Прочие саркоидоз клиника
Таблица 28. Типичные причины генерализованной лимфаденопатии Заболевание Тесты Инфекции Бактериальные сифилис серология бруцеллез серология Вирусные инфекционный мононуклеоз серология, ПЦР ЦМВ-инфекция серология, ПЦР краснуха серология ВИЧ-инфекция серология, ПЦР Протозойные токсоплазмоз серология Опухоли лейкоз гемограмма, миелограмма лимфомы биопсия лимфоузлов Прочие саркоидоз клиника
 Дерматологические проявления болезни в этот период довольно характерны и чаще проявляются в виде себореи, псориаза, ихтиоза, эозинофильного фолликулита, распространенной чесотки. Оральная патология протекает в виде афтозного стоматита, но встречается редко — у 2 -5% больных. Хотя поражения, вызванные вирусом простого герпеса (HSV) свойственны более поздним стадиям болезни, иногда появляются и в ранней фазе. Весьма характернадля оральных поражений Эпштейна-Барр (EBV)-инфекция в виде лейкоплакии, для которой характерно появление белых полос по краям языка, ее приходится дифференцировать с кандидозом полости рта. Лейкоплакия не часто встречается в ранней фазе ВИЧ-1 инфекции, ибо она редка при количестве CD 4+ клеток > 500 в 1 мм 3 и ее появление свидетельствует о прогрессирующем течении болезни. Возможность продукции в ранней фазе вирионов в количествах от 100 млн. до 1 биллиона определяет необходимость проведения противоретровирусной терапии, ибо отсутствие терапии ведет к быстрому падению уровня CD 4+ клеток.
Дерматологические проявления болезни в этот период довольно характерны и чаще проявляются в виде себореи, псориаза, ихтиоза, эозинофильного фолликулита, распространенной чесотки. Оральная патология протекает в виде афтозного стоматита, но встречается редко — у 2 -5% больных. Хотя поражения, вызванные вирусом простого герпеса (HSV) свойственны более поздним стадиям болезни, иногда появляются и в ранней фазе. Весьма характернадля оральных поражений Эпштейна-Барр (EBV)-инфекция в виде лейкоплакии, для которой характерно появление белых полос по краям языка, ее приходится дифференцировать с кандидозом полости рта. Лейкоплакия не часто встречается в ранней фазе ВИЧ-1 инфекции, ибо она редка при количестве CD 4+ клеток > 500 в 1 мм 3 и ее появление свидетельствует о прогрессирующем течении болезни. Возможность продукции в ранней фазе вирионов в количествах от 100 млн. до 1 биллиона определяет необходимость проведения противоретровирусной терапии, ибо отсутствие терапии ведет к быстрому падению уровня CD 4+ клеток.
 Промежуточная стадия . Для промежуточной стадии ВИЧ-инфекции характерно снижение уровня CD 4+ клеток в пределах 200 -500 в 1 мм 3. В отличии от ранней стадии в этой фазе болезни выше риск развития оппортунистической патологии, хотя часто заболевание протекает в субклинической или слабо выраженной клинически форме. У больных при наличии кожных и оральных патологических процессов они прогрессируют дальше или же появляются впервые. Чаще всего выявляется HSV-инфекция, опоясывающий герпес (HZV-инфекция), диарея, периодические подъемы температуры тела, немотивированное снижение массы тела, умеренно выраженный оральный или вагинальный кандидоз. Довольно часто наблюдаются миалгия, артралгия, головная боль и усталость. Изредка наблюдается прогрессирующее поражение почек в виде почечной недостаточности с высокой протеинурией. Поражения респираторного тракта протекают по типу бронхита или пневмонии и обычно обусловлены стрептококком, микоплазмой pneumoniae, H. influenzae, Moraxella catarrhalis. Антиретровирусная терапия, классическим показанием к применению которой является снижение уровня CD 4+ клеток < 500 в 1 мм 3, в этой стадии проводится в США зальцитабином, диданозином и др. Без ретровирусной терапии заболевание в 20 -30% прогрессирует в СПИД.
Промежуточная стадия . Для промежуточной стадии ВИЧ-инфекции характерно снижение уровня CD 4+ клеток в пределах 200 -500 в 1 мм 3. В отличии от ранней стадии в этой фазе болезни выше риск развития оппортунистической патологии, хотя часто заболевание протекает в субклинической или слабо выраженной клинически форме. У больных при наличии кожных и оральных патологических процессов они прогрессируют дальше или же появляются впервые. Чаще всего выявляется HSV-инфекция, опоясывающий герпес (HZV-инфекция), диарея, периодические подъемы температуры тела, немотивированное снижение массы тела, умеренно выраженный оральный или вагинальный кандидоз. Довольно часто наблюдаются миалгия, артралгия, головная боль и усталость. Изредка наблюдается прогрессирующее поражение почек в виде почечной недостаточности с высокой протеинурией. Поражения респираторного тракта протекают по типу бронхита или пневмонии и обычно обусловлены стрептококком, микоплазмой pneumoniae, H. influenzae, Moraxella catarrhalis. Антиретровирусная терапия, классическим показанием к применению которой является снижение уровня CD 4+ клеток < 500 в 1 мм 3, в этой стадии проводится в США зальцитабином, диданозином и др. Без ретровирусной терапии заболевание в 20 -30% прогрессирует в СПИД.
 Поздняя стадия болезни. Для этой фазы ВИЧ-инфекции характерно снижение CD 4+ клеток в пределах 50 -200 в 1 мм 3. Согласно CDC классификации при этом количестве CD 4+ лимфоцитов заболевание следует расценивать, как стадию СПИД. В клинике доминирует оппортунистическая инфекция в виде пневмоцистной пневмонии, токсоплазмоза, криптоспоридиоза, изоспориоза, туберкулеза, а также В-клеточной лимфомы, саркомы Капоши, энцефалита, кандидозного эзофагита. Эти виды патологии сопровождаются миалгией, артралгией, высокой лихорадкой. Развивается неврологическая патология в виде мононевритов, поражения черепно-мозговых нервов и периферических нервов, миелопатии. Цитомегаловирусная патология характерна для этой фазы, но в виде ЦMВ-ретинита, она развивается в основном при снижении СD 4+ клеток менее 50 в 1 мм 3. Возможно развитие рака шейки матки и прямой кишки, вызванные папиллома-вирусом. Изменения функции гормональной системы у женщин проявляются гипогонадизмом, нарушением менструального цикла. У больных возможны развитие гипо- или гипертиреоидизма и, как следствие поражения оппортунистической инфекцией надпочечников, развивается надпочечниковая недостаточность. Гематологические изменения характеризуются анемией, нейтропенией, идиопатической тромбоцитопенией. У больных постепенно снижается уровень общего белка, повышается уровень сывороточных глобулинов, особенно g -глобулиновой фракции.
Поздняя стадия болезни. Для этой фазы ВИЧ-инфекции характерно снижение CD 4+ клеток в пределах 50 -200 в 1 мм 3. Согласно CDC классификации при этом количестве CD 4+ лимфоцитов заболевание следует расценивать, как стадию СПИД. В клинике доминирует оппортунистическая инфекция в виде пневмоцистной пневмонии, токсоплазмоза, криптоспоридиоза, изоспориоза, туберкулеза, а также В-клеточной лимфомы, саркомы Капоши, энцефалита, кандидозного эзофагита. Эти виды патологии сопровождаются миалгией, артралгией, высокой лихорадкой. Развивается неврологическая патология в виде мононевритов, поражения черепно-мозговых нервов и периферических нервов, миелопатии. Цитомегаловирусная патология характерна для этой фазы, но в виде ЦMВ-ретинита, она развивается в основном при снижении СD 4+ клеток менее 50 в 1 мм 3. Возможно развитие рака шейки матки и прямой кишки, вызванные папиллома-вирусом. Изменения функции гормональной системы у женщин проявляются гипогонадизмом, нарушением менструального цикла. У больных возможны развитие гипо- или гипертиреоидизма и, как следствие поражения оппортунистической инфекцией надпочечников, развивается надпочечниковая недостаточность. Гематологические изменения характеризуются анемией, нейтропенией, идиопатической тромбоцитопенией. У больных постепенно снижается уровень общего белка, повышается уровень сывороточных глобулинов, особенно g -глобулиновой фракции.
 Предтерминальная стадия болезни. В этой стадии болезни характерно снижение CD 4+ клеток ниже 50 в 1 мм 3. Глубокий иммунодефицит обусловливает тяжело протекающую оппортунистическую инфекцию в виде атипического микобактериоза, криптококкового менингита, ЦMВ-ретинита, распространенного аспергиллеза, прогрессирующего мультиформного лейкоэнцефалита, диссеминированного гистоплазмоза, кокцидиомикоза, бартонеллеза. Совокупность патологии нивилирует клиническую индивидуальность каждой формы инфекции, приводит к быстрому истощению организма. Поражение вещества мозга полиома-вирусом ведет к нарушению двигательной функции и изменению психики в виде деменции. В этой фазе выражена немотивированная потеря массы тела, что в определенной степени зависит от потери больным аппетита, развития малабсорбции, обусловливающих диарею. Проведение противовирусной терапии снижает риск развития у больных атипического микобактериоза, криптококкоза, CMV- ретинита. Антивирусная терапия и проведение медикаментозной профилактики оппортунистической инфекции существенно продляет жизнь больным.
Предтерминальная стадия болезни. В этой стадии болезни характерно снижение CD 4+ клеток ниже 50 в 1 мм 3. Глубокий иммунодефицит обусловливает тяжело протекающую оппортунистическую инфекцию в виде атипического микобактериоза, криптококкового менингита, ЦMВ-ретинита, распространенного аспергиллеза, прогрессирующего мультиформного лейкоэнцефалита, диссеминированного гистоплазмоза, кокцидиомикоза, бартонеллеза. Совокупность патологии нивилирует клиническую индивидуальность каждой формы инфекции, приводит к быстрому истощению организма. Поражение вещества мозга полиома-вирусом ведет к нарушению двигательной функции и изменению психики в виде деменции. В этой фазе выражена немотивированная потеря массы тела, что в определенной степени зависит от потери больным аппетита, развития малабсорбции, обусловливающих диарею. Проведение противовирусной терапии снижает риск развития у больных атипического микобактериоза, криптококкоза, CMV- ретинита. Антивирусная терапия и проведение медикаментозной профилактики оппортунистической инфекции существенно продляет жизнь больным.
 Терминальная стадия болезни. Клинически трудно определить, когда заболевание из развитой стадии переходит терминальную. Логически под терминальной стадией понимается состояние неуправляемости течения болезни, невозможности остановить прогрессирующее течение патологического процесса с ближайшим неблагоприятным исходом. Больной в терминальной стадии перестает бороться с болезнью, теряет веру в выздоровление. Как в целом клиника ВИЧ-инфекции, так и патология терминальной стадии четко коррелируют с выраженностью падения уровня CD 4+клеток (рис. 3). Поэтому непосредственной причиной смерти чаще всего служат оппортунистические инфекции и саркома Капоши, а у больных ВИЧ/СПИД наркоманов еще и туберкулез.
Терминальная стадия болезни. Клинически трудно определить, когда заболевание из развитой стадии переходит терминальную. Логически под терминальной стадией понимается состояние неуправляемости течения болезни, невозможности остановить прогрессирующее течение патологического процесса с ближайшим неблагоприятным исходом. Больной в терминальной стадии перестает бороться с болезнью, теряет веру в выздоровление. Как в целом клиника ВИЧ-инфекции, так и патология терминальной стадии четко коррелируют с выраженностью падения уровня CD 4+клеток (рис. 3). Поэтому непосредственной причиной смерти чаще всего служат оппортунистические инфекции и саркома Капоши, а у больных ВИЧ/СПИД наркоманов еще и туберкулез.
 Прогноз. В среднем от начала инфицирования до терминальной стадии ВИЧ-инфекция, нося перемежающий характер, длится 10 -15 лет и четко коррелирует с уровнем виремии. Но в одних случаях заболевание трансформируется в СПИД в течение месяцев, в других — многих лет. Можно выделить 3 типа течения болезни: типичное прогрессирование, быстрое прогрессирование и отсутствие прогрессирования. Наблюдения за больными позволили выделить ряд факторов риска прогрессирования болезни. Так, среди лиц, заразившихся вследствие переливания крови прогрессирование выше, чем среди гомосексуалистов. По данным М. Melbye et al. (1987) у лиц с лимфаденопатией прогрессирование в СПИД в ближайшие 2 года было в 22%, при наличии в клинике лейкоплакии — в 42%, а у больных с органическими поражениями — в 100%.
Прогноз. В среднем от начала инфицирования до терминальной стадии ВИЧ-инфекция, нося перемежающий характер, длится 10 -15 лет и четко коррелирует с уровнем виремии. Но в одних случаях заболевание трансформируется в СПИД в течение месяцев, в других — многих лет. Можно выделить 3 типа течения болезни: типичное прогрессирование, быстрое прогрессирование и отсутствие прогрессирования. Наблюдения за больными позволили выделить ряд факторов риска прогрессирования болезни. Так, среди лиц, заразившихся вследствие переливания крови прогрессирование выше, чем среди гомосексуалистов. По данным М. Melbye et al. (1987) у лиц с лимфаденопатией прогрессирование в СПИД в ближайшие 2 года было в 22%, при наличии в клинике лейкоплакии — в 42%, а у больных с органическими поражениями — в 100%.
 Среди возможных лабораторных тестов прогнозирования ВИЧ-инфекции определение уровня CD 4+ лимфоцитов относится к наиболее распространенным и доступным показателям. Так, было установлено, что снижение уровня CD 4+ клеток до 7% в течение первого года наблюдения в СПИД болезнь переходит в 35 раз чаще, чем среди больных, имевших стабильный уровень этих клеток (Burcham J. et al. , 1991). Именно поэтому в клиниках внедрена система обследования больных на уровень CD 4+ лимфоцитов в крови через каждые 3 -4 месяца. Выраженное их снижение является показанием к проведению противовирусной терапии и профилактике пневмоцистной пневмонии и других оппортунистических инфекций. В последние годы внедрение методов определения вирусной нагрузки на плазму методами количественной полимеразной цепной реакции, определения РНК ВИЧ-1 или b. ДНК позволило в более ранние сроки установить начало прогрессирования болезни и своевременно проводить противовирусную терапию.
Среди возможных лабораторных тестов прогнозирования ВИЧ-инфекции определение уровня CD 4+ лимфоцитов относится к наиболее распространенным и доступным показателям. Так, было установлено, что снижение уровня CD 4+ клеток до 7% в течение первого года наблюдения в СПИД болезнь переходит в 35 раз чаще, чем среди больных, имевших стабильный уровень этих клеток (Burcham J. et al. , 1991). Именно поэтому в клиниках внедрена система обследования больных на уровень CD 4+ лимфоцитов в крови через каждые 3 -4 месяца. Выраженное их снижение является показанием к проведению противовирусной терапии и профилактике пневмоцистной пневмонии и других оппортунистических инфекций. В последние годы внедрение методов определения вирусной нагрузки на плазму методами количественной полимеразной цепной реакции, определения РНК ВИЧ-1 или b. ДНК позволило в более ранние сроки установить начало прогрессирования болезни и своевременно проводить противовирусную терапию.
 ОРГАНОПАТОЛОГИЯ ПРИ ВИЧ-ИНФЕКЦИИ К основным клиническим проявлениям ВИЧ/СПИД относятся поражения кожи, нервной системы, желудочно-кишечного тракта, диссеминированные варианты суперинфекции и онкопатология. Среди возбудителей суперинфекций чаще заболевания обусловливают условно-патогенные микроорганизмы, в том числе длительно персистирующие в организме человека, не вызывая патологических процессов в условиях нормального функционирования иммунной системы, а при СПИДе приобретающие злокачественное, рецидивирующее течение (табл. 29).
ОРГАНОПАТОЛОГИЯ ПРИ ВИЧ-ИНФЕКЦИИ К основным клиническим проявлениям ВИЧ/СПИД относятся поражения кожи, нервной системы, желудочно-кишечного тракта, диссеминированные варианты суперинфекции и онкопатология. Среди возбудителей суперинфекций чаще заболевания обусловливают условно-патогенные микроорганизмы, в том числе длительно персистирующие в организме человека, не вызывая патологических процессов в условиях нормального функционирования иммунной системы, а при СПИДе приобретающие злокачественное, рецидивирующее течение (табл. 29).
 Таблица 29. Основные виды патогенов, вызывающие органопатологию у больных ВИЧ-инфекцией Простейшие Вирусы Грибы Бактерии Кнриптоспориди и CMV P. carinii Атипические микобактерии Токсоплазмы HSV Candida М. туберкулеза Изоспоридии HZV Нокардии Сальмонеллы Лямблии EBV Кокцидии Легионеллы Паповавиру с Криптококки Haemophilus
Таблица 29. Основные виды патогенов, вызывающие органопатологию у больных ВИЧ-инфекцией Простейшие Вирусы Грибы Бактерии Кнриптоспориди и CMV P. carinii Атипические микобактерии Токсоплазмы HSV Candida М. туберкулеза Изоспоридии HZV Нокардии Сальмонеллы Лямблии EBV Кокцидии Легионеллы Паповавиру с Криптококки Haemophilus
 Поражение нервной системы Нервная система постоянно вовлекается в патологический процесс при ВИЧ-инфекции, поражение вещества мозга варьирует от незначительных изменений до тяжелых прогрессирующих, но в 30% клинические проявления патологии центральной нервной системы выражены ярко. Чаще всего оппортунистическая инфекция определяет локальный или диффузный патологический процесс: криптококки, токсоплазмы, Candida, CMV, очаговое поражение бывает обусловлено лимфомой. Наиболее характерен ряд симптомокомплексов: менингизм, энцефалит, менингит, гемипарезы, мозжечковая атаксия, судорожный синдром, СПИД-дементный комплекс. Неврологические проявления поражения головного мозга проявляются в одних случаях преимущественным вовлечением в процесс головного мозга, в других — спинного мозга, в третьих — оболочек, а в четвертых — периферических нервов и корешков (табл. 30). В каждом конкретном случае клиника характеризуется свойственной данному виду патологии симптомами. Так, для вакуолярной миелопатии характерны парастезии и слабость в ногах, а при оценке неврологического статуса выявляются парапарез, мышечная спастичность, атаксия. Периферическая невропатия характеризуется парастезиями, слабостью и дистальной атрофией. Клинике СПИД-деменции свойственны ранние и поздние проявления (табл. 31). Больных обычно беспокоит головная боль, тревога с депрессией, нарушение равновесия, снижение остроты зрения, нарушение памяти.
Поражение нервной системы Нервная система постоянно вовлекается в патологический процесс при ВИЧ-инфекции, поражение вещества мозга варьирует от незначительных изменений до тяжелых прогрессирующих, но в 30% клинические проявления патологии центральной нервной системы выражены ярко. Чаще всего оппортунистическая инфекция определяет локальный или диффузный патологический процесс: криптококки, токсоплазмы, Candida, CMV, очаговое поражение бывает обусловлено лимфомой. Наиболее характерен ряд симптомокомплексов: менингизм, энцефалит, менингит, гемипарезы, мозжечковая атаксия, судорожный синдром, СПИД-дементный комплекс. Неврологические проявления поражения головного мозга проявляются в одних случаях преимущественным вовлечением в процесс головного мозга, в других — спинного мозга, в третьих — оболочек, а в четвертых — периферических нервов и корешков (табл. 30). В каждом конкретном случае клиника характеризуется свойственной данному виду патологии симптомами. Так, для вакуолярной миелопатии характерны парастезии и слабость в ногах, а при оценке неврологического статуса выявляются парапарез, мышечная спастичность, атаксия. Периферическая невропатия характеризуется парастезиями, слабостью и дистальной атрофией. Клинике СПИД-деменции свойственны ранние и поздние проявления (табл. 31). Больных обычно беспокоит головная боль, тревога с депрессией, нарушение равновесия, снижение остроты зрения, нарушение памяти.
 Топика поражения Характер поражения Головной мозг а) преобладающие не очаговые СПИД-ассоциированная деменция метаболическая энцефалопатия цитомегаловирусный энцефалит герепетический энцефалит острый ВИЧ-обусловленный энцефалит б) преобладающе очаговые церебральный токсоплазмоз первичная лимфома ЦНС прогрессирующий полиочаговый лейкоэнцефалит криптококковая туберкулема HZV-энцефалит сосудистые расстройства Спинной мозг вакуолярная миелопатия HZV-миелит спинномозговая эпидуральная или интрадуральная лимфома Оболочки мозга асептический менингит (HIV? ) криптококковый менингит лимфома оболочек головного мозга туберкулезный менингит сифилитический менингит листериозный менингит Периферически е нервы и корешки дистальная сенсорно-моторная полинейропатияострая и хроническая демиелинизиующая нейропатия мононейропатия, ассоциированная с асептическим менингитоммононевриты. HZV- и CMV-полирадикулопатиямононейропатии, ассоциированные с лимфоматозным менингитом Мышцы полимиозит и другие миопатии
Топика поражения Характер поражения Головной мозг а) преобладающие не очаговые СПИД-ассоциированная деменция метаболическая энцефалопатия цитомегаловирусный энцефалит герепетический энцефалит острый ВИЧ-обусловленный энцефалит б) преобладающе очаговые церебральный токсоплазмоз первичная лимфома ЦНС прогрессирующий полиочаговый лейкоэнцефалит криптококковая туберкулема HZV-энцефалит сосудистые расстройства Спинной мозг вакуолярная миелопатия HZV-миелит спинномозговая эпидуральная или интрадуральная лимфома Оболочки мозга асептический менингит (HIV? ) криптококковый менингит лимфома оболочек головного мозга туберкулезный менингит сифилитический менингит листериозный менингит Периферически е нервы и корешки дистальная сенсорно-моторная полинейропатияострая и хроническая демиелинизиующая нейропатия мононейропатия, ассоциированная с асептическим менингитоммононевриты. HZV- и CMV-полирадикулопатиямононейропатии, ассоциированные с лимфоматозным менингитом Мышцы полимиозит и другие миопатии
 Ранние проявления Симптомы: 1. Познавательная (умственная) способность: — снижена концентрация — снижение, потеря памяти — умственная заторможенность 2. Двигательная сфера: — шаткая походка — слабость в ногах — нарушение координации — изменение почерка — тремор 3. Поведение: — апатия, замкнутость, депрессия — говорливость, агрессивность, галлюцинации
Ранние проявления Симптомы: 1. Познавательная (умственная) способность: — снижена концентрация — снижение, потеря памяти — умственная заторможенность 2. Двигательная сфера: — шаткая походка — слабость в ногах — нарушение координации — изменение почерка — тремор 3. Поведение: — апатия, замкнутость, депрессия — говорливость, агрессивность, галлюцинации
 Признаки: 1. Умственный статус — психомоторная заторможенность — психоз 2. Неврологическое обследование: — появление патологических рефлексов(хоботковый, хватательный) — снижение согласованности движений — атаксия — гиперрефлексия — тремор — слабость ног Поздние проявления Умственный статус: — общая деменция — психомоторная заторможенность( замедление ответа на устный вопрос, умеренный или абсолютный мутизм, рассеянный взгляд, бессознательное состояние, расторможенность) — возбуждение, дезориентация, — психоз
Признаки: 1. Умственный статус — психомоторная заторможенность — психоз 2. Неврологическое обследование: — появление патологических рефлексов(хоботковый, хватательный) — снижение согласованности движений — атаксия — гиперрефлексия — тремор — слабость ног Поздние проявления Умственный статус: — общая деменция — психомоторная заторможенность( замедление ответа на устный вопрос, умеренный или абсолютный мутизм, рассеянный взгляд, бессознательное состояние, расторможенность) — возбуждение, дезориентация, — психоз
 Неврологические изменения: — слабость( ног > рук) — атаксия — пирамидные спастические параличи, гиперрефлексия, — недержание мочи, стула — миоклонус
Неврологические изменения: — слабость( ног > рук) — атаксия — пирамидные спастические параличи, гиперрефлексия, — недержание мочи, стула — миоклонус
 Поражение желудочно-кишечного тракта Желудочно-кишечный тракт вовлекается в патологический процесс при ВИЧ-инфекции постоянно и может поражаться в различные сроки болезни, так как некоторые клеточные образования его являются мишенью для вируса. Вирус обнаруживается в различных клетках не только слизистой оболочки прямой кишки, особенно у гомосексуалистов, но и во всех отделах кишечника, в клетках, не имеющих CD 4 рецепторов. Очевидно, проникновение вируса в ткани происходит при межклеточном обмене, минуя свободное существование. Сам вирус обусловливает дегенеративные изменения крипт, частично атрофию микроворсинок, в силу чего нарушается пристеночное пищеварение и всасывание. Происходит не только морфо-функциональное нарушение стенки кишечника, но и снижение его резистентности, развитие дисбактериоза и развитие инфекционного процесса, склонного к упорному течению и рецидивированию. Характер поражения может как диффузным, так и локальным в виде стоматита, эзофагита, дуоденита, некротизирующего энтерита, язвенного и псевдомембранозного колита, проктита и др. Диарея — одно из наиболее характерных клинических проявлений поражения желудочно-кишечного тракта при ВИЧ-инфекции, она наблюдается у 70% больных. К наиболее характерным симптомам поражения желудочно-кишечного тракта относятся:
Поражение желудочно-кишечного тракта Желудочно-кишечный тракт вовлекается в патологический процесс при ВИЧ-инфекции постоянно и может поражаться в различные сроки болезни, так как некоторые клеточные образования его являются мишенью для вируса. Вирус обнаруживается в различных клетках не только слизистой оболочки прямой кишки, особенно у гомосексуалистов, но и во всех отделах кишечника, в клетках, не имеющих CD 4 рецепторов. Очевидно, проникновение вируса в ткани происходит при межклеточном обмене, минуя свободное существование. Сам вирус обусловливает дегенеративные изменения крипт, частично атрофию микроворсинок, в силу чего нарушается пристеночное пищеварение и всасывание. Происходит не только морфо-функциональное нарушение стенки кишечника, но и снижение его резистентности, развитие дисбактериоза и развитие инфекционного процесса, склонного к упорному течению и рецидивированию. Характер поражения может как диффузным, так и локальным в виде стоматита, эзофагита, дуоденита, некротизирующего энтерита, язвенного и псевдомембранозного колита, проктита и др. Диарея — одно из наиболее характерных клинических проявлений поражения желудочно-кишечного тракта при ВИЧ-инфекции, она наблюдается у 70% больных. К наиболее характерным симптомам поражения желудочно-кишечного тракта относятся:
 1. Жалобы больного — диарея длительностью свыше 1 мес, — дисфагия, болезненность при глотании, — вздутие живота, — эпигастральные, колитические боли, 2. Объективно со стороны желудочно-кишечного тракта могут быть — лейкоплакия, — кандидозные бляшки, — эрозии и язвы на слизистой пищевода, — изъязвления в перианальной области, — саркома Капоши толстой кишки, — гепато- спленомегалия. Среди возбудителей, вызывающих поражение желудочно-кишечного тракта чаще всего выявляются грибы Кандида, сальмонеллы, шигеллы, вирусы простого герпеса и цитомегаловирус, криптоспоридии и изоспоры (табл. 32).
1. Жалобы больного — диарея длительностью свыше 1 мес, — дисфагия, болезненность при глотании, — вздутие живота, — эпигастральные, колитические боли, 2. Объективно со стороны желудочно-кишечного тракта могут быть — лейкоплакия, — кандидозные бляшки, — эрозии и язвы на слизистой пищевода, — изъязвления в перианальной области, — саркома Капоши толстой кишки, — гепато- спленомегалия. Среди возбудителей, вызывающих поражение желудочно-кишечного тракта чаще всего выявляются грибы Кандида, сальмонеллы, шигеллы, вирусы простого герпеса и цитомегаловирус, криптоспоридии и изоспоры (табл. 32).
 Таблица 32. Энтеропатогены, встречающиеся при ВИЧ-инфекции Место нахождения ВИЧ-инфекция с диареей Рот Candida HSV Пищевод Candida HSV CMV Тонкая и толстая кишки Сальмонеллы CMV Криптоспоридии Изоспора Аноректальная зона HSV
Таблица 32. Энтеропатогены, встречающиеся при ВИЧ-инфекции Место нахождения ВИЧ-инфекция с диареей Рот Candida HSV Пищевод Candida HSV CMV Тонкая и толстая кишки Сальмонеллы CMV Криптоспоридии Изоспора Аноректальная зона HSV
 Поражения кожи и слизистых оболочек при ВИЧ-инфекции относятся к постоянным проявлениям клиники, они имеют место у 84% больны. Из 12 СПИД-индикаторных болезней 5 относятся к патологии кожи. В динамике ВИЧ-инфекции поражения кожи и слизистых оболочек носят рецидивирующий характер, с периодами обострений и ремиссий, а в далеко зашедших фазах болезни преобретают тяжелые, не свойственные их клинике варианты. Этиологически разнообразные виды патологии кожи и слизистых у больных имеют определенную географическую зависимость. Среди патологий кожи наиболее часто встречаются вирусные (простой герпес, опоясывающий герпес, волосатая” лейкоплакия рта, вызванная вирусами Эпштейна-Барр экзантема, остроконечные кондиломы, вызванные вирусом папилломы, кореподобная и краснушноподобная экзантема), бактериальные (пиодермия шанкриформная, стрепто- стафилодермия, кожно-слизистые язвы, бактериальные абсцессы, фурункулез, фолликулит, импетиго, экзема, микобактериальная инфекция, актиномикоз, атипический сифилис, синдром «обожженной кожи»), микотические (кандидоз, дерматомикозы, криптококкоз, гистоплазмоз, отрубевидный лишай) паразитарные (чесотка) инфекции, сосудистые поражения (васкулиты, телеангиэктазии, геморрагии, тромбоцитопеническая пурпура), опухоли (саркома Капоши, лимфома, плоский рак, миелома), папулосквамозные дерматозы (себорейный дерматит, псориаз, розовый лишай). Группу характерных для ВИЧ-инфекции патологий слизистых оболочек входят ангулярный стоматит, афтоз, простой и некротический гингивит.
Поражения кожи и слизистых оболочек при ВИЧ-инфекции относятся к постоянным проявлениям клиники, они имеют место у 84% больны. Из 12 СПИД-индикаторных болезней 5 относятся к патологии кожи. В динамике ВИЧ-инфекции поражения кожи и слизистых оболочек носят рецидивирующий характер, с периодами обострений и ремиссий, а в далеко зашедших фазах болезни преобретают тяжелые, не свойственные их клинике варианты. Этиологически разнообразные виды патологии кожи и слизистых у больных имеют определенную географическую зависимость. Среди патологий кожи наиболее часто встречаются вирусные (простой герпес, опоясывающий герпес, волосатая” лейкоплакия рта, вызванная вирусами Эпштейна-Барр экзантема, остроконечные кондиломы, вызванные вирусом папилломы, кореподобная и краснушноподобная экзантема), бактериальные (пиодермия шанкриформная, стрепто- стафилодермия, кожно-слизистые язвы, бактериальные абсцессы, фурункулез, фолликулит, импетиго, экзема, микобактериальная инфекция, актиномикоз, атипический сифилис, синдром «обожженной кожи»), микотические (кандидоз, дерматомикозы, криптококкоз, гистоплазмоз, отрубевидный лишай) паразитарные (чесотка) инфекции, сосудистые поражения (васкулиты, телеангиэктазии, геморрагии, тромбоцитопеническая пурпура), опухоли (саркома Капоши, лимфома, плоский рак, миелома), папулосквамозные дерматозы (себорейный дерматит, псориаз, розовый лишай). Группу характерных для ВИЧ-инфекции патологий слизистых оболочек входят ангулярный стоматит, афтоз, простой и некротический гингивит.
 Наряду с кожей и слизистыми оболочками нередко у больных выявляется павтология волос и ногтей в виде истончения волос, гипертрихоза, очаговой алопеции, деформации ногтей, изменение их цвета. Патология кожи и слизистых обусловлена как формирующимся иммунодефицитом, так и непосредственным эффектом ВИЧ. Примером прямой зависимости поражения кожи от ВИЧ-инфекции может служить папилломавирусная инфекция кожи и слизистых. Насчитывается свыше 85 типов папилломавирусов, но возможность их вызывать клинически манифестные формы болезни во многом определяется возрастом человека, состоянием иммунной системы организма. Поэтому у больных ВИЧ-инфекцией частота поражения папилломавирусом значительно возрастает. Обследование ВИЧ-инфицированных женщин в США, Европе, Африке и Южной Азии методами гибридизации ДНК и ПЦР позволило выявить генитальный тип папилломавируса у 8 -49% серонегативных и у 37 -78% ВИЧ-серопозитивных проституток, потребительниц внутривенных наркотиков. Напримр, в США среди потребительниц внутривенных наркотиков проституток, не инфицированных ВИЧ папилломавирус обнаружен в 7%, а среди ВИЧ-серопозитивных – в 32% (Van Dournum G. J. ; 1993; Kiviat N. B. , 1997). Среди потребительниц внутривенных наркотиков США, обусловленные папилломавирусом внутриэпителиальные опухоли встречаются в 31% в группе ВИЧ-инфицированных и лишь в 4% у ВИЧ-негативных женщин (Feingold A. R. , 1990).
Наряду с кожей и слизистыми оболочками нередко у больных выявляется павтология волос и ногтей в виде истончения волос, гипертрихоза, очаговой алопеции, деформации ногтей, изменение их цвета. Патология кожи и слизистых обусловлена как формирующимся иммунодефицитом, так и непосредственным эффектом ВИЧ. Примером прямой зависимости поражения кожи от ВИЧ-инфекции может служить папилломавирусная инфекция кожи и слизистых. Насчитывается свыше 85 типов папилломавирусов, но возможность их вызывать клинически манифестные формы болезни во многом определяется возрастом человека, состоянием иммунной системы организма. Поэтому у больных ВИЧ-инфекцией частота поражения папилломавирусом значительно возрастает. Обследование ВИЧ-инфицированных женщин в США, Европе, Африке и Южной Азии методами гибридизации ДНК и ПЦР позволило выявить генитальный тип папилломавируса у 8 -49% серонегативных и у 37 -78% ВИЧ-серопозитивных проституток, потребительниц внутривенных наркотиков. Напримр, в США среди потребительниц внутривенных наркотиков проституток, не инфицированных ВИЧ папилломавирус обнаружен в 7%, а среди ВИЧ-серопозитивных – в 32% (Van Dournum G. J. ; 1993; Kiviat N. B. , 1997). Среди потребительниц внутривенных наркотиков США, обусловленные папилломавирусом внутриэпителиальные опухоли встречаются в 31% в группе ВИЧ-инфицированных и лишь в 4% у ВИЧ-негативных женщин (Feingold A. R. , 1990).
 Поражения кожи и слизистых оболочек, как суперинфекция у больных ВИЧ/СПИД приобретают клиническое течение мало характерное для них у больных без иммунодефицита и плохо поддаются лечению. В клинической диагносьтике ВИЧ-инфекции наибольшее значение имеют следующие виды патологии кожи и слизистых: микотическая инфекция (кандидоз, дерматормикозы, кератомикозы, криптококкоз), вирусная инфекция (опоясыывающий герпес, пузырькоавый лишай, «волосатая» лейкоплакия, контагиозный моллюск, вульгарные бородавки) бактериальная инфекция кожи, паразитозы кожи (чесотка), себорейный дерматит, пмсориаз, саркома Капоши, лимфома.
Поражения кожи и слизистых оболочек, как суперинфекция у больных ВИЧ/СПИД приобретают клиническое течение мало характерное для них у больных без иммунодефицита и плохо поддаются лечению. В клинической диагносьтике ВИЧ-инфекции наибольшее значение имеют следующие виды патологии кожи и слизистых: микотическая инфекция (кандидоз, дерматормикозы, кератомикозы, криптококкоз), вирусная инфекция (опоясыывающий герпес, пузырькоавый лишай, «волосатая» лейкоплакия, контагиозный моллюск, вульгарные бородавки) бактериальная инфекция кожи, паразитозы кожи (чесотка), себорейный дерматит, пмсориаз, саркома Капоши, лимфома.
 Моче-половые проявления СПИД Поражение моче-половой системы при ВИЧ-инфекции обусловлено как непосредственно вирусом, так и является следствием вторичных осложнений инфекционного процесса. Простата имеет собственный механизм защиты от бактериальной инфекции, включающий спермин, спермидин, антибактериальный фактор простаты. Но у больных ВИЧ-инфекцией местный иммунодефицит, в частности снижение бактерицидных свойств простатической жидкости, по-видимому, является причиной развития бактериальной инфекции. Атрофия тестикул чаще всего наблюдается у больных ВИЧ/СПИД, занимая второе место у больных. Опухоли яичек занимают третье место из наиболее распространенных СПИД-ассоциируемых опухолей, следуя за саркомой Капоши и неходжкинской лимфомой.
Моче-половые проявления СПИД Поражение моче-половой системы при ВИЧ-инфекции обусловлено как непосредственно вирусом, так и является следствием вторичных осложнений инфекционного процесса. Простата имеет собственный механизм защиты от бактериальной инфекции, включающий спермин, спермидин, антибактериальный фактор простаты. Но у больных ВИЧ-инфекцией местный иммунодефицит, в частности снижение бактерицидных свойств простатической жидкости, по-видимому, является причиной развития бактериальной инфекции. Атрофия тестикул чаще всего наблюдается у больных ВИЧ/СПИД, занимая второе место у больных. Опухоли яичек занимают третье место из наиболее распространенных СПИД-ассоциируемых опухолей, следуя за саркомой Капоши и неходжкинской лимфомой.
 Документально передача вируса через слезы, мочу или предъякулят не доказана. Более высока концентрация вируса в семенной жидкости, чем в вагинальных секретах. Поэтому передача вируса во время полового акта от мужчины женщине примерно в 2 раза выше, чем от женщины к мужчине. Вагинальный эпителий — барьер для вируса, пока на нем нет язв или повреждений. Шейка матки наиболее вероятный путь проникновения вируса, особенно во время месячных или вскоре после них. Антиспермициды, часто используемые для предотвращения беременности и защиты от вируса могут в действительности повысить передачу вируса, раздражая вагину. Передача вируса от женщины к мужчине наиболее вероятно происходит во время месячных, при анальном половом акте или инфекционный процесс у женщины далеко зашел и характеризуется высокой виремией. Оральный секс – невысокий риск передачи вируса, так как в слюне концентрация вируса мала, значительно уступая ей в половых секретах, если только слизистые барьеры не повреждены ни у партнера, осуществляющего оральный секс, ни у реципиента. Среди гомосексуалистов пассивный партнер во время анального полового акта имеет более высокий риск инфицирования, чем активный. Ссадины анального канала и/ или прямое воздействие на слизистую повышают риск инфицирования пассивного партнера.
Документально передача вируса через слезы, мочу или предъякулят не доказана. Более высока концентрация вируса в семенной жидкости, чем в вагинальных секретах. Поэтому передача вируса во время полового акта от мужчины женщине примерно в 2 раза выше, чем от женщины к мужчине. Вагинальный эпителий — барьер для вируса, пока на нем нет язв или повреждений. Шейка матки наиболее вероятный путь проникновения вируса, особенно во время месячных или вскоре после них. Антиспермициды, часто используемые для предотвращения беременности и защиты от вируса могут в действительности повысить передачу вируса, раздражая вагину. Передача вируса от женщины к мужчине наиболее вероятно происходит во время месячных, при анальном половом акте или инфекционный процесс у женщины далеко зашел и характеризуется высокой виремией. Оральный секс – невысокий риск передачи вируса, так как в слюне концентрация вируса мала, значительно уступая ей в половых секретах, если только слизистые барьеры не повреждены ни у партнера, осуществляющего оральный секс, ни у реципиента. Среди гомосексуалистов пассивный партнер во время анального полового акта имеет более высокий риск инфицирования, чем активный. Ссадины анального канала и/ или прямое воздействие на слизистую повышают риск инфицирования пассивного партнера.
 Miles et al. (1996) нашли в 16% поражение половой системы и в 17% мочевыводящих путей у больных ВИЧ-инфекцией. Дисфункция мочевыводящих путей обусловливает стаз мочи с последующим развитием инфекции моче-половой системы. В ә случаев инфекция обусловлена E. coli, в 1/3 – P. aeruginosa и проявляется дизурией, частыми позывами и часто гематурией. Помимо E. coli, наиболее типичных возбудителей простатита, у больных ВИЧ-инфекцией воспалительный процесс также вызывают Stap. aureus, Klebsiella pneumoniae, Р. aeruginosa, Serratia marcesxens, S. typhi, а также вирусы и грибы. Большинство грам-отрицательных бактерий вызывают простатит, забрасываясь из инфицированной мочи в простатические ходы. Stap. aureus распространяется гематогенно или через инструментарий. Микобактерии туберкулеза и атипические осложняют ВИЧ-инфекцию не редко с локализацией процесса в легких, но они также могут вызывать простатит. Вирусы, включая ВИЧ, цитомегаловирус также обусловливают развитие простатита. Так как цитиомегаловирус располагается внутриклеточно и мало поддается терапии, у больных процесс приобретает рецидивирующий характер.
Miles et al. (1996) нашли в 16% поражение половой системы и в 17% мочевыводящих путей у больных ВИЧ-инфекцией. Дисфункция мочевыводящих путей обусловливает стаз мочи с последующим развитием инфекции моче-половой системы. В ә случаев инфекция обусловлена E. coli, в 1/3 – P. aeruginosa и проявляется дизурией, частыми позывами и часто гематурией. Помимо E. coli, наиболее типичных возбудителей простатита, у больных ВИЧ-инфекцией воспалительный процесс также вызывают Stap. aureus, Klebsiella pneumoniae, Р. aeruginosa, Serratia marcesxens, S. typhi, а также вирусы и грибы. Большинство грам-отрицательных бактерий вызывают простатит, забрасываясь из инфицированной мочи в простатические ходы. Stap. aureus распространяется гематогенно или через инструментарий. Микобактерии туберкулеза и атипические осложняют ВИЧ-инфекцию не редко с локализацией процесса в легких, но они также могут вызывать простатит. Вирусы, включая ВИЧ, цитомегаловирус также обусловливают развитие простатита. Так как цитиомегаловирус располагается внутриклеточно и мало поддается терапии, у больных процесс приобретает рецидивирующий характер.
 Cреди грибов Cryptococcus neoformans и Histoplasma capsulatum чаще всего вызывают простатит у больных ВИЧ-инфекцией. даже после успешной терапии первичной грибковой инфекции в простате сохраняются эти возбудители в виде персистирующих субклинических фокусов, со временм обусловливая рецидив. Проблемой у больных в развитой стадии ВИЧ-инфекции являются также абсцессы простаты, особенно если у больных имеются такие предрасполагающие факторы, как сахарный диабет, ранее проводившаяся катетеризация мочевыводящих путей, инструментальное обследование, обструкция мочевых путей. Рост заболеваемсти типичными и атипичными формами воспалений мочевыводящих путей, простатита, абсцессами простаты, отмечаемый в настоящее время, связан с пандемией ВИЧ-инфекции. У здоровых людей острый бактериальный простатит по данным клинических проявлений, пальцевого ректального обследования и результатов бактериологического исследования мочи обнаруживается в 1 -2%, у асимптоматических больных ВИЧ-инфекцией – в 3%, а у больных СПИДом – в 14% (Staiman V. R. et al. , 1997).
Cреди грибов Cryptococcus neoformans и Histoplasma capsulatum чаще всего вызывают простатит у больных ВИЧ-инфекцией. даже после успешной терапии первичной грибковой инфекции в простате сохраняются эти возбудители в виде персистирующих субклинических фокусов, со временм обусловливая рецидив. Проблемой у больных в развитой стадии ВИЧ-инфекции являются также абсцессы простаты, особенно если у больных имеются такие предрасполагающие факторы, как сахарный диабет, ранее проводившаяся катетеризация мочевыводящих путей, инструментальное обследование, обструкция мочевых путей. Рост заболеваемсти типичными и атипичными формами воспалений мочевыводящих путей, простатита, абсцессами простаты, отмечаемый в настоящее время, связан с пандемией ВИЧ-инфекции. У здоровых людей острый бактериальный простатит по данным клинических проявлений, пальцевого ректального обследования и результатов бактериологического исследования мочи обнаруживается в 1 -2%, у асимптоматических больных ВИЧ-инфекцией – в 3%, а у больных СПИДом – в 14% (Staiman V. R. et al. , 1997).
 Хотя поражение вызвано микроорганизмами, выделить культуру из мочи удается не всегда, так как больные СПИДом получают антимикробные препараты с целью профилактики суперинфекций или лечатся по поводу пневмонии или диареи. Легче выделить возбудитель из секрета простаты или получить уринокультуру после массажа простаты, так как чаще при бактериальном поражении моче-половой системы у больных ВИЧ-инфекцией возбидители локализуются именно в простате. У многих больных ВИЧ-инфекцией, даже не имеющих симптомов поражения моче-половой системы обнаруживается микроскоопически гематурия. Так, Сеspades et al. (1996) нашли микрогематурию у ә из 1326 обследованных больных, но у большинства из них явления прошли самостоятельно, больные не нуждались в лечении у уролога, если до того у больных не было поражений почек или урогенитальной системы.
Хотя поражение вызвано микроорганизмами, выделить культуру из мочи удается не всегда, так как больные СПИДом получают антимикробные препараты с целью профилактики суперинфекций или лечатся по поводу пневмонии или диареи. Легче выделить возбудитель из секрета простаты или получить уринокультуру после массажа простаты, так как чаще при бактериальном поражении моче-половой системы у больных ВИЧ-инфекцией возбидители локализуются именно в простате. У многих больных ВИЧ-инфекцией, даже не имеющих симптомов поражения моче-половой системы обнаруживается микроскоопически гематурия. Так, Сеspades et al. (1996) нашли микрогематурию у ә из 1326 обследованных больных, но у большинства из них явления прошли самостоятельно, больные не нуждались в лечении у уролога, если до того у больных не было поражений почек или урогенитальной системы.
 Наиболее типичное проявление абсцесса простаты – острая задержка мочи, лихорадка, дизурия, частые мочеиспускания, боль. Клинически выявляется увеличение размеров простаты у 75% больных. Бактериологические исследование мочи чаще не дает результатов. При выделении возбудителя наиболее типичны – Enterobacteriaceae и другие грамм-отрицательные микробы. грибы. Лечение длительное, но не предотвращает от рецидивов. Так как антимикробные препараты плохо проникают в ткань простаты, хирургический дренаж в сочетании с антимикробной терапией наиболее оправдан.
Наиболее типичное проявление абсцесса простаты – острая задержка мочи, лихорадка, дизурия, частые мочеиспускания, боль. Клинически выявляется увеличение размеров простаты у 75% больных. Бактериологические исследование мочи чаще не дает результатов. При выделении возбудителя наиболее типичны – Enterobacteriaceae и другие грамм-отрицательные микробы. грибы. Лечение длительное, но не предотвращает от рецидивов. Так как антимикробные препараты плохо проникают в ткань простаты, хирургический дренаж в сочетании с антимикробной терапией наиболее оправдан.
 Атрофия тестикул – наиболее частое нарушение тестикул у больных ВИЧ/СПИДом. Частота развития атрофии коррелирует с длительность ВИЧ-инфнекции, глубиной иммунодефицита, длительностью лихорадки, истощением больного. Гистологичечки обнаруживается перитубулярное интерстициальное воспаление, интерстициальный фибюроз, гиалинизация туберкулярных мембран, сосудистые нарушения, ведущие к ишемии и последующей атрофии. Значительно уменьшается сперматогенез, созревание сперматозоидов останавливается на стадии сперматоцитов. Наиболее частое СПИД-ассоциируемое эндокринное нарушение – нарушение гипофизаро-гипоталямо-тестикулярной оси, встречающееся у ә-1/3 больных. Атрофия тестикул может быть следствием гипогонадизма. ВИЧ сам по себе оказывает цитопатический эффект на герминативную ткань и Сертолиевы клетки, что также может быть причиной атрофии яичек. ВИЧ также связывают с причиной втортичных поражений яичек. Такие условнопатогенные возбудители, как CMV, атипические микобактерии, вызывая поражение тестикул, ведут к их атрофии. По данным литературы у 14 -26% больных ВИЧ-инфекцией имеют цитомегаловирусное поражение яичек. CMV передается половым путем и локализуется интратуберкулярно, в интерстициальной ткани, в эндотелии, вызывая орхит, гранулематозные изменения, сосудистые нарушения, в конечном итлоге приводя к атрофии тестикул. Примерно у 15% больных ВИЧ-инфекцией и у 30 -40% больных в стадии СПИД в течение их жизни развивается карцинома.
Атрофия тестикул – наиболее частое нарушение тестикул у больных ВИЧ/СПИДом. Частота развития атрофии коррелирует с длительность ВИЧ-инфнекции, глубиной иммунодефицита, длительностью лихорадки, истощением больного. Гистологичечки обнаруживается перитубулярное интерстициальное воспаление, интерстициальный фибюроз, гиалинизация туберкулярных мембран, сосудистые нарушения, ведущие к ишемии и последующей атрофии. Значительно уменьшается сперматогенез, созревание сперматозоидов останавливается на стадии сперматоцитов. Наиболее частое СПИД-ассоциируемое эндокринное нарушение – нарушение гипофизаро-гипоталямо-тестикулярной оси, встречающееся у ә-1/3 больных. Атрофия тестикул может быть следствием гипогонадизма. ВИЧ сам по себе оказывает цитопатический эффект на герминативную ткань и Сертолиевы клетки, что также может быть причиной атрофии яичек. ВИЧ также связывают с причиной втортичных поражений яичек. Такие условнопатогенные возбудители, как CMV, атипические микобактерии, вызывая поражение тестикул, ведут к их атрофии. По данным литературы у 14 -26% больных ВИЧ-инфекцией имеют цитомегаловирусное поражение яичек. CMV передается половым путем и локализуется интратуберкулярно, в интерстициальной ткани, в эндотелии, вызывая орхит, гранулематозные изменения, сосудистые нарушения, в конечном итлоге приводя к атрофии тестикул. Примерно у 15% больных ВИЧ-инфекцией и у 30 -40% больных в стадии СПИД в течение их жизни развивается карцинома.
 Опухоли яичек занимают третье место после саркомы капоши и неходжкинской лимфомы. В популяции людей, не инфицированных ВИЧ они встречаются в 0, 004%, а у больных ВИЧ-инфекцией – в в 0, 2%, т. е. частота возрастает в 50 раз. В общей популяции опухоли яичек связаны с крипторхизмом, паховой грыжей, орхитом. В общей популяции среди опухолей 40% приходится на семиномы, а у больных ВИЧ-инфекцией чаще встречаются опухоли не семиномной природы. Терапия обычно включает хирургические лечение, облучение и химиотерапию, больные умирают быстрее от основного заболевания, чем разовьется рецидив опухоли. Лимфома яичек встречается примерно у 5% больных (тестикулярная неоплазма), чаще у лиц стране 50 лет. У 60% больных снижено либидо, у 1/3 развивается импотенция. Импотенция чаще связана с психотравмой и нейрогенными факторами, в частности, СПИД-деменцией, а также в связи с суперинфекцией и злокачественными опухолями.
Опухоли яичек занимают третье место после саркомы капоши и неходжкинской лимфомы. В популяции людей, не инфицированных ВИЧ они встречаются в 0, 004%, а у больных ВИЧ-инфекцией – в в 0, 2%, т. е. частота возрастает в 50 раз. В общей популяции опухоли яичек связаны с крипторхизмом, паховой грыжей, орхитом. В общей популяции среди опухолей 40% приходится на семиномы, а у больных ВИЧ-инфекцией чаще встречаются опухоли не семиномной природы. Терапия обычно включает хирургические лечение, облучение и химиотерапию, больные умирают быстрее от основного заболевания, чем разовьется рецидив опухоли. Лимфома яичек встречается примерно у 5% больных (тестикулярная неоплазма), чаще у лиц стране 50 лет. У 60% больных снижено либидо, у 1/3 развивается импотенция. Импотенция чаще связана с психотравмой и нейрогенными факторами, в частности, СПИД-деменцией, а также в связи с суперинфекцией и злокачественными опухолями.
 О п у х о л и Саркома Капоши. В группу СПИД-ассоциируемых заболеваний входит саркома Капоши, которая, в отличие от саркомы не эпидемического характера, поражает лиц молодого возраста и носит прогрессирующий характер. В 1872 году венгр Мориц Капоши описал заболевание под названием “множественная идиопатическая пигментная гемангиосаркома”. Заболевание в основном проявлялось в виде локализованных узлов коричнево-красного — синюшно-красного цвета с локализацией преимущественно на коже нижних конечностей, чаще у мужчин в возрасте старше 40 лет. Сегодня это классическая форма саркомы Капоши (табл. 33).
О п у х о л и Саркома Капоши. В группу СПИД-ассоциируемых заболеваний входит саркома Капоши, которая, в отличие от саркомы не эпидемического характера, поражает лиц молодого возраста и носит прогрессирующий характер. В 1872 году венгр Мориц Капоши описал заболевание под названием “множественная идиопатическая пигментная гемангиосаркома”. Заболевание в основном проявлялось в виде локализованных узлов коричнево-красного — синюшно-красного цвета с локализацией преимущественно на коже нижних конечностей, чаще у мужчин в возрасте старше 40 лет. Сегодня это классическая форма саркомы Капоши (табл. 33).
 Таблица 33. Сравнительная характеристика вариантов саркомы Капоши Вариант Популяция Клиническая характеристика Течение Классиче ский Преимущест венно европейцы 50 -80 лет Чаще кожа нижних конечностей в виде генерализованных новообразований кровеносных сосудов и расширением капилляров, образующих полости различной формы и величины Медленное, 10 -15 лет, в 1/3 ассоциирует с другими злокачественными опухолями Африкан ский Молодой возраст (25 -40 лет) негры Центрально й Америки Локализация изменчива, характеризуется обширными агрессивно протекающими экзофитными опухолями или опухоли проникают в кости нижних конечностей (соотношение мужчины/женщины — 3/1) Медленное, если нодулярная форма, в остальных случаях медленно прогрессирующее течение с неблагоприятным исходом в ближайшие 5 -8 лет Дети 2 -13 лет Генерализованный лимфаденоматоз, реже вовлекаются кости (соотношение мужчины/женщины — 3/1) При пересадк е почек Чаще евреи и жители средиземно морья, ятрогенное заболевание Может локализоваться в костях или процесс широко распространен с вовлечением тканей (соотношение мужчины/женщины — 3/1) Медленно или быстро прогрессирует, летальность 30% Эпидеми ческий Больные СПИД Диссеминированный процесс с поражением слизистых оболочек и кожи, вовлечением лимфатических узлов и висцеральных органов, чаще желудочно-кишечного тракта и легких. Часто протекает в ассоциации с оппортунистической инфекцией Фульминантное течение, менее чем 20% заболевлевших выживает свыше 2 лет
Таблица 33. Сравнительная характеристика вариантов саркомы Капоши Вариант Популяция Клиническая характеристика Течение Классиче ский Преимущест венно европейцы 50 -80 лет Чаще кожа нижних конечностей в виде генерализованных новообразований кровеносных сосудов и расширением капилляров, образующих полости различной формы и величины Медленное, 10 -15 лет, в 1/3 ассоциирует с другими злокачественными опухолями Африкан ский Молодой возраст (25 -40 лет) негры Центрально й Америки Локализация изменчива, характеризуется обширными агрессивно протекающими экзофитными опухолями или опухоли проникают в кости нижних конечностей (соотношение мужчины/женщины — 3/1) Медленное, если нодулярная форма, в остальных случаях медленно прогрессирующее течение с неблагоприятным исходом в ближайшие 5 -8 лет Дети 2 -13 лет Генерализованный лимфаденоматоз, реже вовлекаются кости (соотношение мужчины/женщины — 3/1) При пересадк е почек Чаще евреи и жители средиземно морья, ятрогенное заболевание Может локализоваться в костях или процесс широко распространен с вовлечением тканей (соотношение мужчины/женщины — 3/1) Медленно или быстро прогрессирует, летальность 30% Эпидеми ческий Больные СПИД Диссеминированный процесс с поражением слизистых оболочек и кожи, вовлечением лимфатических узлов и висцеральных органов, чаще желудочно-кишечного тракта и легких. Часто протекает в ассоциации с оппортунистической инфекцией Фульминантное течение, менее чем 20% заболевлевших выживает свыше 2 лет
 В ходе пандемии ВИЧ-инфекции прослеживается изменение частоты ее развития у больных. Так, по данным Center for Disease Control and Prevention (CDC), если в первые годы пандемии она встречалась у каждого третьего больного СПИДом, то к 1992 году — у 1 из 10 (табл. 34). Особенно часто саркома Капоши выявлялась у гомо- и бисексуалистов. Редко ее встречали среди больных ВИЧ-инфекцией детей.
В ходе пандемии ВИЧ-инфекции прослеживается изменение частоты ее развития у больных. Так, по данным Center for Disease Control and Prevention (CDC), если в первые годы пандемии она встречалась у каждого третьего больного СПИДом, то к 1992 году — у 1 из 10 (табл. 34). Особенно часто саркома Капоши выявлялась у гомо- и бисексуалистов. Редко ее встречали среди больных ВИЧ-инфекцией детей.
 Таблица 34. Случаи СПИДа с предполагаемым или точным наличием саркомы Капоши по годам (CDC) на декабрь 1992 года Годы Всего больных СПИДом Больных с саркомой Капоши 1981 -1983 2 931 32, 7 1984 4 510 27, 8 1985 8 308 22, 4 1986 13 262 19, 3 1987 21 276 15, 5 1988 31 964 12, 7 1989 35 085 12, 1 1990 43 336 12, 0 1991 45 456 11, 1 1992 47 194 9, 9 Всего 253 322 13,
Таблица 34. Случаи СПИДа с предполагаемым или точным наличием саркомы Капоши по годам (CDC) на декабрь 1992 года Годы Всего больных СПИДом Больных с саркомой Капоши 1981 -1983 2 931 32, 7 1984 4 510 27, 8 1985 8 308 22, 4 1986 13 262 19, 3 1987 21 276 15, 5 1988 31 964 12, 7 1989 35 085 12, 1 1990 43 336 12, 0 1991 45 456 11, 1 1992 47 194 9, 9 Всего 253 322 13,
 Этиология. Поиск возбудителя начался задолго до появления ВИЧ-инфекции. В качестве этиологических факторов предполагали CMV, вирус Эпштейна-Барр и другие. В 1995 году Chang and Moore описали новый человеческий герпес-вирус (первоначально названный “с саркомой Капоши ассоциированный герпес-вирус”), позже получивший название человеческий герпес-вирус тип 8 (HHV 8). ДНК этого вируса постоянно обнаруживается в ткани СПИД-ассоциируемой саркомы Капоши, в то время как в нормальной ткани соседних участков не выявляется. В последующие годы было установлено, что HHV 8 связан совсеми типами саркомы Капоши, включая эндемическую у африканцев, классическую у пожилых людей средиземноморья и трансплантат-связанную. Показано, что за 3 -10 лет развитию саркомы Капоши предшествует инфекция, вызванная HHV 8.
Этиология. Поиск возбудителя начался задолго до появления ВИЧ-инфекции. В качестве этиологических факторов предполагали CMV, вирус Эпштейна-Барр и другие. В 1995 году Chang and Moore описали новый человеческий герпес-вирус (первоначально названный “с саркомой Капоши ассоциированный герпес-вирус”), позже получивший название человеческий герпес-вирус тип 8 (HHV 8). ДНК этого вируса постоянно обнаруживается в ткани СПИД-ассоциируемой саркомы Капоши, в то время как в нормальной ткани соседних участков не выявляется. В последующие годы было установлено, что HHV 8 связан совсеми типами саркомы Капоши, включая эндемическую у африканцев, классическую у пожилых людей средиземноморья и трансплантат-связанную. Показано, что за 3 -10 лет развитию саркомы Капоши предшествует инфекция, вызванная HHV 8.
 Механизм передачи вируса неивестен. С помощью ПЦР одни авторы вирус обнаруживали в семенной жидкости и сперме, хотя другие этого не подтвердили. HHV 8 был выявлен в эндотелиальных клетках, циркулирующих CD 20+ лимфоцитах (В-клетки), носовом секрете, бронхоальвеолярной леважной жидкости у больных с легочной локализацией саркомы Капоши. Сейчас все больше специалистов приходит к мнению, что хотя HHV 8 необходим для развития саркомы Капоши, но для ееразвития у конкретного человека этого недостаточно. Показано наличие вируса в организме без каких-либо признаком саркомы. Установлено, что распространение HHV 8 среди здоровой популяции возрастает в географических зонах, где исторически была высока заболеваемость саркомой Капоши – средиземноморье Европы, эндемические очаги Африки.
Механизм передачи вируса неивестен. С помощью ПЦР одни авторы вирус обнаруживали в семенной жидкости и сперме, хотя другие этого не подтвердили. HHV 8 был выявлен в эндотелиальных клетках, циркулирующих CD 20+ лимфоцитах (В-клетки), носовом секрете, бронхоальвеолярной леважной жидкости у больных с легочной локализацией саркомы Капоши. Сейчас все больше специалистов приходит к мнению, что хотя HHV 8 необходим для развития саркомы Капоши, но для ееразвития у конкретного человека этого недостаточно. Показано наличие вируса в организме без каких-либо признаком саркомы. Установлено, что распространение HHV 8 среди здоровой популяции возрастает в географических зонах, где исторически была высока заболеваемость саркомой Капоши – средиземноморье Европы, эндемические очаги Африки.
 Помимо HHV 8 множество других факторов влияют на манифестаци. саркомы Капоши, в частности провоспалительные цитокиныи другие субстанции, продуцируемые ВИЧ-инфицированными мононуклеарами, как ответ на инфекцию, служат мощным фактором роста клеток саркомы Капоши. Эти факторы включают ИЛ-6, ИЛ-1 -бета, основной фибробластический фактор роста, сосудистый эндотелиальный фактор роста, трансформирующий фактор роста-бета и др. Все они могут играть роль регуляторов роста существующих клеток саркомы Капоши. Аналогичную роль играет tat-белок ВИЧ (Levine A. , 1998). .
Помимо HHV 8 множество других факторов влияют на манифестаци. саркомы Капоши, в частности провоспалительные цитокиныи другие субстанции, продуцируемые ВИЧ-инфицированными мононуклеарами, как ответ на инфекцию, служат мощным фактором роста клеток саркомы Капоши. Эти факторы включают ИЛ-6, ИЛ-1 -бета, основной фибробластический фактор роста, сосудистый эндотелиальный фактор роста, трансформирующий фактор роста-бета и др. Все они могут играть роль регуляторов роста существующих клеток саркомы Капоши. Аналогичную роль играет tat-белок ВИЧ (Levine A. , 1998). .
 Патогенез. Первоначально предполагалось, что иммунодефицит является предпосылкой развития саркомы Капоши. Так, еще до пандемии ВИЧ-инфекции выявили, что у рецепиентов почек развивается иммуносупрессия и чаще развивается ятрогеннаяформа саркомы Капоши. После отмены иммуносупрессантов клиническая картина регрессирует. Пандемия, казалось, укрепилаэту точку зрения. Но через несколько лет после начала пандемии выявили, что у ряда лиц саркома развивается при отсутствии иммуносупрессии, при нормальной функции иммунной системы. Стало очевидным, что ВИЧ-инфекция может сопровождатьсяразвитием саркомы Капоши без нарушения функции иммунной системы. Следовательно, механизм развития ее не коррелируетс иммунодефицитом. Дальше было установлено, что активация (а не депрессия!) иммунной системы играет существенную рольв патогенезе саркомы Капоши. Это положение первоначально трактовалось справедливым только для классического, эндемического и ятрогенного вариантов саркомы Капоши. Исследования показали, что у больных с классическим вариантомсаркомы Капоши высок уровень анти-CMV. Это было расценено, как стимулирующий CMV для развития саркомы
Патогенез. Первоначально предполагалось, что иммунодефицит является предпосылкой развития саркомы Капоши. Так, еще до пандемии ВИЧ-инфекции выявили, что у рецепиентов почек развивается иммуносупрессия и чаще развивается ятрогеннаяформа саркомы Капоши. После отмены иммуносупрессантов клиническая картина регрессирует. Пандемия, казалось, укрепилаэту точку зрения. Но через несколько лет после начала пандемии выявили, что у ряда лиц саркома развивается при отсутствии иммуносупрессии, при нормальной функции иммунной системы. Стало очевидным, что ВИЧ-инфекция может сопровождатьсяразвитием саркомы Капоши без нарушения функции иммунной системы. Следовательно, механизм развития ее не коррелируетс иммунодефицитом. Дальше было установлено, что активация (а не депрессия!) иммунной системы играет существенную рольв патогенезе саркомы Капоши. Это положение первоначально трактовалось справедливым только для классического, эндемического и ятрогенного вариантов саркомы Капоши. Исследования показали, что у больных с классическим вариантомсаркомы Капоши высок уровень анти-CMV. Это было расценено, как стимулирующий CMV для развития саркомы
 В африканском варианте саркомы Капоши широко распространенные паразитарные и инфекционные заболевания также расценивались, как постоянный источник антигенного стимула, обеспечивающего развитие саркомы. В случаях ятрогенной саркомы Капоши постоянное инфицирование рецепиентов почек CMV, вирусом Эпштейна-Барр, HSV также является источникомпостоянного антигенного стимула, обеспечивающего развитие саркомы. Этому же способствует действие аллотрансплантата. Затем было установлено, что СПИД-ассоциированную саркому Капоши стимулируют глюкокортикостероиды, такие иммуносупрессоры, как циклоспорин. Следовательно, лекарственные средства, обусловливающие снижение уровня Т-супрессоров и этим активацию иммунной системы, также стимулируют развитие саркомы Капоши. Гомо/бисексуалисты подвержены хроническому антигенному стимулу за счет постоянного инфицирования половым путем различными грибками, простейшими, бактериями и вирусами.
В африканском варианте саркомы Капоши широко распространенные паразитарные и инфекционные заболевания также расценивались, как постоянный источник антигенного стимула, обеспечивающего развитие саркомы. В случаях ятрогенной саркомы Капоши постоянное инфицирование рецепиентов почек CMV, вирусом Эпштейна-Барр, HSV также является источникомпостоянного антигенного стимула, обеспечивающего развитие саркомы. Этому же способствует действие аллотрансплантата. Затем было установлено, что СПИД-ассоциированную саркому Капоши стимулируют глюкокортикостероиды, такие иммуносупрессоры, как циклоспорин. Следовательно, лекарственные средства, обусловливающие снижение уровня Т-супрессоров и этим активацию иммунной системы, также стимулируют развитие саркомы Капоши. Гомо/бисексуалисты подвержены хроническому антигенному стимулу за счет постоянного инфицирования половым путем различными грибками, простейшими, бактериями и вирусами.
 Антигенным стимулом служит и сперма. Постоянное травмирование слизистой оболочки кишечника облегчает проникновение антигенов и иммунизировать организм. Поэтому у ВИЧ-инфицированных гомо/бисексуалистов выше уровень саркомы Капоши. Именно этими обстоятельствами объясняется тот факт, что у больных СПИД-ассоциированной саркомой Капоши не имеет места иммуносупрессия и, наоборот, выявляются признаки иммунной активности. Очевидно, этим объясняется то обстоятельство, что ВИЧ-инфицированные с ранним развитием саркомы Капоши живут дольше, чем те, у кого имеет место дисфункция иммунной системы с развитием оппортунистической инфекции.
Антигенным стимулом служит и сперма. Постоянное травмирование слизистой оболочки кишечника облегчает проникновение антигенов и иммунизировать организм. Поэтому у ВИЧ-инфицированных гомо/бисексуалистов выше уровень саркомы Капоши. Именно этими обстоятельствами объясняется тот факт, что у больных СПИД-ассоциированной саркомой Капоши не имеет места иммуносупрессия и, наоборот, выявляются признаки иммунной активности. Очевидно, этим объясняется то обстоятельство, что ВИЧ-инфицированные с ранним развитием саркомы Капоши живут дольше, чем те, у кого имеет место дисфункция иммунной системы с развитием оппортунистической инфекции.
 Вопрос о генетической предрасположенности к саркоме Капоши также изучался всесторонне. Так, было установлено, что у молодых итальянцев и евреев со СПИД-ассоциированной саркомой Капоши и в определенных регионах Африки при эндемической ее форме имеет место кластерное распределение болезни, что свидетельствует о генетической предрасположенности. Также было показано, что частота саркомы коррелирует с HLA DR 5 у итальянцев и евреев и HLA DR 2 удругих европейцев (Safai B. еt al. , 1991). Но число случаев саркомы Капоши среди членов одной семьи не велико и нет менделевского принципа ее наследования на популяционном уровне. Нет на популяционном уровне и зависимостираспространения саркомы Капоши с принадлежностью HLA. Патогенетический цикл развития СПИД-ассоциированной саркомы Капоши состоит из ряда последовательных превращений.
Вопрос о генетической предрасположенности к саркоме Капоши также изучался всесторонне. Так, было установлено, что у молодых итальянцев и евреев со СПИД-ассоциированной саркомой Капоши и в определенных регионах Африки при эндемической ее форме имеет место кластерное распределение болезни, что свидетельствует о генетической предрасположенности. Также было показано, что частота саркомы коррелирует с HLA DR 5 у итальянцев и евреев и HLA DR 2 удругих европейцев (Safai B. еt al. , 1991). Но число случаев саркомы Капоши среди членов одной семьи не велико и нет менделевского принципа ее наследования на популяционном уровне. Нет на популяционном уровне и зависимостираспространения саркомы Капоши с принадлежностью HLA. Патогенетический цикл развития СПИД-ассоциированной саркомы Капоши состоит из ряда последовательных превращений.
 Необходима генетическая предрасположенность, иммунная недостаточность (больные ВИЧ, инфекцией, старость при классической саркоме Капоши, малярия или другие хронические инфекции и инвазии у жителей Африки, лекарственная иммуносупрессия после пересадки органов). При наличии иммунодефицита HHV 8 активизируется, приводя к серии изменений, приводящих в конечном результате к трансформации нормальных клеток эндотелия сосудов в злокачественные, к опухолевомуросту. HHV 8 несет несколько вирусных генов (вирусный циклин D ген, вирусный ИЛ-6 и др. ) которые теоретически могут вести к нарушению регуляции клеточного цикла.
Необходима генетическая предрасположенность, иммунная недостаточность (больные ВИЧ, инфекцией, старость при классической саркоме Капоши, малярия или другие хронические инфекции и инвазии у жителей Африки, лекарственная иммуносупрессия после пересадки органов). При наличии иммунодефицита HHV 8 активизируется, приводя к серии изменений, приводящих в конечном результате к трансформации нормальных клеток эндотелия сосудов в злокачественные, к опухолевомуросту. HHV 8 несет несколько вирусных генов (вирусный циклин D ген, вирусный ИЛ-6 и др. ) которые теоретически могут вести к нарушению регуляции клеточного цикла.
 Эпидемиология. Заболеваемость саркомой Капоши росла драматические в первое десятилетие пандемии, главным образом у мужчин-гомосексуалистов. ВИЧ-инфекции, в последние 5 лет она стала встречаться значительно реже. Снижение ее совпадает с ростом применения комбинации антиретровирусной терапии, в частности внедрения ингибиторов протеаз. В исследованиях, проведенных в Сан-Франциско при обследовании 60704 мужчин-гомосексуалистов Buchbinder et al. (1997) показано, что с внедрением комбинированной высокоактивной антиретровирусной терапии индекс СПИД-диагнозов СПИД на 100 больных снизился с 17, 6 в 1993 до 1, 7 в 1996 году и одновременно существенно снизилась встречаемость саркомы Капоши с 3 на 100 инфицированных до 0 в 1996 году. Сходные данные получили другие авторы: в 1985 году число больных с саркомой Капоши составило 25, 6 на 100 больных, в 1996 году – 7, 5 из 5622 больных гомо/бисексуалистов. Следовательно, заболеваепмость саркомой Капоши у больных ВИЧ-инфекцией значительно снизилась и снижение совпадает с масштабами применения высокоактивной антиретровирусной терапии гомо/бисексуалистов
Эпидемиология. Заболеваемость саркомой Капоши росла драматические в первое десятилетие пандемии, главным образом у мужчин-гомосексуалистов. ВИЧ-инфекции, в последние 5 лет она стала встречаться значительно реже. Снижение ее совпадает с ростом применения комбинации антиретровирусной терапии, в частности внедрения ингибиторов протеаз. В исследованиях, проведенных в Сан-Франциско при обследовании 60704 мужчин-гомосексуалистов Buchbinder et al. (1997) показано, что с внедрением комбинированной высокоактивной антиретровирусной терапии индекс СПИД-диагнозов СПИД на 100 больных снизился с 17, 6 в 1993 до 1, 7 в 1996 году и одновременно существенно снизилась встречаемость саркомы Капоши с 3 на 100 инфицированных до 0 в 1996 году. Сходные данные получили другие авторы: в 1985 году число больных с саркомой Капоши составило 25, 6 на 100 больных, в 1996 году – 7, 5 из 5622 больных гомо/бисексуалистов. Следовательно, заболеваепмость саркомой Капоши у больных ВИЧ-инфекцией значительно снизилась и снижение совпадает с масштабами применения высокоактивной антиретровирусной терапии гомо/бисексуалистов
 Клиника. Течение саркомы Капоши подразделяется на несколько стадий (табл. 35). В 92% саркома Капоши проявляется локализацией на коже. Патологический процесс у больных ВИЧ-инфекцией в начальной фазе локализован, но по мере прогрессирования СПИДа саркома приобретает генерализованный характер
Клиника. Течение саркомы Капоши подразделяется на несколько стадий (табл. 35). В 92% саркома Капоши проявляется локализацией на коже. Патологический процесс у больных ВИЧ-инфекцией в начальной фазе локализован, но по мере прогрессирования СПИДа саркома приобретает генерализованный характер
 Таблица 35. Клинические проявления при саркоме Капоши Стадия Характер поражения Стадия 1 Кожные проявления, локализованное торпидное течение (классическое) Стадия II Кожные проявления, локализованное агрессивное течение с увеличением или без увеличения лимфатических узлов (африканский локализованный агрессивный вариант) Стадия III Генерализованные кожные проявления и/или поражение лимфатических узлов (африканская лимфаденопатия и эндемический вариант) Стадия IV Висцеральные проявления (эпидемический вариант) Подтипы: А. Нет общих проявлений В. Общие проявления: уменьшение массы тела на 10% и свыше и повышение температуры или высокая стойкая лихорадка
Таблица 35. Клинические проявления при саркоме Капоши Стадия Характер поражения Стадия 1 Кожные проявления, локализованное торпидное течение (классическое) Стадия II Кожные проявления, локализованное агрессивное течение с увеличением или без увеличения лимфатических узлов (африканский локализованный агрессивный вариант) Стадия III Генерализованные кожные проявления и/или поражение лимфатических узлов (африканская лимфаденопатия и эндемический вариант) Стадия IV Висцеральные проявления (эпидемический вариант) Подтипы: А. Нет общих проявлений В. Общие проявления: уменьшение массы тела на 10% и свыше и повышение температуры или высокая стойкая лихорадка
 Еще до развития пандемии ВИЧ-инфекции J. F. Taylor et al. (1971) предложили классификационные варианты саркомы Капоши, сохранившие свое значение и сегодня (табл. 37). Хотя преимущественно саркома локализуется на коже, но нередко вовлекаются в процесс и другие органы и ткани (табл. 38 ).
Еще до развития пандемии ВИЧ-инфекции J. F. Taylor et al. (1971) предложили классификационные варианты саркомы Капоши, сохранившие свое значение и сегодня (табл. 37). Хотя преимущественно саркома локализуется на коже, но нередко вовлекаются в процесс и другие органы и ткани (табл. 38 ).
 Таблица 37. Классификация саркомы Капоши по J. F. Taylor et al. (1971) Клинический тип опухоли кожи Характеристика Возр аст Вовлечение тип опухоли костей, лимфоузлов, кожи Узловая болезненная > 25 редко Цветущая (экзофитная) локально агрессивная > 25 часто Инфильтративная локально агрессивная > 25 редко Лимфаденопатическа я распространенно агрессивная < 25 постоянно
Таблица 37. Классификация саркомы Капоши по J. F. Taylor et al. (1971) Клинический тип опухоли кожи Характеристика Возр аст Вовлечение тип опухоли костей, лимфоузлов, кожи Узловая болезненная > 25 редко Цветущая (экзофитная) локально агрессивная > 25 часто Инфильтративная локально агрессивная > 25 редко Лимфаденопатическа я распространенно агрессивная < 25 постоянно
 Клинически при саркоме Капоши у ВИЧ- больных в 2/3 случаев поражение кожи (рис. 11) носят распространенный характер, у 61% больных имеет место генерализованное вовлечение в патологический процесс лимфатический узлов, в 45% поражен желудочно-кишечный тракт. В стадии СПИДа саркома нередко поражает внутренние органы.
Клинически при саркоме Капоши у ВИЧ- больных в 2/3 случаев поражение кожи (рис. 11) носят распространенный характер, у 61% больных имеет место генерализованное вовлечение в патологический процесс лимфатический узлов, в 45% поражен желудочно-кишечный тракт. В стадии СПИДа саркома нередко поражает внутренние органы.
 Таблица 38. Топография и проявления саркомы Капоши у больных СПИДом Проявления встречаемость, % Поражения кожи: отсутствуют 8 локализованные 27 генерализованные 63 локализованные, прогрессирующие 2 Вовлечение в процесс лимфатических узлов: отсутствует 39 генерализованное 61 Спленомегалия 10 Вовлечение в патологический процесс внутренних органов и тканей: костей 2 печень 10 легкие 10 желудочно-кишечный тракт 45 Общие реакции: повышение температуры и падение массы тела 18 только повышение температуры 8 только потеря массы тела
Таблица 38. Топография и проявления саркомы Капоши у больных СПИДом Проявления встречаемость, % Поражения кожи: отсутствуют 8 локализованные 27 генерализованные 63 локализованные, прогрессирующие 2 Вовлечение в процесс лимфатических узлов: отсутствует 39 генерализованное 61 Спленомегалия 10 Вовлечение в патологический процесс внутренних органов и тканей: костей 2 печень 10 легкие 10 желудочно-кишечный тракт 45 Общие реакции: повышение температуры и падение массы тела 18 только повышение температуры 8 только потеря массы тела
 Прогностическими критериями клинического течения болезни могут быть гематокрит, уровень Т-лимфоцитов и в первую очередь CD 4+ клеток, соотношение CD 4/CD 8, уровень альфа-нтерферона (табл. 39). Наряду с клиникой в оценке прогноза течения саркомы Капоши помогает характеристика Т-хелперной субпопуляции лимфоцитов (табл. 40 ).
Прогностическими критериями клинического течения болезни могут быть гематокрит, уровень Т-лимфоцитов и в первую очередь CD 4+ клеток, соотношение CD 4/CD 8, уровень альфа-нтерферона (табл. 39). Наряду с клиникой в оценке прогноза течения саркомы Капоши помогает характеристика Т-хелперной субпопуляции лимфоцитов (табл. 40 ).
 Таблица 39. Прогностические факторы при эпидемической саркоме Капоши Клинические проявления Показатели Степень выраженности болезни Гематокрит Вовлечение в патологический процесс висцеральных органов Абсолютное содержание Т-хелперов Симптомы общего поражения организма (потеря массы тела, повышение температуры) Соотношение Тх/Тс Предшевствовавшая или присоединившаяся оппортунистическая инфекция Альфа-интерферон
Таблица 39. Прогностические факторы при эпидемической саркоме Капоши Клинические проявления Показатели Степень выраженности болезни Гематокрит Вовлечение в патологический процесс висцеральных органов Абсолютное содержание Т-хелперов Симптомы общего поражения организма (потеря массы тела, повышение температуры) Соотношение Тх/Тс Предшевствовавшая или присоединившаяся оппортунистическая инфекция Альфа-интерферон
 Таблица 40. Показатели Т-клеток у больных саркомой Капоши П р о г н о з Хорош ий Удовлетворит ельный Плохой Т-хелперы (в 1 мкл) (у выживших более 12 мес. ) >300 (85%) 300 -100 0, 5 (95%) 0, 5 — 0, 2 < 0, 2 (25%)
Таблица 40. Показатели Т-клеток у больных саркомой Капоши П р о г н о з Хорош ий Удовлетворит ельный Плохой Т-хелперы (в 1 мкл) (у выживших более 12 мес. ) >300 (85%) 300 -100 0, 5 (95%) 0, 5 — 0, 2 < 0, 2 (25%)
 Лечение. Сегодня имеется достаточно много химиопрепаратов, рекомендуемых для лечения саркомы Капоши у больных СПИДом (табл. 41), хотя эффект от терапии не всегда удовлетворителен, а главное, на фоне имимиунодефицита даже положительный терапевтический эффект при лечении саркомы не определеяет исход болезни.
Лечение. Сегодня имеется достаточно много химиопрепаратов, рекомендуемых для лечения саркомы Капоши у больных СПИДом (табл. 41), хотя эффект от терапии не всегда удовлетворителен, а главное, на фоне имимиунодефицита даже положительный терапевтический эффект при лечении саркомы не определеяет исход болезни.
 Таблица 41. Эффективность терапии эпидемической саркомы Капоши Лечение Эффект, % Химиотерапия: винбластин 26 этопозид 76 винкристин 61 блеомицин 77 винкристин+винбластин 45 блеомицин+винбластин 62 винбластин+метотрексат 77 доксорубицин+блеомицин+винбластин 66 —
Таблица 41. Эффективность терапии эпидемической саркомы Капоши Лечение Эффект, % Химиотерапия: винбластин 26 этопозид 76 винкристин 61 блеомицин 77 винкристин+винбластин 45 блеомицин+винбластин 62 винбластин+метотрексат 77 доксорубицин+блеомицин+винбластин 66 —
 Выбор терапии зависит от формы болезни, локализации процесса, общей характеристики ВИЧ-инфекции. Местное лечение в основном преследует контроль общей эффективности, улучшения внешнего вида больного. В виде местной терапии проводится удаление хирургически путем опухоли, введения в нее винбластина, электрокоагуляции. Радиотерапия при классическом варианте саркомы Капоши применялась часто и используется при СПИД-ассоциированной форме саркомы. Дозы и виды облучения, техника разнообразны от широкопольного облучения при инфильтративной форме саркомы до местного облучения при анатомически неудобных локализациях (лицо, полость рта). Полной регрессии удается добиться в 68 % , только у 9% больных местно процесс прогрессировал (Cooper J. et al. , 1991). Но этот вид терапии дорогостоящий и требует длительного времени. Применение винбластина путем введения в опухоль у 190 больных дало положительный эффект в 13%, частичный — у 78% больных (Newmman S. , 1988). Системная химиотерапия раньше использовалась редко, так классическая саркома Капоши с хорошим результатом лечилась местно. Агрессивный характер СПИД-ассоциируемой саркомы, особенно с вовлечением в процесс лимфатических узлов и висцеральных органов обусловливают необходимость проведения системной химиотерапии.
Выбор терапии зависит от формы болезни, локализации процесса, общей характеристики ВИЧ-инфекции. Местное лечение в основном преследует контроль общей эффективности, улучшения внешнего вида больного. В виде местной терапии проводится удаление хирургически путем опухоли, введения в нее винбластина, электрокоагуляции. Радиотерапия при классическом варианте саркомы Капоши применялась часто и используется при СПИД-ассоциированной форме саркомы. Дозы и виды облучения, техника разнообразны от широкопольного облучения при инфильтративной форме саркомы до местного облучения при анатомически неудобных локализациях (лицо, полость рта). Полной регрессии удается добиться в 68 % , только у 9% больных местно процесс прогрессировал (Cooper J. et al. , 1991). Но этот вид терапии дорогостоящий и требует длительного времени. Применение винбластина путем введения в опухоль у 190 больных дало положительный эффект в 13%, частичный — у 78% больных (Newmman S. , 1988). Системная химиотерапия раньше использовалась редко, так классическая саркома Капоши с хорошим результатом лечилась местно. Агрессивный характер СПИД-ассоциируемой саркомы, особенно с вовлечением в процесс лимфатических узлов и висцеральных органов обусловливают необходимость проведения системной химиотерапии.

 Правда, наличие анемии, оппортунистической инфекции, иммунодефицита ограничивают масштабы и завершенность ее применения у всех нуждающихся больных. Тем не менее она применяется в виде монотерапии при сравнительно умеренно выраженных вариантах клиники и комбинированная химиотерапия — при выраженных. Успех удается добиться у 26 -76% больных (Glaspy G. et al. , 1986; Schaart F. et al. , 1991). Лучшие результаты (88%) получены применении малых доз адриамицина, блеомицина и винкристина (Gill P. S. et al. , 1991). Оппортунистическая инфекция в этой группе развилась в 25% против 61% в группах больных, которым эти лекарственные препараты давали в стандартных дозах. В последние годы в арсенал терапевтических средств при саркоме Капоши включают иммуномодуляторы. В частности альфа-интерферон и стимуляторы эндогенного интерферона. Эффект лечения зависит от состояния иммунной системы: при низких показателях СD 4+ клеток периферической крови эффект часто минимален или отсутствует. Снижает эффективность лечения анемия, при выраженной клинике оппортунистической инфекции
Правда, наличие анемии, оппортунистической инфекции, иммунодефицита ограничивают масштабы и завершенность ее применения у всех нуждающихся больных. Тем не менее она применяется в виде монотерапии при сравнительно умеренно выраженных вариантах клиники и комбинированная химиотерапия — при выраженных. Успех удается добиться у 26 -76% больных (Glaspy G. et al. , 1986; Schaart F. et al. , 1991). Лучшие результаты (88%) получены применении малых доз адриамицина, блеомицина и винкристина (Gill P. S. et al. , 1991). Оппортунистическая инфекция в этой группе развилась в 25% против 61% в группах больных, которым эти лекарственные препараты давали в стандартных дозах. В последние годы в арсенал терапевтических средств при саркоме Капоши включают иммуномодуляторы. В частности альфа-интерферон и стимуляторы эндогенного интерферона. Эффект лечения зависит от состояния иммунной системы: при низких показателях СD 4+ клеток периферической крови эффект часто минимален или отсутствует. Снижает эффективность лечения анемия, при выраженной клинике оппортунистической инфекции
 Получены убедительные данные, что активная антиретровирусная терапия (тритерапия) оказывает лечебный и профилактический эффект и против саркомы Капоши. Весьма эффективны липосомальные антрациклины. Так доксил (липосомальный доксорубицин) вызывает ремиссию у 43% больных при курсе 20 мг/м кв. в вену каждые 2 недели. Дауноксом (липосомальный даунорубицин) вызывает ремиссию у 28% больных при введении в вену по 40 мг/ кв. м. каждые 2 недели. Терапия дауноксом также эффективна, а доксилом более эффективна. чем “золотой стандарт” — адриамицин, блеомицин и винкристин, использунемые в комбинации. Паклитаксел (таксол) лицензирован в США в 1997 году для лечения рецидивов саркомы Капоши как чрезвычайно эффективный препарат. Лечение проводят инфузионно по 100 мг/ кв. м. с введением каждые 2 недели. У 57% больных имеется частичная ремиссия и у 2% полная ремиссия. Препарат умеренно токсичен: у 61% больных значительная нейтропения, у 87% — анемия (Levine A. , 1998).
Получены убедительные данные, что активная антиретровирусная терапия (тритерапия) оказывает лечебный и профилактический эффект и против саркомы Капоши. Весьма эффективны липосомальные антрациклины. Так доксил (липосомальный доксорубицин) вызывает ремиссию у 43% больных при курсе 20 мг/м кв. в вену каждые 2 недели. Дауноксом (липосомальный даунорубицин) вызывает ремиссию у 28% больных при введении в вену по 40 мг/ кв. м. каждые 2 недели. Терапия дауноксом также эффективна, а доксилом более эффективна. чем “золотой стандарт” — адриамицин, блеомицин и винкристин, использунемые в комбинации. Паклитаксел (таксол) лицензирован в США в 1997 году для лечения рецидивов саркомы Капоши как чрезвычайно эффективный препарат. Лечение проводят инфузионно по 100 мг/ кв. м. с введением каждые 2 недели. У 57% больных имеется частичная ремиссия и у 2% полная ремиссия. Препарат умеренно токсичен: у 61% больных значительная нейтропения, у 87% — анемия (Levine A. , 1998).
 Единого подхода к терапии больных нет, но предпочтение отдается монотерапии перед политерапией, к последней рекомендуется прибегать после отсутствия эффекта от применения одного лекарственного препарата. Лимфома. Среди злокачествнных форм поражения лимфоидной ткани выделяются лимфогранулематоз (син. Болезнь Ходжкина) и неходжкинские лимфомы (син: лимфосаркомы). Под лимфомой понимают опухоли, исходящие из лимфоидной ткани, а по типу роста нодулярные и диффузные, причем первые часто трансформируются во вторые. По клеточному составу диффузные лимфомы дифференцируются на небластные, включающие лимфоцитарные, пролимфоцитарные, лимфоплазмоцитарные клетки и бластные, представленные лимфобластами иммунобластами (табл. 42). В последней группе при ВИЧ-инфекции наибольший интерес представляют лимфома Беркитта (африканская лимфома), этиологически связанная с вирусом Эпштейна-Барр, как все бластные лимфомы, характеризующаяся злокачественным течением и быстрой генерализацией.
Единого подхода к терапии больных нет, но предпочтение отдается монотерапии перед политерапией, к последней рекомендуется прибегать после отсутствия эффекта от применения одного лекарственного препарата. Лимфома. Среди злокачествнных форм поражения лимфоидной ткани выделяются лимфогранулематоз (син. Болезнь Ходжкина) и неходжкинские лимфомы (син: лимфосаркомы). Под лимфомой понимают опухоли, исходящие из лимфоидной ткани, а по типу роста нодулярные и диффузные, причем первые часто трансформируются во вторые. По клеточному составу диффузные лимфомы дифференцируются на небластные, включающие лимфоцитарные, пролимфоцитарные, лимфоплазмоцитарные клетки и бластные, представленные лимфобластами иммунобластами (табл. 42). В последней группе при ВИЧ-инфекции наибольший интерес представляют лимфома Беркитта (африканская лимфома), этиологически связанная с вирусом Эпштейна-Барр, как все бластные лимфомы, характеризующаяся злокачественным течением и быстрой генерализацией.
 Таблица 42. Гистологическая характеристика неходжкинских лимфом (по Nadler L. M. , 1993) Характеристика злокачественности лимфоцитов Характер клеток Уд. вес клеток, % В-кле тки Т-кле тки Слабая степень А. малые лимфоциты Диффузная форма, дифференцированные лимфоциты 98 2 В. фолликулы, в основном из малых лимфоцитов Узловая форма, недифференцированные лимфоциты 100 С. фолликулы из смешанных малых и больших клеток Узловая форма, смешанные лимфоциты-гистиоциты 100 Средняя степень Д. фолликулы, в основном из больших клеток Узловая форма, гистиоциты 100 Е. диффузное распространение маленьких лимфоцитов Диффузная форма, недифференцированные лимфоциты 80 20 Ж. диффузное распространение смешанных маленьких и больших клеток Диффузная форма, лимфоциты-гистиоциты 90 10 З. Диффузное распространение, большие клетки Диффузная форма, гистиоциты 80 20 Высокая степень И. Большие иммунобласты Диффузная форма, гистиоциты 80 20 К. Лимфобласты Диффузная форма, лимфобласты 10 90 Л. Малые незрелые клетки, Беркетта Диффузная форма, недифференцированные клетки
Таблица 42. Гистологическая характеристика неходжкинских лимфом (по Nadler L. M. , 1993) Характеристика злокачественности лимфоцитов Характер клеток Уд. вес клеток, % В-кле тки Т-кле тки Слабая степень А. малые лимфоциты Диффузная форма, дифференцированные лимфоциты 98 2 В. фолликулы, в основном из малых лимфоцитов Узловая форма, недифференцированные лимфоциты 100 С. фолликулы из смешанных малых и больших клеток Узловая форма, смешанные лимфоциты-гистиоциты 100 Средняя степень Д. фолликулы, в основном из больших клеток Узловая форма, гистиоциты 100 Е. диффузное распространение маленьких лимфоцитов Диффузная форма, недифференцированные лимфоциты 80 20 Ж. диффузное распространение смешанных маленьких и больших клеток Диффузная форма, лимфоциты-гистиоциты 90 10 З. Диффузное распространение, большие клетки Диффузная форма, гистиоциты 80 20 Высокая степень И. Большие иммунобласты Диффузная форма, гистиоциты 80 20 К. Лимфобласты Диффузная форма, лимфобласты 10 90 Л. Малые незрелые клетки, Беркетта Диффузная форма, недифференцированные клетки
 Лимфома – вторая по частоте опухоль у больных ВИЧ-инфекцией, встречается в 3 -4%. Этот вид опухолей – более поздние проявление болезни и примерно 12 -16% больных в стадии СПИД умирают от лимфомы. В отличие от саркомы Капоши лимфома не связана с какой-либо группой риска. Из 53 042 больных в стадии СПИДа 21 стран мира лимфома развилась у 2, 6% инъекционных наркоманов, 3, 2% трансфузионных рецепиентов, 3, 4% мужчин-гомосексуалистов, 3, 9% больных гемофилией, 2, 6% больных, заразившихся при гетеросексуальном контакте (Levine A. , 1998). Есть мнение, что азидотимидин индуцирует развитие лимфомы, хотя нельзя исключить. что под влиянием терапии АЗТ больные чаще доживают до развития лимфомы. Пока не установлено, снижает ли развитие ее активная антиретровирусная терапия.
Лимфома – вторая по частоте опухоль у больных ВИЧ-инфекцией, встречается в 3 -4%. Этот вид опухолей – более поздние проявление болезни и примерно 12 -16% больных в стадии СПИД умирают от лимфомы. В отличие от саркомы Капоши лимфома не связана с какой-либо группой риска. Из 53 042 больных в стадии СПИДа 21 стран мира лимфома развилась у 2, 6% инъекционных наркоманов, 3, 2% трансфузионных рецепиентов, 3, 4% мужчин-гомосексуалистов, 3, 9% больных гемофилией, 2, 6% больных, заразившихся при гетеросексуальном контакте (Levine A. , 1998). Есть мнение, что азидотимидин индуцирует развитие лимфомы, хотя нельзя исключить. что под влиянием терапии АЗТ больные чаще доживают до развития лимфомы. Пока не установлено, снижает ли развитие ее активная антиретровирусная терапия.
 Этиология и патогенез. Лимфома формируется в результате длительной стимуляции и пролиферации В-клеток. Она может быть индуцирована самим ВИЧ и приводить к поликлональной гипергаммаглобулинемии, хараектерной для ВИЧ-инфекции, так же как и к реактивной лимфаденопатии. При генерализованной лимфаденопатии формируется В-клеточная гиперплазия. Помимо прямого эффекта на В-клетки ВИЧ может также проявить свои эффекты косвенно, индуцируя синтез цитокинов ВИЧ-инфицированными моноцитами и Т-клетками: продукцию ИЛ-6, ИЛ-10. Последние индуцируют пролиферацию В-клеток. Кроме того эти цитокины функционируют как факторы роста В-клеточной лимфомы, а ИЛ-10 является также мощным аутокринным фактором роста. В результате иммуносупресии развивается суперинфекция, обусловленная вирусом Эпштейна-Барр. В этих условиях возможны также генетические “ошибки”, что ведет к моноклональной В-клеточное лимфомы. Наиболее вероятной первопричиной иммунобластной лимфрмы является вирус Эпштейна-Барр (EBV), ДНК которого постоянно обнаруживается в клетках опухоли. Установлена способность латентного мембранного белка вируса присоединяться к клеткам, давая сигнал к их делению.
Этиология и патогенез. Лимфома формируется в результате длительной стимуляции и пролиферации В-клеток. Она может быть индуцирована самим ВИЧ и приводить к поликлональной гипергаммаглобулинемии, хараектерной для ВИЧ-инфекции, так же как и к реактивной лимфаденопатии. При генерализованной лимфаденопатии формируется В-клеточная гиперплазия. Помимо прямого эффекта на В-клетки ВИЧ может также проявить свои эффекты косвенно, индуцируя синтез цитокинов ВИЧ-инфицированными моноцитами и Т-клетками: продукцию ИЛ-6, ИЛ-10. Последние индуцируют пролиферацию В-клеток. Кроме того эти цитокины функционируют как факторы роста В-клеточной лимфомы, а ИЛ-10 является также мощным аутокринным фактором роста. В результате иммуносупресии развивается суперинфекция, обусловленная вирусом Эпштейна-Барр. В этих условиях возможны также генетические “ошибки”, что ведет к моноклональной В-клеточное лимфомы. Наиболее вероятной первопричиной иммунобластной лимфрмы является вирус Эпштейна-Барр (EBV), ДНК которого постоянно обнаруживается в клетках опухоли. Установлена способность латентного мембранного белка вируса присоединяться к клеткам, давая сигнал к их делению.
 К ко-факторам быстрого прогрессирования лимфомы относятся: число CD 4+ клеток < 100 в мкл; возраст старше 35 лет; анамнез инъекционного наркомана; III или IV стадия ВИЧ-инфекции. Средняя продолжительность жизни больных с 2 или 3 такими факторами в среднем составляет 45 недель против 18 недель у больных с 3 и более плохих прогностических факторов. В 1985 году СDС приводит первые данные о неходжкинской лимфоме у больных ВИЧ-инфекцией. Последующие исследования показали, что риск развития лимфомы у больных СПИДом в 100 раз выше, чем в популяции в целом. Среди факторов, предрасполагающих к высокому риску развития злокачественных лимфома преобладают состояния с иммунодефицитами (табл. 43).
К ко-факторам быстрого прогрессирования лимфомы относятся: число CD 4+ клеток < 100 в мкл; возраст старше 35 лет; анамнез инъекционного наркомана; III или IV стадия ВИЧ-инфекции. Средняя продолжительность жизни больных с 2 или 3 такими факторами в среднем составляет 45 недель против 18 недель у больных с 3 и более плохих прогностических факторов. В 1985 году СDС приводит первые данные о неходжкинской лимфоме у больных ВИЧ-инфекцией. Последующие исследования показали, что риск развития лимфомы у больных СПИДом в 100 раз выше, чем в популяции в целом. Среди факторов, предрасполагающих к высокому риску развития злокачественных лимфома преобладают состояния с иммунодефицитами (табл. 43).
 Таблица 43. Заболевания, ассоциирующиеся с высоким риском развития лимфом I. Наследственные иммунодефициты синдром Клейнфельта синдром Чидиак-Хигаши атаксия-телеангиэкиазия синдром Вискотт-Элдрич II. Приобретенные иммунодефициты ятрогенная иммуносупрессия СПИД приобретенная гипогаммаглобулинемия III. Аутоиммунные заболевания синдром Согрена ревматоидный артрит системная красная волчанка IV. Химические и другие факторы фенитоин радиация комбинация химио- и радиотерапии V. Вирусы (помимо ВИЧ) вирус Эпштейна-Барр вирус человеческого Т-клеточного лейкоза
Таблица 43. Заболевания, ассоциирующиеся с высоким риском развития лимфом I. Наследственные иммунодефициты синдром Клейнфельта синдром Чидиак-Хигаши атаксия-телеангиэкиазия синдром Вискотт-Элдрич II. Приобретенные иммунодефициты ятрогенная иммуносупрессия СПИД приобретенная гипогаммаглобулинемия III. Аутоиммунные заболевания синдром Согрена ревматоидный артрит системная красная волчанка IV. Химические и другие факторы фенитоин радиация комбинация химио- и радиотерапии V. Вирусы (помимо ВИЧ) вирус Эпштейна-Барр вирус человеческого Т-клеточного лейкоза
 Стадии болезни и локализация лимфомы у больных ВИЧ-инфекцией представлены в табл. 44. Причем первичная лимфома ЦНС встречается у 1 -3 % больных ВИЧ/СПИД и обычно развивается при количестве CD 4+лимфоцитов менее 50 в мкл.
Стадии болезни и локализация лимфомы у больных ВИЧ-инфекцией представлены в табл. 44. Причем первичная лимфома ЦНС встречается у 1 -3 % больных ВИЧ/СПИД и обычно развивается при количестве CD 4+лимфоцитов менее 50 в мкл.
 Таблица 44. Клинические проявления СПИД-ассоциированной лимфомы ( по Levint A. M, 1988) Стадии Частота, % Локализация Частота, % 1 4 Нервная система 32 2 25 Желудочно-кишечный тракт 26 3 10 Костный мозг 25 4 63 Печень 12 Почки 9 Легкие 9 Сердце 6 Надпочечники
Таблица 44. Клинические проявления СПИД-ассоциированной лимфомы ( по Levint A. M, 1988) Стадии Частота, % Локализация Частота, % 1 4 Нервная система 32 2 25 Желудочно-кишечный тракт 26 3 10 Костный мозг 25 4 63 Печень 12 Почки 9 Легкие 9 Сердце 6 Надпочечники
 Клинически при лимфоме Беркитта у половины больных выявляется первичное поражение периферических, внутригрудных, забрюшинных лимфатических узлов процесс развивается вне их, чаще в миндалинах, желудочно-кишечном тракте, коже, костях или других органах. Заболевание протекает с явлениями интоксикации, проявляющихся лихорадкой, исхуданием, ночными потами, локальным зудом, а также для клиники характерны аутоиммунная гемолитическая анемия, тромбоцитопения, экзантема. В случаях поражения лимфатических узлов чаще на шее или надключичной области лимфатические узлы увеличены в размерах, плотноэластической консистенции, подвижны, так как не спаяны с окружающей клетчаткой. При поражении лимфатических узлов средостения развивается синдром верхней полой вены (расширение вен передней грудной стенки). При поражении миндалин появляется ощущение инородного тела в горле, миндалина быстро увеличивается в размерах. При локализации лимфомы в желудке, чаще в его теле или антральной области клиника напоминает рак или язвенную болезнь. Поражение толстой кишки напоминает также клинику рака. Возможны поражения и паренхиматозных органов.
Клинически при лимфоме Беркитта у половины больных выявляется первичное поражение периферических, внутригрудных, забрюшинных лимфатических узлов процесс развивается вне их, чаще в миндалинах, желудочно-кишечном тракте, коже, костях или других органах. Заболевание протекает с явлениями интоксикации, проявляющихся лихорадкой, исхуданием, ночными потами, локальным зудом, а также для клиники характерны аутоиммунная гемолитическая анемия, тромбоцитопения, экзантема. В случаях поражения лимфатических узлов чаще на шее или надключичной области лимфатические узлы увеличены в размерах, плотноэластической консистенции, подвижны, так как не спаяны с окружающей клетчаткой. При поражении лимфатических узлов средостения развивается синдром верхней полой вены (расширение вен передней грудной стенки). При поражении миндалин появляется ощущение инородного тела в горле, миндалина быстро увеличивается в размерах. При локализации лимфомы в желудке, чаще в его теле или антральной области клиника напоминает рак или язвенную болезнь. Поражение толстой кишки напоминает также клинику рака. Возможны поражения и паренхиматозных органов.
 Лечение системной СПИД-связанной лимфомы включает поливалентную химиотерапию даже при относительно локализованной лимфоме. Первоначально использовали стандартную итенсивно-дозовую схему химиотерапии, но плоная ремисси. Я достигалась редко, а наслоение суперинфекции – частое. Применение низко-дозовой модификации с дополнительным использованием цитозин-арабинозы для защиты ЦНС позволило добиться ремиссии в 50%. Другая схема с использованием инфузии циклофосфамида (750 мг/кв. м. ), доксорубицина (50 мг/кв. м) и этопозида (240 мг/кг) в течение 4 дней, повторные курсы каждые 28 дней (всего 6 курсов) позволила добиться ремиссии в 62% (Levine A. , 1998). Комбинированное применение поливалентной химиотерапии и активной антиретровирусной терапии (циклофосфамид+диксорубицин+этопозид+саквинавир+ставудин +диданозин) повыщает частоту побочных эффектов: в 3 -4 раза увеличивается уровень мукозидов. Однако, смертность снизилась до 13% против 83% не получавших активной антиретровирусной терапии.
Лечение системной СПИД-связанной лимфомы включает поливалентную химиотерапию даже при относительно локализованной лимфоме. Первоначально использовали стандартную итенсивно-дозовую схему химиотерапии, но плоная ремисси. Я достигалась редко, а наслоение суперинфекции – частое. Применение низко-дозовой модификации с дополнительным использованием цитозин-арабинозы для защиты ЦНС позволило добиться ремиссии в 50%. Другая схема с использованием инфузии циклофосфамида (750 мг/кв. м. ), доксорубицина (50 мг/кв. м) и этопозида (240 мг/кг) в течение 4 дней, повторные курсы каждые 28 дней (всего 6 курсов) позволила добиться ремиссии в 62% (Levine A. , 1998). Комбинированное применение поливалентной химиотерапии и активной антиретровирусной терапии (циклофосфамид+диксорубицин+этопозид+саквинавир+ставудин +диданозин) повыщает частоту побочных эффектов: в 3 -4 раза увеличивается уровень мукозидов. Однако, смертность снизилась до 13% против 83% не получавших активной антиретровирусной терапии.
 Другие варианты опухолей. К СПИД-ассоциируемым опухолям также относится интраэпителиальная опухоль шейки матки и инвазивный рак шейки матки. Этиологически этот аид опухолей связвают с вирусом папилломатоза человека (HPV). На сегодня идентифицировано достаточно много типов HPV, HPV 6 и HPV 11 ассоциируются с вирусными кондиломами или с легкими диспластическими изменениями (цервикальная интраэпителиальная неоплазия – 1) и не способствуют развитию в злокачественную опухоль. В то же время HPV типов 16, 18, 31, 33 в большинстве случаев находят в клетках инвазивных карцином, а ДНК вируса интегрирован в ДНК клеток опухоли. HPV типы, вызывающие цервикальный рак, образуют определенные вирусные белки, названные Е 6 и Е 7, являющиеся фундаментальными в злокачественном преобразовании клеток. Е 6 соединяется с р53 -супрессорным геном, интактивируя его функцию, а Е 7 связывается с другим супессором опухолей – геном ретинобластомы (Rb). В результате и р53 и Rb-белки угнетают атипичных прогрессирование клеточных циклов, инактивация этих белков ведет к дисрегуляции клеточного цикла.
Другие варианты опухолей. К СПИД-ассоциируемым опухолям также относится интраэпителиальная опухоль шейки матки и инвазивный рак шейки матки. Этиологически этот аид опухолей связвают с вирусом папилломатоза человека (HPV). На сегодня идентифицировано достаточно много типов HPV, HPV 6 и HPV 11 ассоциируются с вирусными кондиломами или с легкими диспластическими изменениями (цервикальная интраэпителиальная неоплазия – 1) и не способствуют развитию в злокачественную опухоль. В то же время HPV типов 16, 18, 31, 33 в большинстве случаев находят в клетках инвазивных карцином, а ДНК вируса интегрирован в ДНК клеток опухоли. HPV типы, вызывающие цервикальный рак, образуют определенные вирусные белки, названные Е 6 и Е 7, являющиеся фундаментальными в злокачественном преобразовании клеток. Е 6 соединяется с р53 -супрессорным геном, интактивируя его функцию, а Е 7 связывается с другим супессором опухолей – геном ретинобластомы (Rb). В результате и р53 и Rb-белки угнетают атипичных прогрессирование клеточных циклов, инактивация этих белков ведет к дисрегуляции клеточного цикла.
 Ко-факторам развития цервикальтной карциномы, обусловленной HPV являются ранняя половая жизнь, большое количество сексуальных партнеров, курение, иммуносупрессия. У ВИЧ-инфицированных женщин (2015 чел. ) HPV в ПЦР выявляются в 58%, в контроле (577 ВИЧ-негативных женщин) – в 28%. Опухоли шейки матки диагностируются по данным цитологического исследования мазков цервикального канала (атипичные чешуйчатые клетки) или кольпоскопии с биопсией. Лечение цервикальных интраэпителиальных опухолей зависит от стадии развития цитологических изменений. При I cтадии возможна спонтанная регрессия , но в стадии III необходимо лечения в целях предотвращения процесса в инвазивный рак шейки матки. Эффективна комбинированная терапия. включающая криотерапию, лазер, электротерапию тех поражений, которые видны при кольпоскопии и не поражают эндоцервикс. При более обширных поражениях — хирургическое лечение – резекция. У не инфицированных ВИЧ женщин рецидивы через год встречаются в 5 -10%, у ВИЧ-инфицированных – в плоловине случаев. Поэтоиму больным дополнительно назначают 5 -фторурацил в виде мази и дифторметилорнитин через рот, а также вводят HPV-вакцину.
Ко-факторам развития цервикальтной карциномы, обусловленной HPV являются ранняя половая жизнь, большое количество сексуальных партнеров, курение, иммуносупрессия. У ВИЧ-инфицированных женщин (2015 чел. ) HPV в ПЦР выявляются в 58%, в контроле (577 ВИЧ-негативных женщин) – в 28%. Опухоли шейки матки диагностируются по данным цитологического исследования мазков цервикального канала (атипичные чешуйчатые клетки) или кольпоскопии с биопсией. Лечение цервикальных интраэпителиальных опухолей зависит от стадии развития цитологических изменений. При I cтадии возможна спонтанная регрессия , но в стадии III необходимо лечения в целях предотвращения процесса в инвазивный рак шейки матки. Эффективна комбинированная терапия. включающая криотерапию, лазер, электротерапию тех поражений, которые видны при кольпоскопии и не поражают эндоцервикс. При более обширных поражениях — хирургическое лечение – резекция. У не инфицированных ВИЧ женщин рецидивы через год встречаются в 5 -10%, у ВИЧ-инфицированных – в плоловине случаев. Поэтоиму больным дополнительно назначают 5 -фторурацил в виде мази и дифторметилорнитин через рот, а также вводят HPV-вакцину.
 Инвазивный рак шейки матки у больных ВИЧ-инфекцией женщин протекает более тяжело, чем у ВИЧ-негативных, у них быстрее развиваются метастазы: через 2 -3 мес. в 100% возникают рецидивы, а среднее время жизни составляет 9 мес. у больных ВИЧ-инфекцией и 25 мес. у ВИЧ-негативных женщин. В последние годы возросло не только число ВИЧ-инфицированных с различными опухолями, но и спектр опухолей. В том числе увеличилась встречаемость анальных карцином, болезни Ходжкина, множественной миеломы, семиномы, рака яичек, оро-фаренгиальной карциномы
Инвазивный рак шейки матки у больных ВИЧ-инфекцией женщин протекает более тяжело, чем у ВИЧ-негативных, у них быстрее развиваются метастазы: через 2 -3 мес. в 100% возникают рецидивы, а среднее время жизни составляет 9 мес. у больных ВИЧ-инфекцией и 25 мес. у ВИЧ-негативных женщин. В последние годы возросло не только число ВИЧ-инфицированных с различными опухолями, но и спектр опухолей. В том числе увеличилась встречаемость анальных карцином, болезни Ходжкина, множественной миеломы, семиномы, рака яичек, оро-фаренгиальной карциномы
 Диагностика ВИЧ-ИНФЕКЦИИ
Диагностика ВИЧ-ИНФЕКЦИИ
 Клиническая диагностика. Дифференциальный диагноз
Клиническая диагностика. Дифференциальный диагноз
 Ранняя диагностика ВИЧ-инфекции обеспечивает своевременность терапии больного и развертывание профилактических мероприятий в очаге, предупреждающих неумышленную передачу вируса от инфицированного здоровому человеку. Наконец, ранняя диагностика позволяет своевременное проведение диспансеризации, психологической помощи, социальной реабилитации. Первые успехи в терапии больных позволяют при ранней диагностике значительно продлить жизнь больным и даже надеяться на излечение. Сложность ранней диагностики, базирующейся на клинической картине заключается в неспецифичности, полиморфности симптоматики в стадии II, уже не говоря об отсутствии клиники в стадии I. Тем не менее во всех случаях немотивированной утомляемости, наличия ночных потов, головной боли, особенно на фоне кратковременной лихорадки (3 -10 дней) с температурой 38 -38, 50 С, сопровождающейся тонзиллитом, длительного диарейного синдрома, похудания за короткое время, необходимо в первую очередь исключить ВИЧ-инфекцию. Постановке диагноза в этот период помогает выявление при объективном обследовании разнообразной кожной сыпи (пятна, папулы, розеолы, гнойнички) или фурункулеза. Наличие лимфаденопатии, даже в случаях увеличения одной группы лимфатических узлов и тем более при генерализованной уже с большей долей вероятности позволяет заподозрить клинически ВИЧ-инфекцию. Для болезни особенно характерно увеличение заднешейных, подчелюстных, над- и подключичных, подмышечных и локтевых лимфатических узлов. Как правило, они увеличиваются размером до 2 -5 см в диаметре, безболезненны, плотно-эластичной консистенции, изредка сливаются в конгломерат. Весьма характерно для ВИЧ-инфекции увеличение более чем одного узла, более чем одной группы (за исключением паховых), длящееся свыше 3 мес.
Ранняя диагностика ВИЧ-инфекции обеспечивает своевременность терапии больного и развертывание профилактических мероприятий в очаге, предупреждающих неумышленную передачу вируса от инфицированного здоровому человеку. Наконец, ранняя диагностика позволяет своевременное проведение диспансеризации, психологической помощи, социальной реабилитации. Первые успехи в терапии больных позволяют при ранней диагностике значительно продлить жизнь больным и даже надеяться на излечение. Сложность ранней диагностики, базирующейся на клинической картине заключается в неспецифичности, полиморфности симптоматики в стадии II, уже не говоря об отсутствии клиники в стадии I. Тем не менее во всех случаях немотивированной утомляемости, наличия ночных потов, головной боли, особенно на фоне кратковременной лихорадки (3 -10 дней) с температурой 38 -38, 50 С, сопровождающейся тонзиллитом, длительного диарейного синдрома, похудания за короткое время, необходимо в первую очередь исключить ВИЧ-инфекцию. Постановке диагноза в этот период помогает выявление при объективном обследовании разнообразной кожной сыпи (пятна, папулы, розеолы, гнойнички) или фурункулеза. Наличие лимфаденопатии, даже в случаях увеличения одной группы лимфатических узлов и тем более при генерализованной уже с большей долей вероятности позволяет заподозрить клинически ВИЧ-инфекцию. Для болезни особенно характерно увеличение заднешейных, подчелюстных, над- и подключичных, подмышечных и локтевых лимфатических узлов. Как правило, они увеличиваются размером до 2 -5 см в диаметре, безболезненны, плотно-эластичной консистенции, изредка сливаются в конгломерат. Весьма характерно для ВИЧ-инфекции увеличение более чем одного узла, более чем одной группы (за исключением паховых), длящееся свыше 3 мес.
 Нередко в ранней фазе болезни наличие психо-неврологической симптоматики: чувство тревоги, депрессия, шаткость походки, снижение остроты зрения, судорожные припадки с признаками поражения психо-эмоциональной сферы (нарушение памяти, забывчивость, неадекватность поведения, притупление эмоций). К наиболее характерным признакам ранней стадии ВИЧ-инфекции относятся: 1. Снижение массы тела менее, чем на 10%; 2. Изменения на коже и слизистых оболочек (себорйный дерматит, фолликулит, пруриго, псориаз, грибковые поражения ногтей, рецидивирующие язвы в полости рта, некротический гингивит); 3. Опоясывающий герпес у лиц моложе 50 лет; 4. Рецидивирующие инфекции верхних дыхательных путей;
Нередко в ранней фазе болезни наличие психо-неврологической симптоматики: чувство тревоги, депрессия, шаткость походки, снижение остроты зрения, судорожные припадки с признаками поражения психо-эмоциональной сферы (нарушение памяти, забывчивость, неадекватность поведения, притупление эмоций). К наиболее характерным признакам ранней стадии ВИЧ-инфекции относятся: 1. Снижение массы тела менее, чем на 10%; 2. Изменения на коже и слизистых оболочек (себорйный дерматит, фолликулит, пруриго, псориаз, грибковые поражения ногтей, рецидивирующие язвы в полости рта, некротический гингивит); 3. Опоясывающий герпес у лиц моложе 50 лет; 4. Рецидивирующие инфекции верхних дыхательных путей;
 В промежуточной стадии болезни, характеризующейся клиникой развернутой суперинфекции, сформировавшейся в результате иммунодефицита наиболее характерны: 1. Прогрессирующее снижение массы тела свыше 10%; 2. Диарея неясного генеза, продолжающаяся свыше 1 мес. . ; 3. Кандидоз полости рта; 4. Лейкоплакия; 5. Туберкулез легких; 6. Периферическая нейропатия; 7. Локализованные формы саркомы Капоши; 8. Диссеминирующий опоясывающий герпес; 9. Тяжелая, рецидивирующая бактериальная инфекция (пневмония, синуситы, пиомиозит).
В промежуточной стадии болезни, характеризующейся клиникой развернутой суперинфекции, сформировавшейся в результате иммунодефицита наиболее характерны: 1. Прогрессирующее снижение массы тела свыше 10%; 2. Диарея неясного генеза, продолжающаяся свыше 1 мес. . ; 3. Кандидоз полости рта; 4. Лейкоплакия; 5. Туберкулез легких; 6. Периферическая нейропатия; 7. Локализованные формы саркомы Капоши; 8. Диссеминирующий опоясывающий герпес; 9. Тяжелая, рецидивирующая бактериальная инфекция (пневмония, синуситы, пиомиозит).
 Для поздней стадии, позволяющей диагностировать ВИЧ-инфекцию, или, во всяком случае, проводить дифференциальную диагностику, относятся: 1. Пневмоцистная пневмония; 2. Токсоплазмоз; 3. Криптококкоз; 4. CMV-инфекция; 5. Простой герпес; 6. Прогрессирующая многоочаговая лейкоэнцефалопатия; 7. Гистоплазмоз; 8. Кандидозный эзофагит; 9. МАК-инфекция; 10. Сальмонеллезная септицемия; 11. Внелегочной туберкулез; 12. Лимфома, саркома Капоши; 13. Кахексия; 14. ВИЧ-энцефалопатия.
Для поздней стадии, позволяющей диагностировать ВИЧ-инфекцию, или, во всяком случае, проводить дифференциальную диагностику, относятся: 1. Пневмоцистная пневмония; 2. Токсоплазмоз; 3. Криптококкоз; 4. CMV-инфекция; 5. Простой герпес; 6. Прогрессирующая многоочаговая лейкоэнцефалопатия; 7. Гистоплазмоз; 8. Кандидозный эзофагит; 9. МАК-инфекция; 10. Сальмонеллезная септицемия; 11. Внелегочной туберкулез; 12. Лимфома, саркома Капоши; 13. Кахексия; 14. ВИЧ-энцефалопатия.
 • В 1988 ВОЗ предложила в целях клинической диагностики проводить балловую оценку симптомов, имеющихся у подозреваемого на ВИЧ-инфекцию больного: • Персистирующая генерализованная лимфаденопатия 0 • Изменения на коже и слизистых оболочках1 • Снижение массы тела 1 • Выраженная утомляемость1 • Простой герпес2 • Диарея длительностью свыше 1 мес. 4 • Лихорадка длительностью свыше 1 мес. 4 • Снижение массы тела свыше 10%4 • Туберкулез легких 5 • Рецидивирующая бактериальная инфекция 5 • Лейкоплакия полости рта 5 • Стоматит, молочница рта 5 • Локализованная саркома Капоши 8 • Кахексия 12 •
• В 1988 ВОЗ предложила в целях клинической диагностики проводить балловую оценку симптомов, имеющихся у подозреваемого на ВИЧ-инфекцию больного: • Персистирующая генерализованная лимфаденопатия 0 • Изменения на коже и слизистых оболочках1 • Снижение массы тела 1 • Выраженная утомляемость1 • Простой герпес2 • Диарея длительностью свыше 1 мес. 4 • Лихорадка длительностью свыше 1 мес. 4 • Снижение массы тела свыше 10%4 • Туберкулез легких 5 • Рецидивирующая бактериальная инфекция 5 • Лейкоплакия полости рта 5 • Стоматит, молочница рта 5 • Локализованная саркома Капоши 8 • Кахексия 12 •
 При этом сумма баллов от 0 до 3 оценивается как вероятность ВИЧ-инфекции очень мала, 4 -11 баллов — заболевание вероятно, а 12 и свыше — очень вероятно. В целом клиническая диагностика ВИЧ-инфекции – это, прежде всего диагностика спектра СПИД-ассоциированной патологии у больного вторичным иммунодефицитом. Так как ВИЧ-индикаторные заболевания включают 23 нозологические формы, наиболее целесообразен синдромальный подход к диагностике. Почти всегда имеет место у больного синдром общей интоксикации (немотивированная слабость, вялость, быстрая утомляемость) развивающийся на фоне длительного субфебрилитета или лихорадки неясного генеза, чаще в ночное и утреннее время, сопровождающейся обильным потом. Постоянен синдром немотивированной генерализованной периферической лимфаденопатии, в 20% сопровождающийся гепато- спленомегалией различной степени выраженности. Один из ведущих синдромов болезни — синдром бронхо-легочной патологии, правда глубокие поражения легочной ткани в виде пневмоцистной пневмонии развиваются в далеко зашедших случаях болезни, ибо развивается пневмоцистоз на фоне глубокого иммунодефицита. Зато длительностью свыше 1 месяца синдром немотивированной диареи относится к рано появляющимся, для него характерна устойчивость к медикаментозной терапии.
При этом сумма баллов от 0 до 3 оценивается как вероятность ВИЧ-инфекции очень мала, 4 -11 баллов — заболевание вероятно, а 12 и свыше — очень вероятно. В целом клиническая диагностика ВИЧ-инфекции – это, прежде всего диагностика спектра СПИД-ассоциированной патологии у больного вторичным иммунодефицитом. Так как ВИЧ-индикаторные заболевания включают 23 нозологические формы, наиболее целесообразен синдромальный подход к диагностике. Почти всегда имеет место у больного синдром общей интоксикации (немотивированная слабость, вялость, быстрая утомляемость) развивающийся на фоне длительного субфебрилитета или лихорадки неясного генеза, чаще в ночное и утреннее время, сопровождающейся обильным потом. Постоянен синдром немотивированной генерализованной периферической лимфаденопатии, в 20% сопровождающийся гепато- спленомегалией различной степени выраженности. Один из ведущих синдромов болезни — синдром бронхо-легочной патологии, правда глубокие поражения легочной ткани в виде пневмоцистной пневмонии развиваются в далеко зашедших случаях болезни, ибо развивается пневмоцистоз на фоне глубокого иммунодефицита. Зато длительностью свыше 1 месяца синдром немотивированной диареи относится к рано появляющимся, для него характерна устойчивость к медикаментозной терапии.
 Один из синдромов ВИЧ-инфекции — волнообразно текущая артралгия неясной этиологии. К характернейшим проявлениям болезни следует отнести и синдром поражений кожи и слизистых, проявляющийся неспецифической макуло-папулезной сыпью, устойчивой к терапии стероидами экземой, стафилококковым импетиго. К дерматологическим проявлениям также относятся рецидивирующие грибковые (микоз, кандидоз, бактериальные (фолликулиты, фурункулез, гидроаденит), вирусные (герпес) поражения кожи и слизистых оболочек. Наконец, ВИЧ-инфекцию характеризуют и новообразования, в основном в виде саркомы Капоши и лимфомы, а также некоторых других видов опухолей. Наличие у пациента не менее двух клинических и двух клинико-лабораторных (лейко- лифо- нейтропения, гипогаммаглобулинемия) из числа вышеперечисленных симптомов позволяет с высокой степенью уверенности диагностировать ВИЧ-инфекцию. Но в то же время в случае выявления двух из таких весьма часто встречающихся у больных синдромов, как лихорадка и лимфаденопатия, сохраняющихся на протяжении месяца и свыше, стойкая немотивированная диарея, снижение массы тела более чем на 10% или обильные ночные поты дают основание на постановку диагноза и тщательного лабораторного обследования.
Один из синдромов ВИЧ-инфекции — волнообразно текущая артралгия неясной этиологии. К характернейшим проявлениям болезни следует отнести и синдром поражений кожи и слизистых, проявляющийся неспецифической макуло-папулезной сыпью, устойчивой к терапии стероидами экземой, стафилококковым импетиго. К дерматологическим проявлениям также относятся рецидивирующие грибковые (микоз, кандидоз, бактериальные (фолликулиты, фурункулез, гидроаденит), вирусные (герпес) поражения кожи и слизистых оболочек. Наконец, ВИЧ-инфекцию характеризуют и новообразования, в основном в виде саркомы Капоши и лимфомы, а также некоторых других видов опухолей. Наличие у пациента не менее двух клинических и двух клинико-лабораторных (лейко- лифо- нейтропения, гипогаммаглобулинемия) из числа вышеперечисленных симптомов позволяет с высокой степенью уверенности диагностировать ВИЧ-инфекцию. Но в то же время в случае выявления двух из таких весьма часто встречающихся у больных синдромов, как лихорадка и лимфаденопатия, сохраняющихся на протяжении месяца и свыше, стойкая немотивированная диарея, снижение массы тела более чем на 10% или обильные ночные поты дают основание на постановку диагноза и тщательного лабораторного обследования.
 В стадии I заболевание можно заподозрить только по симптому персистирующей генерализованной лимфаденопатии у больного из группы риска или при наличии эпиданамнеза. В стадии II (ранней или слабовыраженной) еще сохраняется соматическое благополучеие, нормальная активность. Поражения кожи и слизистых оболочек нетяжелые, рецидивирующие инфекции респираторного тракта не носят генерализованного характера, потеря массы тела не превышает 10%.
В стадии I заболевание можно заподозрить только по симптому персистирующей генерализованной лимфаденопатии у больного из группы риска или при наличии эпиданамнеза. В стадии II (ранней или слабовыраженной) еще сохраняется соматическое благополучеие, нормальная активность. Поражения кожи и слизистых оболочек нетяжелые, рецидивирующие инфекции респираторного тракта не носят генерализованного характера, потеря массы тела не превышает 10%.
 При прогрессировании болезни, переходе в стадию IIIA появляются симптомы присоединившейся вторичной вирусно-бактеральной или грибковой инфекции кожи и слизистых, хотя потеря массы тела не превышает 10%, а патологической инфекционный процесс пока поверхностный, локализован в пределах кожи и слизистых оболочек в виде опоясывающего герпеса, повторных фарингитов, синуситов и т. п. В стадии IIIБ потеря массы тела прогрессирует, появляется немотивированная диарея, длительная лихорадка, “волосатая” лейкоплакия языка, часто выявляется туберкулез легких (вообще он встречается у больных ВИЧ-инфекцией в 40 %). Инфекционные осложнения динамически развивающегося у больных иммунодефицита уже более стойкого и глубокого характера с вовлечением внутренних органов, хотя еще и без дессиминации. Поражения же кожи и слизистых оболочек более упорного течения, часто повторный или диссеминированный опоясывающий герпес, уже в этой фазе развивается саркома Капоши, пока локализованная. Стадия IIIB характеризуется генерализацией инфекционного процесса, помимо вирусных, бактериальных и грибковых поражений появляются протозойные и паразитарные заболевания, в частности пневмоцистная пневмония, атипичный микобактериоз, туберкулез с внелегочной локализацией, саркома Капоши принимает диссеминированный характер. В этой фазе нередки поражения центральной нервной системы.
При прогрессировании болезни, переходе в стадию IIIA появляются симптомы присоединившейся вторичной вирусно-бактеральной или грибковой инфекции кожи и слизистых, хотя потеря массы тела не превышает 10%, а патологической инфекционный процесс пока поверхностный, локализован в пределах кожи и слизистых оболочек в виде опоясывающего герпеса, повторных фарингитов, синуситов и т. п. В стадии IIIБ потеря массы тела прогрессирует, появляется немотивированная диарея, длительная лихорадка, “волосатая” лейкоплакия языка, часто выявляется туберкулез легких (вообще он встречается у больных ВИЧ-инфекцией в 40 %). Инфекционные осложнения динамически развивающегося у больных иммунодефицита уже более стойкого и глубокого характера с вовлечением внутренних органов, хотя еще и без дессиминации. Поражения же кожи и слизистых оболочек более упорного течения, часто повторный или диссеминированный опоясывающий герпес, уже в этой фазе развивается саркома Капоши, пока локализованная. Стадия IIIB характеризуется генерализацией инфекционного процесса, помимо вирусных, бактериальных и грибковых поражений появляются протозойные и паразитарные заболевания, в частности пневмоцистная пневмония, атипичный микобактериоз, туберкулез с внелегочной локализацией, саркома Капоши принимает диссеминированный характер. В этой фазе нередки поражения центральной нервной системы.
 Согласно рекомендациям ВОЗ, надежная клиническая диагностика ВИЧ-инфекции у взрослых и детей возможна при наличии одного из 12 СПИД-индикаторных заболевания: 1) кандидоз пищевода, трахеи, бронхов, легких; 2) внелегочной криптококкоз; 3) криптоспоридиоз с диареей более одного месяца; 4) цитомегаловирусное поражение какого-либо органа (за исключением и помимо печени, селезенки и лимфатических узлов у больного старше 1 месяца); 5) инфекция, обусловленная вирусом простого герпеса, персистирующая более 1 месяца у больного старше 1 месяца; 6) саркома Капоши у больного моложе 60 лет; 7) лимфома головного мозга у больного моложе 60 лет; 8) лимфоцитарная интерстициальная пневмония у ребенка до 13 лет, 9) диссеминированная инфекция, вызванная бактериями группы Micobacterium avium intracellulare или M. Kansassii; 10) пневмоцистная пневмония; 11) прогрессирующая многоочаговая лейкоэнцефалопатия; 12) токсоплазмоз центральной нервной системы у больных старше 1 месяца. Наличие одного из этих заболеваний позволяет диагностировать ВИЧ-инфекцию при отсутствии серологического иммуноферментного исследования крови или даже при получении серонегативного результата.
Согласно рекомендациям ВОЗ, надежная клиническая диагностика ВИЧ-инфекции у взрослых и детей возможна при наличии одного из 12 СПИД-индикаторных заболевания: 1) кандидоз пищевода, трахеи, бронхов, легких; 2) внелегочной криптококкоз; 3) криптоспоридиоз с диареей более одного месяца; 4) цитомегаловирусное поражение какого-либо органа (за исключением и помимо печени, селезенки и лимфатических узлов у больного старше 1 месяца); 5) инфекция, обусловленная вирусом простого герпеса, персистирующая более 1 месяца у больного старше 1 месяца; 6) саркома Капоши у больного моложе 60 лет; 7) лимфома головного мозга у больного моложе 60 лет; 8) лимфоцитарная интерстициальная пневмония у ребенка до 13 лет, 9) диссеминированная инфекция, вызванная бактериями группы Micobacterium avium intracellulare или M. Kansassii; 10) пневмоцистная пневмония; 11) прогрессирующая многоочаговая лейкоэнцефалопатия; 12) токсоплазмоз центральной нервной системы у больных старше 1 месяца. Наличие одного из этих заболеваний позволяет диагностировать ВИЧ-инфекцию при отсутствии серологического иммуноферментного исследования крови или даже при получении серонегативного результата.
 Не менее сложна дифференсация фаз болезни, т. е. разграничение стадий по клиническим критериям. По мнению специалистов CDC (США) наиболее объективный критерий — количество Т-хелперов, а не клинические проявления, ибо многие из этих состояний часто встречаются у лиц, не инфицированных ВИЧ. В 1991 году Центр определил, что постановка диагноза СПИД может быть в случаях, если: а) у инфицированного имеется одно из 23 СПИД-ассоциированных состояний или б) он ВИЧ-инфицирован и имеет менее 200 СD 4+ клеток/ мм. Лабораторная диагностика
Не менее сложна дифференсация фаз болезни, т. е. разграничение стадий по клиническим критериям. По мнению специалистов CDC (США) наиболее объективный критерий — количество Т-хелперов, а не клинические проявления, ибо многие из этих состояний часто встречаются у лиц, не инфицированных ВИЧ. В 1991 году Центр определил, что постановка диагноза СПИД может быть в случаях, если: а) у инфицированного имеется одно из 23 СПИД-ассоциированных состояний или б) он ВИЧ-инфицирован и имеет менее 200 СD 4+ клеток/ мм. Лабораторная диагностика
 Обследованию на ВИЧ-инфекцию в первую очередь подлежат : 1. Лица, у которых отмечается лихорадка неясного генеза, длительностью свыше 1 мес. , увеличение лимфатических узлов двух и более групп продолжительностью свыше 1 мес. , диарея длительностью свыше 1 мес. , немотивированная потеря массы тела свыше 10%, повторные пневмонии в течение одного года, рецидивирующие гнойно-бактериальные или паразитарные заболевания, чсепсис, рецидивирующая пиодермия, «волосатая» лейкоплакия языка;
Обследованию на ВИЧ-инфекцию в первую очередь подлежат : 1. Лица, у которых отмечается лихорадка неясного генеза, длительностью свыше 1 мес. , увеличение лимфатических узлов двух и более групп продолжительностью свыше 1 мес. , диарея длительностью свыше 1 мес. , немотивированная потеря массы тела свыше 10%, повторные пневмонии в течение одного года, рецидивирующие гнойно-бактериальные или паразитарные заболевания, чсепсис, рецидивирующая пиодермия, «волосатая» лейкоплакия языка;
 2. Лица с клиникой кандидозного эзофагита, кандидоза бронхов и легких, диссеминированного или внелегочного кокцидиомикоза, пневмоцистной пневмонии, внелегочного криптококкоза, криптоспоридиоза с диареей юлительностью свыше 1 мес. , цитомегаловирусного поражения внутренних органов кроме печени, селезенки, лимфатических узлов у больных старше 6 мес. , цитмегаловируснго ретинита с потерей зрения, герпетической инфекции с многоочаговыми язвами длительностью свыше 1 мес. , бронхитом, пневмонией или эзофагитом, рецидивирующего опоясывающего герпеса, дессиминированного или внелегочного гистоплазмоза, туберкулеза легких или внелегочного, изоспориоза с диареей длительностью свыше 1 мес. , распространенной или внелегочной МАК-инфекции, прогрессирующей многофокусной лейкоэнцефалопатии, токсоплазмоза мозга, сальмонеллезной септицемии, саркомы Капоши, лимфомы, лимфоидной интерстициальной пневмонии (у детей)
2. Лица с клиникой кандидозного эзофагита, кандидоза бронхов и легких, диссеминированного или внелегочного кокцидиомикоза, пневмоцистной пневмонии, внелегочного криптококкоза, криптоспоридиоза с диареей юлительностью свыше 1 мес. , цитомегаловирусного поражения внутренних органов кроме печени, селезенки, лимфатических узлов у больных старше 6 мес. , цитмегаловируснго ретинита с потерей зрения, герпетической инфекции с многоочаговыми язвами длительностью свыше 1 мес. , бронхитом, пневмонией или эзофагитом, рецидивирующего опоясывающего герпеса, дессиминированного или внелегочного гистоплазмоза, туберкулеза легких или внелегочного, изоспориоза с диареей длительностью свыше 1 мес. , распространенной или внелегочной МАК-инфекции, прогрессирующей многофокусной лейкоэнцефалопатии, токсоплазмоза мозга, сальмонеллезной септицемии, саркомы Капоши, лимфомы, лимфоидной интерстициальной пневмонии (у детей)
 Лабораторная диагностика ВИЧ-инфекции базируется на трех направлениях: а) индикация ВИЧ и его компонентов, б) выявление анти-ВИЧ, в) определение изменений в иммунной системе. Среди существующих методов лабораторной диагностики наиболее распространены серологические — выявление антител к антигенам вируса.
Лабораторная диагностика ВИЧ-инфекции базируется на трех направлениях: а) индикация ВИЧ и его компонентов, б) выявление анти-ВИЧ, в) определение изменений в иммунной системе. Среди существующих методов лабораторной диагностики наиболее распространены серологические — выявление антител к антигенам вируса.
 В состав ВИЧ входят структурные гены gag (group-specific-antigens), pol (polymerase) и env (envelope), кодирующие трансляцию белков, из которых строится вирус. Группу регуляторных генов ВИЧ составляют tat, трансактиватор всех вирусных белков, rev, регулирующий экспрессию вирусных белков, vif, являющийся вирусным инфекционным фактором, nef — негативный фактор экспрессии и vpx и vpr, функция которых пока не установлена. Ген gag кодирует белки сердцевины вируса и первичным продуктом трансляции его является р53 — белок-предшественник , расщепляющийся на три ( р15, р17 и р 24 ) или с образованием при расщеплении первоначально промежуточного белка р39, который затем расщепляется на белки р17 и р24. У ВИЧ-инфицированных в большинстве случаев образуются антитела именно к этим антигенам, причем антитела к р24 выявляются на ранней стадии инфекции, ибо р24 более иммуногенен, чем р17. Ген роl кодирует белки р51/66 и р31, представляющие собой реверстранскриптазу и эндонуклеазу вируса
В состав ВИЧ входят структурные гены gag (group-specific-antigens), pol (polymerase) и env (envelope), кодирующие трансляцию белков, из которых строится вирус. Группу регуляторных генов ВИЧ составляют tat, трансактиватор всех вирусных белков, rev, регулирующий экспрессию вирусных белков, vif, являющийся вирусным инфекционным фактором, nef — негативный фактор экспрессии и vpx и vpr, функция которых пока не установлена. Ген gag кодирует белки сердцевины вируса и первичным продуктом трансляции его является р53 — белок-предшественник , расщепляющийся на три ( р15, р17 и р 24 ) или с образованием при расщеплении первоначально промежуточного белка р39, который затем расщепляется на белки р17 и р24. У ВИЧ-инфицированных в большинстве случаев образуются антитела именно к этим антигенам, причем антитела к р24 выявляются на ранней стадии инфекции, ибо р24 более иммуногенен, чем р17. Ген роl кодирует белки р51/66 и р31, представляющие собой реверстранскриптазу и эндонуклеазу вируса
 Для выявления антител при ВИЧ-инфекции в основном используют иммуноферментный анализ (ИФА) и иммуноблотинг (ИБ). В первом случае выявляются суммарные антитела к белкам ВИЧ, во втором — к отдельным белкам (табл. 54). В основе ИФА лежит иммобилизация вирусных антигенов на планшетах, на которые сорбируются антитела больного, а комплекс антиген-антитело выявляется с помощью коньюгата антивидового иммуноглобулина с ферментом. Метод довольно специфичен (99%) и достаточно чувствителен (93 -99%), позволяет выявлять вирусспецифические антитела у 95% инфицированных. Отрицательные 5% случаев приходится на ранние этапы инфицирования, когда антител еще мало в сыворотке крови или на терминальные фазы болезни, когда организм уже не в состоянии синтезировать антитела в силу резкого истощения иммунной системы. Кроме того в ходе инфекционного процесса наблюдаются периоды исчезновения антител из крови, что также обусловливает отрицательные результаты ИФА. Наоборот, возможны ложноположительные данные ИФА, в основном у больных с аутоиммунными заболеваниями, при инфекции, вызванной вирусом Эпштейна-Барр, когда происходит перекрестная реакция антител к ревматоидному фактору, вирусу Эпштейн-Барр или к молекулам главного комплекса гистосовместимости. Встречаются подобные ложноположительные реакции в 0, 02 -0, 5% случаев.
Для выявления антител при ВИЧ-инфекции в основном используют иммуноферментный анализ (ИФА) и иммуноблотинг (ИБ). В первом случае выявляются суммарные антитела к белкам ВИЧ, во втором — к отдельным белкам (табл. 54). В основе ИФА лежит иммобилизация вирусных антигенов на планшетах, на которые сорбируются антитела больного, а комплекс антиген-антитело выявляется с помощью коньюгата антивидового иммуноглобулина с ферментом. Метод довольно специфичен (99%) и достаточно чувствителен (93 -99%), позволяет выявлять вирусспецифические антитела у 95% инфицированных. Отрицательные 5% случаев приходится на ранние этапы инфицирования, когда антител еще мало в сыворотке крови или на терминальные фазы болезни, когда организм уже не в состоянии синтезировать антитела в силу резкого истощения иммунной системы. Кроме того в ходе инфекционного процесса наблюдаются периоды исчезновения антител из крови, что также обусловливает отрицательные результаты ИФА. Наоборот, возможны ложноположительные данные ИФА, в основном у больных с аутоиммунными заболеваниями, при инфекции, вызванной вирусом Эпштейна-Барр, когда происходит перекрестная реакция антител к ревматоидному фактору, вирусу Эпштейн-Барр или к молекулам главного комплекса гистосовместимости. Встречаются подобные ложноположительные реакции в 0, 02 -0, 5% случаев.
 Таблица 54. Выявление антител к белкам, кодируемым генами ВИЧ Гены ВИЧ Белки-продуценты генов ИФА Иммуноблот Определение суммарных антител к белкам ВИЧ Определение антител к отдельным белкам GAG р15, р17, р24, р55 — II — POL р31, р51, р66 — II — ENV gp 41, gp 120, gp 160 — II —
Таблица 54. Выявление антител к белкам, кодируемым генами ВИЧ Гены ВИЧ Белки-продуценты генов ИФА Иммуноблот Определение суммарных антител к белкам ВИЧ Определение антител к отдельным белкам GAG р15, р17, р24, р55 — II — POL р31, р51, р66 — II — ENV gp 41, gp 120, gp 160 — II —
 Сравнительно высокий процент ложно-положительных реакций в ИФА в данном случае объясняется качеством тест-систем, но расхождения даже ниже, чем в экономически развитых странах. Сейчас внедряется в практику тест-системы 3 -4 поколения, в основе которых лежит использование в качестве антигена: а) лизатов ВИЧ-1, б) рекомбинантных белков ВИЧ-1, в) введение антигенов субтипа “О” ВИЧ-1, г) коньюгаты, позволяющие определять Ig. M, Ig. G, Ig. A. Все это снижает частоту ложноположительных реакций ИФА при диагностике ВИЧ-инфекции, дает возможность раннего выявления сероконверсии. Улучшение тест-систем, выпускаемых некоторыми фирмами, обусловило более высокую чувствительность, чем иммунный блот, используемый для подтверждения специфичности ИФА. Поэтому ИФА с некоторыми тест-системами может использоваться не только как метод для скрининговых исследований, но и подтверждающих. Антитела к основным внутренним белкам (р17, р24) обнаруживаются у 3/4 инфицированных и примерно у половины больных СПИДом.
Сравнительно высокий процент ложно-положительных реакций в ИФА в данном случае объясняется качеством тест-систем, но расхождения даже ниже, чем в экономически развитых странах. Сейчас внедряется в практику тест-системы 3 -4 поколения, в основе которых лежит использование в качестве антигена: а) лизатов ВИЧ-1, б) рекомбинантных белков ВИЧ-1, в) введение антигенов субтипа “О” ВИЧ-1, г) коньюгаты, позволяющие определять Ig. M, Ig. G, Ig. A. Все это снижает частоту ложноположительных реакций ИФА при диагностике ВИЧ-инфекции, дает возможность раннего выявления сероконверсии. Улучшение тест-систем, выпускаемых некоторыми фирмами, обусловило более высокую чувствительность, чем иммунный блот, используемый для подтверждения специфичности ИФА. Поэтому ИФА с некоторыми тест-системами может использоваться не только как метод для скрининговых исследований, но и подтверждающих. Антитела к основным внутренним белкам (р17, р24) обнаруживаются у 3/4 инфицированных и примерно у половины больных СПИДом.
 Иммуноблотинг используется при диагностике ВИЧ-инфекции в качестве экспертного метода. ИБ сочетает в себе определение антител к отдельным белкам вируса с предварительным электропереносом на нитроцеллюлезную полоску (стрип) антигенов. В ИБ чаще всего выявляются антитела против gp 41, обнаружение же в ИБ антител против р24 при профилактических обследованиях не дает оснований для окончательного решения вопроса об нфицировании. Используемый в последнее время рекомбинантный белок для ИБ улучшает оценку результатов. Ход лабораторной диагностики, применяемой в нашей лаборатории, предствлен на рис.
Иммуноблотинг используется при диагностике ВИЧ-инфекции в качестве экспертного метода. ИБ сочетает в себе определение антител к отдельным белкам вируса с предварительным электропереносом на нитроцеллюлезную полоску (стрип) антигенов. В ИБ чаще всего выявляются антитела против gp 41, обнаружение же в ИБ антител против р24 при профилактических обследованиях не дает оснований для окончательного решения вопроса об нфицировании. Используемый в последнее время рекомбинантный белок для ИБ улучшает оценку результатов. Ход лабораторной диагностики, применяемой в нашей лаборатории, предствлен на рис.

 По нашим данным при использовании тест-систем ведущих фирм мира у больных ВИЧ-инфекцией в иммунном блотинге во всех случаях выявляются антитела к gp 160 и лишь у трети (38, 8%) к р15 (табл. 55). Таблица 55. Выявляемость антител к белкам ВИЧ в иммунном блоте Антитела к белкам ВИЧ % выявления gp 160 100 gp 41 84, 4 gp 120 91, 1 p 31 -34 84, 4 p 65 -68 93, 3 p 24 -25 100 p 55 -52 93, 0 p 17 -18 80, 0 p 51 p 17 -18 38,
По нашим данным при использовании тест-систем ведущих фирм мира у больных ВИЧ-инфекцией в иммунном блотинге во всех случаях выявляются антитела к gp 160 и лишь у трети (38, 8%) к р15 (табл. 55). Таблица 55. Выявляемость антител к белкам ВИЧ в иммунном блоте Антитела к белкам ВИЧ % выявления gp 160 100 gp 41 84, 4 gp 120 91, 1 p 31 -34 84, 4 p 65 -68 93, 3 p 24 -25 100 p 55 -52 93, 0 p 17 -18 80, 0 p 51 p 17 -18 38,
 ВОЗ (1991) предлагает следующий принцип оценки результатов иимунного блота: а) положительный результат — обнаружение в сыворотке крови антител к двум вирусным белкам из группы env с наличием или отсутствием белков — продуцентов gag и pol; б) отрицательный результат — отсутствие каких либо антител и в) неопределенный результат — обнаружение в сыворотке крови антител к белкам из группы gag и pol. Чаще всего неопределенный результат связан с белками- продуцентами экспрессии гена gag ВИЧ-1 р15/17, р24 и р55, ибо в этих случаях возможны или инфицирование или ложноположительный результат. В подобных случаях, если обследуемый не относится к группе риска, а повторный анализ не дает нарастания титра антител, скорее всего человек не инфицирован. Окончательное же решение вопроса о диагнозе возможно только при проведении более высокочувствительных, экспертных методов исследования: пероксидазной цепной реакции, ДНК-зондов или культивирования вируса. Среди серологических методов в случае неопределенных результатов ИБ используется в качестве экспертной диагностики радиоиммуно-преципитация (РИП).
ВОЗ (1991) предлагает следующий принцип оценки результатов иимунного блота: а) положительный результат — обнаружение в сыворотке крови антител к двум вирусным белкам из группы env с наличием или отсутствием белков — продуцентов gag и pol; б) отрицательный результат — отсутствие каких либо антител и в) неопределенный результат — обнаружение в сыворотке крови антител к белкам из группы gag и pol. Чаще всего неопределенный результат связан с белками- продуцентами экспрессии гена gag ВИЧ-1 р15/17, р24 и р55, ибо в этих случаях возможны или инфицирование или ложноположительный результат. В подобных случаях, если обследуемый не относится к группе риска, а повторный анализ не дает нарастания титра антител, скорее всего человек не инфицирован. Окончательное же решение вопроса о диагнозе возможно только при проведении более высокочувствительных, экспертных методов исследования: пероксидазной цепной реакции, ДНК-зондов или культивирования вируса. Среди серологических методов в случае неопределенных результатов ИБ используется в качестве экспертной диагностики радиоиммуно-преципитация (РИП).
 В основе РИП лежит использование белков вируса, меченых радиоактивным йодом, а преципитаты выявляются с помощью бета-счетчиков. К недостаткам метода относятся дорогостоящая аппаратура, необходимость оборудования для этих целей специальных помещений. Рис. 21. Этапы лабораторной диагностики ВИЧ-инфекции Более доступен метод непрямой иммунофлюоресценции с использованием специальных клеточных линий, инфицированных ВИЧ. Чаще всего используют клеточные линии MOLT, H 9, CEM и др. Клетки фиксируют на предметных стеклах с помощью ацетон-метанола, убивающего вирус, но сохраняющего поверхностные антигены. С последними взаимодействуют антитела сыворотки инфицированного. Интерпретация серодиагностики ВИЧ-инфекции представляет иногда определенные трудности. Так, применении твердофазного ИФА (ELISA) необходимо ставить реакцию параллельно набором тестов (ELISA Biatest Mixte, ELISA Abott Mixte, ELISA Behring Mixte), ибо встречаются ситуации, когда два теста ELISA могут быть отрицательными, а третий в последующем положительным при повторном обследовании, что подтверждает диагноз ВИЧ-инфекции. Аналогичная ситуация наблюдается при использовании теста Western-Blot
В основе РИП лежит использование белков вируса, меченых радиоактивным йодом, а преципитаты выявляются с помощью бета-счетчиков. К недостаткам метода относятся дорогостоящая аппаратура, необходимость оборудования для этих целей специальных помещений. Рис. 21. Этапы лабораторной диагностики ВИЧ-инфекции Более доступен метод непрямой иммунофлюоресценции с использованием специальных клеточных линий, инфицированных ВИЧ. Чаще всего используют клеточные линии MOLT, H 9, CEM и др. Клетки фиксируют на предметных стеклах с помощью ацетон-метанола, убивающего вирус, но сохраняющего поверхностные антигены. С последними взаимодействуют антитела сыворотки инфицированного. Интерпретация серодиагностики ВИЧ-инфекции представляет иногда определенные трудности. Так, применении твердофазного ИФА (ELISA) необходимо ставить реакцию параллельно набором тестов (ELISA Biatest Mixte, ELISA Abott Mixte, ELISA Behring Mixte), ибо встречаются ситуации, когда два теста ELISA могут быть отрицательными, а третий в последующем положительным при повторном обследовании, что подтверждает диагноз ВИЧ-инфекции. Аналогичная ситуация наблюдается при использовании теста Western-Blot
 Большие трудности интерпретации результатов при перекресных реакциях и в случаях начальных стадий сероконверсии. В первой ситуации при повторном исследовании через определенный промежуток времени антитела не выявляются, а во втором в иммуноблоте появляются новые полосы, свидетельствующие о появлении антител к протеинам или гликопротеидам ВИЧ, характеризуя динамику ответной иммунной реакции на антигены вируса. В США применяется несколько тестов, позволяющих с достаточной степенью достоверности выявлять ВИЧ-инфицированных: — ELISA — тест (твердофазный иммуноферментный анализ) выявления первого уровня, характеризуется большой чувствительностью, хотя и меньшей специфичностью перед нижеследующими, — Western-blot (иммунный блотинг) — весьма специфичный и наиболее используемый тест, позволяющий дифференцировать ВИЧ-1 и ВИЧ- 2, — антигенемия р25 — тест, эффективный в начальных стадиях заражения
Большие трудности интерпретации результатов при перекресных реакциях и в случаях начальных стадий сероконверсии. В первой ситуации при повторном исследовании через определенный промежуток времени антитела не выявляются, а во втором в иммуноблоте появляются новые полосы, свидетельствующие о появлении антител к протеинам или гликопротеидам ВИЧ, характеризуя динамику ответной иммунной реакции на антигены вируса. В США применяется несколько тестов, позволяющих с достаточной степенью достоверности выявлять ВИЧ-инфицированных: — ELISA — тест (твердофазный иммуноферментный анализ) выявления первого уровня, характеризуется большой чувствительностью, хотя и меньшей специфичностью перед нижеследующими, — Western-blot (иммунный блотинг) — весьма специфичный и наиболее используемый тест, позволяющий дифференцировать ВИЧ-1 и ВИЧ- 2, — антигенемия р25 — тест, эффективный в начальных стадиях заражения
 Внедрение метода полимеразной цепной реакции существенно обогатили лабораторную диагностику вирусных инфекций, в том числе и ВИЧ-инфекции. Полимеразная цепная реакция (ПЦР) является циклическим процессом увеличения в геометрической прогрессии копии ограниченного синтетическими олигонуклеотидами (праймерами) определенного специфического фрагмента ДНК, протекающей под воздействием термостабильной ДНК-полимеразы при строго заданных температурных и временных характеристиках (White T. J. et al. , 1989). Чувствительность ПЦР зависит от специфичности, с которой олигонуклеотиды синтезируют необходимый участок ДНК по отношению к другим неспецифическим участкам нуклеиновой кислоты. Использование различных вариантов ДНК — ДНК-гибридизации с олигонуклеотидными зондами, имеющих ту или иную метку (радиоактивную, флюоресцентную и т. д. ) значительно увеличивает чувствительность и специфичность определения продуктов амплификации. Метод гибридизации нуклеиновых кислот весьма высокоспецифичен, однако без проведения амплификации не всегда чувствителен, ибо в крови не велико количество инфицированных клеток. Сочетание двух методов позволило проводить анализ с минимальным количеством материала. В ПЦР может быть использована ДНК, выделенная из свежеполученного материала (кровь, ткани), а также из замороженного, высушенного или фиксированного.
Внедрение метода полимеразной цепной реакции существенно обогатили лабораторную диагностику вирусных инфекций, в том числе и ВИЧ-инфекции. Полимеразная цепная реакция (ПЦР) является циклическим процессом увеличения в геометрической прогрессии копии ограниченного синтетическими олигонуклеотидами (праймерами) определенного специфического фрагмента ДНК, протекающей под воздействием термостабильной ДНК-полимеразы при строго заданных температурных и временных характеристиках (White T. J. et al. , 1989). Чувствительность ПЦР зависит от специфичности, с которой олигонуклеотиды синтезируют необходимый участок ДНК по отношению к другим неспецифическим участкам нуклеиновой кислоты. Использование различных вариантов ДНК — ДНК-гибридизации с олигонуклеотидными зондами, имеющих ту или иную метку (радиоактивную, флюоресцентную и т. д. ) значительно увеличивает чувствительность и специфичность определения продуктов амплификации. Метод гибридизации нуклеиновых кислот весьма высокоспецифичен, однако без проведения амплификации не всегда чувствителен, ибо в крови не велико количество инфицированных клеток. Сочетание двух методов позволило проводить анализ с минимальным количеством материала. В ПЦР может быть использована ДНК, выделенная из свежеполученного материала (кровь, ткани), а также из замороженного, высушенного или фиксированного.
 Основным клинико-лабораторным показателем диагностики СПИДа среди ВИЧ-инфицированных в повседневной жизни стало определение содержания CD 4+ лимфоцитов: уменьшение уровня ниже 200 клеток/мм является основным критерием постановки диагноза СПИД. Считается, что все ВИЧ-инфицированные лица с количеством CD 4+лимфоцитов 200 клеток/ мм и ниже нуждаются как в противовирусной терапии, так и профилактике пневмоцистной пневмонии. И хотя у 1/3 ВИЧ-инфицированных с количеством СD 4+ лимфоцитов менее 200 клеток/мм отсутствуют клинические проявления, опыт показал, что у них симптомы развиваются в ближайшие 2 месяца, поэтому они все расцениваются как больные в стадии СПИДа. В специализированных лечебных учреждениях, в странах с высоким экономическим потенциалом обычно используют комбинацию нескольких лабораторных тестов.
Основным клинико-лабораторным показателем диагностики СПИДа среди ВИЧ-инфицированных в повседневной жизни стало определение содержания CD 4+ лимфоцитов: уменьшение уровня ниже 200 клеток/мм является основным критерием постановки диагноза СПИД. Считается, что все ВИЧ-инфицированные лица с количеством CD 4+лимфоцитов 200 клеток/ мм и ниже нуждаются как в противовирусной терапии, так и профилактике пневмоцистной пневмонии. И хотя у 1/3 ВИЧ-инфицированных с количеством СD 4+ лимфоцитов менее 200 клеток/мм отсутствуют клинические проявления, опыт показал, что у них симптомы развиваются в ближайшие 2 месяца, поэтому они все расцениваются как больные в стадии СПИДа. В специализированных лечебных учреждениях, в странах с высоким экономическим потенциалом обычно используют комбинацию нескольких лабораторных тестов.
 J. W. Mellors, A. Munoz, J. V. Giorgi et al. (1997) в 4 университетских клинических центрах США с 1984 по 1985 г. наблюдали 4954 мужчины-гомосексуалиста 18 лет без клинических признаков СПИДа. Затем среди них отобрали 1813 участников с исходной серопозитивной реакцией на ВИЧ и 169 участников с сероконверсией, выявленной в течение 18 мес с момента включения в исследование. Из них только у 1604 (81%) участников число клеток CD 4+ и уровень РНК ВИЧ-1 определялись как в начале исследования, так и в ходе наблюдения. Медиана продолжительности наблюдения за участниками, у которых не развился СПИД, составила 9, 6 года. В качестве прогностических тестов определяли число лимфоцитов CD 4+, СD 3+ и СD 8+; уровень РНК ВИЧ-1, b 2 -микроглобулина и неоптерина в крови; среди клинических показателей — кандидозный стоматит или лихорадка в течение 2 или более нед. Критерием оценки являлось время до развития СПИДа и до наступления связанной с ним смерти.
J. W. Mellors, A. Munoz, J. V. Giorgi et al. (1997) в 4 университетских клинических центрах США с 1984 по 1985 г. наблюдали 4954 мужчины-гомосексуалиста 18 лет без клинических признаков СПИДа. Затем среди них отобрали 1813 участников с исходной серопозитивной реакцией на ВИЧ и 169 участников с сероконверсией, выявленной в течение 18 мес с момента включения в исследование. Из них только у 1604 (81%) участников число клеток CD 4+ и уровень РНК ВИЧ-1 определялись как в начале исследования, так и в ходе наблюдения. Медиана продолжительности наблюдения за участниками, у которых не развился СПИД, составила 9, 6 года. В качестве прогностических тестов определяли число лимфоцитов CD 4+, СD 3+ и СD 8+; уровень РНК ВИЧ-1, b 2 -микроглобулина и неоптерина в крови; среди клинических показателей — кандидозный стоматит или лихорадка в течение 2 или более нед. Критерием оценки являлось время до развития СПИДа и до наступления связанной с ним смерти.
 За время наблюдения у 998 больных развился СПИД, 855 больных умерли от него. Прогнозировать прогрессирование ВИЧ-инфекции можно было по уровням РНК ВИЧ-1, неоптерина, b 2 -микроглобулина и числу клеток CD 4+. Относительный риск развития СПИДа и смерти от него прямо коррелировал с уровнем РНК ВИЧ-1. Оценка ожидаемого клинического исхода была более точной, когда с показателем вирусной нагрузки на плазму учитывали число клеток CD 4+, . Прогностическая ценность показателей не не зависела от применения антиретровирусных препаратов. Авторы пришли к выводу, что уровень РНК ВИЧ-1 лучше всего позволяет прогнозировать клинический исход при ВИЧ-инфекции, число клеток CD 4+ в этом смысле менее информативно. Однако прогноз наиболее точен при совместном использовании двух этих показателей. Так, при уровне РНК ВИЧ-1 Ә 500 копий/мл прогрессирование ВИЧ-инфекции до СПИДа через 9 лет наблюдалось у 3, 6% больных, если число клеток CD 4+ было >650/мм 3, и у 22, 1%, если число клеток CD 4+ было менее 750/мм 3. Точно так же, если уровень РНК ВИЧ-1 превышал 30 000 копий/мл, частота прогрессирования ВИЧ-инфекции через 9 лет при исходном числе клеток CD 4+ >500, 351— 500, 201— 350 и менее 200/мм 3, была равна соответственно 76, 3%, 94, 4%, 92, 9% и 100%. Хотя 60% участников в последующем принимали антиретровирусные препараты, исходные показатели концентрации ВИЧ сохраняли свою прогностическую ценность независимо от дальнейшего лечения.
За время наблюдения у 998 больных развился СПИД, 855 больных умерли от него. Прогнозировать прогрессирование ВИЧ-инфекции можно было по уровням РНК ВИЧ-1, неоптерина, b 2 -микроглобулина и числу клеток CD 4+. Относительный риск развития СПИДа и смерти от него прямо коррелировал с уровнем РНК ВИЧ-1. Оценка ожидаемого клинического исхода была более точной, когда с показателем вирусной нагрузки на плазму учитывали число клеток CD 4+, . Прогностическая ценность показателей не не зависела от применения антиретровирусных препаратов. Авторы пришли к выводу, что уровень РНК ВИЧ-1 лучше всего позволяет прогнозировать клинический исход при ВИЧ-инфекции, число клеток CD 4+ в этом смысле менее информативно. Однако прогноз наиболее точен при совместном использовании двух этих показателей. Так, при уровне РНК ВИЧ-1 Ә 500 копий/мл прогрессирование ВИЧ-инфекции до СПИДа через 9 лет наблюдалось у 3, 6% больных, если число клеток CD 4+ было >650/мм 3, и у 22, 1%, если число клеток CD 4+ было менее 750/мм 3. Точно так же, если уровень РНК ВИЧ-1 превышал 30 000 копий/мл, частота прогрессирования ВИЧ-инфекции через 9 лет при исходном числе клеток CD 4+ >500, 351— 500, 201— 350 и менее 200/мм 3, была равна соответственно 76, 3%, 94, 4%, 92, 9% и 100%. Хотя 60% участников в последующем принимали антиретровирусные препараты, исходные показатели концентрации ВИЧ сохраняли свою прогностическую ценность независимо от дальнейшего лечения.
 Полученные результаты подчеркивают важность интерпретации результатов определения концентрации ВИЧ с учетом как клинического состояния, так и числа клеток CD 4+. Этот показатель не только помогает принять решение о времени начала антиретровирусной терапии, в других исследованиях была продемонстрирована его роль в оценке эффективности различных схем антиретровирусной терапии [Hughes M. D. , Johnson V. A. , Hirsch M. S. , et al. 1997] и в определении момента изменения лечебной тактики перед развитием клинической недостаточности [Saag M. S. , Holodniy M. , Kuritzkes D. R. , et al. 1996]. Но при использовании этого показателя следует проявлять осторожность, поскольку различные наборы реактивов для количественного определения уровня РНК ВИЧ могут давать различные результаты; кроме того, концентрацию вируса не следует определять во время или вскоре после успешного лечения ВИЧ-инфекции
Полученные результаты подчеркивают важность интерпретации результатов определения концентрации ВИЧ с учетом как клинического состояния, так и числа клеток CD 4+. Этот показатель не только помогает принять решение о времени начала антиретровирусной терапии, в других исследованиях была продемонстрирована его роль в оценке эффективности различных схем антиретровирусной терапии [Hughes M. D. , Johnson V. A. , Hirsch M. S. , et al. 1997] и в определении момента изменения лечебной тактики перед развитием клинической недостаточности [Saag M. S. , Holodniy M. , Kuritzkes D. R. , et al. 1996]. Но при использовании этого показателя следует проявлять осторожность, поскольку различные наборы реактивов для количественного определения уровня РНК ВИЧ могут давать различные результаты; кроме того, концентрацию вируса не следует определять во время или вскоре после успешного лечения ВИЧ-инфекции
 Лечение ВИЧ-инфекции
Лечение ВИЧ-инфекции
 Общие вопросы терапии больных
Общие вопросы терапии больных
 ВИЧ-инфекция в России, как и в мире в целом, продолжает набирать темпы. Показатель заболеваемости на май 2000 года составил 3 на 100 000 населения, что в 10 раз выше, чем заболеваемость брюшным тифом, выше показателей заболеваемости риккетсиозами, дифтерией, корью, иерсиниозом, примерно такая же, как заболеваемость менингококковой инфекцией, клещевым энцефалитом. На 1. 08. 00 в России зарегистрировано свыше 52 тыс. больных ВИЧ-инфекцией, в том числе свыше 23 тыс. (44% от всех инфицированных) заразились за 7 мес. 2000 года (рис. 1). В Санкт-Петербурге, далеко не лидирующем по заболеваемости городе страны, всего с начала эпидемии зарегистрировано около 2 тыс. больных, причем более 1400 – за семь месяцев 2000 года. т. е. больше, чем за предыдущие 9 лет вместе взятых. Все это свидетельствует о необходимости незамедлительно решать проблемупожизненной дорогостоящей терапии миллионов людей в мире и десятки тысяч – в нашей стране.
ВИЧ-инфекция в России, как и в мире в целом, продолжает набирать темпы. Показатель заболеваемости на май 2000 года составил 3 на 100 000 населения, что в 10 раз выше, чем заболеваемость брюшным тифом, выше показателей заболеваемости риккетсиозами, дифтерией, корью, иерсиниозом, примерно такая же, как заболеваемость менингококковой инфекцией, клещевым энцефалитом. На 1. 08. 00 в России зарегистрировано свыше 52 тыс. больных ВИЧ-инфекцией, в том числе свыше 23 тыс. (44% от всех инфицированных) заразились за 7 мес. 2000 года (рис. 1). В Санкт-Петербурге, далеко не лидирующем по заболеваемости городе страны, всего с начала эпидемии зарегистрировано около 2 тыс. больных, причем более 1400 – за семь месяцев 2000 года. т. е. больше, чем за предыдущие 9 лет вместе взятых. Все это свидетельствует о необходимости незамедлительно решать проблемупожизненной дорогостоящей терапии миллионов людей в мире и десятки тысяч – в нашей стране.
 Рис. 1. Взаимодействия при лечении ВИЧ-инфекции
Рис. 1. Взаимодействия при лечении ВИЧ-инфекции
 Целью терапии больных ВИЧ-инфекцией является максимальное и продолжительное угнетение репликации вируса, восстановление и/или сохранение функции иммунной системы, улучшение качества жизни, снижение связанной со СПИДом заболеваемости и смертности. На сегодняшнем уровне это может быть достигнуто максимальным соблюдением назначенной схемы антиретровирусной терапии, рациональной последовательностью применения препаратов, сохранением резервных схем лечения и препаратов на будущее. Хотя терапия ВИЧ-инфекции остается сложнейшей и нерешеннойпроблемой, определенные успехи, безусловно, имеют место. О наметившихся сдвигах эффективностилекарственной терапии уже в первые годы пандемии свидетельствуют следующие данные: в 1986 году свыше 70% инфицированных в ближайшие 2 года заболели СПИДом или умерли, а среди инфицированных в 1989 году — лишь 20%. ибо в практику лечения больных был внедрен первый антиретровирусный препарат – азидотимидин, ставший базисным для всех последующих схем комбинированной терапии.
Целью терапии больных ВИЧ-инфекцией является максимальное и продолжительное угнетение репликации вируса, восстановление и/или сохранение функции иммунной системы, улучшение качества жизни, снижение связанной со СПИДом заболеваемости и смертности. На сегодняшнем уровне это может быть достигнуто максимальным соблюдением назначенной схемы антиретровирусной терапии, рациональной последовательностью применения препаратов, сохранением резервных схем лечения и препаратов на будущее. Хотя терапия ВИЧ-инфекции остается сложнейшей и нерешеннойпроблемой, определенные успехи, безусловно, имеют место. О наметившихся сдвигах эффективностилекарственной терапии уже в первые годы пандемии свидетельствуют следующие данные: в 1986 году свыше 70% инфицированных в ближайшие 2 года заболели СПИДом или умерли, а среди инфицированных в 1989 году — лишь 20%. ибо в практику лечения больных был внедрен первый антиретровирусный препарат – азидотимидин, ставший базисным для всех последующих схем комбинированной терапии.
 Сегодня арсенал лекарственных средств позволяет подавить вирусную репликацию у большей части больных на определенный, иногда довольно длительныйсрок, перевести заболевание в хроническое течение. Но, тем не менее, терапией удается лишь продлить жизнь больного и нет возможности полностью остановить инфекционный процесс. По мнению Люка Монтанье (1999) мы научились лечить лишь суперинфекции ВИЧ/СПИД, но не сам СПИД. Для успешного лечения больных необходимо решение следующих вопросов: 1) наличие химиотерапевтических средств, направленных непосредственно на ВИЧ, 2) наличие лекарственных препаратов, направленных на ту паразитарную, бактериальную, вирусную, протозойную или грибковую суперинфекцию, в том числе онкопатологию, которая у конкретного больного определяет клинику болезни, 3) коррекциялекарственными средствами иммунодефицита. Теоретически разработка этиотропной терапии ВИЧ-инфекции базируется на ряде принципиальных подходов (табл. 1):
Сегодня арсенал лекарственных средств позволяет подавить вирусную репликацию у большей части больных на определенный, иногда довольно длительныйсрок, перевести заболевание в хроническое течение. Но, тем не менее, терапией удается лишь продлить жизнь больного и нет возможности полностью остановить инфекционный процесс. По мнению Люка Монтанье (1999) мы научились лечить лишь суперинфекции ВИЧ/СПИД, но не сам СПИД. Для успешного лечения больных необходимо решение следующих вопросов: 1) наличие химиотерапевтических средств, направленных непосредственно на ВИЧ, 2) наличие лекарственных препаратов, направленных на ту паразитарную, бактериальную, вирусную, протозойную или грибковую суперинфекцию, в том числе онкопатологию, которая у конкретного больного определяет клинику болезни, 3) коррекциялекарственными средствами иммунодефицита. Теоретически разработка этиотропной терапии ВИЧ-инфекции базируется на ряде принципиальных подходов (табл. 1):
 Таблица 1 Жизненный цикл ВИЧ и антиретровирусные препараты Фазы Обеспеч ение Лекарственные препараты 1. Связывание вириона с мембраной gp 120 CD 4 отсутствуют 2. Инъекция содержимого капсида ВИЧ в клетку отсутствуют 3. Обратная транскрипция с образованием провирусной ДНК Транскр иптаза Нуклеозидные и ненуклеозидные ингибиторы обратной транскриптазы 4. Интеграция провирусной ДНК в ДНК клетки-мишени Интеграз а отсутствуют 5. Транскрипция вирусных полипептидов в хромосомном наборе хозяина отсутствуют 6. Трансляция и рассечение вирусных полипептидов на функционирующие белки Протеаз а Ингибиторы протеазы 7. Сборка вирусов и выход из клетки отсутствуют
Таблица 1 Жизненный цикл ВИЧ и антиретровирусные препараты Фазы Обеспеч ение Лекарственные препараты 1. Связывание вириона с мембраной gp 120 CD 4 отсутствуют 2. Инъекция содержимого капсида ВИЧ в клетку отсутствуют 3. Обратная транскрипция с образованием провирусной ДНК Транскр иптаза Нуклеозидные и ненуклеозидные ингибиторы обратной транскриптазы 4. Интеграция провирусной ДНК в ДНК клетки-мишени Интеграз а отсутствуют 5. Транскрипция вирусных полипептидов в хромосомном наборе хозяина отсутствуют 6. Трансляция и рассечение вирусных полипептидов на функционирующие белки Протеаз а Ингибиторы протеазы 7. Сборка вирусов и выход из клетки отсутствуют
 1) блокада лиганд вируса и в первую очередь gp 120 и gp 41 антилигандами, в частности анти gp 120 и gp 41 – антителами; 2) создание препаратов, имитирующих рецепторы CD 4, которые бы связывались с лигандами вируса и блокировали его возможность соединяться с клетками человека; 3) блокада ферментных систем, обеспечивающих репликацию вируса в клетке-мишени: а) ингибиторы протеаз, осуществляющих “раздевание” вируса, проникшего в цитоплазму клетки-мишени, б) ингибиторы обратной транскриптазы, обеспечивающей транскрипцию РНК вируса в ДНК, в) ингибиторы интегразы, обеспечивающей объединение ДНК вируса с ДНК клетки, г) ингибиторы. Н-РНК-азы, обеспечивающей деградацию нитей РНК вириона, 4) ингибиторы регуляторных генов tatи rev, нарушающих транскрипцию, трансляцию и рассечение вирусных белков; 5) ингибиторы посттрансляционных процессов, а именно гликолизирования и миристилирования белков.
1) блокада лиганд вируса и в первую очередь gp 120 и gp 41 антилигандами, в частности анти gp 120 и gp 41 – антителами; 2) создание препаратов, имитирующих рецепторы CD 4, которые бы связывались с лигандами вируса и блокировали его возможность соединяться с клетками человека; 3) блокада ферментных систем, обеспечивающих репликацию вируса в клетке-мишени: а) ингибиторы протеаз, осуществляющих “раздевание” вируса, проникшего в цитоплазму клетки-мишени, б) ингибиторы обратной транскриптазы, обеспечивающей транскрипцию РНК вируса в ДНК, в) ингибиторы интегразы, обеспечивающей объединение ДНК вируса с ДНК клетки, г) ингибиторы. Н-РНК-азы, обеспечивающей деградацию нитей РНК вириона, 4) ингибиторы регуляторных генов tatи rev, нарушающих транскрипцию, трансляцию и рассечение вирусных белков; 5) ингибиторы посттрансляционных процессов, а именно гликолизирования и миристилирования белков.
 Сегодня с учетом жизненного цикла вирусасозданы препараты, ингибирующие обратную транскриптазу и протеазу. До 1991 года из лекарственных препаратов, непосредственно действующих на ВИЧ, использовался только азидотимидин (фирма Glaxo Wellcome” выпускает его под названием зидовудин, ретровир , в нашей стране торговое название препарата — тимозид ). Азидотимидин(АЗТ) – нуклеозид, ингибитор обратной транскриптазы. Он был создан в 1964 году для лечения онкологических больных. С 1987 года сталприменяться при лечении ВИЧ-инфекции, так как за счет ингибирования обратной транскриптазы тормозит репликацию ВИЧ-1, ВИЧ-2, других ретровирусов и вируса Эпштейна-Барр. Уже первые годы применения азидотимидина в терапии больных позволили снизить летальность, а число суперинфекций уменьшилось в 5 раз, более замедленными темпами развивалась CD 4+ лимфопения, у больных нарастала масса тела.
Сегодня с учетом жизненного цикла вирусасозданы препараты, ингибирующие обратную транскриптазу и протеазу. До 1991 года из лекарственных препаратов, непосредственно действующих на ВИЧ, использовался только азидотимидин (фирма Glaxo Wellcome” выпускает его под названием зидовудин, ретровир , в нашей стране торговое название препарата — тимозид ). Азидотимидин(АЗТ) – нуклеозид, ингибитор обратной транскриптазы. Он был создан в 1964 году для лечения онкологических больных. С 1987 года сталприменяться при лечении ВИЧ-инфекции, так как за счет ингибирования обратной транскриптазы тормозит репликацию ВИЧ-1, ВИЧ-2, других ретровирусов и вируса Эпштейна-Барр. Уже первые годы применения азидотимидина в терапии больных позволили снизить летальность, а число суперинфекций уменьшилось в 5 раз, более замедленными темпами развивалась CD 4+ лимфопения, у больных нарастала масса тела.
 К недостаткам терапии азидотимидином следует отнести в первую очередь формирование более, чем у половины больных устойчивых штаммов вирусов приеме препарата свыше 6 мес. , при этом прослеживается взаимосвязь формирования устойчивости с фазой болезни: при назначении в ранние сроки болезни устойчивость формируется реже, чем в более поздние фазы. Вновь сформировавшиеся резистентные штаммы порой более агрессивны, чем исходный вариант вируса. Накопленный опыт более чем десятилетнего применения азидотимидина поставил перед клиницистами вопрос, чего больше при монотерапии больных азидотимидином или любым другим антиретровирусным препаратом- пользы или вреда. При терапии этими весьма токсичными препаратами в виде монотерапии быстро развивается устойчивость вируса к ним, противовирусноедействие его прекращается, а токсическое продолжается. Очевидно, при монотерапии больше все же вреда.
К недостаткам терапии азидотимидином следует отнести в первую очередь формирование более, чем у половины больных устойчивых штаммов вирусов приеме препарата свыше 6 мес. , при этом прослеживается взаимосвязь формирования устойчивости с фазой болезни: при назначении в ранние сроки болезни устойчивость формируется реже, чем в более поздние фазы. Вновь сформировавшиеся резистентные штаммы порой более агрессивны, чем исходный вариант вируса. Накопленный опыт более чем десятилетнего применения азидотимидина поставил перед клиницистами вопрос, чего больше при монотерапии больных азидотимидином или любым другим антиретровирусным препаратом- пользы или вреда. При терапии этими весьма токсичными препаратами в виде монотерапии быстро развивается устойчивость вируса к ним, противовирусноедействие его прекращается, а токсическое продолжается. Очевидно, при монотерапии больше все же вреда.
 Проблема, насколько важно усовершенствование методик лечения больных, возникла в 1996 году, когда за рубежом был внедрен в широкую практику тест оценки вирусной нагрузки на плазму – полимеразную цепную реакцию (ПЦР), позволившую прогнозировать прогрессирование болезни. Внедрение новых антиретровирусных препаратов и возможность оценки вирусной нагрузки на плазму позволили сформулировать задачу антиретровирусной терапии — снижение вирусной нагрузки до неопределяемого с помощью ПЦР уровня, т. е. ниже 50 копий/мл, так как при такой нагрузке прекращаетсяразрушение иммунной системы вирусом, предотвращающее развитие суперинфекций, значительно падает угроза формирования резистентных штаммов вируса, хотя репликация последнего не прекращается. Среди активных антиретровирусных препаратов в основном используются аналоги нуклеозидов. Онивстраиваются во вновь синтезируемые молекулы РНК или ДНК вируса, действуют как терминаторы цепи, в силу чего прекращают дальнейший синтез нуклеиновой кислоты вируса. Кроме того, они могут конкурировать с внутриклеточными нулеозидтрифосфатами, в результатевыступают конкурентами ингибитора обратной транскриптазы.
Проблема, насколько важно усовершенствование методик лечения больных, возникла в 1996 году, когда за рубежом был внедрен в широкую практику тест оценки вирусной нагрузки на плазму – полимеразную цепную реакцию (ПЦР), позволившую прогнозировать прогрессирование болезни. Внедрение новых антиретровирусных препаратов и возможность оценки вирусной нагрузки на плазму позволили сформулировать задачу антиретровирусной терапии — снижение вирусной нагрузки до неопределяемого с помощью ПЦР уровня, т. е. ниже 50 копий/мл, так как при такой нагрузке прекращаетсяразрушение иммунной системы вирусом, предотвращающее развитие суперинфекций, значительно падает угроза формирования резистентных штаммов вируса, хотя репликация последнего не прекращается. Среди активных антиретровирусных препаратов в основном используются аналоги нуклеозидов. Онивстраиваются во вновь синтезируемые молекулы РНК или ДНК вируса, действуют как терминаторы цепи, в силу чего прекращают дальнейший синтез нуклеиновой кислоты вируса. Кроме того, они могут конкурировать с внутриклеточными нулеозидтрифосфатами, в результатевыступают конкурентами ингибитора обратной транскриптазы.
 . Главная цель при подборе и синтезеаналогов нуклеозидов с ретровирусной активностью – максимальное сродство с обратной транскриптазой и минимальное – с ДНК-полимеразой человека. К наиболее перспективным аналогам нуклеозидов с активностью против обратной транскриптазы относятся: диданозин (видекс, dd. I, 1991), зальцитабин (хивид, dd. C, 1992), ставудин(1994), ламивудин (1995), еще позже появились адефовир, ладанозин (фтористый аналог диданозина), FTC (фтористый аналог ламивудина с более выраженной активностью). Широко в клиническую практику внедрены ненуклеозидные аналоги с активностью против обратной транскриптазы: делавирдин (рескриптаза) и невирапин (вирамун). С 1995 -1996 гг. также внедрены ингибиторы протеазы: индинавир, саквинавир, ритонавир, нелфинавир. Пополнился список ненуклеозиных аналогов, по активности не уступающих эффекту протеазы. Как видно из таблицы 2, 1995 -1997 г. г. были наиболее плодотворными по внедрению в клиническую практику новых лекарственных препаратов с антиретровирусной активностью и для лечения суперинфекций ВИЧ/СПИД(до 10. 99).
. Главная цель при подборе и синтезеаналогов нуклеозидов с ретровирусной активностью – максимальное сродство с обратной транскриптазой и минимальное – с ДНК-полимеразой человека. К наиболее перспективным аналогам нуклеозидов с активностью против обратной транскриптазы относятся: диданозин (видекс, dd. I, 1991), зальцитабин (хивид, dd. C, 1992), ставудин(1994), ламивудин (1995), еще позже появились адефовир, ладанозин (фтористый аналог диданозина), FTC (фтористый аналог ламивудина с более выраженной активностью). Широко в клиническую практику внедрены ненуклеозидные аналоги с активностью против обратной транскриптазы: делавирдин (рескриптаза) и невирапин (вирамун). С 1995 -1996 гг. также внедрены ингибиторы протеазы: индинавир, саквинавир, ритонавир, нелфинавир. Пополнился список ненуклеозиных аналогов, по активности не уступающих эффекту протеазы. Как видно из таблицы 2, 1995 -1997 г. г. были наиболее плодотворными по внедрению в клиническую практику новых лекарственных препаратов с антиретровирусной активностью и для лечения суперинфекций ВИЧ/СПИД(до 10. 99).
 При назначении лекарственных препаратов больному ВИЧ-инфекцией происходит обоюдное взаимодействие между вирусом, лекарственным препаратом и организмом человека (рис. 2).
При назначении лекарственных препаратов больному ВИЧ-инфекцией происходит обоюдное взаимодействие между вирусом, лекарственным препаратом и организмом человека (рис. 2).

 Цель активной антиретровирусной терапии – достигнуть максимальной и длительной супрессии вируса, чтобы создать условия для восстановления иммунной системы, поврежденной ВИЧ. Последнее позволит иммунной системе осуществлять эффективный контроль за репликацией вируса и этим предотвратит развитие суперинфекции, характерной для СПИД. Сегодня идет изучение пределов, до которых возможно восстановление поврежденной ВИЧ иммунной системы, хотя понятно, что полного восстановления у большинства больных, если не у всех, достичь невозможно, тем более в условиях хронической вирусной инфекции, обусловленной ВИЧ. В 1997 году в США разработано новое руководство по лечению больных ВИЧ-инфекцией взрослых и подростков, включающее несколько основополагающих принципов: – раннее назначение антиретровирусныхпрепаратов – регулярная оценка уровня репликационного процесса – индивидуальный подход к антиретровирусной терапии – назначение антиретровирусных препаратов показано даже в случае вирусной нагрузки на плазму ниже уровня определения ПЦР -лица, выявленные в период острой первичной ВИЧ-инфекции (синдром острой сероконверсии) нуждаются в антиретровирусной терапии без учета уровня вирусной нагрузки на плазму (в том числе ниже определяемого в ПЦР) в целяхсупрессии репликации вируса; – обеспечение длительной супрессии вируса за счет комбинации антиретровирусных препаратов постоянного применения с препаратамикурсового, временного применения; – в комплексной антиретровирусной терапии каждый лекарственный препарат назначается в соответствии с его дозировкой, способом и схемой лечения; – комбинация из имеющихся антиретровирусных препаратов ограничивается механизмом их действия, совместимостью и взаимодействием, явлениями синергизма и антагонизма; – при лечении женщин не обращается внимание на наличие беременности; принципы антиретровирусной терапии детей и подростков сохраняются с учетомособенностей их организма, в том числе иммунной системы и своеобразияреакций на лекарственные средства.
Цель активной антиретровирусной терапии – достигнуть максимальной и длительной супрессии вируса, чтобы создать условия для восстановления иммунной системы, поврежденной ВИЧ. Последнее позволит иммунной системе осуществлять эффективный контроль за репликацией вируса и этим предотвратит развитие суперинфекции, характерной для СПИД. Сегодня идет изучение пределов, до которых возможно восстановление поврежденной ВИЧ иммунной системы, хотя понятно, что полного восстановления у большинства больных, если не у всех, достичь невозможно, тем более в условиях хронической вирусной инфекции, обусловленной ВИЧ. В 1997 году в США разработано новое руководство по лечению больных ВИЧ-инфекцией взрослых и подростков, включающее несколько основополагающих принципов: – раннее назначение антиретровирусныхпрепаратов – регулярная оценка уровня репликационного процесса – индивидуальный подход к антиретровирусной терапии – назначение антиретровирусных препаратов показано даже в случае вирусной нагрузки на плазму ниже уровня определения ПЦР -лица, выявленные в период острой первичной ВИЧ-инфекции (синдром острой сероконверсии) нуждаются в антиретровирусной терапии без учета уровня вирусной нагрузки на плазму (в том числе ниже определяемого в ПЦР) в целяхсупрессии репликации вируса; – обеспечение длительной супрессии вируса за счет комбинации антиретровирусных препаратов постоянного применения с препаратамикурсового, временного применения; – в комплексной антиретровирусной терапии каждый лекарственный препарат назначается в соответствии с его дозировкой, способом и схемой лечения; – комбинация из имеющихся антиретровирусных препаратов ограничивается механизмом их действия, совместимостью и взаимодействием, явлениями синергизма и антагонизма; – при лечении женщин не обращается внимание на наличие беременности; принципы антиретровирусной терапии детей и подростков сохраняются с учетомособенностей их организма, в том числе иммунной системы и своеобразияреакций на лекарственные средства.
 Нуклеозидные ингибиторы обратной транскриптазы. Антиретровирусный эффект нуклеозидных ингибиторов обратной транскриптазы можно проследить на примере АЗТ. При приеме внутрь азидотимидин хорошо всасывается, период полувыведения составляет 3 -4 ч, выводится через почки. Терапия предусматривает пожизненный пероральный прием по 100 мг через 5 ч или по 200 мг через 8 ч (имеются и другие схемы лечения). Суточная доза при назначении в виде капсул или сиропа (что зависит от переносимости препарата, стадии болезни) составляет 0, 3 -0, 6 г для взрослых и 0, 01 г/кг массы тела для детей.
Нуклеозидные ингибиторы обратной транскриптазы. Антиретровирусный эффект нуклеозидных ингибиторов обратной транскриптазы можно проследить на примере АЗТ. При приеме внутрь азидотимидин хорошо всасывается, период полувыведения составляет 3 -4 ч, выводится через почки. Терапия предусматривает пожизненный пероральный прием по 100 мг через 5 ч или по 200 мг через 8 ч (имеются и другие схемы лечения). Суточная доза при назначении в виде капсул или сиропа (что зависит от переносимости препарата, стадии болезни) составляет 0, 3 -0, 6 г для взрослых и 0, 01 г/кг массы тела для детей.
 Азидотимидинпо структуре близок к нуклеозиду тимидину, входящему в состав ДНК. В клетке азидотимидин подвергается ферментативному фосфорилированию с образованием азидотимидина трифосфата, являющегосяактивной формой препарата, так как азидотимидинтрифосфат является аналогом тимидинтрифосфата — одного из мономеров ДНК. Механизм подавления синтеза вирусной ДНК, очевидно, состоит в конкурентном ингибировании синтеза цепи ДНК. Под конкурентным ингибированием понимается связывание азидотимидинтрифосфата с обратной транскриптазой в том участке, который в норме связывает обычные нуклеозидтрифосфаты. Терминация синтеза цепи ДНК — обратная транскриптаза ошибочно включает азидотимидинтрифосфат в растущую цепь вирусной ДНК вместо тимидинтрифосфата, но присоединение следующего нуклеотида невозможно, так как в молекуле азидотимидинтрифосфата нет гидроксильной группы, которая необходима для образования связи со следующим нуклеотидом. Вирус не в состоянии исправить эту ошибку и синтез ДНК прекращается
Азидотимидинпо структуре близок к нуклеозиду тимидину, входящему в состав ДНК. В клетке азидотимидин подвергается ферментативному фосфорилированию с образованием азидотимидина трифосфата, являющегосяактивной формой препарата, так как азидотимидинтрифосфат является аналогом тимидинтрифосфата — одного из мономеров ДНК. Механизм подавления синтеза вирусной ДНК, очевидно, состоит в конкурентном ингибировании синтеза цепи ДНК. Под конкурентным ингибированием понимается связывание азидотимидинтрифосфата с обратной транскриптазой в том участке, который в норме связывает обычные нуклеозидтрифосфаты. Терминация синтеза цепи ДНК — обратная транскриптаза ошибочно включает азидотимидинтрифосфат в растущую цепь вирусной ДНК вместо тимидинтрифосфата, но присоединение следующего нуклеотида невозможно, так как в молекуле азидотимидинтрифосфата нет гидроксильной группы, которая необходима для образования связи со следующим нуклеотидом. Вирус не в состоянии исправить эту ошибку и синтез ДНК прекращается
 Аналогичным образом действуют, по-видимому, другие дидезоксинуклеозиды, обладающие активностью против HIV. Все изученные на сегодня нуклеозиды оказались эффективными против ряда ретровирусов, но только в форме трифосфатов Характеристика лекарственных препаратов, представляющих эту группу приведена в табл. 3.
Аналогичным образом действуют, по-видимому, другие дидезоксинуклеозиды, обладающие активностью против HIV. Все изученные на сегодня нуклеозиды оказались эффективными против ряда ретровирусов, но только в форме трифосфатов Характеристика лекарственных препаратов, представляющих эту группу приведена в табл. 3.
 Таблица 3 Характеристика нуклеозидных ингибиторов обратной транскриптазы (НИ ОТ) Название Торговое название Зидовудин (АЗТ, ЗДВ) «Ретровир» Диданозин (ddi) «Видекс» Зальцитабин (ddc) «Хивид» Лекарстве нная форма 100 мг капсулы; 300 мг таблетки; 10 мг/мл раствор в/в; 10 мг/мл раствор per os 25, 50, 100, 150, 200 мг — таблетки; 167, 250 мг — порошки 0, 375 и 0, 75 мг — таблетки Рекоменду емая дозировка 200 мг трижды или 300 мг дважды или с 3 ТС (комбивир) дважды в день Таблетки, 200 мг дважды или 400 мг раз в день <60 кг: 125 мг дважды или 250 мг раз в день 0, 75 мг трижды в день Влияние приема пищи Прием лекарства не связан с приемом пищи Принимать за 1/2 ч до или через 1 ч после еды Прием лекарства не связан с приемом пищи Побочные реакции Угнетение костного мозга: Анемия и/или нейтропения. Субъективные жалобы: симптомы со стороны ЖКТ, головная боль, бессонница, астения. Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного. Панкреатит Периферические невриты Тошнота Диарея Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного. Периферические невриты Стоматит Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного.
Таблица 3 Характеристика нуклеозидных ингибиторов обратной транскриптазы (НИ ОТ) Название Торговое название Зидовудин (АЗТ, ЗДВ) «Ретровир» Диданозин (ddi) «Видекс» Зальцитабин (ddc) «Хивид» Лекарстве нная форма 100 мг капсулы; 300 мг таблетки; 10 мг/мл раствор в/в; 10 мг/мл раствор per os 25, 50, 100, 150, 200 мг — таблетки; 167, 250 мг — порошки 0, 375 и 0, 75 мг — таблетки Рекоменду емая дозировка 200 мг трижды или 300 мг дважды или с 3 ТС (комбивир) дважды в день Таблетки, 200 мг дважды или 400 мг раз в день <60 кг: 125 мг дважды или 250 мг раз в день 0, 75 мг трижды в день Влияние приема пищи Прием лекарства не связан с приемом пищи Принимать за 1/2 ч до или через 1 ч после еды Прием лекарства не связан с приемом пищи Побочные реакции Угнетение костного мозга: Анемия и/или нейтропения. Субъективные жалобы: симптомы со стороны ЖКТ, головная боль, бессонница, астения. Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного. Панкреатит Периферические невриты Тошнота Диарея Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного. Периферические невриты Стоматит Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного.
 Лекарствен ная форма 15, 20, 30, 40 мг — капсулы; 1 мг/мл раствор per os 150 мг — таблетки; 10 мг/мл раствор, per os 300 мг — таблетки 20 мг/мл раствор, per os Рекомендуе мая дозировка >60 кг: 40 мг два раза <60 кг: 30 мг два раза в день 150 мг два раза <50 кг: 2 мг/кг два раза или с 3 ТС (комбивир) два раза в день 300 мг два раза в день Влияние приема пищи Прием лекарства не связан с приемом пищи Алкоголь на 41% снижает концентрацию Побочные реакции Периферически е невриты Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного (Минимальная токсичность) Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного Реакция гиперчувствительности: лихорадка, сыпь, тошнота, рвота, слабость, анорексия (иногда с летальным исходом); Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного
Лекарствен ная форма 15, 20, 30, 40 мг — капсулы; 1 мг/мл раствор per os 150 мг — таблетки; 10 мг/мл раствор, per os 300 мг — таблетки 20 мг/мл раствор, per os Рекомендуе мая дозировка >60 кг: 40 мг два раза <60 кг: 30 мг два раза в день 150 мг два раза <50 кг: 2 мг/кг два раза или с 3 ТС (комбивир) два раза в день 300 мг два раза в день Влияние приема пищи Прием лекарства не связан с приемом пищи Алкоголь на 41% снижает концентрацию Побочные реакции Периферически е невриты Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного (Минимальная токсичность) Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного Реакция гиперчувствительности: лихорадка, сыпь, тошнота, рвота, слабость, анорексия (иногда с летальным исходом); Ацидоз и стеатоз при лечении НИ ОТ наблюдаются редко, но могут угрожать жизни больного
 К недостаткам этих препаратов, как показал накопленный клинический опыт, относятся: а) не полностью подавляют репликацию вируса, б) высокая токсичность, в том числе азидотимидина на костный мозг, диданозина – нейротоксический эффект и способность вызвать тяжелыйгеморрагический панкреатит. Наиболее часто побочные эффекты проявляются анемией, поражением желудочно-кишечного тракта, неврологической симптоматикой, сыпью. К недостаткам всей группы ингибиторов обратной транскриптазы относятся быстрое формирование мутантных форм вируса с появлением у последних резистентности к этим лекарственным препаратам.
К недостаткам этих препаратов, как показал накопленный клинический опыт, относятся: а) не полностью подавляют репликацию вируса, б) высокая токсичность, в том числе азидотимидина на костный мозг, диданозина – нейротоксический эффект и способность вызвать тяжелыйгеморрагический панкреатит. Наиболее часто побочные эффекты проявляются анемией, поражением желудочно-кишечного тракта, неврологической симптоматикой, сыпью. К недостаткам всей группы ингибиторов обратной транскриптазы относятся быстрое формирование мутантных форм вируса с появлением у последних резистентности к этим лекарственным препаратам.
 Ненуклеозидные ингибиторы обратной транскриптазы. Характеристика препаратов этой группы представлена в табл. 4.
Ненуклеозидные ингибиторы обратной транскриптазы. Характеристика препаратов этой группы представлена в табл. 4.
 Название Торговое название Невирапин «Вирамун» Делавирдин «Рескриптор» Ифавиренц «Сустива» Лекарствен ная форма 200 мг — таблетки; 50 мг/5 мл раствор, per os 100 мг — таблетки 50, 100, 200 мг – таблетки Рекомендуе мая дозировка 200 мг per os раз в день в течение 14 дней, затем 200 мг дважды в день 400 мг per os три раза в день или 4 табл. по 100 мг в 100 мл воды 600 мг per os Влияние приема пищи Прием лекарства не связан с приемом пищи Избегать принимать лекарство после жирной пищи, так концентрация на 50% падает Побочные реакции Сыпь Повышение уровней трансаминаз Гепатит Сыпь Повышение уровней трансаминаз Головные боли Сыпь Симптомы со стороны ЦНС Повышение уровней трансаминаз Тератогенность (для обезьян)
Название Торговое название Невирапин «Вирамун» Делавирдин «Рескриптор» Ифавиренц «Сустива» Лекарствен ная форма 200 мг — таблетки; 50 мг/5 мл раствор, per os 100 мг — таблетки 50, 100, 200 мг – таблетки Рекомендуе мая дозировка 200 мг per os раз в день в течение 14 дней, затем 200 мг дважды в день 400 мг per os три раза в день или 4 табл. по 100 мг в 100 мл воды 600 мг per os Влияние приема пищи Прием лекарства не связан с приемом пищи Избегать принимать лекарство после жирной пищи, так концентрация на 50% падает Побочные реакции Сыпь Повышение уровней трансаминаз Гепатит Сыпь Повышение уровней трансаминаз Головные боли Сыпь Симптомы со стороны ЦНС Повышение уровней трансаминаз Тератогенность (для обезьян)
 Ингибиторы протеазы, проникая в инфицированные вирусом клетки, блокируют активность вирусного фермента протеазы, препятствуют распаду длинных цепей протеинов и энзимов на короткие звенья, необходимые ВИЧ для образования новых копий. Без них вирус дефектен и не можетинфицировать клетку. Ингибиторы протеазы более мощно тормозят репликацию вируса, чем ингибиторы обратной транскриптазы и за 1 мес. лечения снижают вирусную нагрузку на 99%, в силу чего наступает ремиссия болезни, повышается уровень CD 4+ лимфоцитов. Действие ингибиторов протеазы осуществляетсяв лимфоидных клетках человека. Поскольку протеаза ВИЧ отличается от протеазы человека, ингибиторы вирусной протеазы действуют избирательно, не блокируя функцию фермента клеток человека. Но к этим препаратам ибыстрее формируются устойчивые клоны вирусов.
Ингибиторы протеазы, проникая в инфицированные вирусом клетки, блокируют активность вирусного фермента протеазы, препятствуют распаду длинных цепей протеинов и энзимов на короткие звенья, необходимые ВИЧ для образования новых копий. Без них вирус дефектен и не можетинфицировать клетку. Ингибиторы протеазы более мощно тормозят репликацию вируса, чем ингибиторы обратной транскриптазы и за 1 мес. лечения снижают вирусную нагрузку на 99%, в силу чего наступает ремиссия болезни, повышается уровень CD 4+ лимфоцитов. Действие ингибиторов протеазы осуществляетсяв лимфоидных клетках человека. Поскольку протеаза ВИЧ отличается от протеазы человека, ингибиторы вирусной протеазы действуют избирательно, не блокируя функцию фермента клеток человека. Но к этим препаратам ибыстрее формируются устойчивые клоны вирусов.
 Таблица 6 Характеристика ингибиторов протеазы (ИП) Название Торговое название Индинавир «Криксиван» Ритонавир «Норвир» Нельфинав ир «Вирацепт» Саквинавир Ампренавир «Агенераза» «Инвираза» «Фортоваза» Лекарствен ная форма 200, 333, 400 мг- капсулы 100 мг — капсулы 600 мг/7, 5 мл раствор per os 250 мг — таблетки; 50 мг/г — порошок per os 200 мг — капсулы 50, 150 мг — таблетки; 15 мг/мл раствор Рекомендуе мая дозировка 200 мг через каждые 8 часов 600 мг через каждые 12 часов 750 мг три раза или 1250 мг два раза в день 400 мг два раза в день с ритонавиром 1200 мг три раза в день 1200 мг два раза в день
Таблица 6 Характеристика ингибиторов протеазы (ИП) Название Торговое название Индинавир «Криксиван» Ритонавир «Норвир» Нельфинав ир «Вирацепт» Саквинавир Ампренавир «Агенераза» «Инвираза» «Фортоваза» Лекарствен ная форма 200, 333, 400 мг- капсулы 100 мг — капсулы 600 мг/7, 5 мл раствор per os 250 мг — таблетки; 50 мг/г — порошок per os 200 мг — капсулы 50, 150 мг — таблетки; 15 мг/мл раствор Рекомендуе мая дозировка 200 мг через каждые 8 часов 600 мг через каждые 12 часов 750 мг три раза или 1250 мг два раза в день 400 мг два раза в день с ритонавиром 1200 мг три раза в день 1200 мг два раза в день
 Влияние приема пищи Принимать за 1 час до или через 2 часа после приема пищи Можно принимать с обезжиренны м молоком или нежирной пищей Принимать, по возможности, вместе с пищей — это может повысить толерантнос ть к лекарству Принимать с пищей Прием пищи не оказывает влияния, если инвиразу принимают с ритонавиром Принимать с большим количеством пищи Можно принимать с нежирной пищей Хранение При комнатной температуре Капсулы — в холодильник е Оральный раствор не хранить в холодильник е При комнатной температуре В холодильник е или при комнатной температуре (до 3 месяцев) При комнатной температуре
Влияние приема пищи Принимать за 1 час до или через 2 часа после приема пищи Можно принимать с обезжиренны м молоком или нежирной пищей Принимать, по возможности, вместе с пищей — это может повысить толерантнос ть к лекарству Принимать с пищей Прием пищи не оказывает влияния, если инвиразу принимают с ритонавиром Принимать с большим количеством пищи Можно принимать с нежирной пищей Хранение При комнатной температуре Капсулы — в холодильник е Оральный раствор не хранить в холодильник е При комнатной температуре В холодильник е или при комнатной температуре (до 3 месяцев) При комнатной температуре
 Побочные реакции Почечно-кам енная болезнь Симптомы ЖКТ, тошнота Повышен непрямого билирубин А также: головная боль, астения, нарушение зрения, головокруже ния, сыпь, металлическ ий привкус во рту, тромбоцитоп ения Гипергликем ия Перераспред еление жировой клетчатки и нарушение липидного обмена Симптомы со стороны ЖКТ, тошнота, рвота, диарея Парестезии Гепатит Астения Нарушения вкуса Лабораторно : повышаются более чем на 200% триглицерид ы, трансаминаз ы Гипергликем ия Перераспред еление жировой клетчатки и нарушения липидного обмена Диарея Гипергликем ия Перераспред еление жировой клетчатки и нарушения липидного обмена Симптомы ЖКТ, тошнота и диарея Головная боль Трансаминаз ы Гипергликем ия Перераспред еление жировой клетчатки и нарушение липидного обмена Симптомы со стороны ЖКТ, тошнота, диарея, боли в животе и диспепсия Головная боль Трансаминаз ы Гипергликем ия Перераспред еление жировой клетчатки и нарушения липидного обмена Симптомы со стороны ЖКТ, тошнота, рвота, диарея Сыпь Парестезии слизистых оболочек рта Гипергликем ия Перераспред еление жировой клетчатки и нарушения липидного обмена
Побочные реакции Почечно-кам енная болезнь Симптомы ЖКТ, тошнота Повышен непрямого билирубин А также: головная боль, астения, нарушение зрения, головокруже ния, сыпь, металлическ ий привкус во рту, тромбоцитоп ения Гипергликем ия Перераспред еление жировой клетчатки и нарушение липидного обмена Симптомы со стороны ЖКТ, тошнота, рвота, диарея Парестезии Гепатит Астения Нарушения вкуса Лабораторно : повышаются более чем на 200% триглицерид ы, трансаминаз ы Гипергликем ия Перераспред еление жировой клетчатки и нарушения липидного обмена Диарея Гипергликем ия Перераспред еление жировой клетчатки и нарушения липидного обмена Симптомы ЖКТ, тошнота и диарея Головная боль Трансаминаз ы Гипергликем ия Перераспред еление жировой клетчатки и нарушение липидного обмена Симптомы со стороны ЖКТ, тошнота, диарея, боли в животе и диспепсия Головная боль Трансаминаз ы Гипергликем ия Перераспред еление жировой клетчатки и нарушения липидного обмена Симптомы со стороны ЖКТ, тошнота, рвота, диарея Сыпь Парестезии слизистых оболочек рта Гипергликем ия Перераспред еление жировой клетчатки и нарушения липидного обмена
 Среди ингибиторов протеазы (табл. 6) наиболее широкое распространение получили криксиван и инвираза в связи с низкой связываемостью с белками плазмы, а следовательно возможностью в активной форме в больших концентрациях накопиться в плазме, а также способностью проникать через гематоэнцефалический барьер. Криксиван (индинавира сульфат) обладает активностью против ВИЧ-1. Обычно назначается по 800 мг (2 капсулы по 400 мг) внутрь каждые 8 часов, причем дозировка одинакова как при монотерапии, так и при сочетании с другими антиретровирусными лекарственными средствами. Рекомендуется применять криксиван в следующих ситуациях: больным, ранее не получавшим антиретровирусной терапии назначают криксиван: а) в сочетании с аналогами нуклеозидов, б) или в виде монотерапии для начального лечения (есливключение аналогов нуклеозидов клинически не оправдано), больным, ранее лечившимся антиретровирусными средствами криксиван назначается: а) в сочетании с аналогами нуклеозидов, б) или в качестве монотерапии для лиц получавших или получающих аналоги нуклеозидов.
Среди ингибиторов протеазы (табл. 6) наиболее широкое распространение получили криксиван и инвираза в связи с низкой связываемостью с белками плазмы, а следовательно возможностью в активной форме в больших концентрациях накопиться в плазме, а также способностью проникать через гематоэнцефалический барьер. Криксиван (индинавира сульфат) обладает активностью против ВИЧ-1. Обычно назначается по 800 мг (2 капсулы по 400 мг) внутрь каждые 8 часов, причем дозировка одинакова как при монотерапии, так и при сочетании с другими антиретровирусными лекарственными средствами. Рекомендуется применять криксиван в следующих ситуациях: больным, ранее не получавшим антиретровирусной терапии назначают криксиван: а) в сочетании с аналогами нуклеозидов, б) или в виде монотерапии для начального лечения (есливключение аналогов нуклеозидов клинически не оправдано), больным, ранее лечившимся антиретровирусными средствами криксиван назначается: а) в сочетании с аналогами нуклеозидов, б) или в качестве монотерапии для лиц получавших или получающих аналоги нуклеозидов.
 В лечении ВИЧ-инфекции произошел коренной перелом, связанный с применением ингибиторов протеаз. Хотя замедлять прогрессирование ВИЧ-инфекции до клинических проявлений СПИДа могут и ингибиторы обратной транскриптазы, эффективность ингибиторов протеаз оказалась намного выше. Отчасти это объясняется различными механизмами действия препаратов этих 2 классов. Ингибиторы обратной транскриптазы подавляют активность ферментов вируса, что способствует транскрипции вирусной РНК на комплементарной цепочке ДНК, которая затем встраивается в геном человека. Дальше комплементарная цепочка ДНК транслируется на мессенджере РНК, кодирующем белки ВИЧ, которые впоследствии встраиваются в зрелые вирусы. Эффективность ингибиторов обратной транскриптазы ограничивается во-первых, когда встраивание комплементарной цепочки ДНК уже произошло, то ингибиторы обратной транскриптазы не влияют на продукцию вирусного белка. Во-вторых, обратная транскриптаза ВИЧ не всегда точно транслируется с мессенджера РНК, для нее характерен высокий уровень мутаций. Если учесть, что количество продуцируемых за сутки вирусов превышает 1010 , все это в совокупности способствует быстрому формированию устойчивости к ингибиторам обратной транскрипт
В лечении ВИЧ-инфекции произошел коренной перелом, связанный с применением ингибиторов протеаз. Хотя замедлять прогрессирование ВИЧ-инфекции до клинических проявлений СПИДа могут и ингибиторы обратной транскриптазы, эффективность ингибиторов протеаз оказалась намного выше. Отчасти это объясняется различными механизмами действия препаратов этих 2 классов. Ингибиторы обратной транскриптазы подавляют активность ферментов вируса, что способствует транскрипции вирусной РНК на комплементарной цепочке ДНК, которая затем встраивается в геном человека. Дальше комплементарная цепочка ДНК транслируется на мессенджере РНК, кодирующем белки ВИЧ, которые впоследствии встраиваются в зрелые вирусы. Эффективность ингибиторов обратной транскриптазы ограничивается во-первых, когда встраивание комплементарной цепочки ДНК уже произошло, то ингибиторы обратной транскриптазы не влияют на продукцию вирусного белка. Во-вторых, обратная транскриптаза ВИЧ не всегда точно транслируется с мессенджера РНК, для нее характерен высокий уровень мутаций. Если учесть, что количество продуцируемых за сутки вирусов превышает 1010 , все это в совокупности способствует быстрому формированию устойчивости к ингибиторам обратной транскрипт
 В отличие от ингибиторов обратной транскриптазы ингибиторы протеаз действуют на этапе репликации вируса, подавляя активность кодируемой вирусом аспартатпротеазы, которая расщепляет крупные белки-предшественники на мелкие пептиды, необходимые для встраивания в вирус. Они предотвращают репликацию вируса после интеграции комплементарной цепочки ДНК в геном клетки и в отличие от ингибиторов обратной транскриптазы могут препятствовать размножению вируса в инфицированной клетке. проникая в инфицированные вирусом клетки Ингибиторы протеазы, , блокируют активность вирусного фермента протеазы, препятствуют распаду длинных цепей протеинов и энзимов на короткие звенья, необходимые ВИЧ для образования новых копий. Без них вирус дефектен и не можетинфицировать клетку. Ингибиторы протеазы более мощно тормозят репликацию вируса, чем ингибиторы обратной транскриптазы и за 1 мес. лечения снижают вирусную нагрузку на 99%, в силу чего наступает ремиссия болезни, повышается уровень CD 4+ лимфоцитов. Действие ингибиторов протеазы осуществляетсяв лимфоидных клетках человека. Поскольку протеаза ВИЧ отличается от протеазы человека, ингибиторы вирусной протеазы действуют избирательно, не блокируя функцию фермента клеток человека. Но к этим препаратам ибыстрее формируются устойчивые клоны вирусов, особенно при использовании ингибиторов протеаз в виде монотерапии.
В отличие от ингибиторов обратной транскриптазы ингибиторы протеаз действуют на этапе репликации вируса, подавляя активность кодируемой вирусом аспартатпротеазы, которая расщепляет крупные белки-предшественники на мелкие пептиды, необходимые для встраивания в вирус. Они предотвращают репликацию вируса после интеграции комплементарной цепочки ДНК в геном клетки и в отличие от ингибиторов обратной транскриптазы могут препятствовать размножению вируса в инфицированной клетке. проникая в инфицированные вирусом клетки Ингибиторы протеазы, , блокируют активность вирусного фермента протеазы, препятствуют распаду длинных цепей протеинов и энзимов на короткие звенья, необходимые ВИЧ для образования новых копий. Без них вирус дефектен и не можетинфицировать клетку. Ингибиторы протеазы более мощно тормозят репликацию вируса, чем ингибиторы обратной транскриптазы и за 1 мес. лечения снижают вирусную нагрузку на 99%, в силу чего наступает ремиссия болезни, повышается уровень CD 4+ лимфоцитов. Действие ингибиторов протеазы осуществляетсяв лимфоидных клетках человека. Поскольку протеаза ВИЧ отличается от протеазы человека, ингибиторы вирусной протеазы действуют избирательно, не блокируя функцию фермента клеток человека. Но к этим препаратам ибыстрее формируются устойчивые клоны вирусов, особенно при использовании ингибиторов протеаз в виде монотерапии.
 Токсичность ингибиторов протеазы довольно выражена, у больных через 1 -2 года терапии развивается липодистрофия и растет холестерин крови. Отрицательные метаболические эффектыингибиторов протеазы значительно снижают эффект терапии. Среди ингибиторов протеазы наиболее широкое распространение получили криксиван и инвираза в связи с низкой связываемостью с белками плазмы, а следовательно возможностью в активной форме в больших концентрациях накопиться в плазме, а также способностью проникать через гематоэнцефалический барьер. Криксиван (индинавира сульфат) обладает активностью против ВИЧ-1.
Токсичность ингибиторов протеазы довольно выражена, у больных через 1 -2 года терапии развивается липодистрофия и растет холестерин крови. Отрицательные метаболические эффектыингибиторов протеазы значительно снижают эффект терапии. Среди ингибиторов протеазы наиболее широкое распространение получили криксиван и инвираза в связи с низкой связываемостью с белками плазмы, а следовательно возможностью в активной форме в больших концентрациях накопиться в плазме, а также способностью проникать через гематоэнцефалический барьер. Криксиван (индинавира сульфат) обладает активностью против ВИЧ-1.
 Рекомендуется применять криксиван в следующих ситуациях: больным, ранее не получавшим антиретровирусной терапии назначают криксиван: • а) в сочетании с аналогами нуклеозидов, б) или в виде монотерапии для начального лечения (есливключение аналогов нуклеозидов клинически не оправдано), • больным, ранее лечившимся антиретровирусными средствами криксиван назначается: а) в сочетании с аналогами нуклеозидов, б) или в качестве монотерапии для лиц получавших или получающих аналоги нуклеозидов. R. M. Gulick et al. (1997) показали, что добавление ингибитора протеаз к двум ингибиторам обратной транскриптазы в значительной степени повышает способность препаратов снижать содержание ВИЧ в крови. Ни у одного больного, принимавшего два ингибитора обратной транскриптазы, содержание вируса не уменьшалось ниже уровня, поддающегося определению, тогда как на фоне трехкомпонентного лечения ингибитором протеаз и двумя ингибиторами обратной транскриптазы такой эффект наблюдался в 90% случаев.
Рекомендуется применять криксиван в следующих ситуациях: больным, ранее не получавшим антиретровирусной терапии назначают криксиван: • а) в сочетании с аналогами нуклеозидов, б) или в виде монотерапии для начального лечения (есливключение аналогов нуклеозидов клинически не оправдано), • больным, ранее лечившимся антиретровирусными средствами криксиван назначается: а) в сочетании с аналогами нуклеозидов, б) или в качестве монотерапии для лиц получавших или получающих аналоги нуклеозидов. R. M. Gulick et al. (1997) показали, что добавление ингибитора протеаз к двум ингибиторам обратной транскриптазы в значительной степени повышает способность препаратов снижать содержание ВИЧ в крови. Ни у одного больного, принимавшего два ингибитора обратной транскриптазы, содержание вируса не уменьшалось ниже уровня, поддающегося определению, тогда как на фоне трехкомпонентного лечения ингибитором протеаз и двумя ингибиторами обратной транскриптазы такой эффект наблюдался в 90% случаев.
 S. M. Hammer et al. (1997) продемонстрировали не только снижение содержания вируса в крови, но и существенное уменьшение комбинированного показателя частоты прогрессирования ВИЧ-инфекции до СПИДа или смерти. Надо отметить, что этот благоприятный эффект наблюдался у больных с тяжелым иммунодефицитом (число лимфоцитов СD 4+ <50/мм 3), чего трудно было бы достичь при моно- или комбинированной терапии ингибиторами обратной транскриптазы. Таким образом, результаты применения ингибиторов протеаз возродили надежду на успешность лечения даже при выраженных клинических проявлениях СПИДа.
S. M. Hammer et al. (1997) продемонстрировали не только снижение содержания вируса в крови, но и существенное уменьшение комбинированного показателя частоты прогрессирования ВИЧ-инфекции до СПИДа или смерти. Надо отметить, что этот благоприятный эффект наблюдался у больных с тяжелым иммунодефицитом (число лимфоцитов СD 4+ <50/мм 3), чего трудно было бы достичь при моно- или комбинированной терапии ингибиторами обратной транскриптазы. Таким образом, результаты применения ингибиторов протеаз возродили надежду на успешность лечения даже при выраженных клинических проявлениях СПИДа.
 Схемы лечения антиретровирусными препаратами. Разработано свыше 200 возможных комбинаций антиретровирусной терапии, но нет ни одной, которая являлась бы наилучшей для всех больных. В каждом конкретном случае важно найти этот лучший вариант. Наиболее эффективна комбинация 3 препаратов: 2 нуклеозидных аналога — ингибитора обратной транскриптазы и 1 ингибитор протеазы, например, азидотимидин + ламивудин + ритонавир или другая комбинация: азидотимидин + диданозин + индинавир. Современная концепция применения антиретровирусных препаратов построена на комплексном применении лекарственных средств с различными точками приложения. Ингибиторы обратной транскриптазы не действуют на латентно-инфицированные клетки, в этих случаях противовирусный эффект оказывают только ингибиторы протеазы. Так, установлено, что для возникновения резистентности к ингибиторам обратной транскриптазы достаточно одной мутации, а к ингибиторам протезы – 3 -4. Правда, как было выявлено, резистентность к одному из аналогов нуклеозидов не всегда носит перекресного характера, чувствительность вируса к нуклеозидам другой группы иногда сохраняется. Чаще всего прибегают к так называемой “тритерапии”, предложенной D. Hu (1995), включающей комбинацию двух ингибиторов обратной транскриптазы (обычно ретровир и эпивир) с одним из ингибиторов протеазы (криксиван или инвираза). Именно за счет применения этого “лекарственного коктейля” удалось снизить показатель смертности в 3 раза, а в стадии тяжелого иммунодефицита с 69, 3 до 23, 1 на 1000 больных (Montaner L. et al. , 1996). В регионах с высоким уровнем инфицированных за счет приема инъекционных наркотических средств особенно целесообразно включение в “тритерапию” эпивира, ибо он обладает одновременно и эффектом против вируса гепатита В, а у больных ВИЧ-инфекциейинъекционных наркоманов в 70 -90% одновременно обнаруживаются вирусы гепатитов В и С.
Схемы лечения антиретровирусными препаратами. Разработано свыше 200 возможных комбинаций антиретровирусной терапии, но нет ни одной, которая являлась бы наилучшей для всех больных. В каждом конкретном случае важно найти этот лучший вариант. Наиболее эффективна комбинация 3 препаратов: 2 нуклеозидных аналога — ингибитора обратной транскриптазы и 1 ингибитор протеазы, например, азидотимидин + ламивудин + ритонавир или другая комбинация: азидотимидин + диданозин + индинавир. Современная концепция применения антиретровирусных препаратов построена на комплексном применении лекарственных средств с различными точками приложения. Ингибиторы обратной транскриптазы не действуют на латентно-инфицированные клетки, в этих случаях противовирусный эффект оказывают только ингибиторы протеазы. Так, установлено, что для возникновения резистентности к ингибиторам обратной транскриптазы достаточно одной мутации, а к ингибиторам протезы – 3 -4. Правда, как было выявлено, резистентность к одному из аналогов нуклеозидов не всегда носит перекресного характера, чувствительность вируса к нуклеозидам другой группы иногда сохраняется. Чаще всего прибегают к так называемой “тритерапии”, предложенной D. Hu (1995), включающей комбинацию двух ингибиторов обратной транскриптазы (обычно ретровир и эпивир) с одним из ингибиторов протеазы (криксиван или инвираза). Именно за счет применения этого “лекарственного коктейля” удалось снизить показатель смертности в 3 раза, а в стадии тяжелого иммунодефицита с 69, 3 до 23, 1 на 1000 больных (Montaner L. et al. , 1996). В регионах с высоким уровнем инфицированных за счет приема инъекционных наркотических средств особенно целесообразно включение в “тритерапию” эпивира, ибо он обладает одновременно и эффектом против вируса гепатита В, а у больных ВИЧ-инфекциейинъекционных наркоманов в 70 -90% одновременно обнаруживаются вирусы гепатитов В и С.
 Оценочным показателем лечения антиретровирусными препаратами являетсядлительность снижения числа копий РНК ВИЧ в плазме и увеличение количества клеток СД 4+ клеток. В большинстве случаев эффект получают через 48 недель. Рекомендуется вирусную нагрузку на плазму определять каждые 3 -4 мес. , а число CD 4+ клеток каждые 3 -6 мес. Эти тесты обязательны перед началом терапии или ее изменением и 4 -8 нед. спустя от начала терапии. При этом необходимо учитывать, что некоторые больные на новое лечение реагируют позже, чем впервые получающие терапию. В оценке комбинации лекарственных средств существенную роль играет количество таблеток/капсул, частота приема лекарств, наличие требований к диете и ее ограничений, удобство приема, потенциальную токсичность и сведения о взаимодействиях различных препаратов.
Оценочным показателем лечения антиретровирусными препаратами являетсядлительность снижения числа копий РНК ВИЧ в плазме и увеличение количества клеток СД 4+ клеток. В большинстве случаев эффект получают через 48 недель. Рекомендуется вирусную нагрузку на плазму определять каждые 3 -4 мес. , а число CD 4+ клеток каждые 3 -6 мес. Эти тесты обязательны перед началом терапии или ее изменением и 4 -8 нед. спустя от начала терапии. При этом необходимо учитывать, что некоторые больные на новое лечение реагируют позже, чем впервые получающие терапию. В оценке комбинации лекарственных средств существенную роль играет количество таблеток/капсул, частота приема лекарств, наличие требований к диете и ее ограничений, удобство приема, потенциальную токсичность и сведения о взаимодействиях различных препаратов.
 Существенным тормозом к широкому применению “тритерапии” ВИЧ-инфекции относится ее дороговизна – около 1000 долл. США в месяц на 1 больного, 12 тыс. долларов в год. В 1996 году на СПИД в США тратилось менее 1% всех расходов на здравоохранение: 6, 7 млрд. долларов или около 20 000 на одного больного в год. Так как активная антиретровирусная терапия весьма дорога, лишь 10 -15% больных ВИЧ-инфекцией живут в странах, где экономика позволяет широко внедрить этот вид терапии. В России ею государство обеспечивает лишь детей. Математическая модель, разработанная доктором Д. Толсоном (1999), позволила получить очень интересные данные об экономических аспектах высоко активной антиретровирусной терапии. На примере больных только в одном крупном городе (Нью-Йорк) было показано, что переход с монотерапии на комбинированную антиретровирусную терапию приводит к увеличению прямых затрат на лекарства на 115%. Тем не менее, суммарные расходы на лекарства (в расчете на одного больного) сократятся, так как исчезнет необходимость осуществлять профилактический прием противогрибковых или антигерпетических препаратов, а также проводить лечение различных СПИД-ассоциированных суперинфекций, сократится потребность в госпитализациях и т. д. (CDC , 2000)
Существенным тормозом к широкому применению “тритерапии” ВИЧ-инфекции относится ее дороговизна – около 1000 долл. США в месяц на 1 больного, 12 тыс. долларов в год. В 1996 году на СПИД в США тратилось менее 1% всех расходов на здравоохранение: 6, 7 млрд. долларов или около 20 000 на одного больного в год. Так как активная антиретровирусная терапия весьма дорога, лишь 10 -15% больных ВИЧ-инфекцией живут в странах, где экономика позволяет широко внедрить этот вид терапии. В России ею государство обеспечивает лишь детей. Математическая модель, разработанная доктором Д. Толсоном (1999), позволила получить очень интересные данные об экономических аспектах высоко активной антиретровирусной терапии. На примере больных только в одном крупном городе (Нью-Йорк) было показано, что переход с монотерапии на комбинированную антиретровирусную терапию приводит к увеличению прямых затрат на лекарства на 115%. Тем не менее, суммарные расходы на лекарства (в расчете на одного больного) сократятся, так как исчезнет необходимость осуществлять профилактический прием противогрибковых или антигерпетических препаратов, а также проводить лечение различных СПИД-ассоциированных суперинфекций, сократится потребность в госпитализациях и т. д. (CDC , 2000)
 На конец 1998 года получали активную антиретровирусную терапию 385 000 американцев, не лечились только больные ВИЧ-инфекцией с бессимптомным течением и те, у кого имелась ранняя стадия болезни. В 1 квартале 1998 года 80% больных получали по крайней мере 1 ингибитор протеазы или ненуклеозидные ингибиторы обратной транскриптазы, 70% получали тритерапию. По данным D. Butcher (1999) у принимавших комбинированную активную антиретровирусную терапию. АЗТ + криксиван + эпивирв течение 3 лет в 70% вирусная нагрузка на плазму не определялась самыми ультрасовременными методами (<50 копий/мл). Комбинация из 2 препаратов менее эффективна, хотя нередко используется сочетание азидотимидин + ламивудин или диданозин + ставудин. Когда применяется ингибитор протеазы, то из ингибиторов обратной транскриптазы лучше использовать препараты, которые больной ранее не принимал. Идут поиски препаратов, которые можно было бы применять 1 -2 раза в день. Установлено, что прием два раза в день нельфинавира и саквинавира (фортовазе) дает такой же эффект, как трехразовый прием. Разработана схема приема двух ингибиторов протеазы один раз в сутки. Предложена удобная схема лечения двумя ингибиторами протеазы — комбинация криксиван (120 мг) + ритонавир (100 мг)один раз в сутки вне зависимости от приема пищи.
На конец 1998 года получали активную антиретровирусную терапию 385 000 американцев, не лечились только больные ВИЧ-инфекцией с бессимптомным течением и те, у кого имелась ранняя стадия болезни. В 1 квартале 1998 года 80% больных получали по крайней мере 1 ингибитор протеазы или ненуклеозидные ингибиторы обратной транскриптазы, 70% получали тритерапию. По данным D. Butcher (1999) у принимавших комбинированную активную антиретровирусную терапию. АЗТ + криксиван + эпивирв течение 3 лет в 70% вирусная нагрузка на плазму не определялась самыми ультрасовременными методами (<50 копий/мл). Комбинация из 2 препаратов менее эффективна, хотя нередко используется сочетание азидотимидин + ламивудин или диданозин + ставудин. Когда применяется ингибитор протеазы, то из ингибиторов обратной транскриптазы лучше использовать препараты, которые больной ранее не принимал. Идут поиски препаратов, которые можно было бы применять 1 -2 раза в день. Установлено, что прием два раза в день нельфинавира и саквинавира (фортовазе) дает такой же эффект, как трехразовый прием. Разработана схема приема двух ингибиторов протеазы один раз в сутки. Предложена удобная схема лечения двумя ингибиторами протеазы — комбинация криксиван (120 мг) + ритонавир (100 мг)один раз в сутки вне зависимости от приема пищи.
 Так как ингибиторы протеазы обладают выраженными побочными эффектами, идет поиск схем, которые бы не включали ингибиторы протеазы, а состояли из трех нуклеозидных аналогов, в частности начинают применять комбинации трех ингибиторов обратной транскриптазы, в каждую включается новыйсильный нуклеозидный аналог абакавир (зиаген). Другие схемы включают ненуклеозидные ингибиторы обратной транскриптазы ифавиренц и невирапин (вирамун). Имеется определенный опыт применения гидроксимочевины (Hydroxyurea), как антиретровирусного препарата. Она была синтезирована против рака, но стала также использоваться в комбинации с диданозином или другим антиретровирусным препаратом и может на длительное время снизить вирусную нагрузку на плазму. Но так как гидроксимочевина токсична для костного мозга, она не может быть использована в комбинации с азидотимидином. Некоторые нуклеозидные аналоги не должны применяться вместе, например, азидотимидин со ставудином или диданозин с зальцитабином. Нельзя в комбинацию включать одновременно лекарственные средства, имеющие одно основание, например dd C и 3 Т С (совпадение по последнему знаку). Если вирус резистентен в одному лекарственному препарату определенного класса, то он резистентен и к другим препаратам этого класса — перекрестсная резистентность. Поэтому при необходимости изменения вида терапии из-за неэффективности применяемого комплекса заменяют все лекарственные препараты. Если больной не ответил положительным эффектом на 2 -3 комбинации, возможности воздействия на патологический процесс можно считать исчерпанными.
Так как ингибиторы протеазы обладают выраженными побочными эффектами, идет поиск схем, которые бы не включали ингибиторы протеазы, а состояли из трех нуклеозидных аналогов, в частности начинают применять комбинации трех ингибиторов обратной транскриптазы, в каждую включается новыйсильный нуклеозидный аналог абакавир (зиаген). Другие схемы включают ненуклеозидные ингибиторы обратной транскриптазы ифавиренц и невирапин (вирамун). Имеется определенный опыт применения гидроксимочевины (Hydroxyurea), как антиретровирусного препарата. Она была синтезирована против рака, но стала также использоваться в комбинации с диданозином или другим антиретровирусным препаратом и может на длительное время снизить вирусную нагрузку на плазму. Но так как гидроксимочевина токсична для костного мозга, она не может быть использована в комбинации с азидотимидином. Некоторые нуклеозидные аналоги не должны применяться вместе, например, азидотимидин со ставудином или диданозин с зальцитабином. Нельзя в комбинацию включать одновременно лекарственные средства, имеющие одно основание, например dd C и 3 Т С (совпадение по последнему знаку). Если вирус резистентен в одному лекарственному препарату определенного класса, то он резистентен и к другим препаратам этого класса — перекрестсная резистентность. Поэтому при необходимости изменения вида терапии из-за неэффективности применяемого комплекса заменяют все лекарственные препараты. Если больной не ответил положительным эффектом на 2 -3 комбинации, возможности воздействия на патологический процесс можно считать исчерпанными.
 При внедрении активной антиретровирусной терапии (тритерапии) полагали. что понадобится 3 года, чтобы полностью очистить инфицированные ВИЧ клетки организма. Но последующие исследования показали, что процесс «полураспада»клеток значительно дольше, для полного очищения организма потребуется 60 лет. Поэтому при имеющихся средствах терапиивозможно только перевести процесс в хроническое течение, а полное излечение недоступно. Врачи медицинского факультета Университета Гете во Франкфурте при обследовании 60 больных ВИЧ/СПИДом установили, что через 36 недель после начала высоко активной антиретровирусной терапии у пациентов, ранее получавших противовирусные препараты, нередко отмечается увеличение показателей вирусной нагрузки. Это обусловлено все более широким распространением среди штаммов ВИЧ резистентности к антиретровирусным лекарствам. Устойчивость к ингибиторам протеазы была выявлена у 45% больных, начавших лечение этими препаратами, и почти у 90% больных, получавших невирапин. В целом резистентность к одному или нескольким противовирусным препаратам развилась в 75% случаев
При внедрении активной антиретровирусной терапии (тритерапии) полагали. что понадобится 3 года, чтобы полностью очистить инфицированные ВИЧ клетки организма. Но последующие исследования показали, что процесс «полураспада»клеток значительно дольше, для полного очищения организма потребуется 60 лет. Поэтому при имеющихся средствах терапиивозможно только перевести процесс в хроническое течение, а полное излечение недоступно. Врачи медицинского факультета Университета Гете во Франкфурте при обследовании 60 больных ВИЧ/СПИДом установили, что через 36 недель после начала высоко активной антиретровирусной терапии у пациентов, ранее получавших противовирусные препараты, нередко отмечается увеличение показателей вирусной нагрузки. Это обусловлено все более широким распространением среди штаммов ВИЧ резистентности к антиретровирусным лекарствам. Устойчивость к ингибиторам протеазы была выявлена у 45% больных, начавших лечение этими препаратами, и почти у 90% больных, получавших невирапин. В целом резистентность к одному или нескольким противовирусным препаратам развилась в 75% случаев
 Активная антиретровирусная терапия требует не только значительных финансовых расходов, но определенный настрой больного, полное подчинение его жизни лечению, строгое соблюдение по часам режима приема лекарств без пропусков, пищевого и водного режима, полное исключение алкоголя и наркотиков. Поэтому врач лишь рекомендует больному активную антиретровирусную терапию, принимает окончательное решение сам больной, оценивая свои волевые качества. По данным американских специалистов около половины больных ВИЧ-инфекцией, находившихся на активной антиретровирусной терапии не смогли полностью реализовать схему лечения в течение одного года из-за ее сложности и огромного количества таблеток. Поэтому идут интенсивные поиски схем леченияс уменьшением числа приемов лекарственных средств. Так, созданкомбивир, содержащий половинную суточной дозы АЗТ и эпивира в одной таблетке (в России зарегистрирован в 1999 году). Активная антиретровирусная терапия не показана больным алкоголизмом, наркоманией, лицам с клиникой энцефалопатии, т. е. всем тем, кто не в состоянии контролировать свое поведение.
Активная антиретровирусная терапия требует не только значительных финансовых расходов, но определенный настрой больного, полное подчинение его жизни лечению, строгое соблюдение по часам режима приема лекарств без пропусков, пищевого и водного режима, полное исключение алкоголя и наркотиков. Поэтому врач лишь рекомендует больному активную антиретровирусную терапию, принимает окончательное решение сам больной, оценивая свои волевые качества. По данным американских специалистов около половины больных ВИЧ-инфекцией, находившихся на активной антиретровирусной терапии не смогли полностью реализовать схему лечения в течение одного года из-за ее сложности и огромного количества таблеток. Поэтому идут интенсивные поиски схем леченияс уменьшением числа приемов лекарственных средств. Так, созданкомбивир, содержащий половинную суточной дозы АЗТ и эпивира в одной таблетке (в России зарегистрирован в 1999 году). Активная антиретровирусная терапия не показана больным алкоголизмом, наркоманией, лицам с клиникой энцефалопатии, т. е. всем тем, кто не в состоянии контролировать свое поведение.
 При лечении активными антиретровирусными препаратами чаще придерживаются схемы: а) один из ингибиторов протеазы: индинавир нелфинавир ритонавир б) плюс одна из комбинаций следующих нуклеозидных аналогов: азидотимидин + диданозин ставудин + диданозин азидотимидин + зальцитабин азидотимидин + ламивудин ставудин + ламивудин
При лечении активными антиретровирусными препаратами чаще придерживаются схемы: а) один из ингибиторов протеазы: индинавир нелфинавир ритонавир б) плюс одна из комбинаций следующих нуклеозидных аналогов: азидотимидин + диданозин ставудин + диданозин азидотимидин + зальцитабин азидотимидин + ламивудин ставудин + ламивудин
 Саквинавир сейчас не рекомендуется как лечение 1 -й линии, так как он менее эффективен по сравнению с другими ингибиторами протеазы, поэтому CDC в 1997 году из 12 лекарственных средств активной антиретровирусной терапии рекомендовал к применению 11 препаратов. Вместо саквинавира входит в практику более эффективная версия саквинавира — фортоваза. Так как ингибиторы протеазы относятся к наиболее значимому компоненту терапии больных, большинство клиницистов не рекомендуют начинать терапию комбинацией, включающей лекарственные средства этой группы. Целесообразнее использовать комбинации: а) 2 нуклеозидных аналога и 1 ненуклеозидный ингибитор обратной транскриптазы; б) 3 нуклеозидных аналога. Только после неудачной попытки остановить патологический процесс этими комбинациями прибегают к третьему варианту: нуклеозидный ингибитор обратной транскриптазы + ненуклеозидный ингибитор обратной транскриптазы + ингибитор протеазы. Этим исчерпывается последний резерв терапии. Обобщенные данные по терапии ВИЧ-инфекции представлены в табл. 7.
Саквинавир сейчас не рекомендуется как лечение 1 -й линии, так как он менее эффективен по сравнению с другими ингибиторами протеазы, поэтому CDC в 1997 году из 12 лекарственных средств активной антиретровирусной терапии рекомендовал к применению 11 препаратов. Вместо саквинавира входит в практику более эффективная версия саквинавира — фортоваза. Так как ингибиторы протеазы относятся к наиболее значимому компоненту терапии больных, большинство клиницистов не рекомендуют начинать терапию комбинацией, включающей лекарственные средства этой группы. Целесообразнее использовать комбинации: а) 2 нуклеозидных аналога и 1 ненуклеозидный ингибитор обратной транскриптазы; б) 3 нуклеозидных аналога. Только после неудачной попытки остановить патологический процесс этими комбинациями прибегают к третьему варианту: нуклеозидный ингибитор обратной транскриптазы + ненуклеозидный ингибитор обратной транскриптазы + ингибитор протеазы. Этим исчерпывается последний резерв терапии. Обобщенные данные по терапии ВИЧ-инфекции представлены в табл. 7.
 Рекомендации разработанные Международным обществом по изучению СПИДа Рекомендащи, разработанные Департаментом здравоохршенняи социальнгой политики США совместно с семейным фондом Г. Дк. Кайзера Показания к началу ангиретровирус ной терапии 1. Острая ВИЧ-инфекция с клинической симптоматикой 2. Бессимтомное течение ВИЧ-инфекциикщси при чисяе лимфоцитов СD 4+ 5000 -10 000 юопий/мл 1. Острая ВИЧ-инфекция с клинической симптоматикой 2. Бессимптомное течение ВИЧ-инфекции при числе лимфоцитов CD 4+ 10 000 копий/мл (метод р-ДНК) * или >20 000 копий/мл (метод ОТ-ПЦР)** Начальная антиретровирус ная терапия Оптимальная схема: 2 НИОТ + 1 высгкоактивный ИП Альтернативные схемы: 1. Два НИ ОТ+ННИ ОТ 2. Два ИП; 2 ИП+ 1 -2 НИ ОТ 3. Один ИП+1 -2 НИ ОТ Оптимальная схема: два НИОТ + 1 высокоактивный ИП ипи 1 -2 НИОТ + 2 ИП (ритонавир и саквинавир) Альтернативные схемы: 1. Два HИ OT+ 1 ННИ ОТ (невирапин или делавирдин) или два НИ ОТ+ 1 ИП (саквинавир) 2. Два HИ OT Показания к изменению антиретровирус ной терапии 1. Неполное снижение уровня РНК ВИЧ, оставшегося в диапазоне от 50 до 5000 копий/мл 2. Снижение числа лимфоцитов CD 4+, ухудшение кпи-ничесвого состояния Неполное снижение уровня РНК ВИЧ (>500 копий/мл) Снижение числа лимфоцитов CD 4+
Рекомендации разработанные Международным обществом по изучению СПИДа Рекомендащи, разработанные Департаментом здравоохршенняи социальнгой политики США совместно с семейным фондом Г. Дк. Кайзера Показания к началу ангиретровирус ной терапии 1. Острая ВИЧ-инфекция с клинической симптоматикой 2. Бессимтомное течение ВИЧ-инфекциикщси при чисяе лимфоцитов СD 4+ 5000 -10 000 юопий/мл 1. Острая ВИЧ-инфекция с клинической симптоматикой 2. Бессимптомное течение ВИЧ-инфекции при числе лимфоцитов CD 4+ 10 000 копий/мл (метод р-ДНК) * или >20 000 копий/мл (метод ОТ-ПЦР)** Начальная антиретровирус ная терапия Оптимальная схема: 2 НИОТ + 1 высгкоактивный ИП Альтернативные схемы: 1. Два НИ ОТ+ННИ ОТ 2. Два ИП; 2 ИП+ 1 -2 НИ ОТ 3. Один ИП+1 -2 НИ ОТ Оптимальная схема: два НИОТ + 1 высокоактивный ИП ипи 1 -2 НИОТ + 2 ИП (ритонавир и саквинавир) Альтернативные схемы: 1. Два HИ OT+ 1 ННИ ОТ (невирапин или делавирдин) или два НИ ОТ+ 1 ИП (саквинавир) 2. Два HИ OT Показания к изменению антиретровирус ной терапии 1. Неполное снижение уровня РНК ВИЧ, оставшегося в диапазоне от 50 до 5000 копий/мл 2. Снижение числа лимфоцитов CD 4+, ухудшение кпи-ничесвого состояния Неполное снижение уровня РНК ВИЧ (>500 копий/мл) Снижение числа лимфоцитов CD 4+
 ПРИМЕЧАНИЕ: * k- метод определения уровня РНК ВИЧ с использованием разветвленной ДНК; ** — полимеразная цепная реакция с использованием обратной транскориптазы; НИ ОТ- нуклеозидные ингибиторы обратной транскриптазы; ННИ ОТ -ненуклеозидные ингибоиторы обратной транскриптазы; ИП -ингибиторы протеазы.
ПРИМЕЧАНИЕ: * k- метод определения уровня РНК ВИЧ с использованием разветвленной ДНК; ** — полимеразная цепная реакция с использованием обратной транскориптазы; НИ ОТ- нуклеозидные ингибиторы обратной транскриптазы; ННИ ОТ -ненуклеозидные ингибоиторы обратной транскриптазы; ИП -ингибиторы протеазы.
 Перед началом активной антиретровирусной терапии проводится полное клинико-лабораторное обследование больного, в том числе уровень вирусной нагрузки на плазму и + Т-лимфоцитов. Если нет клинических симптомов болезни, а количество CD 4+ клеток > 500 в мкл, вирусная нагрузка на плазму менее 10 000 в b. ДНК или 20 000 в RT-PCR (полимеразная цепная реакция), то, по мнению одних клиницистов, от проводимой терапии надо воздержаться, по мнению других- приступить к лечению немедленно, пока иммунная система не подавлена или подавлена умеренно. В случае, если клинических проявлений болезни нет, но уровень CD 4+ клеток < 500 в мкл или вирусная нагрузка на плазму выше 10 000 в b. ДНК или ОТ-ПЦР, необходимо серьезно думать о начале активной антиретровирусной терапии. В случае наличия клиники ВИЧ-инфекции необходимо приступить к терапии без учета количества CD 4+ клеток и уровня вирусной нагрузки на плазму. Большинство клиницистов придерживается точки зрения, что антиретровирусную терапию необходимо начинать при уровне CD 4 -клеток менее 350 в 1 мм 3. Но при этом необходимо учитывать динамику, т. е. предыдущий показатель CD 4+ клеток ниже 350 – это одна ситуация (идет нарастание этих клеток), а выше 350 – другая (динамика угнетения иммунной системы).
Перед началом активной антиретровирусной терапии проводится полное клинико-лабораторное обследование больного, в том числе уровень вирусной нагрузки на плазму и + Т-лимфоцитов. Если нет клинических симптомов болезни, а количество CD 4+ клеток > 500 в мкл, вирусная нагрузка на плазму менее 10 000 в b. ДНК или 20 000 в RT-PCR (полимеразная цепная реакция), то, по мнению одних клиницистов, от проводимой терапии надо воздержаться, по мнению других- приступить к лечению немедленно, пока иммунная система не подавлена или подавлена умеренно. В случае, если клинических проявлений болезни нет, но уровень CD 4+ клеток < 500 в мкл или вирусная нагрузка на плазму выше 10 000 в b. ДНК или ОТ-ПЦР, необходимо серьезно думать о начале активной антиретровирусной терапии. В случае наличия клиники ВИЧ-инфекции необходимо приступить к терапии без учета количества CD 4+ клеток и уровня вирусной нагрузки на плазму. Большинство клиницистов придерживается точки зрения, что антиретровирусную терапию необходимо начинать при уровне CD 4 -клеток менее 350 в 1 мм 3. Но при этом необходимо учитывать динамику, т. е. предыдущий показатель CD 4+ клеток ниже 350 – это одна ситуация (идет нарастание этих клеток), а выше 350 – другая (динамика угнетения иммунной системы).
 Могут быть расхождения между изменениями числа клеток CD 4+ и уровней РНК ВИЧ в плазме, они выявлены у 20% больных, что может затруднить принятие решений в отношении антиретровирусной терапии. Это может быть связано с рядом факторов, влияющих на определение РНК ВИЧ в плазме. Вирусная нагрузка и ее изменения считаются более информативными принятии решений об антиретровирусной терапии по сравнению с определением числа клеток CD 4 +. Прирешении вопроса лечения активными антиретровирусными препаратами учитывается: желание больноголечиться, степень иммунодефицита, которую оценивают на основании числа CD 4 Т-клеток, риск прогрессирования болезни, который определяют на основании измерения вирусной нагрузки, оценка потенциальной пользы и риска терапии у данного больного, особенно с бессимптомной инфекцией. Накопленный за эти годы опыт показал, что принцип подхода к лечению больных ВИЧ-инфекцией– как при сахарном диабете -пожизненное применение антиретровирусных препаратов. Правда в последнее время разрабатывается схема прерывистого приема лекарственных средств с тенденцией все возрастающих “окон” между циклами приема.
Могут быть расхождения между изменениями числа клеток CD 4+ и уровней РНК ВИЧ в плазме, они выявлены у 20% больных, что может затруднить принятие решений в отношении антиретровирусной терапии. Это может быть связано с рядом факторов, влияющих на определение РНК ВИЧ в плазме. Вирусная нагрузка и ее изменения считаются более информативными принятии решений об антиретровирусной терапии по сравнению с определением числа клеток CD 4 +. Прирешении вопроса лечения активными антиретровирусными препаратами учитывается: желание больноголечиться, степень иммунодефицита, которую оценивают на основании числа CD 4 Т-клеток, риск прогрессирования болезни, который определяют на основании измерения вирусной нагрузки, оценка потенциальной пользы и риска терапии у данного больного, особенно с бессимптомной инфекцией. Накопленный за эти годы опыт показал, что принцип подхода к лечению больных ВИЧ-инфекцией– как при сахарном диабете -пожизненное применение антиретровирусных препаратов. Правда в последнее время разрабатывается схема прерывистого приема лекарственных средств с тенденцией все возрастающих “окон” между циклами приема.
 Такимобразом, достигнуты отчетливые положительные эффекты у больных ВИЧ-инфекцией с момента внедрения активной антиретровирусной терапии, которая позволяет снизить уровень вирусной нагрузки на плазму до неопределяемого уровня, повысить уровень CD 4+ клеток в крови, предотвратить присоединение суперинфекции, а в целом перевести заболевание в хроническое течение. Вместе с тем, добиться положительного эффекта удается только у 70 -80% больных получивших полный курс лечения при отсутствии полного выздоровления, (при терапии различных бактериальных заболеваний антибиотиками положительный эффект с полным выздоровлением достигается в 99%), причем почти половина больных, начавших лечение вынуждена его прервать из-за побочных эффектов. Более чем у 90% больных, у которых удалось снизить вирусную нагрузку на плазму до неопределяемых уровней (<400 копий), достигается это через 12 недель после начала терапии, а ниже 20 -50 копий – еще на несколько недель позже. Если через 5 мес. от начала антиретровирусной терапии вирусная нагрузка на плазму выше 400 копий, эффект лечения расценивается как отрицательный.
Такимобразом, достигнуты отчетливые положительные эффекты у больных ВИЧ-инфекцией с момента внедрения активной антиретровирусной терапии, которая позволяет снизить уровень вирусной нагрузки на плазму до неопределяемого уровня, повысить уровень CD 4+ клеток в крови, предотвратить присоединение суперинфекции, а в целом перевести заболевание в хроническое течение. Вместе с тем, добиться положительного эффекта удается только у 70 -80% больных получивших полный курс лечения при отсутствии полного выздоровления, (при терапии различных бактериальных заболеваний антибиотиками положительный эффект с полным выздоровлением достигается в 99%), причем почти половина больных, начавших лечение вынуждена его прервать из-за побочных эффектов. Более чем у 90% больных, у которых удалось снизить вирусную нагрузку на плазму до неопределяемых уровней (<400 копий), достигается это через 12 недель после начала терапии, а ниже 20 -50 копий – еще на несколько недель позже. Если через 5 мес. от начала антиретровирусной терапии вирусная нагрузка на плазму выше 400 копий, эффект лечения расценивается как отрицательный.
 Даже при положительном эффекте не прекращается репликация вируса, ибо, как показали накопленный опыт и проведенные целенаправленные исследования, вирус сохраняется в лимфатических узлах. Эффект от терапии сравнительно не продолжителен. Даже при самом оптимальном варианте больной должен настроится на лечение в течение 20 -30 лет. Многие вопросы еще надо решать, прежде чем будет достигнуто восстановление иммунитета у больного ВИЧ-инфекцией. Как полагает J. Laurence (1998), в лижайшем будующем будут внедрены новые эффективные препараты — цитокины. В перспективе выращивание новой ткани тимуса или трансформирование функции существующейлимфоидной тканив кишечнике и лимфатических узлах, чтобы помочь формированию Т-клеток. Сегодня идет интенсивный поиск новых препаратов с антиретровирусным эффектом. так, установлено. что сине-зеленые водоросли Nostoc ellipsosporum содержат белок циановирин-N, который может стать основой нового поколения лекарств против ВИЧ-инфекции. Лабораторные исследования показали, что этот протеин не только подавляет активность различных штаммов вируса иммунодефицита, но также препятствует его проникновению в клетки иммунной системы. Экспериментальные данные позволяют надеяться, что циановирин-N удастся использовать для изготовления фильтров, освобождающих кровь от возбудителя СПИДа. (Бойд М. ,
Даже при положительном эффекте не прекращается репликация вируса, ибо, как показали накопленный опыт и проведенные целенаправленные исследования, вирус сохраняется в лимфатических узлах. Эффект от терапии сравнительно не продолжителен. Даже при самом оптимальном варианте больной должен настроится на лечение в течение 20 -30 лет. Многие вопросы еще надо решать, прежде чем будет достигнуто восстановление иммунитета у больного ВИЧ-инфекцией. Как полагает J. Laurence (1998), в лижайшем будующем будут внедрены новые эффективные препараты — цитокины. В перспективе выращивание новой ткани тимуса или трансформирование функции существующейлимфоидной тканив кишечнике и лимфатических узлах, чтобы помочь формированию Т-клеток. Сегодня идет интенсивный поиск новых препаратов с антиретровирусным эффектом. так, установлено. что сине-зеленые водоросли Nostoc ellipsosporum содержат белок циановирин-N, который может стать основой нового поколения лекарств против ВИЧ-инфекции. Лабораторные исследования показали, что этот протеин не только подавляет активность различных штаммов вируса иммунодефицита, но также препятствует его проникновению в клетки иммунной системы. Экспериментальные данные позволяют надеяться, что циановирин-N удастся использовать для изготовления фильтров, освобождающих кровь от возбудителя СПИДа. (Бойд М. ,
 Активная антиретровирусная терапия не полностью восстанавливает иммунную систему. Через 8 недель лечения клеточный иммунный ответ на некоторые, но не на все антигены восстанавливается, однако, совсем не восстанавливается иммунный ответ на ВИЧ. Это диктует необходимость внедрения принципиально новых методов терапии, направленной на усиление клеточно-опосредованного иммунитета. В частности проводятся исследования по иммунотерапии. Для этих целей предложен ремун — лишенная gp 120 инактивированная вакцина из цельного вируса. У больных ВИЧ-инфекцией с CD 4 > 350 в 1 мкл, лечившихся активной антиретровирусной терапией, а затем ВИЧ-иммуногеном значительно растет in vitro Т-хелперный ответ на вакцинный антиген, рекомбинантный р24 и цельную вирусную ВИЧ другого типа. Активная антиретровирусная терапия требует не только значительных финансовых расходов, но определенный настрой больного, полное подчинение его жизни лечению, строгое соблюдение по часам режима приема лекарств без пропусков, пищевого и водного режима, полное исключение алкоголя и наркотиков. Поэтому врач лишь рекомендует больному активную антиретровирусную терапию, принимает окончательное решение сам больной, оценивая свои волевые качества.
Активная антиретровирусная терапия не полностью восстанавливает иммунную систему. Через 8 недель лечения клеточный иммунный ответ на некоторые, но не на все антигены восстанавливается, однако, совсем не восстанавливается иммунный ответ на ВИЧ. Это диктует необходимость внедрения принципиально новых методов терапии, направленной на усиление клеточно-опосредованного иммунитета. В частности проводятся исследования по иммунотерапии. Для этих целей предложен ремун — лишенная gp 120 инактивированная вакцина из цельного вируса. У больных ВИЧ-инфекцией с CD 4 > 350 в 1 мкл, лечившихся активной антиретровирусной терапией, а затем ВИЧ-иммуногеном значительно растет in vitro Т-хелперный ответ на вакцинный антиген, рекомбинантный р24 и цельную вирусную ВИЧ другого типа. Активная антиретровирусная терапия требует не только значительных финансовых расходов, но определенный настрой больного, полное подчинение его жизни лечению, строгое соблюдение по часам режима приема лекарств без пропусков, пищевого и водного режима, полное исключение алкоголя и наркотиков. Поэтому врач лишь рекомендует больному активную антиретровирусную терапию, принимает окончательное решение сам больной, оценивая свои волевые качества.
 По данным американских специалистов около половины больных ВИЧ-инфекцией, находившихся на активной антиретровирусной терапии не смогли полностью реализовать схему лечения в течение одного года из-за ее сложности и огромного количества таблеток. Поэтому идут интенсивные поиски схем леченияс уменьшением числа приемов лекарственных средств. Так, созданкомбивир, содержащий половинную суточной дозы АЗТ и эпивира в одной таблетке (в России зарегистрирован в 1999 году). Активная антиретровирусная терапия противопоказана больным алкоголизмом, наркоманией, лицам с клиникой энцефалопатии, т. е. всем тем, кто не в состоянии контролировать свое поведение
По данным американских специалистов около половины больных ВИЧ-инфекцией, находившихся на активной антиретровирусной терапии не смогли полностью реализовать схему лечения в течение одного года из-за ее сложности и огромного количества таблеток. Поэтому идут интенсивные поиски схем леченияс уменьшением числа приемов лекарственных средств. Так, созданкомбивир, содержащий половинную суточной дозы АЗТ и эпивира в одной таблетке (в России зарегистрирован в 1999 году). Активная антиретровирусная терапия противопоказана больным алкоголизмом, наркоманией, лицам с клиникой энцефалопатии, т. е. всем тем, кто не в состоянии контролировать свое поведение
 Терапия больных в бессимптомной фазе ВИЧ-инфекцией. Если вопрос о необходимости антиретровирусной терапии больных с клиническими проявлениями ВИЧ-инфекции дискуссий не вызывает и все решают финансовые возможности государства и больного человека, то лечебная тактика больных в бессимптомной фазе более сложен. Принято считать, что даже при отсутствии клинических проявлений ВИЧ-инфекции (в отличии от большинства других инфекционных заболеваний по внешнему виду больного ВИЧ-инфекцией нельзя определить состояние болезни) любому больному с содержанием клеток CD 4+ <500/мм 3 или содержанием в плазме копий РНК ВИЧ более 10 000 (при определении методом гибридизации с использовании разветвленных зондов — b. ДНК) или 20. 000 (с помощью ОТ-ПЦР) в 1 мл должно быть предложено лечение антиретровирусными препаратами. Обоснованием этому является то обстоятельство, что четко прослеживается взаимосвязь между вирусной нагрузкой, количеством клеток CD 4 + и скоростью прогрессирования ВИЧ-инфекции в СПИД (табл. 8).
Терапия больных в бессимптомной фазе ВИЧ-инфекцией. Если вопрос о необходимости антиретровирусной терапии больных с клиническими проявлениями ВИЧ-инфекции дискуссий не вызывает и все решают финансовые возможности государства и больного человека, то лечебная тактика больных в бессимптомной фазе более сложен. Принято считать, что даже при отсутствии клинических проявлений ВИЧ-инфекции (в отличии от большинства других инфекционных заболеваний по внешнему виду больного ВИЧ-инфекцией нельзя определить состояние болезни) любому больному с содержанием клеток CD 4+ <500/мм 3 или содержанием в плазме копий РНК ВИЧ более 10 000 (при определении методом гибридизации с использовании разветвленных зондов — b. ДНК) или 20. 000 (с помощью ОТ-ПЦР) в 1 мл должно быть предложено лечение антиретровирусными препаратами. Обоснованием этому является то обстоятельство, что четко прослеживается взаимосвязь между вирусной нагрузкой, количеством клеток CD 4 + и скоростью прогрессирования ВИЧ-инфекции в СПИД (табл. 8).
 Таблица 8 Риск прогрессирования ВИЧ-инфекции CD 4 < 350 в мкл Вирусная нагрузка на плазму % СПИДа b. ДНК ОТ-ПЦР 3 года 6 лет 9 лет < 500 30000 >55000 72, 9 92, 7 95, 6 CD 4 < 351 -500 в мкл < 500 30 000 >55 000 47, 9 77, 7 94, 4 CD 4 500 в мкл < 500 30 000 >55 000 32, 6 66, 8 76,
Таблица 8 Риск прогрессирования ВИЧ-инфекции CD 4 < 350 в мкл Вирусная нагрузка на плазму % СПИДа b. ДНК ОТ-ПЦР 3 года 6 лет 9 лет < 500 30000 >55000 72, 9 92, 7 95, 6 CD 4 < 351 -500 в мкл < 500 30 000 >55 000 47, 9 77, 7 94, 4 CD 4 500 в мкл < 500 30 000 >55 000 32, 6 66, 8 76,
 На сегодня имеется два основных подхода к началу терапии у бессимптомных больных ВИЧ-инфекцией. Одни клиницисты, полагая, что. ВИЧ-инфекциявсегда носит прогрессирующий характер, придерживаются более агрессивного подхода с назначением лечения. Другие придерживаются более сдержанного подхода, лечение не назначают сразу, полагая, что больной нуждается в наблюдении врача, но лечение может быть назначено позднее. В этом плане интересна смена позиций одного из крупнейших специалистов по лечению больных, С. Велла(Италия): в 1998 году на наш вопрос, когда начинать активную антиретровирусную терапию, он ответил: “если бы мне поставили диагноз сейчас, то я сразу начал лечиться”, а через 2 года, в 200 году вопрос ему был повторен и ссылаясь на накопленный опыт, он уже считал, что с ранней терапией спешить не следует, необходимо наблюдать и контролировать уровень вирусной нагрузки и содержание CD 4+ клеток. Сторонники агрессивного подхода обосновывают свое мнение на том, чтолечение должно начинаться до развития значительной иммуносупрессии, а целью лечения должно быть достижения неопределяемого уровня виремии. По их мнению всем больнымс числом клеток CD 4+ <500/мм 3 должна назначаться антиретровирусная терапия, так же как и больным с более высокими числами клеток CD 4+, у которых вирусная нагрузка в плазме составляет более 10. 000 (b. ДНК) или 20. 000 (ОТ-ПЦР) в 1 мл.
На сегодня имеется два основных подхода к началу терапии у бессимптомных больных ВИЧ-инфекцией. Одни клиницисты, полагая, что. ВИЧ-инфекциявсегда носит прогрессирующий характер, придерживаются более агрессивного подхода с назначением лечения. Другие придерживаются более сдержанного подхода, лечение не назначают сразу, полагая, что больной нуждается в наблюдении врача, но лечение может быть назначено позднее. В этом плане интересна смена позиций одного из крупнейших специалистов по лечению больных, С. Велла(Италия): в 1998 году на наш вопрос, когда начинать активную антиретровирусную терапию, он ответил: “если бы мне поставили диагноз сейчас, то я сразу начал лечиться”, а через 2 года, в 200 году вопрос ему был повторен и ссылаясь на накопленный опыт, он уже считал, что с ранней терапией спешить не следует, необходимо наблюдать и контролировать уровень вирусной нагрузки и содержание CD 4+ клеток. Сторонники агрессивного подхода обосновывают свое мнение на том, чтолечение должно начинаться до развития значительной иммуносупрессии, а целью лечения должно быть достижения неопределяемого уровня виремии. По их мнению всем больнымс числом клеток CD 4+ <500/мм 3 должна назначаться антиретровирусная терапия, так же как и больным с более высокими числами клеток CD 4+, у которых вирусная нагрузка в плазме составляет более 10. 000 (b. ДНК) или 20. 000 (ОТ-ПЦР) в 1 мл.
 Сторонники более консервативного подхода к началу терапии у бессимптомных больных полагают, чтолечение не следует назначать лицам с содержанием клеток CD 4+ <500/мм 3 и низким уровнем виремии, у которых риск быстрого прогрессирования заболевания невелик, необходим лишь мониторинг лабораторных показателейза исключением тех, кто имеет значительный риск быстрого прогрессирования заболевания из-за высокой вирусной нагрузки. Если принято решение о необходимости терапии, у лиц, не получавшему раньше антиретровирусные препараты, должен быть назначен режим терапии, который может помочь достичь значительное снижение содержания РНК ВИЧ в плазме крови, значительное повышение числа клеток CD 4+ замедление прогрессирования заболевания до стадии СПИДа и смерти.
Сторонники более консервативного подхода к началу терапии у бессимптомных больных полагают, чтолечение не следует назначать лицам с содержанием клеток CD 4+ <500/мм 3 и низким уровнем виремии, у которых риск быстрого прогрессирования заболевания невелик, необходим лишь мониторинг лабораторных показателейза исключением тех, кто имеет значительный риск быстрого прогрессирования заболевания из-за высокой вирусной нагрузки. Если принято решение о необходимости терапии, у лиц, не получавшему раньше антиретровирусные препараты, должен быть назначен режим терапии, который может помочь достичь значительное снижение содержания РНК ВИЧ в плазме крови, значительное повышение числа клеток CD 4+ замедление прогрессирования заболевания до стадии СПИДа и смерти.
 В 1999 году A. S. Fauchi с соавт. разработали схему приема антиретровирусных препаратов для больных ВИЧ-инфекцией. Схема (табл. 9 ) включает один выбор из колонки А и один из колонки В (препараты в колонках расположены не в порядке приоритетности): В качестве альтернативной терапии рекомендуется авторами схема приема комбинации: абакавир+АЗТ+эпивир. Не рекомендуется назначать больным варианты: любая монотерапия АЗТ+ставудин -зальцитабин+диданозин зальцитабин+ставудин -зальцитабин+эпивир.
В 1999 году A. S. Fauchi с соавт. разработали схему приема антиретровирусных препаратов для больных ВИЧ-инфекцией. Схема (табл. 9 ) включает один выбор из колонки А и один из колонки В (препараты в колонках расположены не в порядке приоритетности): В качестве альтернативной терапии рекомендуется авторами схема приема комбинации: абакавир+АЗТ+эпивир. Не рекомендуется назначать больным варианты: любая монотерапия АЗТ+ставудин -зальцитабин+диданозин зальцитабин+ставудин -зальцитабин+эпивир.
 Таблица 9 Схемы выбора комбинации антиретровирусных препаратов Колонка А Колонка В Индинавир Нельфинавир Ритонавир Саквинавир Ритонавир+саквинавир Ифавиренц АЗТ+диданозин Дидинозин+ставудин АЗТ+эпивир Эпивир+ставудин Эпивир+диданозин
Таблица 9 Схемы выбора комбинации антиретровирусных препаратов Колонка А Колонка В Индинавир Нельфинавир Ритонавир Саквинавир Ритонавир+саквинавир Ифавиренц АЗТ+диданозин Дидинозин+ставудин АЗТ+эпивир Эпивир+ставудин Эпивир+диданозин
 Перед началом активной антиретровирусной терапии проводится полное клинико-лабораторное обследование больного, в том числе уровень вирусной нагрузки на плазму и количество CD 4+ Т-лимфоцитов. Таким образом, согласно накопленному опыту, если нет клинических симптомов болезни, а количество CD 4+ клеток > 500 в мкл, вирусная нагрузка на плазму менее 10 000 в b. ДНК или 20 000 в ОТ-ПЦР (полимеразная цепная реакция), то, по мнению одних клиницистов, от проводимой терапии надо воздержаться, по мнению других- приступить к лечению немедленно, пока иммунная система не подавлена или подавлена умеренно. В случае, если клинических проявлений болезни нет, но уровень CD 4+ клеток < 500 в мкл (в последнее время все больше клиницисты склоняются к мысли, что рубежом служить показатель CD 4 < 350 клеток/мм 3 ) или вирусная нагрузка на плазму выше 10 000 в b. ДНК или ОТ-ПЦР, необходимо серьезно думать о начале активной антиретровирусной терапии. В случае наличия клиники ВИЧ-инфекции необходимо приступить к терапии без учета количества CD 4+ клеток и уровня вирусной нагрузки на плазму.
Перед началом активной антиретровирусной терапии проводится полное клинико-лабораторное обследование больного, в том числе уровень вирусной нагрузки на плазму и количество CD 4+ Т-лимфоцитов. Таким образом, согласно накопленному опыту, если нет клинических симптомов болезни, а количество CD 4+ клеток > 500 в мкл, вирусная нагрузка на плазму менее 10 000 в b. ДНК или 20 000 в ОТ-ПЦР (полимеразная цепная реакция), то, по мнению одних клиницистов, от проводимой терапии надо воздержаться, по мнению других- приступить к лечению немедленно, пока иммунная система не подавлена или подавлена умеренно. В случае, если клинических проявлений болезни нет, но уровень CD 4+ клеток < 500 в мкл (в последнее время все больше клиницисты склоняются к мысли, что рубежом служить показатель CD 4 < 350 клеток/мм 3 ) или вирусная нагрузка на плазму выше 10 000 в b. ДНК или ОТ-ПЦР, необходимо серьезно думать о начале активной антиретровирусной терапии. В случае наличия клиники ВИЧ-инфекции необходимо приступить к терапии без учета количества CD 4+ клеток и уровня вирусной нагрузки на плазму.
 Существенным тормозом к широкому применению “тритерапии” ВИЧ-инфекции относится ее дороговизна – около 1000 долл. США в месяц на 1 больного, 12 тыс. долларов в год. В 1996 году на СПИД в США тратилось менее 1% всех расходов на здравоохранение: 6, 7 млад. долларов или около 20 000 на одного больного в год. На конец 1998 года получали активную антиретровирусную терапию 385 000 американцев, не лечились только больные ВИЧ-инфекцией с бессимптомным течением и те, у кого имелась ранняя стадия болезни. В 1 квартале 1998 года 80% больных получали по крайней мере 1 ингибитор протеазы или ненуклеозидные ингибиторы обратной транскриптазы, 70% получали тритерапию.
Существенным тормозом к широкому применению “тритерапии” ВИЧ-инфекции относится ее дороговизна – около 1000 долл. США в месяц на 1 больного, 12 тыс. долларов в год. В 1996 году на СПИД в США тратилось менее 1% всех расходов на здравоохранение: 6, 7 млад. долларов или около 20 000 на одного больного в год. На конец 1998 года получали активную антиретровирусную терапию 385 000 американцев, не лечились только больные ВИЧ-инфекцией с бессимптомным течением и те, у кого имелась ранняя стадия болезни. В 1 квартале 1998 года 80% больных получали по крайней мере 1 ингибитор протеазы или ненуклеозидные ингибиторы обратной транскриптазы, 70% получали тритерапию.
 Лечение больных в фазе острой сероконверсии. Необходимость лечения больных в фазе синдрома острой сероконверсии (СОС) продиктована теми обстоятельствами, что нужно активное влияние на прогрессирование болезни, уменьшить вирусную диссеминацию, остановить процесс на новом устойчивом состоянии. В этом периоде болезни уровень вирусной репликации очень высок, но вирусная популяция наиболее гомогенна, а иммунная система остается относительно интактной. Вместе с тем, многие больные в этот период не попадают еще в поле зрения врача, поэтому опыт лечения больных не велик. В. Tindall. et al. (1991) провели лечение зидовудином (1, 0 в день) в течение 56 дней 14 больных в стадии СОС и сравнили с показателями динамики CD 4+ лимфоцитов и временем перехода в СПИД 28 больных этой же стадии, но не получивших антиретровирусную терапию. В группе леченных зидовудином у 1 из 14 за 12 мес. развился СПИД, а в группе не получивших лечение – у 7 из 28 больных. Не так выражено за период наблюдения и было падение СD 4+ клеток у получавших зидовудин больных.
Лечение больных в фазе острой сероконверсии. Необходимость лечения больных в фазе синдрома острой сероконверсии (СОС) продиктована теми обстоятельствами, что нужно активное влияние на прогрессирование болезни, уменьшить вирусную диссеминацию, остановить процесс на новом устойчивом состоянии. В этом периоде болезни уровень вирусной репликации очень высок, но вирусная популяция наиболее гомогенна, а иммунная система остается относительно интактной. Вместе с тем, многие больные в этот период не попадают еще в поле зрения врача, поэтому опыт лечения больных не велик. В. Tindall. et al. (1991) провели лечение зидовудином (1, 0 в день) в течение 56 дней 14 больных в стадии СОС и сравнили с показателями динамики CD 4+ лимфоцитов и временем перехода в СПИД 28 больных этой же стадии, но не получивших антиретровирусную терапию. В группе леченных зидовудином у 1 из 14 за 12 мес. развился СПИД, а в группе не получивших лечение – у 7 из 28 больных. Не так выражено за период наблюдения и было падение СD 4+ клеток у получавших зидовудин больных.
 S. Kinloch-de Loss et al. (1995, 1997) двойным слепым методом изучили эффективность зидовудина при 6 -месячной терапии в дозе 250 мг 39 больных в стадии клинический выраженного СОС и сравнили с динамикой болезни у 38 больных этой же стадии, но не получивших терапии. В группе получавших зидовудин были более высокие показатели CD 4+, снижение вирусной нагрузки на плазму наблюдалось в обеих группах, но в группе получавших антиретровирусную терапию оно более выражно, хотя и без статистической значимости различий в группах. В последующие 15 мес. в значительно меньшей степени наблюдалось наслоение таких суперинфекций как оральный кандидоз, опоясывающий герпес, оральная волосатая лейкоплакия среди лиц, получивших лечение зидовудином. Но дальнейшие наблюдения в сроки до 28 мес. показали исчезновение разницы между группами, что дало авторам основание высказать мнение о необходимости проведения более массивной антиретровирусной терапии. L. Perrin et al. (1996) изучили влияние 6 -месячной терапии зидовудином и невирапином на вирусемию, уровень провирусной ДНК, содержание CD 4+ и CD 8+ клеток с последующим наблюдением в течение 1, 5 лет. Правда, в стадии СОС было всего 4 больных, но у 2 из них в результате лечения вирусемия исчезла (менее 200 копий/мл РНК ВИЧ) во время лечения, у 3 из 4 больных содержание CD 4+ и CD 8+ клеток находилось в пределах нормы в период лечения.
S. Kinloch-de Loss et al. (1995, 1997) двойным слепым методом изучили эффективность зидовудина при 6 -месячной терапии в дозе 250 мг 39 больных в стадии клинический выраженного СОС и сравнили с динамикой болезни у 38 больных этой же стадии, но не получивших терапии. В группе получавших зидовудин были более высокие показатели CD 4+, снижение вирусной нагрузки на плазму наблюдалось в обеих группах, но в группе получавших антиретровирусную терапию оно более выражно, хотя и без статистической значимости различий в группах. В последующие 15 мес. в значительно меньшей степени наблюдалось наслоение таких суперинфекций как оральный кандидоз, опоясывающий герпес, оральная волосатая лейкоплакия среди лиц, получивших лечение зидовудином. Но дальнейшие наблюдения в сроки до 28 мес. показали исчезновение разницы между группами, что дало авторам основание высказать мнение о необходимости проведения более массивной антиретровирусной терапии. L. Perrin et al. (1996) изучили влияние 6 -месячной терапии зидовудином и невирапином на вирусемию, уровень провирусной ДНК, содержание CD 4+ и CD 8+ клеток с последующим наблюдением в течение 1, 5 лет. Правда, в стадии СОС было всего 4 больных, но у 2 из них в результате лечения вирусемия исчезла (менее 200 копий/мл РНК ВИЧ) во время лечения, у 3 из 4 больных содержание CD 4+ и CD 8+ клеток находилось в пределах нормы в период лечения.
 A. Lafeullade et al. (1997) применили в сочетании зидовудин, диданозин и ламивудин у 10 больных в фазе острой сероконверсии, лечение начали через 5 -28 дней после появления первых клинических проявлений болезни. При этом выявлено снижение РНК ВИЧ в плазме до уровня ниже 200 копий/мл у всех больных в среднем через 108± 32 дня. У больных, лечение у которых началось до 15 дня от момента появления клиники, РКН ВИЧ в плазме нельзя было выявить к 54± 18 дню против 162± 55 дней у тех, лечение у которых начиналось позже. Терапия 3 препаратами приводила также к значительному повышению средних значений соотношения CD 4/CD 8 через 2 мес. терапии за счет повышения уровня CD 4+ и снижения CD 8+ клеток. В отличие от более ранних наблюдений авторов, когда терапия проводилась одним или двумя препаратами, терапия тремя антиретровирусными препаратами было значительно эффективней. К такому же выводу пришел F. Hecht et al. (1998), лечившие 13 больных нельфинавиром, зидовудином и ламивудином. В литературе описан случай, когда больному в фазе острой сероконверсии с яркими клиническими проявлениями было начало лечение зидовудином в комбинации с ламивудином и ритонавиром, но спустя 6 мес. больной прервал лечение. Через 35 дней после прекращения лечения у него вновь развилась клиника синдрома острой сероконверсии, в частности появились лихорадка, фарингит, сыпь, лейкопения, тромбоцитопения, уровень РНК ВИЧ повысился до 1 800 000 копий/мл. Наблюдение демонстрирует эффективность активной антиретровирусной терапии в подавлении клинических проявлений у больного в фазе острой сероконверсии.
A. Lafeullade et al. (1997) применили в сочетании зидовудин, диданозин и ламивудин у 10 больных в фазе острой сероконверсии, лечение начали через 5 -28 дней после появления первых клинических проявлений болезни. При этом выявлено снижение РНК ВИЧ в плазме до уровня ниже 200 копий/мл у всех больных в среднем через 108± 32 дня. У больных, лечение у которых началось до 15 дня от момента появления клиники, РКН ВИЧ в плазме нельзя было выявить к 54± 18 дню против 162± 55 дней у тех, лечение у которых начиналось позже. Терапия 3 препаратами приводила также к значительному повышению средних значений соотношения CD 4/CD 8 через 2 мес. терапии за счет повышения уровня CD 4+ и снижения CD 8+ клеток. В отличие от более ранних наблюдений авторов, когда терапия проводилась одним или двумя препаратами, терапия тремя антиретровирусными препаратами было значительно эффективней. К такому же выводу пришел F. Hecht et al. (1998), лечившие 13 больных нельфинавиром, зидовудином и ламивудином. В литературе описан случай, когда больному в фазе острой сероконверсии с яркими клиническими проявлениями было начало лечение зидовудином в комбинации с ламивудином и ритонавиром, но спустя 6 мес. больной прервал лечение. Через 35 дней после прекращения лечения у него вновь развилась клиника синдрома острой сероконверсии, в частности появились лихорадка, фарингит, сыпь, лейкопения, тромбоцитопения, уровень РНК ВИЧ повысился до 1 800 000 копий/мл. Наблюдение демонстрирует эффективность активной антиретровирусной терапии в подавлении клинических проявлений у больного в фазе острой сероконверсии.
 Активная антиретровирусная терапия и восстановление функции иммунной системы. Сегодня идет изучение пределов, до которых возможно восстановление поврежденной ВИЧ иммунной системы, хотя понятно, что полного восстановления у большинства больных, если не у всех, достичь невозможно, тем более в условиях хронической вирусной инфекции, обусловленной ВИЧ. Первичный дефицит иммунной системы при ВИЧ-инфекции проявляется снижением уровня CD 4+ клеток, на фоне которого идет угнетение ГЗТ, уменьшение пролиферативного ответа, уменьшение продукции цитокинов, таких как. ИЛ-2, ИФН-γ, ИЛ-12. Неконтролируемая вирусная репликация реализуется хроническим активным состоянием иммунной системы. Снижение общего числа CD 4+ клеток идет в том числе и за счет падения содержания клеток памяти. Первичное увеличение CD 8+ клеток, главным образом CD 38+ и HLA-DR+ клеток наблюдается на очень ранних этапах болезни, но с течением времени в конечномсчете происходит уменьшение клеток памяти CD 8, как и пула в целом. Со времени широкого применения активной антиретровирусной терапии значительно уменьшилось у больных ВИЧ-инфекцией развитие суперинфекции и снизилась смертность, что является объективным показателем улучшения функции иммунной системы. У больных под влиянием терапии снижение вирусной нагрузки на плазму идет параллельно увеличению числа СD 4+ клеток. Первоначальная быстрая фаза повышения в первые 4 -12 недель CD 8+ клеток, как оказалось, связана с перераспределением существующих CD 4+ и CD 8+ клеток. Быстрое увеличение фенотипа клеток памяти (CD 45 RO+) сопровождается более медленным, но более устойчивым увеличением общего фенотипа (CD 45 RA+, CD 62 L+). В целом характер изменения CD 4+ и CD 8+ клеток в динамике леченияотражен в табл. 10.
Активная антиретровирусная терапия и восстановление функции иммунной системы. Сегодня идет изучение пределов, до которых возможно восстановление поврежденной ВИЧ иммунной системы, хотя понятно, что полного восстановления у большинства больных, если не у всех, достичь невозможно, тем более в условиях хронической вирусной инфекции, обусловленной ВИЧ. Первичный дефицит иммунной системы при ВИЧ-инфекции проявляется снижением уровня CD 4+ клеток, на фоне которого идет угнетение ГЗТ, уменьшение пролиферативного ответа, уменьшение продукции цитокинов, таких как. ИЛ-2, ИФН-γ, ИЛ-12. Неконтролируемая вирусная репликация реализуется хроническим активным состоянием иммунной системы. Снижение общего числа CD 4+ клеток идет в том числе и за счет падения содержания клеток памяти. Первичное увеличение CD 8+ клеток, главным образом CD 38+ и HLA-DR+ клеток наблюдается на очень ранних этапах болезни, но с течением времени в конечномсчете происходит уменьшение клеток памяти CD 8, как и пула в целом. Со времени широкого применения активной антиретровирусной терапии значительно уменьшилось у больных ВИЧ-инфекцией развитие суперинфекции и снизилась смертность, что является объективным показателем улучшения функции иммунной системы. У больных под влиянием терапии снижение вирусной нагрузки на плазму идет параллельно увеличению числа СD 4+ клеток. Первоначальная быстрая фаза повышения в первые 4 -12 недель CD 8+ клеток, как оказалось, связана с перераспределением существующих CD 4+ и CD 8+ клеток. Быстрое увеличение фенотипа клеток памяти (CD 45 RO+) сопровождается более медленным, но более устойчивым увеличением общего фенотипа (CD 45 RA+, CD 62 L+). В целом характер изменения CD 4+ и CD 8+ клеток в динамике леченияотражен в табл. 10.
 Таблица 10 Изменение CD 4+ и CD 8+ клеток в ответ на активную антиретровирусную терапию Клетки Характер изменения CD 4+ клетки: -изменения незначительны в ранней стадии ВИЧ-инфекции — ухудшение показателей по мере прогрессирования болезни — тенденция к нормализации под влиянием лечения CD 8+ клетки: — раннее увеличение, затем резкое снижение во время прогрессирования в СПИД — положительный эффект под влиянием терапии в первые 6 мес. лечения
Таблица 10 Изменение CD 4+ и CD 8+ клеток в ответ на активную антиретровирусную терапию Клетки Характер изменения CD 4+ клетки: -изменения незначительны в ранней стадии ВИЧ-инфекции — ухудшение показателей по мере прогрессирования болезни — тенденция к нормализации под влиянием лечения CD 8+ клетки: — раннее увеличение, затем резкое снижение во время прогрессирования в СПИД — положительный эффект под влиянием терапии в первые 6 мес. лечения
 Улучшение функции Т-клеток хотя и наблюдается в динамике лечения, но нет полного восстановления их функций. Улучшение ГЗТ на некоторые антигены наступает примерно через 12 недель после терапии и может быть связано с увеличением клеток памяти CD 4. Усиление лимфопролиферативного ответа нанекоторые антигены (цитомегаловирусы, Candida, микобактерии туберкулеза) также наблюдаются в течение первых 24 -48 недель лечения, но не на все антигены. Никакого значительного усиления лимфопролиферативного ответа на ВИЧ-антигены не наблюдается даже через 2 года эффективной антиретровирусной терапии. Исследования. Walker et al. (1996) показали, что ВИЧ-специфический Т-хелперный ответ, как определено с помощью лимфопролиферативного ответа на некоторые антигены ВИЧ, теряется почти немедленно после острой фазы ВИЧ-инфекции (сохраняется лишь у больных с вариантами длительного непрогрессирующего течения). Лечение в острой фазе болезни восстанавливает ВИЧ-специфический Т-хелперный ответ. Эти результаты поддерживают мнение о важности ВИЧ-специфического Т-хелперного иммунного ответа в поддержании вирусной супрессии и нормализации иммунного ответа на вирус.
Улучшение функции Т-клеток хотя и наблюдается в динамике лечения, но нет полного восстановления их функций. Улучшение ГЗТ на некоторые антигены наступает примерно через 12 недель после терапии и может быть связано с увеличением клеток памяти CD 4. Усиление лимфопролиферативного ответа нанекоторые антигены (цитомегаловирусы, Candida, микобактерии туберкулеза) также наблюдаются в течение первых 24 -48 недель лечения, но не на все антигены. Никакого значительного усиления лимфопролиферативного ответа на ВИЧ-антигены не наблюдается даже через 2 года эффективной антиретровирусной терапии. Исследования. Walker et al. (1996) показали, что ВИЧ-специфический Т-хелперный ответ, как определено с помощью лимфопролиферативного ответа на некоторые антигены ВИЧ, теряется почти немедленно после острой фазы ВИЧ-инфекции (сохраняется лишь у больных с вариантами длительного непрогрессирующего течения). Лечение в острой фазе болезни восстанавливает ВИЧ-специфический Т-хелперный ответ. Эти результаты поддерживают мнение о важности ВИЧ-специфического Т-хелперного иммунного ответа в поддержании вирусной супрессии и нормализации иммунного ответа на вирус.
 Исследованияпо изучению утраты Т-клеточных рецепторов у больных различными формами ВИЧ-инфекции дали возможность понять, почему развивается суперинфекция. Было показано, что хотя активная терапия способна резко уменьшить вирусную нагрузку на плазму и увеличить количество CD 4+ клеток, уменьшить возникновение суперинфекции, но у больных, особенно с уже прогрессирующей ВИЧ-инфекцией на момент начала противовирусной терапии, сохраняется суперинфекция. Поэтому встал вопрос о качестве иммунного восстановления после терапии. Исследования показывают, что некоторые субпопуляции Т-клеток, потерянные во время ВИЧ-инфекции, могут не восстанавливаться после противовирусной терапии, оставляя таким образом дефект в Т-клеточном опосредованном иммунитете больных (Laurence J. , 1998). Критическим аспектом иммунного восстановления является скорость восстановленияпростых субпопуляций клеток и клеток памяти, относящихся какк CD 8+, так и CD 4+Т-клеткам. CD 45 RA+ клетки являются медленно пролиферирующими, они распознают новый антиген и организуютряд других иммунных клеток, включая киллерные CD 8+ Т-клетки и В-клетки, осуществляющие защиту от инфекций. После выздоровления от обычной инфекции. CD 4+ Т-клетки памяти(CD 45 RO+) продолжаютциркулироватьи быстро пролиферируют при повторномконтакте с тем же антигеном. Принципиальным различиеммежду простыми (naive) клетками и клетками памятисубпопуляции CD 4+ Т-клеток являетсявысокая зависимость простых клеток от тимуса, в то время какактивность клеток памяти носит периферический характер и не зависит от тимуса.
Исследованияпо изучению утраты Т-клеточных рецепторов у больных различными формами ВИЧ-инфекции дали возможность понять, почему развивается суперинфекция. Было показано, что хотя активная терапия способна резко уменьшить вирусную нагрузку на плазму и увеличить количество CD 4+ клеток, уменьшить возникновение суперинфекции, но у больных, особенно с уже прогрессирующей ВИЧ-инфекцией на момент начала противовирусной терапии, сохраняется суперинфекция. Поэтому встал вопрос о качестве иммунного восстановления после терапии. Исследования показывают, что некоторые субпопуляции Т-клеток, потерянные во время ВИЧ-инфекции, могут не восстанавливаться после противовирусной терапии, оставляя таким образом дефект в Т-клеточном опосредованном иммунитете больных (Laurence J. , 1998). Критическим аспектом иммунного восстановления является скорость восстановленияпростых субпопуляций клеток и клеток памяти, относящихся какк CD 8+, так и CD 4+Т-клеткам. CD 45 RA+ клетки являются медленно пролиферирующими, они распознают новый антиген и организуютряд других иммунных клеток, включая киллерные CD 8+ Т-клетки и В-клетки, осуществляющие защиту от инфекций. После выздоровления от обычной инфекции. CD 4+ Т-клетки памяти(CD 45 RO+) продолжаютциркулироватьи быстро пролиферируют при повторномконтакте с тем же антигеном. Принципиальным различиеммежду простыми (naive) клетками и клетками памятисубпопуляции CD 4+ Т-клеток являетсявысокая зависимость простых клеток от тимуса, в то время какактивность клеток памяти носит периферический характер и не зависит от тимуса.
 Согласно существующей к настоящему времени информации, восстановление CD 4+ Т-клеток после интенсивной антиретровирусной терапии не является следствием дополнительного избыткапродукции клеток после того, как падение уровня. ВИЧ-опосредованным киллингом клеток он был восстановлен, а, скорее, является следствием усиленной продукции Т-клеток, увеличенной миграцией. Т-клеток из тканей в кровь и изменения путей миграции Т-клеток. J. A. Levy et al. (1996) сообщили данные о количестве CD 4+ Т-клеток у врачей, которые получали зидовудин профилактически после нечаянно укола иглой. Проводился многократный подсчет. CD 4+ клеток и серологическое обследование на ВИЧ в течение нескольких месяцев, все они остались серонегативны, но количество CD 4+клеток у них тем не менее удвоилось или утроилось. Наиболее вероятное объяснение этому – действие зидовудина. M. Connors et al. (1997) изучил динамику восстановления CD 4+ Т-клеток у 39 больных ВИЧ-инфекцией, находившихся на лечении зидовудином или зидовудином+α-интерфероном, что сейчас расценивается какстандарт минимального лечения. Установлено, что больные с более низким количеством Т-клеток имели сравнительно более низкую пропорцию простых CD 4+ Т-клеток, тогда какбольные с более высоким количеством. Т-клетокимели относительноболее высокую пропорцию простых Т-клеток.
Согласно существующей к настоящему времени информации, восстановление CD 4+ Т-клеток после интенсивной антиретровирусной терапии не является следствием дополнительного избыткапродукции клеток после того, как падение уровня. ВИЧ-опосредованным киллингом клеток он был восстановлен, а, скорее, является следствием усиленной продукции Т-клеток, увеличенной миграцией. Т-клеток из тканей в кровь и изменения путей миграции Т-клеток. J. A. Levy et al. (1996) сообщили данные о количестве CD 4+ Т-клеток у врачей, которые получали зидовудин профилактически после нечаянно укола иглой. Проводился многократный подсчет. CD 4+ клеток и серологическое обследование на ВИЧ в течение нескольких месяцев, все они остались серонегативны, но количество CD 4+клеток у них тем не менее удвоилось или утроилось. Наиболее вероятное объяснение этому – действие зидовудина. M. Connors et al. (1997) изучил динамику восстановления CD 4+ Т-клеток у 39 больных ВИЧ-инфекцией, находившихся на лечении зидовудином или зидовудином+α-интерфероном, что сейчас расценивается какстандарт минимального лечения. Установлено, что больные с более низким количеством Т-клеток имели сравнительно более низкую пропорцию простых CD 4+ Т-клеток, тогда какбольные с более высоким количеством. Т-клетокимели относительноболее высокую пропорцию простых Т-клеток.
 Такимобразом, достигнуты отчетливые положительные эффекты у больных ВИЧ-инфекцией с момента внедрения активной антиретровирусной терапии, которая позволяет снизить уровень вирусной нагрузки на плазму до неопределяемого уровня, повысить уровень CD 4+ клеток в крови, предотвратить присоединение суперинфекции, а в целом перевести заболевание в хроническое течение. Вместе с тем, добиться положительного эффекта удается только у 70 -80% больных (при терапии различных бактериальных заболеваний антибиотиками положительный эффект достигается в 99%). Терапия требует высокой дисциплины от больного, это тяжелая нагрузка на больного. Она весьма дорога, лишь 10 -15% больных живут в странах, где экономика позволяет широко внедрить этот вид терапии. В России ею государство обеспечивает лишь детей. Даже при положительном эффекте не прекращается репликация вируса. Эффект от терапии сравнительно не продолжителен. Даже при самом оптимальном варианте больной должен настроится на лечение в течение 20 -30 лет.
Такимобразом, достигнуты отчетливые положительные эффекты у больных ВИЧ-инфекцией с момента внедрения активной антиретровирусной терапии, которая позволяет снизить уровень вирусной нагрузки на плазму до неопределяемого уровня, повысить уровень CD 4+ клеток в крови, предотвратить присоединение суперинфекции, а в целом перевести заболевание в хроническое течение. Вместе с тем, добиться положительного эффекта удается только у 70 -80% больных (при терапии различных бактериальных заболеваний антибиотиками положительный эффект достигается в 99%). Терапия требует высокой дисциплины от больного, это тяжелая нагрузка на больного. Она весьма дорога, лишь 10 -15% больных живут в странах, где экономика позволяет широко внедрить этот вид терапии. В России ею государство обеспечивает лишь детей. Даже при положительном эффекте не прекращается репликация вируса. Эффект от терапии сравнительно не продолжителен. Даже при самом оптимальном варианте больной должен настроится на лечение в течение 20 -30 лет.
 Минимальная антиретровирусная терапия Рекомендуемая СDС (1997) активная антиретровирусная терапия, включающая комплекс ингибиторов обратной транскриптазы и протеазы («тритерапия») в силу высокой стоимости не может быть широко применена в странах с низким экономическим уровнем жизни. По оценкам специалистов лишь 10 -15% нуждающихся в терапии больных живут в экономически развитых странах, из всех больных, кому показана высокоактивная антиретровирусная терапия в силу экономических проблем ее могут получить только 5%. В России бесплатной антиретровирусной терапией, включающей ингибиторы протеазы обеспечиваются в основном дети. Поэтому мы разработали принцип минимальной антиретровирусной терапии, обеспечивающий противовирусный, иммуномодулирующий и противоопухолевый эффект, а также оказывающей влияние на определенные звенья патогенеза ВИЧ-инфекции и повышающей неспецифические факторы защиты. Терапия включает: 1) азидотимидин, 2) индуктор эндогенного интерферона, низкомолекулярное производное акредона — циклоферон (фирма «Полисан», Санкт-Петербург), 3) системнуюэнзимотерапию вобэнзимом (МУКОС Фирма, Германия), 4) заместительная терапия дефицита комплемента — введение нативной плазмы доноров). Показана эффективность комплексного лечения больных ВИЧ-инфекцией, у больных, уровень CD 4+ клеток у которых не ниже 200 в мкл, хорошая переносимость терапии, отсутствие побочных действий, ни у одного из больных не потребовалась отмена. Наряду с улучшением самочувствия больных, повышением уровня CD 4+ клеток установлено повышение функциональнойактивности нейтрофилов, повышение показателей активности классического пути комплемента при одновременном снижении альтернативного, уменьшение уровня циркулирующих иммунных комплексов. Терапия также предупреждала развитие оппортунистической инфекции в первую очередь герпесвирусной группы. Стоимость терапии одного больного в год составила 800 -950 долларов США в год против 12 -35 тысяч долларов при использовании классического варианта «тритерапии».
Минимальная антиретровирусная терапия Рекомендуемая СDС (1997) активная антиретровирусная терапия, включающая комплекс ингибиторов обратной транскриптазы и протеазы («тритерапия») в силу высокой стоимости не может быть широко применена в странах с низким экономическим уровнем жизни. По оценкам специалистов лишь 10 -15% нуждающихся в терапии больных живут в экономически развитых странах, из всех больных, кому показана высокоактивная антиретровирусная терапия в силу экономических проблем ее могут получить только 5%. В России бесплатной антиретровирусной терапией, включающей ингибиторы протеазы обеспечиваются в основном дети. Поэтому мы разработали принцип минимальной антиретровирусной терапии, обеспечивающий противовирусный, иммуномодулирующий и противоопухолевый эффект, а также оказывающей влияние на определенные звенья патогенеза ВИЧ-инфекции и повышающей неспецифические факторы защиты. Терапия включает: 1) азидотимидин, 2) индуктор эндогенного интерферона, низкомолекулярное производное акредона — циклоферон (фирма «Полисан», Санкт-Петербург), 3) системнуюэнзимотерапию вобэнзимом (МУКОС Фирма, Германия), 4) заместительная терапия дефицита комплемента — введение нативной плазмы доноров). Показана эффективность комплексного лечения больных ВИЧ-инфекцией, у больных, уровень CD 4+ клеток у которых не ниже 200 в мкл, хорошая переносимость терапии, отсутствие побочных действий, ни у одного из больных не потребовалась отмена. Наряду с улучшением самочувствия больных, повышением уровня CD 4+ клеток установлено повышение функциональнойактивности нейтрофилов, повышение показателей активности классического пути комплемента при одновременном снижении альтернативного, уменьшение уровня циркулирующих иммунных комплексов. Терапия также предупреждала развитие оппортунистической инфекции в первую очередь герпесвирусной группы. Стоимость терапии одного больного в год составила 800 -950 долларов США в год против 12 -35 тысяч долларов при использовании классического варианта «тритерапии».
 Активная антиретровирусная терапия и суперинфекций ВИЧ/СПИД. Со времени широкого применения активной антиретровирусной терапии значительно уменьшилось у больных ВИЧ-инфекцией развитие суперинфекции и снизилась смертность, что является объективным показателем улучшения функции иммунной системы. У больных под влиянием терапии снижение вирусной нагрузки на плазму идет параллельно увеличению числа СD 4+ клеток. Первоначальная быстрая фаза повышения в первые 4 -12 недель CD 8+ клеток, как оказалось, связана с перераспределением существующих CD 4+ и CD 8+ клеток. Быстрое увеличение фенотипа клеток памяти сопровождается более медленным, но более устойчивым увеличением общего фенотипа. В целом характер изменения CD 4+ и CD 8+ клеток в динамике лечениядемонстрирует табл. 11.
Активная антиретровирусная терапия и суперинфекций ВИЧ/СПИД. Со времени широкого применения активной антиретровирусной терапии значительно уменьшилось у больных ВИЧ-инфекцией развитие суперинфекции и снизилась смертность, что является объективным показателем улучшения функции иммунной системы. У больных под влиянием терапии снижение вирусной нагрузки на плазму идет параллельно увеличению числа СD 4+ клеток. Первоначальная быстрая фаза повышения в первые 4 -12 недель CD 8+ клеток, как оказалось, связана с перераспределением существующих CD 4+ и CD 8+ клеток. Быстрое увеличение фенотипа клеток памяти сопровождается более медленным, но более устойчивым увеличением общего фенотипа. В целом характер изменения CD 4+ и CD 8+ клеток в динамике лечениядемонстрирует табл. 11.
 Таблица 11 Изменение CD 4+ и CD 8+ клеток в ответ на активную антиретровирусную терапию Клетки Характер изменения CD 4+ клетки: — изменения незначительны в ранней стадии ВИЧ-инфекции — ухудшение показателей по мере прогрессирования болезни — тенденция к нормализации под влиянием лечения CD 8+ клетки: — раннее увеличение, затем резкое снижение во время прогрессирования в СПИД — положительный эффект под влиянием терапии в первые 6 мес. лечения
Таблица 11 Изменение CD 4+ и CD 8+ клеток в ответ на активную антиретровирусную терапию Клетки Характер изменения CD 4+ клетки: — изменения незначительны в ранней стадии ВИЧ-инфекции — ухудшение показателей по мере прогрессирования болезни — тенденция к нормализации под влиянием лечения CD 8+ клетки: — раннее увеличение, затем резкое снижение во время прогрессирования в СПИД — положительный эффект под влиянием терапии в первые 6 мес. лечения
 Улучшение функции Т-клеток хотя и наблюдается в динамике лечения, но нет полного восстановления их функций. Улучшение ГЗТ на некоторые антигены наступает примерно через 12 недель после терапии и может быть связано с увеличением клеток памяти. Усиление лимфопролиферативного ответа нанекоторые антигены (цитомегаловирусы, Candida, микобактерии туберкулеза) также наблюдаются в течение первых 24 -48 недель лечения, но не на все антигены. Никакого значительного усиления лимфопролиферативного ответа на ВИЧ-антигены не наблюдается даже через 2 года эффективной антиретровирусной терапии. Исследования. Walker et al. (1996) показали, что ВИЧ-специфический Т-хелперный ответ, как определено с помощью лимфопролиферативного ответа на некоторые антигены ВИЧ, теряется почти немедленно после острой фазы ВИЧ-инфекции (сохраняется лишь у больных с вариантами длительного непрогрессирующего течения). Лечение в острой фазе болезни восстанавливает ВИЧ-специфический Т-хелперный ответ. Эти результаты поддерживают мнение о важности ВИЧ-специфического Т-хелперного иммунного ответа в поддержании вирусной супрессии и нормализации иммунного ответа на вирус.
Улучшение функции Т-клеток хотя и наблюдается в динамике лечения, но нет полного восстановления их функций. Улучшение ГЗТ на некоторые антигены наступает примерно через 12 недель после терапии и может быть связано с увеличением клеток памяти. Усиление лимфопролиферативного ответа нанекоторые антигены (цитомегаловирусы, Candida, микобактерии туберкулеза) также наблюдаются в течение первых 24 -48 недель лечения, но не на все антигены. Никакого значительного усиления лимфопролиферативного ответа на ВИЧ-антигены не наблюдается даже через 2 года эффективной антиретровирусной терапии. Исследования. Walker et al. (1996) показали, что ВИЧ-специфический Т-хелперный ответ, как определено с помощью лимфопролиферативного ответа на некоторые антигены ВИЧ, теряется почти немедленно после острой фазы ВИЧ-инфекции (сохраняется лишь у больных с вариантами длительного непрогрессирующего течения). Лечение в острой фазе болезни восстанавливает ВИЧ-специфический Т-хелперный ответ. Эти результаты поддерживают мнение о важности ВИЧ-специфического Т-хелперного иммунного ответа в поддержании вирусной супрессии и нормализации иммунного ответа на вирус.
 Исследованияпо изучению утраты Т-клеточных рецепторов у больных различными формами ВИЧ-инфекции дали возможность понять, почему развивается суперинфекция. Было показано, что хотя активная терапия способна резко уменьшить вирусную нагрузку на плазму и увеличить количество CD 4+ клеток, уменьшить возникновение суперинфекции, но у больных, особенно с уже прогрессирующей ВИЧ-инфекцией на момент начала противовирусной терапии, сохраняется суперинфекция. Поэтому встал вопрос о качестве иммунного восстановления после терапии. Исследования показывают, что некоторые субпопуляции Т-клеток, потерянные во время ВИЧ-инфекции, могут не восстанавливаться после противовирусной терапии, оставляя таким образом дефект в Т-клеточном опосредованном иммунитете больных (Laurence J. , 1998). Согласно существующей к настоящему времени информации, восстановление CD 4+ Т-клеток после интенсивной антиретровирусной терапии не является следствием дополнительного избыткапродукции клеток после того, как падение уровня. ВИЧ-опосредованным киллингом клеток он был восстановлен, а, скорее, является следствием усиленной продукции Т-клеток, увеличенной миграцией. Т-клеток из тканей в кровь и изменения путей миграции Т-клеток
Исследованияпо изучению утраты Т-клеточных рецепторов у больных различными формами ВИЧ-инфекции дали возможность понять, почему развивается суперинфекция. Было показано, что хотя активная терапия способна резко уменьшить вирусную нагрузку на плазму и увеличить количество CD 4+ клеток, уменьшить возникновение суперинфекции, но у больных, особенно с уже прогрессирующей ВИЧ-инфекцией на момент начала противовирусной терапии, сохраняется суперинфекция. Поэтому встал вопрос о качестве иммунного восстановления после терапии. Исследования показывают, что некоторые субпопуляции Т-клеток, потерянные во время ВИЧ-инфекции, могут не восстанавливаться после противовирусной терапии, оставляя таким образом дефект в Т-клеточном опосредованном иммунитете больных (Laurence J. , 1998). Согласно существующей к настоящему времени информации, восстановление CD 4+ Т-клеток после интенсивной антиретровирусной терапии не является следствием дополнительного избыткапродукции клеток после того, как падение уровня. ВИЧ-опосредованным киллингом клеток он был восстановлен, а, скорее, является следствием усиленной продукции Т-клеток, увеличенной миграцией. Т-клеток из тканей в кровь и изменения путей миграции Т-клеток
 J. A. Levy et al. (1996) сообщили данные о количестве CD 4+ Т-клеток у врачей, которые получали зидовудин профилактически после нечаянно укола иглой. Проводился многократный подсчет. CD 4+ клеток и серологическое обследование на ВИЧ в течение нескольких месяцев, все они остались серонегативны, но количество CD 4+клеток у них тем не менее удвоилось или утроилось. Наиболее вероятное объяснение этому – действие зидовудина. Накопленный клиницистами опыт показал , что активная антиретровирусная терапия, является одновременно как методом профилактики суперинфекций. В экономически развитых странах, особенно США и Канаде с 1994 года отмечается снижение суперинфекций и смертности среди наиболее иммуномсупрессированных больных ВИЧ-инфекцией. Прежде всего это касается пневмоцистной пневмонии, комплекса микобактериозов (МАС), цитомегаловирусной инфекции, бактериальной пневмонии, токсоплазмоза, криптококкоза и других инфекций. Значительно снизилась заболеваемость саркомой Капоши, отчасти – неходжкинской лимфомойи др. Это в первую очередь связано с внедрением комбинированной терапии антиретровирусными препаратами, ингибиторов протеаз. Активная терапия приводит к снижению вирусной нагрузки на плазму у значительной части больных с повышением уровня CD 4+ клеток. Клинические исследования показали, что у 80 -90% больных, получавших ингибиторы протеазы, на 6 -12 мес. до границы чувствительности метода. В клинике Д. Гопкинса показано, что в 1996 -97 г. г. применение комбинированной терапии с включением ингибиторов протеазы снижает на 61% риск развития оппортунистической инфекции.
J. A. Levy et al. (1996) сообщили данные о количестве CD 4+ Т-клеток у врачей, которые получали зидовудин профилактически после нечаянно укола иглой. Проводился многократный подсчет. CD 4+ клеток и серологическое обследование на ВИЧ в течение нескольких месяцев, все они остались серонегативны, но количество CD 4+клеток у них тем не менее удвоилось или утроилось. Наиболее вероятное объяснение этому – действие зидовудина. Накопленный клиницистами опыт показал , что активная антиретровирусная терапия, является одновременно как методом профилактики суперинфекций. В экономически развитых странах, особенно США и Канаде с 1994 года отмечается снижение суперинфекций и смертности среди наиболее иммуномсупрессированных больных ВИЧ-инфекцией. Прежде всего это касается пневмоцистной пневмонии, комплекса микобактериозов (МАС), цитомегаловирусной инфекции, бактериальной пневмонии, токсоплазмоза, криптококкоза и других инфекций. Значительно снизилась заболеваемость саркомой Капоши, отчасти – неходжкинской лимфомойи др. Это в первую очередь связано с внедрением комбинированной терапии антиретровирусными препаратами, ингибиторов протеаз. Активная терапия приводит к снижению вирусной нагрузки на плазму у значительной части больных с повышением уровня CD 4+ клеток. Клинические исследования показали, что у 80 -90% больных, получавших ингибиторы протеазы, на 6 -12 мес. до границы чувствительности метода. В клинике Д. Гопкинса показано, что в 1996 -97 г. г. применение комбинированной терапии с включением ингибиторов протеазы снижает на 61% риск развития оппортунистической инфекции.
 Многочисленные исследования показали, что ВИЧ четко влияет на клинические проявления суперинфекций, которые в свою очередь сказываются на репликации ВИЧ и ускоряют прогрессирование болезни. Установлено, что суперинфекция: активируютлатентно протекающуюинфекцию в СD 4+ Т-клетках, повышая репликацию ВИЧ; активирует не инфицированные CD 4+ Т-клетки, что ведет к повышению восприимчивости этих клеток к ВИЧ; повышает уровень провоспалительныхцитокинов, включая ФНО, ИЛ-6, ведущих к увеличению репликации ВИЧ; активирует тканевые макрофаги, инфицированные ВИЧ, что усиливает репликацию ВИЧ; эффективное лечение суперинфекции сопровождается снижением уровня плазменной РНК ВИЧ, но не до уровня, предшествовавшего наслоению суперинфекции
Многочисленные исследования показали, что ВИЧ четко влияет на клинические проявления суперинфекций, которые в свою очередь сказываются на репликации ВИЧ и ускоряют прогрессирование болезни. Установлено, что суперинфекция: активируютлатентно протекающуюинфекцию в СD 4+ Т-клетках, повышая репликацию ВИЧ; активирует не инфицированные CD 4+ Т-клетки, что ведет к повышению восприимчивости этих клеток к ВИЧ; повышает уровень провоспалительныхцитокинов, включая ФНО, ИЛ-6, ведущих к увеличению репликации ВИЧ; активирует тканевые макрофаги, инфицированные ВИЧ, что усиливает репликацию ВИЧ; эффективное лечение суперинфекции сопровождается снижением уровня плазменной РНК ВИЧ, но не до уровня, предшествовавшего наслоению суперинфекции
 Следовательно, предупреждение суперинфекции у больных ВИЧ/СПИД может изменить естественное течение болезни. Но встает вопрос, какие тесты могут быть показателями начала профилактического лечения у больных, получающих активную комбинированную антиретровирусную терапию. Большинство авторов рекомендует базироваться на уровне CD 4+ Т-лимфоцитов, при этом не обращать внимание напоследующее изменение уровня CD 4+ клеток, продолжать терапию, направленную на профилактику суперинфекций. У больных, получающих активную антиретровирусную терапию может не наблюдаться связи между вирусологическими и иммунологическими показателями, может быть повышение уровня CD 4+ клеток даже при если сохраняется высокая вирусная нагрузка на плазму. Даже у больных, получивших активную антиретровирусную терапию с отсутствием эффекта на вирусную нагрузку на плазму выявлен защитный эффект против условнопатогенных возбудителей. Возможно, что мутантный вариант ВИЧ, реплицирующегося в присутствии 3 -4 мощных антиретровирусных препаратов, может быть менее патогенным и, таким образом, менее способным вызывать деструкцию CD 4+ Т-клеток. Однако сомнительна прочность, продолжительность положительного эффекта CD 4+ клеток в присутствии выраженной вирусной нагрузки на плазму. Сложным остается вопрос, когда отменить первичную или вторичную профилактическую терапию суперинфекций. Отсутствуют четкие клинические показатели, по которым можно было бы ориентироваться для прекращения профилактической терапии.
Следовательно, предупреждение суперинфекции у больных ВИЧ/СПИД может изменить естественное течение болезни. Но встает вопрос, какие тесты могут быть показателями начала профилактического лечения у больных, получающих активную комбинированную антиретровирусную терапию. Большинство авторов рекомендует базироваться на уровне CD 4+ Т-лимфоцитов, при этом не обращать внимание напоследующее изменение уровня CD 4+ клеток, продолжать терапию, направленную на профилактику суперинфекций. У больных, получающих активную антиретровирусную терапию может не наблюдаться связи между вирусологическими и иммунологическими показателями, может быть повышение уровня CD 4+ клеток даже при если сохраняется высокая вирусная нагрузка на плазму. Даже у больных, получивших активную антиретровирусную терапию с отсутствием эффекта на вирусную нагрузку на плазму выявлен защитный эффект против условнопатогенных возбудителей. Возможно, что мутантный вариант ВИЧ, реплицирующегося в присутствии 3 -4 мощных антиретровирусных препаратов, может быть менее патогенным и, таким образом, менее способным вызывать деструкцию CD 4+ Т-клеток. Однако сомнительна прочность, продолжительность положительного эффекта CD 4+ клеток в присутствии выраженной вирусной нагрузки на плазму. Сложным остается вопрос, когда отменить первичную или вторичную профилактическую терапию суперинфекций. Отсутствуют четкие клинические показатели, по которым можно было бы ориентироваться для прекращения профилактической терапии.
 Вместе с тем все больше накапливается данных, что у лиц, у которых повышение уровня CD 4+ Т-клеток превышает показатели профилактического значения, не нуждаются в дальнейшем продолжении лечения. Прекращение первичной лекарственной профилактики может быть обоснованным для больных, у которых число CD 4+ Т-клеток после терапии находится стабильно на 50% выше, чем порог для начала профилактики и держится на таком уровне по крайней мере 3 месяца. Вирусная нагрузка при этом может сохраниться на выявляемых ПЦР уровнях. Прекращение поддерживающей терапии несет с собой большой риск, если в организме больного имеется не диагностированная суперинфекция. Сегодня можно с уверенностью сказать. что активная антиретровирусная терапия -наиболее эффективный метод профилактики суперинфекций. Среди больных, у которых под влиянием лечения повышается уровень CD 4+ Т-клеток, риск развития суперинфекций мал. В ходе лечения больных должны учитываться показатели и вирусной нагрузки на плазму и число CD 4+ клеток. Внедрение активной антиретровирусной терапии существенно повлияло на развитие известных форм суперинфекций. Но вместе с тем эта терапия высветила новые проблемы, возникающие в первые 1 -2 мес. лечения. Так, у больных стали регистрироваться локализованные формы микобактериальной инфекции (Chaisson R. E. , 1998).
Вместе с тем все больше накапливается данных, что у лиц, у которых повышение уровня CD 4+ Т-клеток превышает показатели профилактического значения, не нуждаются в дальнейшем продолжении лечения. Прекращение первичной лекарственной профилактики может быть обоснованным для больных, у которых число CD 4+ Т-клеток после терапии находится стабильно на 50% выше, чем порог для начала профилактики и держится на таком уровне по крайней мере 3 месяца. Вирусная нагрузка при этом может сохраниться на выявляемых ПЦР уровнях. Прекращение поддерживающей терапии несет с собой большой риск, если в организме больного имеется не диагностированная суперинфекция. Сегодня можно с уверенностью сказать. что активная антиретровирусная терапия -наиболее эффективный метод профилактики суперинфекций. Среди больных, у которых под влиянием лечения повышается уровень CD 4+ Т-клеток, риск развития суперинфекций мал. В ходе лечения больных должны учитываться показатели и вирусной нагрузки на плазму и число CD 4+ клеток. Внедрение активной антиретровирусной терапии существенно повлияло на развитие известных форм суперинфекций. Но вместе с тем эта терапия высветила новые проблемы, возникающие в первые 1 -2 мес. лечения. Так, у больных стали регистрироваться локализованные формы микобактериальной инфекции (Chaisson R. E. , 1998).
 Изменение комбинации активной антиретровирусной терапии. В ходе лечения больного ВИЧ/СПИД возникают ситуации, требующие решать вопрос об изменения схемы лечения больного, смены лекарственных препаратов. Критериями для изменения антиретровирусной терапии являются снижение вирусной нагрузки на плазму менее 0, 5 -0, 75 log к 4 неделе или менее 1, 0 log к 8 неделе от начала терапии отсутствие снижения вирусной нагрузки на плазму до неопределяемого уровня в течение 4 -6 мес. снижающееся количество CD 4+ клеток клиническое ухудшение Минимальным значимым изменением виремии считается 3 -кратное или 0, 5 log 10 увеличение или уменьшение. Значительное снижение числа клеток CD 4+ – это уменьшение абсолютного числа клеток более чем на 30% от исходного уровня и уменьшение процентного содержания клеток более чем на 3% от исходного уровня.
Изменение комбинации активной антиретровирусной терапии. В ходе лечения больного ВИЧ/СПИД возникают ситуации, требующие решать вопрос об изменения схемы лечения больного, смены лекарственных препаратов. Критериями для изменения антиретровирусной терапии являются снижение вирусной нагрузки на плазму менее 0, 5 -0, 75 log к 4 неделе или менее 1, 0 log к 8 неделе от начала терапии отсутствие снижения вирусной нагрузки на плазму до неопределяемого уровня в течение 4 -6 мес. снижающееся количество CD 4+ клеток клиническое ухудшение Минимальным значимым изменением виремии считается 3 -кратное или 0, 5 log 10 увеличение или уменьшение. Значительное снижение числа клеток CD 4+ – это уменьшение абсолютного числа клеток более чем на 30% от исходного уровня и уменьшение процентного содержания клеток более чем на 3% от исходного уровня.
 Тактика изменения состава препаратов зависит от показаний к смене режима лечения. Так, если получен положительный эффект лечения в отношении антиретровирусного эффекта, но у больного развилась непереносимость или токсические эффекты, следует заменить препарат, который вызвал побочное действие, и предпочтение следует отдавать препаратам этого же класса, но с другим уровнем токсичности или профилем переносимости. Если же достигнут антиретровирусный эффект, но больной получает лечение по схеме, не отвечающей рекомендуемым стандартам, в частности находится на моно- или дитерапии, то можно выбора два. Первый -продолжить лечение, проводя мониторинг вирусной нагрузки и уровня CD 4+ леток, или добавить к схеме лечения препараты таким образом, чтобы новый режим соответствовал рекомендуемым стандартам. Второй – перейти на стандартную схему лечения, так как следует учитывать, что режимы терапии, не включенные в категорию «настоятельно рекомендуемых», в конце концов приводят к неэффективности лечения, а, следовательно, предпочтительным является последний подход, то есть модификация режима.
Тактика изменения состава препаратов зависит от показаний к смене режима лечения. Так, если получен положительный эффект лечения в отношении антиретровирусного эффекта, но у больного развилась непереносимость или токсические эффекты, следует заменить препарат, который вызвал побочное действие, и предпочтение следует отдавать препаратам этого же класса, но с другим уровнем токсичности или профилем переносимости. Если же достигнут антиретровирусный эффект, но больной получает лечение по схеме, не отвечающей рекомендуемым стандартам, в частности находится на моно- или дитерапии, то можно выбора два. Первый -продолжить лечение, проводя мониторинг вирусной нагрузки и уровня CD 4+ леток, или добавить к схеме лечения препараты таким образом, чтобы новый режим соответствовал рекомендуемым стандартам. Второй – перейти на стандартную схему лечения, так как следует учитывать, что режимы терапии, не включенные в категорию «настоятельно рекомендуемых», в конце концов приводят к неэффективности лечения, а, следовательно, предпочтительным является последний подход, то есть модификация режима.
 Более сложна задача смены терапииу больных, у которых оказались неэффективными режимы лечения из категории «настоятельно рекомендуемых». Тем не менее правило здесь одно – смена всего комплекса лекарственных препаратов новыми. При этом надо иметь в виду, что из-за большой скорости возникновения мутаций ВИЧ на фоне терапии часто возникают штаммы, имеющие резистентность к одному или более препаратов, особенно если не удавалось достичь максимальной супрессии вируса. Возможность развития широкой перекрестной резистентности между препаратами одного класса осложняет задачу смены лекарственных средств. Вирусные штаммы, у которых развивается резистентность к одному ингибитору протеазыили ненуклеозидному ингибитору обратной транскриптазы, часто имеют пониженную чувствительность к большинству или всем другим препаратов этих групп. В случаях возникновении лекарственных взаимодействий при использовании комбинации ингибиторов протеазы или ингибиторов протеазы в сочетании с ненуклеозидными ингибиторами обратной транскриптазы, может потребоваться модификации доз препаратов. У некоторых больных варианты лечения могут быть ограничены в связи с назначением антиретровирусных препаратов в прошлом, токсичности или непереносимости.
Более сложна задача смены терапииу больных, у которых оказались неэффективными режимы лечения из категории «настоятельно рекомендуемых». Тем не менее правило здесь одно – смена всего комплекса лекарственных препаратов новыми. При этом надо иметь в виду, что из-за большой скорости возникновения мутаций ВИЧ на фоне терапии часто возникают штаммы, имеющие резистентность к одному или более препаратов, особенно если не удавалось достичь максимальной супрессии вируса. Возможность развития широкой перекрестной резистентности между препаратами одного класса осложняет задачу смены лекарственных средств. Вирусные штаммы, у которых развивается резистентность к одному ингибитору протеазыили ненуклеозидному ингибитору обратной транскриптазы, часто имеют пониженную чувствительность к большинству или всем другим препаратов этих групп. В случаях возникновении лекарственных взаимодействий при использовании комбинации ингибиторов протеазы или ингибиторов протеазы в сочетании с ненуклеозидными ингибиторами обратной транскриптазы, может потребоваться модификации доз препаратов. У некоторых больных варианты лечения могут быть ограничены в связи с назначением антиретровирусных препаратов в прошлом, токсичности или непереносимости.
 Важной проблемой является необходимость временной отмены антиретровирусной терапии, например, при непереносимых побочных эффектах, лекарственных взаимодействиях, первый триместр беременности, а нередко и в связи с тем, что больной принимает решение об отмене терапии из-за финансовой невозможности приобретения лекарственных средств. Хотя отсутствует полное представление о том, какой промежуток дней, недель или месяцев допустим для отмены одного или более лекарств, составляющих схему лечения, в мире идет направленное изучение прерывистых циклов терапии, как запланированной схемы лечения. При этом первостепенное значение имеет риск формирования резистентности к препаратам за время отмены лечения. . У больных, которым приходится вынужденно отказаться от дальнейшего лечения антиретровирусными препаратами по полной схеме на длительное время, теоретически более целесообразно отменить все антиретровирусные препараты одновременно, нежели продолжать лечение одним или двумя препаратами, чтобы уменьшить вероятность возникновения резистентных штаммов вируса.
Важной проблемой является необходимость временной отмены антиретровирусной терапии, например, при непереносимых побочных эффектах, лекарственных взаимодействиях, первый триместр беременности, а нередко и в связи с тем, что больной принимает решение об отмене терапии из-за финансовой невозможности приобретения лекарственных средств. Хотя отсутствует полное представление о том, какой промежуток дней, недель или месяцев допустим для отмены одного или более лекарств, составляющих схему лечения, в мире идет направленное изучение прерывистых циклов терапии, как запланированной схемы лечения. При этом первостепенное значение имеет риск формирования резистентности к препаратам за время отмены лечения. . У больных, которым приходится вынужденно отказаться от дальнейшего лечения антиретровирусными препаратами по полной схеме на длительное время, теоретически более целесообразно отменить все антиретровирусные препараты одновременно, нежели продолжать лечение одним или двумя препаратами, чтобы уменьшить вероятность возникновения резистентных штаммов вируса.
 Спасибо за внимание!!!
Спасибо за внимание!!!

