6 Spectroscopy.ppt
- Количество слайдов: 17
 Спектроскопические методы Спектроскопия – раздел физики и химии, который изучает воздействие света или любого электромагнитного излучения на вещество. Волны с различное длиной волны переносят различное количество энергии, что приводит к различным взаимодействиям внутри вещества. Спектроскопия – латинское слово spectrum - изображение греческое слово (skopein) - смотреть И. Ньютон – 1672 год впервые использовал термин «спектр» при изучении света.
Спектроскопические методы Спектроскопия – раздел физики и химии, который изучает воздействие света или любого электромагнитного излучения на вещество. Волны с различное длиной волны переносят различное количество энергии, что приводит к различным взаимодействиям внутри вещества. Спектроскопия – латинское слово spectrum - изображение греческое слово (skopein) - смотреть И. Ньютон – 1672 год впервые использовал термин «спектр» при изучении света.
 Типы излучения используемые в спектроскопии 1 – электромагнитное излучение 2 – элементарные частицы (электроны, нейтроны, протоны) 3 – ядра атомов ( -частицы) 4 – ионы 5 – ультразвуковые волны Обычно используется электромагнитное излучение (например, инфракрасная и Рамановская спектроскопии) и излучение вызываемое элементарными частицами (например, катодолюминесценция)
Типы излучения используемые в спектроскопии 1 – электромагнитное излучение 2 – элементарные частицы (электроны, нейтроны, протоны) 3 – ядра атомов ( -частицы) 4 – ионы 5 – ультразвуковые волны Обычно используется электромагнитное излучение (например, инфракрасная и Рамановская спектроскопии) и излучение вызываемое элементарными частицами (например, катодолюминесценция)
 М. Планк – 1900 год энергия испускается и поглощается телами не непрерывно, а дискретно, отдельными порциями - квантами А. Эйнштейн – 1905 год электромагнитная энергия существует только в форме квантов излучение представляет собой поток неделимых частиц – фотонов Энергия излучения, E, пропорциональна его частоте, E = h , где h – постоянная Планка (6. 626069. 10 -34 J/s) Фотон обладает и волновыми и корпускулярными свойствами (волновой характер распространения, способность к интерференции, дифракции; способность к взаимодействию с другими материальными частицами, например электронами)
М. Планк – 1900 год энергия испускается и поглощается телами не непрерывно, а дискретно, отдельными порциями - квантами А. Эйнштейн – 1905 год электромагнитная энергия существует только в форме квантов излучение представляет собой поток неделимых частиц – фотонов Энергия излучения, E, пропорциональна его частоте, E = h , где h – постоянная Планка (6. 626069. 10 -34 J/s) Фотон обладает и волновыми и корпускулярными свойствами (волновой характер распространения, способность к интерференции, дифракции; способность к взаимодействию с другими материальными частицами, например электронами)
 Н. Бор – 1913 год - Постулаты Электрон может вращаться вокруг ядра не по любым, а только по некоторым определенным круговым орбитам – стационарным орбитам Двигаясь по стационарной орбите, электрон не излучает электромагнитной энергии Излучение происходит при переходе электрона с одной стационарной орбиты на другую, при этом испускается или поглощается квант электромагнитного излучения, энергия которого равна разности энергии атома в конечном и исходном состоянии
Н. Бор – 1913 год - Постулаты Электрон может вращаться вокруг ядра не по любым, а только по некоторым определенным круговым орбитам – стационарным орбитам Двигаясь по стационарной орбите, электрон не излучает электромагнитной энергии Излучение происходит при переходе электрона с одной стационарной орбиты на другую, при этом испускается или поглощается квант электромагнитного излучения, энергия которого равна разности энергии атома в конечном и исходном состоянии
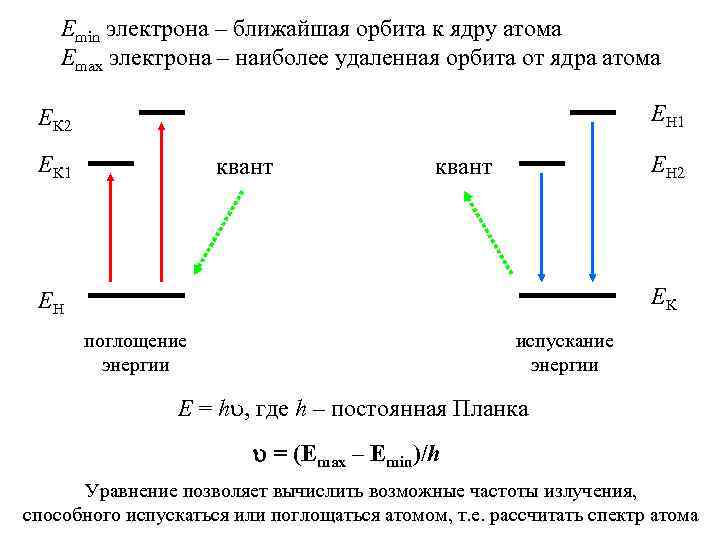 Emin электрона – ближайшая орбита к ядру атома Emax электрона – наиболее удаленная орбита от ядра атома EН 1 EК 2 EК 1 квант EН 2 квант EК EН поглощение энергии испускание энергии E = h , где h – постоянная Планка = (Еmax – Еmin)/h Уравнение позволяет вычислить возможные частоты излучения, способного испускаться или поглощаться атомом, т. е. рассчитать спектр атома
Emin электрона – ближайшая орбита к ядру атома Emax электрона – наиболее удаленная орбита от ядра атома EН 1 EК 2 EК 1 квант EН 2 квант EК EН поглощение энергии испускание энергии E = h , где h – постоянная Планка = (Еmax – Еmin)/h Уравнение позволяет вычислить возможные частоты излучения, способного испускаться или поглощаться атомом, т. е. рассчитать спектр атома
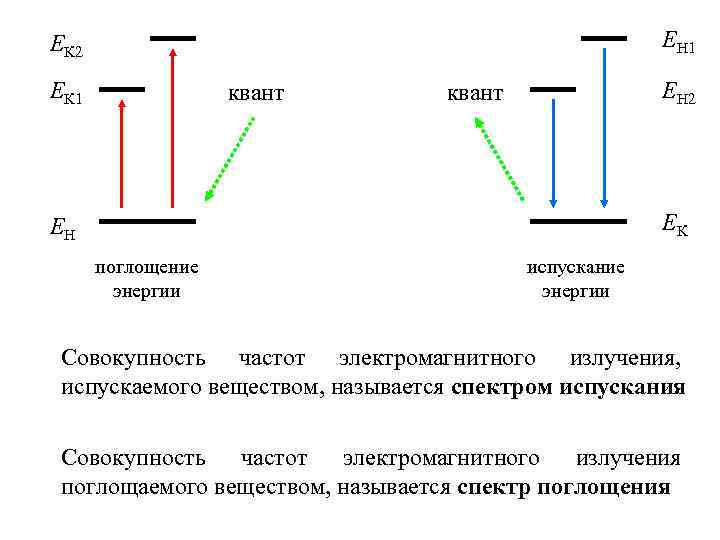 EН 1 EК 2 EК 1 квант EН 2 квант EК EН поглощение энергии испускание энергии Совокупность частот электромагнитного излучения, испускаемого веществом, называется спектром испускания Совокупность частот электромагнитного излучения поглощаемого веществом, называется спектр поглощения
EН 1 EК 2 EК 1 квант EН 2 квант EК EН поглощение энергии испускание энергии Совокупность частот электромагнитного излучения, испускаемого веществом, называется спектром испускания Совокупность частот электромагнитного излучения поглощаемого веществом, называется спектр поглощения
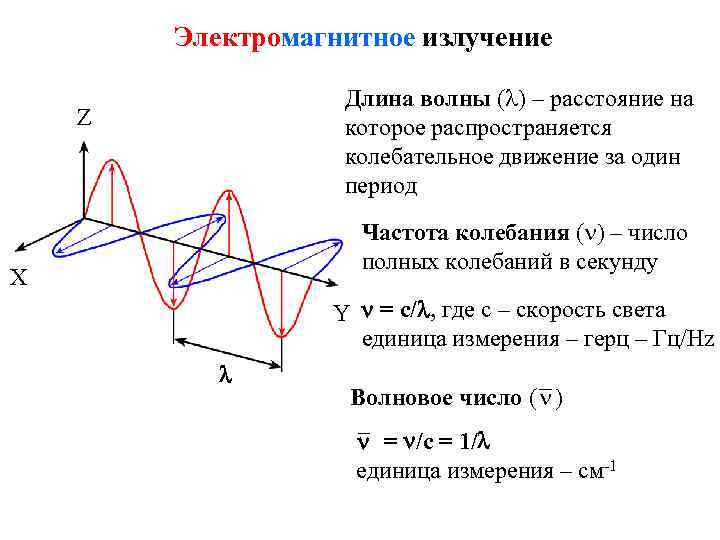 Электромагнитное излучение Длина волны ( ) – расстояние на которое распространяется колебательное движение за один период Z Частота колебания ( ) – число полных колебаний в секунду X Y = c/ , где с – скорость света единица измерения – герц – Гц/Hz Волновое число ( ) = /c = 1/ единица измерения – см-1
Электромагнитное излучение Длина волны ( ) – расстояние на которое распространяется колебательное движение за один период Z Частота колебания ( ) – число полных колебаний в секунду X Y = c/ , где с – скорость света единица измерения – герц – Гц/Hz Волновое число ( ) = /c = 1/ единица измерения – см-1
 что важно помнить… E = hc/ = hc (или E = ħ или E = ħck) Е – энергия излучения h – постоянная Планка – частота с – скорость света – длина волны – волновое число ħ = h/2 - редуцированная постоянная Планка = 2 - угловая (радиальная) частота k = 2 / - волновой вектор
что важно помнить… E = hc/ = hc (или E = ħ или E = ħck) Е – энергия излучения h – постоянная Планка – частота с – скорость света – длина волны – волновое число ħ = h/2 - редуцированная постоянная Планка = 2 - угловая (радиальная) частота k = 2 / - волновой вектор
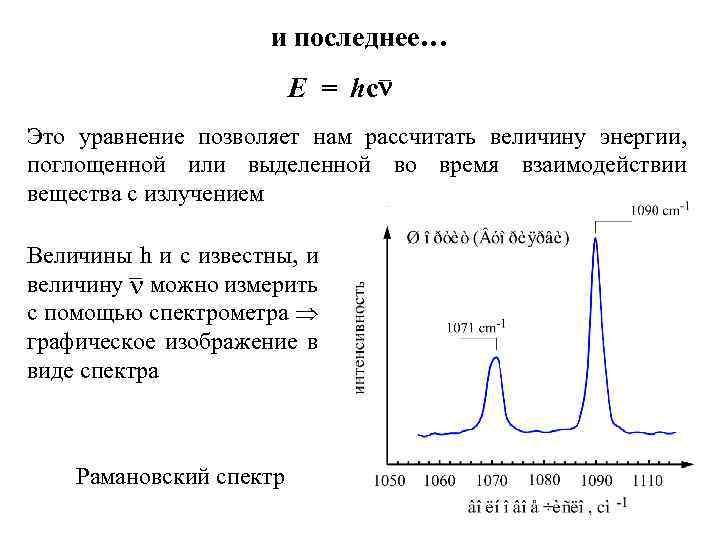 и последнее… E = hc Это уравнение позволяет нам рассчитать величину энергии, поглощенной или выделенной во время взаимодействии вещества с излучением Величины h и c известны, и величину можно измерить с помощью спектрометра графическое изображение в виде спектра Рамановский спектр
и последнее… E = hc Это уравнение позволяет нам рассчитать величину энергии, поглощенной или выделенной во время взаимодействии вещества с излучением Величины h и c известны, и величину можно измерить с помощью спектрометра графическое изображение в виде спектра Рамановский спектр
 Электромагнитные излучения и спектроскопические методы
Электромагнитные излучения и спектроскопические методы
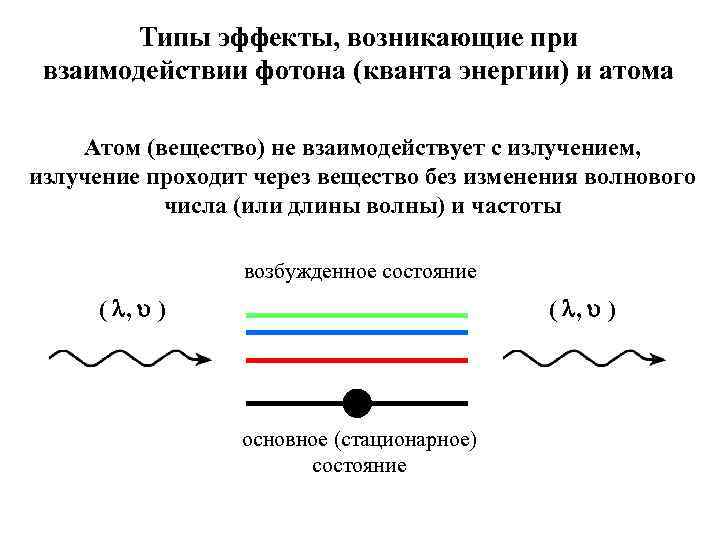 Типы эффекты, возникающие при взаимодействии фотона (кванта энергии) и атома Атом (вещество) не взаимодействует с излучением, излучение проходит через вещество без изменения волнового числа (или длины волны) и частоты возбужденное состояние ( , ) основное (стационарное) состояние
Типы эффекты, возникающие при взаимодействии фотона (кванта энергии) и атома Атом (вещество) не взаимодействует с излучением, излучение проходит через вещество без изменения волнового числа (или длины волны) и частоты возбужденное состояние ( , ) основное (стационарное) состояние
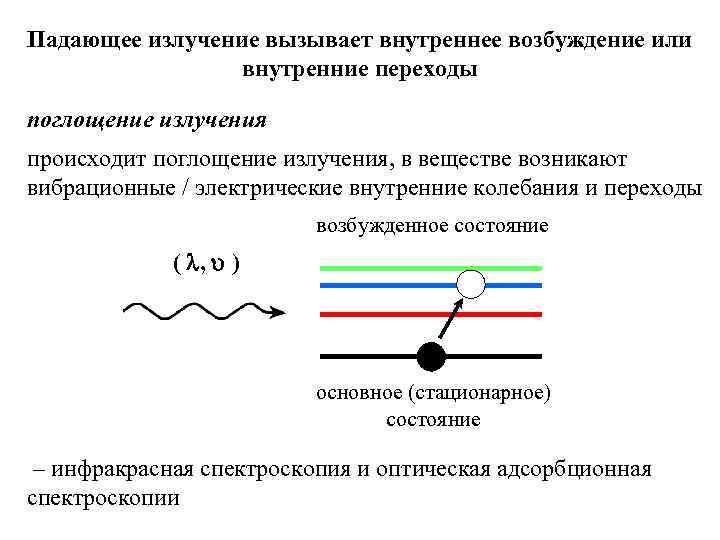 Падающее излучение вызывает внутреннее возбуждение или внутренние переходы поглощение излучения происходит поглощение излучения, в веществе возникают вибрационные / электрические внутренние колебания и переходы возбужденное состояние ( , ) основное (стационарное) состояние – инфракрасная спектроскопия и оптическая адсорбционная спектроскопии
Падающее излучение вызывает внутреннее возбуждение или внутренние переходы поглощение излучения происходит поглощение излучения, в веществе возникают вибрационные / электрические внутренние колебания и переходы возбужденное состояние ( , ) основное (стационарное) состояние – инфракрасная спектроскопия и оптическая адсорбционная спектроскопии
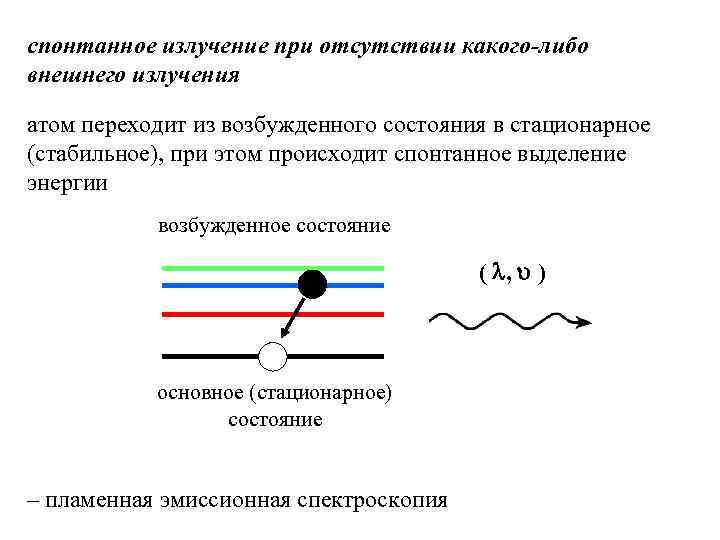 спонтанное излучение при отсутствии какого-либо внешнего излучения атом переходит из возбужденного состояния в стационарное (стабильное), при этом происходит спонтанное выделение энергии возбужденное состояние ( , ) основное (стационарное) состояние – пламенная эмиссионная спектроскопия
спонтанное излучение при отсутствии какого-либо внешнего излучения атом переходит из возбужденного состояния в стационарное (стабильное), при этом происходит спонтанное выделение энергии возбужденное состояние ( , ) основное (стационарное) состояние – пламенная эмиссионная спектроскопия
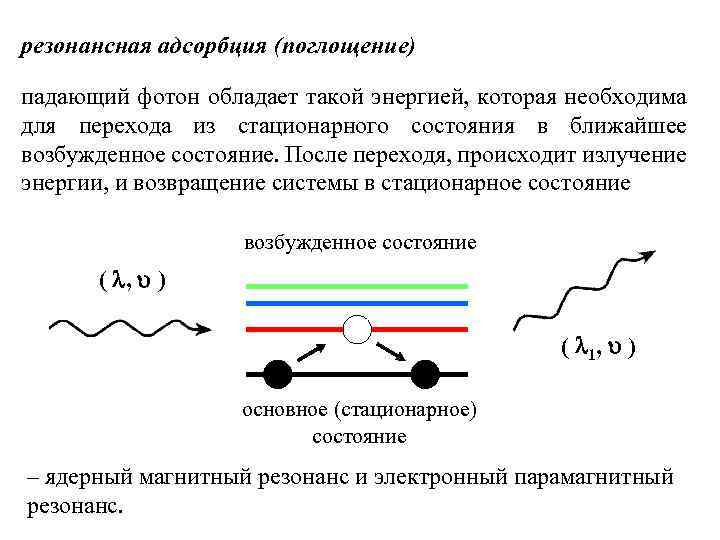 резонансная адсорбция (поглощение) падающий фотон обладает такой энергией, которая необходима для перехода из стационарного состояния в ближайшее возбужденное состояние. После переходя, происходит излучение энергии, и возвращение системы в стационарное состояние возбужденное состояние ( , ) ( 1, ) основное (стационарное) состояние – ядерный магнитный резонанс и электронный парамагнитный резонанс.
резонансная адсорбция (поглощение) падающий фотон обладает такой энергией, которая необходима для перехода из стационарного состояния в ближайшее возбужденное состояние. После переходя, происходит излучение энергии, и возвращение системы в стационарное состояние возбужденное состояние ( , ) ( 1, ) основное (стационарное) состояние – ядерный магнитный резонанс и электронный парамагнитный резонанс.
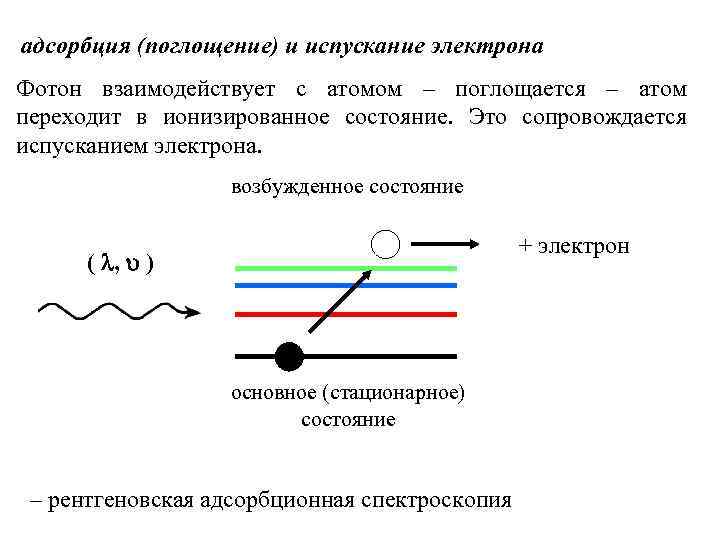 адсорбция (поглощение) и испускание электрона Фотон взаимодействует с атомом – поглощается – атом переходит в ионизированное состояние. Это сопровождается испусканием электрона. возбужденное состояние + электрон ( , ) основное (стационарное) состояние – рентгеновская адсорбционная спектроскопия
адсорбция (поглощение) и испускание электрона Фотон взаимодействует с атомом – поглощается – атом переходит в ионизированное состояние. Это сопровождается испусканием электрона. возбужденное состояние + электрон ( , ) основное (стационарное) состояние – рентгеновская адсорбционная спектроскопия
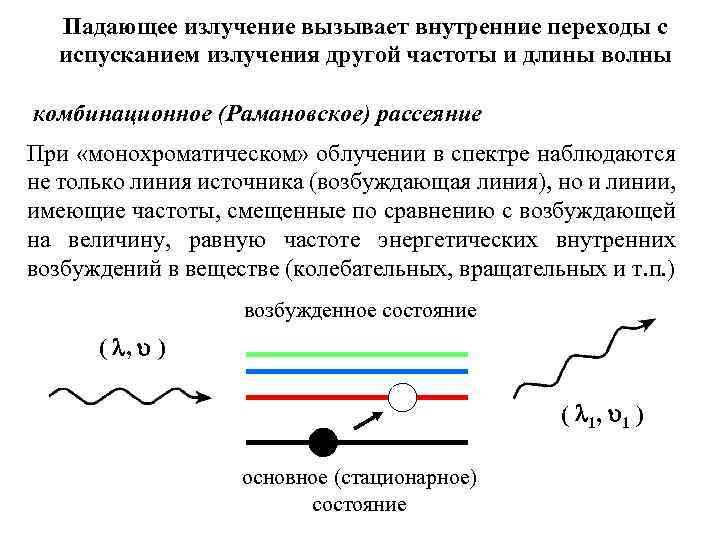 Падающее излучение вызывает внутренние переходы с испусканием излучения другой частоты и длины волны комбинационное (Рамановское) рассеяние При «монохроматическом» облучении в спектре наблюдаются не только линия источника (возбуждающая линия), но и линии, имеющие частоты, смещенные по сравнению с возбуждающей на величину, равную частоте энергетических внутренних возбуждений в веществе (колебательных, вращательных и т. п. ) возбужденное состояние ( , ) ( 1, 1 ) основное (стационарное) состояние
Падающее излучение вызывает внутренние переходы с испусканием излучения другой частоты и длины волны комбинационное (Рамановское) рассеяние При «монохроматическом» облучении в спектре наблюдаются не только линия источника (возбуждающая линия), но и линии, имеющие частоты, смещенные по сравнению с возбуждающей на величину, равную частоте энергетических внутренних возбуждений в веществе (колебательных, вращательных и т. п. ) возбужденное состояние ( , ) ( 1, 1 ) основное (стационарное) состояние
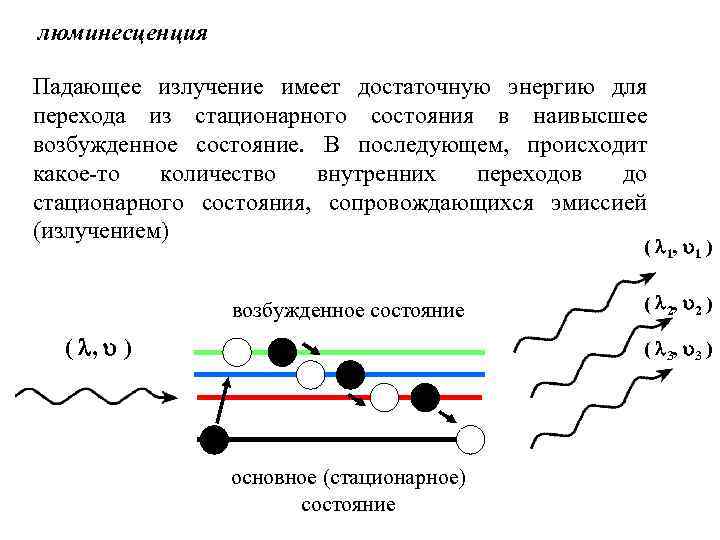 люминесценция Падающее излучение имеет достаточную энергию для перехода из стационарного состояния в наивысшее возбужденное состояние. В последующем, происходит какое-то количество внутренних переходов до стационарного состояния, сопровождающихся эмиссией (излучением) ( 1 , 1 ) возбужденное состояние ( , ) ( 2 , 2 ) ( 3 , 3 ) основное (стационарное) состояние
люминесценция Падающее излучение имеет достаточную энергию для перехода из стационарного состояния в наивысшее возбужденное состояние. В последующем, происходит какое-то количество внутренних переходов до стационарного состояния, сопровождающихся эмиссией (излучением) ( 1 , 1 ) возбужденное состояние ( , ) ( 2 , 2 ) ( 3 , 3 ) основное (стационарное) состояние


