 Спектроскопические методы Исследование материалов
Спектроскопические методы Исследование материалов
 Атомные спектры Пусть исследуется вещество, состоящее из отдельных атомов (атомарный газ) Ядро и электронные орбиты Переходы электронов с орбиты на орбиту сопровождаются излучением (поглощением) света определенной частоты
Атомные спектры Пусть исследуется вещество, состоящее из отдельных атомов (атомарный газ) Ядро и электронные орбиты Переходы электронов с орбиты на орбиту сопровождаются излучением (поглощением) света определенной частоты
 Уровни энергии атомов Водородноподобный атом (ядро и один электрон): n – главное квантовое число Каждой энергии соответствует несколько орбит с орбитальным числом l = 0. . n-1 Для разных масс m уровни энергии различны!
Уровни энергии атомов Водородноподобный атом (ядро и один электрон): n – главное квантовое число Каждой энергии соответствует несколько орбит с орбитальным числом l = 0. . n-1 Для разных масс m уровни энергии различны!
 Многоэлектронные атомы Задача расчета уровней энергии таких систем очень Сложна. Взаимодействие электронов и принцип Паули приводят к тому, что энергетические уровни не будут являться простыми суммами энергий независимых электронов. В соответствии с одноэлектронной проблемой можем ввести понятие конфигурации, например (1 s)22 p, но это лишь приближенно описывает состояние атома (энергии отдельных электронов не сохраняются), сохраняются их суммарные энергия и моменты орбитального и спинового количества движения: L, S, ML, MS + спин-орбитальное взаимодействие
Многоэлектронные атомы Задача расчета уровней энергии таких систем очень Сложна. Взаимодействие электронов и принцип Паули приводят к тому, что энергетические уровни не будут являться простыми суммами энергий независимых электронов. В соответствии с одноэлектронной проблемой можем ввести понятие конфигурации, например (1 s)22 p, но это лишь приближенно описывает состояние атома (энергии отдельных электронов не сохраняются), сохраняются их суммарные энергия и моменты орбитального и спинового количества движения: L, S, ML, MS + спин-орбитальное взаимодействие
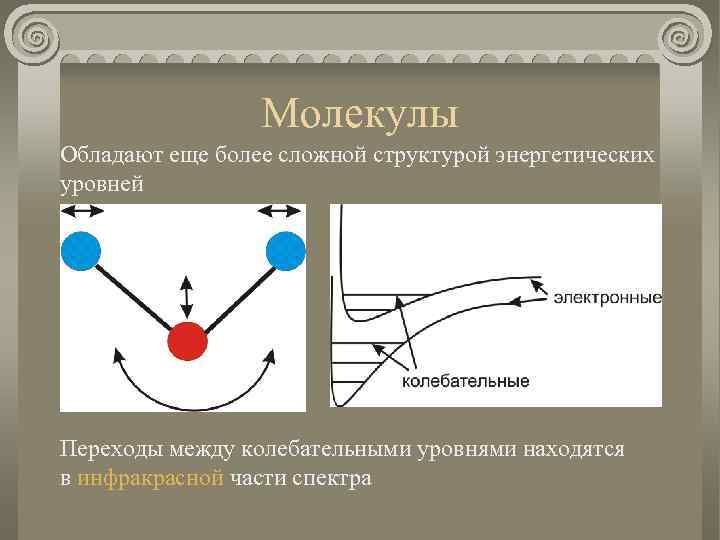 Молекулы Обладают еще более сложной структурой энергетических уровней Переходы между колебательными уровнями находятся в инфракрасной части спектра
Молекулы Обладают еще более сложной структурой энергетических уровней Переходы между колебательными уровнями находятся в инфракрасной части спектра
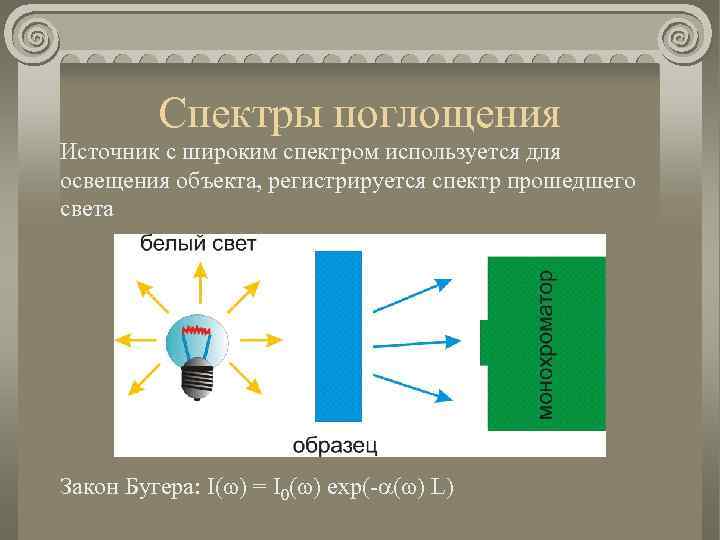 Спектры поглощения Источник с широким спектром используется для освещения объекта, регистрируется спектр прошедшего света Закон Бугера: I(w) = I 0(w) exp(-a(w) L)
Спектры поглощения Источник с широким спектром используется для освещения объекта, регистрируется спектр прошедшего света Закон Бугера: I(w) = I 0(w) exp(-a(w) L)
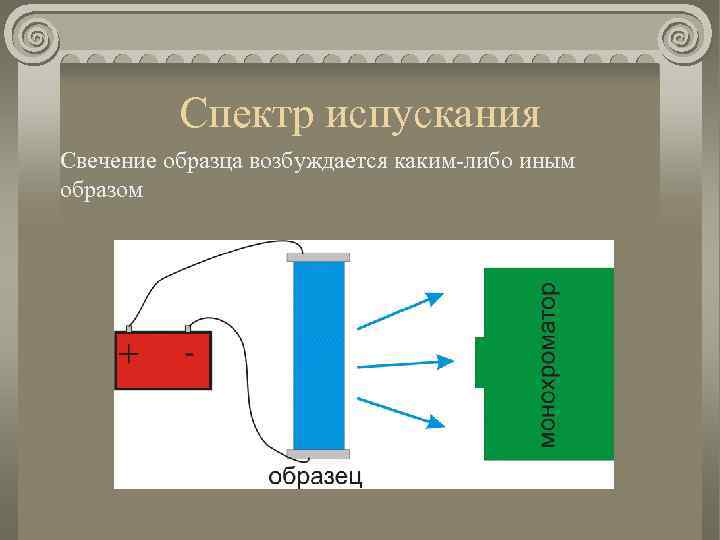 Спектр испускания Свечение образца возбуждается каким-либо иным образом
Спектр испускания Свечение образца возбуждается каким-либо иным образом
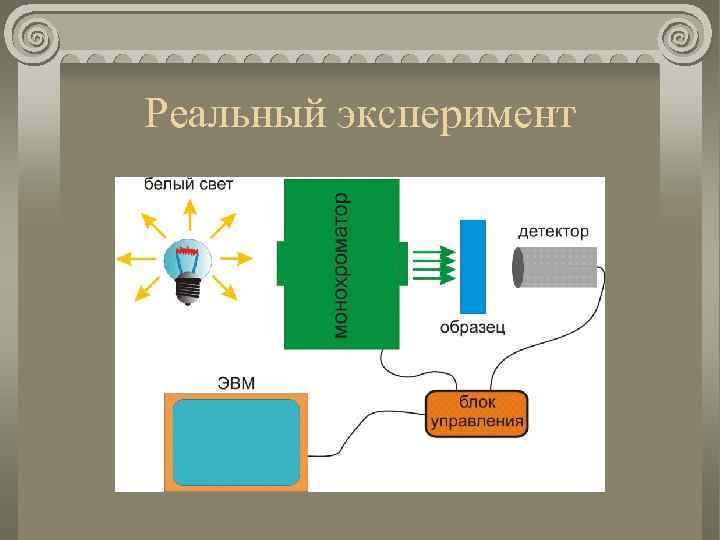 Реальный эксперимент
Реальный эксперимент
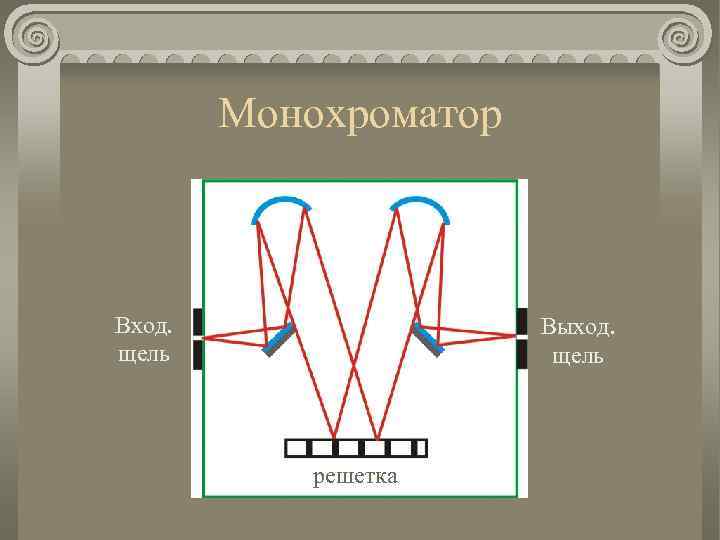 Монохроматор Вход. щель Выход. щель решетка
Монохроматор Вход. щель Выход. щель решетка
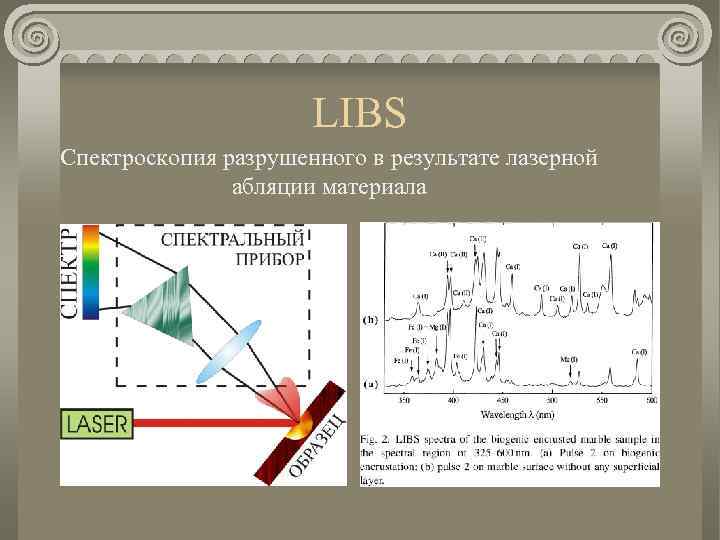 LIBS Спектроскопия разрушенного в результате лазерной абляции материала
LIBS Спектроскопия разрушенного в результате лазерной абляции материала