Лекция 12 Люминесцентная спектроскопия.ppt
- Количество слайдов: 59
 Спектроскопические методы анализа Люминесцентная спектроскопия Лекция 12
Спектроскопические методы анализа Люминесцентная спектроскопия Лекция 12
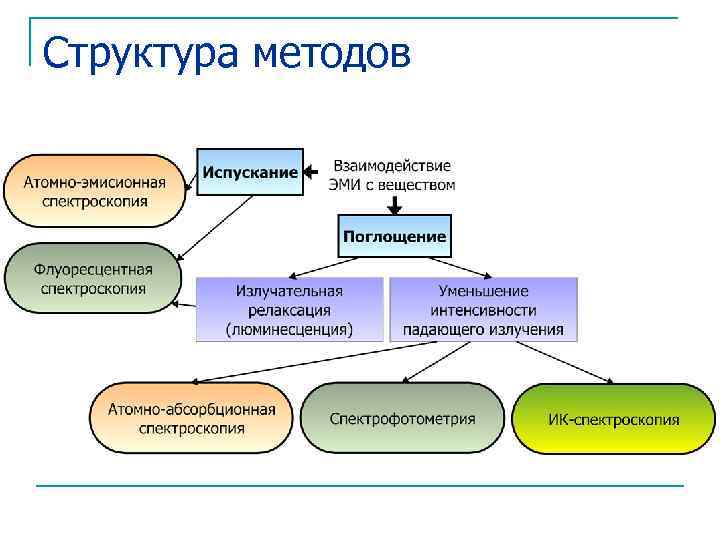 Структура методов
Структура методов
 Определение люминесценции n n n Люминесценция – это свечение атомов, молекул, ионов и других более сложных комплексов, возникающее в результате электронного перехода в этих частицах при их возвращении из возбужденного состояния в основное. Для возбуждения необходимо подводить энергию извне, поскольку она теряется при излучении. Процесс неравновесный.
Определение люминесценции n n n Люминесценция – это свечение атомов, молекул, ионов и других более сложных комплексов, возникающее в результате электронного перехода в этих частицах при их возвращении из возбужденного состояния в основное. Для возбуждения необходимо подводить энергию извне, поскольку она теряется при излучении. Процесс неравновесный.
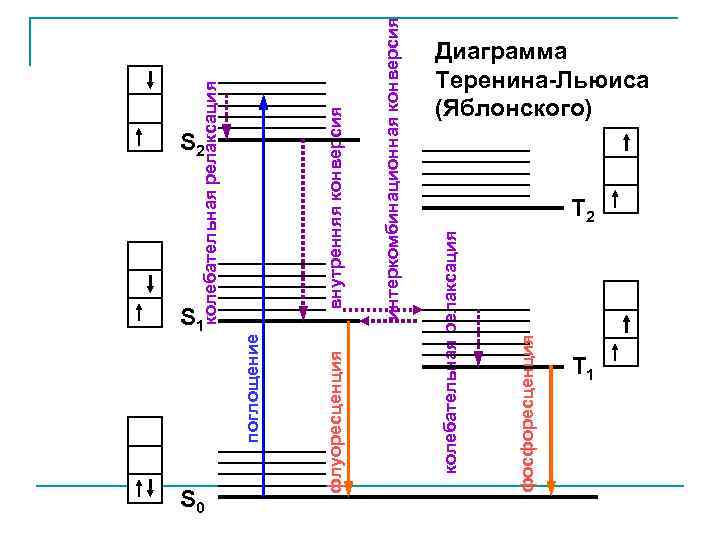 интеркомбинационная конверсия фосфоресценция колебательная релаксация флуоресценция S 0 внутренняя конверсия S 1 поглощение колебательная релаксация S 2 Диаграмма Теренина-Льюиса (Яблонского) T 2 T 1
интеркомбинационная конверсия фосфоресценция колебательная релаксация флуоресценция S 0 внутренняя конверсия S 1 поглощение колебательная релаксация S 2 Диаграмма Теренина-Льюиса (Яблонского) T 2 T 1
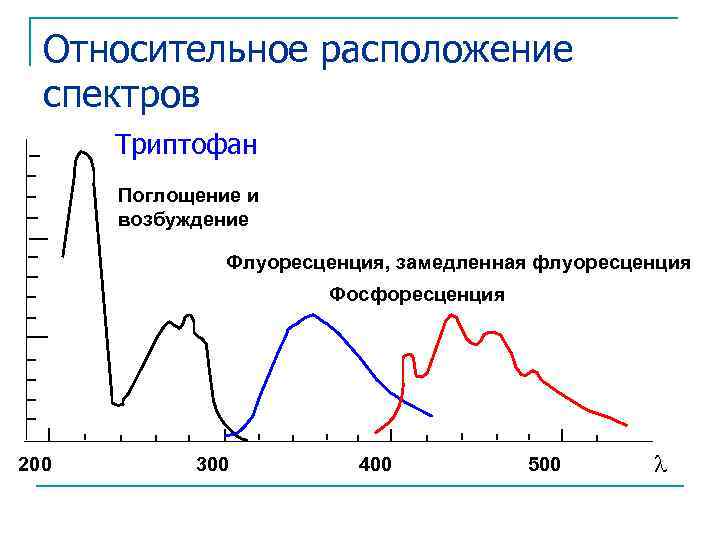 Относительное расположение спектров Триптофан Поглощение и возбуждение Флуоресценция, замедленная флуоресценция Фосфоресценция 200 300 400 500
Относительное расположение спектров Триптофан Поглощение и возбуждение Флуоресценция, замедленная флуоресценция Фосфоресценция 200 300 400 500
 Основные законы флуоресценции
Основные законы флуоресценции
 Основные характеристики люминесценции 1. Спектр возбуждения люминесценции и спектр люминесценции 2. Энергетический и квантовый выход 3. Кинетика люминесценции
Основные характеристики люминесценции 1. Спектр возбуждения люминесценции и спектр люминесценции 2. Энергетический и квантовый выход 3. Кинетика люминесценции
 Спектр возбуждения люминесценции n n n Характеризует активное поглощение люминофоров Обычно представляют в виде зависимости интенсивности излучения от длины волны возбуждающего света Спектр возбуждения люминесценции близок, но не совпадает со спектром поглощения
Спектр возбуждения люминесценции n n n Характеризует активное поглощение люминофоров Обычно представляют в виде зависимости интенсивности излучения от длины волны возбуждающего света Спектр возбуждения люминесценции близок, но не совпадает со спектром поглощения
 Спектры люминесценции n n Обусловлены электронными переходами из возбужденного состояния в основное Обычно представляют в виде зависимости интенсивности излучения от длины волны
Спектры люминесценции n n Обусловлены электронными переходами из возбужденного состояния в основное Обычно представляют в виде зависимости интенсивности излучения от длины волны
 Основные законы люминесценции 1. Правило Стокса и закон Стокса. Ломмеля 2. Правило Каши 3. Закон Вавилова 4. Правило Левшина (зеркальной симметрии)
Основные законы люминесценции 1. Правило Стокса и закон Стокса. Ломмеля 2. Правило Каши 3. Закон Вавилова 4. Правило Левшина (зеркальной симметрии)
 I. Правило Стокса Свет люминесценции имеет меньшую частоту, чем поглощенный возбуждающий свет флуоресценция поглощение ν Область спектра люминесценции, где правило Стокса выполняется «стоксова область» , где не выполняется – «антистоксова область»
I. Правило Стокса Свет люминесценции имеет меньшую частоту, чем поглощенный возбуждающий свет флуоресценция поглощение ν Область спектра люминесценции, где правило Стокса выполняется «стоксова область» , где не выполняется – «антистоксова область»
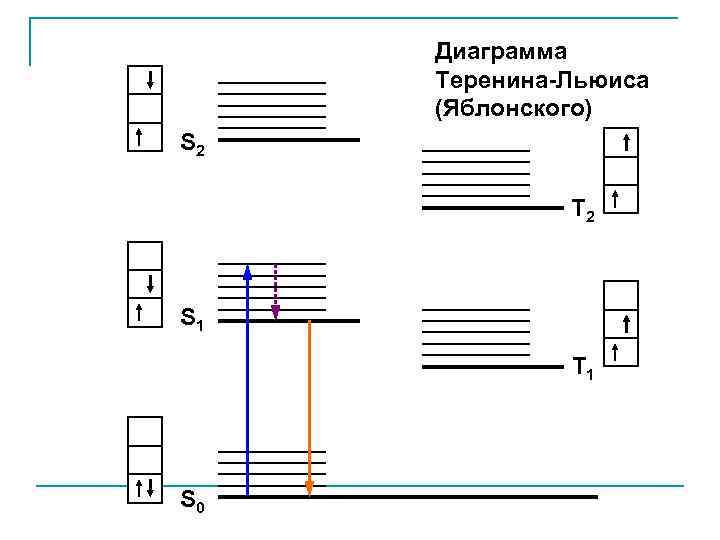 Диаграмма Теренина-Льюиса (Яблонского) S 2 T 2 S 1 T 1 S 0
Диаграмма Теренина-Льюиса (Яблонского) S 2 T 2 S 1 T 1 S 0
 Правило Стокса n n Антистоксова область не противоречит закону сохранения энергии: Некоторая часть молекул до возбуждения имеет запас колебательной энергии h кол Поскольку число электронов, находящихся на колебательных уровнях меньше, чем на основном, интенсивность излучения в антистоксовой области ниже, чем в стоксовой
Правило Стокса n n Антистоксова область не противоречит закону сохранения энергии: Некоторая часть молекул до возбуждения имеет запас колебательной энергии h кол Поскольку число электронов, находящихся на колебательных уровнях меньше, чем на основном, интенсивность излучения в антистоксовой области ниже, чем в стоксовой
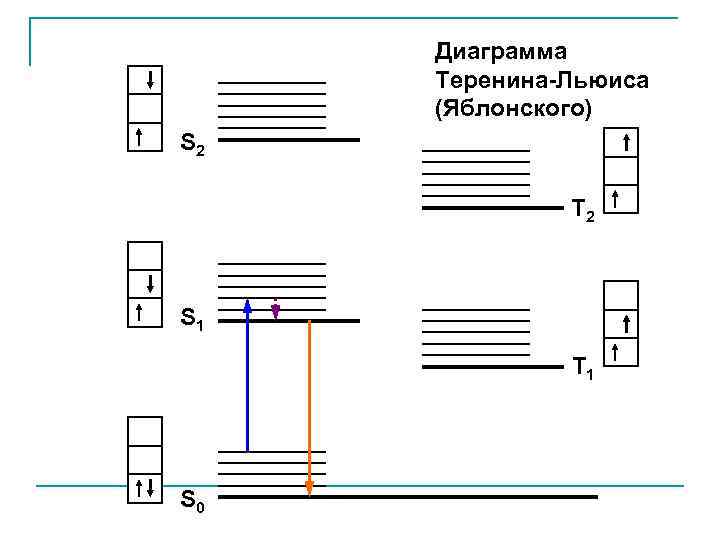 Диаграмма Теренина-Льюиса (Яблонского) S 2 T 2 S 1 T 1 S 0
Диаграмма Теренина-Льюиса (Яблонского) S 2 T 2 S 1 T 1 S 0
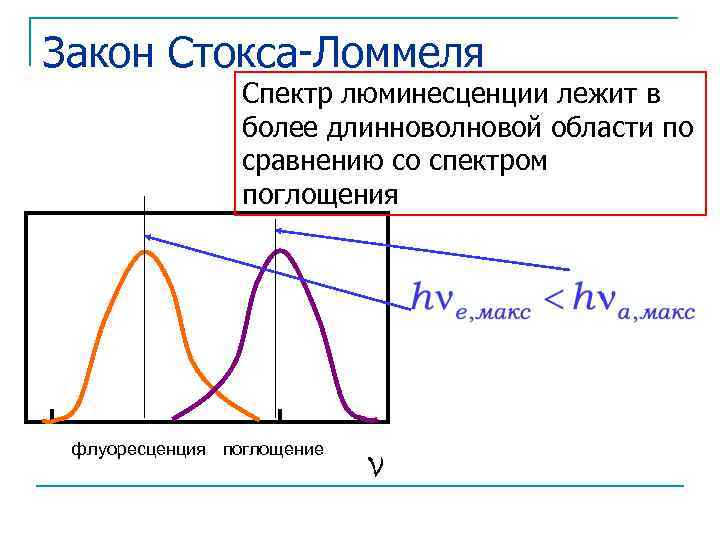 Закон Стокса-Ломмеля Спектр люминесценции лежит в более длинноволновой области по сравнению со спектром поглощения флуоресценция поглощение ν
Закон Стокса-Ломмеля Спектр люминесценции лежит в более длинноволновой области по сравнению со спектром поглощения флуоресценция поглощение ν
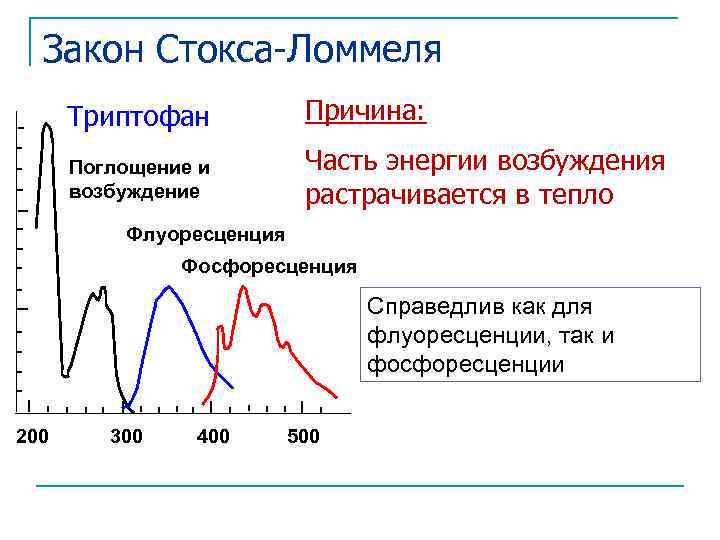 Закон Стокса-Ломмеля Триптофан Причина: Поглощение и возбуждение Часть энергии возбуждения растрачивается в тепло Флуоресценция Фосфоресценция Справедлив как для флуоресценции, так и фосфоресценции 200 300 400 500
Закон Стокса-Ломмеля Триптофан Причина: Поглощение и возбуждение Часть энергии возбуждения растрачивается в тепло Флуоресценция Фосфоресценция Справедлив как для флуоресценции, так и фосфоресценции 200 300 400 500
 II. Правило Каши Спектр люминесценции не зависит от длины волны возбуждения Причина: Молекула живет дольше всего на нижнем подуровне возбужденного состояния и испускает фотон из этого состояния (колебательная релаксация + внутренняя конверсия – очень быстрые процессы)
II. Правило Каши Спектр люминесценции не зависит от длины волны возбуждения Причина: Молекула живет дольше всего на нижнем подуровне возбужденного состояния и испускает фотон из этого состояния (колебательная релаксация + внутренняя конверсия – очень быстрые процессы)
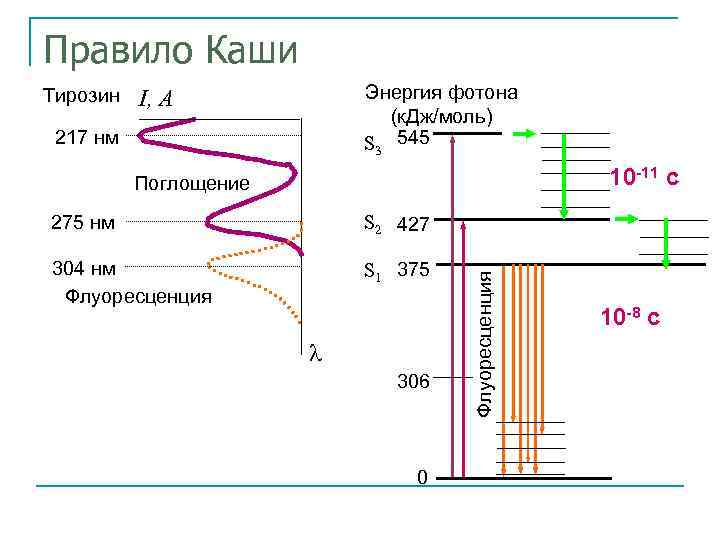 Правило Каши Тирозин Энергия фотона (к. Дж/моль) S 3 545 I, A 217 нм 10 -11 с Поглощение S 2 427 304 нм Флуоресценция S 1 375 306 0 Флуоресценция 275 нм 10 -8 с
Правило Каши Тирозин Энергия фотона (к. Дж/моль) S 3 545 I, A 217 нм 10 -11 с Поглощение S 2 427 304 нм Флуоресценция S 1 375 306 0 Флуоресценция 275 нм 10 -8 с
 Майкл (Михаил) Каша n n n Один из основателей молекулярной биофизики Вместе с Льюисом доказали, что фосфоресценция связана с триплетными состояниями (1944) Правило (1950)
Майкл (Михаил) Каша n n n Один из основателей молекулярной биофизики Вместе с Льюисом доказали, что фосфоресценция связана с триплетными состояниями (1944) Правило (1950)
 III. Выходы люминесценции n Энергетический выход (КПД) φЕ = Ее/Еа n Квантовый выход (NB: только для фотолюминесценции) φК = Nе/Nа = Iе/Iа n Так как энергия кванта равна h , то E e = N e h e и E a = N ah a φК = φЕ (νа /νе) или φК = φЕ (λе/λа) Так как частота (энергия) поглощения больше, чем частота излучения, φК > φЕ
III. Выходы люминесценции n Энергетический выход (КПД) φЕ = Ее/Еа n Квантовый выход (NB: только для фотолюминесценции) φК = Nе/Nа = Iе/Iа n Так как энергия кванта равна h , то E e = N e h e и E a = N ah a φК = φЕ (νа /νе) или φК = φЕ (λе/λа) Так как частота (энергия) поглощения больше, чем частота излучения, φК > φЕ
 Закон Вавилова. Определение 1 Энергетический выход люминесценции прямо пропорционален длине волны возбуждения (обратно пропорционально частоте) Причина: Молекула живет дольше всего на нижнем подуровне возбужденного состояния и безызлучательный переход происходит из этого состояния => чем меньше потери, тем больше выход
Закон Вавилова. Определение 1 Энергетический выход люминесценции прямо пропорционален длине волны возбуждения (обратно пропорционально частоте) Причина: Молекула живет дольше всего на нижнем подуровне возбужденного состояния и безызлучательный переход происходит из этого состояния => чем меньше потери, тем больше выход
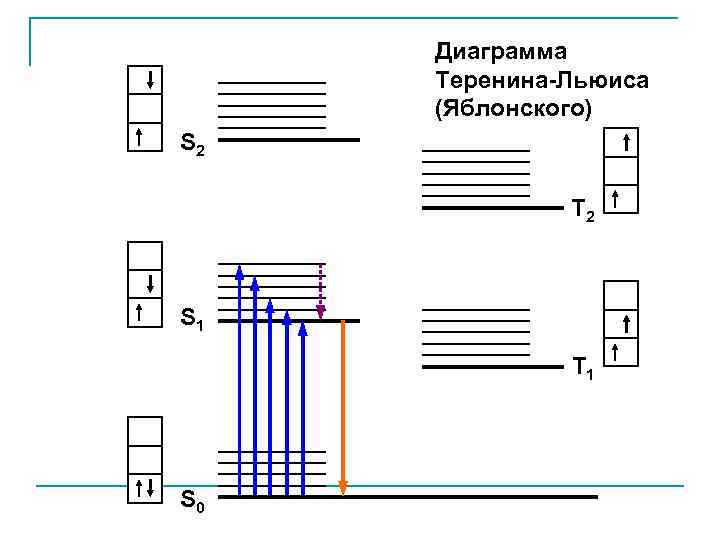 Диаграмма Теренина-Льюиса (Яблонского) S 2 T 2 S 1 T 1 S 0
Диаграмма Теренина-Льюиса (Яблонского) S 2 T 2 S 1 T 1 S 0
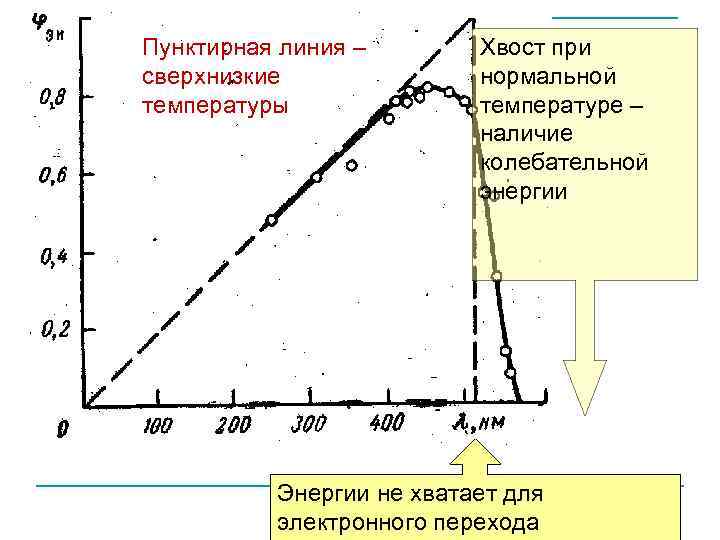 Пунктирная линия – сверхнизкие температуры Хвост при нормальной температуре – наличие колебательной энергии Энергии не хватает для электронного перехода
Пунктирная линия – сверхнизкие температуры Хвост при нормальной температуре – наличие колебательной энергии Энергии не хватает для электронного перехода
 Закон Вавилова. Определение 2 Квантовый выход люминесценции не зависит от длины волны возбуждения (и является характеристикой вещества) φК = φЕ (λе/λа) = = kλа (λе/λа) = = kλе = const Это – лишь другая формулировка закона Вавилова, более удобная для фотолюминесценции
Закон Вавилова. Определение 2 Квантовый выход люминесценции не зависит от длины волны возбуждения (и является характеристикой вещества) φК = φЕ (λе/λа) = = kλа (λе/λа) = = kλе = const Это – лишь другая формулировка закона Вавилова, более удобная для фотолюминесценции
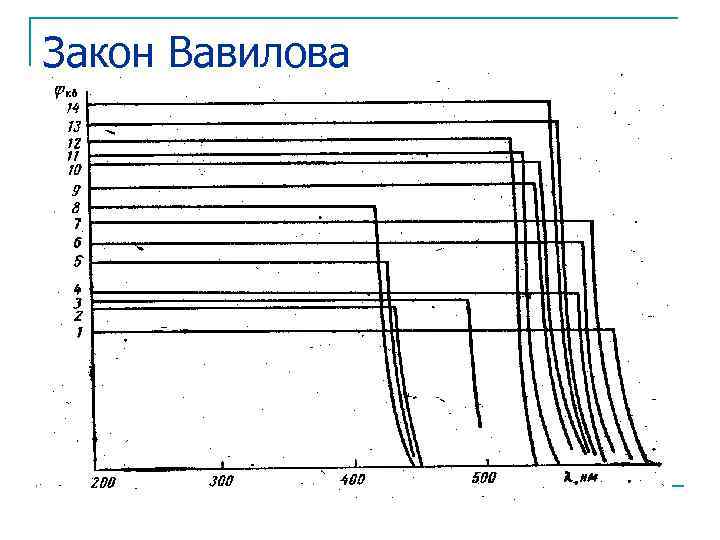 Закон Вавилова
Закон Вавилова
 IV. Правило Левшина (зеркальной симметрии) Нормированные спектры поглощения = f( ) и флуоресценции Ie/ = f( ) зеркально симметричны относительно точки пересечения спектров
IV. Правило Левшина (зеркальной симметрии) Нормированные спектры поглощения = f( ) и флуоресценции Ie/ = f( ) зеркально симметричны относительно точки пересечения спектров
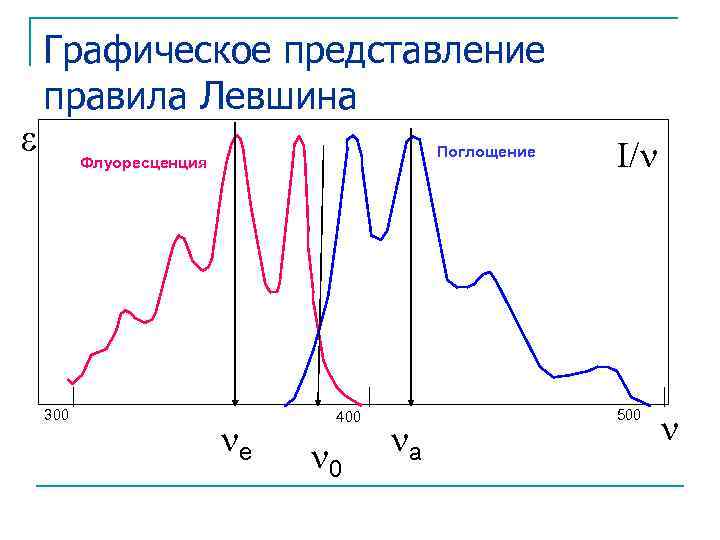 Графическое представление правила Левшина Поглощение Флуоресценция 300 e 400 0 a I/ 500
Графическое представление правила Левшина Поглощение Флуоресценция 300 e 400 0 a I/ 500
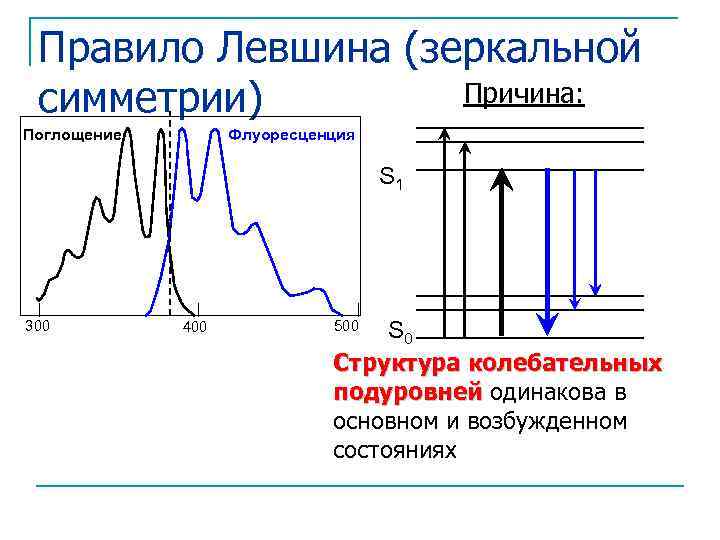 Правило Левшина (зеркальной Причина: симметрии) Поглощение Флуоресценция S 1 300 400 S 0 Структура колебательных подуровней одинакова в основном и возбужденном состояниях 500
Правило Левшина (зеркальной Причина: симметрии) Поглощение Флуоресценция S 1 300 400 S 0 Структура колебательных подуровней одинакова в основном и возбужденном состояниях 500
 Уравнение для количественного анализа
Уравнение для количественного анализа
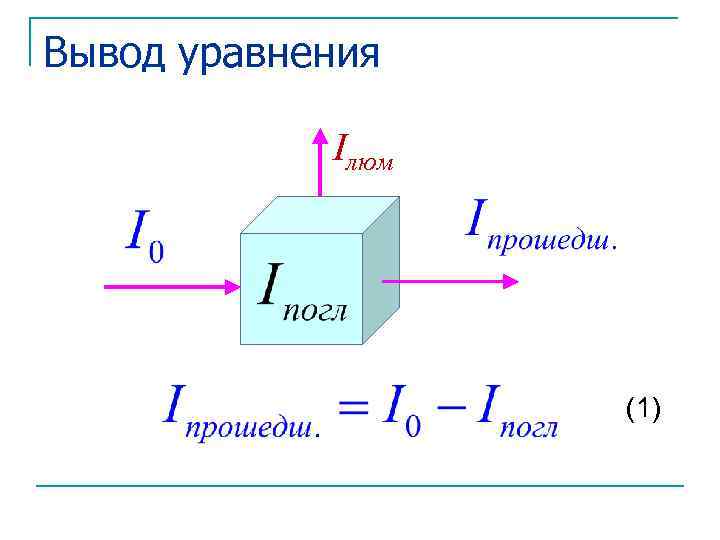 Вывод уравнения Iлюм (1)
Вывод уравнения Iлюм (1)
 Количественный люминесцентный анализ Исходим из закона Бугера-Ламберта-Бера (2) и определения квантового выхода (3)
Количественный люминесцентный анализ Исходим из закона Бугера-Ламберта-Бера (2) и определения квантового выхода (3)
 При условии, что Количественный люминесцентный анализ
При условии, что Количественный люминесцентный анализ
 Отклонения от линейности
Отклонения от линейности
 Отклонения от линейности вызваны 1. Невыполнением условия 2. Явлением концентрационного тушения (верхняя граница диапазона линейности 1 10 -4 3. Эффектом внутреннего фильтра – поглощением люминофором возбуждающего излучения 4. Реабсорбцией (самопоглощением) – поглощением люминофором собственного люминесцентного излучения
Отклонения от линейности вызваны 1. Невыполнением условия 2. Явлением концентрационного тушения (верхняя граница диапазона линейности 1 10 -4 3. Эффектом внутреннего фильтра – поглощением люминофором возбуждающего излучения 4. Реабсорбцией (самопоглощением) – поглощением люминофором собственного люминесцентного излучения
 Тушение люминесценции 1. 2. 3. Под явлением «тушения люминесценции» понимают снижение квантового выхода люминесценции под действием различных факторов Концентрации люминофора Температуры Влияния посторонних веществ
Тушение люминесценции 1. 2. 3. Под явлением «тушения люминесценции» понимают снижение квантового выхода люминесценции под действием различных факторов Концентрации люминофора Температуры Влияния посторонних веществ
 Концентрационное тушение Снижение квантового выхода люминесценции при изменении концентрации люминофора. Причины: n Ассоциация молекул (многие органические красители, фенольные соединения) n Миграция энергии (рост доли безызлучательной релаксации энергии между двумя молекулами люминофора)
Концентрационное тушение Снижение квантового выхода люминесценции при изменении концентрации люминофора. Причины: n Ассоциация молекул (многие органические красители, фенольные соединения) n Миграция энергии (рост доли безызлучательной релаксации энергии между двумя молекулами люминофора)
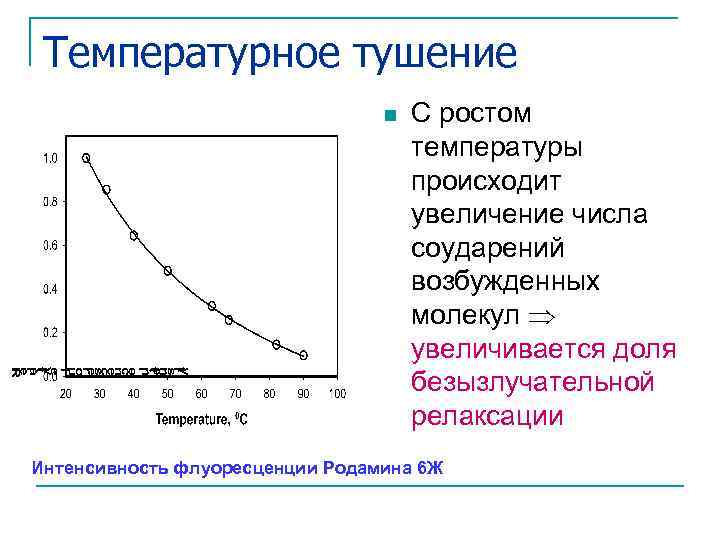 Температурное тушение n С ростом температуры происходит увеличение числа соударений возбужденных молекул увеличивается доля безызлучательной релаксации Интенсивность флуоресценции Родамина 6 Ж
Температурное тушение n С ростом температуры происходит увеличение числа соударений возбужденных молекул увеличивается доля безызлучательной релаксации Интенсивность флуоресценции Родамина 6 Ж
 Тушение посторонними веществами 1. 2. n n n Химическое (статическое) тушение разрушение люминофоров (образование или разрушение комплексов, Физическое (динамическое) тушение передача энергии от люминофора на молекулу-тушитель Растворитель Тяжелые анионы и катионы (иодид-, бромид-ионы, ионы рубидия и цезия) Парамагнитные ионы и молекулы (O 2)
Тушение посторонними веществами 1. 2. n n n Химическое (статическое) тушение разрушение люминофоров (образование или разрушение комплексов, Физическое (динамическое) тушение передача энергии от люминофора на молекулу-тушитель Растворитель Тяжелые анионы и катионы (иодид-, бромид-ионы, ионы рубидия и цезия) Парамагнитные ионы и молекулы (O 2)
 Люминесцентный анализ
Люминесцентный анализ
 Объекты и задачи n n n Флуоресценция природных соединений или образование флуоресцирующих веществ; иммуннофлуоресцентный анализ, Изучение физико-химических свойств систем Микроскопия n n n Флуоресцентная микроскопия, Конфокальная микроскопия, Проточная цитометрия и сортировка
Объекты и задачи n n n Флуоресценция природных соединений или образование флуоресцирующих веществ; иммуннофлуоресцентный анализ, Изучение физико-химических свойств систем Микроскопия n n n Флуоресцентная микроскопия, Конфокальная микроскопия, Проточная цитометрия и сортировка
 Количественный анализ флуориметрия Определение веществ, обладающих собственной люминесценцией 1. q q q 2. 3. полиароматические соединения, витамины (A, В 1, В 2, каротин) гормоны (эстрогены, адреналин, норадреналин), Люминесцентные реакции (аналогично фотометрическим реакциям) – реакции образования люминофоров из исходных веществ Косвенный анализ (аналитический сигнал – тушение люминесценции)
Количественный анализ флуориметрия Определение веществ, обладающих собственной люминесценцией 1. q q q 2. 3. полиароматические соединения, витамины (A, В 1, В 2, каротин) гормоны (эстрогены, адреналин, норадреналин), Люминесцентные реакции (аналогично фотометрическим реакциям) – реакции образования люминофоров из исходных веществ Косвенный анализ (аналитический сигнал – тушение люминесценции)
 Количественный люминесцентный анализ Объекты n Анализ объектов окружающей среды (дистанционный анализ вод и атмосферы) n Определение последовательности аминокислот в белках, нуклеотидов в ДНК n Слежение за движением макромолекул n Использование флуоресцентных меток
Количественный люминесцентный анализ Объекты n Анализ объектов окружающей среды (дистанционный анализ вод и атмосферы) n Определение последовательности аминокислот в белках, нуклеотидов в ДНК n Слежение за движением макромолекул n Использование флуоресцентных меток
 Качественный анализ Несмотря на достаточно широкие полосы люминесценции он возможен, если спектры люминесценции имеют характеристические особенности n n Полиароматические соединения Порфирины Комплексы U(VI) Витамины
Качественный анализ Несмотря на достаточно широкие полосы люминесценции он возможен, если спектры люминесценции имеют характеристические особенности n n Полиароматические соединения Порфирины Комплексы U(VI) Витамины
 Флуориметрия Достоинства n Недеструктивный метод n Низкие пределы обнаружения (10 -11 – 10 -12 М) q n Вплоть до детектирования отдельных молекул В целом, не слишком дорогое и сложное оборудование
Флуориметрия Достоинства n Недеструктивный метод n Низкие пределы обнаружения (10 -11 – 10 -12 М) q n Вплоть до детектирования отдельных молекул В целом, не слишком дорогое и сложное оборудование
 Флуориметрия Недостатки n Достаточно малое число веществ являются люминофорами n Необходима пробоподготовка n Значительные требования к контрольному опыту n Большое число мешающих факторов (отклонения от закона Бера, тушение флуоресценции)
Флуориметрия Недостатки n Достаточно малое число веществ являются люминофорами n Необходима пробоподготовка n Значительные требования к контрольному опыту n Большое число мешающих факторов (отклонения от закона Бера, тушение флуоресценции)
 Фосфориметрия Меньшее число веществ по сравнению с флуоресценцией n Низкие квантовые выходы Приемы n Иммобилизация в жесткой матрице n Использование вязких растворителей n Охлаждение до низких температур (жидкий азот, 77 K) n
Фосфориметрия Меньшее число веществ по сравнению с флуоресценцией n Низкие квантовые выходы Приемы n Иммобилизация в жесткой матрице n Использование вязких растворителей n Охлаждение до низких температур (жидкий азот, 77 K) n
 Низкая вероятность T 1 -S 0 перехода имеет следствие n n n 1. Тушение становится значительным; при комнатной температуре фосфоресценция практически не наблюдается, 2. Одним из главных тушителей является кислород! 3. Метод определения кислорода в тканях и жидкостях
Низкая вероятность T 1 -S 0 перехода имеет следствие n n n 1. Тушение становится значительным; при комнатной температуре фосфоресценция практически не наблюдается, 2. Одним из главных тушителей является кислород! 3. Метод определения кислорода в тканях и жидкостях
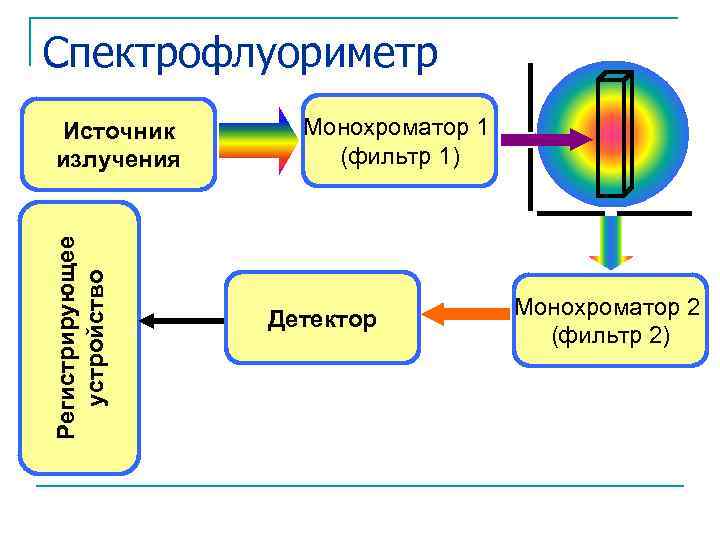 Спектрофлуориметр Регистрирующее устройство Источник излучения Монохроматор 1 (фильтр 1) Детектор Монохроматор 2 (фильтр 2)
Спектрофлуориметр Регистрирующее устройство Источник излучения Монохроматор 1 (фильтр 1) Детектор Монохроматор 2 (фильтр 2)
 Приборы n n Монохроматоры, детекторы, система регистрации не отличается от спектрофотометрии) Источники излучения q q q n Требования к источникам излучения q Высокая интенсивность q q n Чаще всего – УФ-источники Лампы накаливания Лазеры Стабильность Соответствие спектру поглощения люминофоров Могут быть монохроматическими (выполняется правило Каши и закон Вавилова
Приборы n n Монохроматоры, детекторы, система регистрации не отличается от спектрофотометрии) Источники излучения q q q n Требования к источникам излучения q Высокая интенсивность q q n Чаще всего – УФ-источники Лампы накаливания Лазеры Стабильность Соответствие спектру поглощения люминофоров Могут быть монохроматическими (выполняется правило Каши и закон Вавилова
 Приборы n n n Флуориметры (монохроматоры – светофильтры) Спектрофлуориметры (монохроматоры – дифракционные решетки или призмы) Флуориметрические приставки к спектрофотометрам Флуориметрические сенсоры Флуориметрические детекторы
Приборы n n n Флуориметры (монохроматоры – светофильтры) Спектрофлуориметры (монохроматоры – дифракционные решетки или призмы) Флуориметрические приставки к спектрофотометрам Флуориметрические сенсоры Флуориметрические детекторы
 Применение люминесценции в физикохимической биологии
Применение люминесценции в физикохимической биологии
 Изучение физико-химических свойств систем n n n Визуализация биологических систем – флуоресцентная микроскопия Доступность для кислорода – фосфоресценция, Вращательная подвижность молекул – поляризация флуоресценции Поступательная диффузия – эксимеризация пирена, Расстояние между группами – перенос энергии, Изучение биопотенциалов – распределение заряженных зондов,
Изучение физико-химических свойств систем n n n Визуализация биологических систем – флуоресцентная микроскопия Доступность для кислорода – фосфоресценция, Вращательная подвижность молекул – поляризация флуоресценции Поступательная диффузия – эксимеризация пирена, Расстояние между группами – перенос энергии, Изучение биопотенциалов – распределение заряженных зондов,
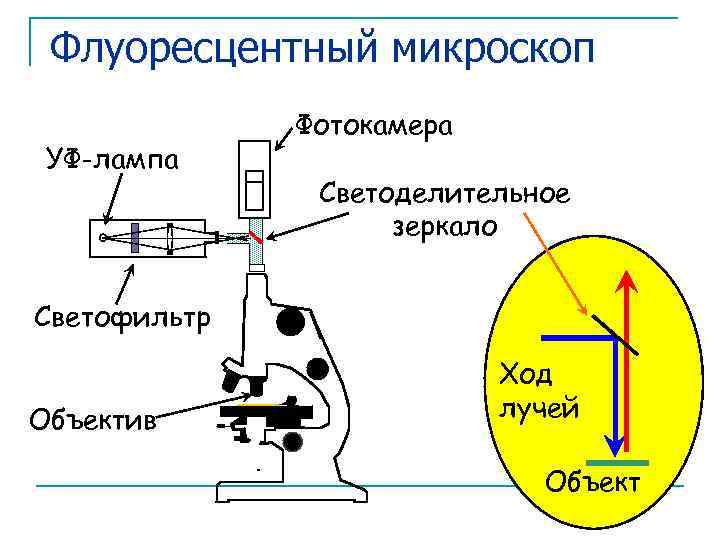 Флуоресцентный микроскоп УФ-лампа Фотокамера Светоделительное зеркало Светофильтр Объектив Ход лучей Объект
Флуоресцентный микроскоп УФ-лампа Фотокамера Светоделительное зеркало Светофильтр Объектив Ход лучей Объект
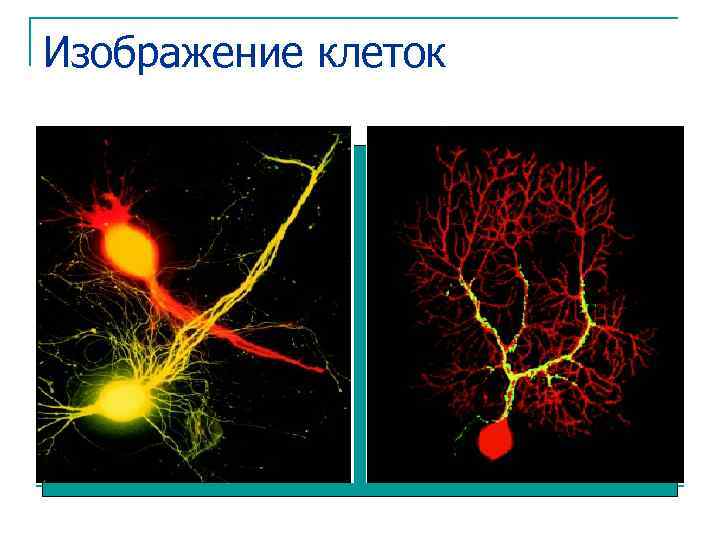 Изображение клеток
Изображение клеток
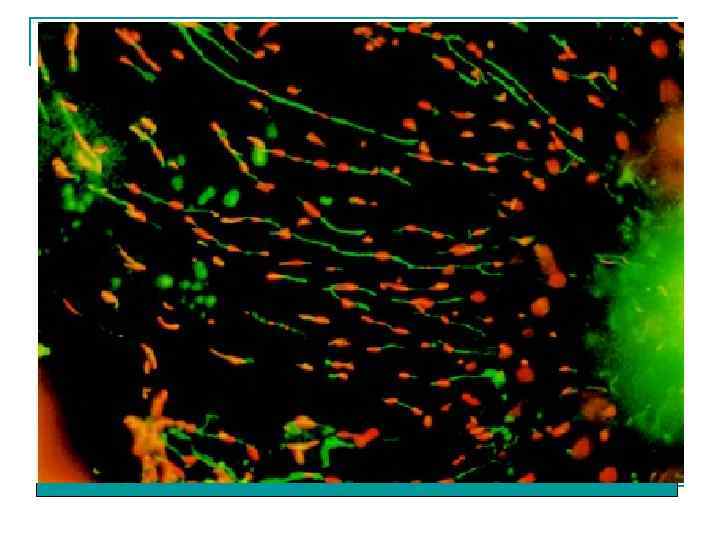
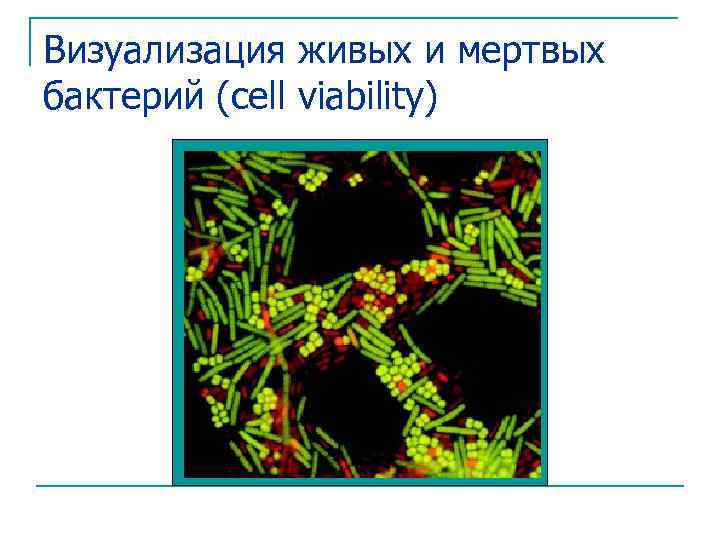 Визуализация живых и мертвых бактерий (cell viability)
Визуализация живых и мертвых бактерий (cell viability)
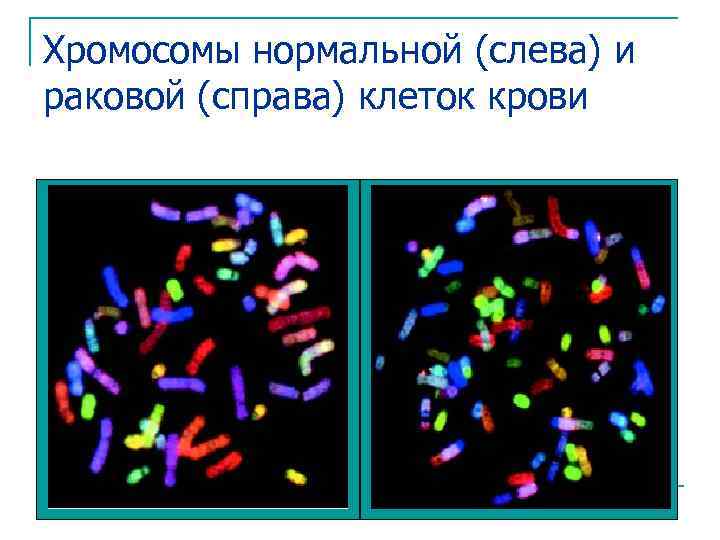 Хромосомы нормальной (слева) и раковой (справа) клеток крови
Хромосомы нормальной (слева) и раковой (справа) клеток крови
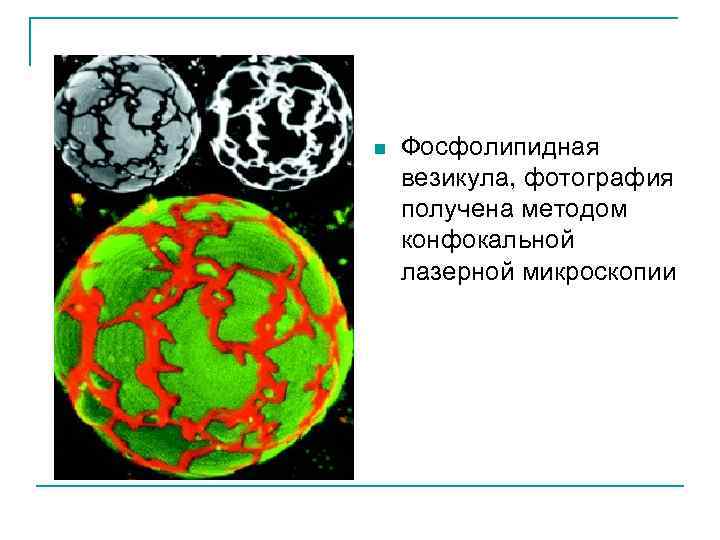 n Фосфолипидная везикула, фотография получена методом конфокальной лазерной микроскопии
n Фосфолипидная везикула, фотография получена методом конфокальной лазерной микроскопии
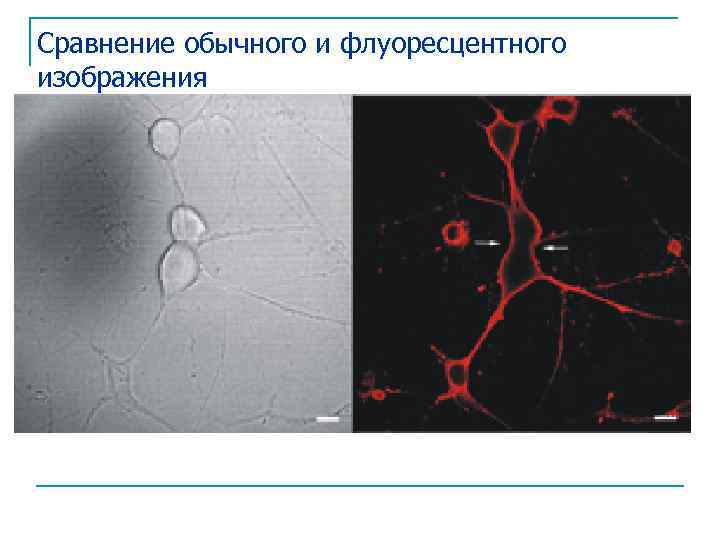 Сравнение обычного и флуоресцентного изображения
Сравнение обычного и флуоресцентного изображения


