Спектр. методы анализа.pptx
- Количество слайдов: 47
 Спектральные методы исследования органических соединений
Спектральные методы исследования органических соединений
 I. Спектральные методы исследования количественного и качественного состава и строения органических веществ основаны на взаимодействии атомов и молекул с электромагнитным излучением. При этом происходит поглощение или испускание (эмиссия). Взаимодействие возможно в широком интервале по принципу квантового поглощения энергии.
I. Спектральные методы исследования количественного и качественного состава и строения органических веществ основаны на взаимодействии атомов и молекул с электромагнитным излучением. При этом происходит поглощение или испускание (эмиссия). Взаимодействие возможно в широком интервале по принципу квантового поглощения энергии.
 Е полн. = Е вращения мол. + Е колеб. ат. + Е элект. перех. По закону Бора:
Е полн. = Е вращения мол. + Е колеб. ат. + Е элект. перех. По закону Бора:
 Характеристики электромагнитного излучения: Волновые – длина волны λ (м, см, нм) частота колебаний (см-1, Гц) Энергетические – энергия перехода Е (э. В, Дж/моль)
Характеристики электромагнитного излучения: Волновые – длина волны λ (м, см, нм) частота колебаний (см-1, Гц) Энергетические – энергия перехода Е (э. В, Дж/моль)
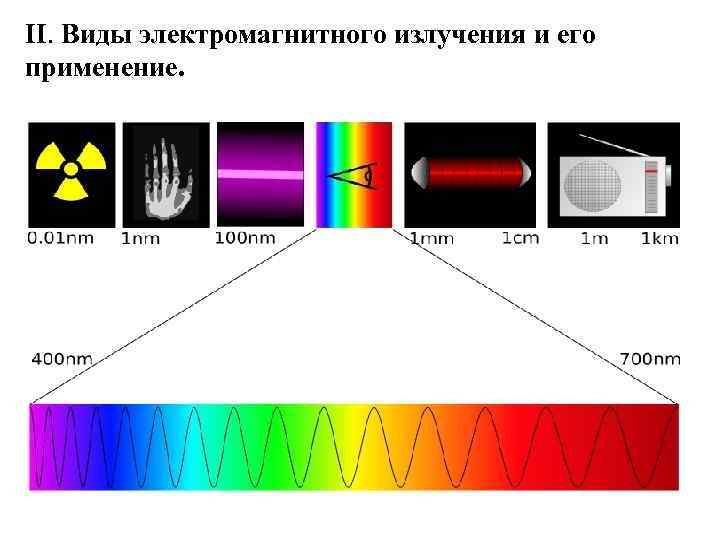 II. Виды электромагнитного излучения и его применение.
II. Виды электромагнитного излучения и его применение.
 Изменение спин электронов и ядер, атомов в крист. решетках ИК(колебательная спектроскопия) Электронные спектры поглощения и испускания (УФ и ФЭС) Рентгено-структурный анализ Ядерные реакции
Изменение спин электронов и ядер, атомов в крист. решетках ИК(колебательная спектроскопия) Электронные спектры поглощения и испускания (УФ и ФЭС) Рентгено-структурный анализ Ядерные реакции
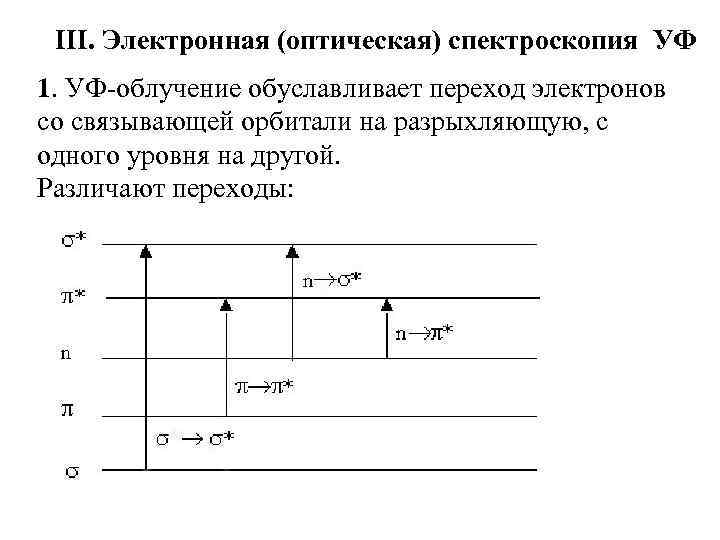 III. Электронная (оптическая) спектроскопия УФ 1. УФ-облучение обуславливает переход электронов со связывающей орбитали на разрыхляющую, с одного уровня на другой. Различают переходы:
III. Электронная (оптическая) спектроскопия УФ 1. УФ-облучение обуславливает переход электронов со связывающей орбитали на разрыхляющую, с одного уровня на другой. Различают переходы:
 2. n, σ, π- электроны и связи имеют разную энергию, и возбуждаются излучениями с разной Е, т. е. с разной λ – длиной волны. Соединения с одинарными, двойными связями, системой сопряжения, с неподеленными парами электронов будут поглощать в разных участках спектра. Область применения 200 -1000 нм
2. n, σ, π- электроны и связи имеют разную энергию, и возбуждаются излучениями с разной Е, т. е. с разной λ – длиной волны. Соединения с одинарными, двойными связями, системой сопряжения, с неподеленными парами электронов будут поглощать в разных участках спектра. Область применения 200 -1000 нм
 3. УФ- спектроскопия – спектроскопия поглощения. Закон Бугера-Ламберта-Бера I- интенсивность падающего излучения Iо - интенсивность прошедшего излечения ε – молярный коэффициент экстинции С – концентрация L – толщина слоя Д – оптическая плотность образца
3. УФ- спектроскопия – спектроскопия поглощения. Закон Бугера-Ламберта-Бера I- интенсивность падающего излучения Iо - интенсивность прошедшего излечения ε – молярный коэффициент экстинции С – концентрация L – толщина слоя Д – оптическая плотность образца
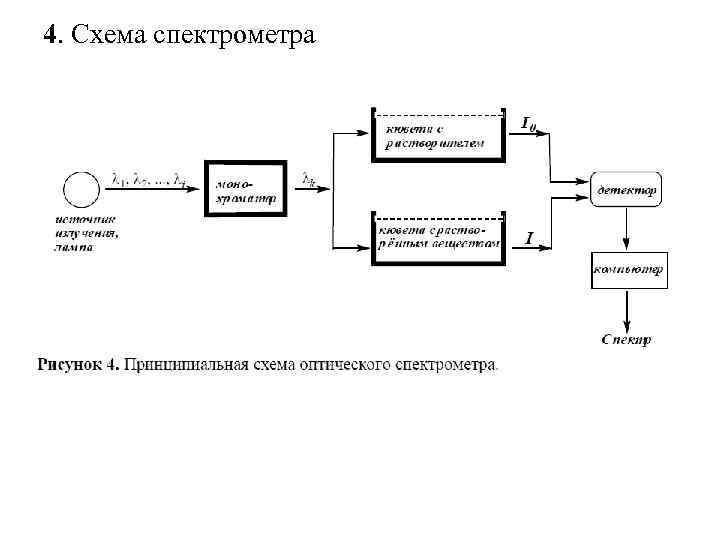 4. Схема спектрометра
4. Схема спектрометра
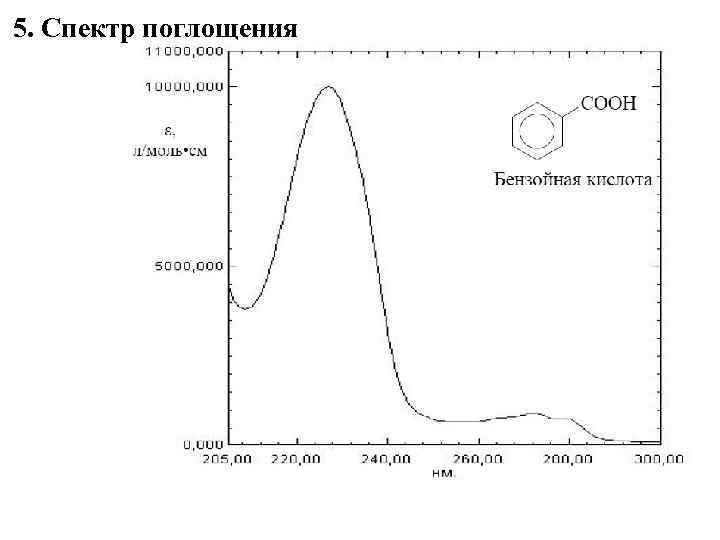 5. Спектр поглощения
5. Спектр поглощения
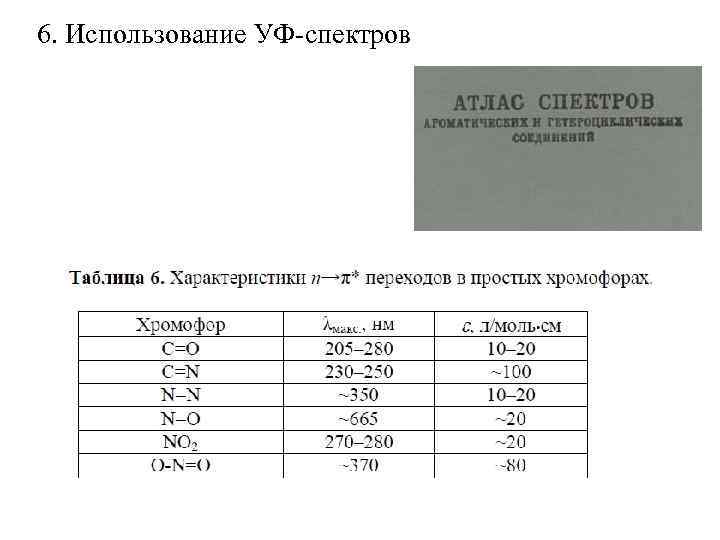 6. Использование УФ-спектров
6. Использование УФ-спектров
 7. Зависимость сдвига от строения соединения 1. С-С связь 120 нм (связь прочная, Е большая, длина малая, σ-σ*) 2. Связь С-Cl σ-σ*+ n- σ* 200 нм (Е уменьшается, длина увеличивается) 3. С=С изолир π-π* 160 нм (Е снижается, длина увеличивается) 4. С=О π-π*+ n- π* 270 нм 5. С=С- сопряженные > 200 нм Чем длиннее сопряжение, тем меньше Е. Хромофор, ауксохром
7. Зависимость сдвига от строения соединения 1. С-С связь 120 нм (связь прочная, Е большая, длина малая, σ-σ*) 2. Связь С-Cl σ-σ*+ n- σ* 200 нм (Е уменьшается, длина увеличивается) 3. С=С изолир π-π* 160 нм (Е снижается, длина увеличивается) 4. С=О π-π*+ n- π* 270 нм 5. С=С- сопряженные > 200 нм Чем длиннее сопряжение, тем меньше Е. Хромофор, ауксохром

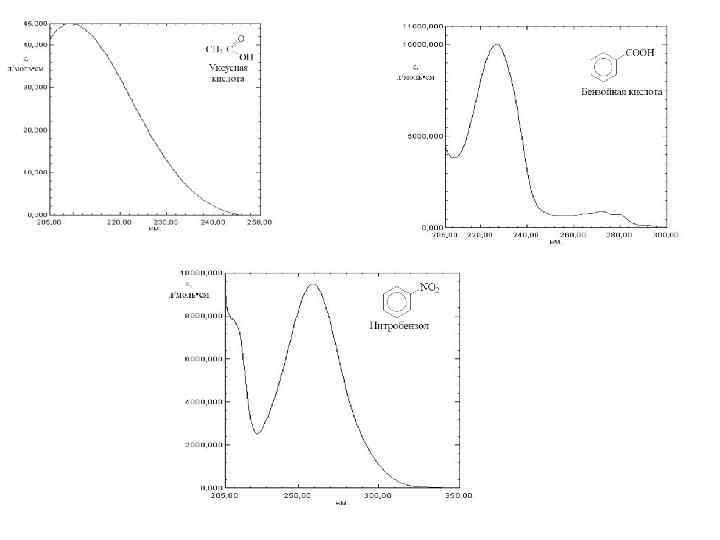
 Электронная спектроскопия (УФ) –строго индивидуальная характеристика соединений. Применение: 1. Метод определения строения 2. Спектры зависят от условий измерений (фазового состояния, растворителя, р. Н, температуры), можно изучать внутримолекулярные взаимодействия, таутомерию, комплексообразования, процессы ионизации. 3. I~C, можно определить степень чистоты, С веществ в растворе, исследовать кинетику реакции.
Электронная спектроскопия (УФ) –строго индивидуальная характеристика соединений. Применение: 1. Метод определения строения 2. Спектры зависят от условий измерений (фазового состояния, растворителя, р. Н, температуры), можно изучать внутримолекулярные взаимодействия, таутомерию, комплексообразования, процессы ионизации. 3. I~C, можно определить степень чистоты, С веществ в растворе, исследовать кинетику реакции.
 IV. Колебательная спектроскопия (ИК – инфракрасная 1. Атомы и группы атомов в молекуле находятся в постоянном движении – колебаниях. Интенсивность и частота колебаний зависят от массы тела и прочности связи, след. характеризуют Е связи. 2. Число колебаний в молекуле из n атомов = (3 n-6), где 3 n –число степеней свободы или положений в пространстве. Основные колебания в молекуле фундаментальные. 3. Колебания валентные (по связи) – ν ↔, деформационные (поперек связи) – δ ↕ Валентные: симм. и несимм. Деформационные: плоские и неплоские, маятниковые, ножничные, крутильные и др.
IV. Колебательная спектроскопия (ИК – инфракрасная 1. Атомы и группы атомов в молекуле находятся в постоянном движении – колебаниях. Интенсивность и частота колебаний зависят от массы тела и прочности связи, след. характеризуют Е связи. 2. Число колебаний в молекуле из n атомов = (3 n-6), где 3 n –число степеней свободы или положений в пространстве. Основные колебания в молекуле фундаментальные. 3. Колебания валентные (по связи) – ν ↔, деформационные (поперек связи) – δ ↕ Валентные: симм. и несимм. Деформационные: плоские и неплоские, маятниковые, ножничные, крутильные и др.
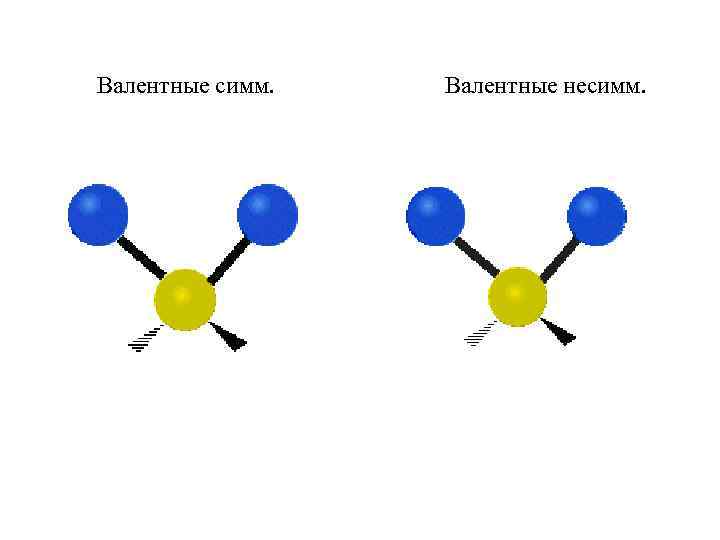 Валентные симм. Валентные несимм.
Валентные симм. Валентные несимм.
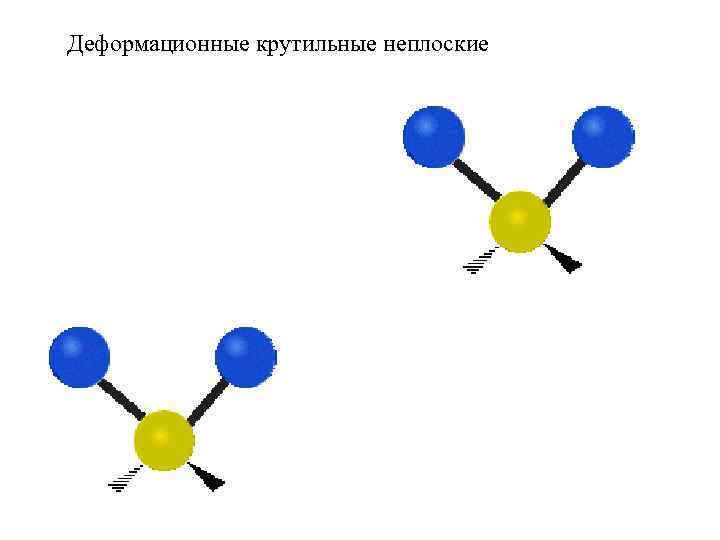 Деформационные крутильные неплоские
Деформационные крутильные неплоские
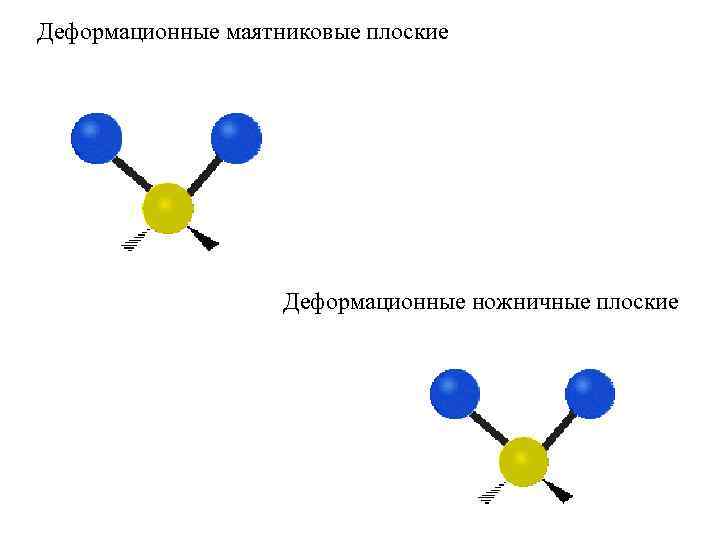 Деформационные маятниковые плоские Деформационные ножничные плоские
Деформационные маятниковые плоские Деформационные ножничные плоские
 4. Переход от одного колебательного уровня до другого квантово -дискретно. Е ~ 0. 5 – 0. 05 э. В, длина волны λ ~ 2. 5 -25 мкм или волновое число ν ~ 4000 -400 см-1 5. Устройство ИК-спектрометров Образец: раствор, пленки выпаривания, таблетки с KBr.
4. Переход от одного колебательного уровня до другого квантово -дискретно. Е ~ 0. 5 – 0. 05 э. В, длина волны λ ~ 2. 5 -25 мкм или волновое число ν ~ 4000 -400 см-1 5. Устройство ИК-спектрометров Образец: раствор, пленки выпаривания, таблетки с KBr.
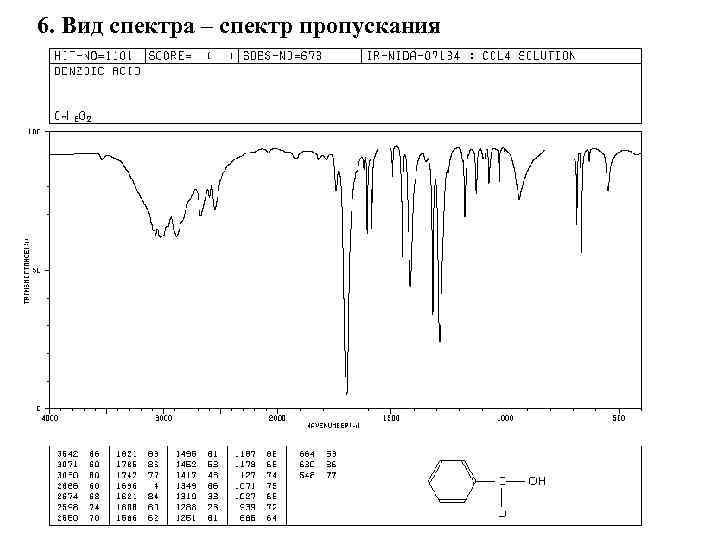 6. Вид спектра – спектр пропускания
6. Вид спектра – спектр пропускания
 7. Положение (частота) максимума поглощения, ее интенсивность I и полуширина зависят от массы связанных атомов, групп, типа и прочности связи, геометрического строения, распределения зарядов и т. Каждая группа атомов и связь имеют свои индивидуальные полосы. ИК спектры информативнее, чем УФ спектры. По многочисленным экспериментальным данным, современным методам расчета составлены таблицы, атласы, стандарты.
7. Положение (частота) максимума поглощения, ее интенсивность I и полуширина зависят от массы связанных атомов, групп, типа и прочности связи, геометрического строения, распределения зарядов и т. Каждая группа атомов и связь имеют свои индивидуальные полосы. ИК спектры информативнее, чем УФ спектры. По многочисленным экспериментальным данным, современным методам расчета составлены таблицы, атласы, стандарты.
 8. Область колебаний групп 2000 -4000 см -1 Валентные колебания связей Х-Н 1350 -1950 см -1 валентные колебания кратных и одинарных связей (С=О, С=С, С=N, NO 2 , C-O, C-N) 600 -1500 см -1 область скелетных колебаний (отпечатки пальцев) валентные и деформационные колебания одинарных связей X-Y, участвующих в построении скелета.
8. Область колебаний групп 2000 -4000 см -1 Валентные колебания связей Х-Н 1350 -1950 см -1 валентные колебания кратных и одинарных связей (С=О, С=С, С=N, NO 2 , C-O, C-N) 600 -1500 см -1 область скелетных колебаний (отпечатки пальцев) валентные и деформационные колебания одинарных связей X-Y, участвующих в построении скелета.
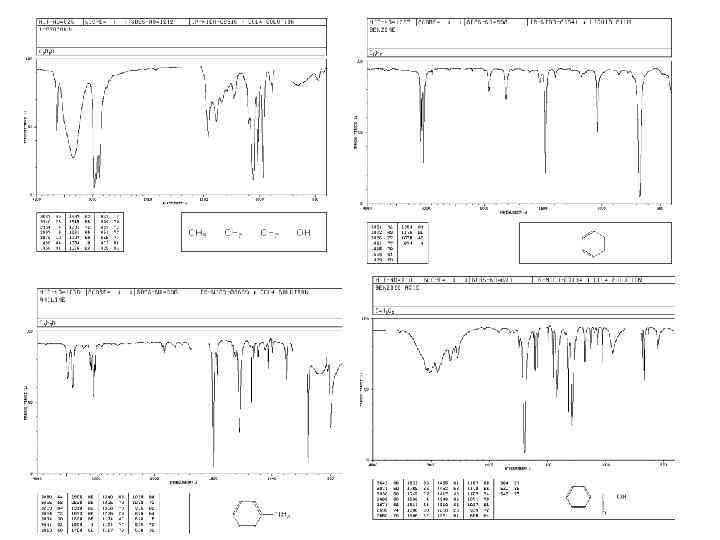

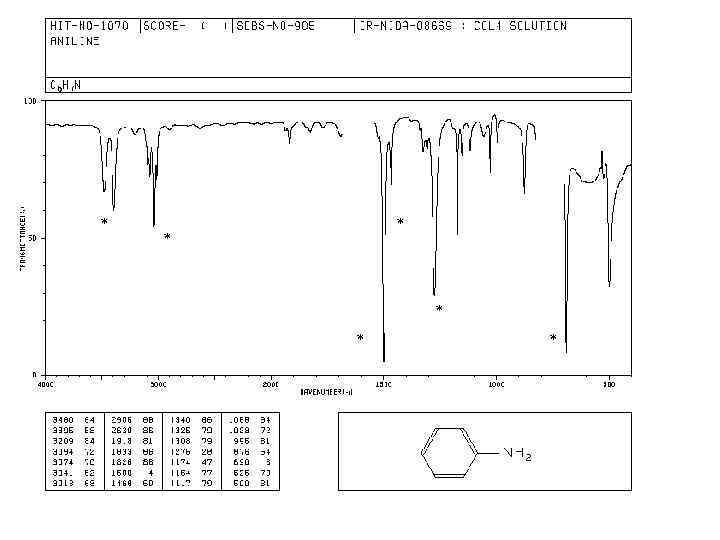 * * *
* * *
 V. Спектроскопия магнитного резонанса ЯМР- 1 Н и 13 С 1. Метод основан на явлении резонансного поглощения Е (радиочастотной электромагнитной) соединением с ненулевым магнитным моментом ядер. Ядра атомов при вращении вокруг собственной связи имеют собственный момент количества вращения (спин). Естественные изотопы, содержащиеся у всех соединений H 1, C 13 , N 15, P 31 и др. = 1/2 При действии переменного радиочастотного электромагнитного поля (генератор) 10 -600 МГц при определенной частоте происходит переориентация спинов ядер, сопровождающееся поглощением энергии. Δ Е характерна для конкретного типа ядер. Атомы одного типа в молекуле различно экранированы есоседних атомов. Чем больше экран, тем сильнее поле сдвига.
V. Спектроскопия магнитного резонанса ЯМР- 1 Н и 13 С 1. Метод основан на явлении резонансного поглощения Е (радиочастотной электромагнитной) соединением с ненулевым магнитным моментом ядер. Ядра атомов при вращении вокруг собственной связи имеют собственный момент количества вращения (спин). Естественные изотопы, содержащиеся у всех соединений H 1, C 13 , N 15, P 31 и др. = 1/2 При действии переменного радиочастотного электромагнитного поля (генератор) 10 -600 МГц при определенной частоте происходит переориентация спинов ядер, сопровождающееся поглощением энергии. Δ Е характерна для конкретного типа ядер. Атомы одного типа в молекуле различно экранированы есоседних атомов. Чем больше экран, тем сильнее поле сдвига.
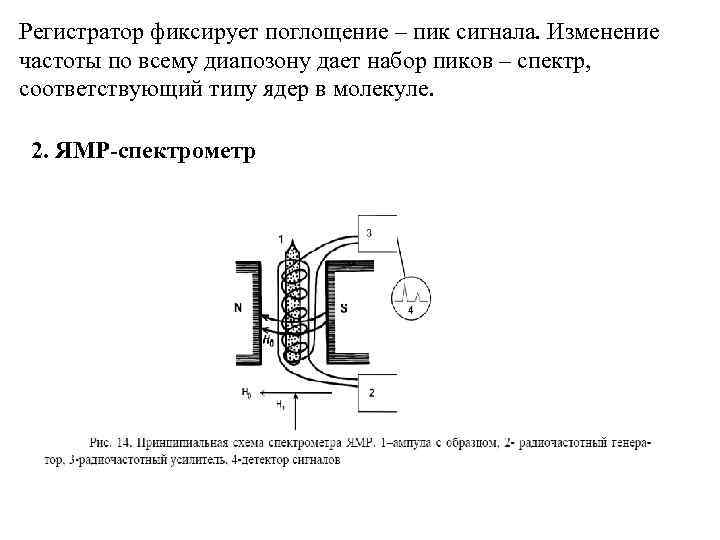 Регистратор фиксирует поглощение – пик сигнала. Изменение частоты по всему диапозону дает набор пиков – спектр, соответствующий типу ядер в молекуле. 2. ЯМР-спектрометр
Регистратор фиксирует поглощение – пик сигнала. Изменение частоты по всему диапозону дает набор пиков – спектр, соответствующий типу ядер в молекуле. 2. ЯМР-спектрометр
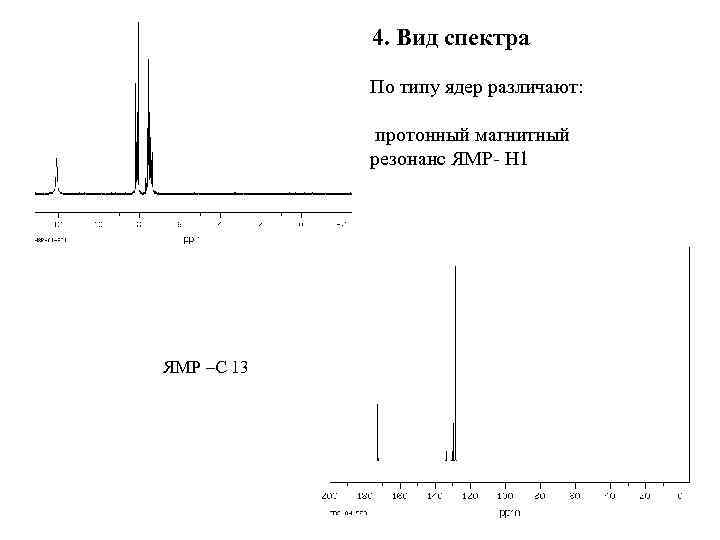 4. Вид спектра По типу ядер различают: протонный магнитный резонанс ЯМР- Н 1 ЯМР –С 13
4. Вид спектра По типу ядер различают: протонный магнитный резонанс ЯМР- Н 1 ЯМР –С 13
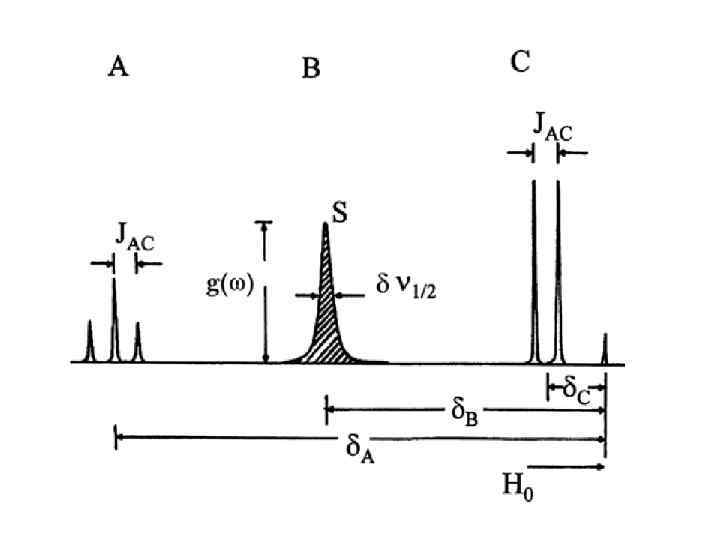
 5. Основные параметры спектра: 1. Химический сдвиг относительно образца 1. γ-γо - м. д. Эталон ТМС γо 2. Интегральная интенсивность сигнала пропорциональна числу химически эквивалентных атомов. 3. Константа спин-спинового взаимодействия (Y, Гц) Сигнал атома расщепляется от соседних одноименных атомов n+1 (Синглет, дуплет, триплет, мультиплет)
5. Основные параметры спектра: 1. Химический сдвиг относительно образца 1. γ-γо - м. д. Эталон ТМС γо 2. Интегральная интенсивность сигнала пропорциональна числу химически эквивалентных атомов. 3. Константа спин-спинового взаимодействия (Y, Гц) Сигнал атома расщепляется от соседних одноименных атомов n+1 (Синглет, дуплет, триплет, мультиплет)
 4. Влияние на величину сдвига 1. Электронное строение гибридизация, функции, сопряжение, конформации, концентрация, растворитель, температура
4. Влияние на величину сдвига 1. Электронное строение гибридизация, функции, сопряжение, конформации, концентрация, растворитель, температура
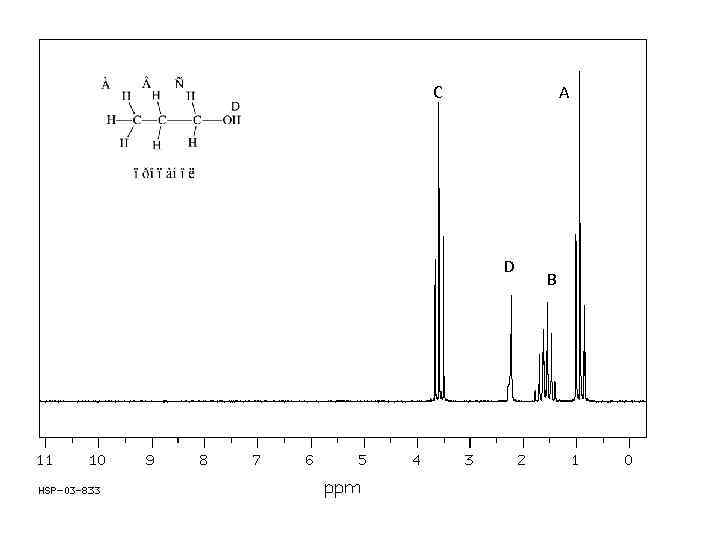 C A D B
C A D B
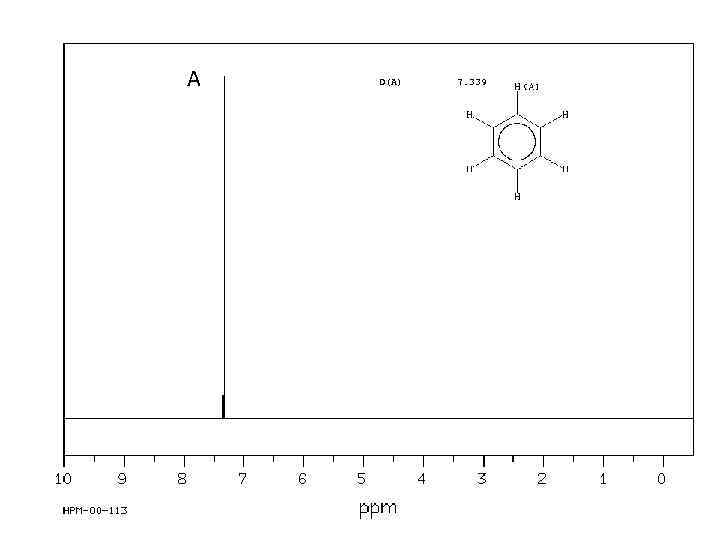 А D(A) 7. 339
А D(A) 7. 339
 Bд C тр D тр A 12. 09 Aс B 8. 12 C 7. 62 D 7. 45
Bд C тр D тр A 12. 09 Aс B 8. 12 C 7. 62 D 7. 45
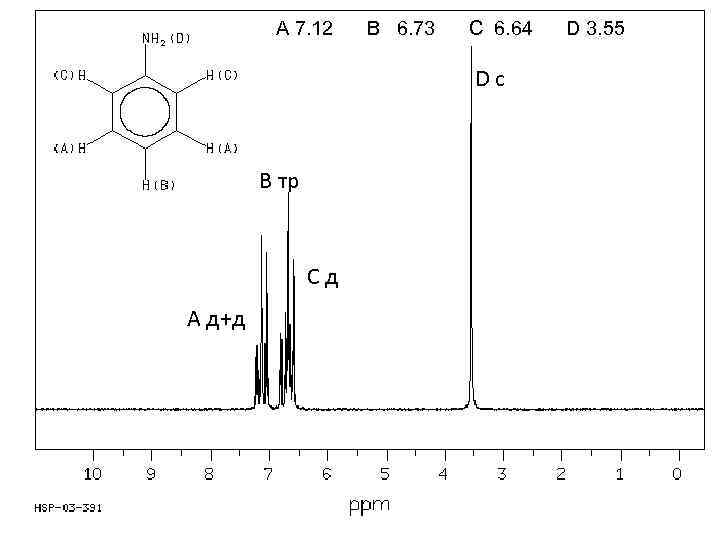 A 7. 12 B 6. 73 C 6. 64 Dс В тр Сд А д+д D 3. 55
A 7. 12 B 6. 73 C 6. 64 Dс В тр Сд А д+д D 3. 55
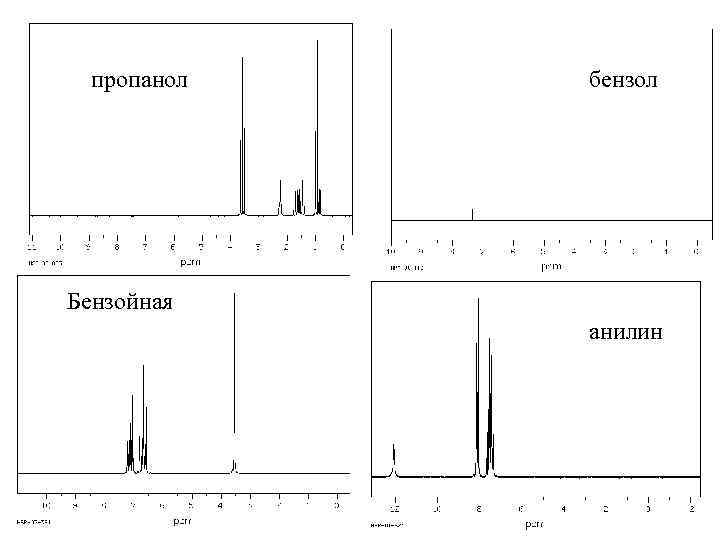 пропанол бензол Бензойная анилин
пропанол бензол Бензойная анилин
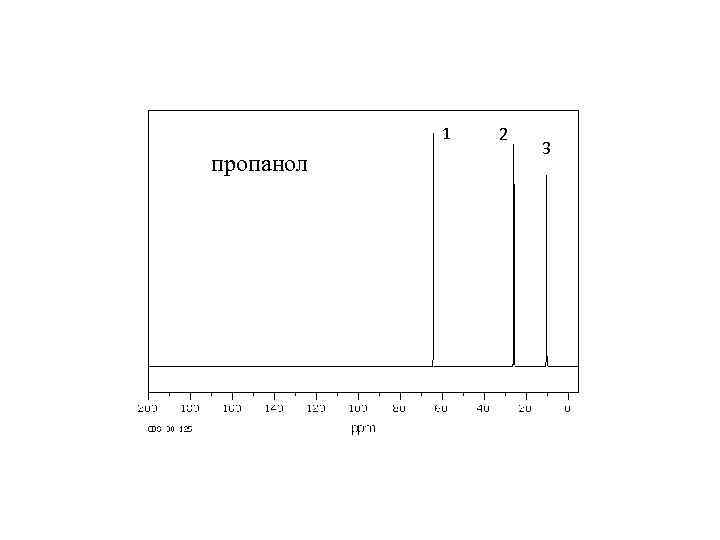 1 пропанол 2 3
1 пропанол 2 3
 1 128. 36 1000 1
1 128. 36 1000 1
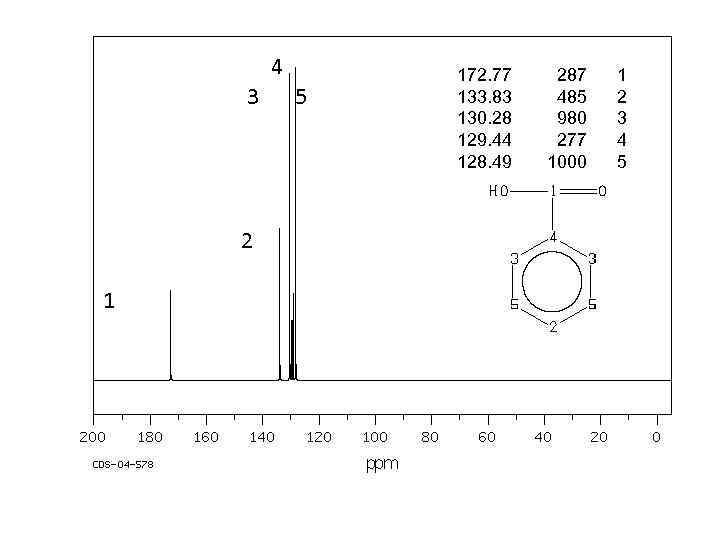 4 3 2 1 5 172. 77 133. 83 130. 28 129. 44 128. 49 287 485 980 277 1000 1 2 3 4 5
4 3 2 1 5 172. 77 133. 83 130. 28 129. 44 128. 49 287 485 980 277 1000 1 2 3 4 5
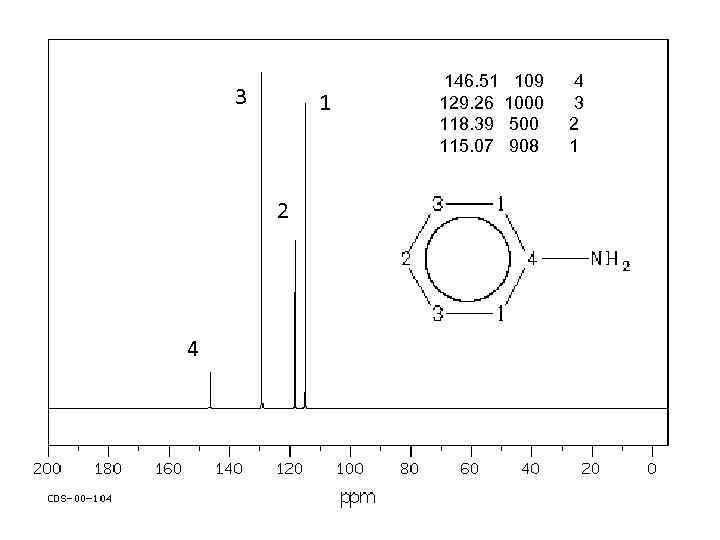 3 1 2 4 146. 51 109 129. 26 1000 118. 39 500 115. 07 908 4 3 2 1
3 1 2 4 146. 51 109 129. 26 1000 118. 39 500 115. 07 908 4 3 2 1
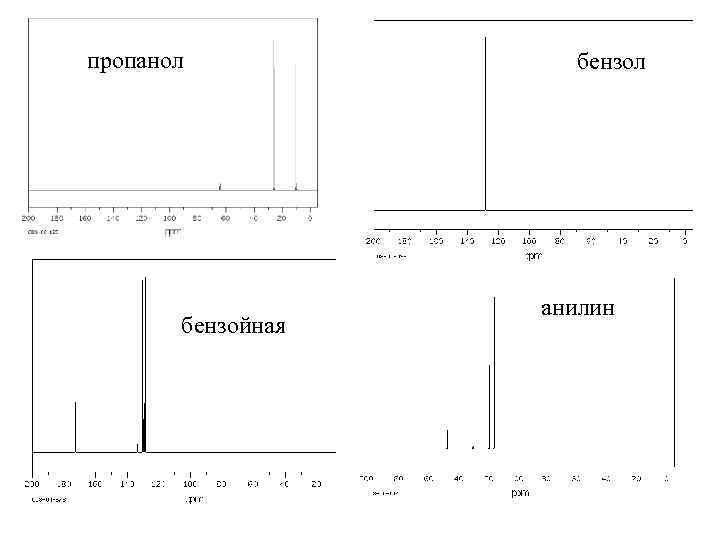 пропанол бензойная бензол анилин
пропанол бензойная бензол анилин
 5. Самый информативный, позволяет установить строение, прочности решать стереохимические задачи, проводить кинетические исследования, количественный и качественный анализ, ЯМР-томография в медицине.
5. Самый информативный, позволяет установить строение, прочности решать стереохимические задачи, проводить кинетические исследования, количественный и качественный анализ, ЯМР-томография в медицине.
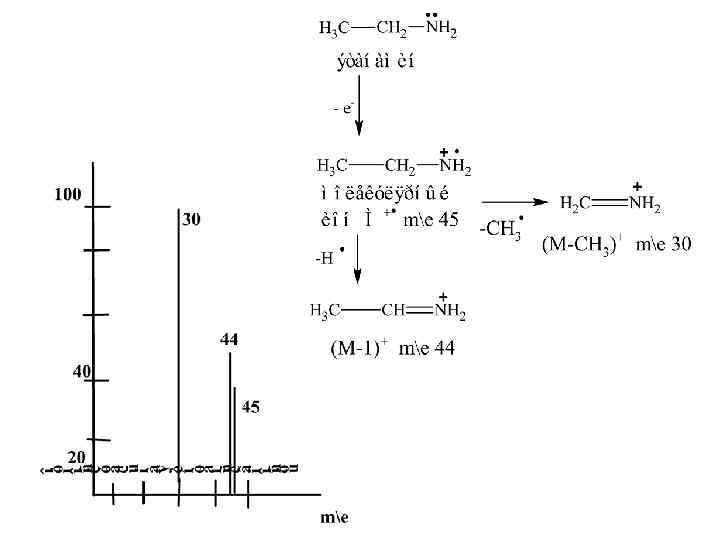
 VI. Масс-спектрометрия Основана на ионизации молекул под действием различных факторов: потока электронов, коротковолнового излучения и др. . Образуется ион-радикал – молекулярный ион М+ Распадается с образованием наиболее устойчивого состояния с разрывом химических связей постадийно. В зависимости от массы и заряда ионы регистрируют. По фрагментам можно составить первоначальную структуру соединения. Используется для установления структуры соединения и его молекулярной массы.
VI. Масс-спектрометрия Основана на ионизации молекул под действием различных факторов: потока электронов, коротковолнового излучения и др. . Образуется ион-радикал – молекулярный ион М+ Распадается с образованием наиболее устойчивого состояния с разрывом химических связей постадийно. В зависимости от массы и заряда ионы регистрируют. По фрагментам можно составить первоначальную структуру соединения. Используется для установления структуры соединения и его молекулярной массы.
 VII. Рентгенография Основана на явлении дифракции рентгеновских лучей, длины волн которых соизмеримы с межатомными расстояниями в исследуемом соединении. Используется для изучения пространственного расположения атомов в кристаллах. При облучении монокристалла рентгеновскими лучами происходит их отражение электронами атомов. Отклонения регистрируются на фотопленке в виде пятен различного почернения. По пятнам строят карту, а по ней рассчитывают межатомные расстояния, валентные углы и т. д.
VII. Рентгенография Основана на явлении дифракции рентгеновских лучей, длины волн которых соизмеримы с межатомными расстояниями в исследуемом соединении. Используется для изучения пространственного расположения атомов в кристаллах. При облучении монокристалла рентгеновскими лучами происходит их отражение электронами атомов. Отклонения регистрируются на фотопленке в виде пятен различного почернения. По пятнам строят карту, а по ней рассчитывают межатомные расстояния, валентные углы и т. д.


