5a8caf86de6f0c2c1a6159b1d45410c0.ppt
- Количество слайдов: 10
 Создание Центра доклинических исследований (Центра) для доступа российских разработчиков лекарственных, диагностических и иммунобиологических (вакцин) препаратов к международным стандартам оценки безопасности инновационных продуктов медицинского назначения. Дубна, 3 декабря 2010 г.
Создание Центра доклинических исследований (Центра) для доступа российских разработчиков лекарственных, диагностических и иммунобиологических (вакцин) препаратов к международным стандартам оценки безопасности инновационных продуктов медицинского назначения. Дубна, 3 декабря 2010 г.
 Цель проекта Создание Центра доклинических исследований (Центра) для доступа российских разработчиков лекарственных, диагностических и иммунобиологических (вакцин) препаратов к международным стандартам оценки безопасности инновационных продуктов медицинского назначения. DUBNA, Moscow Region Albuquerque, New Mexico, USA
Цель проекта Создание Центра доклинических исследований (Центра) для доступа российских разработчиков лекарственных, диагностических и иммунобиологических (вакцин) препаратов к международным стандартам оценки безопасности инновационных продуктов медицинского назначения. DUBNA, Moscow Region Albuquerque, New Mexico, USA
 Задачи Центра 1. Внедрение современных существующих и разработка новых методик определения безопасности фармакологически активных субстанций, медпрепаратов и вакцин в России; 2. Создание в России базы для развития инновационных разработок в области субстанций, медпрепаратов и вакцин с использованием нанотехнологий; 3. Обеспечение качества доклинических исследований на уровне мировых стандартов, активное участие в мониторинге, реализации и разработке отечественных стандартов и процедур сертификации; 4. Формирование единого информационного ресурса по вопросам безопасности наносубстанций, наномедпрепаратов и нановакцин, в т. ч. создание банка стандартных образцов, по которым проведены исследования безопасности. 3
Задачи Центра 1. Внедрение современных существующих и разработка новых методик определения безопасности фармакологически активных субстанций, медпрепаратов и вакцин в России; 2. Создание в России базы для развития инновационных разработок в области субстанций, медпрепаратов и вакцин с использованием нанотехнологий; 3. Обеспечение качества доклинических исследований на уровне мировых стандартов, активное участие в мониторинге, реализации и разработке отечественных стандартов и процедур сертификации; 4. Формирование единого информационного ресурса по вопросам безопасности наносубстанций, наномедпрепаратов и нановакцин, в т. ч. создание банка стандартных образцов, по которым проведены исследования безопасности. 3
 Задачи Центра (2) § В данном центре будут проводится различные виды доклинических исследований ( «ДИ) в соответствии с так называемым GLP-стандартом, обязательным для применения в США и Европе. § Ни одна фармакологическая субстанция (лекарственные, диагностические препараты, вакцины) не может выйти на рынок без доклинических исследований, определяющих уровень токсичности и побочные эффекты для человека и окружающей среды. На сегодняшний день экспорт российских лекарств или разработка лекарств западными компаниями в России невозможна в связи отсутствием центра, проводящего ДИ по GLP-стандарту. На текущий момент в России таких центров нет, и не анонсировано какой-либо компанией планов по их строительству.
Задачи Центра (2) § В данном центре будут проводится различные виды доклинических исследований ( «ДИ) в соответствии с так называемым GLP-стандартом, обязательным для применения в США и Европе. § Ни одна фармакологическая субстанция (лекарственные, диагностические препараты, вакцины) не может выйти на рынок без доклинических исследований, определяющих уровень токсичности и побочные эффекты для человека и окружающей среды. На сегодняшний день экспорт российских лекарств или разработка лекарств западными компаниями в России невозможна в связи отсутствием центра, проводящего ДИ по GLP-стандарту. На текущий момент в России таких центров нет, и не анонсировано какой-либо компанией планов по их строительству.
 Параметры Центра Площадка для размещения Центра: § Расположение: Особая Экономическая Зона, г. Дубна § Основа проекта: аналогичный проект, реализованный в США Лавлесским институтом респираторных исследований; § Качество: центр будет отвечать GLP стандарту, продукция будет одобрена FDA (подразделение Минздрава США, регулирующее пищевую и медицинскую отрасли). § Персонал 139 человек: Управленческий персонал – 11 человек Исследовательский персонал – 81 человек Вспомогательный персонал – 47 человек
Параметры Центра Площадка для размещения Центра: § Расположение: Особая Экономическая Зона, г. Дубна § Основа проекта: аналогичный проект, реализованный в США Лавлесским институтом респираторных исследований; § Качество: центр будет отвечать GLP стандарту, продукция будет одобрена FDA (подразделение Минздрава США, регулирующее пищевую и медицинскую отрасли). § Персонал 139 человек: Управленческий персонал – 11 человек Исследовательский персонал – 81 человек Вспомогательный персонал – 47 человек
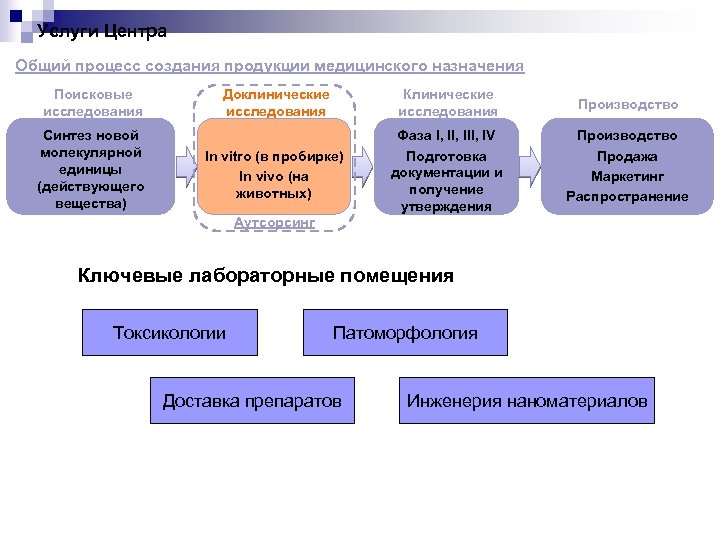 Услуги Центра Общий процесс создания продукции медицинского назначения Поисковые исследования Синтез новой молекулярной единицы (действующего вещества) Доклинические исследования Клинические исследования Производство In vitro (в пробирке) In vivo (на животных) Фаза I, III, IV Подготовка документации и получение утверждения Производство Продажа Маркетинг Распространение Аутсорсинг Ключевые лабораторные помещения Токсикологии Патоморфология Доставка препаратов Инженерия наноматериалов
Услуги Центра Общий процесс создания продукции медицинского назначения Поисковые исследования Синтез новой молекулярной единицы (действующего вещества) Доклинические исследования Клинические исследования Производство In vitro (в пробирке) In vivo (на животных) Фаза I, III, IV Подготовка документации и получение утверждения Производство Продажа Маркетинг Распространение Аутсорсинг Ключевые лабораторные помещения Токсикологии Патоморфология Доставка препаратов Инженерия наноматериалов
 Общая схема проведения исследований
Общая схема проведения исследований
 Мировые стандарты в России Российские стандарты GLP гармонизированы с международными но пока не внедряются Российские стандарты GCP полностью гармонизированы с международными Российские стандарты GMP полностью гармонизированы с международными Clin. Star, Evidence ICON, Parexel, PSI, Quintiles, Bonasana и еще около 80 КИО Существует более 100 компаний, работающих по правилам GMP, основные из них: ОАО «Фармстандарт» , ОАО «Нижфарм» , ОАО «Отечественные лекарства» , НПФ «Материя Медика Холдинг» , ООО «Фарм Центр» , НПО «Микроген» , ОАО «Верофарм» , ОАО «Акрихин» , ООО «Биотек» , ОАО «Мосхимфармпрепараты» проводят по контракту клинические исследования и контролируют выполнение норм GCP в 1000 медицинских учреждениях.
Мировые стандарты в России Российские стандарты GLP гармонизированы с международными но пока не внедряются Российские стандарты GCP полностью гармонизированы с международными Российские стандарты GMP полностью гармонизированы с международными Clin. Star, Evidence ICON, Parexel, PSI, Quintiles, Bonasana и еще около 80 КИО Существует более 100 компаний, работающих по правилам GMP, основные из них: ОАО «Фармстандарт» , ОАО «Нижфарм» , ОАО «Отечественные лекарства» , НПФ «Материя Медика Холдинг» , ООО «Фарм Центр» , НПО «Микроген» , ОАО «Верофарм» , ОАО «Акрихин» , ООО «Биотек» , ОАО «Мосхимфармпрепараты» проводят по контракту клинические исследования и контролируют выполнение норм GCP в 1000 медицинских учреждениях.
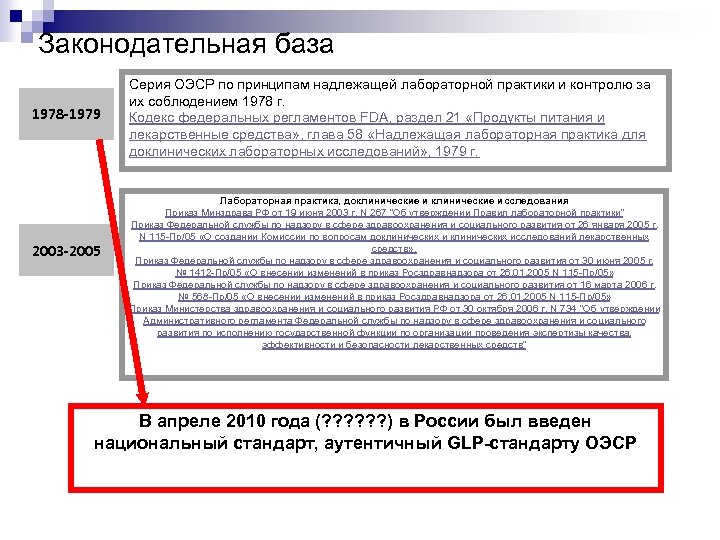 Законодательная база 1978 -1979 2003 -2005 Серия ОЭСР по принципам надлежащей лабораторной практики и контролю за их соблюдением 1978 г. Кодекс федеральных регламентов FDA, раздел 21 «Продукты питания и лекарственные средства» , глава 58 «Надлежащая лабораторная практика для доклинических лабораторных исследований» , 1979 г. Лабораторная практика, доклинические исследования Приказ Минздрава РФ от 19 июня 2003 г. N 267 "Об утверждении Правил лабораторной практики" Приказ Федеральной службы по надзору в сфере здравоохранения и социального развития от 26 января 2005 г. N 115 -Пр/05 «О создании Комиссии по вопросам доклинических исследований лекарственных средств» , Приказ Федеральной службы по надзору в сфере здравоохранения и социального развития от 30 июня 2005 г. № 1412 -Пр/05 «О внесении изменений в приказ Росздравнадзора от 26. 01. 2005 N 115 -Пр/05» Приказ Федеральной службы по надзору в сфере здравоохранения и социального развития от 16 марта 2006 г. № 568 -Пр/05 «О внесении изменений в приказ Росздравнадзора от 26. 01. 2005 N 115 -Пр/05» Приказ Министерства здравоохранения и социального развития РФ от 30 октября 2006 г. N 734 "Об утверждении Административного регламента Федеральной службы по надзору в сфере здравоохранения и социального развития по исполнению государственной функции по организации проведения экспертизы качества, эффективности и безопасности лекарственных средств" В апреле 2010 года (? ? ? ) в России был введен национальный стандарт, аутентичный GLP-стандарту ОЭСР
Законодательная база 1978 -1979 2003 -2005 Серия ОЭСР по принципам надлежащей лабораторной практики и контролю за их соблюдением 1978 г. Кодекс федеральных регламентов FDA, раздел 21 «Продукты питания и лекарственные средства» , глава 58 «Надлежащая лабораторная практика для доклинических лабораторных исследований» , 1979 г. Лабораторная практика, доклинические исследования Приказ Минздрава РФ от 19 июня 2003 г. N 267 "Об утверждении Правил лабораторной практики" Приказ Федеральной службы по надзору в сфере здравоохранения и социального развития от 26 января 2005 г. N 115 -Пр/05 «О создании Комиссии по вопросам доклинических исследований лекарственных средств» , Приказ Федеральной службы по надзору в сфере здравоохранения и социального развития от 30 июня 2005 г. № 1412 -Пр/05 «О внесении изменений в приказ Росздравнадзора от 26. 01. 2005 N 115 -Пр/05» Приказ Федеральной службы по надзору в сфере здравоохранения и социального развития от 16 марта 2006 г. № 568 -Пр/05 «О внесении изменений в приказ Росздравнадзора от 26. 01. 2005 N 115 -Пр/05» Приказ Министерства здравоохранения и социального развития РФ от 30 октября 2006 г. N 734 "Об утверждении Административного регламента Федеральной службы по надзору в сфере здравоохранения и социального развития по исполнению государственной функции по организации проведения экспертизы качества, эффективности и безопасности лекарственных средств" В апреле 2010 года (? ? ? ) в России был введен национальный стандарт, аутентичный GLP-стандарту ОЭСР
 Потенциальные направления развития и рынки Центра Мировой фармацевтический рынок, млрд. долл. Рост: 6, 4% в год Мировой рынок доклинических исследований, млрд. долл. Рост: 4, 4% в год Мировой объем сектора технологий доставки лекарственных препаратов с использованием нанотехнологий: 2010 г. 3. 39 млрд. долл. Источник: IMS Health Российский фармацевтический рынок, млрд. долл. Рост 2010 -2015 П: 12, 7% в год Источник: IMS Health Российский рынок доклинических исследований, млн. долл. Рост 2010 -2015 П: 2012 г. 26 млрд. долл. Проведение нанотоксикологических исследований нанопродукции Национальные и международные институты здравоохранения начинают уделять пристальное внимание воздействию новых продуктов, создаваемых на основе нанотехнологий. Вводимые системы сертификации (в частности «Наносертифика» ) предполагают подтверждение безопасности разработки. Центр будет оснащен оборудованием для исследования нанопродукции. Проведение доклинических исследований лекарственных средств Создание в РФ GLP-центра доклинических исследований, отвечающего мировым стандартам и привлекательному для зарубежных компаний уровнем цен. Поддержка отечественной фармацевтической промышленности, в том числе реализации принятой программы «Фарма-2020» , как для обеспечения внутреннего спроса так и для наращивания экспорта отвечающей мировым стандартам качества фармпродукции.
Потенциальные направления развития и рынки Центра Мировой фармацевтический рынок, млрд. долл. Рост: 6, 4% в год Мировой рынок доклинических исследований, млрд. долл. Рост: 4, 4% в год Мировой объем сектора технологий доставки лекарственных препаратов с использованием нанотехнологий: 2010 г. 3. 39 млрд. долл. Источник: IMS Health Российский фармацевтический рынок, млрд. долл. Рост 2010 -2015 П: 12, 7% в год Источник: IMS Health Российский рынок доклинических исследований, млн. долл. Рост 2010 -2015 П: 2012 г. 26 млрд. долл. Проведение нанотоксикологических исследований нанопродукции Национальные и международные институты здравоохранения начинают уделять пристальное внимание воздействию новых продуктов, создаваемых на основе нанотехнологий. Вводимые системы сертификации (в частности «Наносертифика» ) предполагают подтверждение безопасности разработки. Центр будет оснащен оборудованием для исследования нанопродукции. Проведение доклинических исследований лекарственных средств Создание в РФ GLP-центра доклинических исследований, отвечающего мировым стандартам и привлекательному для зарубежных компаний уровнем цен. Поддержка отечественной фармацевтической промышленности, в том числе реализации принятой программы «Фарма-2020» , как для обеспечения внутреннего спроса так и для наращивания экспорта отвечающей мировым стандартам качества фармпродукции.


