05 емельянов Современные принципы лечения лимфомы Ходжкина и АККЛ_final (1).pptx
- Количество слайдов: 54
 Современные принципы лечения лимфомы Ходжкина и анапластической крупноклеточной лимфомы Емельянов Сергей Анатольевич зав. химиотерапевтическим отделением БУЗ УР «РКОД им. С. Г. Примушко МЗ УР» Confidential and Proprietary Business Information. For Internal Use Only.
Современные принципы лечения лимфомы Ходжкина и анапластической крупноклеточной лимфомы Емельянов Сергей Анатольевич зав. химиотерапевтическим отделением БУЗ УР «РКОД им. С. Г. Примушко МЗ УР» Confidential and Proprietary Business Information. For Internal Use Only.
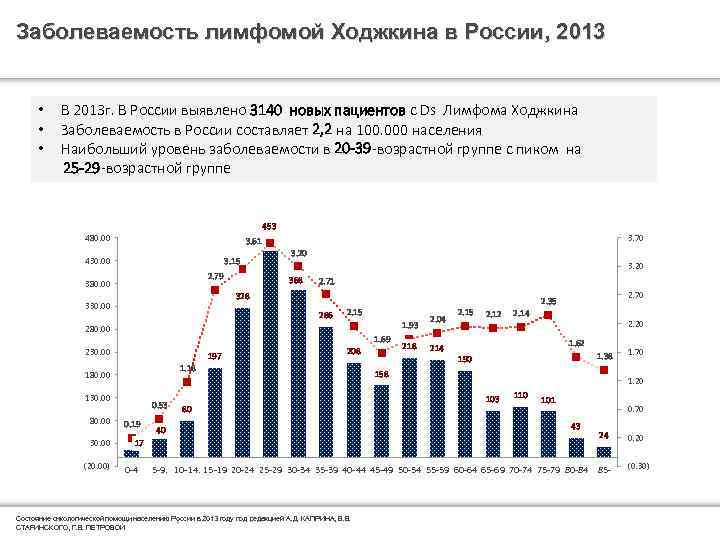 Заболеваемость лимфомой Ходжкина в России, 2013 • • • В 2013 г. В России выявлено 3140 новых пациентов с Ds Лимфома Ходжкина Заболеваемость в России составляет 2, 2 на 100. 000 населения Наибольший уровень заболеваемости в 20 -39 -возрастной группе с пиком на 25 -29 -возрастной группе 453 480. 00 3. 70 3. 61 430. 00 3. 15 2. 79 380. 00 3. 20 368 2. 71 328 330. 00 286 2. 15 1. 93 280. 00 1. 69 230. 00 197 1. 18 180. 00 130. 00 80. 00 30. 00 (20. 00) 0. 53 0. 19 208 218 2. 04 214 2. 15 2. 12 2. 14 2. 20 1. 62 1. 38 190 158 80 40 17 0 -4 2. 70 2. 35 1. 20 103 110 101 0. 70 43 24 5 -9. 10 -14. 15 -19 20 -24 25 -29 30 -34 35 -39 40 -44 45 -49 50 -54 55 -59 60 -64 65 -69 70 -74 75 -79 80 -84 85 - Состояние онкологической помощи населению России в 2013 году под редакцией А. Д. КАПРИНА, В. В. Confidential and Proprietary Business Information. For Internal Use Only. СТАРИНСКОГО, Г. В. ПЕТРОВОЙ 1. 70 0. 20 (0. 30)
Заболеваемость лимфомой Ходжкина в России, 2013 • • • В 2013 г. В России выявлено 3140 новых пациентов с Ds Лимфома Ходжкина Заболеваемость в России составляет 2, 2 на 100. 000 населения Наибольший уровень заболеваемости в 20 -39 -возрастной группе с пиком на 25 -29 -возрастной группе 453 480. 00 3. 70 3. 61 430. 00 3. 15 2. 79 380. 00 3. 20 368 2. 71 328 330. 00 286 2. 15 1. 93 280. 00 1. 69 230. 00 197 1. 18 180. 00 130. 00 80. 00 30. 00 (20. 00) 0. 53 0. 19 208 218 2. 04 214 2. 15 2. 12 2. 14 2. 20 1. 62 1. 38 190 158 80 40 17 0 -4 2. 70 2. 35 1. 20 103 110 101 0. 70 43 24 5 -9. 10 -14. 15 -19 20 -24 25 -29 30 -34 35 -39 40 -44 45 -49 50 -54 55 -59 60 -64 65 -69 70 -74 75 -79 80 -84 85 - Состояние онкологической помощи населению России в 2013 году под редакцией А. Д. КАПРИНА, В. В. Confidential and Proprietary Business Information. For Internal Use Only. СТАРИНСКОГО, Г. В. ПЕТРОВОЙ 1. 70 0. 20 (0. 30)
 Важно помнить • Несмотря на высокий процент достижения излечиваемости после проведения начальной терапии (химиотерапия ± лучевая терапия), 5 -10% пациентов с ЛХ не отвечают на терапию 1 -й линии, 10 -30% рецидивируют после достижения первичной полной ремиссии 1 • Для этой группы пациентов стандартом терапии является проведение ВДХТ с последующей ауто. ТГСК после терапии «спасения» 1 • Однако, некоторые пациенты имеют неблагоприятные прогностические факторы, ухудшающие прогноз достижения оптимальных результатов терапии после проведения ВДХТ/ауто. ТГСК 2 ауто. ГСК – аутологичные гемопоэтические стволовые клетки 1. Ansell SM. Am J Hematol. 2012; 87: 1096– 103. 2. Gobbi PG, et al. Crit Rev Oncol Hematol. 2013; 85: 216– 37. Confidential and Proprietary Business Information. 2 3. Moskowitz C, et al. BMT Tandem Meetings (ASBMT/CIBMTR) 2014. Abstract 148. 4. http: //www. clinicaltrials. gov/ct 2/show/NCT 01100502.
Важно помнить • Несмотря на высокий процент достижения излечиваемости после проведения начальной терапии (химиотерапия ± лучевая терапия), 5 -10% пациентов с ЛХ не отвечают на терапию 1 -й линии, 10 -30% рецидивируют после достижения первичной полной ремиссии 1 • Для этой группы пациентов стандартом терапии является проведение ВДХТ с последующей ауто. ТГСК после терапии «спасения» 1 • Однако, некоторые пациенты имеют неблагоприятные прогностические факторы, ухудшающие прогноз достижения оптимальных результатов терапии после проведения ВДХТ/ауто. ТГСК 2 ауто. ГСК – аутологичные гемопоэтические стволовые клетки 1. Ansell SM. Am J Hematol. 2012; 87: 1096– 103. 2. Gobbi PG, et al. Crit Rev Oncol Hematol. 2013; 85: 216– 37. Confidential and Proprietary Business Information. 2 3. Moskowitz C, et al. BMT Tandem Meetings (ASBMT/CIBMTR) 2014. Abstract 148. 4. http: //www. clinicaltrials. gov/ct 2/show/NCT 01100502.
 Терапия 1 -й линии • Более 80% пациентов младше 60 лет с первичным диагнозом ЛХ могут быть излечены1 • Стандартом 1 -й линии терапии является комбинированная терапия (ХТ с последующей лучевой терапией)2 – Ранние стадии благоприятный прогноз: 2– 3 цикла ABVD с последующей лучевой терапией на пораженные области 30 Гр2 – Ранние стадии промежуточный риск: – 4 цикла ABVD с последующей лучевой терапией на пораженные области 30 Гр2; Пациентам моложе 60 лет возможно проведение более интенсивного лечения: 2 цикла ABVD c последующими 2 циклами BEACOPPescalated и последующей лучевой терапией на пораженные области 30 Гр2 Распространенные стадии • Пациенты младше 50 лет низкой группы риска: 6– 8 циклов ABVD с последующей лучевой терапией на пораженные области 30 Гр2 Пациенты младше 50 лет высокой группы риска и 50 -60 лет, соматически сохранные: 6 циклов BEACOPРescalated с последующей лучевой терапией на пораженные области 30 Гр2, 3 * может потребоваться введение G-КСФ, чтобы купировать последствия возможной токсичности применении BEACOPPescalated 2, 3 • Пациенты старше 60 лет: 6 -8 циклов ABVD с последующей лучевой терапией на пораженные области 30 Гр2, BEACOPPescalated не рекомендуется 2 Российские клинические рекомендации по диагностике и лечению лимфопролиферативных заболеваний. Современная Онкология, 2014 3 Confidential and Proprietary Business Information.
Терапия 1 -й линии • Более 80% пациентов младше 60 лет с первичным диагнозом ЛХ могут быть излечены1 • Стандартом 1 -й линии терапии является комбинированная терапия (ХТ с последующей лучевой терапией)2 – Ранние стадии благоприятный прогноз: 2– 3 цикла ABVD с последующей лучевой терапией на пораженные области 30 Гр2 – Ранние стадии промежуточный риск: – 4 цикла ABVD с последующей лучевой терапией на пораженные области 30 Гр2; Пациентам моложе 60 лет возможно проведение более интенсивного лечения: 2 цикла ABVD c последующими 2 циклами BEACOPPescalated и последующей лучевой терапией на пораженные области 30 Гр2 Распространенные стадии • Пациенты младше 50 лет низкой группы риска: 6– 8 циклов ABVD с последующей лучевой терапией на пораженные области 30 Гр2 Пациенты младше 50 лет высокой группы риска и 50 -60 лет, соматически сохранные: 6 циклов BEACOPРescalated с последующей лучевой терапией на пораженные области 30 Гр2, 3 * может потребоваться введение G-КСФ, чтобы купировать последствия возможной токсичности применении BEACOPPescalated 2, 3 • Пациенты старше 60 лет: 6 -8 циклов ABVD с последующей лучевой терапией на пораженные области 30 Гр2, BEACOPPescalated не рекомендуется 2 Российские клинические рекомендации по диагностике и лечению лимфопролиферативных заболеваний. Современная Онкология, 2014 3 Confidential and Proprietary Business Information.
 Терапия 2 -й линии: терапия «спасения» + ВДХТ/ауто. ТГСК • Стандарт терапии резистентной формы ЛХ и рецидива заболевания высокодозная химиотерапия (ВДХТ) под прикрытием/под защитой ауто. ТГСК 1, 2 • Терапия «спасения» часто назначается до ВДХТ с ауто. ТГСК с целью уменьшения опухолевой массы и мобилизации стволовых клеток 3 а также с целью определения чувствительности опухоли к ХТ. • Выбор режима 2 -линии химиотерапии зависит от формы рецидива и предшествующей терапии 2 - Пациентам группы низкого риска, с рецидивом после 2 циклов ХТ и лучевой терапии может быть рекомендована интенсифицированная ХТ (напр. , BEACOPP escalated)3 Пациентам с локализированными стадиями процесса и поздним рецидивом может быть рекомендовано в качестве терапии «спасения» проведение лучевой терапии 3 • Основным фактором, определяющим отдаленные результаты ВДХТ с ауто. ТГСК, является ответ опухоли на циторедуктивную химиотерапию, т. е. на терапию «спасения» 1. Schmitz N, et al. Lancet 2002; 359(9323): 2065 -2071. 2. National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology Hodgkin Lymphoma. V. 2. 2014. 3. Eichenauer DA, et al. ESMO Guidelines Working Group. Ann Oncol. 2011; 22: vi 55– 8. Confidential and Proprietary Business Information. 4
Терапия 2 -й линии: терапия «спасения» + ВДХТ/ауто. ТГСК • Стандарт терапии резистентной формы ЛХ и рецидива заболевания высокодозная химиотерапия (ВДХТ) под прикрытием/под защитой ауто. ТГСК 1, 2 • Терапия «спасения» часто назначается до ВДХТ с ауто. ТГСК с целью уменьшения опухолевой массы и мобилизации стволовых клеток 3 а также с целью определения чувствительности опухоли к ХТ. • Выбор режима 2 -линии химиотерапии зависит от формы рецидива и предшествующей терапии 2 - Пациентам группы низкого риска, с рецидивом после 2 циклов ХТ и лучевой терапии может быть рекомендована интенсифицированная ХТ (напр. , BEACOPP escalated)3 Пациентам с локализированными стадиями процесса и поздним рецидивом может быть рекомендовано в качестве терапии «спасения» проведение лучевой терапии 3 • Основным фактором, определяющим отдаленные результаты ВДХТ с ауто. ТГСК, является ответ опухоли на циторедуктивную химиотерапию, т. е. на терапию «спасения» 1. Schmitz N, et al. Lancet 2002; 359(9323): 2065 -2071. 2. National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology Hodgkin Lymphoma. V. 2. 2014. 3. Eichenauer DA, et al. ESMO Guidelines Working Group. Ann Oncol. 2011; 22: vi 55– 8. Confidential and Proprietary Business Information. 4
 Терапия 2 -й линии: терапия «спасения» + ВДХТ/ауто. ТГСК Частота Полная ответа, (%) ремиссия, (%) Режим ХТ Литература ICE (ifosfamide, carboplatin, etoposide) 88 26 Moskowitz et al (2001) IVE (ifosfamide, epirubicin, etoposide) 85 37 Proctor et al (2001) MINE (mitoxantrone, ifosfamide, vinorelbine, etoposide) 75 34 Ferme et al (1995) IVOx (ifosfamide, etoposide, oxaliplatin) 76 32 Sibon et al (2011) IGEV (ifosfamide, gemcitabine, vinorelbine) 81 54 Santoro et al (2007) GEM-P (gemcitabine, cisplatin, methylprednisolone) 80 24 Chau et al (2003) GDP (gemcitabine, dexamethasone, cisplatin) 70 52 Baetz et al (2003) GVD (gemcitabine, vinorelbine, liposomal doxorubicin) 70 19 Bartlett et al (2007) Mini-BEAM (carmustine, etoposide, cytarabine, melphalan) 84 32 Colwill et al (1995) Dexa-BEAM (dexamethasone, carmustine, etoposide, cytarabine, melphalan) ESHAP (etoposide, methylprednisolone, cytarabine, cisplatin) 81 27 Schmitz et al (2002) 73 41 Aparicio et al (1999) ASHAP (doxorubicin, methylprednisolone, cytarabine, cisplatin) 70 34 Rodriguez et al (1999) DHAP (dexamethasone, cytarabine, cisplatin) 89 21 Josting et al (2002) DHA-Ox (dexamethasone, cytarabine, oxaliplatin) 74 43 Rigacci et al (2010) Bendamustine (NB. more heavily pre-treated cohort) 53 33 Moskowitz et al (2013) 5 Collins GP, et al. Br J Haematol. 2013; 164; 39– 52. Confidential and Proprietary Business Information.
Терапия 2 -й линии: терапия «спасения» + ВДХТ/ауто. ТГСК Частота Полная ответа, (%) ремиссия, (%) Режим ХТ Литература ICE (ifosfamide, carboplatin, etoposide) 88 26 Moskowitz et al (2001) IVE (ifosfamide, epirubicin, etoposide) 85 37 Proctor et al (2001) MINE (mitoxantrone, ifosfamide, vinorelbine, etoposide) 75 34 Ferme et al (1995) IVOx (ifosfamide, etoposide, oxaliplatin) 76 32 Sibon et al (2011) IGEV (ifosfamide, gemcitabine, vinorelbine) 81 54 Santoro et al (2007) GEM-P (gemcitabine, cisplatin, methylprednisolone) 80 24 Chau et al (2003) GDP (gemcitabine, dexamethasone, cisplatin) 70 52 Baetz et al (2003) GVD (gemcitabine, vinorelbine, liposomal doxorubicin) 70 19 Bartlett et al (2007) Mini-BEAM (carmustine, etoposide, cytarabine, melphalan) 84 32 Colwill et al (1995) Dexa-BEAM (dexamethasone, carmustine, etoposide, cytarabine, melphalan) ESHAP (etoposide, methylprednisolone, cytarabine, cisplatin) 81 27 Schmitz et al (2002) 73 41 Aparicio et al (1999) ASHAP (doxorubicin, methylprednisolone, cytarabine, cisplatin) 70 34 Rodriguez et al (1999) DHAP (dexamethasone, cytarabine, cisplatin) 89 21 Josting et al (2002) DHA-Ox (dexamethasone, cytarabine, oxaliplatin) 74 43 Rigacci et al (2010) Bendamustine (NB. more heavily pre-treated cohort) 53 33 Moskowitz et al (2013) 5 Collins GP, et al. Br J Haematol. 2013; 164; 39– 52. Confidential and Proprietary Business Information.
 Брентуксимаб ведотин – первый таргетный препарат в лечении лимфомы Ходжкина и АККЛ Конъюгат антитела с лекарственным веществом, состоящий из 3 компонентов: антитело, специфичное для антигена CD 30 человека (рекомбинантный химерный Ig. G 1) агент, разрушающий микротрубочки веретена деления - монометил ауристатин Е (MAE) связующий компонент (линкер), расщепляемый протеазами, ковалентно связывающий MMAE и антитело к CD 30 Основное действие препарата – доставка цитотоксического агента к клетке – мишени 6
Брентуксимаб ведотин – первый таргетный препарат в лечении лимфомы Ходжкина и АККЛ Конъюгат антитела с лекарственным веществом, состоящий из 3 компонентов: антитело, специфичное для антигена CD 30 человека (рекомбинантный химерный Ig. G 1) агент, разрушающий микротрубочки веретена деления - монометил ауристатин Е (MAE) связующий компонент (линкер), расщепляемый протеазами, ковалентно связывающий MMAE и антитело к CD 30 Основное действие препарата – доставка цитотоксического агента к клетке – мишени 6
 МОНОМЕТИЛ АУРИСТАТИН Е • Получен в начале 2000 г. г. из оболочки морского моллюска Долабелла Аурикуляриа • Препарат антимитотического действия: ингибирует полимеризацию тубулина, блокирует G 2/M-переход в клеточном цикле и вызывает апоптоз опухолевой клетки • Противоопухолевая эффективность в 200 раз выше эффективности винбластина • Токсичность оказалась столь высока, что явилось препятствием для его клинического применения Francisco JA. , et al, Blood, 2003
МОНОМЕТИЛ АУРИСТАТИН Е • Получен в начале 2000 г. г. из оболочки морского моллюска Долабелла Аурикуляриа • Препарат антимитотического действия: ингибирует полимеризацию тубулина, блокирует G 2/M-переход в клеточном цикле и вызывает апоптоз опухолевой клетки • Противоопухолевая эффективность в 200 раз выше эффективности винбластина • Токсичность оказалась столь высока, что явилось препятствием для его клинического применения Francisco JA. , et al, Blood, 2003
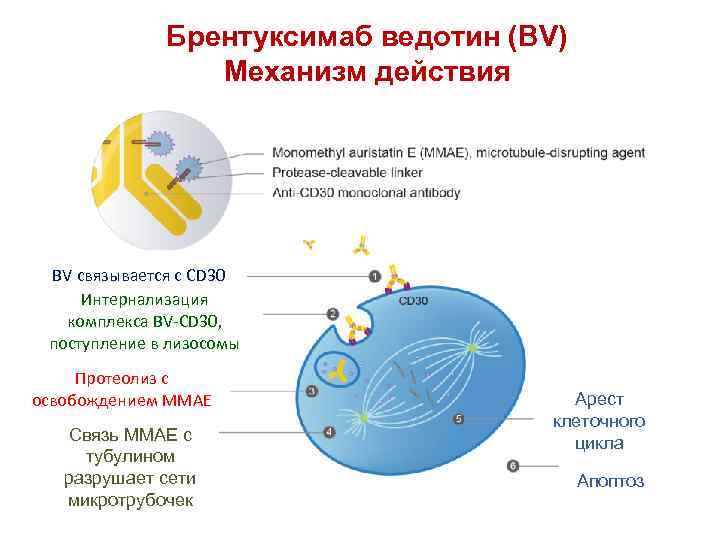 Брентуксимаб ведотин (BV) Механизм действия BV связывается с CD 30 Интернализация комплекса BV-CD 30, поступление в лизосомы Протеолиз с освобождением ММАЕ Связь ММАЕ с тубулином разрушает сети микротрубочек Арест клеточного цикла Апоптоз
Брентуксимаб ведотин (BV) Механизм действия BV связывается с CD 30 Интернализация комплекса BV-CD 30, поступление в лизосомы Протеолиз с освобождением ММАЕ Связь ММАЕ с тубулином разрушает сети микротрубочек Арест клеточного цикла Апоптоз
 ЛИМФОМА ХОДЖКИНА И БРЕНТУКСИМАБ ВЕДОТИН ОБЗОР КЛИНИЧЕСКИХ ДАННЫХ
ЛИМФОМА ХОДЖКИНА И БРЕНТУКСИМАБ ВЕДОТИН ОБЗОР КЛИНИЧЕСКИХ ДАННЫХ
 КЛИНИЧЕСКИЕ ДАННЫЕ II ФАЗЫ - ПАЦИЕНТЫ С РЕЦИДИВИРУЮЩЕЙ/РЕФРАКТЕРНОЙ ЛИМФОМОЙ ХОДЖКИНА, КОТОРЫМ БЫЛА ВЫПОЛНЕНА ТГСК - ПАЦИЕНТЫ С РЕЦИДИВИРУЮЩЕЙ/РЕФРАКТЕРНОЙ ХОДЖКИНА, КОТОРЫМ ТГСК НЕ ВЫПОЛНЯЛАСЬ
КЛИНИЧЕСКИЕ ДАННЫЕ II ФАЗЫ - ПАЦИЕНТЫ С РЕЦИДИВИРУЮЩЕЙ/РЕФРАКТЕРНОЙ ЛИМФОМОЙ ХОДЖКИНА, КОТОРЫМ БЫЛА ВЫПОЛНЕНА ТГСК - ПАЦИЕНТЫ С РЕЦИДИВИРУЮЩЕЙ/РЕФРАКТЕРНОЙ ХОДЖКИНА, КОТОРЫМ ТГСК НЕ ВЫПОЛНЯЛАСЬ
 БРЕНТУКСИМАБ ВЕДОТИН ПАЦИЕНТЫ С РЕЦИДИВИРУЮЩЕЙ/РЕФРАКТЕРНОЙ ЛИМФОМОЙ ХОДЖКИНА, КОТОРЫМ ВЫПОЛНЕНА ТРАНСПЛАНТАЦИЯ СТВОЛОВЫХ КЛЕТОК
БРЕНТУКСИМАБ ВЕДОТИН ПАЦИЕНТЫ С РЕЦИДИВИРУЮЩЕЙ/РЕФРАКТЕРНОЙ ЛИМФОМОЙ ХОДЖКИНА, КОТОРЫМ ВЫПОЛНЕНА ТРАНСПЛАНТАЦИЯ СТВОЛОВЫХ КЛЕТОК
 SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК Критерии включения Терапия (n=102) • Рецидивирующая или рефрактерная CD 30+ ЛХ* • Брентуксимаб ведотин 1, 8 мг/кг в/в каждые 3 недели • Возраст ≥ 12 лет • • Размер опухоли ≥ 1, 5 см Амбулаторное введение в течение 30 минут • Статус по шкале ECOG 0 1 • Максимальное кол-во циклов - 16 • Предшествующая ауто. ТГСК • Наблюдение Рестадирование ** после 2, 4, 7, 10, 13 16 циклов Каждые 12 недель Первичная конечная точка: оценка частоты общего ответа * Гистологическое подтверждение в центральной лаборатории CD 30 - позитивная ЛХ ** Пересмотренные критерии ответа для злокачественной лимфомы (Cheson 2007) Younes A, et al. J Clin Oncol 2012; 30: 2183 -2189.
SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК Критерии включения Терапия (n=102) • Рецидивирующая или рефрактерная CD 30+ ЛХ* • Брентуксимаб ведотин 1, 8 мг/кг в/в каждые 3 недели • Возраст ≥ 12 лет • • Размер опухоли ≥ 1, 5 см Амбулаторное введение в течение 30 минут • Статус по шкале ECOG 0 1 • Максимальное кол-во циклов - 16 • Предшествующая ауто. ТГСК • Наблюдение Рестадирование ** после 2, 4, 7, 10, 13 16 циклов Каждые 12 недель Первичная конечная точка: оценка частоты общего ответа * Гистологическое подтверждение в центральной лаборатории CD 30 - позитивная ЛХ ** Пересмотренные критерии ответа для злокачественной лимфомы (Cheson 2007) Younes A, et al. J Clin Oncol 2012; 30: 2183 -2189.
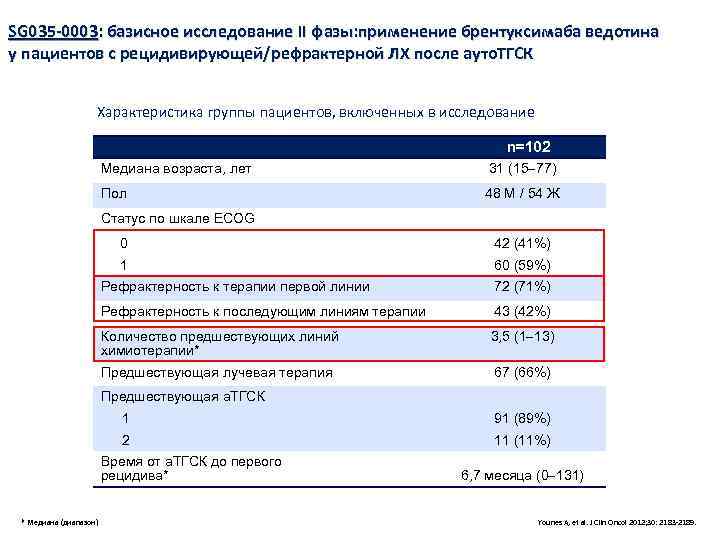 SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК Характеристика группы пациентов, включенных в исследование n=102 Медиана возраста, лет 31 (15 77) Пол 48 M / 54 Ж Статус по шкале ECOG 0 42 (41%) 1 60 (59%) Рефрактерность к терапии первой линии 72 (71%) Рефрактерность к последующим линиям терапии 43 (42%) Количество предшествующих линий химиотерапии* 3, 5 (1 13) Предшествующая лучевая терапия 67 (66%) Предшествующая а. ТГСК 1 91 (89%) 2 11 (11%) Время от а. ТГСК до первого рецидива* * Медиана (диапазон) 6, 7 месяца (0 131) Younes A, et al. J Clin Oncol 2012; 30: 2183 -2189.
SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК Характеристика группы пациентов, включенных в исследование n=102 Медиана возраста, лет 31 (15 77) Пол 48 M / 54 Ж Статус по шкале ECOG 0 42 (41%) 1 60 (59%) Рефрактерность к терапии первой линии 72 (71%) Рефрактерность к последующим линиям терапии 43 (42%) Количество предшествующих линий химиотерапии* 3, 5 (1 13) Предшествующая лучевая терапия 67 (66%) Предшествующая а. ТГСК 1 91 (89%) 2 11 (11%) Время от а. ТГСК до первого рецидива* * Медиана (диапазон) 6, 7 месяца (0 131) Younes A, et al. J Clin Oncol 2012; 30: 2183 -2189.
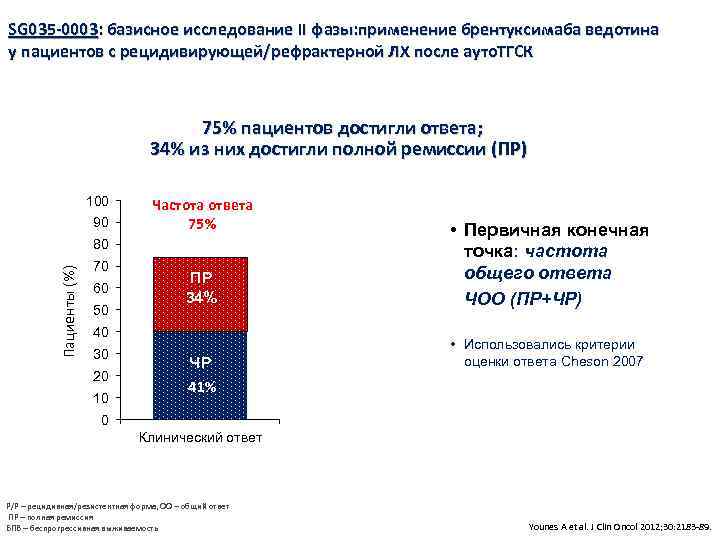 SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК 75% пациентов достигли ответа; 34% из них достигли полной ремиссии (ПР) 100 90 Частота ответа 75% ПР 34% • Первичная конечная точка: частота общего ответа ЧОО (ПР+ЧР) ЧР • Использовались критерии оценки ответа Cheson 2007 Пациенты (%) 80 70 60 50 40 30 20 10 41% 0 Клинический ответ Р/Р – рецидивная/резистентная форма, ОО – общий ответ ПР – полная ремиссия БПВ – беспрогрессивная выживаемость Younes A et al. J Clin Oncol 2012; 30: 2183 -89.
SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК 75% пациентов достигли ответа; 34% из них достигли полной ремиссии (ПР) 100 90 Частота ответа 75% ПР 34% • Первичная конечная точка: частота общего ответа ЧОО (ПР+ЧР) ЧР • Использовались критерии оценки ответа Cheson 2007 Пациенты (%) 80 70 60 50 40 30 20 10 41% 0 Клинический ответ Р/Р – рецидивная/резистентная форма, ОО – общий ответ ПР – полная ремиссия БПВ – беспрогрессивная выживаемость Younes A et al. J Clin Oncol 2012; 30: 2183 -89.
 SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК IRF (N=102) Медиана времени достижения объективного ответа 5, 7 недели (5, 1– 56) Медиана длительности объективного ответа 6, 7 месяца (3, 6– 14, 8) Медиана времени достижения полной ремиссии 12 недель (5, 1– 56) Медиана длительности полной ремиссии 20, 5 месяцев (10, 8, –) Медиана общей выживаемости (ОВ) 40, 5 месяцев (28, 7 –) Расчетная 3 -летняя выживаемость 54% Медиана беспрогрессивной выживаемости - ВБП 5, 6 месяца (44, 64) (5, 0, 9, 0) Медиана количества циклов терапии: 9 (1– 16) Younes A, et al. J Clin Oncol 2012; 30: 2183 -2189. 15
SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК IRF (N=102) Медиана времени достижения объективного ответа 5, 7 недели (5, 1– 56) Медиана длительности объективного ответа 6, 7 месяца (3, 6– 14, 8) Медиана времени достижения полной ремиссии 12 недель (5, 1– 56) Медиана длительности полной ремиссии 20, 5 месяцев (10, 8, –) Медиана общей выживаемости (ОВ) 40, 5 месяцев (28, 7 –) Расчетная 3 -летняя выживаемость 54% Медиана беспрогрессивной выживаемости - ВБП 5, 6 месяца (44, 64) (5, 0, 9, 0) Медиана количества циклов терапии: 9 (1– 16) Younes A, et al. J Clin Oncol 2012; 30: 2183 -2189. 15
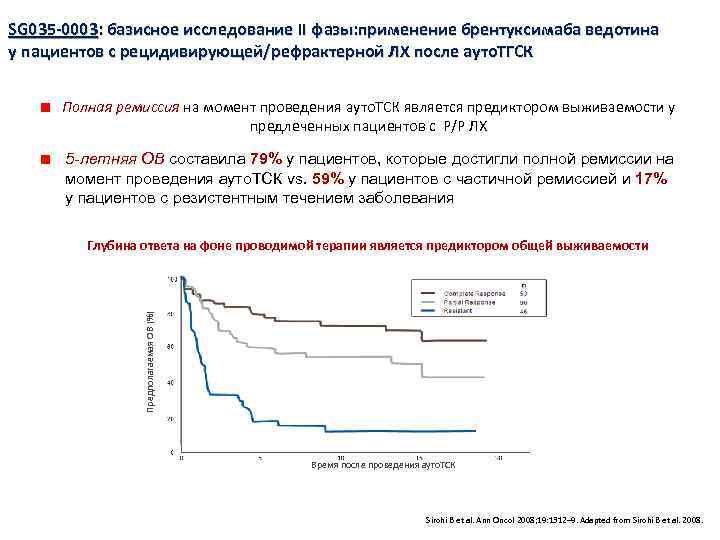 SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК Полная ремиссия на момент проведения ауто. ТСК является предиктором выживаемости у предлеченных пациентов с Р/Р ЛХ 5 -летняя ОВ составила 79% у пациентов, которые достигли полной ремиссии на момент проведения ауто. ТСК vs. 59% у пациентов с частичной ремиссией и 17% у пациентов с резистентным течением заболевания Предполагаемая ОВ (%) Глубина ответа на фоне проводимой терапии является предиктором общей выживаемости Время после проведения ауто. ТСК Sirohi B et al. Ann Oncol 2008; 19: 1312– 9. Adapted from Sirohi B et al. 2008.
SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК Полная ремиссия на момент проведения ауто. ТСК является предиктором выживаемости у предлеченных пациентов с Р/Р ЛХ 5 -летняя ОВ составила 79% у пациентов, которые достигли полной ремиссии на момент проведения ауто. ТСК vs. 59% у пациентов с частичной ремиссией и 17% у пациентов с резистентным течением заболевания Предполагаемая ОВ (%) Глубина ответа на фоне проводимой терапии является предиктором общей выживаемости Время после проведения ауто. ТСК Sirohi B et al. Ann Oncol 2008; 19: 1312– 9. Adapted from Sirohi B et al. 2008.
 SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК Медиана длительности наблюдения с момента приема первой дозы: 26, 5 месяцев (1, 8– 30, 9) n = 102 a Медиана общей выживаемости, месяцы не достигнута (27, 0, –) 2 -х летняя общая выживаемость 65% (55, 74) медиана беспрогрессивной выживаемости 5, 6 месяцев (5, 0, 9, 0) 2 -х летняя беспрогрессивная выживаемость 25% (16, 34) Медиана БПВ у пациентов с ПРb 29, 0 месяцев Медиана БПВ у пациентов с алло. ТГСК после терапии (n=8) 5, 6 месяцев (5, 0, 9, 0) У 12 из 15 длительно наблюдающихся пациентов сохраняется полная ремиссия, у 3 – частичная ремиссия a Популяция, подходящая для лечения; b Пациенты с полной ремиссией n=34 c не цензурировано; d цензурировано алло. ТГСК = аллогенная трансплантация гемопоэтических стволовых клеток ; Smith S, et al. Oral presentation at EHA 2012, Amsterdam, Netherlands (Abstract #1109).
SG 035 -0003: базисное исследование II фазы: применение брентуксимаба ведотина у пациентов с рецидивирующей/рефрактерной ЛХ после ауто. ТГСК Медиана длительности наблюдения с момента приема первой дозы: 26, 5 месяцев (1, 8– 30, 9) n = 102 a Медиана общей выживаемости, месяцы не достигнута (27, 0, –) 2 -х летняя общая выживаемость 65% (55, 74) медиана беспрогрессивной выживаемости 5, 6 месяцев (5, 0, 9, 0) 2 -х летняя беспрогрессивная выживаемость 25% (16, 34) Медиана БПВ у пациентов с ПРb 29, 0 месяцев Медиана БПВ у пациентов с алло. ТГСК после терапии (n=8) 5, 6 месяцев (5, 0, 9, 0) У 12 из 15 длительно наблюдающихся пациентов сохраняется полная ремиссия, у 3 – частичная ремиссия a Популяция, подходящая для лечения; b Пациенты с полной ремиссией n=34 c не цензурировано; d цензурировано алло. ТГСК = аллогенная трансплантация гемопоэтических стволовых клеток ; Smith S, et al. Oral presentation at EHA 2012, Amsterdam, Netherlands (Abstract #1109).
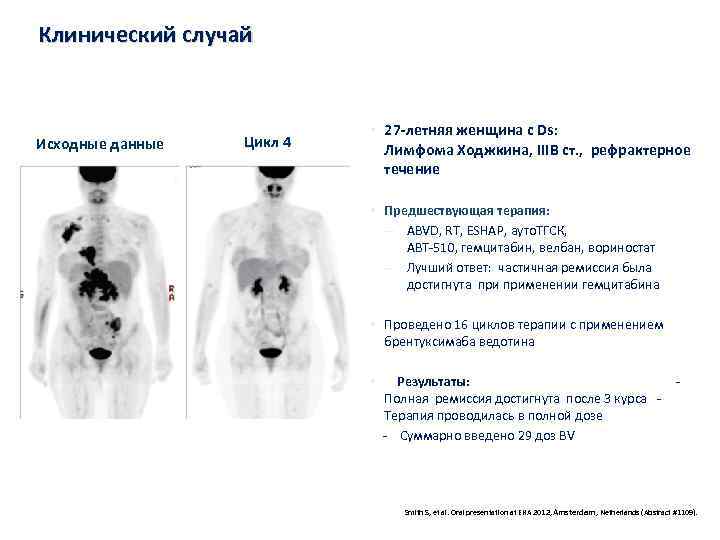 Клинический случай Исходные данные Цикл 4 • 27 -летняя женщина с Ds: Лимфома Ходжкина, IIIB ст. , рефрактерное течение • Предшествующая терапия: ABVD, RT, ESHAP, ауто. ТГСК, ABT-510, гемцитабин, велбан, вориностат Лучший ответ: частичная ремиссия была достигнута применении гемцитабина • Проведено 16 циклов терапии с применением брентуксимаба ведотина Результаты: - Полная ремиссия достигнута после 3 курса - Терапия проводилась в полной дозе - Суммарно введено 29 доз BV • Smith S, et al. Oral presentation at EHA 2012, Amsterdam, Netherlands (Abstract #1109).
Клинический случай Исходные данные Цикл 4 • 27 -летняя женщина с Ds: Лимфома Ходжкина, IIIB ст. , рефрактерное течение • Предшествующая терапия: ABVD, RT, ESHAP, ауто. ТГСК, ABT-510, гемцитабин, велбан, вориностат Лучший ответ: частичная ремиссия была достигнута применении гемцитабина • Проведено 16 циклов терапии с применением брентуксимаба ведотина Результаты: - Полная ремиссия достигнута после 3 курса - Терапия проводилась в полной дозе - Суммарно введено 29 доз BV • Smith S, et al. Oral presentation at EHA 2012, Amsterdam, Netherlands (Abstract #1109).
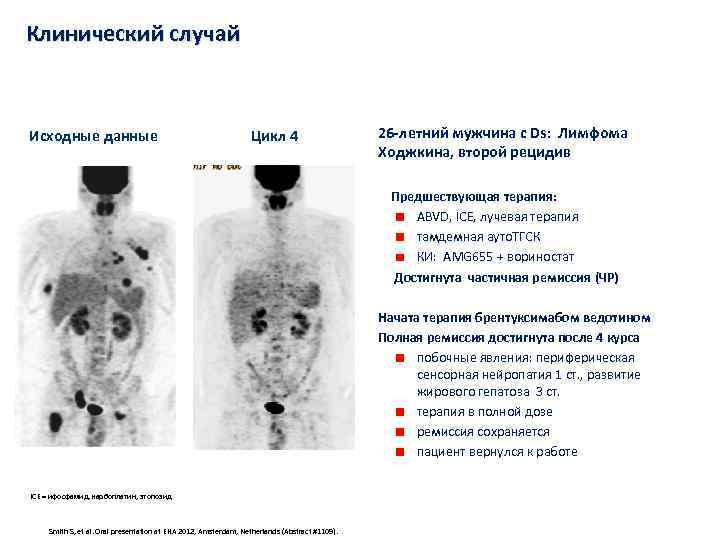 Клинический случай Исходные данные Цикл 4 26 -летний мужчина с Ds: Лимфома Ходжкина, второй рецидив Предшествующая терапия: ABVD, ICE, лучевая терапия тамдемная ауто. ТГСК КИ: AMG 655 + вориностат Достигнута частичная ремиссия (ЧР) Начата терапия брентуксимабом ведотином Полная ремиссия достигнута после 4 курса побочные явления: периферическая сенсорная нейропатия 1 ст. , развитие жирового гепатоза 3 ст. терапия в полной дозе ремиссия сохраняется пациент вернулся к работе ICE = ифосфамид, карбоплатин, этопозид Smith S, et al. Oral presentation at EHA 2012, Amsterdam, Netherlands (Abstract #1109).
Клинический случай Исходные данные Цикл 4 26 -летний мужчина с Ds: Лимфома Ходжкина, второй рецидив Предшествующая терапия: ABVD, ICE, лучевая терапия тамдемная ауто. ТГСК КИ: AMG 655 + вориностат Достигнута частичная ремиссия (ЧР) Начата терапия брентуксимабом ведотином Полная ремиссия достигнута после 4 курса побочные явления: периферическая сенсорная нейропатия 1 ст. , развитие жирового гепатоза 3 ст. терапия в полной дозе ремиссия сохраняется пациент вернулся к работе ICE = ифосфамид, карбоплатин, этопозид Smith S, et al. Oral presentation at EHA 2012, Amsterdam, Netherlands (Abstract #1109).
 БРЕНТУКСИМАБ ВЕДОТИН ПАЦИЕНТЫ С РЕЦИДИВИРУЮЩЕЙ/РЕФРАКТЕРНОЙ ЛИМФОМОЙ ХОДЖКИНА, КОТОРЫМ ТСК НЕ ВЫПОЛНЯЛАСЬ
БРЕНТУКСИМАБ ВЕДОТИН ПАЦИЕНТЫ С РЕЦИДИВИРУЮЩЕЙ/РЕФРАКТЕРНОЙ ЛИМФОМОЙ ХОДЖКИНА, КОТОРЫМ ТСК НЕ ВЫПОЛНЯЛАСЬ
 BV I фаза КИ и программа «расширенного доступа» Эффективность у пациентов с Р/Р ЛХ, которым ауто. ТГСК не выполнялась Количество пациентов n=41 100 • Проанализированы данные пациентов с Р/Р ЛХ, которым ауто. ТСК не могла быть выполнена: пациенты, достигшие ответа, % 90 80 Клинический ответ 70 15 пациентов включены в КИ I фазы 60 26 пациентов были включены в программу «расширенного доступа» 50 40 30 20 10 • Доза: 1. 8 мг/кг брентуксимаба ведотина в/в каждые 3 недели ЧОО 54% ПР 22% 0 • Клинически значимые ответы: частота общего ответа - 54% полная ремиссия - 22% Clinical Response ADCETRIS Sm. PC, October 2012
BV I фаза КИ и программа «расширенного доступа» Эффективность у пациентов с Р/Р ЛХ, которым ауто. ТГСК не выполнялась Количество пациентов n=41 100 • Проанализированы данные пациентов с Р/Р ЛХ, которым ауто. ТСК не могла быть выполнена: пациенты, достигшие ответа, % 90 80 Клинический ответ 70 15 пациентов включены в КИ I фазы 60 26 пациентов были включены в программу «расширенного доступа» 50 40 30 20 10 • Доза: 1. 8 мг/кг брентуксимаба ведотина в/в каждые 3 недели ЧОО 54% ПР 22% 0 • Клинически значимые ответы: частота общего ответа - 54% полная ремиссия - 22% Clinical Response ADCETRIS Sm. PC, October 2012
 BV I фаза КИ и программа «расширенного доступа» Ретроспективный анализ 2 клинических мультицентровых исследований I фазы в которые были включены пациенты, отказавшиеся от ауто. ТСК и пациенты, у которых ТСК не выполнялась - исследование SG 035 -0001 (n =10 patients): дозы препарата 0. 1, 0. 2, 0. 6, 1. 2, 1. 8 и 2. 7 мг/кг BV в/в каждые 3 недели – исследование SG 035 -0002 (n=10 пациентов): дозы препарата 0. 4, 0. 8, 1. 0, 1. 2, и 1. 4 мг/кг BV в/в каждые 3 недели Рестадирование проводилось каждые 2 цикла согласно критериям Cheson 2007 Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
BV I фаза КИ и программа «расширенного доступа» Ретроспективный анализ 2 клинических мультицентровых исследований I фазы в которые были включены пациенты, отказавшиеся от ауто. ТСК и пациенты, у которых ТСК не выполнялась - исследование SG 035 -0001 (n =10 patients): дозы препарата 0. 1, 0. 2, 0. 6, 1. 2, 1. 8 и 2. 7 мг/кг BV в/в каждые 3 недели – исследование SG 035 -0002 (n=10 пациентов): дозы препарата 0. 4, 0. 8, 1. 0, 1. 2, и 1. 4 мг/кг BV в/в каждые 3 недели Рестадирование проводилось каждые 2 цикла согласно критериям Cheson 2007 Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
 BV I фаза КИ и программа «расширенного доступа» Основные данные Медиана возраста Пол Кол-во пациентов (всего 20) 32 13 муж / 7 жен ECOG статус, n (%) 0 10 (50) 1 6 (30) 2 4 (20) Предшествующие линии терапии, медиана 3 (1– 7) Предшествующая лучевая терапия, n (%) 9 (45) Вовлечение в процесс костного мозга, n (%) 4 (20) Наличие В-симптомов, n (%) 7 (35) ECOG, Eastern Cooperative Oncology Group Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
BV I фаза КИ и программа «расширенного доступа» Основные данные Медиана возраста Пол Кол-во пациентов (всего 20) 32 13 муж / 7 жен ECOG статус, n (%) 0 10 (50) 1 6 (30) 2 4 (20) Предшествующие линии терапии, медиана 3 (1– 7) Предшествующая лучевая терапия, n (%) 9 (45) Вовлечение в процесс костного мозга, n (%) 4 (20) Наличие В-симптомов, n (%) 7 (35) ECOG, Eastern Cooperative Oncology Group Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
 BV I фаза КИ и программа «расширенного доступа» Глубина и длительность ответа n (%) Результаты терапии N = 20 (%) Частота ОО 6 (30) ПР 2 (10) ЧР 4 (20) Стабилизация 10 (50) Прогрессия 2 (10) Не определен 2 (10) • Длительность ответа: v Медиана не достигнута v Все пациенты живы Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
BV I фаза КИ и программа «расширенного доступа» Глубина и длительность ответа n (%) Результаты терапии N = 20 (%) Частота ОО 6 (30) ПР 2 (10) ЧР 4 (20) Стабилизация 10 (50) Прогрессия 2 (10) Не определен 2 (10) • Длительность ответа: v Медиана не достигнута v Все пациенты живы Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
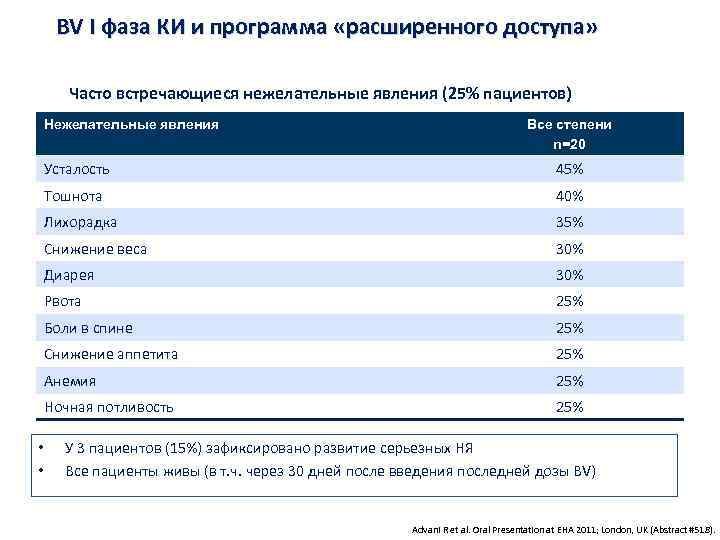 BV I фаза КИ и программа «расширенного доступа» Часто встречающиеся нежелательные явления (25% пациентов) Нежелательные явления Все степени n=20 Усталость 45% Тошнота 40% Лихорадка 35% Снижение веса 30% Диарея 30% Рвота 25% Боли в спине 25% Снижение аппетита 25% Анемия 25% Ночная потливость 25% • • У 3 пациентов (15%) зафиксировано развитие серьезных НЯ Все пациенты живы (в т. ч. через 30 дней после введения последней дозы BV) Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
BV I фаза КИ и программа «расширенного доступа» Часто встречающиеся нежелательные явления (25% пациентов) Нежелательные явления Все степени n=20 Усталость 45% Тошнота 40% Лихорадка 35% Снижение веса 30% Диарея 30% Рвота 25% Боли в спине 25% Снижение аппетита 25% Анемия 25% Ночная потливость 25% • • У 3 пациентов (15%) зафиксировано развитие серьезных НЯ Все пациенты живы (в т. ч. через 30 дней после введения последней дозы BV) Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
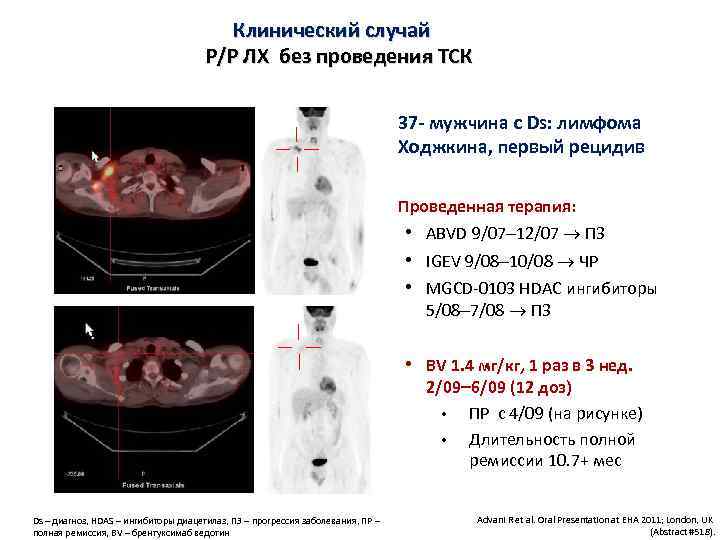 Клинический случай Р/Р ЛХ без проведения ТСК • 37 - мужчина с Ds: лимфома Ходжкина, первый рецидив • Проведенная терапия: • ABVD 9/07 12/07 ПЗ • IGEV 9/08 10/08 ЧР • MGCD-0103 HDAC ингибиторы 5/08 7/08 ПЗ • BV 1. 4 мг/кг, 1 раз в 3 нед. 2/09 6/09 (12 доз) • ПР с 4/09 (на рисунке) • Длительность полной ремиссии 10. 7+ мес Ds – диагноз, HDAS – ингибиторы диацетилаз, ПЗ – прогрессия заболевания, ПР – полная ремиссия, BV – брентуксимаб ведотин Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
Клинический случай Р/Р ЛХ без проведения ТСК • 37 - мужчина с Ds: лимфома Ходжкина, первый рецидив • Проведенная терапия: • ABVD 9/07 12/07 ПЗ • IGEV 9/08 10/08 ЧР • MGCD-0103 HDAC ингибиторы 5/08 7/08 ПЗ • BV 1. 4 мг/кг, 1 раз в 3 нед. 2/09 6/09 (12 доз) • ПР с 4/09 (на рисунке) • Длительность полной ремиссии 10. 7+ мес Ds – диагноз, HDAS – ингибиторы диацетилаз, ПЗ – прогрессия заболевания, ПР – полная ремиссия, BV – брентуксимаб ведотин Advani R et al. Oral Presentation at EHA 2011; London, UK (Abstract #518).
 Клинические результаты программы «расширенного доступа» Ретроспективный анализ: BV у пациентов с Р/Р CD 30+ лимфомами, которым не проводилась высокодозная ХТ или ТСК • конечные точки: ОО, ЧР, ПЗ, OВ, БПВ, безопасность • пациенты: 16 пациентов с ЛХ или с. АККЛ были включены в программу (GHSG) • пациенты не получали высокодозную ХТ или ТСК медиана возраста: 48. 5 лет (24– 74) CD 30+ р/р ЛХ: n=14; рецидив с. АККЛ: n=2 стадии заболевания IIA: n=1; IIB: n=5; IIIA: n=2; IIIB: n=1; IVA: n=2; IVB: n=5 медиана кол-ва проведенных курсов ХТ до начала терапии BV: 3 (range, 2– 6) рефрактерность к проводимой ранее ХТ: n=13 терапия: Брентуксимаб ведотин 1. 8 мг/кг в/в в течение 30 минут каждые 3 недели Р/Р – рецидивная/резистентная форма , ХТ – химиотерапия, BV – брентуксимаб ведотин, ТСК – трансплантация стволовых клеток , ОО – общая выживаемость, ЧР – частичная ремиссия, , ПЗ – прогрессия заболевания, ОВ – общая выживаемость, БПВ – беспрогрессивная выживаемость, GHSG = German Hodgkin Study Group; Rothe A et al. ASH 2012, Atlanta, GA, USA (Abstract 2743)
Клинические результаты программы «расширенного доступа» Ретроспективный анализ: BV у пациентов с Р/Р CD 30+ лимфомами, которым не проводилась высокодозная ХТ или ТСК • конечные точки: ОО, ЧР, ПЗ, OВ, БПВ, безопасность • пациенты: 16 пациентов с ЛХ или с. АККЛ были включены в программу (GHSG) • пациенты не получали высокодозную ХТ или ТСК медиана возраста: 48. 5 лет (24– 74) CD 30+ р/р ЛХ: n=14; рецидив с. АККЛ: n=2 стадии заболевания IIA: n=1; IIB: n=5; IIIA: n=2; IIIB: n=1; IVA: n=2; IVB: n=5 медиана кол-ва проведенных курсов ХТ до начала терапии BV: 3 (range, 2– 6) рефрактерность к проводимой ранее ХТ: n=13 терапия: Брентуксимаб ведотин 1. 8 мг/кг в/в в течение 30 минут каждые 3 недели Р/Р – рецидивная/резистентная форма , ХТ – химиотерапия, BV – брентуксимаб ведотин, ТСК – трансплантация стволовых клеток , ОО – общая выживаемость, ЧР – частичная ремиссия, , ПЗ – прогрессия заболевания, ОВ – общая выживаемость, БПВ – беспрогрессивная выживаемость, GHSG = German Hodgkin Study Group; Rothe A et al. ASH 2012, Atlanta, GA, USA (Abstract 2743)
 Клинические результаты программы «расширенного доступа» • Безопасность: профиль безопасности полностью соответствовал ранее опубликованным данным* Не потребовалось снижение дозы Ни один пациент не прекратил терапию из-за токсичности • Характеристика ответа, n (%) Ответ: Общий ответ Все пациенты (n=16) 11 (69%) Полная ремиссия 5 Частичная ремиссия 6 6 из 11 пациентов имели рефрактерность к терапии; 4 пациента, достигшие ответа имели тяжелую сопутствующую патологию 3 из 5 пациентов с прогрессией заболевания умерли * Полная информация отражена в инструкции по применению Rothe A et al. ASH 2012, Atlanta, GA, USA (Abstract 2743)
Клинические результаты программы «расширенного доступа» • Безопасность: профиль безопасности полностью соответствовал ранее опубликованным данным* Не потребовалось снижение дозы Ни один пациент не прекратил терапию из-за токсичности • Характеристика ответа, n (%) Ответ: Общий ответ Все пациенты (n=16) 11 (69%) Полная ремиссия 5 Частичная ремиссия 6 6 из 11 пациентов имели рефрактерность к терапии; 4 пациента, достигшие ответа имели тяжелую сопутствующую патологию 3 из 5 пациентов с прогрессией заболевания умерли * Полная информация отражена в инструкции по применению Rothe A et al. ASH 2012, Atlanta, GA, USA (Abstract 2743)
 Клинические результаты программы «расширенного доступа» Результаты: БПВ и ОВ • 6 из 16 пациентов проведена трансплантация стволовых клеток после терапии BV аутологичная ТСК: 4 пациента аллогенная ТСК: 2 пациента • Mедиана беспрогрессивной выживаемости: 9 месяцев (диапазон: от 1 до 15 мес) • 11 из 16 пациентов оставались живы на момент анализа; медиана ОВ не была достигнута • 12 -месячная ОВ: 68% • 12 -месячная БПВ: 22% БПВ - беспрогрессивная выживаемость; ОВ – общая выживаемость, ТСК – трансплантация стволовых клеток Rothe A et al. ASH 2012, Atlanta, GA, USA (Abstract 2743)
Клинические результаты программы «расширенного доступа» Результаты: БПВ и ОВ • 6 из 16 пациентов проведена трансплантация стволовых клеток после терапии BV аутологичная ТСК: 4 пациента аллогенная ТСК: 2 пациента • Mедиана беспрогрессивной выживаемости: 9 месяцев (диапазон: от 1 до 15 мес) • 11 из 16 пациентов оставались живы на момент анализа; медиана ОВ не была достигнута • 12 -месячная ОВ: 68% • 12 -месячная БПВ: 22% БПВ - беспрогрессивная выживаемость; ОВ – общая выживаемость, ТСК – трансплантация стволовых клеток Rothe A et al. ASH 2012, Atlanta, GA, USA (Abstract 2743)
 Клинические результаты программы «расширенного доступа» Способ применения и дозы • • 1, 8 мг/кг в/в капельно в течение 30 минут каждые 3 недели Доза может быть уменьшена до 1. 2 мг/кг при развитии или прогрессировании периферической нейропатии Режим введения Среднее кол-во циклов в опубликованных результатах клинических исследований Лимфома Ходжкина с. АККЛ 9 ( от 1 до 16) 7 (от 1 до 16) с. АККЛ – системная анапластическая крупноклеточная лимфома Younes A et al. J Clin Oncol. 2012; 30: 2183– 89; Pro B et al. J Clin Oncol. 2012; 30: 2190 -96; ADCETRISTM U. S. Package Insert, January 2012; ADCETRIS Sm. PC, 2013 30
Клинические результаты программы «расширенного доступа» Способ применения и дозы • • 1, 8 мг/кг в/в капельно в течение 30 минут каждые 3 недели Доза может быть уменьшена до 1. 2 мг/кг при развитии или прогрессировании периферической нейропатии Режим введения Среднее кол-во циклов в опубликованных результатах клинических исследований Лимфома Ходжкина с. АККЛ 9 ( от 1 до 16) 7 (от 1 до 16) с. АККЛ – системная анапластическая крупноклеточная лимфома Younes A et al. J Clin Oncol. 2012; 30: 2183– 89; Pro B et al. J Clin Oncol. 2012; 30: 2190 -96; ADCETRISTM U. S. Package Insert, January 2012; ADCETRIS Sm. PC, 2013 30
 Какое количество курсов необходимо? Период наблюдения: 3 года • Наблюдение: медиана времени от начала терапии: 32. 7 месяца (1. 8– 48. 3) • Пациенты получили в среднем 9 циклов терапии BV (от 1 до 16) Чем больше курсов получили пациенты, тем лучше был достигнутый ответ Характер ответа ПР ЧО СЗ медиана ПЗ среднее значение 5 10 15 Кол-во проведенных циклов BV ПР – полная ремиссия; ЧО – частичный ответ; СЗ – стабильное заболевание; ПЗ – прогрессия заболевания Gopal A, et al. ASH 2013, New Orleans, LA, USA (Abstract 4382)
Какое количество курсов необходимо? Период наблюдения: 3 года • Наблюдение: медиана времени от начала терапии: 32. 7 месяца (1. 8– 48. 3) • Пациенты получили в среднем 9 циклов терапии BV (от 1 до 16) Чем больше курсов получили пациенты, тем лучше был достигнутый ответ Характер ответа ПР ЧО СЗ медиана ПЗ среднее значение 5 10 15 Кол-во проведенных циклов BV ПР – полная ремиссия; ЧО – частичный ответ; СЗ – стабильное заболевание; ПЗ – прогрессия заболевания Gopal A, et al. ASH 2013, New Orleans, LA, USA (Abstract 4382)
 ВЫВОД: обобщенные результаты клинических исследований применения BV у пациентов с рецидивной и резистентной формами ЛХ Пациенты с рецидивом и резистентностью после проведенной АТСК • 75% пациентов достигают объективного ответа (ЧОО) • • 34% пациентов достигли полной ремиссии (ПР) • Предполагаемая 3 -летняя общая выживаемость составляет 54% • Терапия BV связана с более длительной безрецидивной выживаемостью по сравнению с результатами применении ранее применявшейся терапии • Профиль побочных эффектов был прогнозируемым, управляемым; периферическая нейропатия - наиболее распространенный ПЭ купировался при модификации дозы препарата Медиана общей выживаемости составила 40. 5 мес. • Пациенты с рецидивом и резистентностью без АТСК • Значительно выше показатели в группе пациентов, получавших терапию BV: частота достижения общих ответов - 54% и достижения полной ремиссии – 22%
ВЫВОД: обобщенные результаты клинических исследований применения BV у пациентов с рецидивной и резистентной формами ЛХ Пациенты с рецидивом и резистентностью после проведенной АТСК • 75% пациентов достигают объективного ответа (ЧОО) • • 34% пациентов достигли полной ремиссии (ПР) • Предполагаемая 3 -летняя общая выживаемость составляет 54% • Терапия BV связана с более длительной безрецидивной выживаемостью по сравнению с результатами применении ранее применявшейся терапии • Профиль побочных эффектов был прогнозируемым, управляемым; периферическая нейропатия - наиболее распространенный ПЭ купировался при модификации дозы препарата Медиана общей выживаемости составила 40. 5 мес. • Пациенты с рецидивом и резистентностью без АТСК • Значительно выше показатели в группе пациентов, получавших терапию BV: частота достижения общих ответов - 54% и достижения полной ремиссии – 22%
 СИСТЕМНАЯ АНАПЛАСТИЧЕСКАЯ КРУПНОКЛЕТОЧНАЯ ЛИМФОМА И БРЕНТУКСИМАБ ВЕДОТИН ОБЗОР КЛИНИЧЕСКИХ ДАННЫХ
СИСТЕМНАЯ АНАПЛАСТИЧЕСКАЯ КРУПНОКЛЕТОЧНАЯ ЛИМФОМА И БРЕНТУКСИМАБ ВЕДОТИН ОБЗОР КЛИНИЧЕСКИХ ДАННЫХ
 АККЛ: CD 30 -экспрессирующая лимфома • Редкое и агрессивное заболевание • с. АККЛ ALK(+) и ALK(-) клинически и иммунофенотипически отличаются друг от друга • Первичная кожная лимфома имеет лучший прогноз Image courtesy of S Pileri - s. ALCL CD 30 immunostaining Jacobsen E. Oncologist. 2006; 11: 831 -840. Stein H et al. Blood. 2000; 96: 3681 -3695 Savage KJ et al. Blood. 2008; 111: 5496 -5504
АККЛ: CD 30 -экспрессирующая лимфома • Редкое и агрессивное заболевание • с. АККЛ ALK(+) и ALK(-) клинически и иммунофенотипически отличаются друг от друга • Первичная кожная лимфома имеет лучший прогноз Image courtesy of S Pileri - s. ALCL CD 30 immunostaining Jacobsen E. Oncologist. 2006; 11: 831 -840. Stein H et al. Blood. 2000; 96: 3681 -3695 Savage KJ et al. Blood. 2008; 111: 5496 -5504
 ALK(–) пациенты имеют худший прогноз, чем пациенты с ALK(+) в первой линии терапии ALK(+) Общая выживаемость (%) 87 70% ALK(–) 80 5 -OВ 72 49% 60 40 20 p=0. 016 0 0 5 10 Время (годы) 15 This research was originally published in Blood. Savage K, et al. ALK- anaplastic large-cell lymphoma is clinically and immuno- phenotypically different from both ALK(+) ALCL and peripheral T -cell lymphoma, not otherwise specified: report from the International Peipheral T-Cell Lymphoma Project. Blood. 2008; 111: 5496– 504. © the American Society of Hematology. n 100 - ALK(–) пациенты имеют худший прогноз, чем пациенты с ALK(+) в первой линии терапии 1 -4 – Различия наиболее выражены у пациентов старше 40 лет5 – Прогностический индекс для периферической Т-клеточной лимфомы, неспецифицированной периферической Т-клеточной лимфомы - PIT и Международный прогностический индекс - IPI также используются для прогноза при ALK(+) и ALK(–) заболеваниях1 -4, 6, 7 1. Savage K et al. Blood 2008; 111: 5496– 504; 2. Gascoyne R et al. Blood 1999; 93: 3919– 21; 3. ten Berge R et al. Histopathology 2003; 43: 462– 9; 4. Schmitz N et al. Blood 2010; 116: 3418– 25; 5. Oki Y et al. Expert Opin Biol Ther 2012; 12: 623 – 32; 6. Gallamini A et al. Blood 2004; 103: 2474– 9; 7. Foss FM et al. Blood 2011; 117: 6756– 67.
ALK(–) пациенты имеют худший прогноз, чем пациенты с ALK(+) в первой линии терапии ALK(+) Общая выживаемость (%) 87 70% ALK(–) 80 5 -OВ 72 49% 60 40 20 p=0. 016 0 0 5 10 Время (годы) 15 This research was originally published in Blood. Savage K, et al. ALK- anaplastic large-cell lymphoma is clinically and immuno- phenotypically different from both ALK(+) ALCL and peripheral T -cell lymphoma, not otherwise specified: report from the International Peipheral T-Cell Lymphoma Project. Blood. 2008; 111: 5496– 504. © the American Society of Hematology. n 100 - ALK(–) пациенты имеют худший прогноз, чем пациенты с ALK(+) в первой линии терапии 1 -4 – Различия наиболее выражены у пациентов старше 40 лет5 – Прогностический индекс для периферической Т-клеточной лимфомы, неспецифицированной периферической Т-клеточной лимфомы - PIT и Международный прогностический индекс - IPI также используются для прогноза при ALK(+) и ALK(–) заболеваниях1 -4, 6, 7 1. Savage K et al. Blood 2008; 111: 5496– 504; 2. Gascoyne R et al. Blood 1999; 93: 3919– 21; 3. ten Berge R et al. Histopathology 2003; 43: 462– 9; 4. Schmitz N et al. Blood 2010; 116: 3418– 25; 5. Oki Y et al. Expert Opin Biol Ther 2012; 12: 623 – 32; 6. Gallamini A et al. Blood 2004; 103: 2474– 9; 7. Foss FM et al. Blood 2011; 117: 6756– 67.
 Плохой прогноз у рецидивирующих пациентов с. АККЛ Общая выживаемость при неудаче первичной терапии v Агрессивность с. АККЛ делают трудным достижение высоких результатов терапии 1. 0 0. 9 v Улучшение ОВ, длительные стойкие ответы на терапии должны быть достижимы, и некоторые терапевтические опции уже доступны для решения этих задач 0. 8 0. 7 Выживаемость v У 40 65% пациентов развиваются рецидивы после инициальной терапии Meдиана = 3. 3 мес. n = 61 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0 0 1 2 3 4 5 6 7 8 9 10 Время (годы) Savage KJ et al. Blood. 2008; 111(12): 5496 -504
Плохой прогноз у рецидивирующих пациентов с. АККЛ Общая выживаемость при неудаче первичной терапии v Агрессивность с. АККЛ делают трудным достижение высоких результатов терапии 1. 0 0. 9 v Улучшение ОВ, длительные стойкие ответы на терапии должны быть достижимы, и некоторые терапевтические опции уже доступны для решения этих задач 0. 8 0. 7 Выживаемость v У 40 65% пациентов развиваются рецидивы после инициальной терапии Meдиана = 3. 3 мес. n = 61 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0 0 1 2 3 4 5 6 7 8 9 10 Время (годы) Savage KJ et al. Blood. 2008; 111(12): 5496 -504
 РЕКОМЕНДАЦИИ И СОВРЕМЕННЫЕ ТЕРАПЕВТИЧЕСКИЕ ОПЦИИ
РЕКОМЕНДАЦИИ И СОВРЕМЕННЫЕ ТЕРАПЕВТИЧЕСКИЕ ОПЦИИ
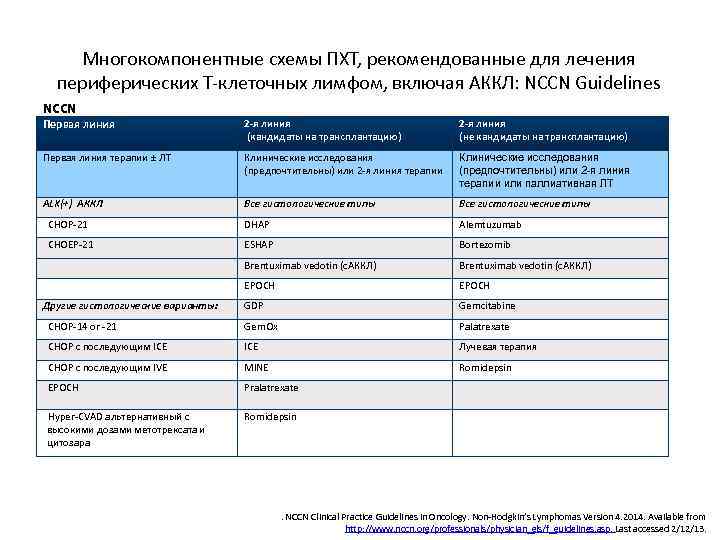 Многокомпонентные схемы ПХТ, рекомендованные для лечения периферических Т-клеточных лимфом, включая АККЛ: NCCN Guidelines NCCN Первая линия 2 -я линия (кандидаты на трансплантацию) 2 -я линия (не кандидаты на трансплантацию) Первая линия терапии ± ЛT Клинические исследования (предпочтительны) или 2 -я линия терапии или паллиативная ЛТ ALK(+) АККЛ Все гистологические типы CHOP-21 DHAP Alemtuzumab CHOEP-21 ESHAP Bortezomib Brentuximab vedotin (с. AККЛ) EPOCH GDP Gemcitabine CHOP-14 or -21 Gem. Ox Palatrexate CHOP с последующим ICE Лучевая терапия CHOP с последующим IVE MINE Romidepsin EPOCH Pralatrexate Hyper-CVAD альтернативный с высокими дозами метотрексата и цитозара Romidepsin Другие гистологические варианты: . NCCN Clinical Practice Guidelines in Oncology. Non-Hodgkin’s Lymphomas Version 4. 2014. Available from http: //www. nccn. org/professionals/physician_gls/f_guidelines. asp. Last accessed 2/12/13.
Многокомпонентные схемы ПХТ, рекомендованные для лечения периферических Т-клеточных лимфом, включая АККЛ: NCCN Guidelines NCCN Первая линия 2 -я линия (кандидаты на трансплантацию) 2 -я линия (не кандидаты на трансплантацию) Первая линия терапии ± ЛT Клинические исследования (предпочтительны) или 2 -я линия терапии или паллиативная ЛТ ALK(+) АККЛ Все гистологические типы CHOP-21 DHAP Alemtuzumab CHOEP-21 ESHAP Bortezomib Brentuximab vedotin (с. AККЛ) EPOCH GDP Gemcitabine CHOP-14 or -21 Gem. Ox Palatrexate CHOP с последующим ICE Лучевая терапия CHOP с последующим IVE MINE Romidepsin EPOCH Pralatrexate Hyper-CVAD альтернативный с высокими дозами метотрексата и цитозара Romidepsin Другие гистологические варианты: . NCCN Clinical Practice Guidelines in Oncology. Non-Hodgkin’s Lymphomas Version 4. 2014. Available from http: //www. nccn. org/professionals/physician_gls/f_guidelines. asp. Last accessed 2/12/13.
 Проблемы в достижении полной ремиссии особенно актуальны при рецидивах НХЛ и пациентов с резистентностью • Достижение ПР является проблемой при рецидивах и резистентности с. АККЛ – Агрессивное заболевание 1, 2 – Отсутствие эффективных препаратов 3– 11 • • На ХТ лечении частота ПР составляет 0– 22% при рецидивах и резистентности периферической Т-клеточной лимфомы1 >50% пациентов с АККЛ, получивших АТСК рецидивируют в течение 10 лет12 Лечение Частота ПР (%) 1 -я линия 44 (CHOP)13 2 -я линия 16– 37 (терапия спасения до АТСК)14– 18 66 (терапия спасения + ATСК)12 3 -я линия 0– 22 (ХТ)3– 11 1. Zinzani P et al. J Clin Oncol 1996; 14: 955– 62; 2. Stein H et al. Blood 2000; 96: 3681– 95; 3. Dueck G et al. Cancer 2010; 116: 4541– 8; 4. Ansell S et al. J Clin Oncol 2007; 25: 2764– 9; 5. Pohlman B et al. Presentation at the 51 st ASH Annual Meeting. Abstract 920 (oral session); 6. d’Amore F et al. Br J Haematol 2010; 150: 565– 73; 7. Kong LR et al. Leuk Lymphoma 1997; 26: 89– 97; 8. Tsimberidou AM et al. Cancer 2004; 100: 342– 9; 9. Piekarz R et al. Blood 2011; 117: 5827– 34; 10. Dang NH et al. Br J Haematol 2007; 136: 439– 47; 11. O’Connor OA et al. J Clin Oncol 2011; 29: 1182– 9; 12. Fanin R et al. Bone Marrow Transplant 1999; 23: 437– 42; 13. Fisher RI et al. N Engl J Med 1993; 328: 1002– 6; 14. Velasquez W et al. Blood 1988; 71: 117– 22; 15. Velasquez W et al. J Clin Oncol 1994; 12: 1169– 76; 16. Crump M et al. Cancer 2004; 101: 1835– 42; 17. Lopez A et al. Eur J Haematol 2008; 80: 127– 32; 18. Zelenetz A et al. Ann Oncol 2003; 14: i 5–i 10.
Проблемы в достижении полной ремиссии особенно актуальны при рецидивах НХЛ и пациентов с резистентностью • Достижение ПР является проблемой при рецидивах и резистентности с. АККЛ – Агрессивное заболевание 1, 2 – Отсутствие эффективных препаратов 3– 11 • • На ХТ лечении частота ПР составляет 0– 22% при рецидивах и резистентности периферической Т-клеточной лимфомы1 >50% пациентов с АККЛ, получивших АТСК рецидивируют в течение 10 лет12 Лечение Частота ПР (%) 1 -я линия 44 (CHOP)13 2 -я линия 16– 37 (терапия спасения до АТСК)14– 18 66 (терапия спасения + ATСК)12 3 -я линия 0– 22 (ХТ)3– 11 1. Zinzani P et al. J Clin Oncol 1996; 14: 955– 62; 2. Stein H et al. Blood 2000; 96: 3681– 95; 3. Dueck G et al. Cancer 2010; 116: 4541– 8; 4. Ansell S et al. J Clin Oncol 2007; 25: 2764– 9; 5. Pohlman B et al. Presentation at the 51 st ASH Annual Meeting. Abstract 920 (oral session); 6. d’Amore F et al. Br J Haematol 2010; 150: 565– 73; 7. Kong LR et al. Leuk Lymphoma 1997; 26: 89– 97; 8. Tsimberidou AM et al. Cancer 2004; 100: 342– 9; 9. Piekarz R et al. Blood 2011; 117: 5827– 34; 10. Dang NH et al. Br J Haematol 2007; 136: 439– 47; 11. O’Connor OA et al. J Clin Oncol 2011; 29: 1182– 9; 12. Fanin R et al. Bone Marrow Transplant 1999; 23: 437– 42; 13. Fisher RI et al. N Engl J Med 1993; 328: 1002– 6; 14. Velasquez W et al. Blood 1988; 71: 117– 22; 15. Velasquez W et al. J Clin Oncol 1994; 12: 1169– 76; 16. Crump M et al. Cancer 2004; 101: 1835– 42; 17. Lopez A et al. Eur J Haematol 2008; 80: 127– 32; 18. Zelenetz A et al. Ann Oncol 2003; 14: i 5–i 10.
 Рекомендации и проблемы в лечении: выводы • Рекомендации по лечению с. АККЛ содержатся в рекомендациях для лечения периферической Т-клеточной лимфомы • Нет стандартных рекомендаций по лечению во 2 -й линии при АККЛ • Рецидивы и резистентность при АККЛ остаются важными нерешенными медицинскими проблемами: – Агрессивное заболевание – Ограничены терапевтические опции, плохие результаты терапии • На существующей терапии низкая частота достижения ПР. Лечение ассоциировано с высокой токсичностью, включая поздние осложнения ХТ и ЛТ • Выживаемость при АККЛ остается без изменений в течение последних 10 лет • Четкое понимание высокой эффективности, хорошей переносимости новых препаратов для 2 -й линии терапии и после АТСК • На таргетной терапии улучшаются показатели эффективности, снижается токсичность терапии по сравнению с существующей ХТ
Рекомендации и проблемы в лечении: выводы • Рекомендации по лечению с. АККЛ содержатся в рекомендациях для лечения периферической Т-клеточной лимфомы • Нет стандартных рекомендаций по лечению во 2 -й линии при АККЛ • Рецидивы и резистентность при АККЛ остаются важными нерешенными медицинскими проблемами: – Агрессивное заболевание – Ограничены терапевтические опции, плохие результаты терапии • На существующей терапии низкая частота достижения ПР. Лечение ассоциировано с высокой токсичностью, включая поздние осложнения ХТ и ЛТ • Выживаемость при АККЛ остается без изменений в течение последних 10 лет • Четкое понимание высокой эффективности, хорошей переносимости новых препаратов для 2 -й линии терапии и после АТСК • На таргетной терапии улучшаются показатели эффективности, снижается токсичность терапии по сравнению с существующей ХТ
 AДЦЕТРИС - II ФАЗА ИССЛЕДОВАНИЙ У ПАЦИЕНТОВ ПРИ РЕЦИДИВАХ И РЕЗИСТЕНТНОСТИ САККЛ
AДЦЕТРИС - II ФАЗА ИССЛЕДОВАНИЙ У ПАЦИЕНТОВ ПРИ РЕЦИДИВАХ И РЕЗИСТЕНТНОСТИ САККЛ
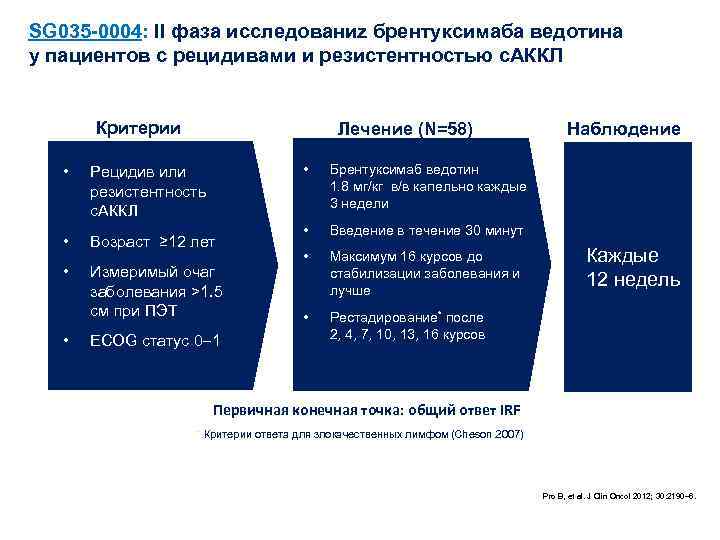 SG 035 -0004: II фаза исследованиz брентуксимаба ведотина у пациентов с рецидивами и резистентностью с. АККЛ Критерии Лечение (N=58) • • Рецидив или резистентность с. АККЛ • Возраст ≥ 12 лет • Измеримый очаг заболевания >1. 5 cм при ПЭТ • ECOG статус 0 1 Брентуксимаб ведотин 1. 8 мг/кг в/в капельно каждые 3 недели • Введение в течение 30 минут • Максимум 16 курсов до стабилизации заболевания и лучше • Наблюдение Рестадирование* после 2, 4, 7, 10, 13, 16 курсов Каждые 12 недель Первичная конечная точка: общий ответ IRF * Критерии ответа для злокачественных лимфом (Cheson 2007) Pro B, et al. J Clin Oncol 2012; 30: 2190– 6.
SG 035 -0004: II фаза исследованиz брентуксимаба ведотина у пациентов с рецидивами и резистентностью с. АККЛ Критерии Лечение (N=58) • • Рецидив или резистентность с. АККЛ • Возраст ≥ 12 лет • Измеримый очаг заболевания >1. 5 cм при ПЭТ • ECOG статус 0 1 Брентуксимаб ведотин 1. 8 мг/кг в/в капельно каждые 3 недели • Введение в течение 30 минут • Максимум 16 курсов до стабилизации заболевания и лучше • Наблюдение Рестадирование* после 2, 4, 7, 10, 13, 16 курсов Каждые 12 недель Первичная конечная точка: общий ответ IRF * Критерии ответа для злокачественных лимфом (Cheson 2007) Pro B, et al. J Clin Oncol 2012; 30: 2190– 6.
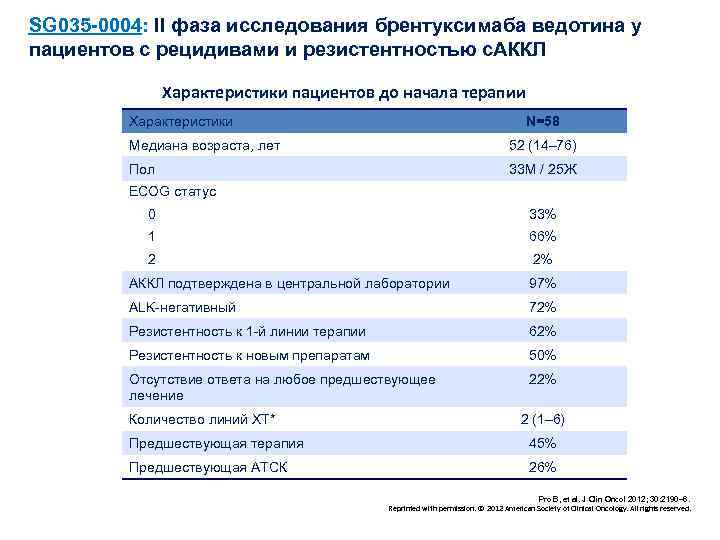 SG 035 -0004: II фаза исследования брентуксимаба ведотина у пациентов с рецидивами и резистентностью с. АККЛ Характеристики пациентов до начала терапии Характеристики N=58 Meдиана возраста, лет 52 (14– 76) Пол 33 M / 25 Ж ECOG статус 0 33% 1 66% 2 2% АККЛ подтверждена в центральной лаборатории 97% ALK-негативный 72% Резистентность к 1 -й линии терапии 62% Резистентность к новым препаратам 50% Отсутствие ответа на любое предшествующее лечение 22% Количество линий ХТ* 2 (1– 6) Предшествующая терапия 45% Предшествующая АТСК 26% Pro B, et al. J Clin Oncol 2012; 30: 2190– 6. Reprinted with permission. © 2012 American Society of Clinical Oncology. All rights reserved.
SG 035 -0004: II фаза исследования брентуксимаба ведотина у пациентов с рецидивами и резистентностью с. АККЛ Характеристики пациентов до начала терапии Характеристики N=58 Meдиана возраста, лет 52 (14– 76) Пол 33 M / 25 Ж ECOG статус 0 33% 1 66% 2 2% АККЛ подтверждена в центральной лаборатории 97% ALK-негативный 72% Резистентность к 1 -й линии терапии 62% Резистентность к новым препаратам 50% Отсутствие ответа на любое предшествующее лечение 22% Количество линий ХТ* 2 (1– 6) Предшествующая терапия 45% Предшествующая АТСК 26% Pro B, et al. J Clin Oncol 2012; 30: 2190– 6. Reprinted with permission. © 2012 American Society of Clinical Oncology. All rights reserved.
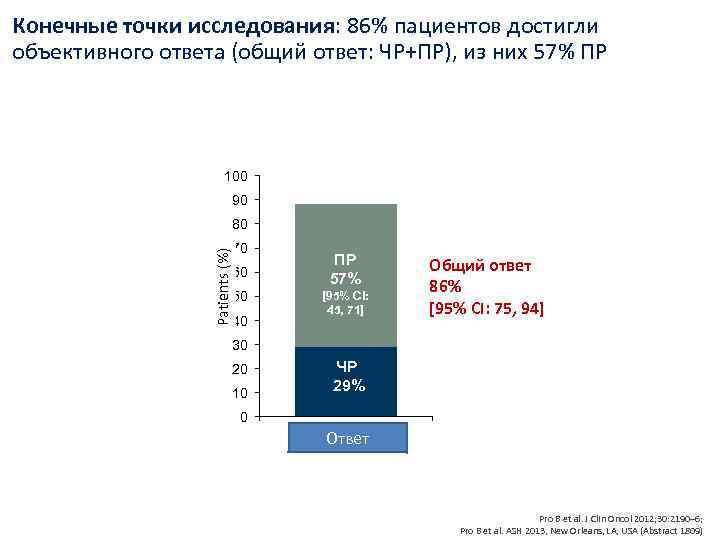 Конечные точки исследования: 86% пациентов достигли объективного ответа (общий ответ: ЧР+ПР), из них 57% ПР 100 90 80 Patients (%) 70 60 50 40 ПР 57% [95% CI: 45, 71] Общий ответ 86% [95% CI: 75, 94] 30 20 10 ЧР 29% 0 Clinical response Ответ Pro B et al. J Clin Oncol 2012; 30: 2190– 6; Pro B et al. ASH 2013, New Orleans, LA, USA (Abstract 1809)
Конечные точки исследования: 86% пациентов достигли объективного ответа (общий ответ: ЧР+ПР), из них 57% ПР 100 90 80 Patients (%) 70 60 50 40 ПР 57% [95% CI: 45, 71] Общий ответ 86% [95% CI: 75, 94] 30 20 10 ЧР 29% 0 Clinical response Ответ Pro B et al. J Clin Oncol 2012; 30: 2190– 6; Pro B et al. ASH 2013, New Orleans, LA, USA (Abstract 1809)
 Ключевые ответы на терапию (4 -летнее наблюдение, данные ASH 2014) Meдиана наблюдения от первой дозы = 46. 3 месяцев (от 0. 8 до 57. 7) (n=58) Объективный ответ % (95% CI) 86 (75, 94) ПР, % (95% CI) 57 (45, 71) Meдиана ВБП, месяцы (95% CI) • • 20. 0 (9. 4, -) Медиана времени до объективного ответа 5. 9 недель (от 4. 3 до 14) Медиана времени до ПР 11. 9 недель (от 5. 1 до 50. 3) Медиана количества курсов – 7 курсов (1 -16) Медиана количества курсов до объективного ответа – 8 курсов (1 -16) SG 035 -0004: Phase 2 study of brentuximab vedotin in patients with R/R s. ALCL: overview Pro et al. ASH Dec 2014, Abstract 3095; Pro B et al. J Clin Oncol 2012; 30: 2190 -96 Reused with permission. © 2012 Journal of Clinical Oncology. American Society of Clinical Oncology.
Ключевые ответы на терапию (4 -летнее наблюдение, данные ASH 2014) Meдиана наблюдения от первой дозы = 46. 3 месяцев (от 0. 8 до 57. 7) (n=58) Объективный ответ % (95% CI) 86 (75, 94) ПР, % (95% CI) 57 (45, 71) Meдиана ВБП, месяцы (95% CI) • • 20. 0 (9. 4, -) Медиана времени до объективного ответа 5. 9 недель (от 4. 3 до 14) Медиана времени до ПР 11. 9 недель (от 5. 1 до 50. 3) Медиана количества курсов – 7 курсов (1 -16) Медиана количества курсов до объективного ответа – 8 курсов (1 -16) SG 035 -0004: Phase 2 study of brentuximab vedotin in patients with R/R s. ALCL: overview Pro et al. ASH Dec 2014, Abstract 3095; Pro B et al. J Clin Oncol 2012; 30: 2190 -96 Reused with permission. © 2012 Journal of Clinical Oncology. American Society of Clinical Oncology.
 Meдиана общей выживаемости 55. 1 месяцев (4 -летнее наблюдение, ASH 2014) • • Meдиана наблюдения до первой дозы брентуксимаба: 46. 3 мес. (0. 8 – 57. 7 мес. ) Расчетная 4 -ОВ: 64% (95% CI: 51%, 76%) Общая выживаемость Pro et al. ASH Dec 2014, Abstract 3095
Meдиана общей выживаемости 55. 1 месяцев (4 -летнее наблюдение, ASH 2014) • • Meдиана наблюдения до первой дозы брентуксимаба: 46. 3 мес. (0. 8 – 57. 7 мес. ) Расчетная 4 -ОВ: 64% (95% CI: 51%, 76%) Общая выживаемость Pro et al. ASH Dec 2014, Abstract 3095
 ВБП в зависимости от ответа на терапию (4 -летнее наблюдение, ASH 2014) • Meдиана ВБП 20 месяцев (95% CI: 9. 4, NE) • 19/38 (50%) пациентов с ПР не имеют прогрессирования 11 пациентов получили консолидацию АТСК 8 пациентов не получали после брентуксимаба никакой терапии Pro et al. ASH Dec 2014, Abstract 3095
ВБП в зависимости от ответа на терапию (4 -летнее наблюдение, ASH 2014) • Meдиана ВБП 20 месяцев (95% CI: 9. 4, NE) • 19/38 (50%) пациентов с ПР не имеют прогрессирования 11 пациентов получили консолидацию АТСК 8 пациентов не получали после брентуксимаба никакой терапии Pro et al. ASH Dec 2014, Abstract 3095
 ВБП и ОВ в зависимости от данных ПЭТ после 4 -х курсов брентуксимаба и исходного ALK статуса (4 -летнее наблюдение, ASH 2014) Общая выживаемость и Выживаемость без прогрессирования 4 -ВБП (95% CI) 4 -ОВ (95% CI) ПЭТ+ (n=20) 16% (0%, 32%) 50% (28%, 72%) ПЭТ- (n=28) 63% (44%, 83%) 86% (72%, 99%) ALK+ (n=16) 37% (11%, 62%) 56% (32%, 81%) ALK- (n=42) 38% (22%, 54%) 67% (52%, 81%) Статус ПЭТ после 4 курсов ALK статус У 10 пациентов не было выполнено ПЭТ после 4 курсов из-за НЯ (3 пациента), прогрессирования (5 пациентов), решению исследователя (1 пациент), решение пациента (1 пациент) v Нет различий в 4 -ВБП по статусу ALK Pro et al. ASH Dec 2014, Abstract 3095
ВБП и ОВ в зависимости от данных ПЭТ после 4 -х курсов брентуксимаба и исходного ALK статуса (4 -летнее наблюдение, ASH 2014) Общая выживаемость и Выживаемость без прогрессирования 4 -ВБП (95% CI) 4 -ОВ (95% CI) ПЭТ+ (n=20) 16% (0%, 32%) 50% (28%, 72%) ПЭТ- (n=28) 63% (44%, 83%) 86% (72%, 99%) ALK+ (n=16) 37% (11%, 62%) 56% (32%, 81%) ALK- (n=42) 38% (22%, 54%) 67% (52%, 81%) Статус ПЭТ после 4 курсов ALK статус У 10 пациентов не было выполнено ПЭТ после 4 курсов из-за НЯ (3 пациента), прогрессирования (5 пациентов), решению исследователя (1 пациент), решение пациента (1 пациент) v Нет различий в 4 -ВБП по статусу ALK Pro et al. ASH Dec 2014, Abstract 3095
 Нежелательные явления ≥ 20% при 4 -летнем наблюдении (данные ASH, 2014) НЯ Периферическая нейропатия Тошнота Утомляемость Повышение температуры Диарея Сыпь Запор Нейтропения • Все степени % 57 40 38 34 29 24 22 21 Степень 3 % 17 2 3 0 2 12 Степень 4 % 0 0 2 0 0 9 Другие НЯ 3/4 степени, встречающиеся у ≥ 5 пациентов: тромбоцитопения 14% (8), анемия 7% (4) Pro et al. ASH Dec 2014, Abstract 3095.
Нежелательные явления ≥ 20% при 4 -летнем наблюдении (данные ASH, 2014) НЯ Периферическая нейропатия Тошнота Утомляемость Повышение температуры Диарея Сыпь Запор Нейтропения • Все степени % 57 40 38 34 29 24 22 21 Степень 3 % 17 2 3 0 2 12 Степень 4 % 0 0 2 0 0 9 Другие НЯ 3/4 степени, встречающиеся у ≥ 5 пациентов: тромбоцитопения 14% (8), анемия 7% (4) Pro et al. ASH Dec 2014, Abstract 3095.
 Обзор по безопасности N=58 Meдиана количества курсов, n Пациенты, остающиеся на терапии, n (%) 7 (1– 16) 9 (16) Модификация дозы Пациенты с отсроченным из-за НЯ введением, n (%) 23 (40) Редукция дозы до 1. 2 мг/кг, n (%) 7 (12) Прекращение терапии из-за НЯ, n (%) 14 (24) • Не было смертей, связанных с терапией в последующие 30 дней последней дозы • Наиболее частое НЯ для прекращения терапии - периферическая сенсорная нейропатия (10%) • Наиболее частое НЯ для редукции дозы - периферическая сенсорная нейропатия (7%) • Наиболее частое НЯ для отсроченного введения очередной дозы: периферическая сенсорная нейропатия (14%) и нейтропения (12%) Pro B et al. J Clin Oncol 2012; 30: 2190– 6.
Обзор по безопасности N=58 Meдиана количества курсов, n Пациенты, остающиеся на терапии, n (%) 7 (1– 16) 9 (16) Модификация дозы Пациенты с отсроченным из-за НЯ введением, n (%) 23 (40) Редукция дозы до 1. 2 мг/кг, n (%) 7 (12) Прекращение терапии из-за НЯ, n (%) 14 (24) • Не было смертей, связанных с терапией в последующие 30 дней последней дозы • Наиболее частое НЯ для прекращения терапии - периферическая сенсорная нейропатия (10%) • Наиболее частое НЯ для редукции дозы - периферическая сенсорная нейропатия (7%) • Наиболее частое НЯ для отсроченного введения очередной дозы: периферическая сенсорная нейропатия (14%) и нейтропения (12%) Pro B et al. J Clin Oncol 2012; 30: 2190– 6.
 Клинический случай с. АККЛ Исходно После 4 курсов 48 -летний мужчина, ALK+ АККЛ Получал терапию: CHOP VAPEC B AТСК • После 4 курсов рестадирование: ПР • После 1 -й дозы тумор-лизис синдром • Всего проведено 8 курсов Pro B et al. J Clin Oncol 2012; 30: 2190– 6. Reprinted with permission. © 2012 American Society of Clinical Oncology. All rights reserved.
Клинический случай с. АККЛ Исходно После 4 курсов 48 -летний мужчина, ALK+ АККЛ Получал терапию: CHOP VAPEC B AТСК • После 4 курсов рестадирование: ПР • После 1 -й дозы тумор-лизис синдром • Всего проведено 8 курсов Pro B et al. J Clin Oncol 2012; 30: 2190– 6. Reprinted with permission. © 2012 American Society of Clinical Oncology. All rights reserved.
 Заключение по исследованию брентуксимаба ведотина у пациентов с с. АККЛ (ASH, 2014) У пациентов с с. АККЛ: • 86% общая частота ответов • 57% пациентов достигли ПР • Расчетная 4 -ОВ 64% • Me OВ 55. 1 месяцев • Me ВБП 20. 0 месяцев (ОВ и ВБП не зависят от ALK статуса) • 50% пациентов в ПР • Наблюдаются без признаков прогрессирования • Профиль НЯ включает обратимую периферическую нейропатию, как наиболее частое НЯ, для купирования которого достаточно редукции дозы Pro et al. ASH Dec 2014, Abstract 3095.
Заключение по исследованию брентуксимаба ведотина у пациентов с с. АККЛ (ASH, 2014) У пациентов с с. АККЛ: • 86% общая частота ответов • 57% пациентов достигли ПР • Расчетная 4 -ОВ 64% • Me OВ 55. 1 месяцев • Me ВБП 20. 0 месяцев (ОВ и ВБП не зависят от ALK статуса) • 50% пациентов в ПР • Наблюдаются без признаков прогрессирования • Профиль НЯ включает обратимую периферическую нейропатию, как наиболее частое НЯ, для купирования которого достаточно редукции дозы Pro et al. ASH Dec 2014, Abstract 3095.
 Спасибо за внимание! дозы. C .
Спасибо за внимание! дозы. C .


