Сепсис, 2008.Шабалов.ppt
- Количество слайдов: 181

Современные представления о сепсисе новорождённых Шабалов Николай Павлович РВМА, СПб. ГПМА, С. -Петербург

Частота сепсиса в США (Angus D. C. et al. , Crit. Care Med. , 2001, 29, 1303 -1310) 750 000 больных в год (умирает 100 000); 42 000 больных детей в год (умирает 4 400); частота у детей до 1 год – 5, 3/1000; частота у детей 5 -14 лет – 0, 2/1000 (Martin G. S. et al. , N. Engl. J. Med. , 2003, Apr 17; 348(16), 15461554) Согласно американской национальной базы госпитализированных пациентов с 1979 по 2000 гг. ежегодный прирост частоты сепсиса составил 8, 7% и в пересчете на 100 000 населения за указанный период возрос с 83 случаев в 1979 году до 240 случаев в 2000 году. Прямые экономические убытки от сепсиса составляют 50 000 $ на одного больного; суммарные ежегодные затраты на сепсис в США превышают 17 млрд. $.

Частота неонатального сепсиса В Российской Федерации По данным главного неонатолога МЗ РФ Е. Н. Байбариной в 2003 году в РФ зарегистрировано 449 случаев сепсиса новорожденных, но, если экстраполировать данные иностранной литературы, то число больных новорождённых сепсисом, как минимум, должно было бы быть 10 000 – 14 000.

Установлено, что один документированный случай сепсиса приходится на 11 -23 случаев, когда новорожденным назначают лечение, исходя из подозрения на наличие сепсиса (Gerdes J. S. , 1991)

Watson R. S. , Linde-Zwirble W. T. , Lidicker J et al. (Crit. Care Med. -2003. - Vol. 29. -(Suppl. ). -A 8. ) • описывается более 42000 случаев сепсиса в 1995 году при уровне летальности 10, 3%, что составило 7% от всей детской смертности, затратах на лечение 1, 97 миллиардов долларов. • В 1999 году частота встречаемости сепсиса возросла (47700 пациентов) при снижении летальности до 9, 0%, сокращении длительности лечения на одни сутки и росте стоимости терапии одного ребенка на 4300 долларов. Затраты на лечение составили 2, 3 миллиарда долларов.

Бактериальный сепсис у новорожденных РФ в 2003 г (Е. Н. Байбарина, 2005) Показатели Доношенные Недоношенные с массой тела более 1000 г менее 1000 г Частота (%) Умерло Летальность 0, 014 50 26% 0, 28 74 33% 0, 96 22 69%
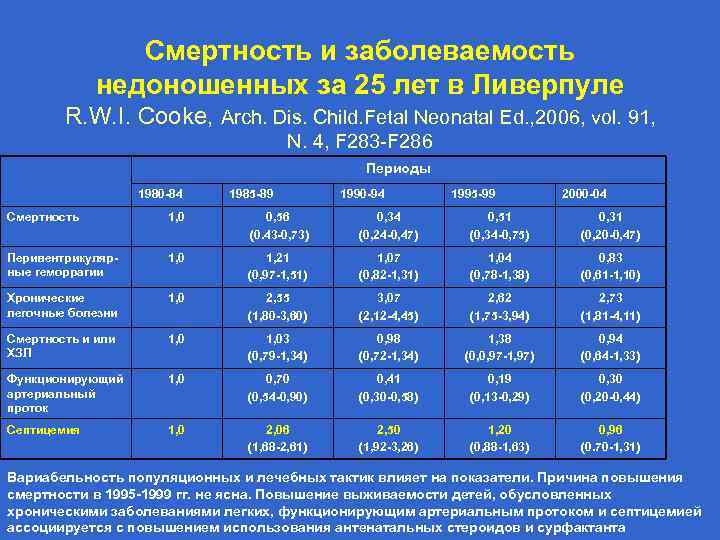
Смертность и заболеваемость недоношенных за 25 лет в Ливерпуле R. W. I. Cooke, Arch. Dis. Child. Fetal Neonatal Ed. , 2006, vol. 91, N. 4, F 283 -F 286 Периоды 1980 -84 1985 -89 1990 -94 1995 -99 2000 -04 Смертность 1, 0 0, 56 (0. 43 -0, 73) 0, 34 (0, 24 -0, 47) 0, 51 (0, 34 -0, 75) 0, 31 (0, 20 -0, 47) Перивентрикулярные геморрагии 1, 0 1, 21 (0, 97 -1, 51) 1, 07 (0, 82 -1, 31) 1, 04 (0, 78 -1, 38) 0, 83 (0, 61 -1, 10) Хронические легочные болезни 1, 0 2, 55 (1, 80 -3, 60) 3, 07 (2, 12 -4, 45) 2, 62 (1, 75 -3, 94) 2, 73 (1, 81 -4, 11) Смертность и или ХЗЛ 1, 03 (0, 79 -1, 34) 0, 98 (0, 72 -1, 34) 1, 38 (0, 0, 97 -1, 97) 0, 94 (0, 64 -1, 33) Функционирующий артериальный проток 1, 0 0, 70 (0, 54 -0, 90) 0, 41 (0, 30 -0, 58) 0, 19 (0, 13 -0, 29) 0, 30 (0, 20 -0, 44) Септицемия 1, 0 2, 06 (1, 68 -2, 61) 2, 50 (1, 92 -3, 26) 1, 20 (0, 88 -1, 63) 0, 96 (0. 70 -1, 31) Вариабельность популяционных и лечебных тактик влияет на показатели. Причина повышения смертности в 1995 -1999 гг. не ясна. Повышение выживаемости детей, обусловленных хроническими заболеваниями легких, функционирующим артериальным протоком и септицемией ассоциируется с повышением использования антенатальных стероидов и сурфактанта

Зарегистрированная заболеваемость сепсисом новорождённых в Санкт. Петербурге в 2007 году • Из 43 275 новорождённых диагноз сепсис поставлен у 28 детей (0, 7 на 1000 живорожденных) • Инфекции перинатального периода зарегистрированы у 840 детей (19, 4 на 1000 живорожденных)

ЧАСТОТА СЕПСИСОВ НА АУТОПСИЙНОМ МАТЕРИАЛЕ ДГБ № 1 СПб 1994 -2000 ГОДЫ (на 1316 вскрытий 143 сепсиса) С. Д. Попов 1994 1995 1996 1997 1998 1999 2000 7% 14% 12% 13% 8% 10% 12%
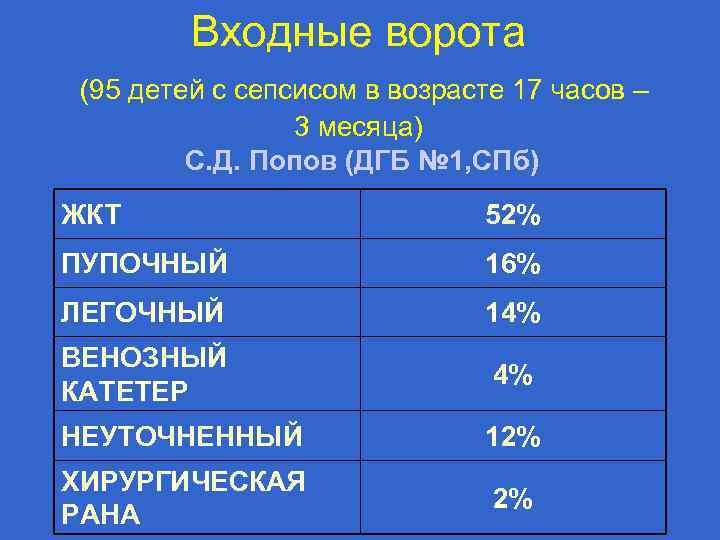
Входные ворота (95 детей с сепсисом в возрасте 17 часов – 3 месяца) С. Д. Попов (ДГБ № 1, СПб) ЖКТ 52% ПУПОЧНЫЙ 16% ЛЕГОЧНЫЙ 14% ВЕНОЗНЫЙ КАТЕТЕР 4% НЕУТОЧНЕННЫЙ 12% ХИРУРГИЧЕСКАЯ РАНА 2%
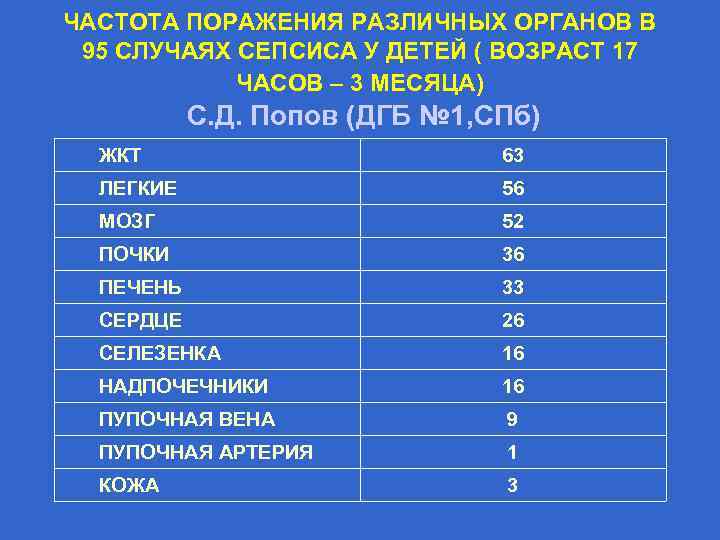
ЧАСТОТА ПОРАЖЕНИЯ РАЗЛИЧНЫХ ОРГАНОВ В 95 СЛУЧАЯХ СЕПСИСА У ДЕТЕЙ ( ВОЗРАСТ 17 ЧАСОВ – 3 МЕСЯЦА) С. Д. Попов (ДГБ № 1, СПб) ЖКТ 63 ЛЕГКИЕ 56 МОЗГ 52 ПОЧКИ 36 ПЕЧЕНЬ 33 СЕРДЦЕ 26 СЕЛЕЗЕНКА 16 НАДПОЧЕЧНИКИ 16 ПУПОЧНАЯ ВЕНА 9 ПУПОЧНАЯ АРТЕРИЯ 1 КОЖА 3

ТИПЫ И ЧАСТОТА ТКАНЕВЫХ РЕАКЦИЙ С. Д. Попов (ДГБ № 1, СПб) НЕКРОТИЧЕСКИЕ 36% ГНОЙНЫЕ 25% ГНОЙНЫЕ + НЕКРОТИЧЕСКИЕ 23% ГРАНУЛЕМАТОЗНЫЕ 2% ГРАНУЛЕМАТОЗНЫЕ + НЕКРОТИЧЕСКИЕ 4% НЕКРОТИЧЕСКИЕ+ ГНОЙНЫЕ+ ГРАНУЛЕМАТОЗНЫЕ 4% НЕКРОТИЧЕСКИЕ+ СЕРОЗНЫЕ 4% СЕРОЗНЫЕ 2%

Иммунные органы характеризовались незрелостью и истощением лимфоидной ткани. С. Д. Попов (ДГБ № 1, СПб)

Заключение С. Д. Попова • В большинстве случаев сепсис развивался у пациентов с различными вариантами иммунодефицита • Candida, Klebsiella, E coli, Serratia, Enterococcus, Pseudomonas – основные этиологические агенты. • ЖКТ и легкие были самыми частыми входными воротами • Метастатические очаги часто проявлялись некрозами без значительной экссудативной реакции • Тщательный анализ патологоанатомических данных позволяет разработать мероприятия по предупреждению инфекционных осложнений

Михаил Степанович Маслов (1885 – 1961)

«О сепсисе можно говорить тогда, когда бактериемия интенсивная или длительная, когда прорывы в кровяное русло из очага происходят повторно, когда организм не в состоянии противодействовать прорывам, не в состоянии обезвреживать микробов и когда в организме создаются какие-то благоприятные условия для оседания и размножения их в определенных органах и тканях. Следовательно, развитие сепсиса возможно при наличии инфекционного очага, с одной стороны, и своеобразной реактивности детского организма, с другой стороны» . М. С. Маслов «Сепсис и септические состояния» , Л. , 1959

«Громадная роль инфекта при сепсисе очевидна. Но в то же время ясно, что сепсис обуславливается не столько какиминибудь особенностями микроба, сколько особенностями самой реакции организма. Если стрептококк, этот самый частый возбудитель сепсиса, вызывает еще чаще абсцесс, флегмону, рожу, скарлатину и т. д. , то это происходит, разумеется, не потому что существуют стрептококки септические, флегмонозные, рожистые, скарлатинозные, а потому, что реакции организма на стрептококк исключительно разнообразны. Таким образом, мы логически приходим к выводу, что ПРОБЛЕМА СЕПСИСА ЕСТЬ ПРОБЛЕМА ПРЕЖДЕ ВСЕГО МАКРОБИОЛОГИЧЕСКАЯ» (И. В. Давыдовский, 1938)

Сепсис (от греч. «гниение» синоним– заражение крови)– генерализованный инфекционный процесс возникающий в условиях сниженного иммунитета имеющий прогрессирующее течение который в отсутствие адекватной антибактериальной терапии приводит к тяжелым множественным органным поражениям и смерти. Причины сниженного иммунитета могут быть разные» (Воробьев А. И. 1985)


Развитие взглядов на ведущее патогенетическое звено при сепсисе прошло несколько этапов (Цыбулькин Э. К. , 2001): 1. Начало века- патогенный микроорганизм. 2. С 20 -х годов- реакция Санарелли-Шварцмана. 3. 50 -е годы- эндотоксинемия. 4. 60 -х годов- реакция макроорганизма. 5. 70 -е годы- активация комплемента и нейтрофилов. 6. 80 -е годы- цитокины и метаболиты арахидоновой кислоты. 7. 90 -е годы- межклеточные взаимоотношения, регулируемые этапным включением медиаторов воспаления и иммуномодуляторов.

Эдуард Кузьмич Цыбулькин 1938 -2001


СИНДРОМ СИСТЕМНОГО ВОСПАЛИТЕЛЬНОГО ОТВЕТА (SIRS) 1. Температура тела выше 38 С или ниже 36 С 2. Тахикардия выше 90 ударов в минуту 3. Тахипноэ свыше 20 в минуту 4. Количество лейкоцитов >12 х10 /л, <4 х109/л или число молодых форм превышает 10% 1991 год; конференция американской коллегии торакальных хирургов (АССР) и общества медицины критических состояний (SCCM)

Варианты течения сепсиса • Сепсис = SIRS + инфекция • Тяжелый сепсис = сепсис с органной дисфункцией, гипоперфузией или гипотензией • Септический шок = сепсис с артериальной гипотензией, несмотря на адекватной волемическое возмещение

БАКТЕРИЯ очаг инфекции Сепсис + по крайней мере одно из следующего: острые нарушения сознания, гипоксемия, повышение уровня лактата плазмы, олигурия Сепсис синдром + гипотензия или симптом “белого пятна” 3 секунды и , сохраняющиеся более часа, несмотря на вливание жидкости и фармакопрепараты и требующие вазопрессорной поддержки бактериемия сепсис Клинически доказанная инфекция + гипертермия/гипотермия тахикардия тахипноэ аномальное количество лейкоцитов сепсис синдром ранний септический шок рефрактерный септический шок ПОН СМЕРТЬ Сепсис синдром + гипотензия или симптом “белого пятна”- 3 секунды и >, быстро отвечающие на внутривенное введение жидкости и/или фармакотерапию Любая комбинация из: ДВС СДР взрослого типа ОПН острая печеночная недостаточность острая дисфункция ЦНС

В 13 издании «Справочника Харрисона по внутренним болезням» (СПб. , Питер, 1999, стр. 218) дано такое определение сепсиса: «Сепсис- системный воспалительный ответ организма на инфекцию любыми бактериальными микроорганизмами. Септический шок возникает в результате избыточной реакции гомеостатических механизмов на инфекцию, ведущих к гипотензии и полиорганной недостаточности» Согласно G. U. Meduri (1999) «Сверхагрессивный и нерегулируемый системный воспалительный ответ- главная детерминанта сепсиса» , а по образному выражению C. Moggi et al. (1996) при сепсисе наблюдается «цитокиновый шторм» . Сепсис – болезнь адаптации.

Согласно R. Bone, септический процесс - динамическое взаимодействие “системного воспалительного ответа” (systemic inflammatory response syndrome - SIRS), определяемого цитокинами TNF, IL 1, 6, 8 и др. и “компенсаторного антивоспалительного ответа” (compensatory antiinflammatory response syndrome - CARS), определяемого цитокинами IL 4, 10, 11, 13 и др. При преобладании SIRS-компонента развиваются кардиоваскулярная компроментация, моно- или полиорганные дисфункции, а CARS – супрессия иммунной системы. По данным D. Wilkinson (1998), летальность при сепсисе у детей при недостаточности одной системы (органу) – 1%, двух – 11%, трех – 50%, четырех и более – 75% и выше. По данным зарубежных авторов у детей старше месяца сепсис развивается у 21 -23% с SIRS инфекционного генеза

Сывороточная концентрация ИФН-гамма у новорожденных в зависимости от наличия или отсутствия подтверждённой ВУИ, пкг/мл (50 перцентиль; 75 перцентиль) В. А. Сергеева (2004) Дети с ВУИ Гаммаинтерферон Дети без ВУИ 100, 0; 108, 0 180, 9; 282, 7
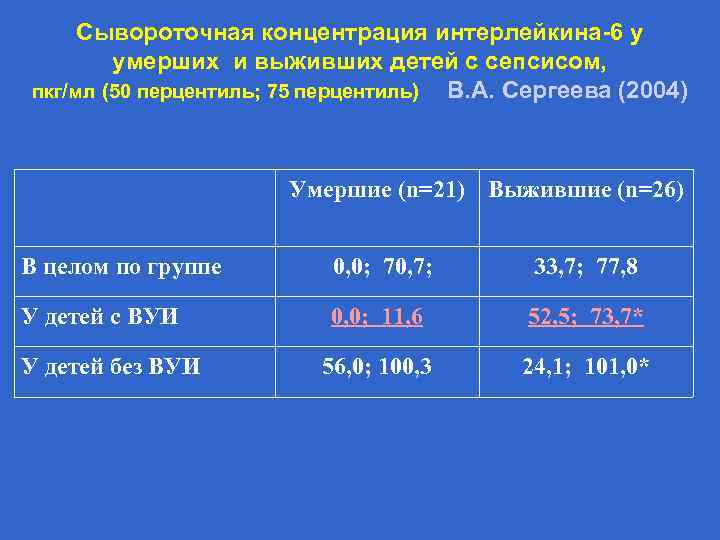
Сывороточная концентрация интерлейкина-6 у умерших и выживших детей с сепсисом, пкг/мл (50 перцентиль; 75 перцентиль) В. А. Сергеева (2004) Умершие (n=21) Выжившие (n=26) В целом по группе 0, 0; 70, 7; 33, 7; 77, 8 У детей с ВУИ 0, 0; 11, 6 52, 5; 73, 7* 56, 0; 100, 3 24, 1; 101, 0* У детей без ВУИ
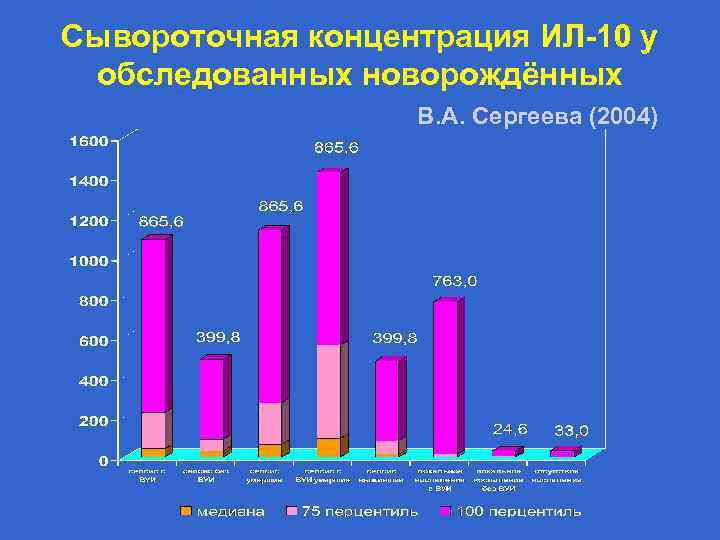
Сывороточная концентрация ИЛ-10 у обследованных новорождённых В. А. Сергеева (2004)
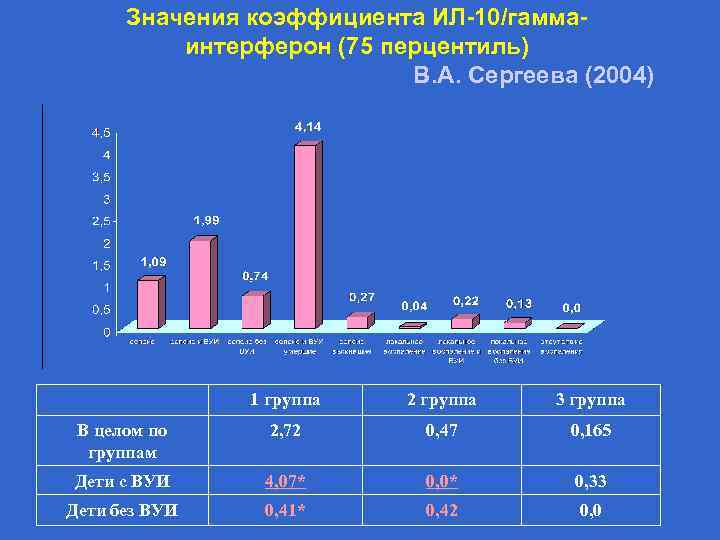
Значения коэффициента ИЛ-10/гаммаинтерферон (75 перцентиль) В. А. Сергеева (2004) 1 группа 2 группа 3 группа В целом по группам 2, 72 0, 47 0, 165 Дети с ВУИ 4, 07* 0, 0* 0, 33 Дети без ВУИ 0, 41* 0, 42 0, 0

Значение индекса ИФН-гамма/ИЛ-10 в зависимости от наличия подтверждённого внутриутробного инфицирования и исхода заболевания (75 перцентиль) В. А. Сергеева (2004) Дети с ВУИ Дети без ВУИ В целом 13, 82 115, 3 Выжившие в 1 группе 4, 25 10, 74 Умершие в 1 группе 0, 47 0, 0 Выжившие 8, 0* Умершие 0, 96*

Вывод неонатальный сепсис, особенно у новорождённых с внутриутробным инфицированием, протекает на фоне нарушенного баланса Т-хелперов 1 -го и 2 -го типов и угнетения клеточного звена иммунного ответа с преобладанием системного противовоспалительного ответа, что при отсутствии специфической терапии обусловливает более тяжёлое течение сепсиса и неблагоприятный прогноз.

Сепсис – инфекционное ациклическое заболевание (т. е. без лечения приводящее к смерти), в основе которого лежит дисфункция фагоцитарно-макрофагальной системы и неадекватный системный воспалительный ответ иммунокомпромиссного организма на бактериальную, как правило, условно патогенную (чаще госпитальную) инфекцию. Нередкой причиной сепсиса являются грибы. Сепсис характеризуется генерализованным повреждением эндотелия сосудистого русла, интоксикацией, расстройствами гемостаза с обязательным ДВС-синдромом и

Диагностические критерии сепсиса 2001 SCCM/ESICM/ACCP/ATS/SIS международная конференция по дефиниции сепсиса (Levy M. M. et al. , Crit. Care VTd. , 2003, vol. 31, № 4, p. 1250 -1256) Первостепенные консенсусные точки • Существующие концепции сепсиса, тяжелого сепсиса и септического шока выглядят здравыми и должны оставаться такими какими описаны 10 лет назад. • Существующие определения не позволяют точно выявлять стадии ответа макроорганизма на инфекцию. • Признаки и симптомы сепсиса значительно изменились по сравнению с теми что были первоначально установлены в 1991 году. • Список этих признаков и симптомов для диагностики сепсиса представлен. • Будущее лежит в развитии системы стадийности, которая будет характеризовать прогрессирование сепсиса. Новая система PIRO предположительно будет характеризовать и определять стадии ответа хозяина на инфекцию.

Концепция PIRO • Predisposition (предрасположенность) • Infection (инфекция) • Response (реакция) • Organ dysfunction (органная дисфункция) • Возраст, генетические факторы, сопутствующие заболевания, иммуносупрессивная терапия и др. • Локализация очага инфекции, возбудитель инфекции • Клинические проявления инфекционного процесса (температура тела, ЧСС, уровень лейкоцитоза, концентрация С-реактивного белка, прокальцитонина и др. ) • Для оценки степени органной дисфункции используют разные шкалы, например, SOFA

Диагностические критерии сепсиса 2001 SCCM/ESICM/ACCP/ATS/SIS международная конференция по дефиниции сепсиса (Levy M. M. et al. , Crit. Care VTd. , 2003, vol. 31, № 4, p. 1250 -1256) Инфекция – патологический процесс, индуцированный микроорганизмами. Инфекция документированная или предполагаемая и несколько из представленных ниже симптомов

Общие симптомы 2001 SCCM/ESICM/ACCP/ATS/SIS международная конференция по дефиниции сепсиса (Levy M. M. et al. , Crit. Care VTd. , 2003, vol. 31, № 4, p. 12501256) • Лихорадка (температура более 38, 00 С) • Гипотермия (температура менее 36, 00 С). • Частота сердечных сокращений более 90 в минуту или более двух квадратичных отклонений от возрастной нормы • Тахипное • Изменение ментального статуса • Значительный отек или задержка жидкости более 20 мл/кг в течение 24 часов • Гипергликемия (глюкоза плазмы крови более 120 мг/дл или 7, 7 ммоль/л) при отсутствии диабета

Показатели воспаления 2001 SCCM/ESICM/ACCP/ATS/SIS международная конференция по дефиниции сепсиса (Levy M. M. et al. , Crit. Care VTd. , 2003, vol. 31, № 4, p. 12501256) • Лейкоцитоз (число лейкоцитов более 12000/мкл) • Лейкопения (число лейкоцитов менее 4000/мкл) • Более чем 10% лейкоцитов представлены незрелыми клетками • С-реактивный белок плазмы крови превышает нормальные значения на 2 квадратичных отклонения • Прокальциотонин плазмы крови превышает нормальные значения на 2 квадратичных отклонения

• Кардиоваскулярная дисфункция • Несмотря на назначение изотонической жидкости внутривенно болюсно > 40 мл/кг падение артериального давления (гипотензия) менее 5 возрастного перцентиля или систолическое давление снижено на 2 квадратичных отклонения от возрастной нормы • - или необходимость в вазопрессорах для поддержания артериального давления в пределах нормы (допамин > 5 мкг/кг/мин или добутамин, адреналин или норадреналин в любой дозировке) • - или два из 5 ниже перечисленных симптомов • 1. Необъяснимый метаболический ацидоз, дефицит оснований >5. 0 m. Eq/L • 2. Увеличение содержания лактата в артериальной крови более чем в 2 раза от нормального • 3. Олигоурия (диурез менее 0, 5 мл/кг/час) • 4. Удлинение времени капиллярного наполнения более чем на 5 секунд • 5. Разница между центральной и периферической температурой >3˚ C

Критерии органной дисфункции у взрослых согласно конференции IPSSC (2005) • Респираторная дисфункция оксигенации - Pa. O 2/Fi. O 2 <300 в отсутствии порока сердца синего типа или наличия сопутствующей патологии легких - или Pa. CO 2> 65 torr или 20 мм рт ст сверх обычного содержания Pa. CO 2 - или доказанная необходимостьв кислороде или >на 50% Fi. O 2 для поддержания сатурации > 92% - или необходимость в неэлективной инвазивной или неинвазивной искусственной вентиляции легких индекс • • Неврологическая дисфункция • - Оценка по шкале ком Глазго < 11 баллов • - острое изменение ментального статуса с уменьшением оценки по шкале ком Глазго < 3 баллов от исходного

Критерии органной дисфункции у взрослых согласно конференции IPSSC (2005)
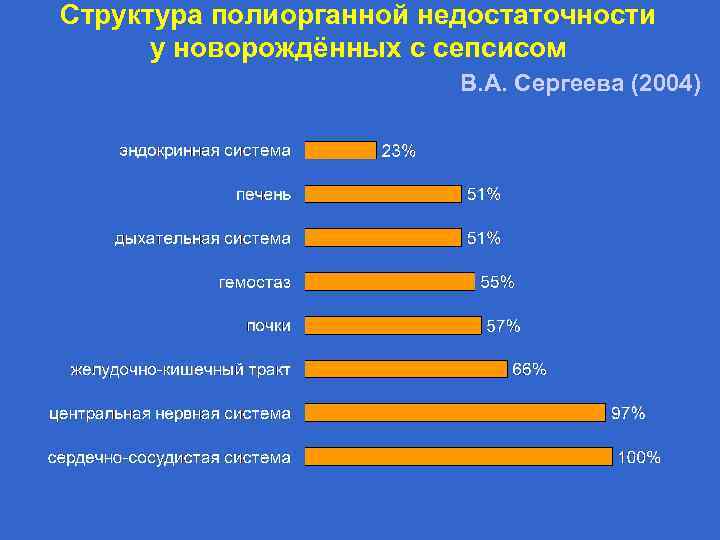
Структура полиорганной недостаточности у новорождённых с сепсисом В. А. Сергеева (2004)

Данные корреляционной зависимости значений ИЛ-10 и степени полиорганной недостаточности В. А. Сергеева (2004) Система органов Интерлейкин-10 Центральная нервная система r=0, 54, р=0, 1 Дыхательная система r=0, 01, р=0, 97 Гемодинамика r=0, 24, р=0, 12 Желудочно-кишечный тракт r=0, 05, р=0, 74 Гемостаз r=0, 62, р=0, 0001* Метаболизм r=0, 07, р=0, 68 Печень r=0, 37, р=0, 02* Почки r=-0, 28, р=0, 06

Диагностические критерии сепсиса у детей 2001 SCCM/ESICM/ACCP/ATS/SIS международная конференция по дефиниции сепсиса (Levy M. M. et al. , Crit. Care VTd. , 2003, vol. 31, № 4, p. 1250 -1256) Диагностическими критериями сепсиса у детей служат показатели воспаления + инфекция с гипер- или гипотермией (ректальная температура выше 38, 50 С или ниже 360 С), тахикардия (может отсутствовать у гипотермичных пациентов) и по крайней мере одно из следующих проявлений органной дисфункции – изменение ментального статуса, гипоксемия, гиперлактатемия или скачущий пульс.

Международная консенсусная конференция по педиатрическому сепсису: определения сепсиса и органной дисфункции у детей. (Pediatric Critical Care Medicine – 2005. - Vol. 6, N. 1. - P. 2 -8) Синдром системного воспалительного ответа Присутствие, по меньшей мере, двух из следующих четырех критериев, один из которых обязательно: аномальная температура или число лейкоцитов Центральная температура > 38, 50 С или < 36. 00 С Тахикардия, определяемая как средняя частота сердечных сокращений, превышающая 2 квадратичных отклонения от возрастной нормы в отсутствии внешних стимулов, длительного приема лекарств, болевого стимула или иной необъяснимый персистирующий подъем в течение более чем 0, 5 -4 часов или для детей менее 1 года - брадикардия определяемая как средняя частота сердечных сокращений менее 10 возрастного перцентиля в отсутствии внешнего вагусного стимула, назначения β-блокаторов или врожденных пороков сердца или необъяснимой персистирующей депрессии длительностью более 0, 5 часа. Средняя частота дыханий превышающая 2 квадратичных отклонения от возрастной нормы или необходимость в искусственной вентиляции легких при остром процессе не связанной с нейромышечными заболеваниями или воздействием общей анестезии Число лейкоцитов увеличено или снижено по сравнению с возрастной нормой (только не вторичная к химиотерапии - индуцированная лейкопения) или > 10% незрелых нейтрофилов

Диагностические критерии сепсиса 2001 SCCM/ESICM/ACCP/ATS/SIS международная конференция по дефиниции сепсиса (Levy M. M. et al. , Crit. Care VTd. , 2003, vol. 31, № 4, p. 1250 -1256) В будущем, если это будет поддержано дальнейшими эпидемиологическими данными, возможно, что использование чисто биохимических или иммунологических показателей будет более предпочтительным для идентификации SIRS нежели клинические данные. Может быть воспаление презентуется когда повышается концентрация интерлейкина 6, прокальцитонина или С-реактивного белка, но для поддержки данного заключения необходимо проведение крупных проспективных исследований.

МАРКЕРЫ СЕПСИСА Белки острой фазы 1. C-реактивный белок 2. a 1 кислый гликопротеид (орозомукоид) 3. С 3 Цитокины и их рецепторы 4. ИЛ-2 R –(растворимый рецептор- s. IL 2 -R)– маркер ранней стадии сепсиса у недоношенных 5. ФНОα 6. ИЛ-6 + ИЛ-8 + липополисахарид-связывающий протеин 7. адреномедулин 8. ИЛ-10 9. Г-КСФ 10. “растворимые” молекулы адгезии CD 14, s. ELAM-1, MIP-1α 11. Экстрацеллюлярная фосфолипаза А 2 12. Прокальцитонин (ПКТ) – маркер диагноза тяжести и прогноза при септическом шоке 13. Высокоподвижный белок фагоцитов Химические субстанции бактериального происхождения 14. Эндотоксин 15. Другие бактериальные метаболиты

Прокальцитонин (ПСТ) • • ПСТ – полипептид с молекулярной массой 14, 5 к. Да, состоит из 116 аминокислотных остатков, предшественник кальцитонина, лишенный гормональной активности, синтезируемый в С-клетках щитовидной железы и практически не поступающий в кровь. Повышение концентрации ПСТ в крови происходит при бактериальных инфекциях и сепсисе даже у больных перенесших тотальную резекцию щитовидной железы (Assicot M. et al. , Lancet, 1993, 341 (8844), 515 -518). Период полужизни ПСТ ~ 24 часа. ПСТ при бактериальных инфекциях синтезируется в лейкоцитах, нейроэндокринных клетках кишечника, легких и печени. У здоровых добровольцев после инъекции бактериального эндотоксина уровень ПСТ в крови повышается в 1700 раз (начало через 2 -3 часа, плато через 6 -8 часов) вслед за подъемом уровня провоспалительных цитокитнов IL-6, TNF -α (через 90 и 180 минут). Снижение уровня ПСТ на 30% - признак уменьшения тяжести инфекционного процесса. Роль ПКТ при тяжелых инфекциях до конца не ясна и в эксперименте введение ПСТ увеличивало, а антител к нему снижало смертность животных при сепсисе. Однако, есть указания, ПСТ тормозит синтез TNF-α и простагландина Е 2, тромбоксана В 2, т. е. имеет противовоспалительный эффект. Измерение уровня ПСТ в крови является специфическим маркером тяжести бактериальных инфекций и он не повышается при вирусных инфекциях и аутоиммунных процессах (обзор Н. В. Белобородовой, 2006).
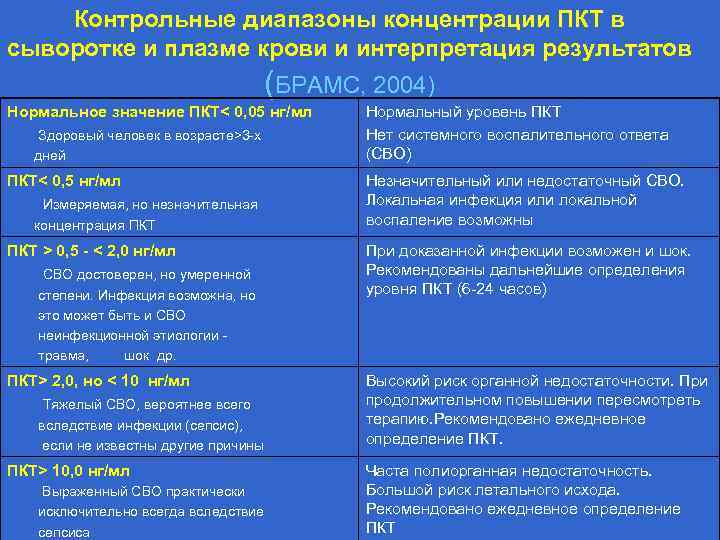
Контрольные диапазоны концентрации ПКТ в сыворотке и плазме крови и интерпретация результатов (БРАМС, 2004) Нормальное значение ПКТ< 0, 05 нг/мл Здоровый человек в возрасте>3 -х дней ПКТ< 0, 5 нг/мл Измеряемая, но незначительная концентрация ПКТ > 0, 5 - < 2, 0 нг/мл СВО достоверен, но умеренной степени. Инфекция возможна, но это может быть и СВО неинфекционной этиологии травма, шок др. ПКТ> 2, 0, но < 10 нг/мл Тяжелый СВО, вероятнее всего вследствие инфекции (сепсис), если не известны другие причины ПКТ> 10, 0 нг/мл Выраженный СВО практически исключительно всегда вследствие сепсиса Нормальный уровень ПКТ Нет системного воспалительного ответа (СВО) Незначительный или недостаточный СВО. Локальная инфекция или локальной воспаление возможны При доказанной инфекции возможен и шок. Рекомендованы дальнейшие определения уровня ПКТ (6 -24 часов) Высокий риск органной недостаточности. При продолжительном повышении пересмотреть терапию. Рекомендовано ежедневное определение ПКТ. Часта полиорганная недостаточность. Большой риск летального исхода. Рекомендовано ежедневное определение ПКТ
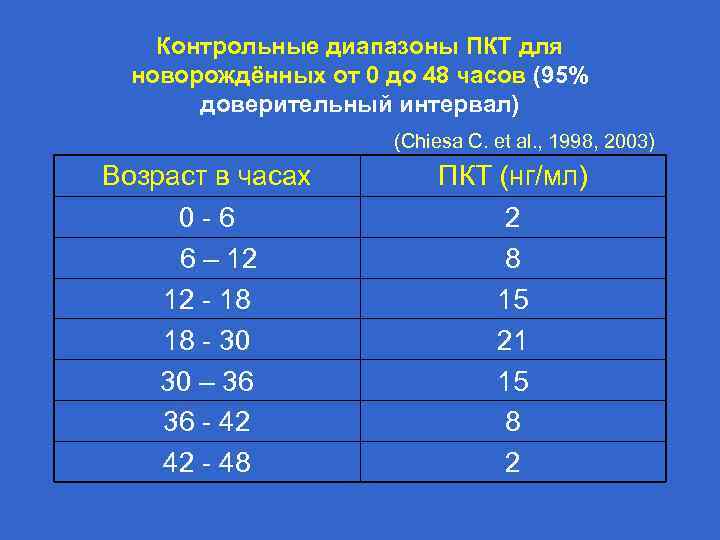
Контрольные диапазоны ПКТ для новорождённых от 0 до 48 часов (95% доверительный интервал) (Chiesa C. et al. , 1998, 2003) Возраст в часах 0 - 6 6 – 12 12 - 18 18 - 30 30 – 36 36 - 42 42 - 48 ПКТ (нг/мл) 2 8 15 21 15 8 2

Прокальцитонин у недоношенных детей в первые дни жизни: введение возрастных номограмм D. Turner et al. , Arch. Dis. Child. Fetal Neonatal Ed. , 2006, vol. 91, N. 4, F 283 F 286 • У доношенных новорождённых после рождения отмечен подъем в крови уровня ПКТ с пиком около 20 нг/мл к 24 часам жизни. • На основе изучения 332 образцов крови, полученных у 100 недоношенных со сроком гестации от 24 до 36 недель (медиана 32 недели) установлен более низкий (по сравнению с доношенными) пик подъема концентрации ПКТ – 28 часов, в отличие от доношенных диагностическую ценность имеет подъем выше 0, 5 нг/мл после 96 часов. • ПКТ не проникает через плаценту и лихорадка у матери, хориоамнионит, высев микробов из плаценты не влияют на уровень ПКТ у ребенка. • У инфицированных детей уровни ПКТ были выше, чем представленные в номограмме
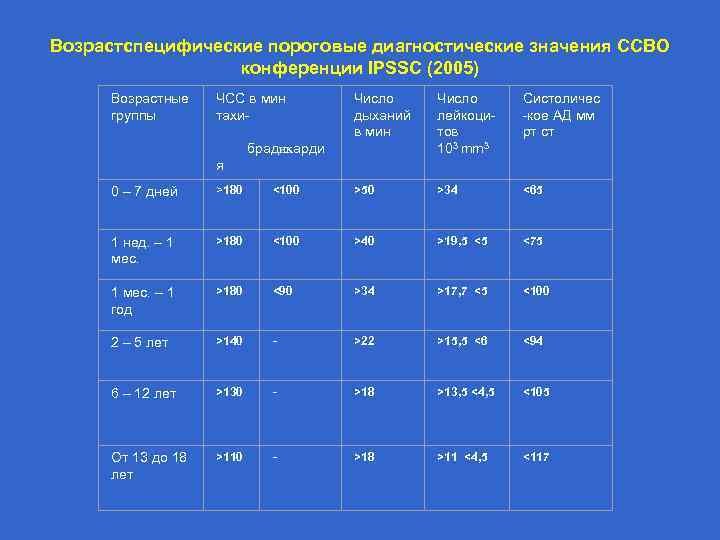
Возрастспецифические пороговые диагностические значения ССВО конференции IPSSC (2005) Возрастные группы ЧСС в мин тахи- Число дыханий в мин Число лейкоцитов 103 mm 3 Систоличес -кое АД мм рт ст брадикарди я 0 – 7 дней >180 <100 >50 >34 <65 1 нед. – 1 мес. >180 <100 >40 >19, 5 <5 <75 1 мес. – 1 год >180 <90 >34 >17, 7 <5 <100 2 – 5 лет >140 - >22 >15, 5 <6 <94 6 – 12 лет >130 - >18 >13, 5 <4, 5 <105 От 13 до 18 лет >110 - >18 >11 <4, 5 <117

Клинические критерии SIRS у новорожденных: 1. Расстройство температурного гомеостата (гипертермия или гипотермия) 2. Одышка или тахипное более 50 в 1 минуту (у детей на ИВЛ – р. СО 2 менее 32 мм. рт. ст. ) 3. Тахикардия более 180 в 1 минуту или брадикардия менее 100 в 1 минуту 4. Утрата коммуникабельности анорексия угнетение и/или судороги 5. Олигурия (диурез менее 0, 5 мл/кг/час в сутки или в течение 6 часов менее 1, 0 мл/кг/час на фоне адекватной инфузионной терапии)

Лабораторные признаки SIRS у новорожденных: 1. Внезапно возникший тяжелый метаболический лактат-ацидоз с гипокапнией (последнее при отсутствии поражения легких) 2. Лейкоцитоз (кол-во лейкоцитов у детей первого дня жизни >30000, 2 -7 дней >15000 и старше >12000 в 1 мкл капиллярной крови) или лейкопения (кол-во лейкоцитов в 1 мкл крови <6000 и далее <5000) с нейтрофилезом (количество нейтрофилов в 1 мкл капиллярной крови у детей первого дня жизни >15000 2 -7 дней >7500 и 8 дней и старше > 6500) или нейтропения (соответственно в указанные выше дни число нейтрофилов <5000 2000, и 1750)

Лабораторные признаки SIRS у новорожденных: 3. Регенераторный или регенераторно-дегенеративный сдвиг лейкоцитарной формулы при числе палочкоядерных и более молодых форм >500. в мкл (в первый день жизни >2000 в мкл) 4. Токсическая зернистость нейтрофилов 5. Индекс иммунологической реактивности (ИИР) менее 2, 5 и лейкоцитарный индекс интоксикации (ЛИИ) более 3, 5 6. Тромбоцитопения 7. Анемия

Лабораторные признаки SIRS у новорожденных: 8. Внезапно возникшее укорочение или удлинение активированного частичного тромбопластинового времени (АЧТВ) или протромбинового времени (ПТВ) 9. Повышение уровня СR-протеина или других острофазовых белков 10. Увеличение СОЭ более 10 мм в час 11. Бактериемия 12. Гипергликемия более 7, 5 ммоль/л на фоне адекватной инфузионной терапии (глюкоза 5 -6 мг/кг/мин) 13. Гиперкалиемия более 6, 5 ммоль/л

Наиболее существенные факторы высокого риска развития неонатального сепсиса: 1. Смерть предыдущих детей в семье от системных бактериальных инфекций в возрасте до 3 -х месяцев (подозрение на наследственный иммунодефицит) 2. Многочисленные аборты в анамнезе 3. Гестоз у матери продолжавшийся более 4 недель 4. Хронические очаги инфекции, прежде всего в урогенитальной сфере, желудочно-кишечном тракте, эндокринные и аутоиммунные заболевания у матери 5. Клинически выраженные бактериальные инфекционные процессы у матери непосредственно до родов и в родах 6. Клинически выявленный бактериальный вагиноз у матери 7. Обнаружение у матери в родовых путях стрептококка В или его антигенов

Наиболее существенные факторы высокого риска развития неонатального сепсиса: 8. Безводный промежуток более 12 часов 9. Рождение ребенка с очень низкой и особенно экстремально низкой массой тела 10. Тахикардия у плода без лихорадки, гипотензии, кровопотери у матери или введения ей лекарств, вызывающих тахикардию 11. Асфиксия при рождении или другая патология потребовавшая реанимационных пособий и длительного воздержания от энтерального питания 12. Хирургические операции особенно с обширным травмированием тканей 13. Врожденные пороки развития с поврежденными кожными покровами ожоги

Наиболее существенные факторы высокого риска развития неонатального сепсиса: 14. СДР-синдром 1 типа и отек легких 15. Респираторный дистресс у доношенного новорождённого, не улучшающийся или ухудшающийся на фоне 6 -и часовой рациональной ИВЛ 16. Многодневные катетеризации пупочной и центральных вен, дефицитное питание 17. Внутриутробные инфекции (ВУИ) 18. Множественные пороки развития или более 5 стигм дизэмбриогенеза 19. Длительные и массивные курсы антибактериальной терапии у новорождённых. 20. Использование схем де-эскалационной терапии в первую неделю жизни

Сепсис следует диагностировать у детей с факторами высокого риска + 4 клинических и 4 лабораторных признака SIRS инфекционного генеза. Если у ребенка имеется клинически очевидный очаг инфекции то для диагностики сепсиса достаточно 4 клинических и трех лабораторных признаков SIRS инфекционного генеза
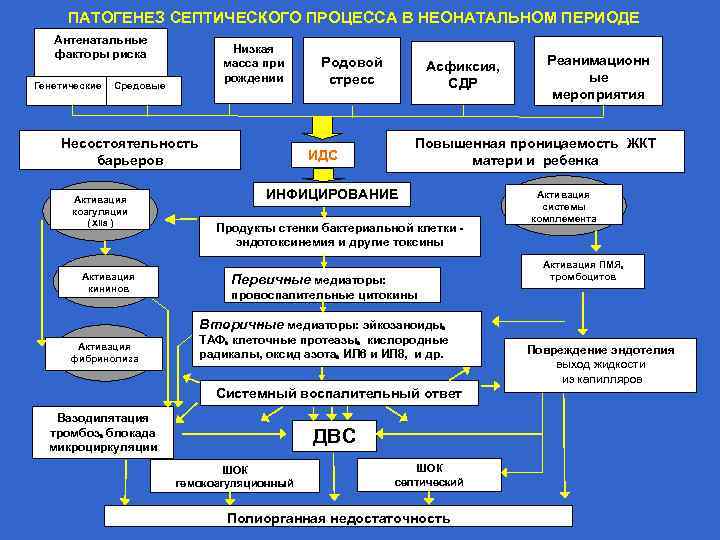
ПАТОГЕНЕЗ СЕПТИЧЕСКОГО ПРОЦЕССА В НЕОНАТАЛЬНОМ ПЕРИОДЕ Антенатальные факторы риска Генетические Низкая масса при рождении Средовые Несостоятельность барьеров Активация коагуляции ( XIIа ) Активация кининов Родовой стресс Асфиксия, СДР Реанимационн ые мероприятия Повышенная проницаемость ЖКТ матери и ребенка ИДС ИНФИЦИРОВАНИЕ Продукты стенки бактериальной клетки эндотоксинемия и другие токсины Активация системы комплемента Активация ПМЯ тромбоцитов Первичные медиаторы: провоспалительные цитокины Вторичные медиаторы: эйкозаноиды Активация фибринолиза ТАФ клеточные протеазы кислородные радикалы, оксид азота ИЛ 6 и ИЛ 8, и др. Системный воспалительный ответ Вазодилятация тромбоз блокада микроциркуляции ДВС ШОК гемокоагуляционный ШОК септический Полиорганная недостаточность Повреждение эндотелия выход жидкости из капилляров

МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ БОЛЕЗНЕЙ 10 -го пересмотра (приказ МЗ РФ, 1997) P 36 Бактериальный сепсис новорожденного Включено: врожденная септицемия (транзиторная бактериемия ? !) P 36. 0 Сепсис новорожденного, обусловленный стрептококком группы B • • • P 36. 1 Сепсис новорожденного, обусловленный другими и неуточненными стрептококками • P 36. 2 Сепсис новорожденного, обусловленный золотистым стафилококком [Staphylococcus aureus] • P 36. 3 Сепсис новорожденного, обусловленный другими и неуточненными стафилококками • P 36. 4 Сепсис новорожденного, обусловленный кишечной палочкой [Escherichia coli] • P 36. 5 Сепсис новорожденного, обусловленный анаэробными микроорганизмами • P 36. 8 Сепсис новорожденного, обусловленный другими бактериальными агентами • P 36. 9 Бактериальный сепсис новорожденного неуточненный
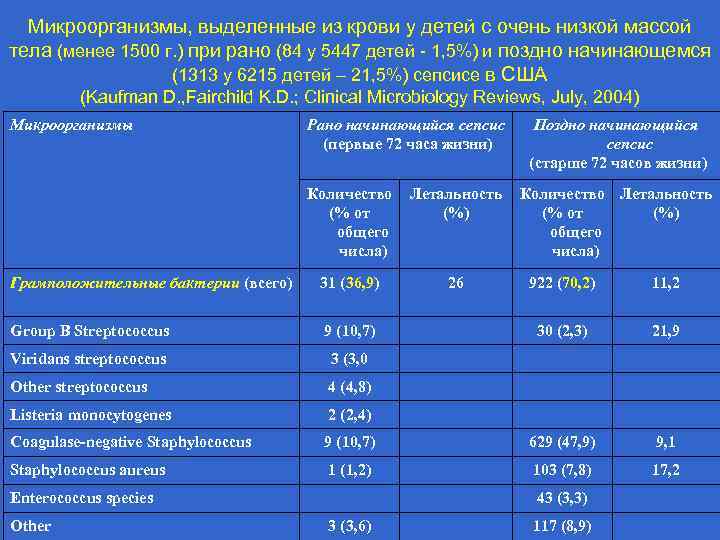
Микроорганизмы, выделенные из крови у детей с очень низкой массой тела (менее 1500 г. ) при рано (84 у 5447 детей - 1, 5%) и поздно начинающемся (1313 у 6215 детей – 21, 5%) сепсисе в США (Kaufman D. , Fairchild K. D. ; Clinical Microbiology Reviews, July, 2004) Микроорганизмы Рано начинающийся сепсис (первые 72 часа жизни) Количество (% от общего числа) Летальность (%) Грамположительные бактерии (всего) 31 (36, 9) 26 Group B Streptococcus 9 (10, 7) Viridans streptococcus 3 (3, 0 Other streptococcus 4 (4, 8) Listeria monocytogenes 2 (2, 4) Coagulase-negative Staphylococcus aureus Поздно начинающийся сепсис (старше 72 часов жизни) 922 (70, 2) 11, 2 30 (2, 3) 21, 9 9 (10, 7) 629 (47, 9) 9, 1 1 (1, 2) 103 (7, 8) 17, 2 Enterococcus species Other Количество Летальность (% от (%) общего числа) 43 (3, 3) 3 (3, 6) 117 (8, 9)
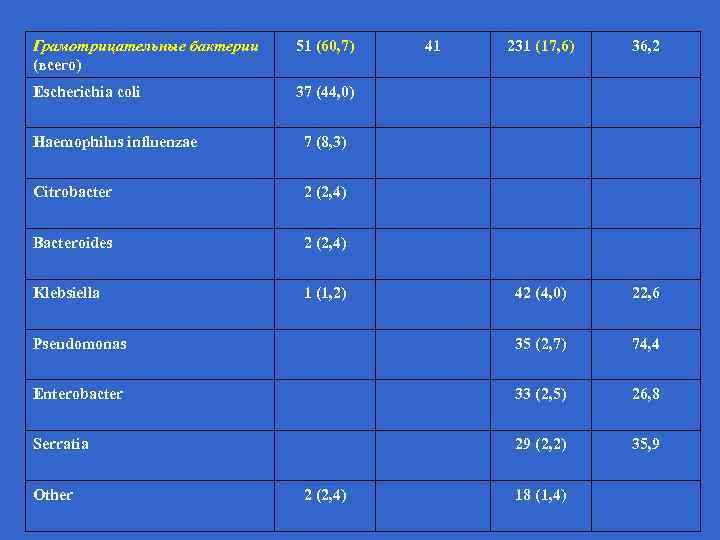
Грамотрицательные бактерии (всего) 51 (60, 7) Escherichia coli 231 (17, 6) 36, 2 37 (44, 0) 42 (4, 0) 22, 6 Pseudomonas 35 (2, 7) 74, 4 Enterobacter 33 (2, 5) 26, 8 Serratia 29 (2, 2) 35, 9 Haemophilus influenzae 7 (8, 3) Citrobacter 2 (2, 4) Bacteroides 2 (2, 4) Klebsiella 1 (1, 2) 41 Other 2 (2, 4) 18 (1, 4)

Посев крови ( «Сепсис в начале XXI века» //под ред. В. С. Савельева и Б. Р. Гельфанда, Litterra, 2006) • Кровь для исследования необходимо взять до назначения антибиотиков или перед очередным назначением. • Необходимым минимумом забора являются две пробы, взятые из вен разных конечностей с интервалом 30 минут. Оптимальным является взятие 3 -х проб. Забор крови на высоте лихорадки не повышает чувствительности метода (категория доказательности С). • Не показано преимуществ забора крови из артерии (категория доказательности С).

Категория доказательств для обоснованности применения клинических рекомендаций ( «Сепсис в начале XXI века» //под ред. В. С. Савельева и Б. Р. Гельфанда, Litterra, 2006) • А – основаны на результатах по крайней мере двух больших рандомизированных исследований • В - основаны на результатах по крайней мере одного большого рандомизированного исследования • С – основаны на результатах небольших рандомизироаныых исследований с неопределенными результатами • D – основаны на результатах нерандомизированных исследований с одновременным контролем • Е - основаны на результатах нерандомизированных исследований с ретроспективным контролем, анализе серии случаев, неконтролируемых исследованиях или мнении экспертов

Посев крови • Чувствительность при сепсисе 25 -48% и отрицательные результаты не могут гарантировать отсутствие бактериемии (Н. В. Белобородова (2006) • Причины: повреждение бактерий антибиотиками или факторами иммунной защиты, при бактериальной транслокации – гепатоэнтерогенная циркуляция бактерий без проникновения их в системный кровоток. • Согласно Marshall J. , Sweeney D. (Arch. Surg. , 1990, 121 (1), 17 -22) у больных с хирургическим сепсисом при отрицательной гемокультуре летальность была выше, чем у больных с доказанной бактериемией. • Посев не позволяет выявить концентрацию химических субстанций бактериального происхождения, а именно они играют решающую роль в запуске воспалительного каскада.

Патогенез бактериемии при сепсисе • Частота инфекционных осложнений у больных с обширными хирургическими операциями, например при сложных ВПС, или, находящихся в тяжелом, критическом состоянии составляет 15 -30% и её нельзя объяснить лишь экзогенным инфицированием и по современным представлениям имеет место транслокация эндогенной бактериальной флоры кишечника. • Функционирование кишечного барьера определяется кислой средой желудка, двигательной и секреторной активностью тонкой кишки, пищеварительными ферментами, нормальной кишечной микрофлорой, секреторными иммуноглобулинами, уровнем Ig. M в крови и состоянием фагоцитарно-макрофагальной системы. У новорождённых это всё зависит от течения внутриутробного и интранатального периодов. • При гипоксемии, ишемии кишечника, расстройствах микроциркуляции, голодании (отсутствии энтерального питания!) проницаемость кишечного барьера повышается и происходит транслокация бактериальной флоры кишечника в кровь (смена лидеров при сепсисе по С. Я. Далецкому).


Возрастные группы детей применительно к определению тяжелого сепсиса (Pediatric Critical Care Medicine – 2005. - Vol. 6, N. 1. - P. 2 -8) Новорожденные 0 – 7 дней Новорожденные 1 неделя – 1 месяц Младенцы 1 месяц – 1 год Дошкольники 2 – 5 лет Школьники 6 – 12 лет Подростки 13 лет – менее 18 лет
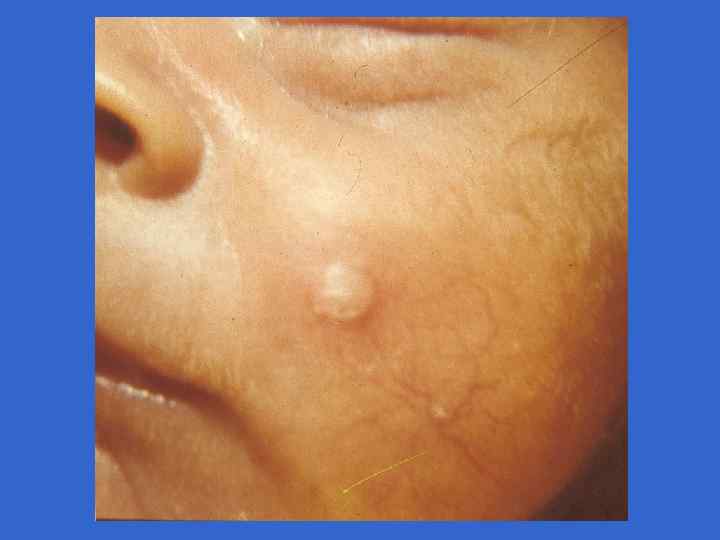
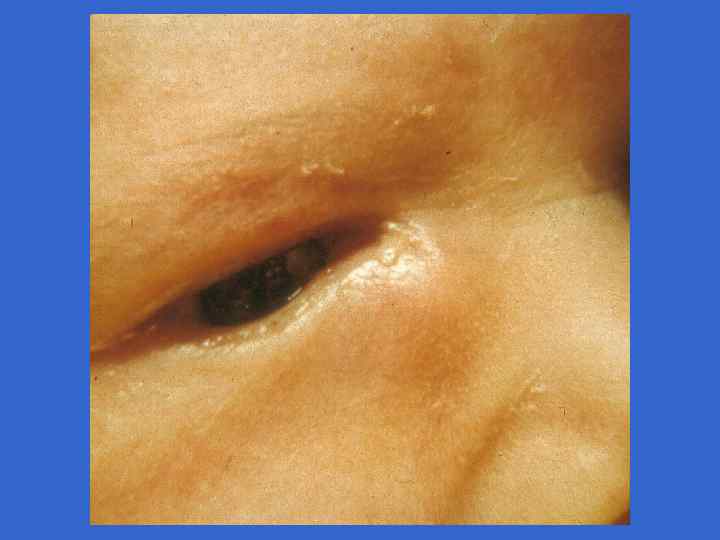
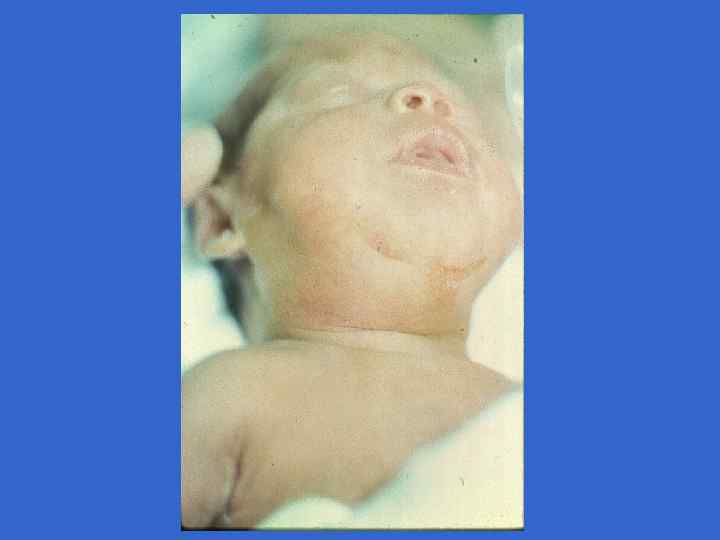
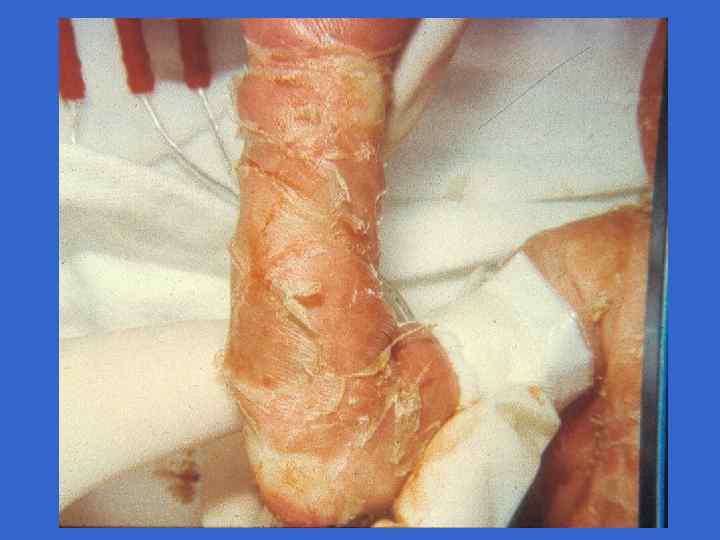
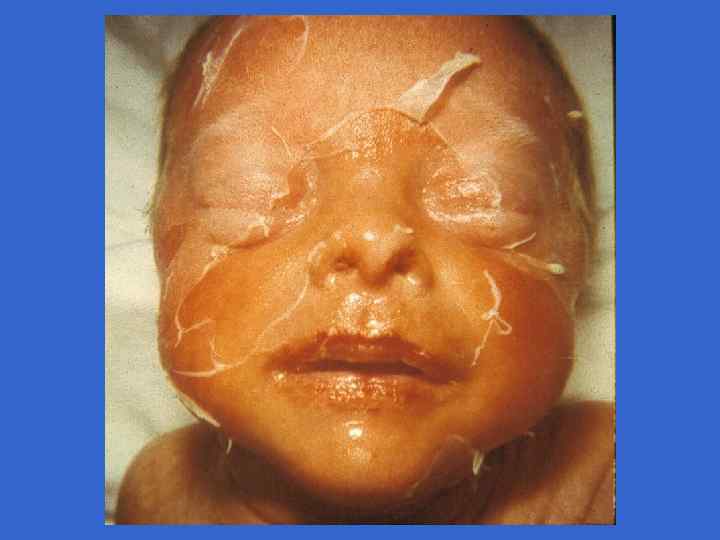
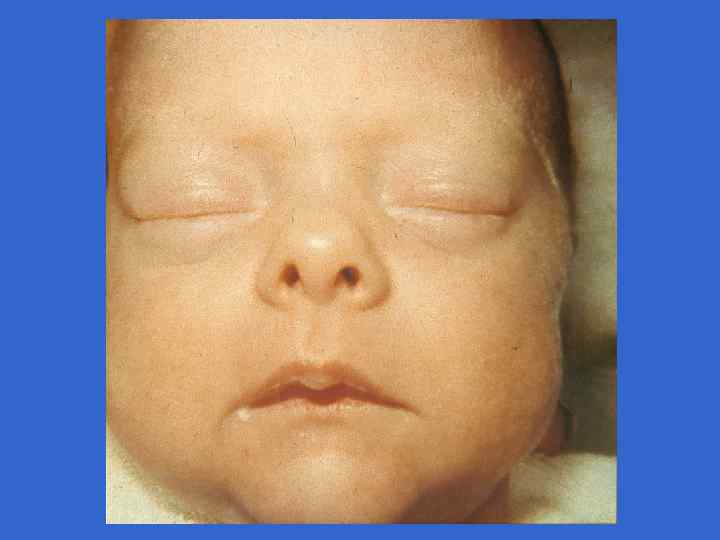
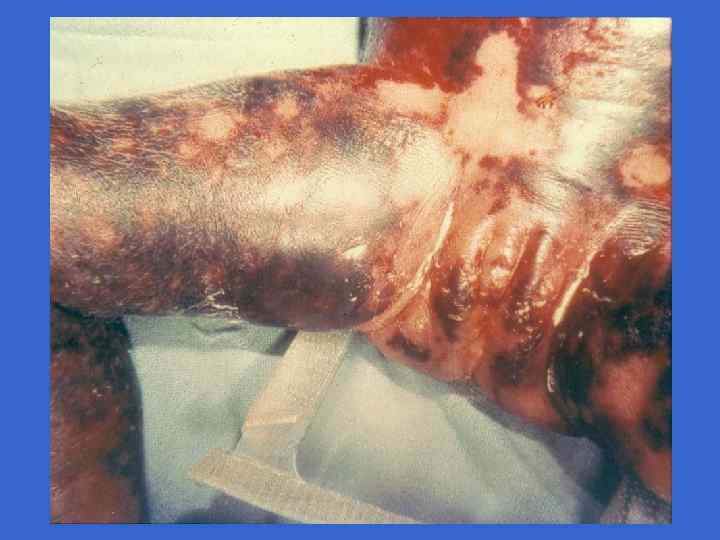
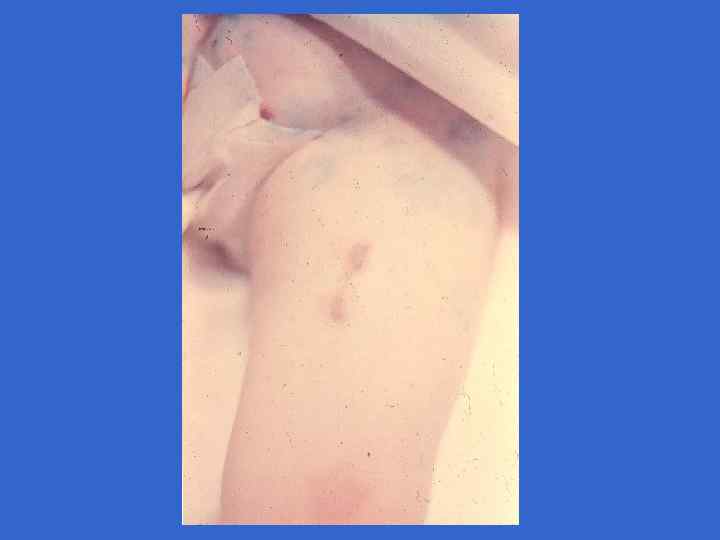
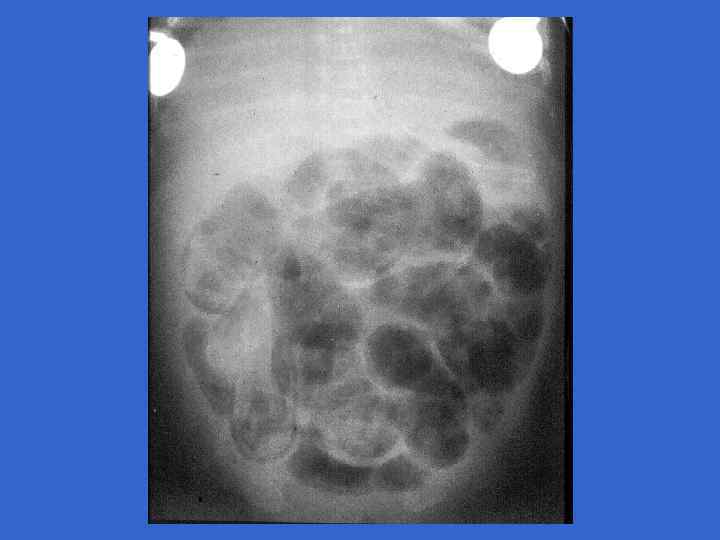
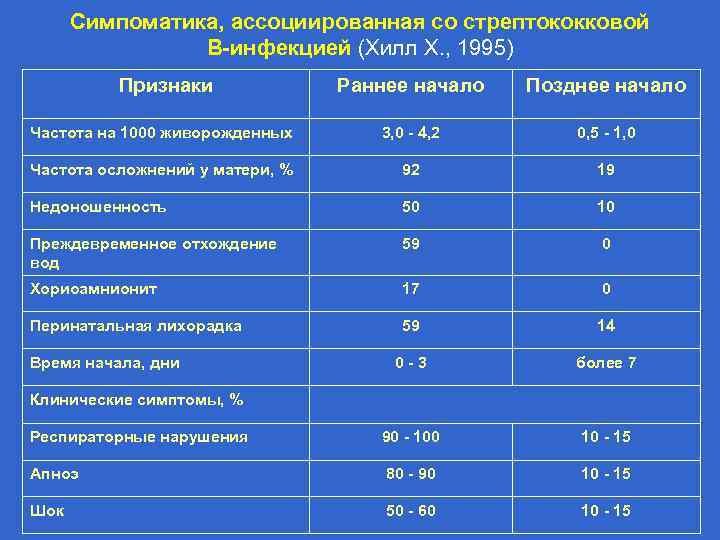
Симпоматика, ассоциированная со стрептококковой В-инфекцией (Хилл Х. , 1995) Признаки Раннее начало Позднее начало Частота на 1000 живорожденных 3, 0 - 4, 2 0, 5 - 1, 0 Частота осложнений у матери, % 92 19 Недоношенность 50 10 Преждевременное отхождение вод 59 0 Хориоамнионит 17 0 Перинатальная лихорадка 59 14 0 - 3 более 7 Респираторные нарушения 90 - 100 10 - 15 Апноэ 80 - 90 10 - 15 Шок 50 - 60 10 - 15 Время начала, дни Клинические симптомы, %
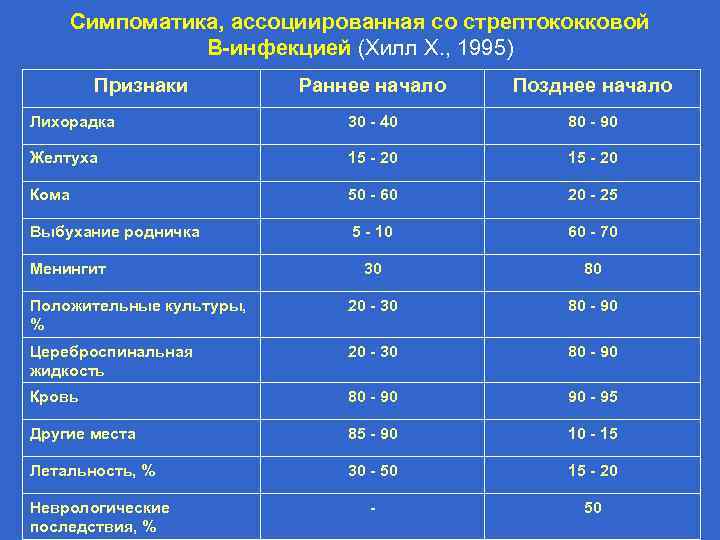
Симпоматика, ассоциированная со стрептококковой В-инфекцией (Хилл Х. , 1995) Признаки Раннее начало Позднее начало Лихорадка 30 - 40 80 - 90 Желтуха 15 - 20 Кома 50 - 60 20 - 25 Выбухание родничка 5 - 10 60 - 70 30 80 Положительные культуры, % 20 - 30 80 - 90 Цереброспинальная жидкость 20 - 30 80 - 90 Кровь 80 - 90 90 - 95 Другие места 85 - 90 10 - 15 Летальность, % 30 - 50 15 - 20 - 50 Менингит Неврологические последствия, %

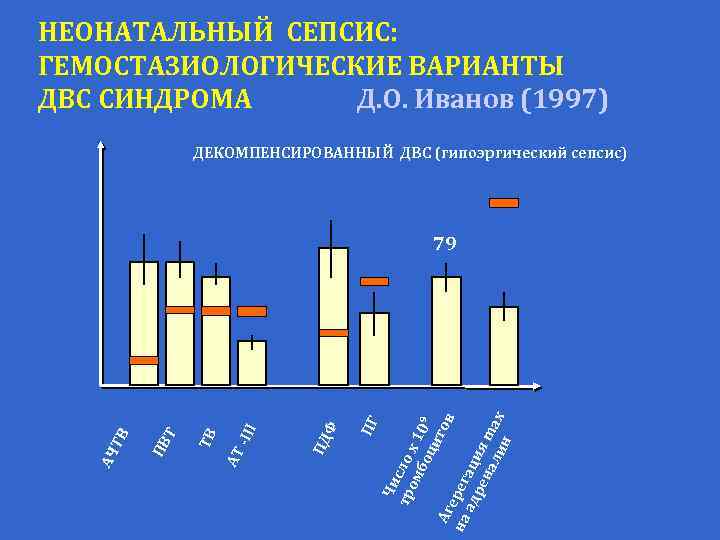
НЕОНАТАЛЬНЫЙ СЕПСИС: ГЕМОСТАЗИОЛОГИЧЕСКИЕ ВАРИАНТЫ ДВС СИНДРОМА Д. О. Иванов (1997) ДЕКОМПЕНСИРОВАННЫЙ ДВС (гипоэргический сепсис) Чи тр сло ом х 1 бо 0 9 ци то Аг в ер на ег ад аци ре на я ma ли н x ПГ Ф ПД III АТ - ТВ Т ПВ АЧ ТВ 79
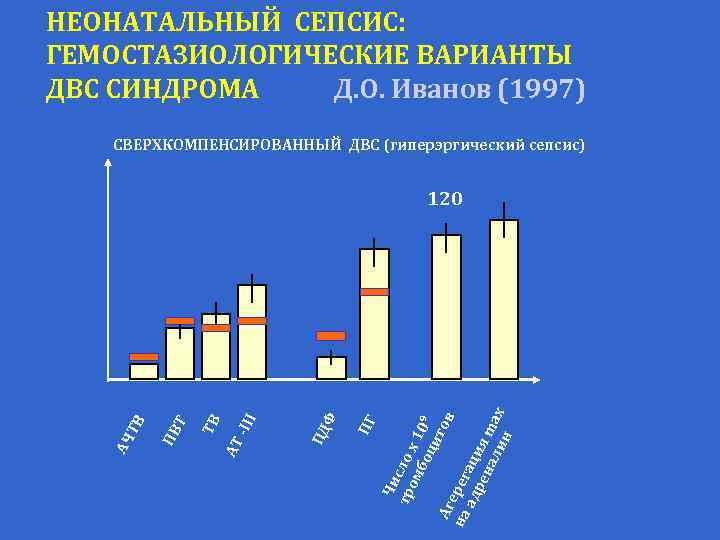
НЕОНАТАЛЬНЫЙ СЕПСИС: ГЕМОСТАЗИОЛОГИЧЕСКИЕ ВАРИАНТЫ ДВС СИНДРОМА Д. О. Иванов (1997) СВЕРХКОМПЕНСИРОВАННЫЙ ДВС (гиперэргический сепсис) Чи тр сло ом х 1 бо 0 9 ци то Аг в ер на ег ад аци ре на я ma ли н x ПГ Ф ПД III АТ - ТВ Т ПВ АЧ ТВ 120

НЕОНАТАЛЬНЫЙ СЕПСИС: ГЕМОСТАЗИОЛОГИЧЕСКИЕ ВАРИАНТЫ ДВС СИНДРОМА Д. О. Иванов (1997) НЕОНАТАЛЬНЫЙ СЕПСИС (параметры гемостаза воспаления иммунитета) G Ig. M ЦИ К Ig ФН Г Т 1 -А IХ Х Ф VI II ДЕКОМПЕНСИРОВАННЫЙ ДВС (гипоэргический сепсис)
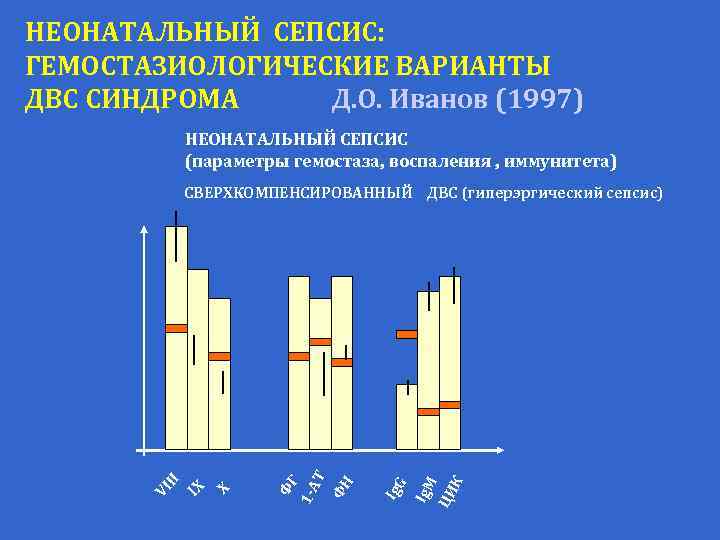
НЕОНАТАЛЬНЫЙ СЕПСИС: ГЕМОСТАЗИОЛОГИЧЕСКИЕ ВАРИАНТЫ ДВС СИНДРОМА Д. О. Иванов (1997) НЕОНАТАЛЬНЫЙ СЕПСИС (параметры гемостаза воспаления иммунитета) Ig. M ЦИ К G Ig Х Г 1 -А Т ФН IХ Ф VI II СВЕРХКОМПЕНСИРОВАННЫЙ ДВС (гиперэргический сепсис)

ГОРМОНЫ ПРИ НЕОНАТАЛЬНОМ СЕПСИСЕ Д. О. Иванов (2002) Резистентность к СТГ (СТГ >50 нг/мл; диапазон 51– 135) Центральная супрессия продукции ТТГ (ТТГ 0 06 0 47; Т 3 0 58 -0 81) 46 1% 12 8% Синдром “Low T 3” (Т 3 <1 0 нг/мл диапазон 0 5 -1 0) ТТГ не изменен 10 3% Снижены СТГ и ТТГ 12 8%
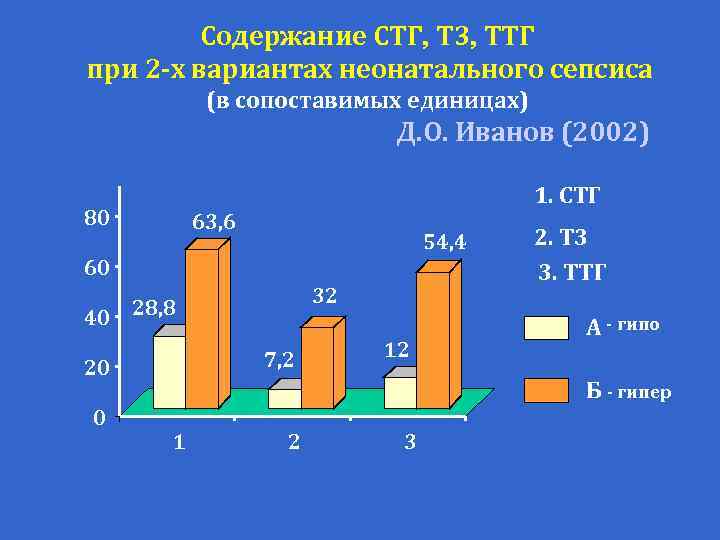
Содержание СТГ Т 3 ТТГ при 2 -х вариантах неонатального сепсиса (в сопоставимых единицах) Д. О. Иванов (2002) 80 1. СТГ 63, 6 54, 4 60 32 40 28, 8 7, 2 20 0 12 2. Т 3 3. ТТГ А - гипо Б - гипер 1 2 3
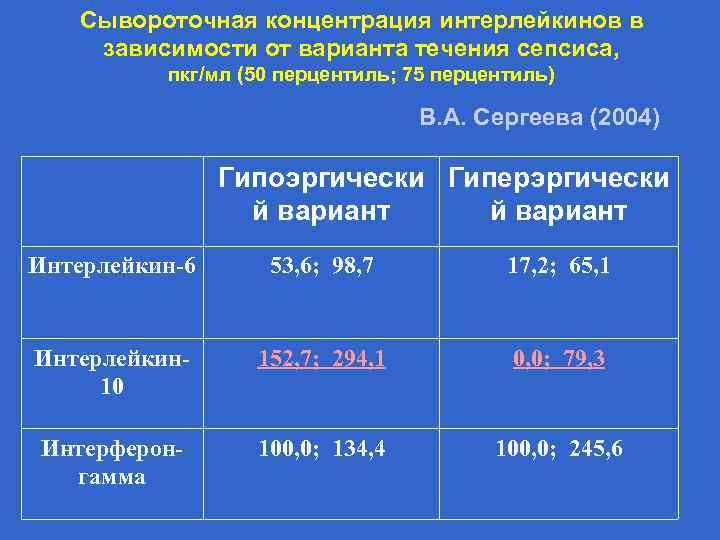
Сывороточная концентрация интерлейкинов в зависимости от варианта течения сепсиса, пкг/мл (50 перцентиль; 75 перцентиль) В. А. Сергеева (2004) Гипоэргически Гиперэргически й вариант Интерлейкин-6 53, 6; 98, 7 17, 2; 65, 1 Интерлейкин 10 152, 7; 294, 1 0, 0; 79, 3 Интерферонгамма 100, 0; 134, 4 100, 0; 245, 6

Гипоэргический вариант • При нем отсутствует адекватная инфекционному процессу гиперпластическая реакция со стороны органов кроветворения и иммуногенеза, отсутствует или минимально выражен локальный сосудисто-пролиферативный компонент воспаления, адекватная реакция нейроэндокринной системы, а также имеют место тяжелые нарушения обмена веществ, и прежде всего энергетического. • Характерно преобладание деструктивных изменений в очаге воспаления, угнетение и дегенеративные изменения в органах кроветворения и в клетках периферической крови. Типичный гипоэргический сепсис развивается у детей с очень низкой массой тела при рождении, ЗВУР гипопластического и диспластического типов или с первичными наследственными иммунодефицитами, глубокими нейтропениями и лимфоцитопениями различного генеза. У доношенных детей чаще всего это кандида-сепсис, синегнойный сепсис.

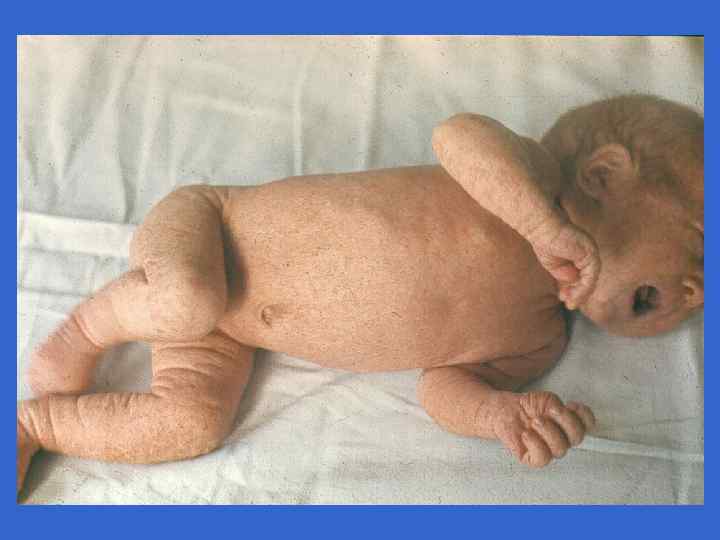
Гиперэргический вариант • При данном варианте максимально выражена пролиферативная реакция соединительной ткани и крови, доминируют реакции чрезмерной активации продукции провоспалительных цитокинов и каскада плазменных протеаз «протеолитический взрыв» гранулоцитов, тромбоцитов, эндотелия. Этот вариант сепсиса чаще развивается у доношенных детей и у новорожденных с массой тела более 1500 гр. Часто этот вариант обусловлен стрептококками группы В, листериями, эшерихиями. Обычно он возникает под влянием супервирулентных особых штаммов микробов.

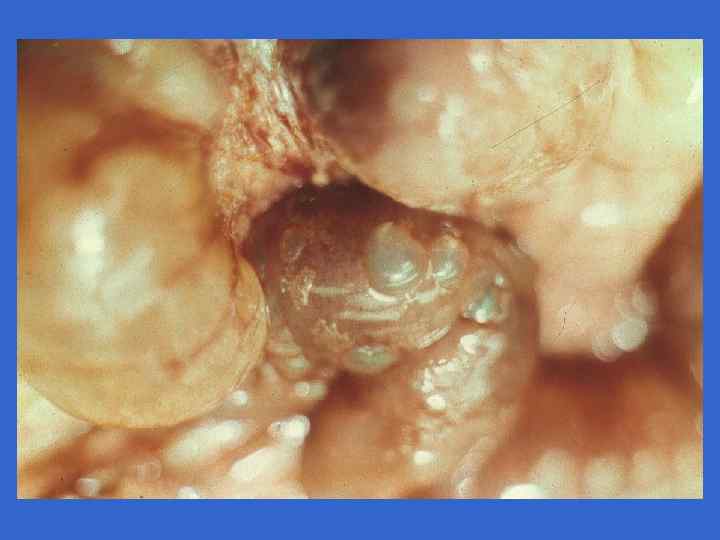
Возбудители
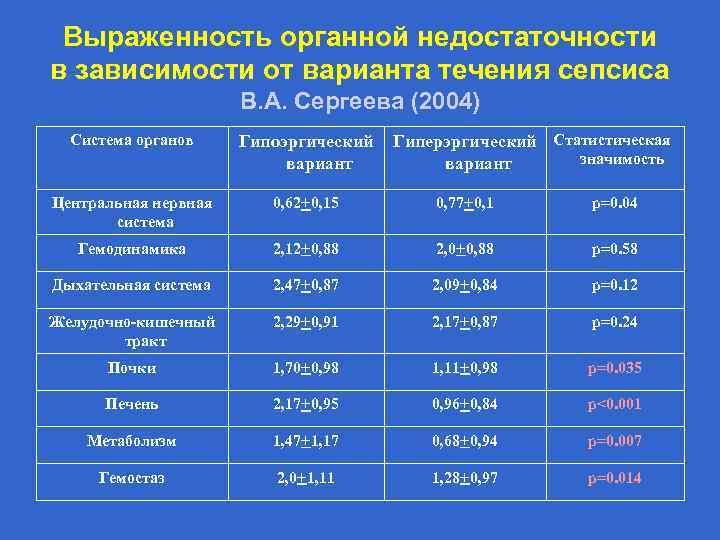
Выраженность органной недостаточности в зависимости от варианта течения сепсиса В. А. Сергеева (2004) Система органов Гипоэргический вариант Гиперэргический Статистическая значимость вариант Центральная нервная система 0, 62+0, 15 0, 77+0, 1 р=0. 04 Гемодинамика 2, 12+0, 88 2, 0+0, 88 р=0. 58 Дыхательная система 2, 47+0, 87 2, 09+0, 84 р=0. 12 Желудочно-кишечный тракт 2, 29+0, 91 2, 17+0, 87 р=0. 24 Почки 1, 70+0, 98 1, 11+0, 98 p=0. 035 Печень 2, 17+0, 95 0, 96+0, 84 p<0. 001 Метаболизм 1, 47+1, 17 0, 68+0, 94 p=0. 007 Гемостаз 2, 0+1, 11 1, 28+0, 97 p=0. 014

Вывод повышение иммуносупрессорной активности сыворотки крови не только определяет более раннее начало сепсиса и протекание его по гипоэргическому типу, но и обусловливает более тяжёлое течение полиорганной недостаточности у новорождённых детей.







Лечение «Делаются понятными основные принципы лечения. Они основаны на мероприятиях против возбудителей сепсиса и на мероприятиях, направленных на повышение резистентности, на выработку естественных защитных сил» . Маслов М. С. , 1959
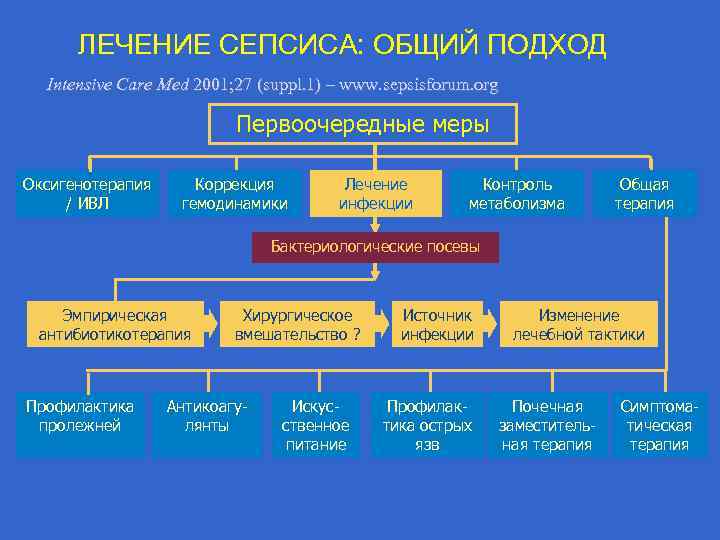
ЛЕЧЕНИЕ СЕПСИСА: ОБЩИЙ ПОДХОД Intensive Care Med 2001; 27 (suppl. 1) – www. sepsisforum. org Первоочередные меры Oксигенотерапия / ИВЛ Коррекция гемодинамики Лечение инфекции Контроль метаболизма Общая терапия Бактериологические посевы Эмпирическая антибиотикотерапия Профилактика пролежней Хирургическое вмешательство ? Антикоагулянты Искусственное питание Источник инфекции Профилактика острых язв Изменение лечебной тактики Почечная заместительная терапия Симптоматическая терапия

Сепсис: санация очага инфекции Intensive Care Med 2001: 27 (suppl. 1) – www. sepsisforum. org Сrit Care Med 2004; 32: 858 -873 • Диагностика очага инфекции – роль УЗИ, КТ, других методов • Дренирование очага инфекции • Некрэктомия, удаление инородного тела • Хирургическое вмешательство при очаге инфекции в полом органе - ушивание - удаление - выведение стомы

Сепсис: aнтибиотики ( «Сепсис в начале XXI века» //под ред. В. С. Савельева и Б. Р. Гельфанда, Litterra, 2006) • Ранняя адекватная эмпирическая антибактериальная терапия сепсиса приводит к снижению летальности и частоты осложнений как при грамотрицательной так и грамположительной, грибковой этиологии (уровень доказательности С)

Сепсис: aнтибиотики Intensive Care Med 2001: 27 (suppl. 1) – www. sepsisforum. org Сrit Care Med 2004; 32: 858 -873 • Контроль посевов! Посев крови до антибиотикотерапии - минимум 2 раза с интервалом 10 -15 минут • Эмпирическая а/б терапия в течение 1 ч после постановки диагноза: - β-лактам+аминогликозид - в том числе - карбоксипенициллины уреидопенициллины+ингибиторы β-лактамазы или - цефалоспорины 3 -4 поколения - карбапенемы +аминогликозид

Антибиотикотерапия • Антибактериальная схема должна быть оценена после 48– 72 часов терапии на основе микробиологических и клинических данных с целью использования антибиотиков узкого спектра для предотвращения развития резистентности, а также для снижения токсичности и материальных затрат. • В типичных случаях продолжительность антибиотикотерапии составляет 10 -14 дней и определяется клиническим и лабораторным ответом пациента.

Сепсис: aнтибиотики Intensive Care Med 2001: 27 (suppl. 1) – www. sepsisforum. org • Грам (-) инфекция - β-лактам+аминогликозид - карбапенем - фторхинолоны - азтреонам • Анаэробная флора: метронидазол • MRSA и катетер-зависимый сепсис: ванкомицин, тейкопланин, линезолид, стрептограмин

Сепсис: aнтибиотики Intensive Care Med 2001: 27 (suppl. 1) – www. sepsisforum. org • Грибковая инфекция: флюконазол/каспофунгин или амфотерицин • Избегать эмпирического применения гликопептидов и флюконазола • Деэскалационная терапия • Ротация антибиотиков ? • Cелективная деконтаминация кишечника (? ) - при абдоминальном сепсисе

Де-Эскалационная антибиотикотерапия • термин возникший на рубеже веков предполагающий выбор при стартовой антиинфекционной терапии госпитальных инфекций (в частности при ВАП) наиболее мощного и эффективного антибиотика с последующим переходом на антибиотик более узкого спектра действия в зависимости от вида и чувствительности выделенного возбудителя. Наиболее подходящими для такой цели являются карбапенемы - имипенем/циластатин (Тиенам Примаксин) и меропенем (Меронем). В связи с рядом фармакокинетических факторов предпочтителен Тиенам. В тоже время к тиенаму резистентны некоторые метициллин-резистентные стафилококки энтерококки стрептококки В и синегнойные палочки а потому шаблонное назначение его как антибиотика первого ряда при ВАП не всегда целесообразно. Кроме того у больных леченных этим антибиотиком нередко развиваются перекрестные инфекции в частности у примерно 16% кандидозы и другие микозы.

• Другим вариантом стартовой де-эскалационной терапии при ВАП является назначение цефалоспоринов III поколения (обычно - цефтазидим) или IV поколения (обычно - цефепим) в сочетании с такими аминогликозидами как амикацин и нетилмицин или ванкомицином. Лишь при ВАП вызванной энтеробактерами рекомендуют стартовать с фторхинолонов и/или карбапеномов. В настоящее время у больных новорожденных с инфекциями и любыми проблемами с животом (вздутие отечность передней брюшной стенки диарея и т. д. ) к стартовой антибиотикотерапии принято добавлять метронидазол • Третьим вариантом стартовой де-эскалационной терапии является комбинация пиперациллина/тазобактама (Тазоцин) с аминогликозидом или ванкомицином 75 мг/кг каждые 12 часов в первую неделю жизни и каждые 8 часов позднее
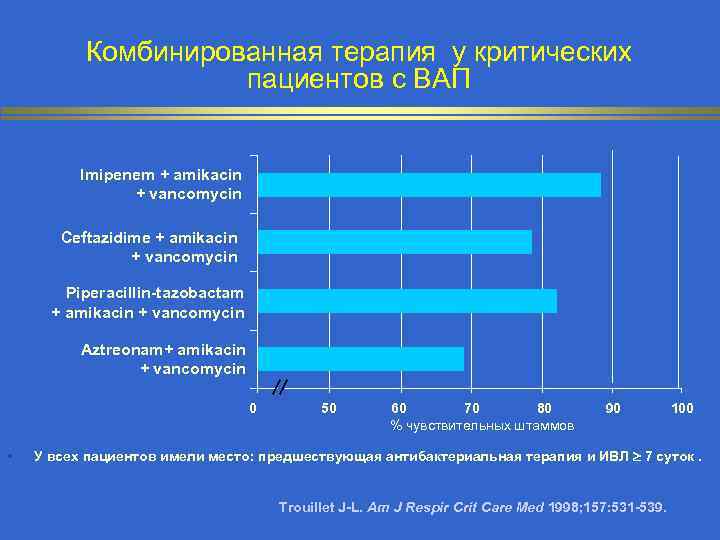
Комбинированная терапия у критических пациентов с ВАП Imipenem + amikacin + vancomycin Ceftazidime + amikacin + vancomycin Piperacillin-tazobactam + amikacin + vancomycin Aztreonam+ amikacin + vancomycin 0 • 50 60 70 80 % чувствительных штаммов 90 100 У всех пациентов имели место: предшествующая антибактериальная терапия и ИВЛ 7 суток. Trouillet J-L. Am J Respir Crit Care Med 1998; 157: 531 -539.

Проблемные микроорганизмы для действия имипенема: ØMRSA – метициллин-резистентные стафилококки ØPseudomonas aeruginosa (обычно, резистентность приобретается в процесса лечения и по данным С. Н. Козлова в 1999 году в России 20% штаммов Р. aeruginosa отделений интенсивной терапии были устойчивы к имипенему) ØXanthomonas (Pseudomonas maltophilia, некоторых штаммов cepacia) ØEnterococcus faecium (streptococcus faecium), резистентные к ампициллину ØStenotrophomonas maltophilia ØLegionella spp. ØChlamydia spp. ØM. pneumoniae Для устойчивых микроорганизмов (кроме Р. aeruginosa) характерна перекрестная резистентность к имипенему и меропенему.

Режимы дозирования аминогликозидов у новорожденных (ритм и дозы* в мг/кг) (Американская академия педиатрии Red book 27 издание 2006) Антибиотик Путь введени я Дети 0 -4 недель Дети первой недели жизни Дети 7 дней и старше Масса тела менее 1200 г Масса тела 1200 – 2000 г Масса тела более 2000 г Масса тела 1200 – 2000 более 2000 г г Амикацин В/В В/М 7 5 каждые 1824 часа 7 5 каждые 12 часов 7 5 -10 каждые 8 или 12 часов 10 каждые 8 часов Гентамицин В/В В/М 2 5 каждые 1824 часа 2 5 каждые 12 часов 2 5 каждые 8 или 12 часов 2 5 каждые 8 часов Тобрамицин В/В В/М 2 5 каждые 1824 часа 2 5 каждые 12 часов 2 5 каждые 8 или 12 часов 2 5 каждые 8 часов Неомицин Только er p os 25 каждые часов 25 каждые 6 часов … 6

• В 90 х годах установлено что однократно введенные в суточной дозе аминогликозиды обладают хорошим терапевтическим эффектом. В 10 -м издании неонатальной фармакопеи Англии (“Neonatal formulary” BMJ Books 1998 – русский перевод: “Современная терапия в неонатологии” - М. МЕДпресс 2000 - СНТ) рекомендуют начинать терапию новорожденных гентамицином или тобрамицином с 5 мг/кг (нетилмицин - 6 мг/кг) вводимыми внутривенно или внутримышечно каждые 24 часа. Если минимальная концентрация препарата после третьего введения превышает 2 мг/л интервал введения должен быть увеличен до 36 ч. Концентрация препарата проверяться после введения второй дозы. Детям более 2 мес. некоторые клиницисты предпочитают назначать гентамицин и тобрамицин в начале в нагрузочной дозе 5 мг/кг (нетилмицин - 6 мг/кг) внутривенно или внутримышечно с последующим введением 3 5 мг/кг (нетилмицин - 4 мг/кг) каждые 12 ч. В этом же издании рекомендуют амикацин новорожденным назначать по 15 мг/кг внутримышечно или внутривенно каждые 24 часа (интервал увеличивают до 36 часов если после 2 -го введения концентрация амикацина в крови более 5 мг/л) и у детей старше 2 мес. – нагрузочная доза - та же и, далее, каждые 12 часов - по 10 мг/кг. )

Документы, которыми надо руководствоваться

Документы, которыми надо руководствоваться
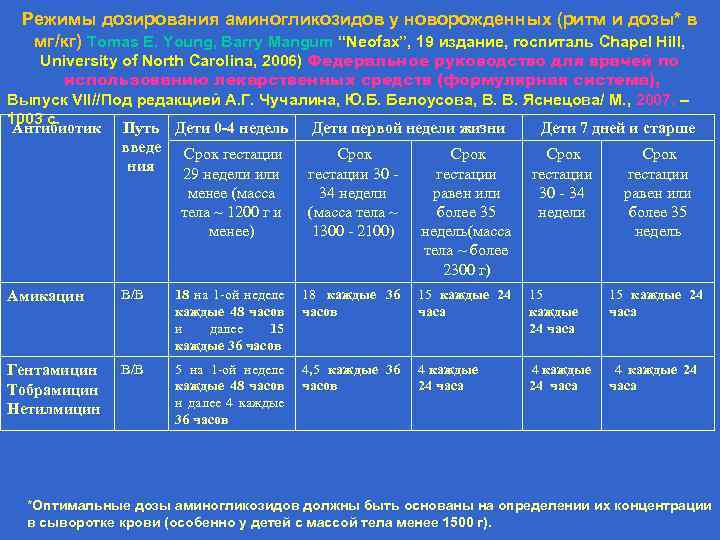
Режимы дозирования аминогликозидов у новорожденных (ритм и дозы* в мг/кг) Tomas E. Young, Barry Mangum “Neofax”, 19 издание, госпиталь Chapel Hill, University of North Carolina, 2006) Федеральное руководство для врачей по использованию лекарственных средств (формулярная система), Выпуск VII//Под редакцией А. Г. Чучалина, Ю. Б. Белоусова, В. В. Яснецова/ М. , 2007. – 1003 с. Антибиотик Путь Дети 0 -4 недель Дети первой недели жизни Дети 7 дней и старше введе Срок гестации Срок ния 29 недели или гестации 30 - гестации менее (масса тела ~ 1200 г и менее) 34 недели (масса тела ~ 1300 - 2100) равен или более 35 недель(масса тела ~ более 2300 г) 30 - 34 недели равен или более 35 недель Амикацин В/В 18 на 1 -ой неделе каждые 48 часов и далее 15 каждые 36 часов 18 каждые 36 часов 15 каждые 24 часа Гентамицин Тобрамицин Нетилмицин В/В 5 на 1 -ой неделе каждые 48 часов и далее 4 каждые 36 часов 4 5 каждые 36 часов 4 каждые 24 часа *Оптимальные дозы аминогликозидов должны быть основаны на определении их концентрации в сыворотке крови (особенно у детей с массой тела менее 1500 г).
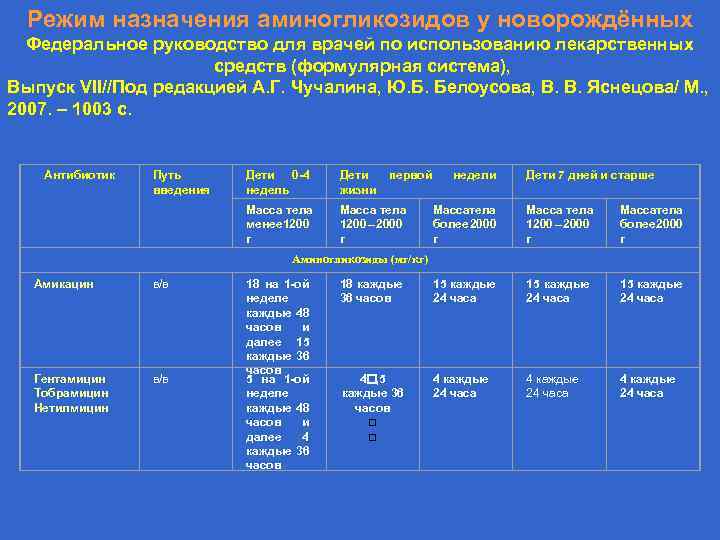
Режим назначения аминогликозидов у новорождённых Федеральное руководство для врачей по использованию лекарственных средств (формулярная система), Выпуск VII//Под редакцией А. Г. Чучалина, Ю. Б. Белоусова, В. В. Яснецова/ М. , 2007. – 1003 с. Антибиотик Путь введения Дети 0 -4 недель Дети жизни первой Масса тела менее 200 1 г Масса тела 1200 – 2000 г недели Дети 7 дней и старше Масса ела т более 000 2 г Масса тела 1200 – 2000 г Масса ела т более 000 2 г 18 каждые 36 часов 15 каждые 24 часа 4 , 5 каждые 36 часов 4 каждые 24 часа Аминогликозиды (мг/кг) Амикацин в/в Гентамицин Тобрамицин Нетилмицин в/в 18 на 1 -ой неделе каждые 48 часов и далее 15 каждые 36 часов 5 на 1 -ой неделе каждые 48 часов и далее 4 каждые 36 часов

ПРИНЦИПЫ ТЕРАПИИ ШОКА (зависят от этиологии и патогенетического варианта ШОКА) • • Восстановление ОЦК Обеспечение легочной вентиляции Коррекция ацидоза Восстановление адекватных: гемостаза, гемореологии и микроциркуляции Подержание сердечной деятельности Восстановление функции почек Стабилизация клеточных мембран Энергообеспечение

СЕПСИС: ЦЕЛИ ИНФУЗИОННОЙ ТЕРАПИИ • Общая цель: улучшение транспорта кислорода, том числе за счет улучшения реологических свойств крови, и его утилизации тканями • Гемодинамическая поддержка при низком АКД – допамин и/или норадреналин при низком сердечном индексе - добутамин (категория доказательности В и С) • Кристаллоиды – коррекция водноэлектролитного баланса • Коллоиды – объемозамещение

Сепсис: инфузионная терапия Intensive Care Med 2001: 27 (suppl. 1) – www. sepsisforum. org Сrit Care Med 2004; 32: S 451 -S 455 Опасности кристаллоидов: • Гиперволемия – перегрузка миокарда, гипергидратация малого круга кровообращения • Тканевой отек • Угнетение иммунитета • Гиперхлоремический ацидоз – Na. Cl • Гипоосмолярность – раствор Рингера • Нарушения микроциркуляции – гиперкоагуляция, энтеропатия и др.

Сепсис: инфузионная терапия Коллоиды • Желатины - аллергические реакции, короткое действие • Декстраны – аллергические реакции, влияние на гемостаз • Альбумин – высокая стоимость, клиническая эффективность (? ) • Гидроксиэтилкрахмалы

Сепсис: инфузионная терапия (Ю. С. Александрович и В. И. Гордеев, 2006) Преимущества гидроксиэтилкрахмалов при сепсисе: • Эффективное объемозамещение • Снижение количества побочных эффектов (гемостаз, аллергия) • Улучшение микроциркуляции • Уменьшение активации эндотелия • Уменьшение капиллярной утечки

Растворы гидроксиэтилкрахмалов (ГЭК) (Ю. С. Александрович и В. И. Гордеев, 2006) Показатель ГЭК 450/0. 7 ГЭК 200/0. 5 ГЭК 130/0. 4 Вязкость плазмы Агрегация эритроцитов Влияние на коагуляцию ++ + +/- Накопление в плазме и РЭС ++ + - Влияние на почки + +/- - Улучшение микроциркуляции - + ++

ОТЛИЧИТЕЛЬНЫE ОСОБЕННОСТИ ВОЛЮВЕНА (Ю. С. Александрович и В. И. Гордеев, 2006) 1 Существенно снижено влияние на коагуляцию по сравнению с ГЭК 200/0, 5 (ХАЕС-стерил, Рефортан, Инфукол, Гемохес) и ГЭК 450/0. 7 (Стабизол). 1 Значительно меньшее влияние на уровень VIII фактора свертывания крови и фактор Виллебранда. 1 Значительно снижено накопление в тканях (до 75%) по сравнению с ГЭК 200/0, 5. 1 Отсутствие кумуляция в плазме – даже после повторных введений свыше 10 дней. 1 Молекулярный вес выше почечного порога. 1 Волемический эффект 100%. 1 Эффект плато - 4 часов. 1 Клинически значимая волемическая стабилизация до 6 часов (волемический эффект сравним с ГЭК 200/0, 5).

СТАРТОВАЯ ИНФУЗИОННАЯ ТЕРАПИЯ (Ю. С. Александрович и В. И. Гордеев, 2006) Инфузионная терапия начинается немедленно после постановки диагноза и не откладывается до поступления в отделение интенсивной терапии. У детей инфузию жидкости рекомендуется начинать в виде болюсов из расчета 20 мл/кг за 5 -10 минут, под контролем мониторинга сердечного выброса (реографический мониторинг гемодинамики, оценка пульсового давления), ЧСС, диуреза, времени наполнения капилляров и уровня сознания. В типичных случаях, у детей с тяжелым сепсисом и септическим шоком имеется выраженный дефицит жидкости, и для адекватной начальной инфузионной терапии может потребоваться объем 40– 60 мл/кг/час и больше (Carcillo J. A. et al. , 1991; Ceneviva G. et al. 1988).

Парэнтеральное питание в педиатрии. Особенности метаболизма - Очень ограниченные запасы энергии, особенно у недоношенных новорожденных - «Неразвитость» путей метаболизма аминокислот и ферментных систем (фенилаланин-гидроксилаза, цистатионаза) - Высокая потребность в нутриентах, в том числе для обеспечения роста и развития - Даже кратковременное голодание может нарушить развитие мозга и снижение интеллектуальных способностей с будущем (ASPEN, 2001) - Больше незаменимых аминокислот – тирозин, цистеин, пролин, глицин незаменимы у детей - Потребность в таурине |Am J Perinatol, 2001
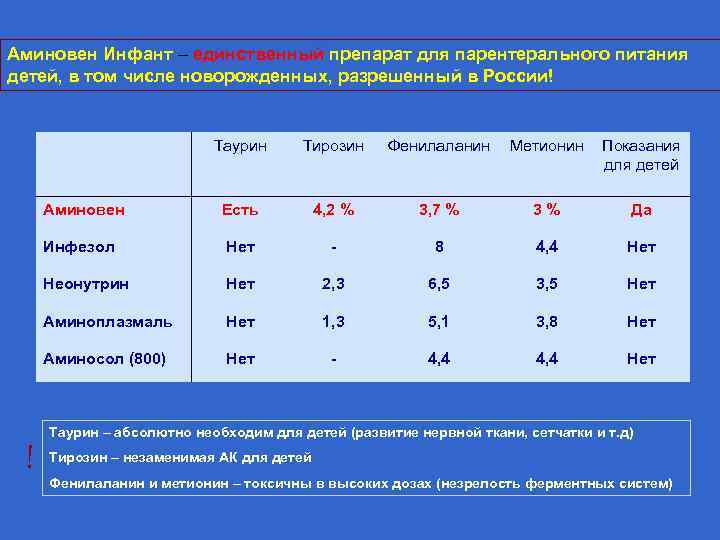
Аминовен Инфант – единственный препарат для парентерального питания детей, в том числе новорожденных, разрешенный в России! Таурин Тирозин Фенилаланин Метионин Показания для детей Аминовен Есть 4, 2 % 3, 7 % 3 % Да Инфезол Нет - 8 4, 4 Нет Неонутрин Нет 2, 3 6, 5 3, 5 Нет Аминоплазмаль Нет 1, 3 5, 1 3, 8 Нет Аминосол (800) Нет - 4, 4 Нет Таурин – абсолютно необходим для детей (развитие нервной ткани, сетчатки и т. д) ! Тирозин – незаменимая АК для детей Фенилаланин и метионин – токсичны в высоких дозах (незрелость ферментных систем)

ЖИРОВЫЕ ЭМУЛЬСИИ ЛИПОВЕНОЗ 10%, 20% - (Fresenius Kabi) ИНТРАЛИПИД 10%, 20% - (Fresenius Kabi)

Вазопрессоры и инотропная терапия Добутамин – инотроп выбора при лечении пациентов с подтвержденным или подозреваемым низким минутным сердечным выбросом при наличии адекватного давления наполнения в левом желудочке (или клиническом подтверждении адекватности инфузионной терапии) и адекватном среднем артериальном давлении. Стартовая доза добутамина составляет 2, 0 -5, 0 мкг/кг/мин. Комбинированное использование вазопрессора адреналина (стартовая доза 0, 03 -0, 1 мкг/кг/мин) и инотропного препарата добутамина показано для раздельного поддержания среднего артериального давления и минутного сердечного выброса в требуемых пределах.

Сепсис: контроль метаболизма Van den Berghe G et al. NEJM 2001; 345: 1359 -1367 Hotchkiss RS et al. NEJM 2003; 348: 138 -150 • Устранение метаболического ацидоза Не использовать бикарбонат при р. Н>7, 25 • Коррекция электролитных нарушений • Коррекция гипергликемии - поддержание глюкозы крови 4, 4 -6, 1 ммоль/л - инсулин снижает частоту инфекционных осложнений, так как улучшает фагоцитоз и предотвращает апоптоз клеток (категория доказательности С) ( «Сепсис в начале XXI века» //под ред. В. С. Савельева и Б. Р. Гельфанда, Litterra, 2006)

Критериями эффективности интенсивной терапии (Ю. С. Александрович и В. И. Гордеев, 2006) нормальный психический статус, · время наполнения капилляров 2 секунды и меньше, · нормальный пульс без различий между периферическим и центральным пульсом, · теплые конечности, · диурез > 1 мл на кг в час, · сниженние уровня лактата и дефицит оснований (ВЕ), · смешанная венозная сатурация кислорода или верхней полой вены > 70%. ·

СТЕРОИДЫ (Ю. С. Александрович и В. И. Гордеев, 2006) При отсутствии шока не следует назначать кортикостероиды для лечения сепсиса. Терапия гидрокортизоном показана детям с катехоламиновой резистентностью и подозреваемой или подтвержденной надпочечниковой недостаточностью. Стероиды показаны при тяжелом СШ и менингококцемии, а также детям, которые получали до этого стероидную терапию по поводу хронических болезней и детям с патологией гипофиза или надпочечников (категория доказательности В) ( «Сепсис в начале XXI века» //под ред. В. С. Савельева и Б. Р. Гельфанда, Litterra, 2006). Нет строгих рекомендаций, но предполагается, что надпочечниковая недостаточность в случае катехоламин-резистентного СШ возникает при концентрации кортизола <18µg/дл (496 нмоль/л). Рекомендации по дозе варьируют от 1 -2 мг/кг для однократного болюсного введения (основываясь на клиническом диагнозе надпочечниковой недостаточности) до 50 мг/кг/24 часа в виде постоянной инфузии (при эмпирической терапии шока).

Терапия сепсиса: дополнительные компоненты (? ) Intensive Care Med 2001: 27 (suppl. 1) – www. sepsisforum. org Сrit Care Med 2004; 32: 858 -873 • Глюкокортикоиды - При рефрактерном септическом шоке и адреналовой недостаточности (до 60% больных с СШ) - в течение 5 -7 сут. гидрокортизон 200 -300 мг/сут в/в - В фибропролиферативную фазу ОРДС - метилпреднизолон, начиная с 2 мг/кг

Назначение препаратов крови • Концентрацию гемоглобина у детей с тяжелым сепсисом и септическим шоком необходимо поддерживать в нормальных возрастных пределах (> либо = 10 г/дл. [100 г/л]). • Не рекомендуется рутинное использование свежезамороженной плазмы для коррекции патологии свертывания при отсутствии кровотечения или планируемых инвазивных процедур.

Риск инфицирования при переливании компонентов крови в России (В. Покровский, Е. Селиванов, Ю. Суханов, В. Максимов, 2006) • 1 случай гепатита В на 5 000 трансфузий • 1 случай гепатита С на 2 000 трансфузий • 1 случай ВИЧ-инфицирования на 600 000 Ориентировочно ежегодно переливается 7 млн. доз компонентов крови, следовательно, число заболевших ежегодно составляет: • Гепатит В – 1400 • Гепатит С – 3500 • ВИЧ-инфекция – 12 человек Суммарные затраты на лечение посттрансфузионных инфекций составляют 133, 4 млн. $

Искусственная вентиляция при сепсисиндуцированном остром легочном повреждении (ОЛП)/ остром респираторном дистресс синдроме (ОРДС) При ОЛП/ОРДС использование высоких дыхательных объемов, ассоциированных с высоким давлением плато не рекомендуется. Высокое давление на вдохе может быть снижено посредством снижения дыхательного объема до 6 мл/кг (ранее рекомендовалось до 12 мл/кг) при давлении плато < 30 cm водного столба (Amato M. B. et al. , 1998). Рекомендуется, ребенка нуждающегося в потенциально «вредных» уровнях Fi. O 2 переворачивать на живот (на 7 часов в день), так как было показано, что большинство пациентов с ОЛП/ОРДС реагируют на положение на животе улучшением оксигенации (Gatinoni L. et al. , 2001).

Терапия сепсиса: дополнительные компоненты (? ) Intensive Care Med 2001: 27 (suppl. 1) – www. sepsisforum. org Сrit Care Med 2004; 32: 858 -873 • Антицитокиновая терапия: антитела и рецепторы к LРS, TNF, IL - не улучшают исход • Аналоги L-аргинина - не улучшают исход • Метиленовый синий 2 мг/кг в/в: ингибирует NOS и гуанилатциклазу, уменьшает вазодилатацию и депрессию миокарда • Вазопрессин 0, 01 -0, 04 ЕД/мин в/в: уменьшает вазодилатацию, но может снизить ударный объем и сердечный выброс

Терапия сепсиса: дополнительные компоненты (? ) Intensive Care Med 2001: 27 (suppl. 1) – www. sepsisforum. org Сrit Care Med 2004; 32: 858 -873 • Антимедиаторная терапия - НПВП – ибупрофен и др. - пентоксифиллин (трентал) , лизофиллин улучшают реологические свойства крови - ингибиторы избыточного ПОЛ - вит. С, Е, ацетилцистеин - антитромбин III - антагонисты рецепторов к эндотелину - активированный протеин С

Терапия сепсиса: дополнительные компоненты Сrit Care Med 2004; 32: S 534 -S 541 Активированный протеин С (АПС, дротрекогин, Зигрис) – снижение летальности на 6, 1% Эффекты: • антикоагулянтный • профибринолитический • противовоспалительный Постоянная инфузия 24 мкг/кг/ч – 4 сут. Показан при дисфункции > 2 органов Введение АПС в дозе 24 мкг/кг/час в течение 96 часов снижает риск летального исхода на 19, 4% - категория доказательности А ( «Сепсис в начале XXI века» //под ред. В. С. Савельева и Б. Р. Гельфанда, Litterra, 2006)

Лечение «Можно ли одними антибиотиками вылечить ребенка от сепсиса? На это можно дать совершенно четкий ответ-нельзя. Сепсис - это заболевание, вызванное микробом, но в организме с измененной реактивностью. Поэтому совершенно необходимо применение средств и мероприятий, повышающих естественную резистентность организма, вызывающих к жизни защитные силы» . Маслов М. С. , 1959

ИММУНОМОДУЛИРУЮЩАЯ ТЕРАПИЯ Данных об эффективности иммуномодулирующей терапии, подтвержденных рандомизированными клиническими исследованиями немного. Так, сообщается, что поликлональный внутривенный иммуноглобулин уменьшает частоту смертности и является перспективным адъювантом в лечении сепсиса и септического шока. В тоже время, нет убедительных данных об эффективности такой терапии у детей. Вспомогательная терапия моноклональными внутривенными иммуноглобулинами остается экспериментальной (Alejandria M. M. et al. , 2002). Раннее применение Пентаглобина в дозе 5 мл/кг в течение 3 -х дней подряд повышает выживаемость при сепсисе – категория доказательности А ( «Сепсис в начале XXI века» //под ред. В. С. Савельева и Б. Р. Гельфанда, Litterra, 2006)

В Red book (27 издание, 2006) указано: «Результаты большинства клинических испытаний указывают, что использование внутривенных иммуноглобулинов не снижает частоту или смертность от поздно начинающихся инфекций у детей с массой тела при рождении менее 1500 г. В настоящее время внутривенные иммуноглобулины не рекомендованы для рутинного введения с целью предотвращения поздно начинающихся инфекций у недоношенных детей» .

Пентаглобин обеспечивает не только специфический пассивный иммунитет (прежде всего к граммотрицательным бактериям), но за счет повышенного содержания Ig. M неспецифически активирует фагоцитоз (в 1000 раз активнее чем Ig. G), Т-лимфоциты хелперы (амплифаеры - усилители), имеющие рецептор FcμR, со всеми последствиями для продукции цитокинов. Кроме того, Ig. M лучше других классов ИГ активирует систему комплемента по классическому пути и обладает, таким образом, наибольшей комплементопосредованной цитотоксической активностью. Как пентамер, он наиболее активно агглютинирует бактерии - одна молекула Ig. M способна уничтожить одну бактерию, но для этого необходимо 2000 молекул Ig. G. Эти свойства пентаглобина одновременно с терапевтическим эффектом служат и профилактике ИДС, т. е. препятствуют присоединению оппортунистических возбудителей. Показания для назначения пентаглобина (РАСПМ, 2001): - Тяжелые бактериальные инфекции. - Сепсис - Профилактика инфекций у больных с ИДС и высоким риском гнойносептических заболеваний, например, после обширных хирургических операций и у детей с ОНМТ, находящихся в критическом состоянии. - Заместительная терапия при первичных и вторичных ИДС. Дозировка новорожденным: 5 мл/кг массы тела в сутки дней, вводить с помощью инфузионного насоса со скоростью не более 1, 7 мл/кг/час. Назначают ежедневно в течение 3 -х дней подряд. Форма выпуска: 5% раствор в ампулах по 10 мл и 20 мл. флаконах по 100 мл.
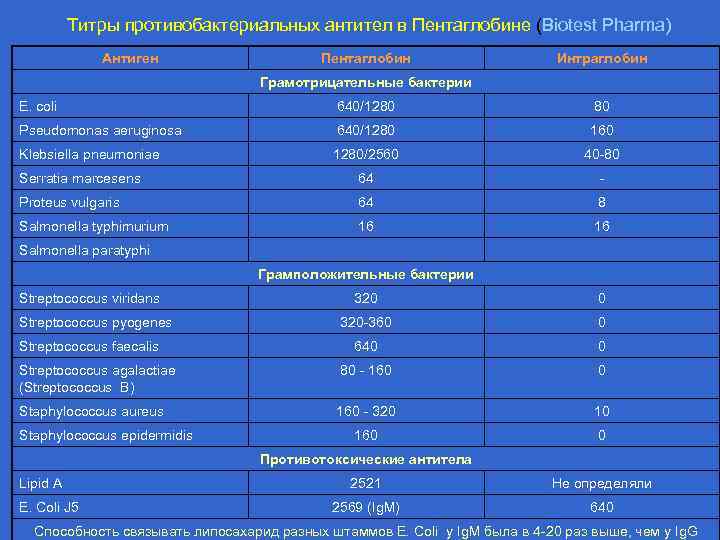
Титры противобактериальных антител в Пентаглобине (Biotest Pharma) Антиген Пентаглобин Интраглобин Грамотрицательные бактерии E. coli 640/1280 80 Pseudomonas aeruginosa 640/1280 160 Klebsiella pneumoniae 1280/2560 40 -80 Serratia marcesens 64 - Proteus vulgaris 64 8 Salmonella typhimurium 16 16 Salmonella paratyphi Грамположительные бактерии Streptococcus viridans 320 0 320 -360 0 640 0 Streptococcus agalactiae (Streptococcus B) 80 - 160 0 Staphylococcus aureus 160 - 320 10 160 0 Streptococcus pyogenes Streptococcus faecalis Staphylococcus epidermidis Противотоксические антитела Lipid A E. Coli J 5 2521 Не определяли 2569 (Ig. M) 640 Способность связывать липосахарид разных штаммов E. Coli у Ig. M была в 4 -20 раз выше, чем у Ig. G

Титры антител в Пентаглобине • Пентаглобин содержит более высокие концентрации антител против основных неонатальных бактериальных патогенов по сравнению со стандартными ИГВВ. Например, содержание антител против эндотоксина E. Coli G 5 в Пентаглобине составляет 2560 Ед по гемаагглютининовому тесту, а в стандартных ИГВВ – 640 Ед. • В Пентаглобине находятся в высоких титрах нейтрализующие антитела к вирусам группы герпеса (1: 42 200), вирусу Эпштейна-Барра (1: 286), вирусу краснухи (1: 128), парвовирусу в 19 (1: 1000), вирусам парагриппа 1, 2, 3 типов, ветряной оспы, вируса Коксаки I-V, вирусам полиомиелита 1, 2, 3 типов, адоновирсам, вируса гепатита А и В, к вирусу цитомегалии (15 -20 Ед/мл, в Нео. Цитотекте – 100 Ед/мл) и др. «Формуляр по использованию препаратов иммуноглобулинов для внутривенного введения в неонатологии» , РАСПМ, 2006

Мета-анализ эффективности внутривенных иммуноглобулинов у критически больных взрослых с сепсисом (A. F. Turgeon et al. , Ann. Intern. med. , 6 February 2007) Мета-анализ 20 рандомизированных исследований, влючивших 2621 больного с сепсисом показал, использование в терапии больных с сепсисом поликлональных внутривенных иммуноглобулинов достоверно снижает летальность (ОР = 0, 64) что зависит от дозы (оптимально 1 г/кг) и длительности применения (более 2 -х дней)и , как было показано при предыдущем анализе (Cochrane Review, February 2005), терапия Пентаглобином оказалась более эффективной в плане снижения летальности (ОР = 0, 48), что свидетельствует об увеличении шансов выжить при септическом шоке в 2 раза.

Применение Пентаглобина при сепсисе у детей (El-Nawawy et al. , 2005) Применение Пентаглобина при сепсисе у 100 детей в рамках проспективного рандомизированного исследования сопровождалось снижением летальности с 56 до 28%, сокращением длительности пребывания в ОРИТ с 9, 1 до 6, 1 суток, а также снижением частоты развития частоты осложнений, в том числе ДВС-синдрома с 24 до 4%. (цит. по Н. В. Белобородовой и Д. А. Попову, Анестезиология и реаниматология № 6, 2006)

Сравнение двух типов иммуноглобулинов в лечении сепсиса у недоношенных новорождённых (проспективное, рандомизированное с исторической контрольной группой – Haque K. H. et al. , 1995) Летальность: • Пентаглобин – 6, 8% • Интраглобин – 15, 8% • Группа сравнения – 21, 8% • Пентаглобин – 65 детей • Интраглобин – 65 детей • Группа сравнения - • Диагноз сепсиса 65 детей • Дозировка: 250 мг/кг (5 мл/кг) в течение 3 -4 часов 4 дня подряд подтвержден лабораторными параметрами и положительной культурой крови

Пентаглобин в лечении сепсиса у недоношенных новорождённых (проспективное, рандомизированное плацебоконтролируемое – Hellwege H. H. et al. , 1997) Летальность: • Пентаглобин – 44 • Пентаглобин – ребенка 3, 1% • Группа сравнения - • Группа 44 ребенка сравнения – 21, 9% • Дозировка: 5 мл/кг в течение 3 часов 4 дня подряд

Показания к назначению Пентаглобина у новорождённых • Тяжелые инфекции бактериальной, вирусной и смешанной этиологии. • Сепсис у новорожденных и детей раннего возраста. • Профилактика инфекций у больных с иммунодефицитными состояниями и высоким риском развития гнойно-септических заболеваний. • Заместительная терапия при первичных и вторичных иммунодефицитах. «Формуляр по использованию препаратов иммуноглобулинов для внутривенного введения в неонатологии» , РАСПМ, 2006

Пентаглобин – золотой стандарт лечения при сепсисе и септическом шоке Пентаглобин является единственным ВВИГ, эффективность которого в плане снижения летальности при сепсисе и септическом шоке подтверждена с позиций доказательной медицины (надежность доказательств – категория Ia, рекомендации – категория А). Обоснованность включения Пентаглобина в комплексную терапию пациентов с сепсисом и септическим шоком подтверждена данными метаанализа, проведенного группой независимых ученых Соchrane Infection Disease Group, указавшей что это снижает летальность в 2, 1 раза. (Alejandria M. M. et al. The Cochrane Library, 2005, Issure 3, Oxfort Update Software)

Согласно Н. В. Белобородовой (2006) частота инфекционных осложнений у детей после обширных хирургических вмешательств в связи с ВПС на фоне традиционной терапии была 43%, а при профилактическом введении Пентаглобина 5% (снижение в 8 раз!). В тоже время, рационально систематическое определение в крови концентрации ПСТ и при уровне его более 2 нг/мл применять Пентаглобин.

Экстракорпоральные методы детоксикации ( «Сепсис в начале XXI века» //под ред. В. С. Савельева и Б. Р. Гельфанда, Litterra, 2006) «В настоящее время отсутствуют контролируемые исследования, подтверждающие необходимость применения методов экстракорпорального очищения крови (гемодиализ, гемосорбция, плазмообмен – плазмаферез, плазмофильтрация) как одного из основных направлений патогенетической терапии сепсиса и септического шока. Использование их оправдано в случае развития полиорганной недостаточности с доминированием почечной недостаточности» .

Лечение различных вариантов сепсиса новорожденных Препараты Гипоэргический Гиперэргический Антибиотики Эффективны при рациональном выборе и максимальной дозе. Рано противогрибковые препараты Недостаточный эффект даже при рациональном выборе Интраглобин Положительный эффект дискуссионен Пентаглобин Показано раннее курсовое применение Может быть эффективен при раннем однократном применении Специфическая иммунотерапия Положительный эффект Недостаточный эффект Возможно ухудшение

Лечение различных вариантов сепсиса новорожденных Препараты Гипоэргический Гиперэргический Переливание свежей крови Положительный эффект Ухудшение Переливание Положительный Ухудшение нейтрофильной эффект массы Назначение GM-CSF Ухудшение Глюкокортикоиды Положительный эффект Ухудшение Плазмаферез Нет эффекта Эффект дискуссионен Антиагрегантная Нет эффекта Положительный терапия (трентал и др. ) или ухудшение эффект Положительный эффект в первые часы болезни

• В конце прошлого и начале нынешнего века появилось много иммуностимуляторов различного происхождения и механизма действия. В отечественной литературе есть работы, в которых сообщается о применении препаратов тимического происхождения, различных цитокинов при лечении новорожденных с инфекционной патологией. Например, о лечении отечественным рекомбинантным человеческим интерлейкином-2 ( «Ронколекин» ) новорожденных с сепсисом и лимфоцитопенией. Подчеркнем, что в зарубежной литературе таких работ нет.

По данным ВОЗ • иммуностимуляторы, относящиеся к тимическим факторам, такие как естественные (получаемых из зобной железы крупного рогатого скота) и синтетические (тимогены) запрещены к продаже в большинстве стран мира, из-за возможного риска развития бычьей губковидной энцефалопатии • использование левамизола ограничено из-за риска возникновения у пациентов агранулоцитоза World Health Organization. Fact Sheet 113. (accessed July 20, 2005) 2005

По разрешению Фармкомитета МЗСР Российскому медицинскому университету разрешено клиническое испытание применения у новорожденных отечественного препарата «Ронколейкин» (ИЛ-2) • ИЛ-2 стимулирует пролиферацию иммунокомпетентных клеток в сторону Th 1 лифоцитов, уменьшает апоптоз иммунокомпетентных клеток. • Согласно М. В. Дегтяревой ( 2006) показанием для применения у новорождённых Ронколейкина является абсолютная лимфоцитопения и внутривенное (2 -х кратное с интервалом 72 часа) введение его в дозе 50 -100 тыс. МЕ/кг (в изотоническом растворе натрия хлорида в течение 2 -х часов) привело к 2 -х кратному снижению летальности при неонатальном сепсисе (гипоэргическом) и в 3, 7 раза – при госпитальной пневмонии. • Р. Ханферян (2006) сочетал интратрахеальное (100000 МЕ)и парентеральное введение Ронколейкина с парентеральным и добился существенного снижения летальности при внутриутробной пневмонии.

• Мы с осторожностью относимся к этим рекомендациям и применяли в неонатальной клинике в комплексной терапии лишь Виферон. Согласно рекомендациям Г. М. Дементьевой, Виферон 1 (150 000 ЕД в свечах) назначали детям с сепсисом в период репарации дважды в сутки в течение 5 дней, затем делали 5 -дневный перерыв и повторяли 5 -дневный курс. Наше впечатление от терапии положительное.

• Другие интерфероны и интерлейкины мы не применяли, опасаясь как прямых, так и отдаленных побочных эффектов. Надо помнить, 3– 5% лимфоцитов у новорожденного – материнские, и потому, вводя новорожденному тимические препараты или интерлейкины, мы не можем гарантировать отсутствие стимуляции материнских лимфоцитов, для которых половина антигенов ребенка – чужие, отцовские (мужей по антигенам еще никто не выбирал!), а значит, и последствия такой терапии в катамнезе непредсказуемы. Вообще нам кажется роль материнских лимфоцитов, попавших к ребенку, до сих пор не изучена и, по нашему мнению, может быть очень велика, в частности при гиперергическом сепсисе, БЛД. Не стоит тормошить медведя в берлоге!

Профилактика «Особого внимания заслуживает организация профилактики сепсиса и септических состояний. Профилактика сепсиса у новорожденных и недоношенных детей является делом очень сложным. Она не дает эффекта, если применяют какое-либо одно новое мероприятие. Существующая система профилактики сепсиса в наших учреждениях основана на обязательном ношении халатов, обязательном тщательном мытье рук» Маслов М. С. , 1959.

Основные пути снижения частоты госпитальных инфекций • Мытье рук с использованием антисептических средств, одноразовые перчатки при работе с внутривенными линиями, интубационными трубками, катетерами • Использование одноразового материала • Централизованное приготовление инфузионных растворов и бактериальные фильтры • Рациональная обработка аппаратов для ИВЛ и кувезов • Рациональное применение антибиотиков • Обучение персонала (сестра-учитель!) • Эпидемиологический контроль: введение постоянного инфекционного контроля (внутренний противоинфекционный аудит)

Инфекционный контроль • Перчатки пластиковые • Жидкое бактерицидное мыло • Бумажные полотенца • Бактерицидные растворы для обработки рук • Мойте руки! • Мойте руки!

Инфекционный контроль При любых манипуляциях с повреждением кожных покровов интубациях установке зонда необходимо надеть одноразовые перчатки. Медицинским сестрам это по первоначалу кажется не удобным но надо внушать мысль – перчатки это не только защита ребенка от микробов взрослого но и защита медицинского работника от инфекционных агентов ребенка (что при наличии достаточно широкого распространения вирусов гепатита и ВИЧ – быстро усваивается персоналом). В отделениях патологии новорожденных Санкт-Петербурга над кроваткой больного гнойно-воспалительным заболеванием висит транспарант: «Осторожно!!! Я инфицирован! Пожалуйста оденьте перчатки!» .

Инфекционный контроль Централизованное приготовление инфузионных растворов • Нет разноса инфекции • Меньше трагических для больного ошибок в дозировке лекарств • Значительный экономический эффект • Персональная ответственность за хранение и расход медикаментов

Инфекционный контроль Оборудование аптеки • • Отдельное помещение Холодильник Вытяжной шкаф Сейф для хранения учетных препаратов • Полки для хранения инфузионных растворов • Бактерицидная лампа
Сепсис: профилактика инфекции • Одноразовые комплексы: дыхательные фильтры, контуры, эндотрахеальные и трахеостомические трубки

Сепсис: профилактика инфекции Закрытые аспирационные системы: • Санация трахеи без прерывания ИВЛ • Существенно снижается негативное влияние процедуры санации трахеи и риск осложнений
Сепсис: профилактика инфекции • Защитные фиксирующие наклейки для операционных ран, венозных, артериальных, эпидуральных катетеров

Перспективы повышения эффективности лечения госпитальных инфекций Директор НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи академик РАМН Александр Леонидович Гинцбург (МГ, № 62, 18. 8. 2006): «Феномен социального поведения бактерий (чувство кворума) был впервые обнаружен около 25 лет назад. Но то, что 99% бактерий существуют в природных экосистемах не в виде свободно плавающих клеток, а специфически организованных, прикрепленных к биосубстрату биопленок, стало известно лишь в последнее десятилетие минувшего века благодаря развитию и применению новых микробиологических и молекулярно-биологических методов исследования…С наличием биопленок связана множественная устойчивость к антибиотикам. Биопленки имеют такую структуру, что препараты просто не могут «добраться» до бактерий»

Перспективы повышения эффективности лечения госпитальных инфекций • «Появились сообщения о веществах, способных ингибировать синтез автоиндукторов (образования биопленок). Например, для P. aeruginosa в качестве таких ингибиторов названы различные аналоги Sаденозилметионина (гептрал), определенные макролидные антибиотики, применяемые в субминимальных концентрациях, эритромицин. Из окружающей среды выделены бактерии, способные вызывать деградацию молекул автоиндукторов или метаболизировать их. Могу сказать только, что методы, которые позволят разрушать биопленки, спасут миллионы жизней и сохранят громадные материальные средства. И сколько осталось ждать по вашим прогнозам? (вопрос корреспондента). Думаю, 2 -3 года, не больше»

Сепсис, 2008.Шабалов.ppt