Современные методы идентификации микроорганизмов



































































Современные методы идентификации микроорганизмов.ppt
- Количество слайдов: 68
 Современные методы идентификации микроорганизмов
Современные методы идентификации микроорганизмов
 ИММУНОФЕРМЕНТНЫЙ АНАЛИЗ: ПРИНЦИПЫ И ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ПРИМЕНЕНИЮ
ИММУНОФЕРМЕНТНЫЙ АНАЛИЗ: ПРИНЦИПЫ И ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ПРИМЕНЕНИЮ
 ПОКОЛЕНИЯ СЕРОЛОГИЧЕСКИХ РЕКЦИЙ 1. Преципитация в геле 2. Реакции агглютинации пластинчатые (кровяно капельная при туляремии, Хеддльсона при бруцеллезе реакции агглютинации развернутые (Видаля, Райта) реакции гемагглютаниции (РПГА+РНГА, РТПГА) Ко агглютинация латекс агглютинация 3. ИФА 4. Иммунохромотогафические реакции
ПОКОЛЕНИЯ СЕРОЛОГИЧЕСКИХ РЕКЦИЙ 1. Преципитация в геле 2. Реакции агглютинации пластинчатые (кровяно капельная при туляремии, Хеддльсона при бруцеллезе реакции агглютинации развернутые (Видаля, Райта) реакции гемагглютаниции (РПГА+РНГА, РТПГА) Ко агглютинация латекс агглютинация 3. ИФА 4. Иммунохромотогафические реакции
 Метод иммуноферментного анализа (ИФА) основывается на двух принципиальных научных открытиях. способность ферментов и антител или антигенов, прикрепленных к твердой основой ( т. ИФА ) , сохранять свою функциональную активность, т. е. ферменты могут расщеплять субстрат, антитела связывать антигены, а антигены – антитела. создании комплекса антитело фермент ( Аb F ) в виде конъюгата , сохраняющего свою биологическую активность в растворе. Аb F конъюгаты характеризуются высочайшей специфичностью и чувствительностью до 97 99%.
Метод иммуноферментного анализа (ИФА) основывается на двух принципиальных научных открытиях. способность ферментов и антител или антигенов, прикрепленных к твердой основой ( т. ИФА ) , сохранять свою функциональную активность, т. е. ферменты могут расщеплять субстрат, антитела связывать антигены, а антигены – антитела. создании комплекса антитело фермент ( Аb F ) в виде конъюгата , сохраняющего свою биологическую активность в растворе. Аb F конъюгаты характеризуются высочайшей специфичностью и чувствительностью до 97 99%.
 В настоящее время метод т. ИФА используется для определения широкого класса веществ: – гормонов, – онкомаркеров, – лекарственных препаратов в крови больного (так называемый, мониторинг лекарственных препаратов), – наркотиков, – бактерий, – вирусов и антител против них, – определение иммуноглобулинов (видовая принадлежность, субклассы, специфичность), а также идентификация лимфоцитов (субпопуляций).
В настоящее время метод т. ИФА используется для определения широкого класса веществ: – гормонов, – онкомаркеров, – лекарственных препаратов в крови больного (так называемый, мониторинг лекарственных препаратов), – наркотиков, – бактерий, – вирусов и антител против них, – определение иммуноглобулинов (видовая принадлежность, субклассы, специфичность), а также идентификация лимфоцитов (субпопуляций).
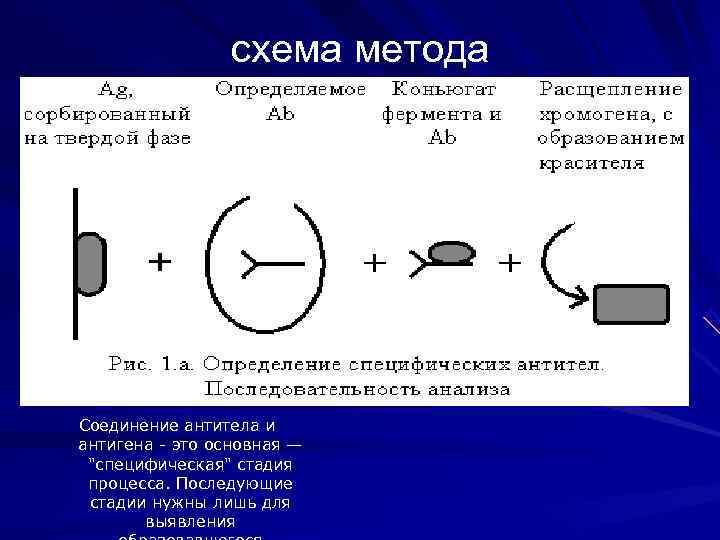
 схема метода Соединение антитела и антигена - это основная — "специфическая" стадия процесса. Последующие стадии нужны лишь для выявления
схема метода Соединение антитела и антигена - это основная — "специфическая" стадия процесса. Последующие стадии нужны лишь для выявления
 На второй стадии анализа в лунку вносят Ab с заранее прикрепленным к ним ферментом, способные связаться с Ab человека, закрепившимися на инфекционном агенте. Это так называемый конъюгат. Если в ячейке имеются образовавшиеся на первой стадии процесса иммунные комплексы, то возникает “молекулярная цепочка”, на конце которой находится фермент. На следующей стадии в лунку добавляется раствор бесцветного вещества — хромогена. Это вещество приобретает окраску после расщепления его присутствующим в ячейке ферментом То есть, если все элементы цепочки присутствуют, в лунке образуется окрашенный комплекс
На второй стадии анализа в лунку вносят Ab с заранее прикрепленным к ним ферментом, способные связаться с Ab человека, закрепившимися на инфекционном агенте. Это так называемый конъюгат. Если в ячейке имеются образовавшиеся на первой стадии процесса иммунные комплексы, то возникает “молекулярная цепочка”, на конце которой находится фермент. На следующей стадии в лунку добавляется раствор бесцветного вещества — хромогена. Это вещество приобретает окраску после расщепления его присутствующим в ячейке ферментом То есть, если все элементы цепочки присутствуют, в лунке образуется окрашенный комплекс
 D 0556 Вектогеп В - HBs-антиген - стрип (комплект 3)
D 0556 Вектогеп В - HBs-антиген - стрип (комплект 3)
 СОСТАВ НАБОРА lпланшет разборный с иммобилизованными антителами к HBs. Ag; lположительный контрольный образец, инактивированный (К+), содержит 20± 10 нг/мл HBs. Ag 2 субтипа (красная прозрачная жидкость); lслабоположительный контрольный образец, инактивированный (К+слаб), содержит 0, 2± 0, 1 нг/мл HBs. Ag 3 субтипа (лиофильно высушенная масса кремового цвета); lотрицательный контрольный образец, инактивированный (К , жёлтая прозрачная или с лёгкой опалесценцией жидкость); lконъюгат (концентрат, моноклональные антитела к HBs. Ag, меченые пероксидазой хрена; жидкость синего цвета); lраствор для разведения конъюгата (РК); lцитратно фосфатный буферный раствор с перекисью водорода (ЦФР); lконцентрат фосфатно солевого буферного раствора с твином (ФСБ ТХ 25); lтетраметилбензидин (ТМБ); lстоп реагент lклейкая плёнка для планшета; lпластиковая ёмкость; lодноразовые наконечники.
СОСТАВ НАБОРА lпланшет разборный с иммобилизованными антителами к HBs. Ag; lположительный контрольный образец, инактивированный (К+), содержит 20± 10 нг/мл HBs. Ag 2 субтипа (красная прозрачная жидкость); lслабоположительный контрольный образец, инактивированный (К+слаб), содержит 0, 2± 0, 1 нг/мл HBs. Ag 3 субтипа (лиофильно высушенная масса кремового цвета); lотрицательный контрольный образец, инактивированный (К , жёлтая прозрачная или с лёгкой опалесценцией жидкость); lконъюгат (концентрат, моноклональные антитела к HBs. Ag, меченые пероксидазой хрена; жидкость синего цвета); lраствор для разведения конъюгата (РК); lцитратно фосфатный буферный раствор с перекисью водорода (ЦФР); lконцентрат фосфатно солевого буферного раствора с твином (ФСБ ТХ 25); lтетраметилбензидин (ТМБ); lстоп реагент lклейкая плёнка для планшета; lпластиковая ёмкость; lодноразовые наконечники.
 СПОСОБ ПРИМЕНЕНИЯ При работе с исследуемыми сыворотками и контрольными образцами следует соблюдать меры предосторожности, принятые при работе с потенциально инфекционным материалом: * работать в резиновых перчатках; * не пипетировать растворы ртом; * все использованные материалы подвергать обработке 6% ным раствором перекиси водорода (не менее 6 часов). Внимание! Несоблюдение описанных требований может привести к искаженному результату ИФА. * Для приготовления растворов и проведения ИФА следует использовать чистую мерную посуду и автоматические пипетки с погрешностью измерения объёмов не более 5%. * Желательно использовать свежеотобранные образцы сыворотки (плазмы) крови. Допускается использование образцов, хранившихся при (2 8)°С не более 5 суток, либо при минус 20 ± 3°С не более 1 мес. * Нельзя использовать проросшие, гиперлипидные сыворотки или подвергавшиеся многократному замораживанию и оттаиванию.
СПОСОБ ПРИМЕНЕНИЯ При работе с исследуемыми сыворотками и контрольными образцами следует соблюдать меры предосторожности, принятые при работе с потенциально инфекционным материалом: * работать в резиновых перчатках; * не пипетировать растворы ртом; * все использованные материалы подвергать обработке 6% ным раствором перекиси водорода (не менее 6 часов). Внимание! Несоблюдение описанных требований может привести к искаженному результату ИФА. * Для приготовления растворов и проведения ИФА следует использовать чистую мерную посуду и автоматические пипетки с погрешностью измерения объёмов не более 5%. * Желательно использовать свежеотобранные образцы сыворотки (плазмы) крови. Допускается использование образцов, хранившихся при (2 8)°С не более 5 суток, либо при минус 20 ± 3°С не более 1 мес. * Нельзя использовать проросшие, гиперлипидные сыворотки или подвергавшиеся многократному замораживанию и оттаиванию.
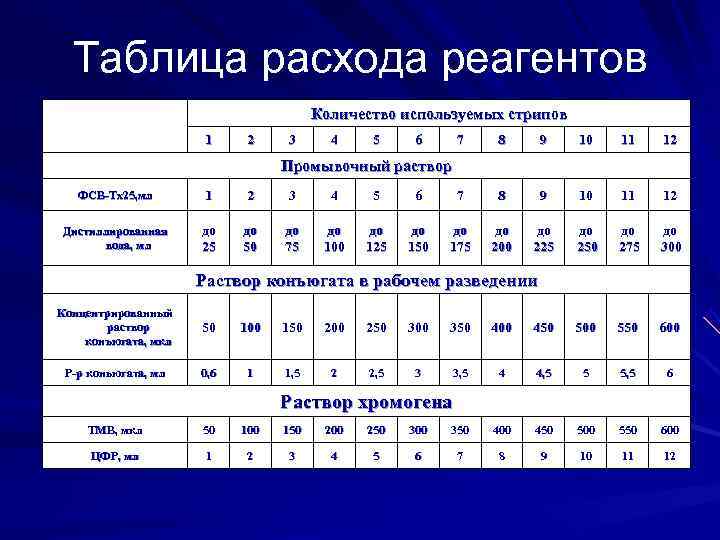
 3. 1. ПРИГОТОВЛЕНИЕ РЕАГЕНТОВ При постановке ИФА для приготовления реагентов необходимо пользоваться таблицей расхода реагентов на стр. 10. 3. 1. 1. Промывочный раствор Использовать для промывки лунок стрипов Взболтать содержимое флакона с ФСБ Тх25. При выпадении осадка солей в концентрате прогреть его перед разведением до полного растворения осадка. В соответствии с числом стрипов отобрать в чистый флакон необходимое количество ФСБ Тх25 и довести до соответствующего объёма дистиллированной водой. Хранение: при (2 -8)°С до 72 ч. 3. 1. 2. Слабоположительный контрольный образец Во флакон с К + слабый добавить 500 мкл дистиллированной воды и тщательно перемешать в течение 5 мин. Использовать в течение рабочего дня (8 - 10 часов). Слабоположительный контрольный образец К+слаб предназначен для контроля качества лабораторной постановки ИФА.
3. 1. ПРИГОТОВЛЕНИЕ РЕАГЕНТОВ При постановке ИФА для приготовления реагентов необходимо пользоваться таблицей расхода реагентов на стр. 10. 3. 1. 1. Промывочный раствор Использовать для промывки лунок стрипов Взболтать содержимое флакона с ФСБ Тх25. При выпадении осадка солей в концентрате прогреть его перед разведением до полного растворения осадка. В соответствии с числом стрипов отобрать в чистый флакон необходимое количество ФСБ Тх25 и довести до соответствующего объёма дистиллированной водой. Хранение: при (2 -8)°С до 72 ч. 3. 1. 2. Слабоположительный контрольный образец Во флакон с К + слабый добавить 500 мкл дистиллированной воды и тщательно перемешать в течение 5 мин. Использовать в течение рабочего дня (8 - 10 часов). Слабоположительный контрольный образец К+слаб предназначен для контроля качества лабораторной постановки ИФА.
 Таблица расхода реагентов Количество используемых стрипов 1 2 3 4 5 6 7 8 9 10 11 12 Промывочный раствор ФСВ-Тх25, мл 1 2 3 4 5 6 7 8 9 10 11 12 Дистиллированная до до до вода, мл 25 50 75 100 125 150 175 200 225 250 275 300 Раствор конъюгата в рабочем разведении Концентрированный раствор 50 100 150 200 250 300 350 400 450 500 550 600 конъюгата, мкл конъюгата, Р-р коньюгата, мл коньюгата, 0, 6 1 1, 5 2 2, 5 3 3, 5 4 4, 5 5 5, 5 6 Раствор хромогена ТМВ, мкл 50 100 150 200 250 300 350 400 450 500 550 600 ЦФР, мл 1 2 3 4 5 6 7 8 9 10 11 12
Таблица расхода реагентов Количество используемых стрипов 1 2 3 4 5 6 7 8 9 10 11 12 Промывочный раствор ФСВ-Тх25, мл 1 2 3 4 5 6 7 8 9 10 11 12 Дистиллированная до до до вода, мл 25 50 75 100 125 150 175 200 225 250 275 300 Раствор конъюгата в рабочем разведении Концентрированный раствор 50 100 150 200 250 300 350 400 450 500 550 600 конъюгата, мкл конъюгата, Р-р коньюгата, мл коньюгата, 0, 6 1 1, 5 2 2, 5 3 3, 5 4 4, 5 5 5, 5 6 Раствор хромогена ТМВ, мкл 50 100 150 200 250 300 350 400 450 500 550 600 ЦФР, мл 1 2 3 4 5 6 7 8 9 10 11 12
 3. 2. ПРОВЕДЕНИЕ ИФА 3. 2. 1. Подготовить необходимое количество срипов к работе. Оставшиеся сразу упаковать во избежание губительного воздействия влаги. Для этого стрипы необходимо снять с рамки, поместить в цефленовый пакет с влагопоглотителем, тщательно закрыть пакет пластиковой застёжкой. Упакованные таким образом стрипы хранить при (2 8)°С до конца срока годности. Приготовить промывочный раствор (п. 3. 1. 1), слабоположительный контрольный образец (п. 3. 1. 2) и раствор конъюгата (п. 3. 1. 3). Положительный (К+) и отрицательный (К ) контрольные образцы готовы к использованию и не требуют дополнительного разведения. 1. Внести контрольные образцы: в лунки А 1, В 1 по 0, 1 мл К , в лунку С 1 – 0, 1 мл К+слаб, а в лунку D 1 — 0, 1 мл К+. В остальные лунки внести по 0, 1 мл исследуемых сывороток. При постановке анализа на 2 и более стрипах для К использовать 3 лунки. 2. Во все лунки внести по 0, 05 мл при готовленного раствораконъюгата. Внимание! Для внесения раствора- конъюгата использовать пластиковую ёмкость и одноразовые наконечники из набора. 3. 2. 4. Стрипы заклеить клейкой плёнкой и инкубировать в соответствии с выбранной программой
3. 2. ПРОВЕДЕНИЕ ИФА 3. 2. 1. Подготовить необходимое количество срипов к работе. Оставшиеся сразу упаковать во избежание губительного воздействия влаги. Для этого стрипы необходимо снять с рамки, поместить в цефленовый пакет с влагопоглотителем, тщательно закрыть пакет пластиковой застёжкой. Упакованные таким образом стрипы хранить при (2 8)°С до конца срока годности. Приготовить промывочный раствор (п. 3. 1. 1), слабоположительный контрольный образец (п. 3. 1. 2) и раствор конъюгата (п. 3. 1. 3). Положительный (К+) и отрицательный (К ) контрольные образцы готовы к использованию и не требуют дополнительного разведения. 1. Внести контрольные образцы: в лунки А 1, В 1 по 0, 1 мл К , в лунку С 1 – 0, 1 мл К+слаб, а в лунку D 1 — 0, 1 мл К+. В остальные лунки внести по 0, 1 мл исследуемых сывороток. При постановке анализа на 2 и более стрипах для К использовать 3 лунки. 2. Во все лунки внести по 0, 05 мл при готовленного раствораконъюгата. Внимание! Для внесения раствора- конъюгата использовать пластиковую ёмкость и одноразовые наконечники из набора. 3. 2. 4. Стрипы заклеить клейкой плёнкой и инкубировать в соответствии с выбранной программой
 4. РЕГИСТРАЦИЯ И ОЦЕНКА РЕЗУЛЬТАТОВ 1. Результаты ИФА регистрировать с помощью спектрофотометра, измеряя оптическую плотность в двухволновом режиме: основной фильтр 450 нм, референс фильтр в диапазоне 620 650 нм. Допустима регистрация результатов только с фильтром 450 нм. Выведения спектрофотометра на нулевой уровень ( «бланк» ) осуществлять по воздуху. 2. Оценка отрицательных и положительных контролен 4. 2. 1. ОП К отр не должна превышать 0, 15. Исключить ОП К отр, превышающие 0, 15. 1. Вычислить ОПср. К отр.
4. РЕГИСТРАЦИЯ И ОЦЕНКА РЕЗУЛЬТАТОВ 1. Результаты ИФА регистрировать с помощью спектрофотометра, измеряя оптическую плотность в двухволновом режиме: основной фильтр 450 нм, референс фильтр в диапазоне 620 650 нм. Допустима регистрация результатов только с фильтром 450 нм. Выведения спектрофотометра на нулевой уровень ( «бланк» ) осуществлять по воздуху. 2. Оценка отрицательных и положительных контролен 4. 2. 1. ОП К отр не должна превышать 0, 15. Исключить ОП К отр, превышающие 0, 15. 1. Вычислить ОПср. К отр.
 4. 2. 4. Реакцию учитывать, если осталось больше половины отрицательных контролей; среднее значение ОПср. К+ не менее чем в 4 раза превышает Опср. К отр, 4. 3. Для оценки результатов анализа исследуемых сывороток вычислить критический уровень оптической плотности (ОПкрит): ОПкрит = ОПср. К+ 0, 04 Значение ОП К+ слаб должно превышать ОПкрыт. 4. 4. ПРИМЕР УЧЁТА РЕЗУЛЬТАТОВ РЕАКЦИИ ОП К-отр = 0, 065; 0, 060; 0, 070 ОП К+ = 1, 8; 1, 7 ОП К+ слаб = 0, 170; 0, 160 ОПср К-отр = (0, 065 + 0, 060 + 0, 070) / 3 = 0, 065 ОПср К+ = (1, 8 + 1, 7) / 2 = 1, 75 ОПср К+слаб = (0, 170 + 0, 160) / 2 = 0, 165 Оценка отрицательных контролей:
4. 2. 4. Реакцию учитывать, если осталось больше половины отрицательных контролей; среднее значение ОПср. К+ не менее чем в 4 раза превышает Опср. К отр, 4. 3. Для оценки результатов анализа исследуемых сывороток вычислить критический уровень оптической плотности (ОПкрит): ОПкрит = ОПср. К+ 0, 04 Значение ОП К+ слаб должно превышать ОПкрыт. 4. 4. ПРИМЕР УЧЁТА РЕЗУЛЬТАТОВ РЕАКЦИИ ОП К-отр = 0, 065; 0, 060; 0, 070 ОП К+ = 1, 8; 1, 7 ОП К+ слаб = 0, 170; 0, 160 ОПср К-отр = (0, 065 + 0, 060 + 0, 070) / 3 = 0, 065 ОПср К+ = (1, 8 + 1, 7) / 2 = 1, 75 ОПср К+слаб = (0, 170 + 0, 160) / 2 = 0, 165 Оценка отрицательных контролей:
 Реакцию можно учитывать, т. к. осталось больше половины отрицательных контролей (три из трёх) и: ОПср К+ / ОПср К отр = 1, 75 / 0, 065 = 26, 9 > 4. Расчёт ОП крит ОП Крит = 0, 065 + 0, 04 = 0, 105 ОПср. К+слаб больше ОПкрит. 4. 5. ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ Положительными считать образцы, показавшие ОП, превышающую или равную ОПкрит. Положительный результат означает, что тестируемая сыворотка содержит HBs. Ag или неспецифически реагирующий агент. Сыворотки, давшие первичный положи тельный результат, олжны д быть проверены повторно, и специфичность реакции должна быть подтверждена с помощью набора «Вектогеп В HBs антиген подтверждающий тест стрип» (комплект 5).
Реакцию можно учитывать, т. к. осталось больше половины отрицательных контролей (три из трёх) и: ОПср К+ / ОПср К отр = 1, 75 / 0, 065 = 26, 9 > 4. Расчёт ОП крит ОП Крит = 0, 065 + 0, 04 = 0, 105 ОПср. К+слаб больше ОПкрит. 4. 5. ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ Положительными считать образцы, показавшие ОП, превышающую или равную ОПкрит. Положительный результат означает, что тестируемая сыворотка содержит HBs. Ag или неспецифически реагирующий агент. Сыворотки, давшие первичный положи тельный результат, олжны д быть проверены повторно, и специфичность реакции должна быть подтверждена с помощью набора «Вектогеп В HBs антиген подтверждающий тест стрип» (комплект 5).
 Для качественного проведения ИФА в планшетах необходимо современное лабораторное оборудование, позволяющее стандартизировать и контролировать все этапы иммуноанализа: автоматические анализаторы (синоним: спектрофотометры вертикального сканирования, ридеры) для 96 луночных планшетов с вертикальной фотометрией; программируемые промыватели планшетов (вошеры); программируемые вибротермостаты для планшетов (синонимы: термостатируемые шейкеры, термошейкеры, шейкер термостаты).
Для качественного проведения ИФА в планшетах необходимо современное лабораторное оборудование, позволяющее стандартизировать и контролировать все этапы иммуноанализа: автоматические анализаторы (синоним: спектрофотометры вертикального сканирования, ридеры) для 96 луночных планшетов с вертикальной фотометрией; программируемые промыватели планшетов (вошеры); программируемые вибротермостаты для планшетов (синонимы: термостатируемые шейкеры, термошейкеры, шейкер термостаты).
 Дополнительно при подготовке образцов, реагентов и проведения ИФА используются: ротаторы устройства для оптимального перемешивания крови с добавками в пробирках и стандартизации условий подготовки образцов к анализу; центрифуги для отделения сыворотки или плазмы крови; дозирующие устройства полуавтоматические пипетки фиксированного и переменного объема (одноканальные, 8 и 12 канальные); первичные пробирки или системы для забора венозной и капиллярной крови; подробнее вторичные пробирки, в которых хранится исследуемый образец; вспомогательное общелабораторное оборудование (вортексы, миксеры, р. Н метры, системы для очистки воды и др. ). подробнее
Дополнительно при подготовке образцов, реагентов и проведения ИФА используются: ротаторы устройства для оптимального перемешивания крови с добавками в пробирках и стандартизации условий подготовки образцов к анализу; центрифуги для отделения сыворотки или плазмы крови; дозирующие устройства полуавтоматические пипетки фиксированного и переменного объема (одноканальные, 8 и 12 канальные); первичные пробирки или системы для забора венозной и капиллярной крови; подробнее вторичные пробирки, в которых хранится исследуемый образец; вспомогательное общелабораторное оборудование (вортексы, миксеры, р. Н метры, системы для очистки воды и др. ). подробнее
 Микропланшетные анализаторы Анализатор иммуноферментных реакций УНИПЛАН (АИФР 01, Пикон, РФ). Микропланшетный фотометр Immunochem 2100 (НTI, США).
Микропланшетные анализаторы Анализатор иммуноферментных реакций УНИПЛАН (АИФР 01, Пикон, РФ). Микропланшетный фотометр Immunochem 2100 (НTI, США).
 Микропланшетный ридер 2020 (Anthos Labtec, Австрия) Микропланшетный ридер 2010 (Anthos Labtec, Австрия). Микропланшетный фотометр Multiskan ЕХ (Termo Fisher Scintific).
Микропланшетный ридер 2020 (Anthos Labtec, Австрия) Микропланшетный ридер 2010 (Anthos Labtec, Австрия). Микропланшетный фотометр Multiskan ЕХ (Termo Fisher Scintific).
 Автоматические промыватели планшетов для ИФА Промыватель планшет автоматический ПРОПЛАН (Пикон, РФ). Автоматический промыватель иммунопланшет Immuno. Chem 2600 (США).
Автоматические промыватели планшетов для ИФА Промыватель планшет автоматический ПРОПЛАН (Пикон, РФ). Автоматический промыватель иммунопланшет Immuno. Chem 2600 (США).
 Автоматический промыватель иммунопланшет Stat Fax 2600 (Awareness Technology, США). Автоматическое промывочное устройство Fluido 96 W 2 (Anthos Labtec, Австрия). Автоматический промыватель Wellwash 4 MK II (Termo. Fisher Scientific).
Автоматический промыватель иммунопланшет Stat Fax 2600 (Awareness Technology, США). Автоматическое промывочное устройство Fluido 96 W 2 (Anthos Labtec, Австрия). Автоматический промыватель Wellwash 4 MK II (Termo. Fisher Scientific).
 Термошейкеры для ИФА Термошейкер для иммунопланшет PST 60 HL (Biosan, Латвия). Термошейкер Immunochem 2200. 4 (НTI, США) Цифровой шейкер термостат ST 3 М (ELMI, Латвия).
Термошейкеры для ИФА Термошейкер для иммунопланшет PST 60 HL (Biosan, Латвия). Термошейкер Immunochem 2200. 4 (НTI, США) Цифровой шейкер термостат ST 3 М (ELMI, Латвия).
 Современная аппаратура и оснащение бактериологической лаборатории
Современная аппаратура и оснащение бактериологической лаборатории
 Тест системы для идентификации бактерий На современном этапе для биохимической идентификации микроорганизмов используют готовые тест системы. Коммерческие тест системы это готовые полистероловые планшеты с сухими дифференциальными средами или субстратами.
Тест системы для идентификации бактерий На современном этапе для биохимической идентификации микроорганизмов используют готовые тест системы. Коммерческие тест системы это готовые полистероловые планшеты с сухими дифференциальными средами или субстратами.
 Широко используются в практических лабораториях диагностические системы AРI (фирмs производители: «bio Merieux» (Франция), «Becton Dickinson» и « Micro Scan» (США), «Micro Tax» фирма производитель «Sy Lab» (Австрия)) С помощью тест систем идентификация бактерий проводится в течение 3 48 ч. СИБ системы индикаторных бумажек и одноразовых диагностических пластин для идентификации энтеробактерий и стафилококков (НИИЭМ «Диагностические системы» )
Широко используются в практических лабораториях диагностические системы AРI (фирмs производители: «bio Merieux» (Франция), «Becton Dickinson» и « Micro Scan» (США), «Micro Tax» фирма производитель «Sy Lab» (Австрия)) С помощью тест систем идентификация бактерий проводится в течение 3 48 ч. СИБ системы индикаторных бумажек и одноразовых диагностических пластин для идентификации энтеробактерий и стафилококков (НИИЭМ «Диагностические системы» )
 Этапы проведения идентификации 1 этап. Выделение чистой культуры. 2 этап. Подготовка бактериальной суспензии. 3 этап. Инокуляция культуры в лунки планшета. 4 этап. Оценка результатов 5 этап. Идентификация культуры. Данные этапы проводятся в соответствии с инструкцией производителя.
Этапы проведения идентификации 1 этап. Выделение чистой культуры. 2 этап. Подготовка бактериальной суспензии. 3 этап. Инокуляция культуры в лунки планшета. 4 этап. Оценка результатов 5 этап. Идентификация культуры. Данные этапы проводятся в соответствии с инструкцией производителя.
 Автоматические приборы для идентификации и определения антибиотикочувствительности
Автоматические приборы для идентификации и определения антибиотикочувствительности
 Идентификация микроорганизмов и определение их чувствительности к антибиотикам с применением автоматического микробиологического анализатора VITEK 2 Compact Методические рекомендации МР 02. 032 08
Идентификация микроорганизмов и определение их чувствительности к антибиотикам с применением автоматического микробиологического анализатора VITEK 2 Compact Методические рекомендации МР 02. 032 08
 Общие положения Идентификация основана на анализе изменения биохимических субстратов под действием микроорганизмов. Определение чувствительности производится на основании подавления роста микроорганизмов под действием различных концентраций антибиотиков. При этом определяются минимальные ингибирующие концентрации (МИК) антибиотиков, которые выражаются в мг/л и интерпретируются в виде категорий «устойчив» , «чувствителен» , «умеренно устойчив» .
Общие положения Идентификация основана на анализе изменения биохимических субстратов под действием микроорганизмов. Определение чувствительности производится на основании подавления роста микроорганизмов под действием различных концентраций антибиотиков. При этом определяются минимальные ингибирующие концентрации (МИК) антибиотиков, которые выражаются в мг/л и интерпретируются в виде категорий «устойчив» , «чувствителен» , «умеренно устойчив» .
 Сущность метода Работа в анализаторе VITEK 2 Compact проводится с чистой культурой микроорганизма. В качестве расходных материалов используются пластиковые карты, содержащие биохимические субстраты (ID карты, карты для идентификации) или антибиотики в различных концентрациях (AST карты, карты для определения чувствительности). Карты под вакуумом, создаваемом анализатором, в автоматическом режиме заполняются суспензией чистой культуры микроорганизмов, запаиваются и помещаются в карусель, где они инкубируются и регулярно (каждые 15 минут) сканируются оптической системой анализатора. Для считывания ID карт используется колориметрия (анализатор содержит 2 оптических модуля и использует волны 660, 428 и 568 нанометров) для считывания AST карт – турбидиметрия (фиксируются изменение плотности микробной суспензии под влиянием антибиотика).
Сущность метода Работа в анализаторе VITEK 2 Compact проводится с чистой культурой микроорганизма. В качестве расходных материалов используются пластиковые карты, содержащие биохимические субстраты (ID карты, карты для идентификации) или антибиотики в различных концентрациях (AST карты, карты для определения чувствительности). Карты под вакуумом, создаваемом анализатором, в автоматическом режиме заполняются суспензией чистой культуры микроорганизмов, запаиваются и помещаются в карусель, где они инкубируются и регулярно (каждые 15 минут) сканируются оптической системой анализатора. Для считывания ID карт используется колориметрия (анализатор содержит 2 оптических модуля и использует волны 660, 428 и 568 нанометров) для считывания AST карт – турбидиметрия (фиксируются изменение плотности микробной суспензии под влиянием антибиотика).
 Сущность метода Результаты сканирования подвергаются компьютерной обработке. По завершении идентификация анализатор найдет в базе данных соответствие тестируемому микроорганизму или проведет определение чувствительности к антибиотикам, после чего карта сбрасывается в специальный приемник.
Сущность метода Результаты сканирования подвергаются компьютерной обработке. По завершении идентификация анализатор найдет в базе данных соответствие тестируемому микроорганизму или проведет определение чувствительности к антибиотикам, после чего карта сбрасывается в специальный приемник.
 Методы отбора и подготовки проб. Исследуемый материал инокулируется на питательные среды согласно методам микробиологических исследований, утвержденных в установленном порядке. Чашки инкубируются 18 24 (48) ч до получения изолированных колоний. Колонии микроорганизмов для исследования на VITEK 2 Compact рекомендуется брать с неселективных питательных сред. Используется только чистая культура микроорганизмов.
Методы отбора и подготовки проб. Исследуемый материал инокулируется на питательные среды согласно методам микробиологических исследований, утвержденных в установленном порядке. Чашки инкубируются 18 24 (48) ч до получения изолированных колоний. Колонии микроорганизмов для исследования на VITEK 2 Compact рекомендуется брать с неселективных питательных сред. Используется только чистая культура микроорганизмов.
 Аппаратура, материалы, реактивы и питательные среды Анализатор Vitek 2 Compact Суспензиальный раствор (0, 45% раствор хлорида натрия) Диспенсер суспензиального раствора Пластиковые пробирки для анализатора Vitek 2 Compact Карты для идентификации Карты для определения чувствительности Петли бактериологические Тампоны стерильные Денситометр
Аппаратура, материалы, реактивы и питательные среды Анализатор Vitek 2 Compact Суспензиальный раствор (0, 45% раствор хлорида натрия) Диспенсер суспензиального раствора Пластиковые пробирки для анализатора Vitek 2 Compact Карты для идентификации Карты для определения чувствительности Петли бактериологические Тампоны стерильные Денситометр
 Подготовка к испытанию Перед началом работы необходимо, следуя инструкциям программного обеспечения, ввести информацию об используемых AST картах, а также произвести ряд общих настроек Чистая культура (материал одной или нескольких изолированных колоний) с помощью бактериологической петли или тампона вносится в пластиковую пробирку с суспензиальным раствором и гомогенизируется там до достижения требуемой плотности бактериальной суспензии: – для грамположительных и грамотрицательных бактерий: 0, 5 0, 63 Mc. F*, – для прихотливых бактерий: 2, 7 3, 3 Mc. F, – для бацилл 1, 8 2, 2 Mc. F, – для грибов: 1, 8 2, 2 Mc. F.
Подготовка к испытанию Перед началом работы необходимо, следуя инструкциям программного обеспечения, ввести информацию об используемых AST картах, а также произвести ряд общих настроек Чистая культура (материал одной или нескольких изолированных колоний) с помощью бактериологической петли или тампона вносится в пластиковую пробирку с суспензиальным раствором и гомогенизируется там до достижения требуемой плотности бактериальной суспензии: – для грамположительных и грамотрицательных бактерий: 0, 5 0, 63 Mc. F*, – для прихотливых бактерий: 2, 7 3, 3 Mc. F, – для бацилл 1, 8 2, 2 Mc. F, – для грибов: 1, 8 2, 2 Mc. F.
 Подготовка к испытанию Выбор карты для исследования производится: – на основании окраски по грамму или пробы с КОН, позволяющей разделить бактерии на грамположительные и грамотрицательные. Карты VITEK 2 GP (грам положительные) и VITEK 2 GN (грам отрицательные). – Микроорганизмы, прихотливые к условиям культивирования (нейссерии, гемофилы и проч. ) идентифицируются при помощи карт VITEK 2 NH, – грибы – карт VITEK 2 YST. – карты VITEK 2 BCL предназначены для идентификации микроорганизмов рода Bacillus. Пробирки с суспензиями устанавливаются в кассету, напротив них в специальные прорези (слоты) устанавливаются соотвествующие карты, так, чтобы относящаяся к карте пластиковая трубочка была погружена в пробирку.
Подготовка к испытанию Выбор карты для исследования производится: – на основании окраски по грамму или пробы с КОН, позволяющей разделить бактерии на грамположительные и грамотрицательные. Карты VITEK 2 GP (грам положительные) и VITEK 2 GN (грам отрицательные). – Микроорганизмы, прихотливые к условиям культивирования (нейссерии, гемофилы и проч. ) идентифицируются при помощи карт VITEK 2 NH, – грибы – карт VITEK 2 YST. – карты VITEK 2 BCL предназначены для идентификации микроорганизмов рода Bacillus. Пробирки с суспензиями устанавливаются в кассету, напротив них в специальные прорези (слоты) устанавливаются соотвествующие карты, так, чтобы относящаяся к карте пластиковая трубочка была погружена в пробирку.
 Проведение испытания Работа в режиме виртуальной кассеты Работа в режиме «Загрузил и пошел» Внесение даных об образце
Проведение испытания Работа в режиме виртуальной кассеты Работа в режиме «Загрузил и пошел» Внесение даных об образце
 Обработка результатов После считывания карт, полученные результаты анализируются программным обеспечением. Результаты исследования карт можно просмотреть (распечатать) в соответствующем окне интерфейса.
Обработка результатов После считывания карт, полученные результаты анализируются программным обеспечением. Результаты исследования карт можно просмотреть (распечатать) в соответствующем окне интерфейса.
 Ограничение метода Корректная идентификация и определение чувтствительности с использованием анализатора VITEK 2 Compact возможны только для микроорганизмов, имеющих клиническое значение.
Ограничение метода Корректная идентификация и определение чувтствительности с использованием анализатора VITEK 2 Compact возможны только для микроорганизмов, имеющих клиническое значение.
 VITEK 2 Compact
VITEK 2 Compact
 VITEK 2 Compact
VITEK 2 Compact
 VITEK® 2 (Вайтек 2)
VITEK® 2 (Вайтек 2)
 «Санитарно бактериологические исследования методом разделенного импеданса» . МУК 4. 2. 2578 10
«Санитарно бактериологические исследования методом разделенного импеданса» . МУК 4. 2. 2578 10
 Методические указания. «Санитарно бактериологические исследования методом разделенного импеданса» . МУК 4. 2. 2578 10 (введены взамен МУК 4. 2. 590 96 "Бактериологические исследования с использованием микробиологического экспресс анализатора " Бак. Трак 4100" и методических указаний "Использование метода измерения электрического сопротивления (импеданса) для санитарно бактериологического исследования объектов окружающей среды", 2005 г.
Методические указания. «Санитарно бактериологические исследования методом разделенного импеданса» . МУК 4. 2. 2578 10 (введены взамен МУК 4. 2. 590 96 "Бактериологические исследования с использованием микробиологического экспресс анализатора " Бак. Трак 4100" и методических указаний "Использование метода измерения электрического сопротивления (импеданса) для санитарно бактериологического исследования объектов окружающей среды", 2005 г.
 Сущность импедансного метода Методические указания содержат описание метода ускоренного микробиологического исследования продовольственного сырья, пищевых продуктов и других объектов внешней среды с использованием микробиологических экспресс анализаторов, регистрирующих изменения электрического сопротивления (импеданса) питательной среды, происходящего под влиянием процессов роста и жизнедеятельности микроорганизмов в исследуемой пробе.
Сущность импедансного метода Методические указания содержат описание метода ускоренного микробиологического исследования продовольственного сырья, пищевых продуктов и других объектов внешней среды с использованием микробиологических экспресс анализаторов, регистрирующих изменения электрического сопротивления (импеданса) питательной среды, происходящего под влиянием процессов роста и жизнедеятельности микроорганизмов в исследуемой пробе.
 Предлагаемый метод на основе метода разделенного импеданса позволяет получать быстрые (в течение нескольких часов) и надежные результаты для большого числа одновременно исследуемых образцов. Импеданс сопротивление потоку переменного тока через проводящий материал; является функцией активной проводимости, емкостного сопротивления и применяемой частоты.
Предлагаемый метод на основе метода разделенного импеданса позволяет получать быстрые (в течение нескольких часов) и надежные результаты для большого числа одновременно исследуемых образцов. Импеданс сопротивление потоку переменного тока через проводящий материал; является функцией активной проводимости, емкостного сопротивления и применяемой частоты.
 Импедансная микробиология является непрямым культуральным методом обнаружения микроорганизмов с использованием определения электрического импеданса. Изменения импеданса обычно происходят в питательной среде по мере того, как ее химический состав изменяется в результате роста и метаболической активности микроорганизмов. Экспоненциальные изменения импедансного сигнала могут наблюдаться, когда количество микроорганизмов достигает порога около 106 107 клеток/мл.
Импедансная микробиология является непрямым культуральным методом обнаружения микроорганизмов с использованием определения электрического импеданса. Изменения импеданса обычно происходят в питательной среде по мере того, как ее химический состав изменяется в результате роста и метаболической активности микроорганизмов. Экспоненциальные изменения импедансного сигнала могут наблюдаться, когда количество микроорганизмов достигает порога около 106 107 клеток/мл.
 Время определения импеданса (IDT) время, необходимое для достижения значимого изменения импеданса Значение IDT обратно пропорционально начальной концентрации микроорганизмов в исследуемой пробе. Ход кривых импедансного сигнала соответствует и отражает кривую роста микроорганизмов в исследуемой пробе.
Время определения импеданса (IDT) время, необходимое для достижения значимого изменения импеданса Значение IDT обратно пропорционально начальной концентрации микроорганизмов в исследуемой пробе. Ход кривых импедансного сигнала соответствует и отражает кривую роста микроорганизмов в исследуемой пробе.
 наибольшее распространение получили приборы серии "Бак. Трак 4000" производства фирмы "SY LAB Gerate Gmb. H" (Австрия). Приборы "Бак. Трак 4300", "Бак. Трак 4100" и "Бак. Трак 4250", внесены в Реестр средств измерений как кондуктометрические анализаторы для микробиологических исследований. Метод, основанный на измерении импеданса, приборы "Бак. Трак 4300", "Бак. Трак 4100" и "Бак. Трак 4250", внесены в Национальные стандарты ряда европейских стран: Германии DIN 10115, 10120, 10121, Австрии ONORM 10115, 10120, 10121, Франции AFNOR NF V 08 105 (Микробиология продуктов питания и кормов: указания по импедансному методу для микробиологических исследований), AFNOR NF V 08 106 (Определение количества E. coli в морепродуктах качественным методом, используя метод прямого импеданса). Метод валидирован как альтернативный метод анализа в соответствии с ISO 16140: 2003 Институтом стандартизации AFNOR, Франция.
наибольшее распространение получили приборы серии "Бак. Трак 4000" производства фирмы "SY LAB Gerate Gmb. H" (Австрия). Приборы "Бак. Трак 4300", "Бак. Трак 4100" и "Бак. Трак 4250", внесены в Реестр средств измерений как кондуктометрические анализаторы для микробиологических исследований. Метод, основанный на измерении импеданса, приборы "Бак. Трак 4300", "Бак. Трак 4100" и "Бак. Трак 4250", внесены в Национальные стандарты ряда европейских стран: Германии DIN 10115, 10120, 10121, Австрии ONORM 10115, 10120, 10121, Франции AFNOR NF V 08 105 (Микробиология продуктов питания и кормов: указания по импедансному методу для микробиологических исследований), AFNOR NF V 08 106 (Определение количества E. coli в морепродуктах качественным методом, используя метод прямого импеданса). Метод валидирован как альтернативный метод анализа в соответствии с ISO 16140: 2003 Институтом стандартизации AFNOR, Франция.
 Прибор "Бак. Трак" является автоматизированной экспресс системой для ускоренной количественной и качественной оценки степени микробной контаминации продовольственного сырья, пищевых продуктов, косметической и фармацевтической продукции, питьевой воды и других объектов внешней среды.
Прибор "Бак. Трак" является автоматизированной экспресс системой для ускоренной количественной и качественной оценки степени микробной контаминации продовольственного сырья, пищевых продуктов, косметической и фармацевтической продукции, питьевой воды и других объектов внешней среды.
 Приборы "Бак. Трак" серии 4000 на основе метода разделенного импеданса регистрируют 2 определенных показателя импеданса для каждого измерения. – М величина (импеданс среды) – Е величина (импеданс электрода). Измерения М параметра представляет собой относительное изменение (уменьшение) импеданса среды, выраженное в процентах к начальному измерению. М параметр в основном отображает ту часть импеданса, которая связана с активной проводимостью. На него непосредственное влияние оказывает ионный состав среды при росте микроорганизмов, а также используемый для анализа образец. При высокой электропроводимости питательной среды данный параметр теряет значимость. На величину Е параметра состав питательной среды влияет уже не в столь сильной мере, что весьма важно в случаях, когда используются среды с высоким содержанием солей (т. е. в них добавлены соли в качестве селективных компонентов, используемых для обнаружения патогенных микроорганизмов).
Приборы "Бак. Трак" серии 4000 на основе метода разделенного импеданса регистрируют 2 определенных показателя импеданса для каждого измерения. – М величина (импеданс среды) – Е величина (импеданс электрода). Измерения М параметра представляет собой относительное изменение (уменьшение) импеданса среды, выраженное в процентах к начальному измерению. М параметр в основном отображает ту часть импеданса, которая связана с активной проводимостью. На него непосредственное влияние оказывает ионный состав среды при росте микроорганизмов, а также используемый для анализа образец. При высокой электропроводимости питательной среды данный параметр теряет значимость. На величину Е параметра состав питательной среды влияет уже не в столь сильной мере, что весьма важно в случаях, когда используются среды с высоким содержанием солей (т. е. в них добавлены соли в качестве селективных компонентов, используемых для обнаружения патогенных микроорганизмов).
 Бактериологический анализатор Бак. Трак 4300
Бактериологический анализатор Бак. Трак 4300
 Бактериологический анализатор Био. Трак 4250
Бактериологический анализатор Био. Трак 4250
 Определение количества микроорганизмов в пищевых продуктах и объектах окружающей среды методом наиболее вероятного числа с применением автоматического экспресс анализатора ТЕМПО Методические рекомендации
Определение количества микроорганизмов в пищевых продуктах и объектах окружающей среды методом наиболее вероятного числа с применением автоматического экспресс анализатора ТЕМПО Методические рекомендации
 Общие положения Автоматический анализатор ТЕМРО предназначен для: подсчета жизнеспособных аэробных мезофильных микроорганизмов в продуктах питания и объектах окружающей среды за 40 – 48 часов (тест ТЕМПО TVC); подсчета общего числа колиформ (БГКП) в продуктах питания и объектах окружающей среды за 24 часа (тест ТЕМПО ТС); подсчета колиформ в продуктах питания и объектах окружающей среды за 24 часа (тест ТЕМПО СС); подсчета Escherichia coli в продуктах питания и объектах окружающей среды за 24 часа (тест ТЕМПО ЕС); подсчета энтеробактерий в продуктах питания и объектах окружающей среды за 22 27 часов (тест ТЕМПО ЕВ); подсчета коагулазоположительных стафилококков в продуктах питания и объектах окружающей среды за 24 27 часов без необходимости подтверждения результата (тест ТЕМПО STA); подсчета лактобактерий в продуктах питания и объектах окружающей среды за 40 48 часов (тест ТЕМПО LAB).
Общие положения Автоматический анализатор ТЕМРО предназначен для: подсчета жизнеспособных аэробных мезофильных микроорганизмов в продуктах питания и объектах окружающей среды за 40 – 48 часов (тест ТЕМПО TVC); подсчета общего числа колиформ (БГКП) в продуктах питания и объектах окружающей среды за 24 часа (тест ТЕМПО ТС); подсчета колиформ в продуктах питания и объектах окружающей среды за 24 часа (тест ТЕМПО СС); подсчета Escherichia coli в продуктах питания и объектах окружающей среды за 24 часа (тест ТЕМПО ЕС); подсчета энтеробактерий в продуктах питания и объектах окружающей среды за 22 27 часов (тест ТЕМПО ЕВ); подсчета коагулазоположительных стафилококков в продуктах питания и объектах окружающей среды за 24 27 часов без необходимости подтверждения результата (тест ТЕМПО STA); подсчета лактобактерий в продуктах питания и объектах окружающей среды за 40 48 часов (тест ТЕМПО LAB).
 Общие положения Количественный учет микроорганизмов основан на методе наиболее вероятного числа, соединенном с технологией карт ТЕМРО. Метод определения наиболее вероятного числа основан на высеве продукта и (или) разведений навески продукта или смывной жидкости в жидкую питательную среду, инкубировании посевов, учете видимых признаков роста микроорганизмов, пересеве, при необходимости, культуральной жидкости на агаризованные среды для подтверждения роста микроорганизмов, подсчете их количества с помощью таблицы НВЧ (ИСО 7218 96 п. 9. 4).
Общие положения Количественный учет микроорганизмов основан на методе наиболее вероятного числа, соединенном с технологией карт ТЕМРО. Метод определения наиболее вероятного числа основан на высеве продукта и (или) разведений навески продукта или смывной жидкости в жидкую питательную среду, инкубировании посевов, учете видимых признаков роста микроорганизмов, пересеве, при необходимости, культуральной жидкости на агаризованные среды для подтверждения роста микроорганизмов, подсчете их количества с помощью таблицы НВЧ (ИСО 7218 96 п. 9. 4).
 Сущность методики Автоматический анализатор ТЕМРО состоит из двух блоков – станции пробоподготовки и станции учета результатов. Станция пробоподготовки служит для приготовления суспензии, создания связи между информацией об образце и среде и картой ТЕМПО в программе ТЕМПО Prer, заполнения и запаивания карт в вакуумной станции. Карта содержит 48 ячеек (лунок) различного объема, 16 лунок объемом 0, 00225 см 3, 16 лунок объемом 0, 0225 см 3 и 16 лунок объемом 0, 225 см 3, что позволяет производить количественный учет на основе метода наиболее вероятного числа без приготовления последовательных разведений. Лунки являются реакционными зонами, в которых происходит определение микробного роста. После заполнения карты ТЕМРО помещают в обычный термостат.
Сущность методики Автоматический анализатор ТЕМРО состоит из двух блоков – станции пробоподготовки и станции учета результатов. Станция пробоподготовки служит для приготовления суспензии, создания связи между информацией об образце и среде и картой ТЕМПО в программе ТЕМПО Prer, заполнения и запаивания карт в вакуумной станции. Карта содержит 48 ячеек (лунок) различного объема, 16 лунок объемом 0, 00225 см 3, 16 лунок объемом 0, 0225 см 3 и 16 лунок объемом 0, 225 см 3, что позволяет производить количественный учет на основе метода наиболее вероятного числа без приготовления последовательных разведений. Лунки являются реакционными зонами, в которых происходит определение микробного роста. После заполнения карты ТЕМРО помещают в обычный термостат.
 Определение общего микробного числа 1. Определение основано на способности микроорганизмов продуцировать внеклеточные ферменты. 2. В состав питательной среды входит специфический субстрат, меченый 4 метил умбеллифероном. 3. Во время роста микроорганизмы выделяют в культуральную жидкость ферменты, которые расщепляют субстрат, в результате чего освобождается свободный 4 метил умбеллиферон, обладающий флуоресцентной способностью.
Определение общего микробного числа 1. Определение основано на способности микроорганизмов продуцировать внеклеточные ферменты. 2. В состав питательной среды входит специфический субстрат, меченый 4 метил умбеллифероном. 3. Во время роста микроорганизмы выделяют в культуральную жидкость ферменты, которые расщепляют субстрат, в результате чего освобождается свободный 4 метил умбеллиферон, обладающий флуоресцентной способностью.
 Определение количества E. Coli 1. Определение основано на способности 96% штаммов E. Coli продуцировать фермент β глюкуронидазу. 2. В состав питательной среды ТЕМРО ЕС входит специфический субстат – 4 метил умбеллиферил β D глюкуронид. 3. Во время роста микроорганизмы выделяют в культуральную жидкость β глюкуронидазу, которая расщепляет субстрат. При этом в питательную среду выделяется свободный 4 метилумбеллиферон, обладающий флуоресцентной способностью.
Определение количества E. Coli 1. Определение основано на способности 96% штаммов E. Coli продуцировать фермент β глюкуронидазу. 2. В состав питательной среды ТЕМРО ЕС входит специфический субстат – 4 метил умбеллиферил β D глюкуронид. 3. Во время роста микроорганизмы выделяют в культуральную жидкость β глюкуронидазу, которая расщепляет субстрат. При этом в питательную среду выделяется свободный 4 метилумбеллиферон, обладающий флуоресцентной способностью.
 4. Количество продуктов реакции прямо пропорционально численности популяции микроорганизмов. 5. Наличие флуоресцентнго сигнала считывается и фиксируется в автоматическом режиме ридером ТЕМРО Reader. 6. В зависимости от количества и объема положительных лунок, а так же разведения производится подсчет общего числа микроорганизмов в исходном образце методом наиболее вероятного числа в автоматическом режиме.
4. Количество продуктов реакции прямо пропорционально численности популяции микроорганизмов. 5. Наличие флуоресцентнго сигнала считывается и фиксируется в автоматическом режиме ридером ТЕМРО Reader. 6. В зависимости от количества и объема положительных лунок, а так же разведения производится подсчет общего числа микроорганизмов в исходном образце методом наиболее вероятного числа в автоматическом режиме.
 Определение количества бактерий семейства Enterobacteriaceae и колиформ Определение основано на способности микроорганизмов менять р. Н среды во время культивирования. Снижение значения р. Н среды в процессе культивирования обусловлено углеводным метаболизмом. В питательную среду добавлен 4 метил умбеллиферон, обладающий флуоресцентной способностью только при значениях р. Н ≥ 6. В качестве дополнительного источника углеводов в питательную среду для определения бактерий семейства Enterobacteriaceae добавлена глюкоза, для определения количества колиформ – лактоза.
Определение количества бактерий семейства Enterobacteriaceae и колиформ Определение основано на способности микроорганизмов менять р. Н среды во время культивирования. Снижение значения р. Н среды в процессе культивирования обусловлено углеводным метаболизмом. В питательную среду добавлен 4 метил умбеллиферон, обладающий флуоресцентной способностью только при значениях р. Н ≥ 6. В качестве дополнительного источника углеводов в питательную среду для определения бактерий семейства Enterobacteriaceae добавлена глюкоза, для определения количества колиформ – лактоза.
 В процессе роста бактерии усваивают углеводы, что приводит к снижению уровняя р. Н среды прямо пропорционально численности популяции исследуемых микроорганизмов. Когда р. Н среды достигает значений ≤ 6, 4 метил умбеллиферон теряет способность к флуоресценции. Отсутствие флуоресцентнго сигнала считывается и фиксируется в автоматическом режиме ТЕМРО Reader. В зависимости от количества и объема положительных лунок, а так же разведения производится подсчет общего числа микроорганизмов в исходном образце методом наиболее вероятного числа в автоматическом режиме.
В процессе роста бактерии усваивают углеводы, что приводит к снижению уровняя р. Н среды прямо пропорционально численности популяции исследуемых микроорганизмов. Когда р. Н среды достигает значений ≤ 6, 4 метил умбеллиферон теряет способность к флуоресценции. Отсутствие флуоресцентнго сигнала считывается и фиксируется в автоматическом режиме ТЕМРО Reader. В зависимости от количества и объема положительных лунок, а так же разведения производится подсчет общего числа микроорганизмов в исходном образце методом наиболее вероятного числа в автоматическом режиме.
 Проведение испытания Определение количества аэробных мезофильных микроорганизмов в продуктах питания. Определение общего числа колиформ (БГКП) в продуктах питания Подсчет колиформ в продуктах питания Подсчет Eshcerichia coli в продуктах питания Подсчет энтеробактерий в продуктах питания Подсчет Staphyllococcus aureus в продуктах питания. Подсчет лактобактерий в продуктах питания. Определение микробного загрязнения объектов окружающей среды обитания методом смывов
Проведение испытания Определение количества аэробных мезофильных микроорганизмов в продуктах питания. Определение общего числа колиформ (БГКП) в продуктах питания Подсчет колиформ в продуктах питания Подсчет Eshcerichia coli в продуктах питания Подсчет энтеробактерий в продуктах питания Подсчет Staphyllococcus aureus в продуктах питания. Подсчет лактобактерий в продуктах питания. Определение микробного загрязнения объектов окружающей среды обитания методом смывов
 Обработка результатов После считывания карт, полученные результаты анализируются программным обеспечением. На основе количества положительных лунок, их объема, степени разведения программа рассчитывает результат в КОЕ/г или КОЕ/см 3 исходного образца или смыва методом наиболее вероятного числа. При исследовании объектов окружающей среды методом смывов количество микроорганизмов на 1 см 2 исследуемого образца вычисляют по формуле: М=(М 1 х V)/S, Где: М – количество микроорганизмов на 1 см 2, КОЕ/ см 2; М 1 – количество микроорганизмов в 1 мл смывной жидкости, КОЕ/ см 3; V – объем смывной жидкости, внесенной в питательную среду, см 3; S – площадь исследованной поверхности, см 2.
Обработка результатов После считывания карт, полученные результаты анализируются программным обеспечением. На основе количества положительных лунок, их объема, степени разведения программа рассчитывает результат в КОЕ/г или КОЕ/см 3 исходного образца или смыва методом наиболее вероятного числа. При исследовании объектов окружающей среды методом смывов количество микроорганизмов на 1 см 2 исследуемого образца вычисляют по формуле: М=(М 1 х V)/S, Где: М – количество микроорганизмов на 1 см 2, КОЕ/ см 2; М 1 – количество микроорганизмов в 1 мл смывной жидкости, КОЕ/ см 3; V – объем смывной жидкости, внесенной в питательную среду, см 3; S – площадь исследованной поверхности, см 2.
 Ограничение метода Неправильное заполнение карты (пустые лунки и/или остатки суспензии во флаконе после заполнения), а также нарушение правил забора и хранения образцов может привести к получению ложных результатов. Принимая во внимание то, что флуоресцентный сигнал может изменяться при интенсивной окраске исходного раствора, необходимо разведение таких образцов не менее 1/400. Не рекомендуется использовать наборы ТЕМРО для испытаний продуктов, обладающих высокой ферментативной активностью.
Ограничение метода Неправильное заполнение карты (пустые лунки и/или остатки суспензии во флаконе после заполнения), а также нарушение правил забора и хранения образцов может привести к получению ложных результатов. Принимая во внимание то, что флуоресцентный сигнал может изменяться при интенсивной окраске исходного раствора, необходимо разведение таких образцов не менее 1/400. Не рекомендуется использовать наборы ТЕМРО для испытаний продуктов, обладающих высокой ферментативной активностью.
 Станция пробоподготовки внесение образца и питательной среды в карты
Станция пробоподготовки внесение образца и питательной среды в карты
 Станция для считывание карт и выдача результата
Станция для считывание карт и выдача результата
 Станция для считывания
Станция для считывания

