Сиквенс как он есть вообще.ppt
- Количество слайдов: 86
 Современные методы анализа нуклеотидной последовательности ДНК
Современные методы анализа нуклеотидной последовательности ДНК
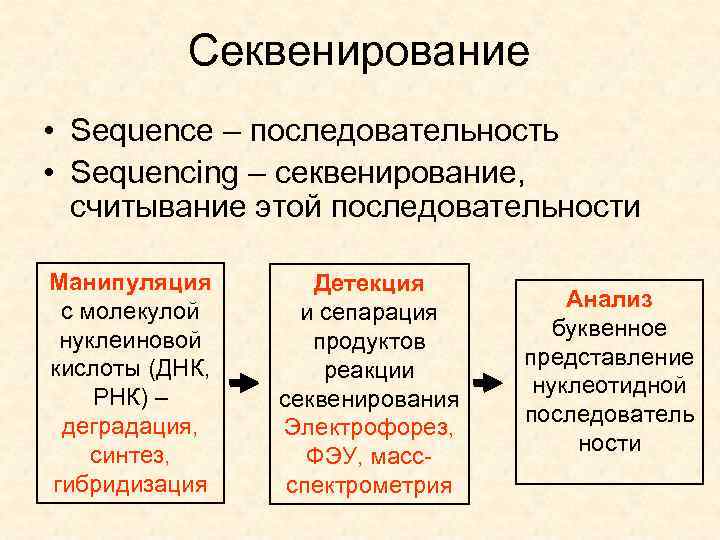 Секвенирование • Sequence – последовательность • Sequencing – секвенирование, считывание этой последовательности Манипуляция с молекулой нуклеиновой кислоты (ДНК, РНК) – деградация, синтез, гибридизация Детекция и сепарация продуктов реакции секвенирования Электрофорез, ФЭУ, массспектрометрия Анализ буквенное представление нуклеотидной последователь ности
Секвенирование • Sequence – последовательность • Sequencing – секвенирование, считывание этой последовательности Манипуляция с молекулой нуклеиновой кислоты (ДНК, РНК) – деградация, синтез, гибридизация Детекция и сепарация продуктов реакции секвенирования Электрофорез, ФЭУ, массспектрометрия Анализ буквенное представление нуклеотидной последователь ности
 • Секвенирование по Максаму-Гилберту (метод химической деградации) • Секвенирование по Сенгеру (метод ферментативного построения) • Методы высокопроизводительного геномного севенирования: ü Пиросеквенирование. Технология 454 Life Science ü «Мостиковая ПЦР» . Технология Solexa ü Секвенирование лигированием. Технология SOLIDTM System, Applied Biosystems • "Секвенирование единичной молекулы" (single molecule sequencing) ü Разработки Helicos Biosciences ü Секвенирование "через нанопоры"
• Секвенирование по Максаму-Гилберту (метод химической деградации) • Секвенирование по Сенгеру (метод ферментативного построения) • Методы высокопроизводительного геномного севенирования: ü Пиросеквенирование. Технология 454 Life Science ü «Мостиковая ПЦР» . Технология Solexa ü Секвенирование лигированием. Технология SOLIDTM System, Applied Biosystems • "Секвенирование единичной молекулы" (single molecule sequencing) ü Разработки Helicos Biosciences ü Секвенирование "через нанопоры"
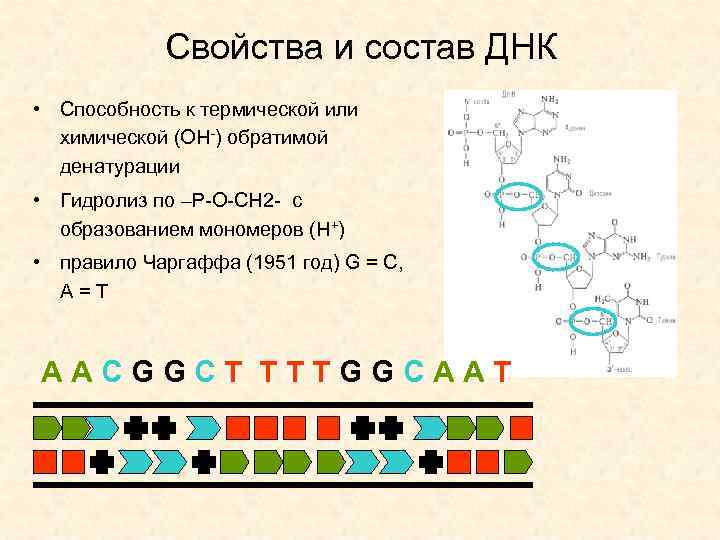 Свойства и состав ДНК • Способность к термической или химической (ОН-) обратимой денатурации • Гидролиз по –Р-О-СН 2 - с образованием мономеров (Н+) • правило Чаргаффа (1951 год) G = С, А = Т A A C G G C T T G G C A A T
Свойства и состав ДНК • Способность к термической или химической (ОН-) обратимой денатурации • Гидролиз по –Р-О-СН 2 - с образованием мономеров (Н+) • правило Чаргаффа (1951 год) G = С, А = Т A A C G G C T T G G C A A T
 Это уже почти история… A. M. Maxam, W. Gilbert, 1977 определение нуклеотидной последовательности ДНК методом химической деградации F. Sanger, 1977 определение нуклеотидной последовательности ДНК методом ферментативного построения
Это уже почти история… A. M. Maxam, W. Gilbert, 1977 определение нуклеотидной последовательности ДНК методом химической деградации F. Sanger, 1977 определение нуклеотидной последовательности ДНК методом ферментативного построения
 Это уже почти история… A. M. Maxam, W. Gilbert, 1977 F. Sanger, 1977 определение нуклеотидной P. Nyren и A. Lundin 1985 последовательности ДНК – 1987 методом ферментативного методом химической метод анализа ДНКпостроения деградации полимеразной активности, основанный на определении пирофосфата
Это уже почти история… A. M. Maxam, W. Gilbert, 1977 F. Sanger, 1977 определение нуклеотидной P. Nyren и A. Lundin 1985 последовательности ДНК – 1987 методом ферментативного методом химической метод анализа ДНКпостроения деградации полимеразной активности, основанный на определении пирофосфата
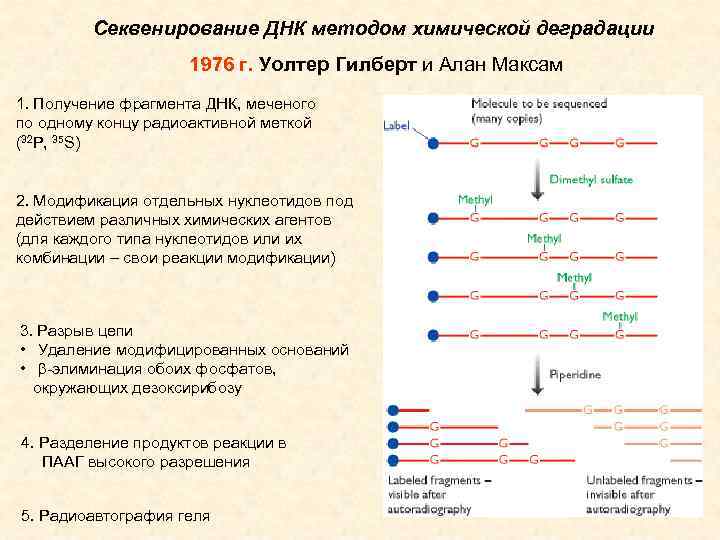 Секвенирование ДНК методом химической деградации 1976 г. Уолтер Гилберт и Алан Максам 1. Получение фрагмента ДНК, меченого по одному концу радиоактивной меткой (32 P, 35 S) 2. Модификация отдельных нуклеотидов под действием различных химических агентов (для каждого типа нуклеотидов или их комбинации – свои реакции модификации) 3. Разрыв цепи • Удаление модифицированных оснований • -элиминация обоих фосфатов, окружающих дезоксирибозу 4. Разделение продуктов реакции в ПААГ высокого разрешения 5. Радиоавтография геля
Секвенирование ДНК методом химической деградации 1976 г. Уолтер Гилберт и Алан Максам 1. Получение фрагмента ДНК, меченого по одному концу радиоактивной меткой (32 P, 35 S) 2. Модификация отдельных нуклеотидов под действием различных химических агентов (для каждого типа нуклеотидов или их комбинации – свои реакции модификации) 3. Разрыв цепи • Удаление модифицированных оснований • -элиминация обоих фосфатов, окружающих дезоксирибозу 4. Разделение продуктов реакции в ПААГ высокого разрешения 5. Радиоавтография геля
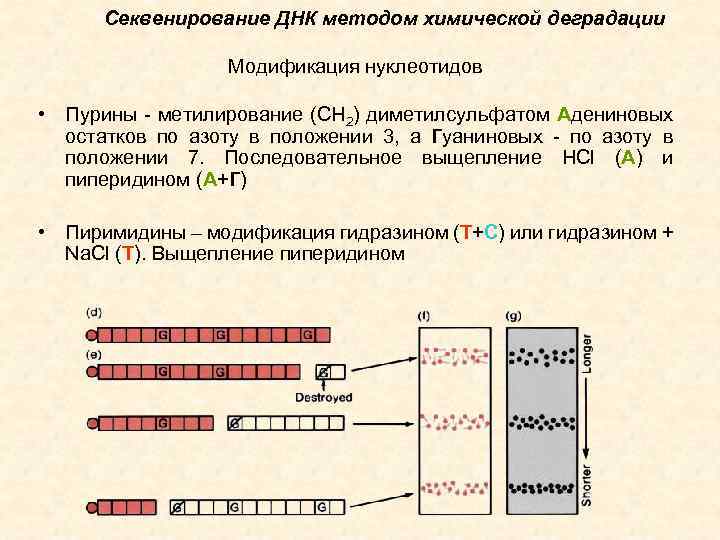 Секвенирование ДНК методом химической деградации Модификация нуклеотидов • Пурины - метилирование (СН 2) диметилсульфатом Адениновых остатков по азоту в положении 3, а Гуаниновых - по азоту в положении 7. Последовательное выщепление HCl (А) и пиперидином (А+Г) • Пиримидины – модификация гидразином (Т+С) или гидразином + Na. Cl (T). Выщепление пиперидином
Секвенирование ДНК методом химической деградации Модификация нуклеотидов • Пурины - метилирование (СН 2) диметилсульфатом Адениновых остатков по азоту в положении 3, а Гуаниновых - по азоту в положении 7. Последовательное выщепление HCl (А) и пиперидином (А+Г) • Пиримидины – модификация гидразином (Т+С) или гидразином + Na. Cl (T). Выщепление пиперидином
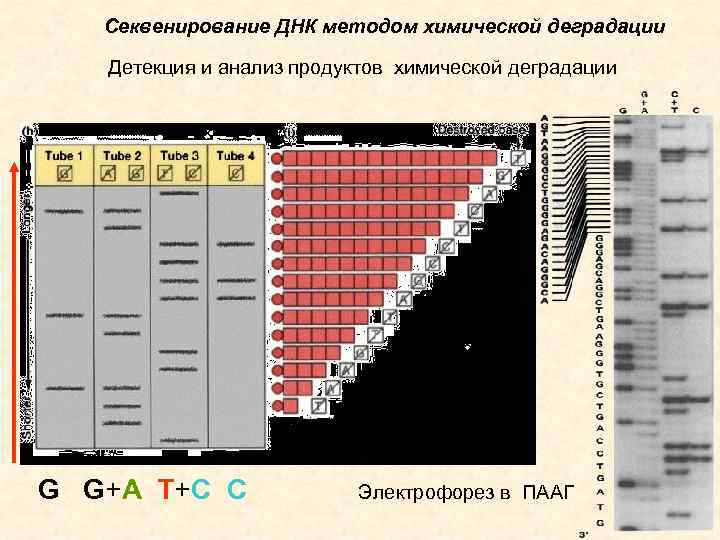 Секвенирование ДНК методом химической деградации Детекция и анализ продуктов химической деградации G G+A T+C C Электрофорез в ПААГ
Секвенирование ДНК методом химической деградации Детекция и анализ продуктов химической деградации G G+A T+C C Электрофорез в ПААГ
 Секвенирование ДНК методом химической деградации Преимущества Недостатки • Возможность анализа «сложных» участков ДНК с сильной вторичной структурой • относительно низкая производительность • высокотоксичные реагенты • Анализируется исходная последовательность ДНК, а не ее вновь синтезированная копия меньшая вероятность ошибки • Не требуется ничего знать об исходной последовательности (не нужны праймеры) • Нет ферментативных реакций Ø Применим только для одноцепочечных молекул ДНК длиной не более 150 н. о. Ø Практическое использование – контроль качества химического синтеза олигонуклеотидов
Секвенирование ДНК методом химической деградации Преимущества Недостатки • Возможность анализа «сложных» участков ДНК с сильной вторичной структурой • относительно низкая производительность • высокотоксичные реагенты • Анализируется исходная последовательность ДНК, а не ее вновь синтезированная копия меньшая вероятность ошибки • Не требуется ничего знать об исходной последовательности (не нужны праймеры) • Нет ферментативных реакций Ø Применим только для одноцепочечных молекул ДНК длиной не более 150 н. о. Ø Практическое использование – контроль качества химического синтеза олигонуклеотидов
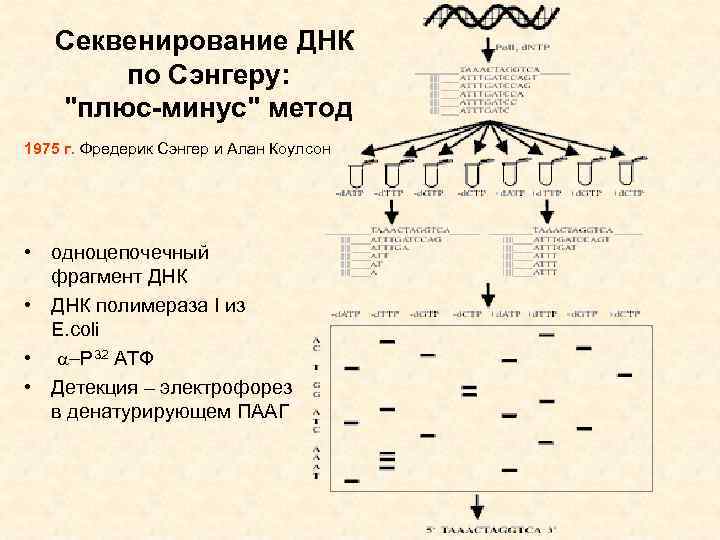 Секвенирование ДНК по Сэнгеру: "плюс-минус" метод 1975 г. Фредерик Сэнгер и Алан Коулсон • одноцепочечный фрагмент ДНК • ДНК полимераза I из E. coli • a-P 32 ATФ • Детекция – электрофорез в денатурирующем ПААГ
Секвенирование ДНК по Сэнгеру: "плюс-минус" метод 1975 г. Фредерик Сэнгер и Алан Коулсон • одноцепочечный фрагмент ДНК • ДНК полимераза I из E. coli • a-P 32 ATФ • Детекция – электрофорез в денатурирующем ПААГ
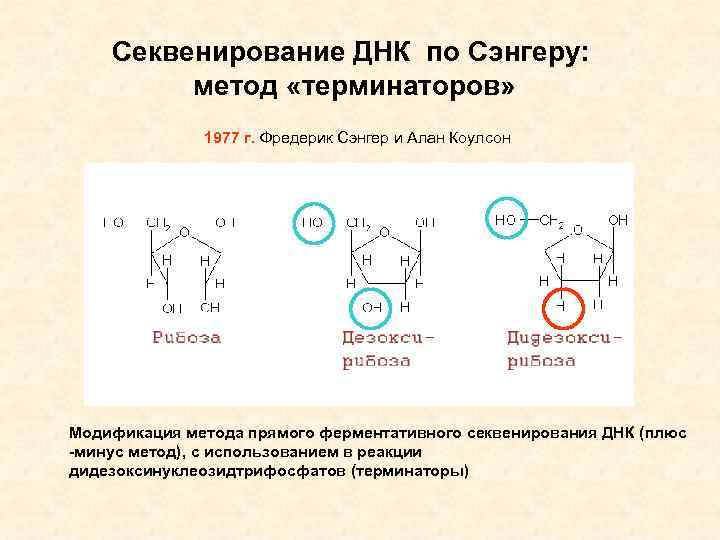 Секвенирование ДНК по Сэнгеру: метод «терминаторов» 1977 г. Фредерик Сэнгер и Алан Коулсон Модификация метода прямого ферментативного секвенирования ДНК (плюс -минус метод), с использованием в реакции дидезоксинуклеозидтрифосфатов (терминаторы)
Секвенирование ДНК по Сэнгеру: метод «терминаторов» 1977 г. Фредерик Сэнгер и Алан Коулсон Модификация метода прямого ферментативного секвенирования ДНК (плюс -минус метод), с использованием в реакции дидезоксинуклеозидтрифосфатов (терминаторы)
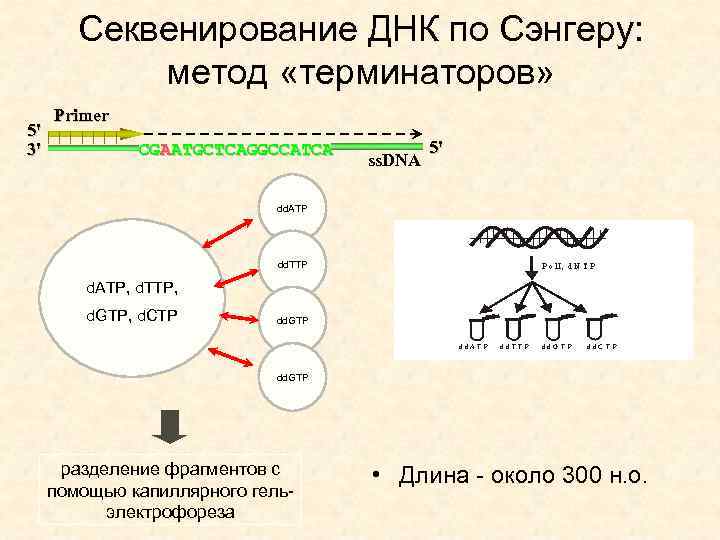 Секвенирование ДНК по Сэнгеру: метод «терминаторов» 5' 3' Primer CGAATGCTCAGGCCATCA ss. DNA 5' dd. ATP dd. TTP d. ATP, d. TTP, d. GTP, d. CTP dd. GTP разделение фрагментов с помощью капиллярного гельэлектрофореза • Длина - около 300 н. о.
Секвенирование ДНК по Сэнгеру: метод «терминаторов» 5' 3' Primer CGAATGCTCAGGCCATCA ss. DNA 5' dd. ATP dd. TTP d. ATP, d. TTP, d. GTP, d. CTP dd. GTP разделение фрагментов с помощью капиллярного гельэлектрофореза • Длина - около 300 н. о.
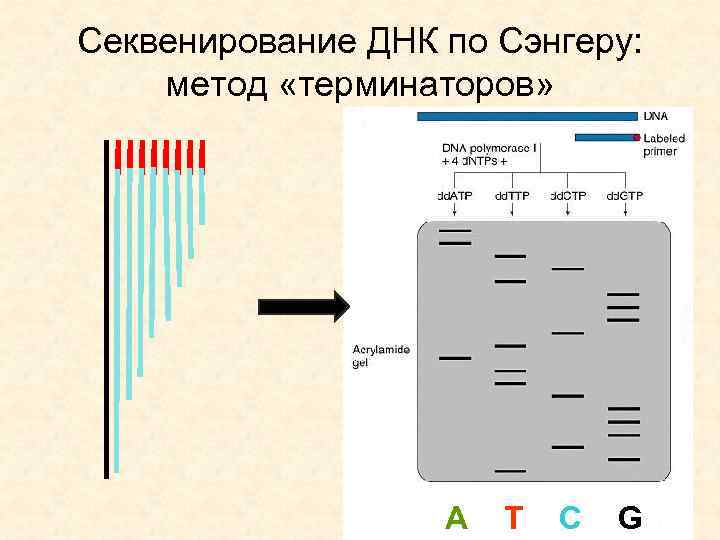 Секвенирование ДНК по Сэнгеру: метод «терминаторов» A T C G
Секвенирование ДНК по Сэнгеру: метод «терминаторов» A T C G
 Флуоресцентные красители Acridine 2 -(N-акридинил-4 -аминобутил)-1, 3 -пропандиол Pyrene 1 -пирен-бутановая кислота Dansyl 6 -(5 -диметилфминонафталин-1 сульфонил)аминопропанол R 110 JOE R 6 G TAMRA ROX FAM Dabsyl 5(6)-карбоксифлуоресцеин 5(6)-карбоксиродамин 110 6 -карбокси-4', 5'-дихлор-2', 7'-диметоксифлуоресцеин 5(6)-карбоксиродамин R 6 G 5(6)-карбокситетраметилродамин 5(6)-карбокси-Х-родамин 4 -((4 -(диметиламино)-фенил)азо)бензолсульфоновая кислота
Флуоресцентные красители Acridine 2 -(N-акридинил-4 -аминобутил)-1, 3 -пропандиол Pyrene 1 -пирен-бутановая кислота Dansyl 6 -(5 -диметилфминонафталин-1 сульфонил)аминопропанол R 110 JOE R 6 G TAMRA ROX FAM Dabsyl 5(6)-карбоксифлуоресцеин 5(6)-карбоксиродамин 110 6 -карбокси-4', 5'-дихлор-2', 7'-диметоксифлуоресцеин 5(6)-карбоксиродамин R 6 G 5(6)-карбокситетраметилродамин 5(6)-карбокси-Х-родамин 4 -((4 -(диметиламино)-фенил)азо)бензолсульфоновая кислота
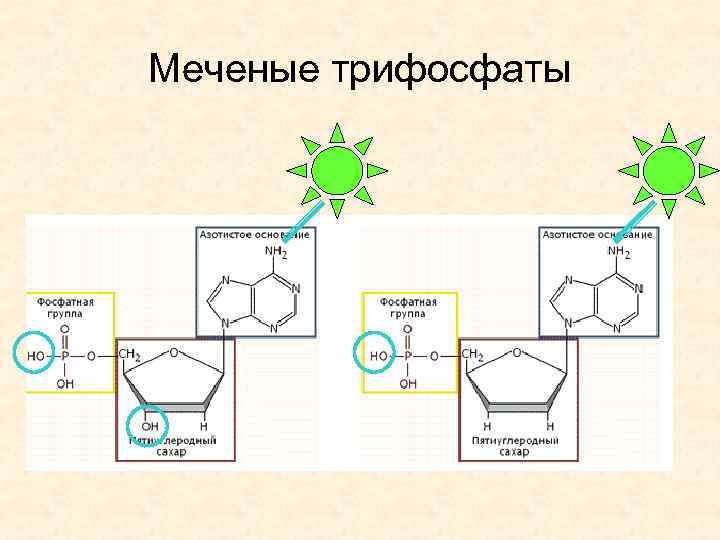 Меченые трифосфаты
Меченые трифосфаты
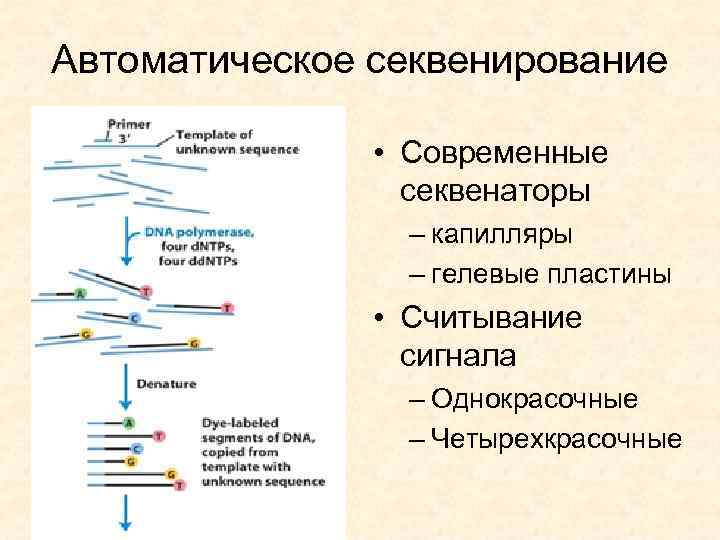 Автоматическое секвенирование • Современные секвенаторы – капилляры – гелевые пластины • Считывание сигнала – Однокрасочные – Четырехкрасочные
Автоматическое секвенирование • Современные секвенаторы – капилляры – гелевые пластины • Считывание сигнала – Однокрасочные – Четырехкрасочные
 Секвенирование на основе капиллярного электрофореза
Секвенирование на основе капиллярного электрофореза
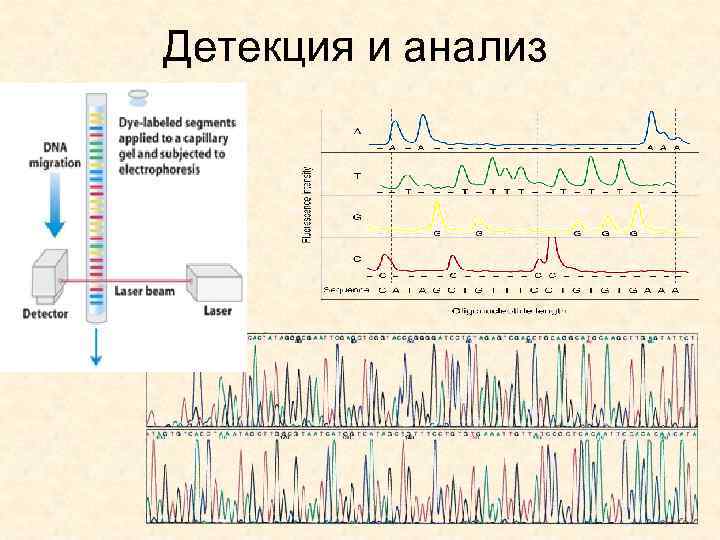 Детекция и анализ
Детекция и анализ
 Приборная база ABI PRISM® 3730 XL Genetic Analyzer (Applied Biosystems)
Приборная база ABI PRISM® 3730 XL Genetic Analyzer (Applied Biosystems)
 Секвенатор ABI Prism 3100 • 16 капилляров длиной 50 см в сборке. • Средняя длина чтения – 650 п. н. • Время рабочего цикла – 2, 5 часа. • Аргоновый лазер с длинами волн 488 и 514 нм для возбуждения флюоресценции. • Работает в 96 - и 384 -луночном форматах. • Автономен, не требует постоянного присутствия оператора. • Электрокинетический ввод образцов. • Ввод полимера в капилляры шприцевым насосом
Секвенатор ABI Prism 3100 • 16 капилляров длиной 50 см в сборке. • Средняя длина чтения – 650 п. н. • Время рабочего цикла – 2, 5 часа. • Аргоновый лазер с длинами волн 488 и 514 нм для возбуждения флюоресценции. • Работает в 96 - и 384 -луночном форматах. • Автономен, не требует постоянного присутствия оператора. • Электрокинетический ввод образцов. • Ввод полимера в капилляры шприцевым насосом
 Секвенатор ABI Prism 3730 XL • 96 капилляров длиной 50 см в сборке. • Средняя длина чтения – 850 п. н. • Время рабочего цикла – 2, 0 часа. • Аргоновый лазер с длинами волн 488 и 514 нм для возбуждения флюоресценции. • Работает в 96 - и 384 луночном форматах. • Автономен, не требует постоянного присутствия оператора. • Электрокинетический ввод образцов. • Ввод полимера в капилляры автономной насосной системой
Секвенатор ABI Prism 3730 XL • 96 капилляров длиной 50 см в сборке. • Средняя длина чтения – 850 п. н. • Время рабочего цикла – 2, 0 часа. • Аргоновый лазер с длинами волн 488 и 514 нм для возбуждения флюоресценции. • Работает в 96 - и 384 луночном форматах. • Автономен, не требует постоянного присутствия оператора. • Электрокинетический ввод образцов. • Ввод полимера в капилляры автономной насосной системой
 Факторы, влияющие на качество секвенирования • • Концентрация образца Тип образца Очистка образца Приборные особенности
Факторы, влияющие на качество секвенирования • • Концентрация образца Тип образца Очистка образца Приборные особенности
 Концентрация образца 100 -200 пар 1 -3 нг 200 -500 пар 500 -1000 пар 1000 -2000 пар 3 -10 нг 5 -20 нг 10 -40 нг Свыше 2000 пар 40 -100 нг Плазмиды Космиды, ВАС, геномы 200 -500 нг 1 мкг
Концентрация образца 100 -200 пар 1 -3 нг 200 -500 пар 500 -1000 пар 1000 -2000 пар 3 -10 нг 5 -20 нг 10 -40 нг Свыше 2000 пар 40 -100 нг Плазмиды Космиды, ВАС, геномы 200 -500 нг 1 мкг
 Sequence Scanner V 1. 0
Sequence Scanner V 1. 0
 Sequence Scanner V 1. 0
Sequence Scanner V 1. 0
 Мало!!!
Мало!!!
 Мало!!!
Мало!!!
 Мало!!!
Мало!!!
 Много!!!
Много!!!
 Много!!!
Много!!!
 Много!!!
Много!!!
 Много!!!
Много!!!
 Много!!!
Много!!!
 С генома
С генома
 Недоочистка SAP, Exonuclease I Очистка через гель
Недоочистка SAP, Exonuclease I Очистка через гель
 Недоочистка
Недоочистка
 Недоочистка
Недоочистка
 Праймеры!!!
Праймеры!!!
 Особенности прибора (3730)
Особенности прибора (3730)
 Особенности прибора (3100)
Особенности прибора (3100)
 Геномное секвенирование
Геномное секвенирование
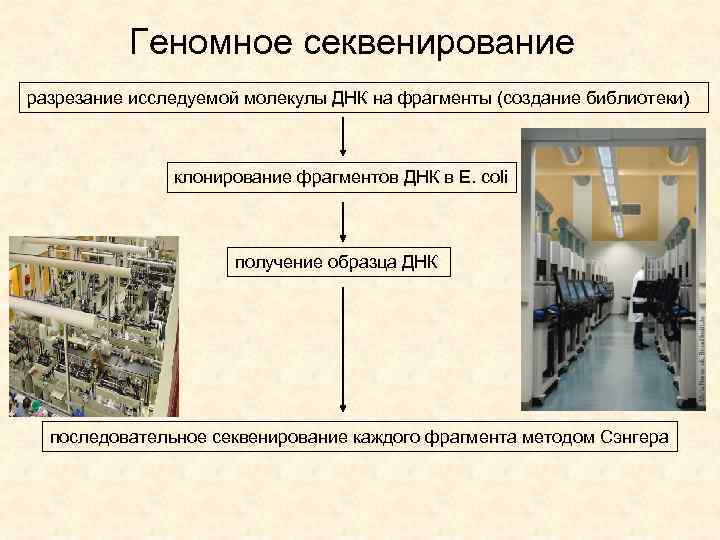 Геномное секвенирование разрезание исследуемой молекулы ДНК на фрагменты (создание библиотеки) клонирование фрагментов ДНК в E. сoli получение образца ДНК последовательное секвенирование каждого фрагмента методом Сэнгера
Геномное секвенирование разрезание исследуемой молекулы ДНК на фрагменты (создание библиотеки) клонирование фрагментов ДНК в E. сoli получение образца ДНК последовательное секвенирование каждого фрагмента методом Сэнгера
 • 1990 – 2001 (2003) гг. Проект "Геном человека" (США) • Расшифровано 3 млрд. нуклеотидных пар • Средняя стоимость проекта – 3 млрд. US-долларов (1 доллар/нп) • В начале проекта цена прочтения одного основания – 10 долларов. В конце проекта – 5 центов. • 2003 г. J. Craig Venter Science Foundation объявил конкурс: приз в 0. 5 млн. USD тому, кто снизит общую стоимость секвенирования генома человека (или генома похожей сложности) до 1000 долларов • 2006 г. X Prize Foundation объявил розыгрыш приза в 10 млн. $ за секвенирование геномов. Условие - 100 человеческих геномов за 10 дней, по цене не более 10 000 $ за геном «…говорят, что скоро в программе Олимпийских игр появится новый вид спорта — геномное секвенирование…»
• 1990 – 2001 (2003) гг. Проект "Геном человека" (США) • Расшифровано 3 млрд. нуклеотидных пар • Средняя стоимость проекта – 3 млрд. US-долларов (1 доллар/нп) • В начале проекта цена прочтения одного основания – 10 долларов. В конце проекта – 5 центов. • 2003 г. J. Craig Venter Science Foundation объявил конкурс: приз в 0. 5 млн. USD тому, кто снизит общую стоимость секвенирования генома человека (или генома похожей сложности) до 1000 долларов • 2006 г. X Prize Foundation объявил розыгрыш приза в 10 млн. $ за секвенирование геномов. Условие - 100 человеческих геномов за 10 дней, по цене не более 10 000 $ за геном «…говорят, что скоро в программе Олимпийских игр появится новый вид спорта — геномное секвенирование…»
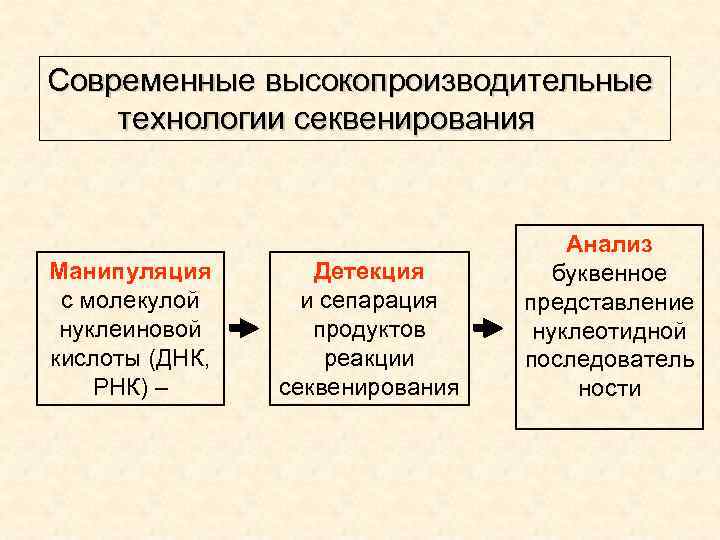 Современные высокопроизводительные технологии секвенирования Манипуляция с молекулой нуклеиновой кислоты (ДНК, РНК) – Детекция и сепарация продуктов реакции секвенирования Анализ буквенное представление нуклеотидной последователь ности
Современные высокопроизводительные технологии секвенирования Манипуляция с молекулой нуклеиновой кислоты (ДНК, РНК) – Детекция и сепарация продуктов реакции секвенирования Анализ буквенное представление нуклеотидной последователь ности
 Современные технологии секвенирования Высокопроизводительное параллельное секвенирование популяций клонально амплифицированных молекул ДНК "Секвенирование единичных молекул" (Single Molecule Sequencing)
Современные технологии секвенирования Высокопроизводительное параллельное секвенирование популяций клонально амплифицированных молекул ДНК "Секвенирование единичных молекул" (Single Molecule Sequencing)
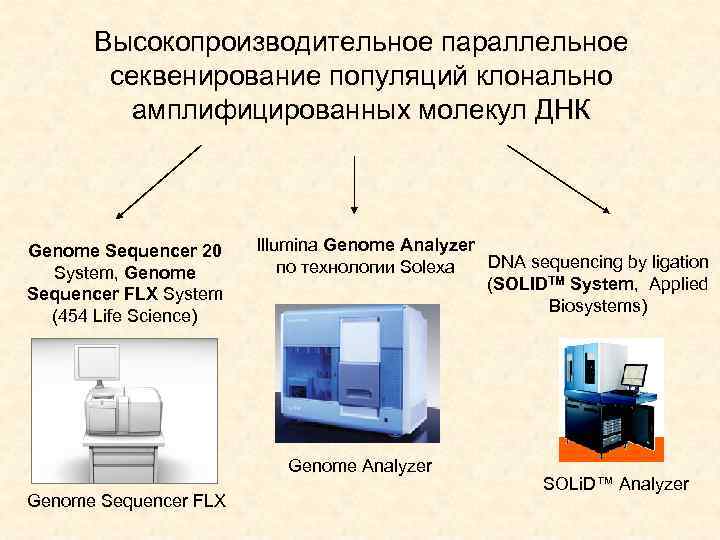 Высокопроизводительное параллельное секвенирование популяций клонально амплифицированных молекул ДНК Genome Sequencer 20 System, Genome Sequencer FLX System (454 Life Science) Illumina Genome Analyzer DNA sequencing by ligation по технологии Solexa (SOLIDTM System, Applied Biosystems) Genome Analyzer Genome Sequencer FLX SOLi. D™ Analyzer
Высокопроизводительное параллельное секвенирование популяций клонально амплифицированных молекул ДНК Genome Sequencer 20 System, Genome Sequencer FLX System (454 Life Science) Illumina Genome Analyzer DNA sequencing by ligation по технологии Solexa (SOLIDTM System, Applied Biosystems) Genome Analyzer Genome Sequencer FLX SOLi. D™ Analyzer
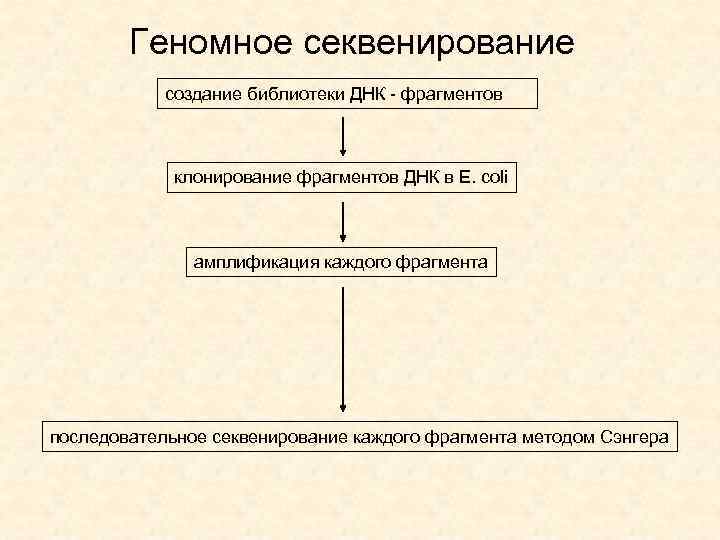 Геномное секвенирование создание библиотеки ДНК - фрагментов клонирование фрагментов ДНК в E. сoli амплификация каждого фрагмента последовательное секвенирование каждого фрагмента методом Сэнгера
Геномное секвенирование создание библиотеки ДНК - фрагментов клонирование фрагментов ДНК в E. сoli амплификация каждого фрагмента последовательное секвенирование каждого фрагмента методом Сэнгера
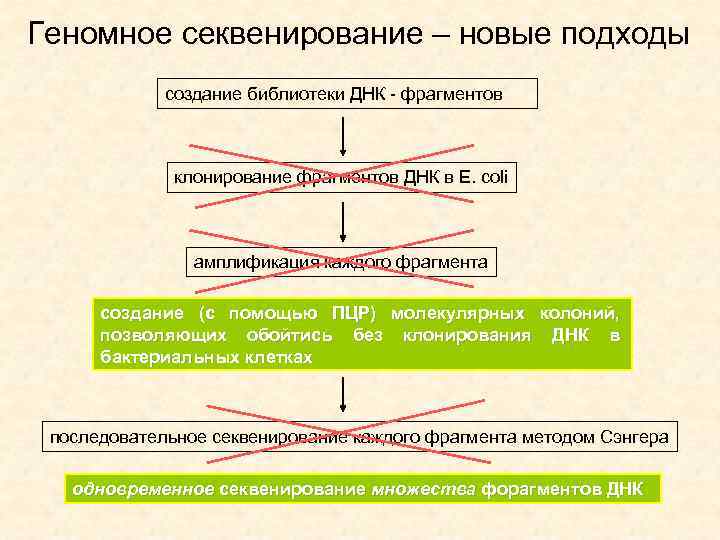 Геномное секвенирование – новые подходы создание библиотеки ДНК - фрагментов клонирование фрагментов ДНК в E. сoli амплификация каждого фрагмента создание (с помощью ПЦР) молекулярных колоний, позволяющих обойтись без клонирования ДНК в бактериальных клетках последовательное секвенирование каждого фрагмента методом Сэнгера одновременное секвенирование множества форагментов ДНК
Геномное секвенирование – новые подходы создание библиотеки ДНК - фрагментов клонирование фрагментов ДНК в E. сoli амплификация каждого фрагмента создание (с помощью ПЦР) молекулярных колоний, позволяющих обойтись без клонирования ДНК в бактериальных клетках последовательное секвенирование каждого фрагмента методом Сэнгера одновременное секвенирование множества форагментов ДНК
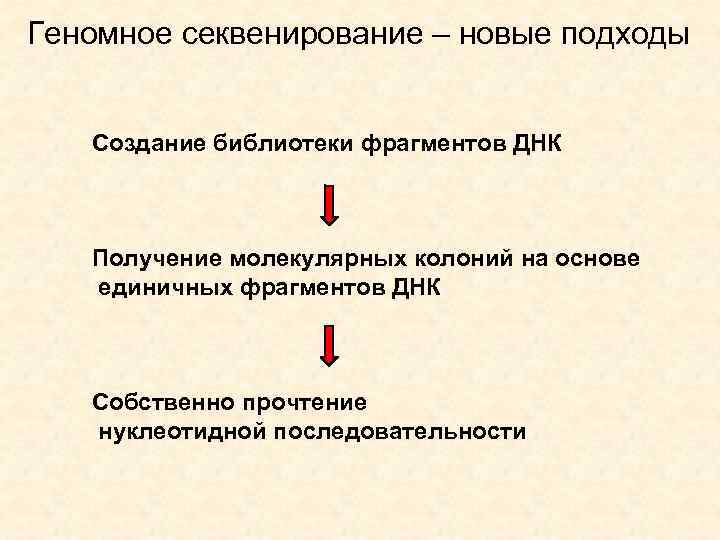 Геномное секвенирование – новые подходы Создание библиотеки фрагментов ДНК Получение молекулярных колоний на основе единичных фрагментов ДНК Собственно прочтение нуклеотидной последовательности
Геномное секвенирование – новые подходы Создание библиотеки фрагментов ДНК Получение молекулярных колоний на основе единичных фрагментов ДНК Собственно прочтение нуклеотидной последовательности
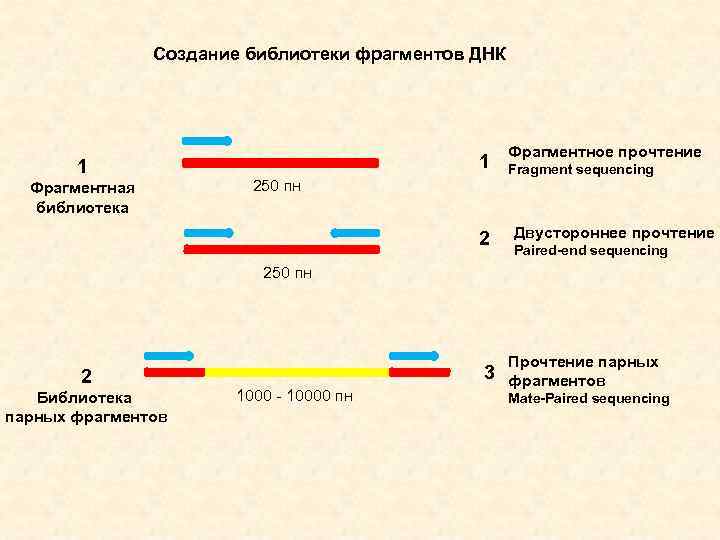 Создание библиотеки фрагментов ДНК 1 Фрагментная библиотека 1 250 пн 2 Фрагментное прочтение Fragment sequencing Двустороннее прочтение Paired-end sequencing 250 пн 2 Библиотека парных фрагментов 3 1000 - 10000 пн Прочтение парных фрагментов Mate-Paired sequencing
Создание библиотеки фрагментов ДНК 1 Фрагментная библиотека 1 250 пн 2 Фрагментное прочтение Fragment sequencing Двустороннее прочтение Paired-end sequencing 250 пн 2 Библиотека парных фрагментов 3 1000 - 10000 пн Прочтение парных фрагментов Mate-Paired sequencing
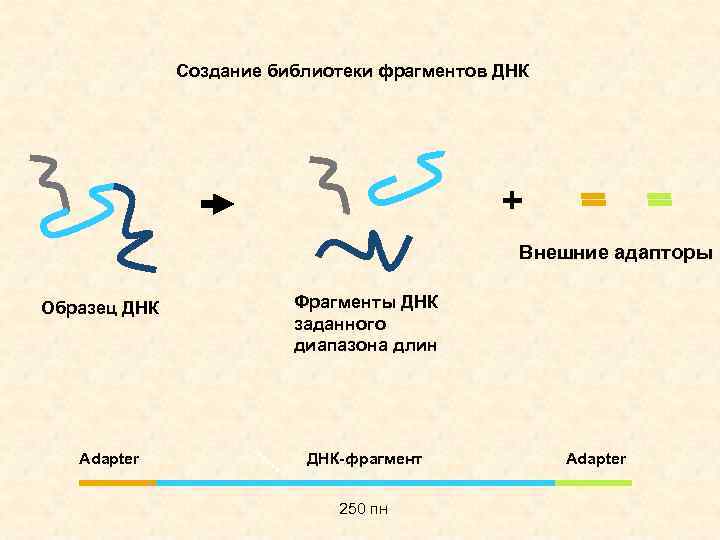 Создание библиотеки фрагментов ДНК + Внешние адапторы Образец ДНК Adapter Фрагменты ДНК заданного диапазона длин ДНК-фрагмент 250 пн Adapter
Создание библиотеки фрагментов ДНК + Внешние адапторы Образец ДНК Adapter Фрагменты ДНК заданного диапазона длин ДНК-фрагмент 250 пн Adapter
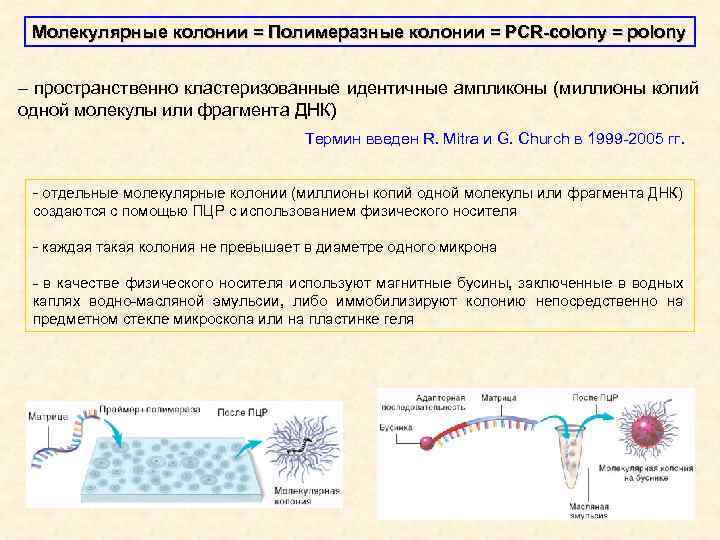 Молекулярные колонии = Полимеразные колонии = PCR-colony = polony – пространственно кластеризованные идентичные ампликоны (миллионы копий одной молекулы или фрагмента ДНК) Термин введен R. Mitra и G. Church в 1999 -2005 гг. - отдельные молекулярные колонии (миллионы копий одной молекулы или фрагмента ДНК) создаются с помощью ПЦР с использованием физического носителя - каждая такая колония не превышает в диаметре одного микрона - в качестве физического носителя используют магнитные бусины, заключенные в водных каплях водно-масляной эмульсии, либо иммобилизируют колонию непосредственно на предметном стекле микроскопа или на пластинке геля
Молекулярные колонии = Полимеразные колонии = PCR-colony = polony – пространственно кластеризованные идентичные ампликоны (миллионы копий одной молекулы или фрагмента ДНК) Термин введен R. Mitra и G. Church в 1999 -2005 гг. - отдельные молекулярные колонии (миллионы копий одной молекулы или фрагмента ДНК) создаются с помощью ПЦР с использованием физического носителя - каждая такая колония не превышает в диаметре одного микрона - в качестве физического носителя используют магнитные бусины, заключенные в водных каплях водно-масляной эмульсии, либо иммобилизируют колонию непосредственно на предметном стекле микроскопа или на пластинке геля
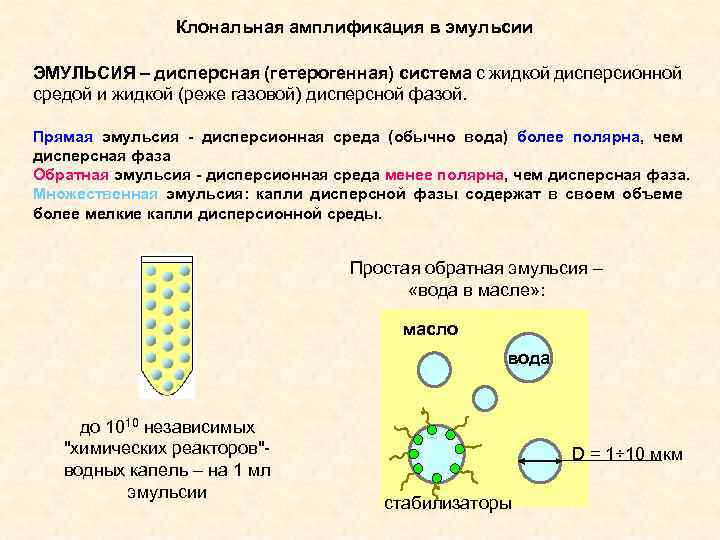 Клональная амплификация в эмульсии ЭМУЛЬСИЯ – дисперсная (гетерогенная) система с жидкой дисперсионной средой и жидкой (реже газовой) дисперсной фазой. Прямая эмульсия - дисперсионная среда (обычно вода) более полярна, чем дисперсная фаза Обратная эмульсия - дисперсионная среда менее полярна, чем дисперсная фаза. Множественная эмульсия: капли дисперсной фазы содержат в своем объеме более мелкие капли дисперсионной среды. Простая обратная эмульсия – «вода в масле» : масло вода до 1010 независимых "химических реакторов"- водных капель – на 1 мл эмульсии D = 1÷ 10 мкм стабилизаторы
Клональная амплификация в эмульсии ЭМУЛЬСИЯ – дисперсная (гетерогенная) система с жидкой дисперсионной средой и жидкой (реже газовой) дисперсной фазой. Прямая эмульсия - дисперсионная среда (обычно вода) более полярна, чем дисперсная фаза Обратная эмульсия - дисперсионная среда менее полярна, чем дисперсная фаза. Множественная эмульсия: капли дисперсной фазы содержат в своем объеме более мелкие капли дисперсионной среды. Простая обратная эмульсия – «вода в масле» : масло вода до 1010 независимых "химических реакторов"- водных капель – на 1 мл эмульсии D = 1÷ 10 мкм стабилизаторы
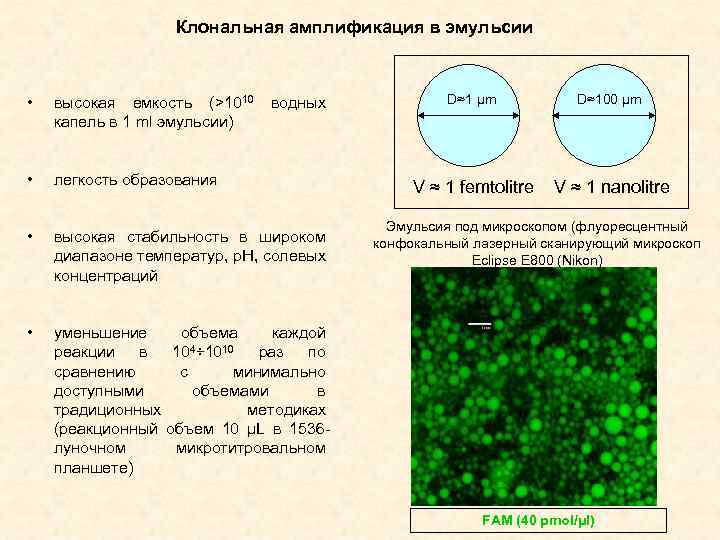 Клональная амплификация в эмульсии • высокая емкость (>1010 водных капель в 1 ml эмульсии) • легкость образования • высокая стабильность в широком диапазоне температур, р. Н, солевых концентраций • D≈1 μm D≈100 μm V ≈ 1 femtolitre V ≈ 1 nanolitre уменьшение объема каждой реакции в 104÷ 1010 раз по сравнению с минимально доступными объемами в традиционных методиках (реакционный объем 10 μL в 1536 луночном микротитровальном планшете) Эмульсия под микроскопом (флуоресцентный конфокальный лазерный сканирующий микроскоп Eclipse E 800 (Nikon) FAM (40 pmol/μl)
Клональная амплификация в эмульсии • высокая емкость (>1010 водных капель в 1 ml эмульсии) • легкость образования • высокая стабильность в широком диапазоне температур, р. Н, солевых концентраций • D≈1 μm D≈100 μm V ≈ 1 femtolitre V ≈ 1 nanolitre уменьшение объема каждой реакции в 104÷ 1010 раз по сравнению с минимально доступными объемами в традиционных методиках (реакционный объем 10 μL в 1536 луночном микротитровальном планшете) Эмульсия под микроскопом (флуоресцентный конфокальный лазерный сканирующий микроскоп Eclipse E 800 (Nikon) FAM (40 pmol/μl)
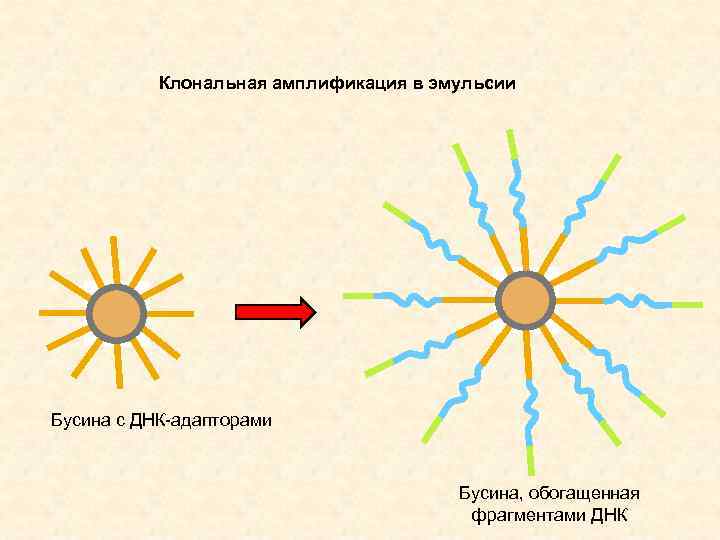 Клональная амплификация в эмульсии Бусина с ДНК-адапторами Бусина, обогащенная фрагментами ДНК
Клональная амплификация в эмульсии Бусина с ДНК-адапторами Бусина, обогащенная фрагментами ДНК
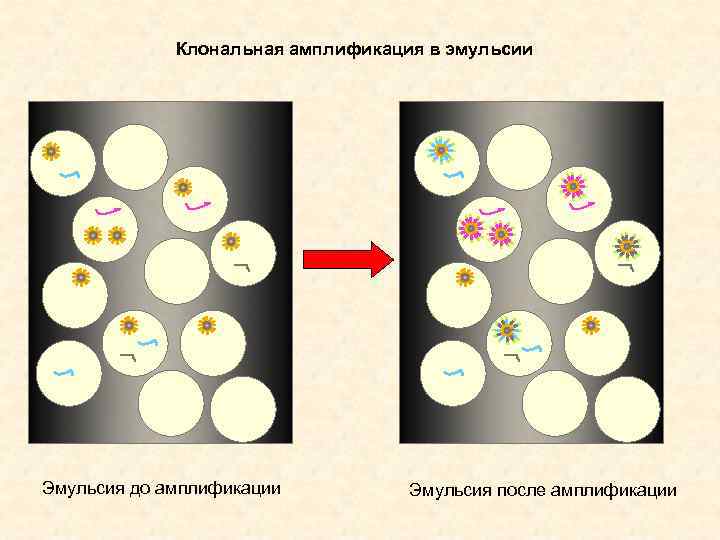 Клональная амплификация в эмульсии Эмульсия до амплификации Эмульсия после амплификации
Клональная амплификация в эмульсии Эмульсия до амплификации Эмульсия после амплификации
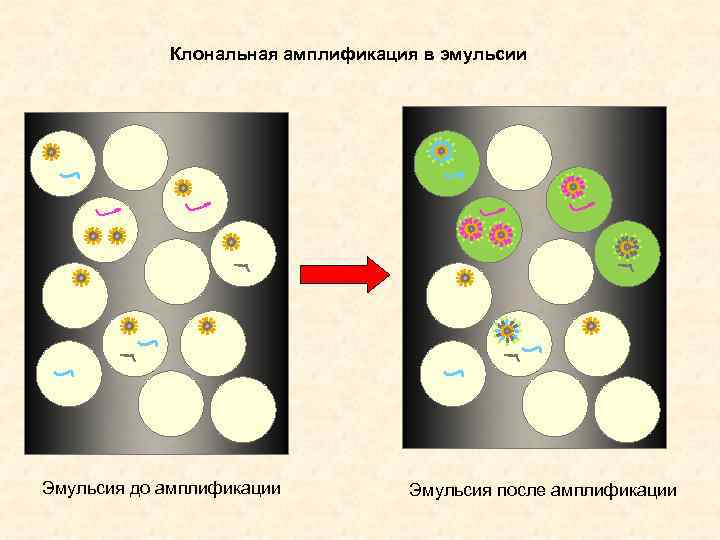 Клональная амплификация в эмульсии Эмульсия до амплификации Эмульсия после амплификации
Клональная амплификация в эмульсии Эмульсия до амплификации Эмульсия после амплификации
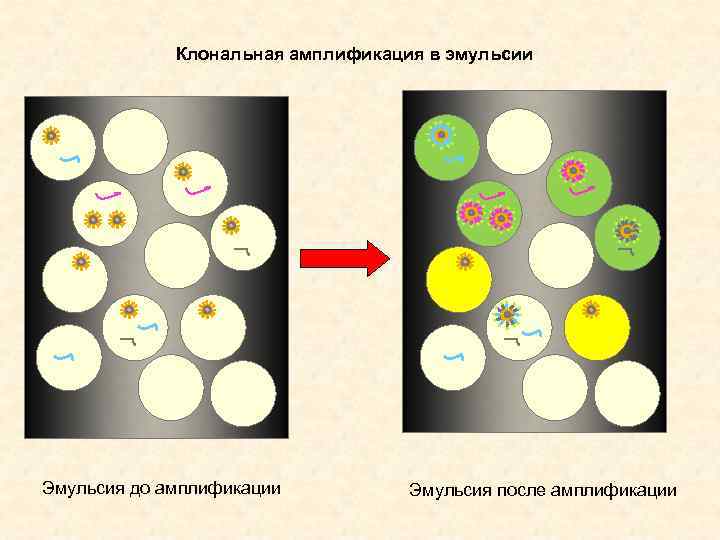 Клональная амплификация в эмульсии Эмульсия до амплификации Эмульсия после амплификации
Клональная амплификация в эмульсии Эмульсия до амплификации Эмульсия после амплификации
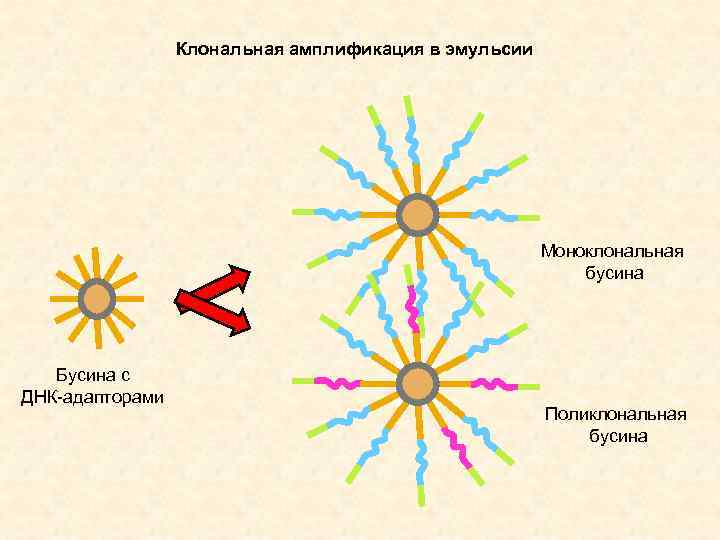 Клональная амплификация в эмульсии Моноклональная бусина Бусина с ДНК-адапторами Поликлональная бусина
Клональная амплификация в эмульсии Моноклональная бусина Бусина с ДНК-адапторами Поликлональная бусина
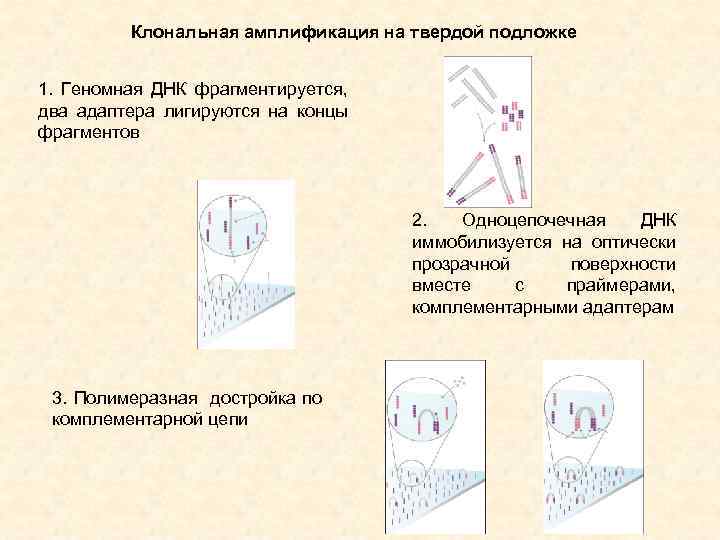 Клональная амплификация на твердой подложке 1. Геномная ДНК фрагментируется, два адаптера лигируются на концы фрагментов 2. Одноцепочечная ДНК иммобилизуется на оптически прозрачной поверхности вместе с праймерами, комплементарными адаптерам 3. Полимеразная достройка по комплементарной цепи
Клональная амплификация на твердой подложке 1. Геномная ДНК фрагментируется, два адаптера лигируются на концы фрагментов 2. Одноцепочечная ДНК иммобилизуется на оптически прозрачной поверхности вместе с праймерами, комплементарными адаптерам 3. Полимеразная достройка по комплементарной цепи
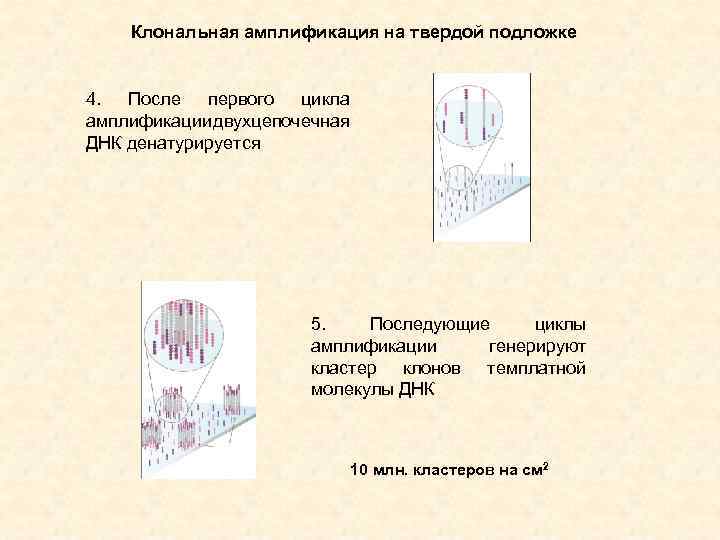 Клональная амплификация на твердой подложке 4. После первого цикла амплификации двухцепочечная ДНК денатурируется 5. Последующие циклы амплификации генерируют кластер клонов темплатной молекулы ДНК 10 млн. кластеров на см 2
Клональная амплификация на твердой подложке 4. После первого цикла амплификации двухцепочечная ДНК денатурируется 5. Последующие циклы амплификации генерируют кластер клонов темплатной молекулы ДНК 10 млн. кластеров на см 2
 454 SEQUENCINGTM TECHNOLOGY 454 Life Science Corp. , Roche Diagnostics Margulies et al, 2005; Leamon, 2003; Dressman, 2003 и др. • Genome Sequencer 20 System • Roche (454) Genome Sequencer FLX System 1 Создание библиотеки - стандартно 2 Клональная амплификация- эмульсионная ПЦР 3 Ключевой момент - пиросеквенирование
454 SEQUENCINGTM TECHNOLOGY 454 Life Science Corp. , Roche Diagnostics Margulies et al, 2005; Leamon, 2003; Dressman, 2003 и др. • Genome Sequencer 20 System • Roche (454) Genome Sequencer FLX System 1 Создание библиотеки - стандартно 2 Клональная амплификация- эмульсионная ПЦР 3 Ключевой момент - пиросеквенирование
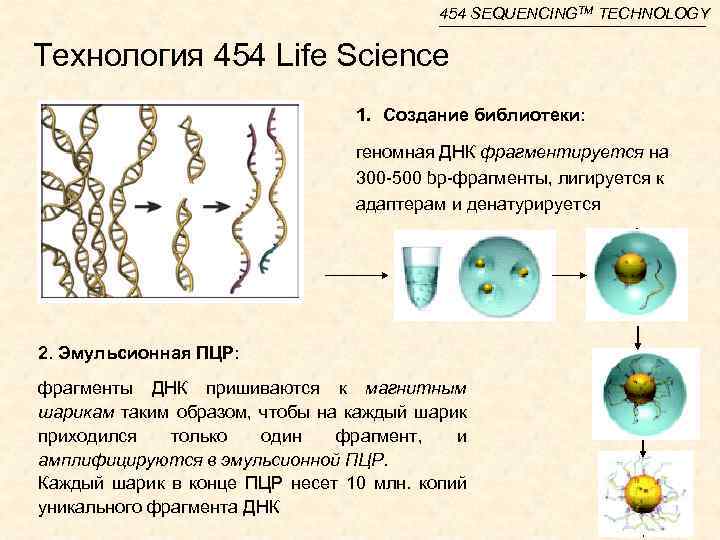 454 SEQUENCINGTM TECHNOLOGY Технология 454 Life Science 1. Создание библиотеки: геномная ДНК фрагментируется на 300 -500 bp-фрагменты, лигируется к адаптерам и денатурируется 2. Эмульсионная ПЦР: фрагменты ДНК пришиваются к магнитным шарикам таким образом, чтобы на каждый шарик приходился только один фрагмент, и амплифицируются в эмульсионной ПЦР. Каждый шарик в конце ПЦР несет 10 млн. копий уникального фрагмента ДНК
454 SEQUENCINGTM TECHNOLOGY Технология 454 Life Science 1. Создание библиотеки: геномная ДНК фрагментируется на 300 -500 bp-фрагменты, лигируется к адаптерам и денатурируется 2. Эмульсионная ПЦР: фрагменты ДНК пришиваются к магнитным шарикам таким образом, чтобы на каждый шарик приходился только один фрагмент, и амплифицируются в эмульсионной ПЦР. Каждый шарик в конце ПЦР несет 10 млн. копий уникального фрагмента ДНК
 454 SEQUENCINGTM TECHNOLOGY 3. Иммобилизация на твердой поверхности: эмульсия разбивается, шарики, несущие клоны одноцепочечной ДНК, распределяются в лунки специально разработанного оптоволоконного чипа Pico. Titer. Plate. TM [Leamon, 2003] Один шарик – одна лунка! 4. Пиросеквенирование: необходимые реагенты, иммобилизованные на шариках меньшего размера, поступают в каждую лунку
454 SEQUENCINGTM TECHNOLOGY 3. Иммобилизация на твердой поверхности: эмульсия разбивается, шарики, несущие клоны одноцепочечной ДНК, распределяются в лунки специально разработанного оптоволоконного чипа Pico. Titer. Plate. TM [Leamon, 2003] Один шарик – одна лунка! 4. Пиросеквенирование: необходимые реагенты, иммобилизованные на шариках меньшего размера, поступают в каждую лунку
 454 SEQUENCINGTM TECHNOLOGY Pico. Titer. Plate. TM • - это срез блока, полученного путём вытягивания и сплавления оптических волокон • Каждое волокно имеет сердечник, который затем вытравливается, образуя лунки ≈ 55 мкм глубиной, диаметром 44 мкм, с расстоянием ≈ 50 мкм между центрами соседних лунок • Объём лунки — 75 пиколитров • Плотность размещения лунок на поверхности слайда — 480 лунок на квадратный миллиметр • Каждый слайд несёт около 1, 6 миллионов лунок, в каждую из которых попадает одна бусинка с ДНК-матрицей • Лунки достаточно глубоки, чтобы бусинки, несущие ДНК-матрицу, не выскакивали из них под действием конвекции • Лунки достаточно мелкие для осуществления быстрой диффузии нуклеотидов в лунку и быстрого вымывания оставшихся нуклеотидов и продуктов реакции в конце каждого цикла 1. 6 млн. отдельных PCR реакций в объеме 75 p. L
454 SEQUENCINGTM TECHNOLOGY Pico. Titer. Plate. TM • - это срез блока, полученного путём вытягивания и сплавления оптических волокон • Каждое волокно имеет сердечник, который затем вытравливается, образуя лунки ≈ 55 мкм глубиной, диаметром 44 мкм, с расстоянием ≈ 50 мкм между центрами соседних лунок • Объём лунки — 75 пиколитров • Плотность размещения лунок на поверхности слайда — 480 лунок на квадратный миллиметр • Каждый слайд несёт около 1, 6 миллионов лунок, в каждую из которых попадает одна бусинка с ДНК-матрицей • Лунки достаточно глубоки, чтобы бусинки, несущие ДНК-матрицу, не выскакивали из них под действием конвекции • Лунки достаточно мелкие для осуществления быстрой диффузии нуклеотидов в лунку и быстрого вымывания оставшихся нуклеотидов и продуктов реакции в конце каждого цикла 1. 6 млн. отдельных PCR реакций в объеме 75 p. L
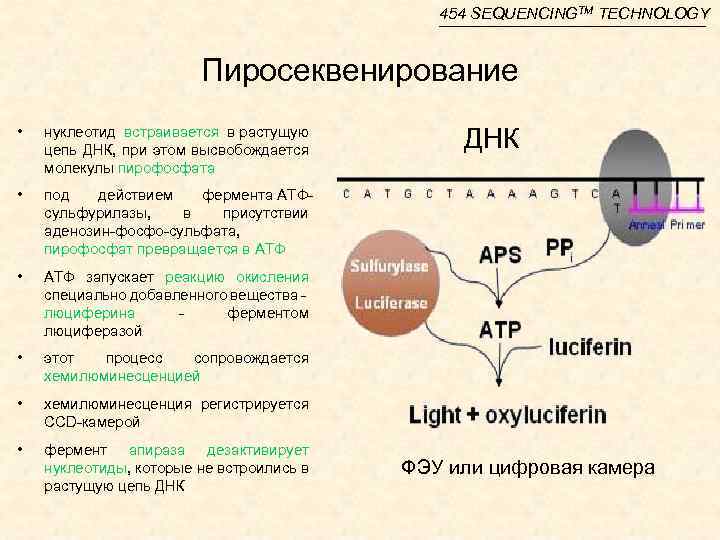 454 SEQUENCINGTM TECHNOLOGY Пиросеквенирование • нуклеотид встраивается в растущую цепь ДНК, при этом высвобождается молекулы пирофосфата • под действием фермента АТФсульфурилазы, в присутствии аденозин-фосфо-сульфата, пирофосфат превращается в АТФ • АТФ запускает реакцию окисления специально добавленного вещества - люциферина - ферментом люциферазой • этот процесс сопровождается хемилюминесценцией • хемилюминесценция регистрируется CCD-камерой • фермент апираза дезактивирует нуклеотиды, которые не встроились в растущую цепь ДНК ФЭУ или цифровая камера
454 SEQUENCINGTM TECHNOLOGY Пиросеквенирование • нуклеотид встраивается в растущую цепь ДНК, при этом высвобождается молекулы пирофосфата • под действием фермента АТФсульфурилазы, в присутствии аденозин-фосфо-сульфата, пирофосфат превращается в АТФ • АТФ запускает реакцию окисления специально добавленного вещества - люциферина - ферментом люциферазой • этот процесс сопровождается хемилюминесценцией • хемилюминесценция регистрируется CCD-камерой • фермент апираза дезактивирует нуклеотиды, которые не встроились в растущую цепь ДНК ФЭУ или цифровая камера
 454 SEQUENCINGTM TECHNOLOGY • Один цикл секвенирования (run, "прогон") – примерно 5 ч. • Один цикл - 200, 000 ÷ 350, 000 реакций, а теперь уже 1. 6 млн. реакций! • В каждой реакции изначально прочитывалось около 100 оснований, потом 250, а теперь уже около 400 • В 2005 году по технологии Life Sciences за один раз (!!!) был расшифрован 600 000 -нуклеотидный геном бактерии Mycoplasma genitalium с точностью 99, 4%. Весь процесс занял примерно одни сутки
454 SEQUENCINGTM TECHNOLOGY • Один цикл секвенирования (run, "прогон") – примерно 5 ч. • Один цикл - 200, 000 ÷ 350, 000 реакций, а теперь уже 1. 6 млн. реакций! • В каждой реакции изначально прочитывалось около 100 оснований, потом 250, а теперь уже около 400 • В 2005 году по технологии Life Sciences за один раз (!!!) был расшифрован 600 000 -нуклеотидный геном бактерии Mycoplasma genitalium с точностью 99, 4%. Весь процесс занял примерно одни сутки
 SOLEXA CLONAL SINGLE MOLECULE ARRAY Illumina Genome Analyzer по технологии Solexa Bennett, 2004; Adessi et al. , 2000 Genome Analyzer 1 Создание библиотеки - стандартно 2 Ключевой момент – "мостиковая ПЦР" (bridge PCR) "мостиковая ПЦР" на поверхности стекла 3 Секвенирование – по методу Сэнгера
SOLEXA CLONAL SINGLE MOLECULE ARRAY Illumina Genome Analyzer по технологии Solexa Bennett, 2004; Adessi et al. , 2000 Genome Analyzer 1 Создание библиотеки - стандартно 2 Ключевой момент – "мостиковая ПЦР" (bridge PCR) "мостиковая ПЦР" на поверхности стекла 3 Секвенирование – по методу Сэнгера
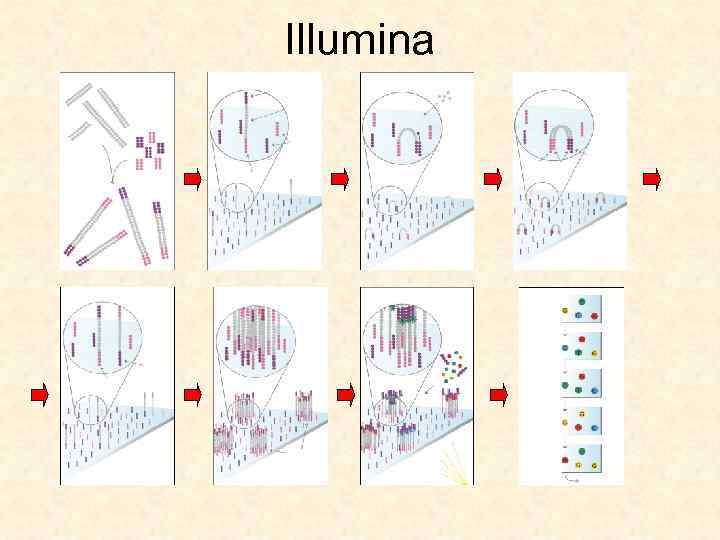 Illumina
Illumina
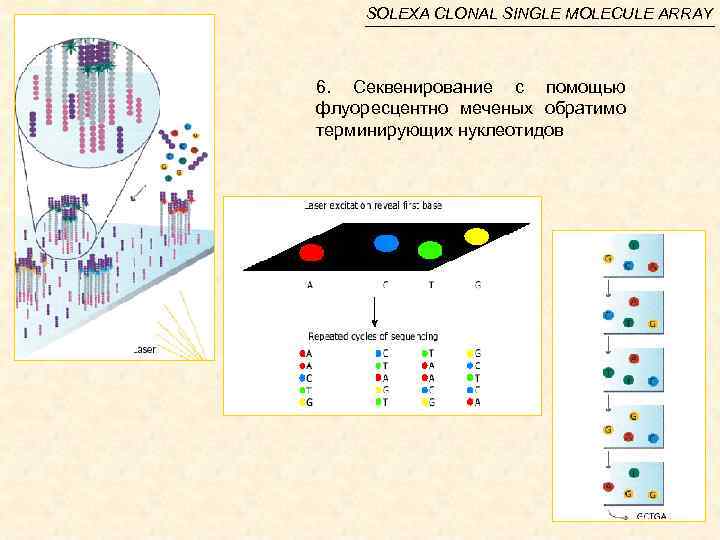 SOLEXA CLONAL SINGLE MOLECULE ARRAY 6. Секвенирование с помощью флуоресцентно меченых обратимо терминирующих нуклеотидов
SOLEXA CLONAL SINGLE MOLECULE ARRAY 6. Секвенирование с помощью флуоресцентно меченых обратимо терминирующих нуклеотидов
 чип Прибор для формирования кластеров на чипе Прибор для получения парной библиотеки
чип Прибор для формирования кластеров на чипе Прибор для получения парной библиотеки
 SOLIDTM System, Applied Biosystems Группа George M. Church (Shendure, Mitra et al. , 2005) SOLi. D™ Analyzer 1 Создание библиотеки - стандартно 2 Клональная амплификация- эмульсионная ПЦР 3 Ключевой момент – «сиквенс посредством лигирования»
SOLIDTM System, Applied Biosystems Группа George M. Church (Shendure, Mitra et al. , 2005) SOLi. D™ Analyzer 1 Создание библиотеки - стандартно 2 Клональная амплификация- эмульсионная ПЦР 3 Ключевой момент – «сиквенс посредством лигирования»
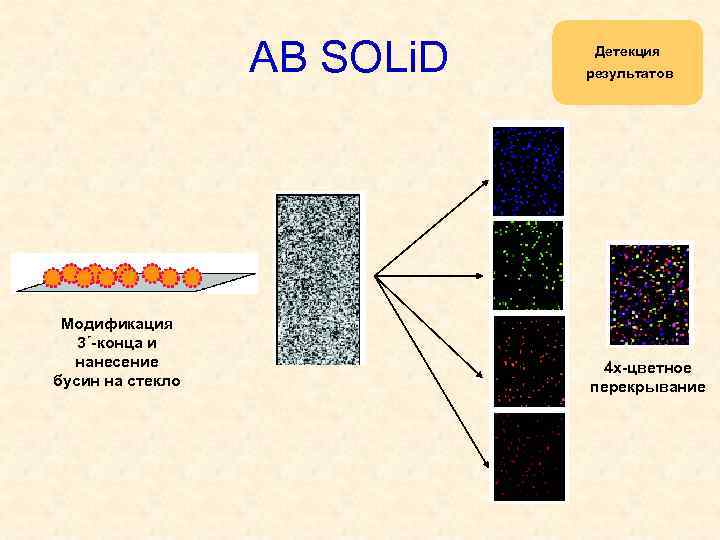 АВ SOLi. D Модификация 3´-конца и нанесение бусин на стекло Детекция результатов 4 х-цветное перекрывание
АВ SOLi. D Модификация 3´-конца и нанесение бусин на стекло Детекция результатов 4 х-цветное перекрывание
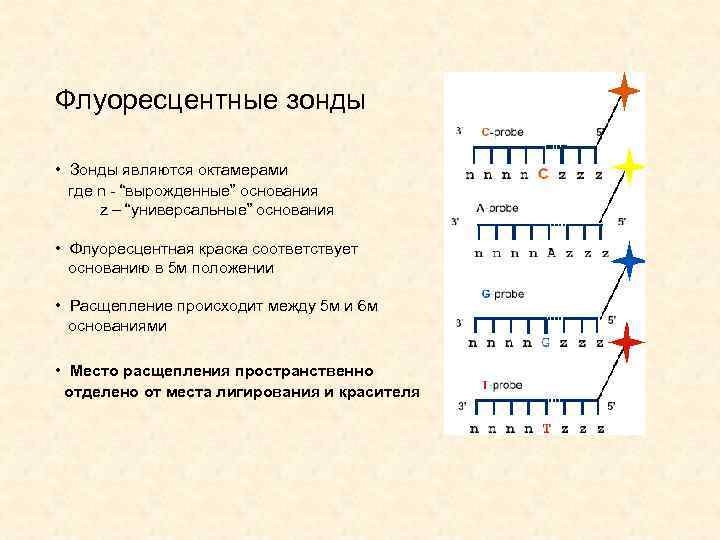 Флуоресцентные зонды • Зонды являются октамерами где n - “вырожденные” основания z – “универсальные” основания • Флуоресцентная краска соответствует основанию в 5 м положении • Расщепление происходит между 5 м и 6 м основаниями • Место расщепления пространственно _ _отделено от места лигирования и красителя
Флуоресцентные зонды • Зонды являются октамерами где n - “вырожденные” основания z – “универсальные” основания • Флуоресцентная краска соответствует основанию в 5 м положении • Расщепление происходит между 5 м и 6 м основаниями • Место расщепления пространственно _ _отделено от места лигирования и красителя
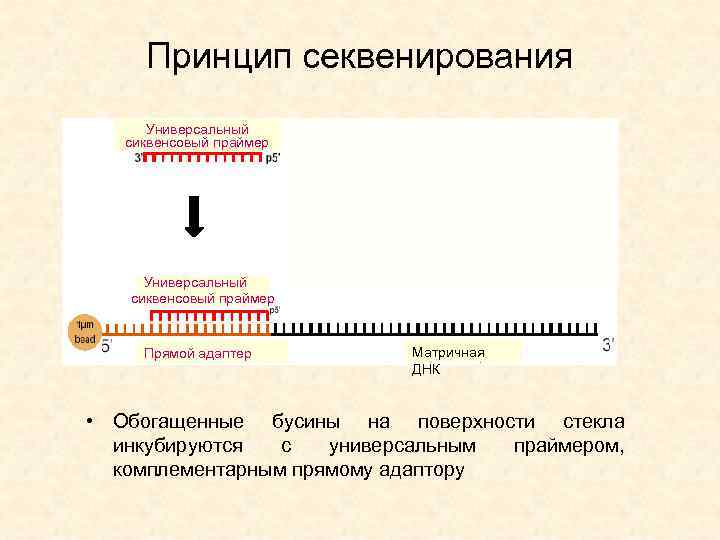 Принцип секвенирования Универсальный сиквенсовый праймер Прямой адаптер Матричная ДНК • Обогащенные бусины на поверхности стекла инкубируются с универсальным праймером, комплементарным прямому адаптору
Принцип секвенирования Универсальный сиквенсовый праймер Прямой адаптер Матричная ДНК • Обогащенные бусины на поверхности стекла инкубируются с универсальным праймером, комплементарным прямому адаптору
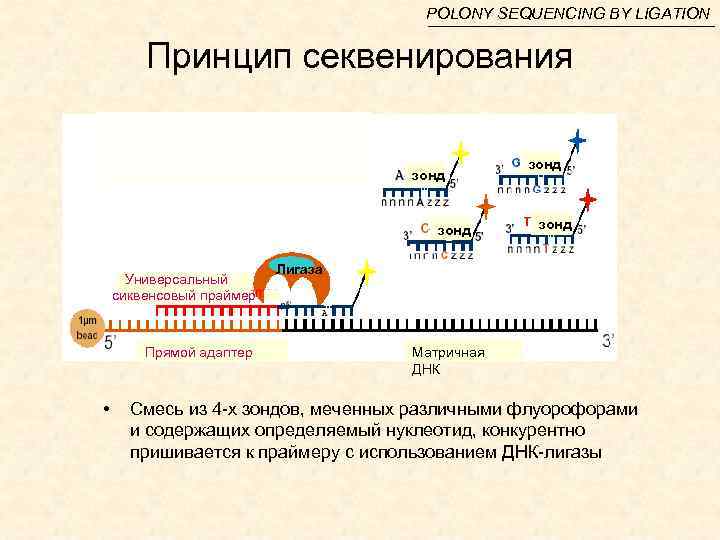 POLONY SEQUENCING BY LIGATION Принцип секвенирования Универсальный сиквенсовый праймер Лигаза зонд Универсальный сиквенсовый праймер Прямой адаптер • зонд Лигаза Матричная ДНК Смесь из 4 -х зондов, меченных различными флуорофорами и содержащих определяемый нуклеотид, конкурентно пришивается к праймеру с использованием ДНК-лигазы
POLONY SEQUENCING BY LIGATION Принцип секвенирования Универсальный сиквенсовый праймер Лигаза зонд Универсальный сиквенсовый праймер Прямой адаптер • зонд Лигаза Матричная ДНК Смесь из 4 -х зондов, меченных различными флуорофорами и содержащих определяемый нуклеотид, конкурентно пришивается к праймеру с использованием ДНК-лигазы
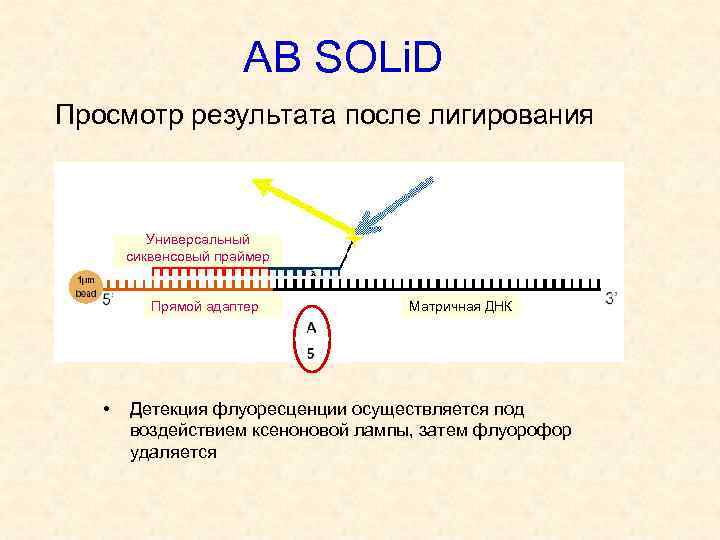 АВ SOLi. D Просмотр результата после лигирования Универсальный сиквенсовый праймер Прямой адаптер • Матричная ДНК Детекция флуоресценции осуществляется под воздействием ксеноновой лампы, затем флуорофор удаляется
АВ SOLi. D Просмотр результата после лигирования Универсальный сиквенсовый праймер Прямой адаптер • Матричная ДНК Детекция флуоресценции осуществляется под воздействием ксеноновой лампы, затем флуорофор удаляется
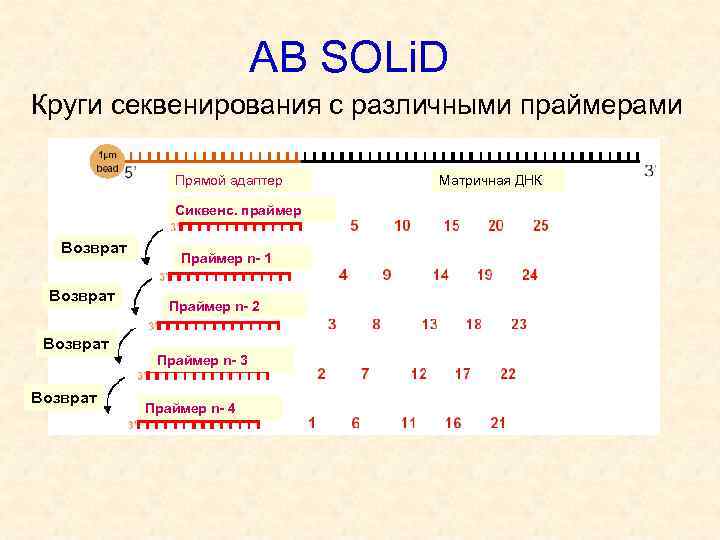 АВ SOLi. D Круги секвенирования с различными праймерами Прямой адаптер Сиквенс. праймер Возврат Праймер n- 1 Праймер n- 2 Возврат Праймер n- 3 Возврат Праймер n- 4 Матричная ДНК
АВ SOLi. D Круги секвенирования с различными праймерами Прямой адаптер Сиквенс. праймер Возврат Праймер n- 1 Праймер n- 2 Возврат Праймер n- 3 Возврат Праймер n- 4 Матричная ДНК
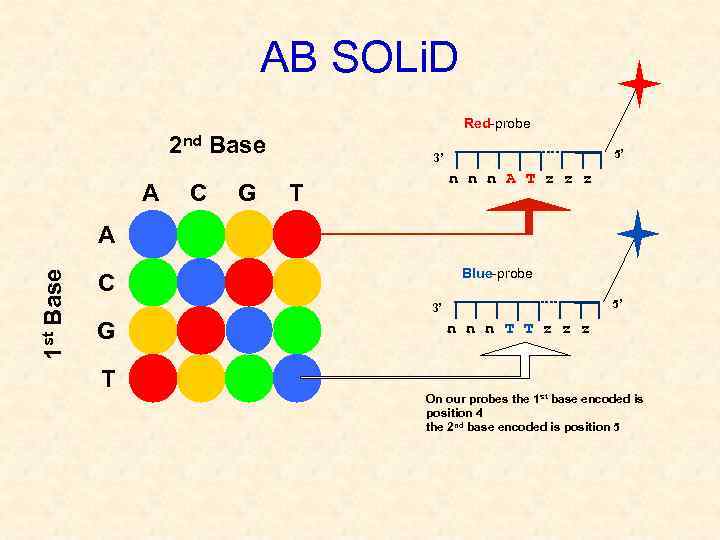 АВ SOLi. D Red-probe 2 nd Base A C G 5’ 3’ n n n A T z z z T 1 st Base A Blue-probe C 5’ 3’ G T n n n T T z z z On our probes the 1 st base encoded is position 4 the 2 nd base encoded is position 5
АВ SOLi. D Red-probe 2 nd Base A C G 5’ 3’ n n n A T z z z T 1 st Base A Blue-probe C 5’ 3’ G T n n n T T z z z On our probes the 1 st base encoded is position 4 the 2 nd base encoded is position 5
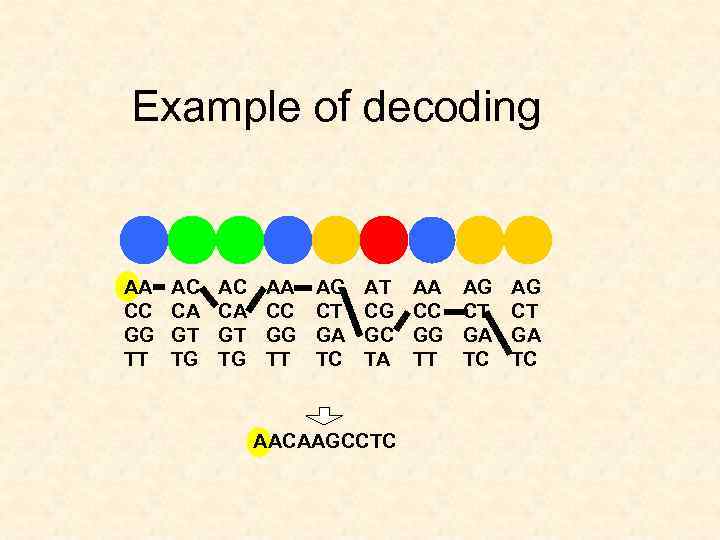 Example of decoding AA CC GG TT AC CA GT TG AA CC GG TT AG CT GA TC AT CG GC TA AACAAGCCTC AA CC GG TT AG CT GA TC
Example of decoding AA CC GG TT AC CA GT TG AA CC GG TT AG CT GA TC AT CG GC TA AACAAGCCTC AA CC GG TT AG CT GA TC
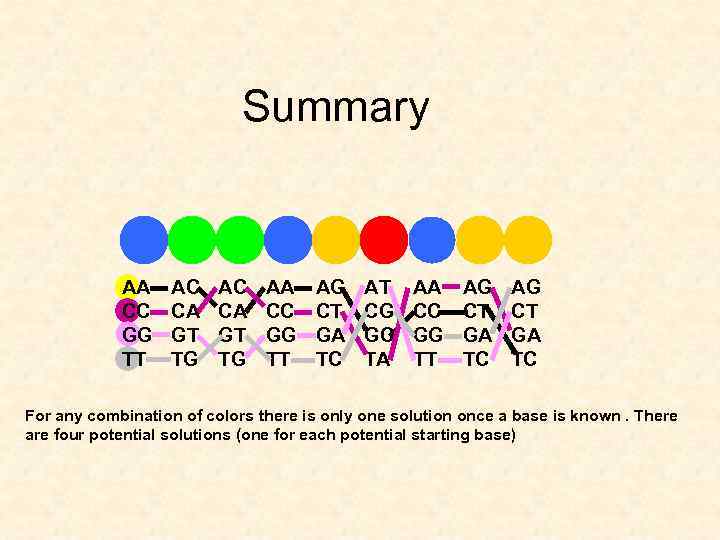 Summary AA CC GG TT AC CA GT TG AA CC GG TT AG CT GA TC AT CG GC TA AA CC GG TT AG CT GA TC For any combination of colors there is only one solution once a base is known. There are four potential solutions (one for each potential starting base)
Summary AA CC GG TT AC CA GT TG AA CC GG TT AG CT GA TC AT CG GC TA AA CC GG TT AG CT GA TC For any combination of colors there is only one solution once a base is known. There are four potential solutions (one for each potential starting base)
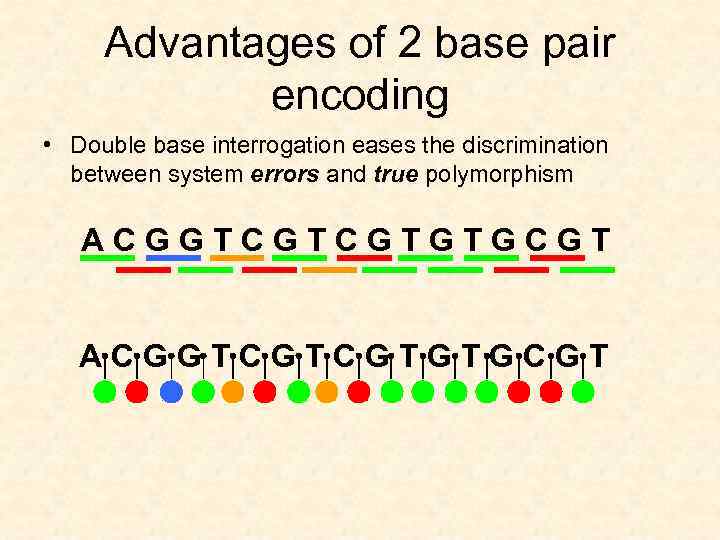 Advantages of 2 base pair encoding • Double base interrogation eases the discrimination between system errors and true polymorphism A C G G T C G T G T G C G T
Advantages of 2 base pair encoding • Double base interrogation eases the discrimination between system errors and true polymorphism A C G G T C G T G T G C G T
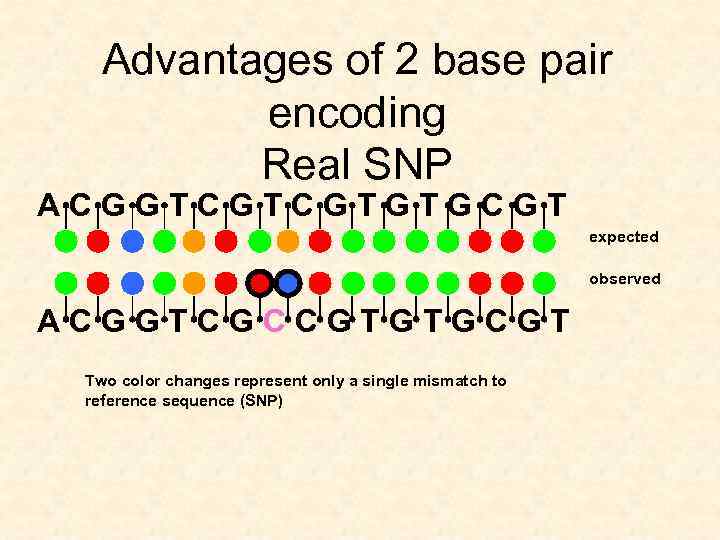 Advantages of 2 base pair encoding Real SNP A C G G T C G T G C G T expected observed A C G G T C G C C G T G C G T Two color changes represent only a single mismatch to reference sequence (SNP)
Advantages of 2 base pair encoding Real SNP A C G G T C G T G C G T expected observed A C G G T C G C C G T G C G T Two color changes represent only a single mismatch to reference sequence (SNP)
 Современные технологии секвенирования Высокопроизводительное параллельное секвенирование популяций клонально амплифицированных молекул ДНК "Секвенирование единичных молекул" (Single Molecule Sequencing)
Современные технологии секвенирования Высокопроизводительное параллельное секвенирование популяций клонально амплифицированных молекул ДНК "Секвенирование единичных молекул" (Single Molecule Sequencing)
 На сегодняшний день… Секвенирование и ресеквенирование геномов Способность секвенировать целый геном из одной некультивируемой клетки позволит нам выявить все чудовищное биоразнообразие Метагеномика
На сегодняшний день… Секвенирование и ресеквенирование геномов Способность секвенировать целый геном из одной некультивируемой клетки позволит нам выявить все чудовищное биоразнообразие Метагеномика


