Современное определение иммунитета Врожденный и приобретенный иммунитет


Современное определение иммунитета Врожденный и приобретенный иммунитет Лектор: канд. биол. наук, доцент Анфиногенова Оксана Ивановна

Под невосприимчивостью к заразным болезням надо понимать общую систему явлений, благодаря которым организм может выдержать нападение болезнетворных микробов (И. И. Мечников)

Иммунитет представляет собой целостную систему биологических механизмов самозащиты организма, с помощью которых он распознает и уничтожает все чужеродное (т. е. генетически отличающееся от него), если оно проникает в организм или возникает в нем. С помощью этих механизмов поддерживается структурная и функциональная целостность организма на протяжении всей его жизни, т. е. сохраняется физическое здоровье людей и обеспечивается исцеление от многих болезней

Иммунитет может быть: n естественный (врожденный, видовой, неспецифический) n и приобретенный или специфический иммунитет

Приобретённым иммунитетом называют такую невосприимчивость организма к инфекционным агентам, которая формируется в процессе его индивидуального развития и характеризуется строгой специфичностью. Приобретённая антиинфекционная резистентность складывается из гуморального и клеточного иммунитета. Она всегда антигенспецифическая.

Механизмы защиты от инфекции

n В отличие от врожденных (неспецифических) факторов резистентности, антигенспецифические обладают способностью узнавать и запоминать пространственную конфигурацию антигена и защищать организм при повторном его введении – то есть свойством иммунологической памяти. Кроме того приобретенный иммунитет не передается по наследству, а формируется в процессе индивидуальной жизни в результате взаимодействия с соответствующими возбудителями или их антигенами.

В зависимости от механизма образования приобретенный иммунитет подразделяется на искусственный и естественный, а каждый из них в свою очередь – на активный и пассивный. n Естественный активный иммунитет возникает вследствие перенесенного заболевания в той или иной форме, в том числе легкой и скрытой. Такой иммунитет называется также постинфекционным. n Естественный пассивный иммунитет создается в результате передачи ребенку от матери антител через плаценту и грудное молоко. Организм ребенка в этом случае сам не участвует в активной выработке антител.

n Искусственный активный иммунитет – иммунитет , образующийся в результате прививок вакцинами, т. е. поствакцинальный. n Искусственный пассивный иммунитет обусловлен введением иммунных сывороток или препаратов гамма- глобулина , содержащих соответствующие антитела.

Естественный, врождённый иммунитет представляет собой невосприимчивость одного вида животных или человека к микроорганизмам, вызывающим заболевания у других видов. Он определяется факторами неспецифической резистентности организма , которые передаются по наследству. Эти защитные механизмы осуществляются за счёт так называемых антигеннеспецифических реакций. В этом случае нейтрализация, разрушение и вывод из организма чужеродных веществ происходит без узнавания и запоминания особенностей их строения

В осуществлении реакций врождённого иммунитета участвуют: а) клетки: n - пограничных тканей (кожа, слизистая ЖКТ, дыхательных путей и урогенитального тракта); n - крови ( полиморфноядерные лейкоциты, моноциты, натуральные киллеры); n - эндотелия сосудов; n - резистентные макрофаги; б) гуморальные факторы: n - белки острой фазы; n - лизоцим; n - комплемент и его компоненты n - интерфероны

Механические защитные барьеры: Кожа Неповрежденная кожа представляет собой обычно непроницаемый барьер для микроорганизмов. Она обладает хорошей бактерицидной активностью в отношении тех микроорганизмов, которые не являются представителями её нормальной микрофлоры. Так, если нанести на кожу взвесь стрептококков, то количество их через 30 минут уменьшится в 3 раза, через 1 час в 20 раз, а через 2 – 3 часа их останется лишь небольшое количество. Более эффектное действие проявляет чистая кожа. Гибель микроорганизмов значительно замедляется на загрязненной коже. Нарушения целостности кожи, ранения – частая причина проникновения в организм возбудителей, в особенности гнойно-воспалительных болезней

Слизистые оболочки выполняют роль не только факторов механической защиты. Они обладают некоторыми приспособлениями и свойствами, которые уменьшают возможность проникновения возбудителя в организм. Так, например, покрытые слизью реснички мерцательного эпителия адсорбируют на себе микроорганизмы, содержащиеся во вдыхаемом воздухе, и способствуют его очищению

Нормальная микрофлора организма Защитный эффект нормальной микрофлоры заключается в том, что между её представителями и патогенными микроорганизмами, которые попадают в данную область, неизбежно возникают сложные формы взаимоотношений, от конкуренции до прямого антагонизма, природа которых может быть самой различной (конкуренция за питательные вещества, обусловленная различной скоростью размножения, выделение антибиотических веществ, изменение р. Н среды в сторону, неблагоприятную для конкурента).

Функции выделительной системы К числу неспецифических защитных механизмов организма следует отнести и функции выделительных систем. Освобождение организма от микробов, продуктов их жизнедеятельности и токсинов происходит с помощью желудочно-кишечного тракта, мочевыводящих путей, половых желез, дыхательной и других систем. Типичным примером такого рода неспецифической защитной реакции является рвота, часто наблюдаемая как при бактериальных, так и небактериальных кишечных отравлениях. При попадании в организм достаточно больших доз микробов или их токсинов нормальная физиологическая деятельность, т. е. реактивность многих органов, в том числе выделительных систем, в результате воздействия микробных антигенов на рецепторы тканей изменяется. Учащается дыхание, изменяется кровообращение, расширяются кровеносные сосуды и реализуется ряд других реакций, направленных на освобождение организма от возбудителей и нейтрализацию их вредного воздействия.

Противомикробные вещества Давно установлено, что из тканей и жидкостей организма можно выделить много различных веществ с противомикробной активностью. Нередко эти вещества действуют избирательно. Например, из сыворотки непастеризованного молока выделен белок лактенин , который оказывает сильное бактерицидное действие на стрептококки группы А, но менее активен в отношении других микроорганизмов. Лактенин обнаружен и в молоке матери. Антимикробным действием обладают также пептиды, выделяемые из тканей. Один из них, с большим содержанием лизина, действует на стафилококки, стрептококки, сибиреязвенную палочку, а некоторые пептиды, с большим содержанием аргинина, активны против туберкулезной палочки

Фагоцитоз Это один из мощных факторов резистентности организма. Фагоцитарными свойствами обладают зернистые лейкоциты крови и лимфы, главным образом полиморфноядерные нейтрофилы (микрофаги), а также моноциты (макрофаги) и различные клетки ретикулоэндотелиальной системы. По классификации ВОЗ (1972 г) все макрофаги объединены в систему мононуклеарных фагоцитов.

Нейтрофилы – это наиболее объемная популяция лейкоцитов. В отсутствие воспалительного процесса нейтрофилы в основном находятся в кровяносном русле, где они составляют большую часть циркулирующих лейкоцитов. Однако в ответ на воспалительный стимул происходит быстрое и часто массивное перераспределение нейтрофилов в поврежденные ткани. Нейтрофилы всегда рассматривались как основные эффекторные клетки при остром воспалении, а их роль в противобактериальной и противогрибковой защите организма хорошо изучена. Длительное время считалось, что нейтрофилы не способны к синтезу белка и являются лишь пассивными участниками эффекторного звена иммунного ответа. Данные, накопленные за последние два десятилетия, заставили пересмотреть роль нейтрофилов и их участие в афферентном звене иммунного ответа – модуляции клеточного и гуморального иммунитета через синтез и продукцию иммунорегуляторных цитокинов

Период пребывания нейтрофилов в периферической крови составляет примерно 6 – 8 часов, и это, вероятно объясняет их продукцию с удивительно высокой скоростью – 2, 5 биллионов клеток в час После выхода из кровотока нейтрофилы, находясь под воздействием стимулов, выделяют различные секреторные продукты, которые способны взаимодействовать как с микроорганизмами, так и с клетками тканей. Факторы секреции нейтрофилов преимущественно накапливаются в лизосомальных гранулах. Эти гранулы, согласно их морфологии и содержанию, делятся на азурофильные (первичные) и специфические (вторичные). Азурофильные гранулы появляются уже на стадии промиелоцита , а специфические – на стадии миелоцита и метамиелоцита. В зрелых нейтрофилах новообразование гранул не происходит. После активации нейтрофилов гранулы перемещаются к мембране, и слияние с ней инициирует экзоцитоз , в результате которого содержимое гранул выходит в межклеточную жидкость. Помимо этих продуктов нейтрофилы в результате респираторного взрыва высвобождают значительное количество метаболитов кислорода, включая супероксид анион (О-2), перекись водорода Н 2 О 2, гидрохлорид, гидроксильный радикал (ОН-). В своих азурофильных гранулах нейтрофилы содержат большое количество миелопероксидазы. Кроме того, нейтрофилы также продуцируют длительноживущие оксиданты способные индуцировать длительные кислородзависимые реакции. Оба типа гранул содержат более 20 различных протеолитических ферментов, активных по отношению к компонентам интерстициальной ткани.

Азурофильные гранулы содержат большое количество сериновых протеаз, эластаз. Количественно эластазы составляют наибольшую часть продуктов азурофильных гранул. Эластаза получила такое название благодаря своему субстрату – эластину, который легко подвергается деградации. Считается что, эластазы необходимы для деградации микроорганизмов в фаголизосомах , а также для пенетрации тканей и миграции нейтрофилов в тканях. Таким образом эластазы могут быть реальным фактором, приводящим к деструкции тканей в зоне нейтрофильного воспаления. В легких эластаза участвует в патогенезе деструктивных заболеваний, например эмфиземы. Описано воздействие эластазы на эпителиальные клетки, подавляется функция реснитчатого эпителия, повышается секреция слизи. Вторичные гранулы также содержат два фермента, которые обладают специфической протеолитической активностью: гепараназа и желатиназа. Длительное время нейтрофилы рассматривали как клетки не способные к синтезу белка, а лишь как пассивные участники эфферентного звена иммуного ответа. В настоящее время получены убедительные доказательства продукции нейтрофилами различных цитокинов.

Цитокины, продуцируемые нейтрофилами n Туморнекротизирующий фактор альфа n Интерлейкин -1 n Интерлейкин – 6 n Интерлейкин – 8 и хемокины n Интерлейкин – 12 n Трансформирующий ростовой фактор бетта n Колониестимулирующие факторы

В настоящее время фагоцитоз рассматривается как многостадийный процесс и состоит из следующих этапов n Активации n Адгезии n Диапедеза n Хемотаксиса n Опсонизации объекта фагоцитоза n Поглощения n Киллинга n Переваривания микроорганизма
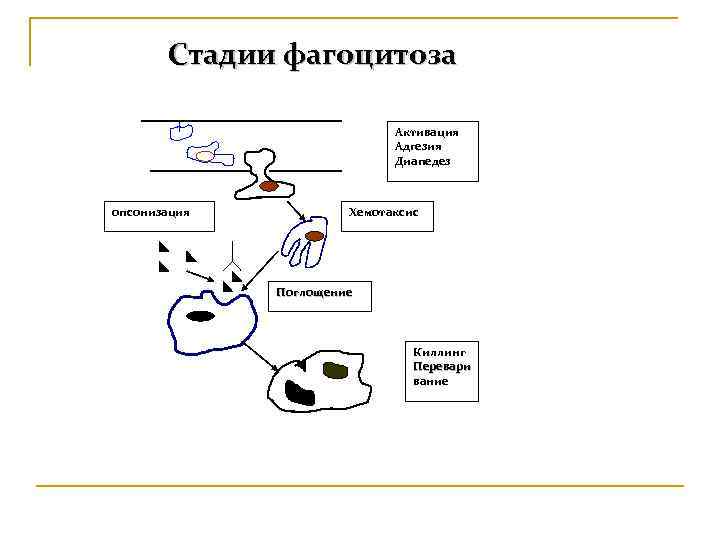
Стадии фагоцитоза Активация Адгезия Диапедез опсонизация Хемотаксис Поглощение Киллинг Перевари вание

Активное перемещение относится к числу наиболее характерных признаков нейтрофила. Он двигается гораздо быстрее других лейкоцитов и более чувствителен к действию разнообразных модуляторов миграционной функции. Быстрый выход нейтрофилов из сосудистого русла по направлению к очагу воспаления или инфицированным тканям является ключевым этапом в системе защиты организма от внедрения микроорганизмов

n Нейтрофилы, находясь в сосудистом русле, прилипают к эндотелию, образу я пристеночный пул. Прилипание (адгезия) происходит благодаря молекулам адгезии нейтрофилов - β 2 интегринам. Адгезины нейтрофилов связываются с соответствующими молекулами, представленными на поверхности эндотелиальных клеток преимущественно посткапиллярных венул. n Хемотаксис отражает способность клетки активно перемещаться в направлении стимулирующих агентов, которые носят название хемоаттрактантов (факторов хемотаксиса). Необходимое условие для направленного движения – градиент концентрации хемоаттрактанта

Опсонины – это сывороточные факторы, в обязанности которых входит превращение бактерий в материал для фагоцитоза. Большинство патогенных микробов должны подвергнуться опсонизации прежде, чем будут адгезированы фагоцитирующими клетками. В настоящее время наиболее важными сывороточными опсонинами считаются система комплемента и иммуноглобулины (Ig. G).

Выделяют три основных пути поглощения нейтрофилом микроорганизмов: n пиноцитоз, n эндоцитоз (рецептор-опосредованное взаимодействие) n и фагоцитоз

Нейтрофилы способны убивать микроорганизмы с помощью двух принципиально различных механизмов: n кислородозависимый n кислородонезависимый

Кислородозависимые механизмы С того момента, когда инициируется фагоцитоз происходит резкая активация гексозомонофосфатного шунта, генерирующего НАДФ. Н используется для восстановления молекулярного кислорода, связанного с уникальным мембранным цитохромом , что вызывает бурное потребление кислорода. В результате образуются: n -надпероксидный анион n - пероксид водорода n - синглетный (активный) кислород n - гидроксильные радикалы Все они служат мощными бактерицидными агентами. Более того, сочетание пероксида , миелопероксидазы и ионов галогенов создает мощную систему галогенирования, способную вызвать гибель как бактерий, так и вирусов

В процессе кислородозависимых механизмов потребляются ионы водорода и слегка повышается р. Н , а это создает оптимальные условия для функционирования семейства катионных белков. Эти белки разрушают бактериальную мембрану, как за счет протеазного эффекта, так и за счет непосредственного присоединения к поверхности микроорганизма. n Низкие значения р. Н , лизоцим и лактоферрин представляют собой кислородонезависимые бактерицидные и бактериостатические факторы, которые могут действовать в анаэробных условиях. В конце концов убитые микроорганизмы расщепляются гидролитическими ферментами, и продукты деградации высвобождаются из клетки.

Система интерферонов Давно было подмечено, что если ввести в организм два вируса одновременно или с интервалом не более 24 часов между ними наблюдается какое-то взаимодействие, проявляющееся во взаимном угнетении (интерференция). В 1957 году Л. Айзекс и Дж. Линдеман обнаружили, что явление интерференции связано с образованием в клетках, которые были заражены вирусом, особого белка – интерферона. Установлено, что существует не один интерферон, а целая система их, в которой выделены три основных типа: ИНФ-α , ИНФ-β и ИНФ-γ. Интерфероны, синтезируемые в клетках человека различаются по своим физико-химическим свойствам; рецепторам, с помощью которых они взаимодействуют с клетками; кислоточувствительностью ; антигенной специфичностью. Они продуцируются различными клетками и обладают достаточно мощной противовирусной активностью.

В крови и тканях имеется целый ряд гуморальных факторов, которых можно отнести к факторам естественной резистентности организма. Это так называемые острофазные белки , образующиеся в организме при остром воспалении. Среди них С-реактивный протеин, фибронектин , сывороточный амилопротеин А, α- антитрипсин и β 2 - макроглобулин, гаптоглобин. Все они участвуют в детоксикации , фагоцитозе, определяют эффективность воспалительной реакции.

Киллерные клетки (натуральные киллеры НК, естественные киллеры ЕК) Название этих клеток происходит от английского (natural killer – природные убийцы). Они найдены в лимфоидной ткани животных всех изучаемых видов, кроме кошек. Хотя НК клетки относятся к лимфоцитам они не обладают свойствами ни зрелых Т-, ни зрелых В- лимфоцитов, и имеют свойственные только им маркеры. Их киллерная активность не зависит от представления им чужеродного антигена, они сами способны распознавать и лизировать пораженные вирусом клетки, а также различные варианты опухолевых клеток
2 Иммунитет врожденный и приобретенный.ppt
- Количество слайдов: 33

