431ae539f689da97c178a287c3f30703.ppt
- Количество слайдов: 79

Современная система обеспечения качества лекарственных средств Ягудина Роза Исмаиловна доктор фарм. наук, профессор Москва, 15 октября 2007 г.

n n Лекарственные средства – вещества, применяемые для профилактики, диагностики, лечения болезни, предотвращения беременности, полученные из крови, плазмы крови, а также органов, тканей человека или животного, растений, микроорганизмов, минералов, методами синтеза или с применением биологических технологий. Лекарственные препараты – дозированные лекарственные средства в определенной лекарственной форме

Какие бывают лекарственные средства? § § § § § оригинальные и генерические отечественные и зарубежные рецептурные и безрецептурные природного происхождения и синтетические наркотические, психотропные, сильнодействующие, ядовитые по лекарственным формам по пути введения по ФТГ с доказанной клинической эффективностью и без и т. д.

Особые свойства лекарственного средства как продукта Эффективные лечебные технологии
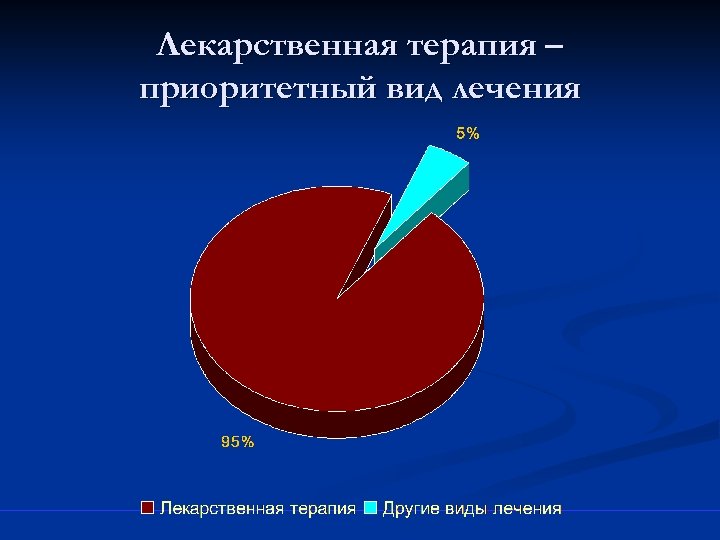
Лекарственная терапия – приоритетный вид лечения

Особые свойства лекарственного средства как продукта Социальный продукт n Финансовые интересы n Инновационный продукт n Потребитель самостоятельно не может оценить качество ЛС n
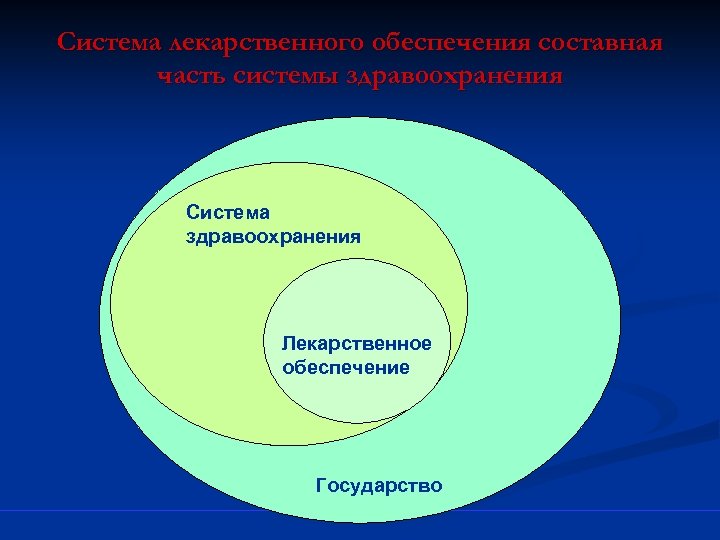
Система лекарственного обеспечения составная часть системы здравоохранения Система здравоохранения Лекарственное обеспечение Государство

Организация лекарственного обеспечения населения – динамичный процесс Факторы, влияющие на систему лекарственного обеспечения: - Социально-экономическая ситуация в стране Заболеваемость населения Развитие демографической ситуации в стране Совершенствование системы здравоохранения в стране Развитие системы государственной поддержки граждан нуждающихся в социальной защите Развитие научно-исследовательской деятельности, повышение качества научных исследований, внедрение новых технологий. Состояние и развитие фармацевтического рынка и фармацевтической промышленности и др.
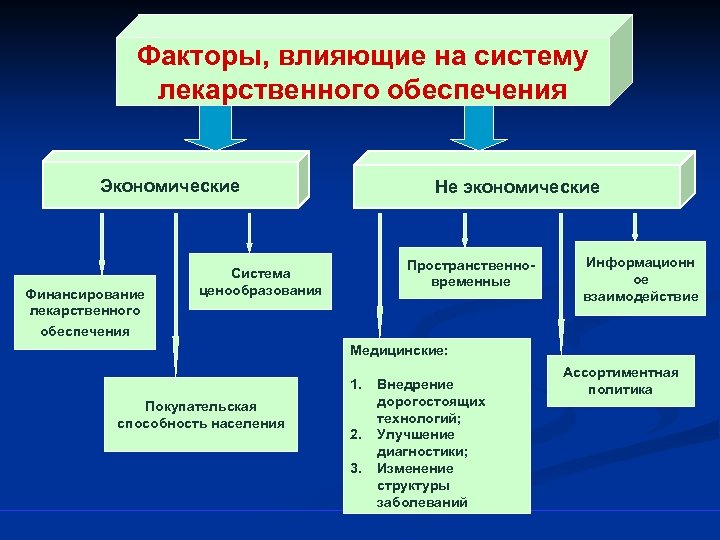
Факторы, влияющие на систему лекарственного обеспечения. Экономические Финансирование лекарственного обеспечения Не экономические Пространственновременные Система ценообразования Информационн ое взаимодействие Медицинские: 1. Покупательская способность населения 2. 3. Внедрение дорогостоящих технологий; Улучшение диагностики; Изменение структуры заболеваний Ассортиментная политика
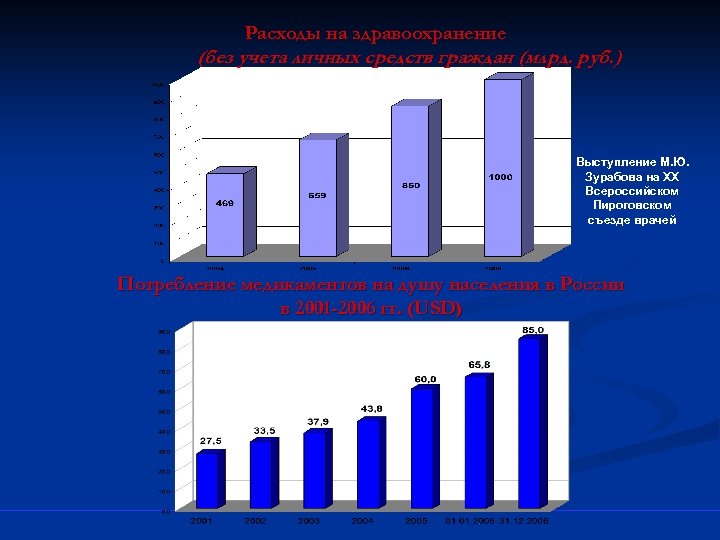
Расходы на здравоохранение (без учета личных средств граждан (млрд. руб. ) Выступление М. Ю. Зурабова на XX Всероссийском Пироговском съезде врачей Потребление медикаментов на душу населения в России в 2001 -2006 гг. (USD)

Особенности фармацевтического рынка России n Преобладание генериков n Широкая распространенность «традиционных препаратов» n Большая синонимия
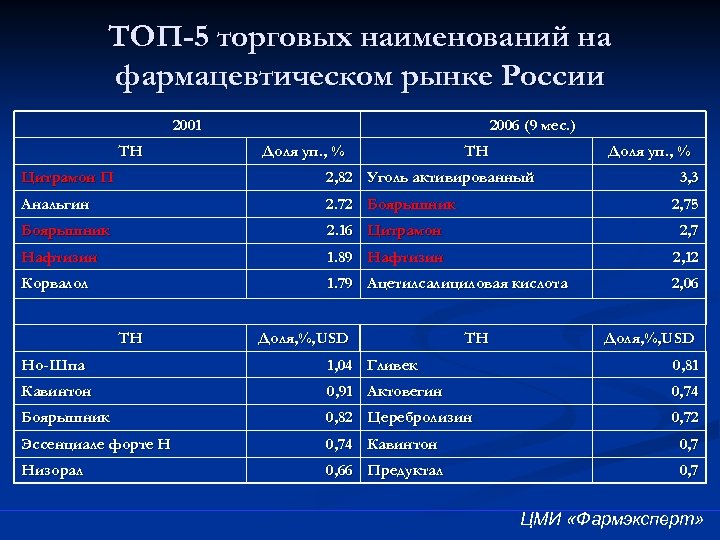
ТОП-5 торговых наименований на фармацевтическом рынке России 2001 ТН 2006 (9 мес. ) Доля уп. , % ТН Доля уп. , % Цитрамон П 2, 82 Уголь активированный Анальгин 2. 72 Боярышник 2. 16 Цитрамон 2, 7 Нафтизин 1. 89 Нафтизин 2, 12 Корвалол 1. 79 Ацетилсалициловая кислота 2, 06 ТН Доля, %, USD 3, 3 2, 75 ТН Доля, %, USD Но-Шпа 1, 04 Гливек 0, 81 Кавинтон 0, 91 Актовегин 0, 74 Боярышник 0, 82 Церебролизин 0, 72 Эссенциале форте Н 0, 74 Кавинтон 0, 7 Низорал 0, 66 Предуктал 0, 7 ЦМИ «Фармэксперт»

Доля лекарственной формы «Настойки» на фармацевтическом рынке России Настойки 48 271 377$ 5, 15% рынка (в натуральном выражении) Сумма USD Кол-во упаковок Боярышник 24 843 137 86 242 560 Перца стручкового настойка 8 905 344 26 019 880 Валериана 3 645 613 14 807 266 Пустырника настойка 3 591 784 16 310 770 Торговое наименование ЦМИ «Фармэксперт»
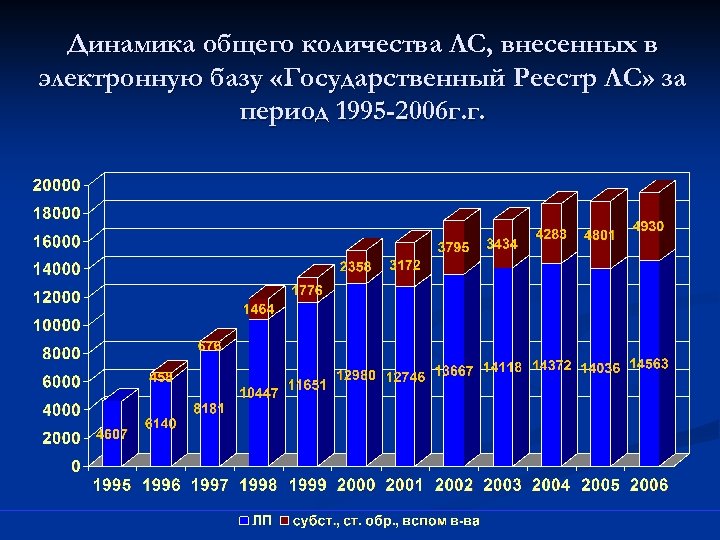
Динамика общего количества ЛС, внесенных в электронную базу «Государственный Реестр ЛС» за период 1995 -2006 г. г.


n Обращение лекарственных средств – обобщенное понятие деятельности, включающей разработку, исследования, производство, изготовление, хранение, упаковку, перевозку, государственную регистрацию, стандартизацию и контроль качества, продажу, маркировку, рекламу, применение лекарственных средств, уничтожение лекарственных средств, пришедших в негодность, или лекарственных средств с истекшим сроком годности и иные действия в сфере обращения лекарственных средств.
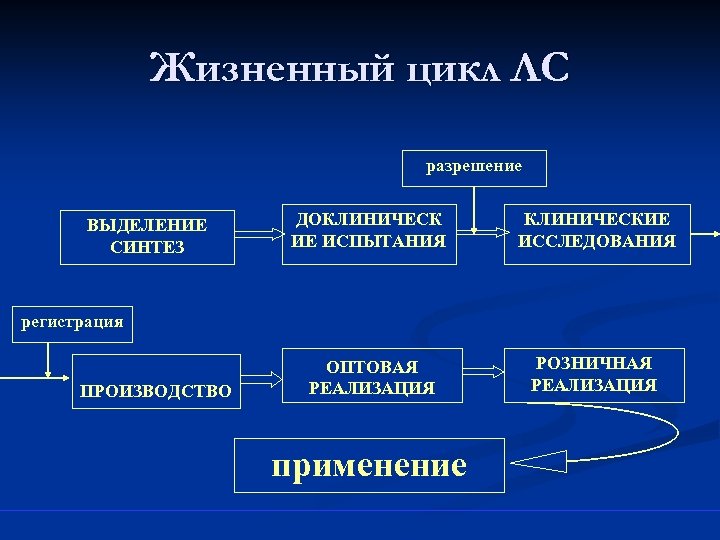
Жизненный цикл ЛС разрешение ВЫДЕЛЕНИЕ СИНТЕЗ ДОКЛИНИЧЕСК ИЕ ИСПЫТАНИЯ КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ ОПТОВАЯ РЕАЛИЗАЦИЯ РОЗНИЧНАЯ РЕАЛИЗАЦИЯ регистрация ПРОИЗВОДСТВО применение

Субъекты сферы обращения лекарственных средств n Производители n n n Дистрибуторы n n n Федеральные Региональные Аптечные организации n n n Отечественные Зарубежные Аптеки Аптечные пункты Аптечные киоски Аптечные магазины ЛПУ
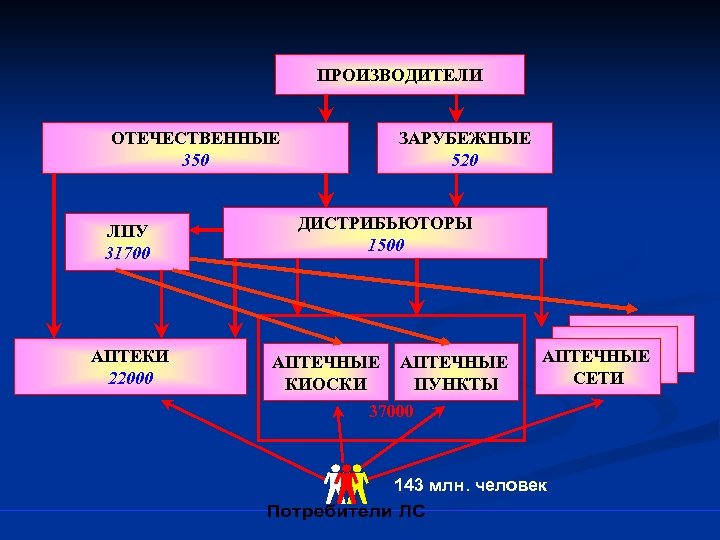
ПРОИЗВОДИТЕЛИ ОТЕЧЕСТВЕННЫЕ 350 ЛПУ 31700 АПТЕКИ 22000 ЗАРУБЕЖНЫЕ 520 ДИСТРИБЬЮТОРЫ 1500 АПТЕЧНЫЕ КИОСКИ АПТЕЧНЫЕ ПУНКТЫ АПТЕЧНЫЕ СЕТИ 37000 143 млн. человек
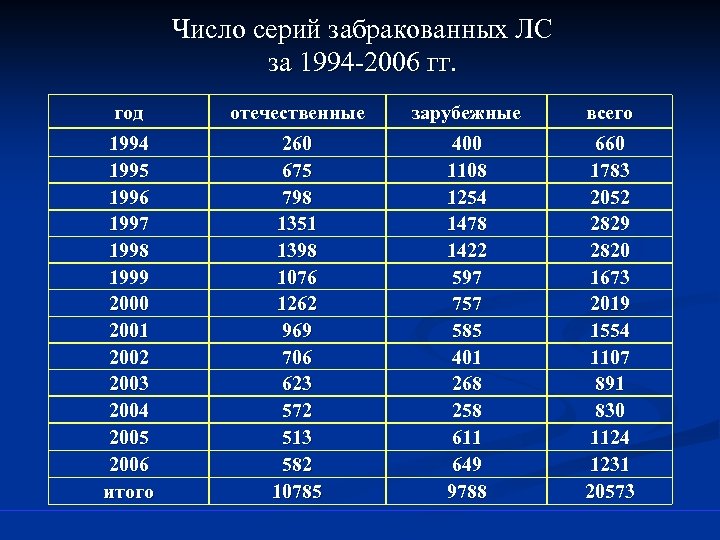
Число серий забракованных ЛС за 1994 -2006 гг. год отечественные зарубежные всего 1994 1995 1996 1997 1998 1999 2000 2001 2002 2003 2004 2005 2006 итого 260 675 798 1351 1398 1076 1262 969 706 623 572 513 582 10785 400 1108 1254 1478 1422 597 757 585 401 268 258 611 649 9788 660 1783 2052 2829 2820 1673 2019 1554 1107 891 830 1124 1231 20573
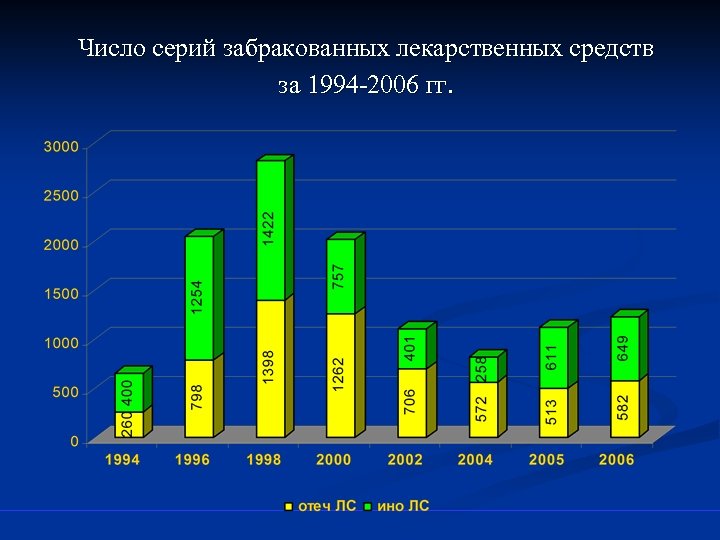
Число серий забракованных лекарственных средств за 1994 -2006 гг.
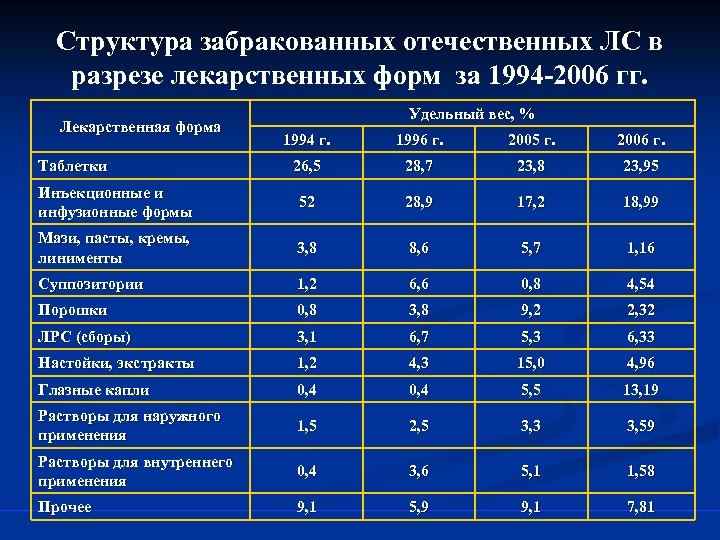
Структура забракованных отечественных ЛС в разрезе лекарственных форм за 1994 -2006 гг. Лекарственная форма Удельный вес, % 1994 г. 1996 г. 2005 г. 2006 г. 26, 5 28, 7 23, 8 23, 95 Инъекционные и инфузионные формы 52 28, 9 17, 2 18, 99 Мази, пасты, кремы, линименты 3, 8 8, 6 5, 7 1, 16 Суппозитории 1, 2 6, 6 0, 8 4, 54 Порошки 0, 8 3, 8 9, 2 2, 32 ЛРС (сборы) 3, 1 6, 7 5, 3 6, 33 Настойки, экстракты 1, 2 4, 3 15, 0 4, 96 Глазные капли 0, 4 5, 5 13, 19 Растворы для наружного применения 1, 5 2, 5 3, 3 3, 59 Растворы для внутреннего применения 0, 4 3, 6 5, 1 1, 58 Прочее 9, 1 5, 9 9, 1 7, 81 Таблетки
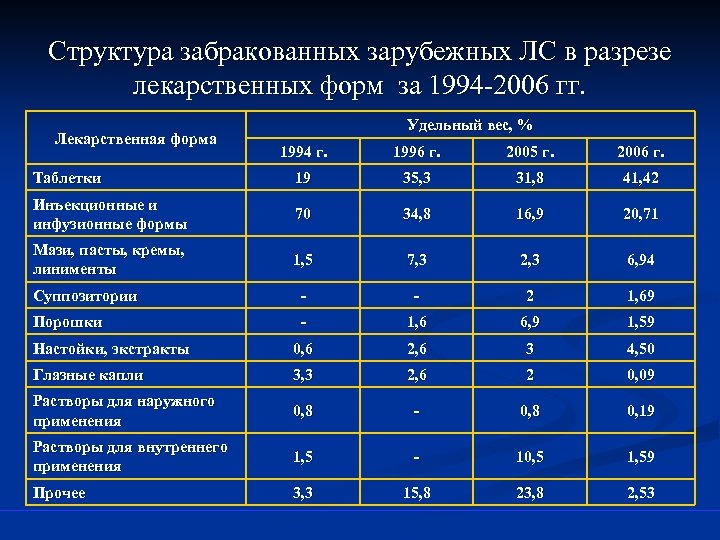
Структура забракованных зарубежных ЛС в разрезе лекарственных форм за 1994 -2006 гг. Лекарственная форма Удельный вес, % 1994 г. 1996 г. 2005 г. 2006 г. Таблетки 19 35, 3 31, 8 41, 42 Инъекционные и инфузионные формы 70 34, 8 16, 9 20, 71 Мази, пасты, кремы, линименты 1, 5 7, 3 2, 3 6, 94 Суппозитории - - 2 1, 69 Порошки - 1, 6 6, 9 1, 59 Настойки, экстракты 0, 6 2, 6 3 4, 50 Глазные капли 3, 3 2, 6 2 0, 09 Растворы для наружного применения 0, 8 - 0, 8 0, 19 Растворы для внутреннего применения 1, 5 - 10, 5 1, 59 Прочее 3, 3 15, 8 23, 8 2, 53
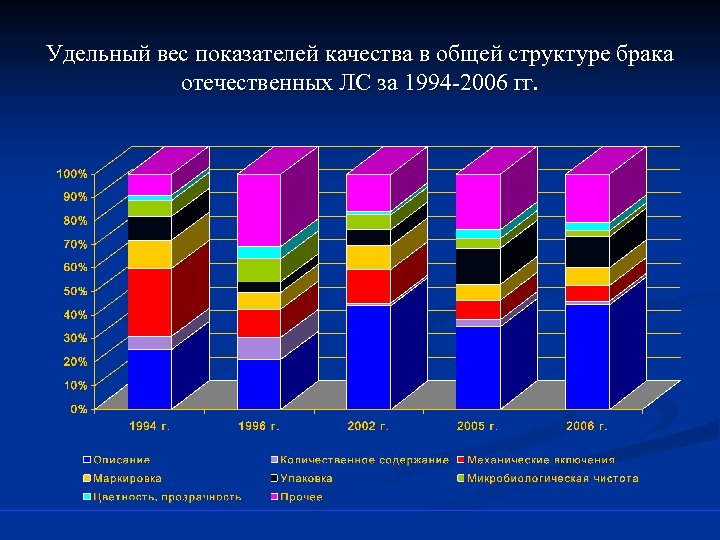
Удельный вес показателей качества в общей структуре брака отечественных ЛС за 1994 -2006 гг.
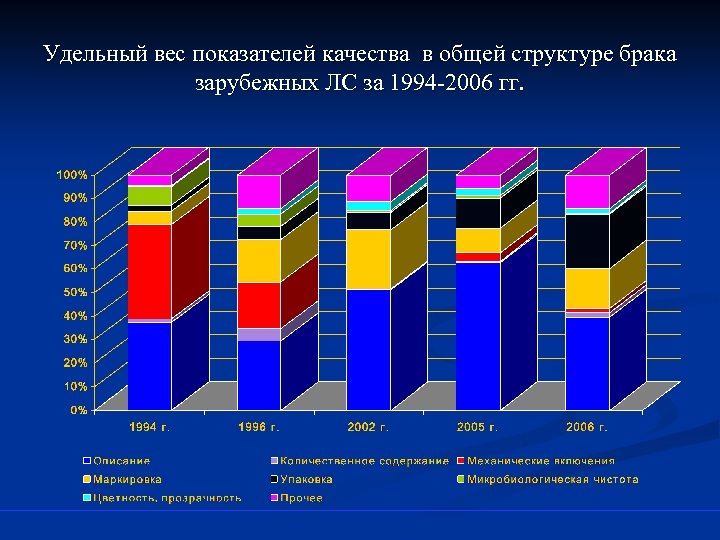
Удельный вес показателей качества в общей структуре брака зарубежных ЛС за 1994 -2006 гг.

n. Стандартизация в сфере обращения лекарственных средств - деятельность по разработке и установлению норм, правил и характеристик в целях обеспечения качества, эффективности, безопасности лекарственных средств и их рационального применения. n. Объекты стандартизации в сфере обращения лекарственных средств üОсновные этапы «жизненного цикла» лекарственного средства üОсновные параметры самого лекарственного средства

n. Объекты стандартизации в сфере обращения лекарственных средств üОсновные этапы «жизненного цикла» лекарственного средства
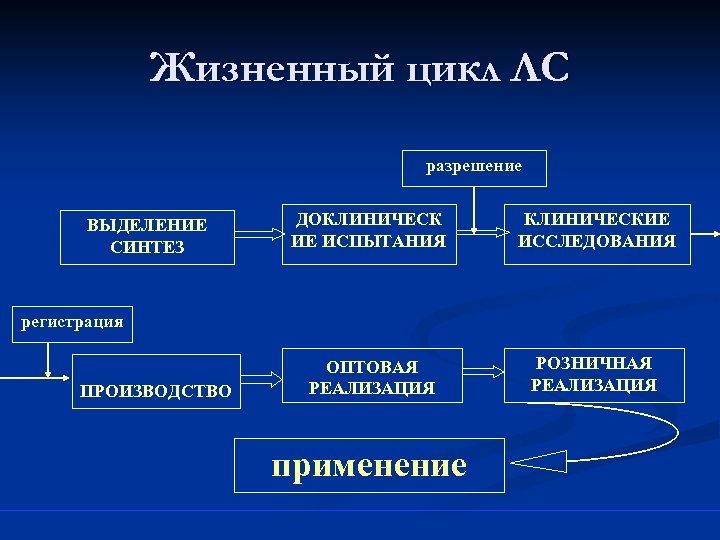
Жизненный цикл ЛС разрешение ВЫДЕЛЕНИЕ СИНТЕЗ ДОКЛИНИЧЕСК ИЕ ИСПЫТАНИЯ КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ ОПТОВАЯ РЕАЛИЗАЦИЯ РОЗНИЧНАЯ РЕАЛИЗАЦИЯ регистрация ПРОИЗВОДСТВО применение

Комплекс стандартов GXP n n n GLP- правила надлежащей (качественной) лабораторной практики GCP – правила надлежащей (качественной) клинической практики GMP – правила надлежащей (качественной) производственной практики GDP – правила надлежащей (качественной) дистрибьюторской практики GPP – правила надлежащей (качественной) аптечной практики

Доклинические исследования правила качественной лабораторной практики (GLP) n Методические рекомендации по экспериментальному доклиническому изучению новых фармакологических веществ (Москва, 2000 г. ) n Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ (Москва, 2005 г. )

Клинические исследования правила качественной клинической практики (GCP) ГОСТ Р 52379 - 2005 «Надлежащая клиническая практика» Дата введения - 1 апреля 2006 г. Правила представляют собой этический и научный стандарт качества планирования и проведения исследований на человеке, а также документального оформления и представления результатов. Соблюдение этих правил служит гарантией достоверности результатов клинических испытаний, безопасности, охраны прав и здоровья испытуемых в соответствии с основополагающими принципами Хельсинкской декларации

Регистрация - это процесс последовательных и научнообоснованных испытательных, экспертных и административноправовых действий, переводящих с медико-юридических позиций биологически активное вещество в статус лекарственного средства Бабаян Э. А.

Производство лекарственных средств ГОСТ Р 52249 -2004 «Правила производства и контроля качества лекарственных средств Содержание Введение n Основные разделы n Приложения - 18 n

Оптовая торговля лекарственными средствами правила качественной дистрибьюторской практики - (GDP) n ОСТ 91500. 05. 0005 -2002 «Правила оптовой торговли лекарственными средствами» n Введен в действие Приказом Минздрава России от 15 марта 2002 г. № 80

Розничная торговля лекарственными средствами правила качественной аптечной практики (GPP) Приказ Минздрава России от 04. 03. 2003 г. № 80 «Об утверждении Отраслевого стандарта «Правила отпуска (реализации) лекарственных средств в аптечных организациях. Основные положения»

Отраслевой стандарт «Правила отпуска (реализации) лекарственных средств в аптечных организациях. Основные положения» ОСТ 91500. 05. 0007 - 2003 П. 5. 4 Лекарственные средства (лекарственные препараты) следует хранить раздельно с учетом их физических и физико – химических свойств, воздействия на них различных факторов внешней среды в соответствии с установленными требованиями (Приказ Минздрава России от 13 ноября 1997 г. № 377 «Об утверждении инструкции по организации хранения в аптечных учреждениях различных групп лекарственных средств и изделий медицинского назначения» )

Температурные режимы n n Комнатная температура - (18 – 20) Прохладная (холодная) - (12 – 15) Органопрепараты - (0 – 15) Медицинские жирные масла (4 – 12)

Объекты стандартизации в сфере обращения лекарственных средств üОсновные параметры самого лекарственного средства

Стандарт качества ЛС - нормативный документ, содержащий перечень нормируемых показателей и методов контроля качества ЛС, утверждаемых Минздравом России ОСТ «Стандарты качества ЛС. Основные положения» ОСТ 91500. 05. 001. 00 n n n Фармакопейная статья - государственный стандарт качества ЛС на ЛС под МНН, содержащий обязательный перечень показателей и методов контроля качества с учетом его лекарственной формы Фармакопейная статья предприятия - стандарт качества ЛС на ЛС под ТН, содержащий перечень показателей и методов контроля качества ЛС производства конкретного предприятия, учитывающий конкретную технологию данного предприятия, и прошедший экспертизу и регистрацию в установленном порядке Государственная фармакопея - сборник государственных стандартов качества ЛС, имеющий законодательный характер
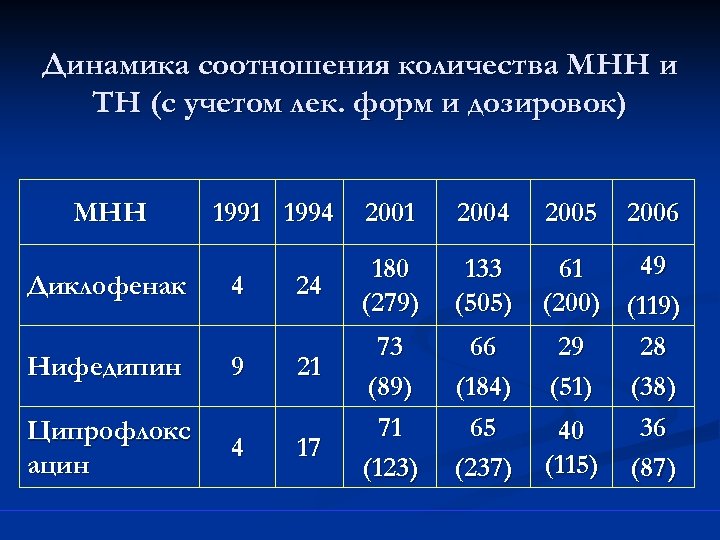
Динамика соотношения количества МНН и ТН (с учетом лек. форм и дозировок) МНН Диклофенак 1991 1994 4 24 Нифедипин 9 21 Ципрофлокс ацин 4 17 2001 2004 180 (279) 49 133 61 (505) (200) (119) 66 29 28 (184) (51) (38) 65 36 40 (237) (115) (87) 73 (89) 71 (123) 2005 2006

Информация о ЛС – неотъемлемый элемент ЛС Лекарственное средство - это единое целое действующего фармакологического вещества в определенной лекарственной форме и информации о нем

Государственный информационный стандарт ЛС ОСТ «Государственный информационный стандарт Основные положения» ОСТ 91500. 05. 0002 -2001 Структура ГИСЛС Фармакопейная статья ЛС Формулярная статья ЛС КФС (ТКФС, КФС ЛП)

Государственный информационный стандарт ЛС: Основные положения Государственный информационный стандарт ЛС (ГИСЛС) – совокупность НД, содержащих официальную информацию о ЛС, разрешенных к медицинскому применению, являющихся первоисточниками информации о ЛС. ГИСЛС – официальный источник информации о ЛС и ЛП в сфере обращения ЛС.

ОСТ 91500. 05. 0002 -2001 «Информационный стандарт лекарственного средства. Основные положения» Общие требования ·ГИСЛС является официальным первоисточником информации о лекарственной средстве в сфере обращения лекарственных средств. ·Иные источники информации о лекарственном средстве должны соответствовать данным, содержащимся в ГИСЛС. · Информация о лекарственном средстве осуществляется в соответствии с требованиями ГИСЛС

Типовая клинико-фармакологи-ческая статья лекарственного средства – более 3 тыс. на сегодняшний день

Типовая клинико – фармакологическая статья ТКФС – официальный документ, содержащий сведения об основных свойствах ЛС или часто используемых (стандартных) его комбинаций, определяющих эффективность и безопасность ЛС
www. regmed. ru
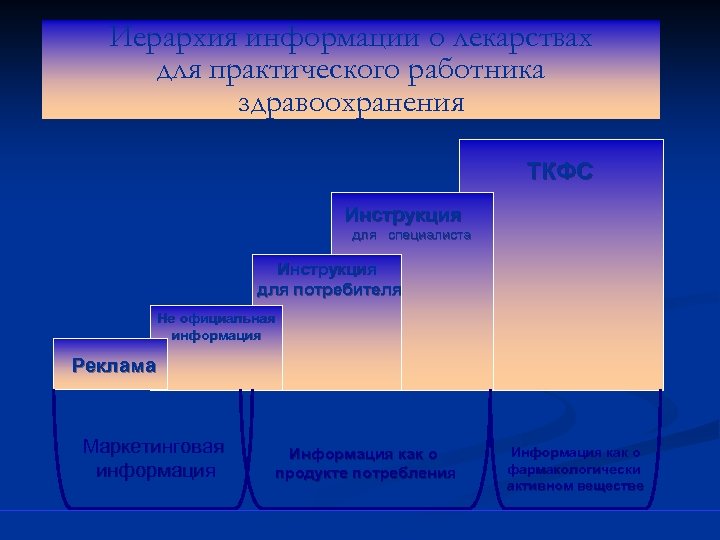
Иерархия информации о лекарствах для практического работника здравоохранения ТКФС Инструкция для специалиста Инструкция для потребителя Не официальная информация Реклама Маркетинговая информация Информация как о продукте потребления Информация как о фармакологически активном веществе

Информационная доступность

Справочник - - издание, содержащее краткие сведения научного, общественно-политического, прикладного или бытового характера. Официальные • Государственный реестр ЛС • Справочник ЛС, отпускаемых по рецепту врача (фельдшера) при оказании дополнительной бесплатной медицинской помощи отдельным категориям граждан, имеющим право на получение государственной социальной помощи Неофициальные • ВИДАЛЬ • РЛС • Большая Российская энциклопедия лекарств • Синонимы лекарственных средств • Фармакологический справочник • Справочник лекарственных средств

Сравнение содержания раздела побочные эффекты статьи на ацетилсалициловую кислоту в справочнике ВИДАЛЬ и Государственном реестре Государственный реестр ВИДАЛЬ Тошнота, снижение аппетита, гастралгия, диарея, аллергические реакции (кожная сыпь, ангионевротический отек, бронхоспазм), нарушение функции печени, нарушение функции почек, тромбоцитопения, анемия. При длительном применении – головокружение, головная боль, рвота, эрозивно-язвенные поражения ЖКТ, гипокоагуляция, кровотечения, нарушения зрения, шум в ушах лейкопения, синдром Рейе, «аспириновая» астма, снижение остроты слуха, папиллярный некроз, асептический менингит, усиление симптомов ХСН, отеки ?
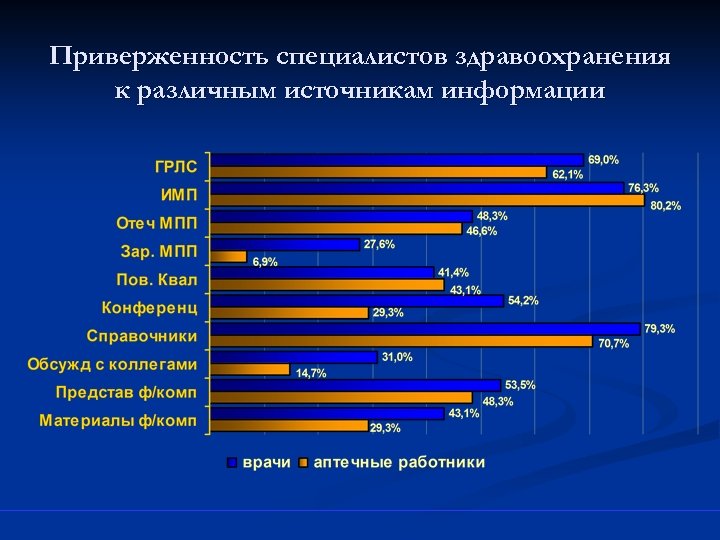
Приверженность специалистов здравоохранения к различным источникам информации
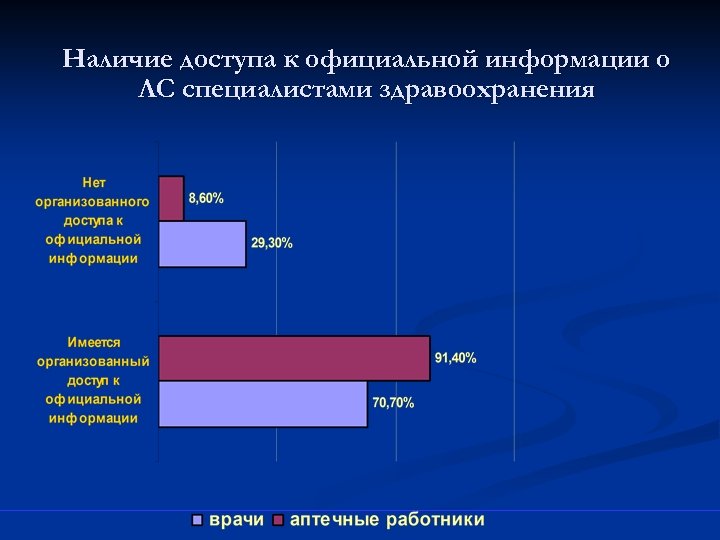
Наличие доступа к официальной информации о ЛС специалистами здравоохранения

Информационный стандарт и реальная практика Препарат – ИБУПРОФЕН: нежелательные реакции Видаль (2005, стр. 1358) Отсутствуют: Со стороны пищеварительной системы: НПВП-гастропатия (нарушения свертывания крови, беременность, период лактации РЛС (2006, стр 314) Отсутствуют: нарушения свертывания крови, беременность I и II триместры, период лактации ТКФС Гиперчувствительность, эрозивно-язвенные заболевания органов ЖКТ (в т. ч. язвенная болезнь желудка и 12 -перстной кишки в стадии обострения, язвенный колит, пептическая язва, болезнь Крона неспецифический язвенный колит), "аспириновая" астма, нарушения свертывания крови (в т. ч. гемофилия, удлинение времени кровотечения, склонность к кровотечениям, геморрагический диатез), беременность, период лактации, детский возраст до 2 лет (капли для приема внутрь), до 3 мес (суспензия для приема внутрь для детей), до 12 лет (капсулы, капсулы пролонгированного действия)

Препарат – ИБУПРОФЕН: нежелательные реакции Видаль (2005, стр. 1358)Отсутствуют: ТКФС Со стороны пищеварительной системы: НПВП-гастропатия (тошнота, рвота, боль в животе, изжога, снижение аппетита, диарея, метеоризм, боль и дискомфорт в эпигастральной области), изъязвления слизистой оболочки ЖКТ (в ряде случаев осложняются перфорацией и кровотечениями); раздражение, сухость слизистой оболочки полости рта или боль во рту, изъязвление слизистой оболочки десен, афтозный стоматит, панкреатит, запор, гепатит. Со стороны дыхательной системы: одышка, бронхоспазм. Со стороны органов чувств: снижение слуха, звон или шум в ушах, обратимый токсический неврит зрительного нерва, нечеткость зрения или диплопия, сухость и раздражение глаз, отек конъюнктивы и век (аллергического генеза), скотома. Со стороны нервной системы: головная боль, головокружение, бессонница, тревожность, нервозность и раздражительность, психомоторное возбуждение, сонливость, депрессии, спутанность сознания, галлюцинации, редко - асептический менингит (чаще у пациентов с аутоиммунными заболеваниями). РЛС (2006, стр. 314) Отсутствуют: Со стороны ССС: развитие или усугубление СН, тахикардия, НПВП-гастропатия (боль в животе, боль в эпигастральной области), повышение АД. раздражение, сухость слизистой оболочки полости рта или боль во рту, Со стороны мочевыделительной системы: острая почечная изъязвление слизистой оболочки десен, афтозный стоматит, панкреатит, недостаточность, аллергический нефрит, нефротический гепатит, снижение слуха, обратимый токсический неврит зрительного нерва, синдром (отеки), полиурия, цистит. сухость и раздражение глаз, отек конъюнктивы и век (аллергического генеза), Аллергические реакции: кожная сыпь (обычно эритематозная, скотома, тревожность, нервозность и раздражительность, сонливость, крапивница), кожный зуд, ангионевротический отек, депрессии, спутанность сознания, галлюцинации, редко - асептический анафилактоидные реакции, анафилактический шок, менингит (чаще у пациентов с аутоиммунными заболеваниями), развитие бронхоспазм, лихорадка, мультиформная экссудативная или усугубление СН, Тахикардия, острая почечная недостаточность, эритема (в т. ч. синдром Стивенса-Джонсона), токсический аллергический нефрит, полиурия, цистит, анафилактоидные реакции, эпидермальный некролиз (синдром Лайелла), эозинофилия, анафилактический шок, бронхоспазм, лихорадка, мультиформная экссудативная аллергический ринит. эритема, (в т. ч. синдром Стивенса-Джонсона), токсический эпидермальный Со стороны органов кроветворения: анемия (в т. ч. некролиз (синдром Лайелла), эозинофилия, аллергический ринит, анемия гемолитическая, апластическая), тромбоцитопения и (в т. ч. апластическая), тромбоцитопеническая пурпура, усиление потоотделения. тромбоцитопеническая пурпура, агранулоцитоз, лейкопения. Риск развития изъязвлений слизистой оболочки ЖКТ, кровотечения (желудочно Прочие: усиление потоотделения. -кишечного, десневого, маточного, геморроидального), нарушений зрения Риск развития изъязвлений слизистой оболочки ЖКТ, (нарушения цветового зрения, скотомы, амблиопии) возрастает при длительном Кровотечения (желудочно-кишечного, десневого, маточного, применении в больших дозах. геморроидального), нарушений зрения (нарушения цветового зрения, скотомы, амблиопии) возрастает при длительном USP DI (2002) Полное соответствие применении в больших дозах. НПВП-гастропатия (боль в животе, изжога, метеоризм), раздражение, сухость слизистой оболочки полости рта или боль во рту, изъязвление слизистой оболочки десен, афтозный стоматит, панкреатит, запор, гепатит, снижение слуха, звон или шум в ушах, обратимый токсический неврит зрительного нерва, сухость и раздражение глаз, отек конъюнктивы и век (аллергического генеза), котома, тревожность, депрессии, спутанность сознания, галлюцинации, развитие или усугубление СН, тахикардия, повышение АД, острая почечная недостаточность, аллергический нефрит, кожный зуд, анафилактоидные реакции, анафилактический шок, бронхоспазм, лихорадка, мультиформная экссудативная эритема (в т. ч. синдром Стивенса-Джонсона), токсический эпидермальный некролиз (синдром Лайелла), эозинофилия, аллергический ринит, тромбоцитопеническая пурпура, лейкопения, усиление потоотделения, Риск развития изъязвлений слизистой оболочки ЖКТ, кровотечения (желудочнокишечного, десневого, маточного, геморроидального), нарушений зрения (нарушения цветового зрения, скотомы, амблиопии) возрастает при длительном применении в больших дозах. . .
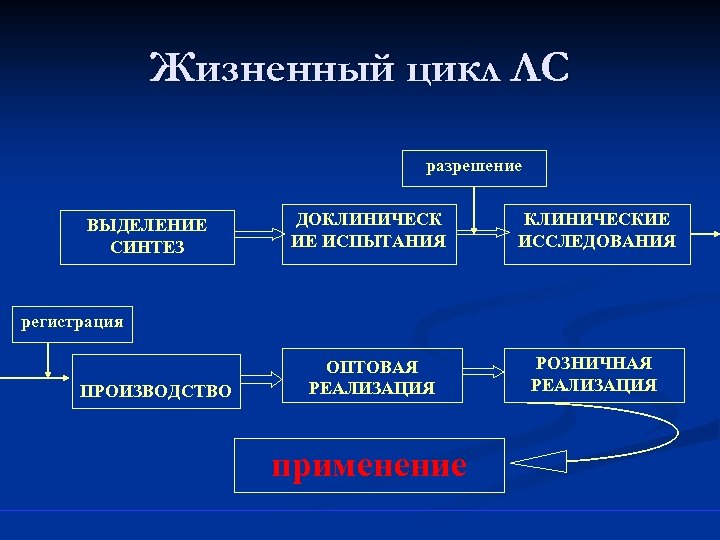
Жизненный цикл ЛС разрешение ВЫДЕЛЕНИЕ СИНТЕЗ ДОКЛИНИЧЕСК ИЕ ИСПЫТАНИЯ КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ ОПТОВАЯ РЕАЛИЗАЦИЯ РОЗНИЧНАЯ РЕАЛИЗАЦИЯ регистрация ПРОИЗВОДСТВО применение

Стандартизация применения ЛС Концепция рационального применения ЛС

Рациональное использование ЛС Правильное ЛС для Правильного пациента в Правильной дозе в Правильное время по Правильной цене

Развитие концепции рационального использования ЛС n Перечень основных ЛС n n n 40 –е г. – Норвегия, 60 -е г. – Куба и т. д. 1975 г. – 28 сессия ВАЗ – концепция основных ЛС (основные ЛС – ЛС, необходимые для профилактики и лечения наиболее распространенных заболеваний) 1977 г. – Первый перечень основных ЛС ВОЗ 1981 г. – Программа по основным ЛС ВОЗ 1985 г. – Конференция экспертов по рациональному использованию ЛС (Найроби) Формулярная система (основа – принципы доказательной медицины)

Развитие концепции рационального использования ЛС в России n Перечень жизненно важных ЛС n n Формулярная система n n n Первый перечень утвержден в 1992 г. , с 1995 г. Перечни формируются по МНН С 1993 г. По 1998 г. – проект РФМ, С 1999 г. – Формулярная система. Федеральное руководство по использованию ЛС Программа ДЛО n 2005 г. (перечни, ценообразование, контроль)

Роль государства в формировании ассортиментной политики: n n n n Регистрация ЛС Перечень жизненно необходимых и важнейших лекарственных средств утвержден распоряжением Правительства РФ от 29. 12. 2005 № 2343 -р Перечень «Минимальный ассортимент лекарственных средств, необходимых для оказания медицинской помощи» утвержден приказом Минздравсоцразвития РФ от 29. 04. 2005 № 312 Перечни лекарственных средств, отпускаемых по рецептам врача (фельдшера) при оказании дополнительной бесплатной медицинской помощи отдельным категориям граждан, имеющим право на получение государственной социальной помощи утверждены приказами Минздравсоцразвития РФ от 02. 12. 2004 № 296; от 24. 12. 2004 № 321; от 31. 03. 2005 № 245; от 28. 09. 2005 № 601; от 30. 12. 2005 № 811, от 18. 09. 2006 № 665) Перечень ЛС, отпускаемых без рецепта врача (приказы МЗСР № 578 от 13. 09. 2005 и № 823 от 04. 12. 2006) Стандарты лечения(около 180) Перчень ЛС для лечения больных гемофилией, муковисцидозом, гипофизарным нанизмом, болезню Гоше, миелолейкозом, рассеянным склерозом и после транслантанции органов и тканей

Для рационального использования ограниченных ресурсов необходимо применять результаты фармакоэкономических и фармакоэпидемиологических исследований

Фармакоэкономика Фармакоэпидемиология

n Фармакоэкономика изучает в сравнительном плане соотношение между затратами и эффективностью, безопасностью, качеством жизни при альтернативных схемах лечения (профилактики) заболевания

Барьеры для лекарственных средств при включении в списки льготного обеспечения Допуск к программам возмещения и воздействие на услуги производителей Затраты эффективность Безопасность, эффективность и качество « 4 -й барьер» « 5 -й барьер» 65

Фармакоэпидемиология – раздел клинической фармакологии, изучающий применение лекарственных средств и их эффекты на уровне популяции или больших групп людей. Основной ее целью является содействие рациональному применению наиболее эффективных и безопасных лекарственных средств. 3

Основные данные об эффективности и безопасности лекарственных средств должны быть получены из результатов клинических исследований, выполненных в соответствии с принципами медицины, основанной на доказательствах (Evidence Based Medicine). Наибольшего доверия заслуживают результаты крупных международных многоцентровых рандомизированных двойных «слепых» плацебо контролируемых клинических исследований. Их недостатки: - «идеальный» контингент пациентов далек от реального - ограничения по количеству пациентов - ограничения по времени проведения. 7
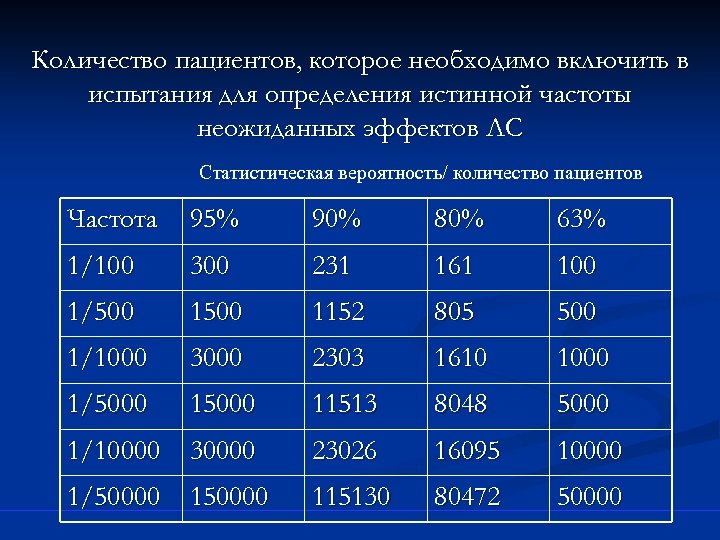
Количество пациентов, которое необходимо включить в испытания для определения истинной частоты неожиданных эффектов ЛС Статистическая вероятность/ количество пациентов Частота 95% 90% 80% 63% 1/100 300 231 161 100 1/500 1152 805 500 1/1000 3000 2303 1610 1000 1/5000 11513 8048 5000 1/10000 30000 23026 16095 10000 1/50000 115130 80472 50000

Предпосылки развития фармакоэпидемиологии Проблемы оценки эффективности: фармакоэпидемиологические исследования дополняют результаты клинических исследований и осуществляют: • учет факторов реальной клинической практики (оценка влияния сопутствующей терапии и сопутствующих заболеваний, данные о терапии пожилых пациентов, детей, и беременных) • оценки отдаленной клинической перспективы • учет редких осложнений 8

Основные задачи фармакоэпидемиологического исследования • выявление новых, ранее неизвестных эффектов ЛС (как благоприятных, так и нежелательных); • определение взаимосвязи этих эффектов с приемом ЛС; • оценка риска/частоты развития выявленных эффектов в популяции • определение потребности в лекарственных средствах 10
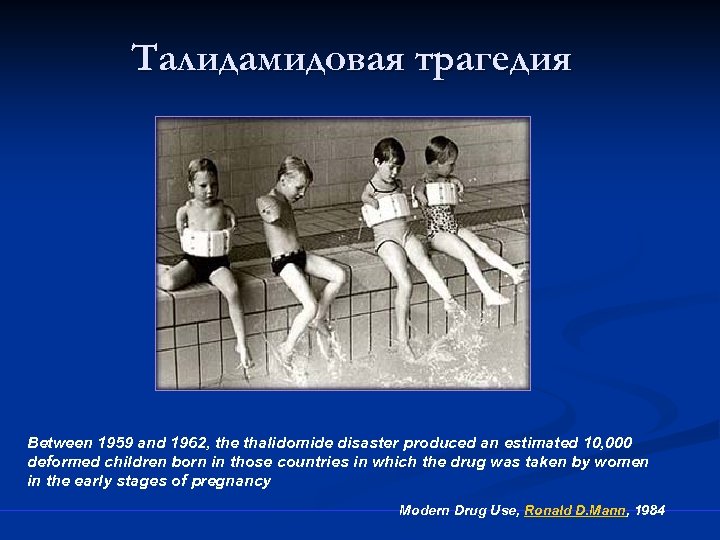
Талидамидовая трагедия Between 1959 and 1962, the thalidomide disaster produced an estimated 10, 000 deformed children born in those countries in which the drug was taken by women in the early stages of pregnancy Modern Drug Use, Ronald D. Mann, 1984

Непрерывность изучения безопасности лекарственных препаратов Предрегистрационные исследования ЛС ДКИ КИ Регистрация Пострегистрационные исследования ЛС Метод СС Рецептурный мониторинг Мониторинги стационаров КИ

Медико - социальные катастрофы, связанные с применением ЛП Растворитель диэтиленгликоль для сульфаниламида (1937) Регистрация смертельных исходов у детей Талидомид (1961) Церивастатин (1983 – 2001) Амедицин Фокомелия Рабдомиолиз Продположительная реакция идиосинкразии Глазо-слизисто-кожный синдром и склеротический перитонит Кардиотоксичность (удлинение интервала QT) Прокталол (1994) Терфенадин и астемизол (2001) Фенфлурамин Поражение клапанов сердца (через 24 года после регистрации) Метипранолол Увеит Вигабатрин Нарушение полей зрения Цизаприд Удлинение интервала QT

Отзыв ЛС с фармрынка России за последние 10 лет 235 по МНН (514 с учетом лекформ и n Всего отозвано: дозировок) n По причине небезопасности: 8 Среди отозванных ЛС: n Астемизол n Терфенадин n Церивастатин n Ацетилсалициловая к-та (лекформы для детей) n По данным системы СС: 0

«История возвращается» n 1995 г. – на Гаити зарегистрировано 89 смертей из-за применения парацетамолового сиропа от кашля, изготовленного на основе диэтиленгликоля n 1998 г. – в Индии зарегистрировано 30 смертей детей из-за применения сиропа от кашля такого же происхождения http: //www. who. int/mediacentre/factsheets/fs 275/ru/index. html n 2004 г. - в Панаме зарегистрировано 38 смертельных случая и 32 тяжелых отравления из-за употребления микстур от кашля, противоаллергической мази и противоаллергическом ЛС несоответствующего качества (производства одной из государственных фармацевтических фабрик Панамы ) – в препарате обнаружен диэтиленгликоль http: //e-news. com. ua/ru/show/126278. html

Современные показания к назначению талидомида n Лепра FDA n Бактериальный менингит J Infect Dis 2000; 182: 983 -987 n Тяжелые кожные проявления при саркоидозе Baughman R. P. et all. , 2002 Nguyen Y. T. et al. , 2004 Walter M. C. et al. , 2003 n Множественная и рефрактерная миелома Singhal S et al, N Engl J Med 1999 341: 1565 -1571 Barlogie B. et al, Blood 2000 96: 514 a Hideshima T et al, Blood 2000 96: 2943 -2950 n Синдром Лайелла J. Am. Board Fam. Pract. , Gregory A. 2000, 13(5): 364 -370 Clin. Exp. Dermatol. , Jarrett P. 1997, May; 22(3): 146 -147

Актуальность оценки НР для России n n n Многонациональная страна Большое количество зарегистрированных ЛП Отсутствие надлежащей системы Фармаконадзора Отсутствие адекватной методологии оценки НР ЛП Широкое потребление ЛП, не используемых за рубежом, т. е. отсутствие возможности экстраполяции зарубежных данных на отечественную практику Отсутствие широкомасштабных наблюдательных исследований «То, что не ясно, следует выяснить. То, что трудно творить, следует делать с величайшей настойч Конфуций

Если бы все это было чуточку проще … 21

Спасибо за внимание!
431ae539f689da97c178a287c3f30703.ppt