лекция по микро мониторингу (2).ppt
- Количество слайдов: 98
 СОВЕРШЕНСТВОВАНИЕ ЭПИДЕМИОЛОГИЧЕСКОГО НАДЗОРА ЗА ИНФЕКЦИЯМИ, СВЯЗАННЫМИ С ОКАЗАНИЕМ МЕДИЦИНСКОЙ ПОМОЩИ НА ОСНОВЕ ОПТИМИЗАЦИИ МИКРОБИОЛОГИЧЕСКОГО МОНИТОРИНГА Пермь - 2012
СОВЕРШЕНСТВОВАНИЕ ЭПИДЕМИОЛОГИЧЕСКОГО НАДЗОРА ЗА ИНФЕКЦИЯМИ, СВЯЗАННЫМИ С ОКАЗАНИЕМ МЕДИЦИНСКОЙ ПОМОЩИ НА ОСНОВЕ ОПТИМИЗАЦИИ МИКРОБИОЛОГИЧЕСКОГО МОНИТОРИНГА Пермь - 2012
 Факторы роста внутрибольничных инфекций в современных условиях Øсоздание крупных больничных комплексов со своеобразной экологической системой Øформирование мощного искусственного (артифициального) механизма передачи возбудителей инфекций Øактивизация естественных механизмов передачи возбудителей (воздушно-капельного и контактнобытового) Øналичие большого количества источников возбудителей инфекций - пациентов, поступающих в стационар с ГСИ Øширокое бесконтрольное применение антибиотиков, способствующих появлению лекарственной устойчивости микроорганизмов Øформирование внутрибольничных штаммов микроорганизмов, обладающих селективными преимуществами и экологической пластичностью Øувеличение контингентов риска – пациентов, выхаживаемых и излечиваемых благодаря достижениям современной медицины Øвозрастание доли тяжелобольных пациентов со сниженной неспецифической резистентностью Øснижение неспецифической резистентности у всего населения земного шара в силу его эволюционной неподготовленности к стремительно изменяющимся условиям жизни Ø широкое использование для диагностики сложной техники и оборудования, требующее особых методов стерилизации
Факторы роста внутрибольничных инфекций в современных условиях Øсоздание крупных больничных комплексов со своеобразной экологической системой Øформирование мощного искусственного (артифициального) механизма передачи возбудителей инфекций Øактивизация естественных механизмов передачи возбудителей (воздушно-капельного и контактнобытового) Øналичие большого количества источников возбудителей инфекций - пациентов, поступающих в стационар с ГСИ Øширокое бесконтрольное применение антибиотиков, способствующих появлению лекарственной устойчивости микроорганизмов Øформирование внутрибольничных штаммов микроорганизмов, обладающих селективными преимуществами и экологической пластичностью Øувеличение контингентов риска – пациентов, выхаживаемых и излечиваемых благодаря достижениям современной медицины Øвозрастание доли тяжелобольных пациентов со сниженной неспецифической резистентностью Øснижение неспецифической резистентности у всего населения земного шара в силу его эволюционной неподготовленности к стремительно изменяющимся условиям жизни Ø широкое использование для диагностики сложной техники и оборудования, требующее особых методов стерилизации
 Внутрибольничные инфекции – новые горизонты профилактики В. И. Покровский, В. Г. Акимкин, Н. И. Брико, Е. Б. Брусина, Л. П. Зуева, О. В. Ковалишена, В. Л. Стасенко, А. В. Тутельян, И. В. Фельдблюм, В. В. Шкарин
Внутрибольничные инфекции – новые горизонты профилактики В. И. Покровский, В. Г. Акимкин, Н. И. Брико, Е. Б. Брусина, Л. П. Зуева, О. В. Ковалишена, В. Л. Стасенко, А. В. Тутельян, И. В. Фельдблюм, В. В. Шкарин
 Цель концепции профилактики ИСМП • определение стратегии профилактики ИСМП для снижения уровня заболеваемости и связанной с ней нетрудоспособности, смертности пациентов, а также экономического ущерба на основе разработки теоретических основ управления ИСМП и внедрения в практику здравоохранения научно обоснованной системы эпидемиологического надзора и комплекса эффективных организационных, профилактических, противоэпидемических и лечебно-диагностических мероприятий
Цель концепции профилактики ИСМП • определение стратегии профилактики ИСМП для снижения уровня заболеваемости и связанной с ней нетрудоспособности, смертности пациентов, а также экономического ущерба на основе разработки теоретических основ управления ИСМП и внедрения в практику здравоохранения научно обоснованной системы эпидемиологического надзора и комплекса эффективных организационных, профилактических, противоэпидемических и лечебно-диагностических мероприятий
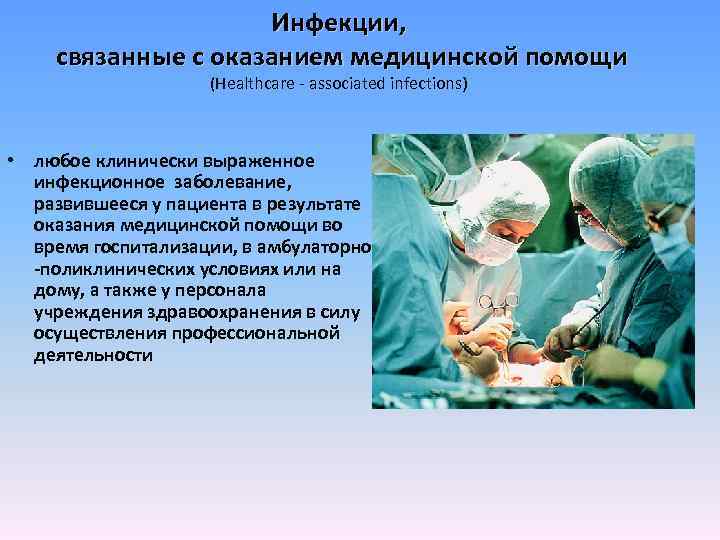 Инфекции, связанные с оказанием медицинской помощи (Healthcare - associated infections) • любое клинически выраженное инфекционное заболевание, развившееся у пациента в результате оказания медицинской помощи во время госпитализации, в амбулаторно -поликлинических условиях или на дому, а также у персонала учреждения здравоохранения в силу осуществления профессиональной деятельности
Инфекции, связанные с оказанием медицинской помощи (Healthcare - associated infections) • любое клинически выраженное инфекционное заболевание, развившееся у пациента в результате оказания медицинской помощи во время госпитализации, в амбулаторно -поликлинических условиях или на дому, а также у персонала учреждения здравоохранения в силу осуществления профессиональной деятельности
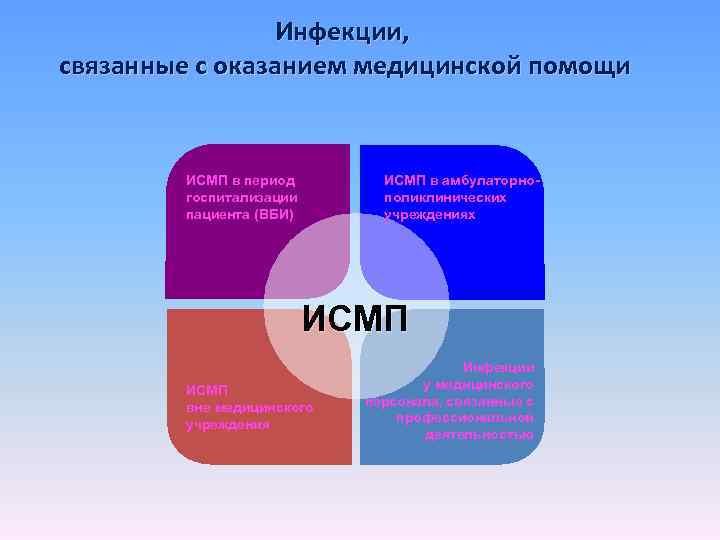 Инфекции, связанные с оказанием медицинской помощи ИСМП в период госпитализации пациента (ВБИ) ИСМП в амбулаторнополиклинических учреждениях ИСМП вне медицинского учреждения Инфекции у медицинского персонала, связанные с профессиональной деятельностью
Инфекции, связанные с оказанием медицинской помощи ИСМП в период госпитализации пациента (ВБИ) ИСМП в амбулаторнополиклинических учреждениях ИСМП вне медицинского учреждения Инфекции у медицинского персонала, связанные с профессиональной деятельностью
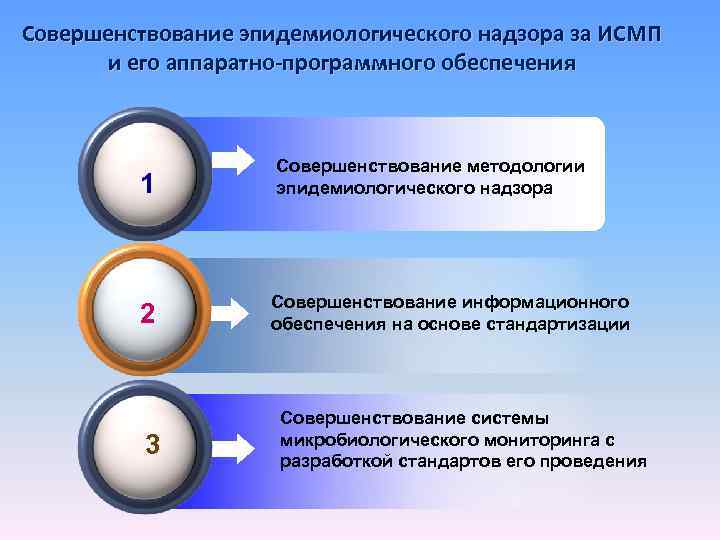 Совершенствование эпидемиологического надзора за ИСМП и его аппаратно-программного обеспечения 1 2 Title 3 Совершенствование методологии эпидемиологического надзора Совершенствование информационного обеспечения на основе стандартизации Совершенствование системы микробиологического мониторинга с разработкой стандартов его проведения
Совершенствование эпидемиологического надзора за ИСМП и его аппаратно-программного обеспечения 1 2 Title 3 Совершенствование методологии эпидемиологического надзора Совершенствование информационного обеспечения на основе стандартизации Совершенствование системы микробиологического мониторинга с разработкой стандартов его проведения
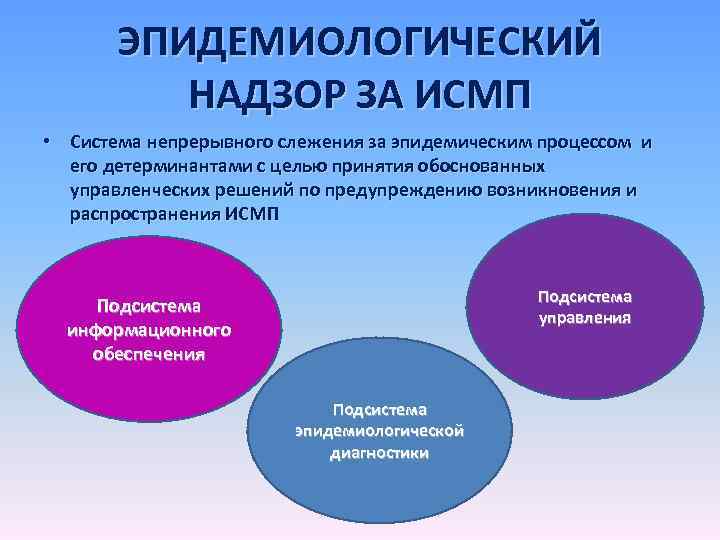 ЭПИДЕМИОЛОГИЧЕСКИЙ НАДЗОР ЗА ИСМП • Система непрерывного слежения за эпидемическим процессом и его детерминантами с целью принятия обоснованных управленческих решений по предупреждению возникновения и распространения ИСМП Подсистема управления Подсистема информационного обеспечения Подсистема эпидемиологической диагностики
ЭПИДЕМИОЛОГИЧЕСКИЙ НАДЗОР ЗА ИСМП • Система непрерывного слежения за эпидемическим процессом и его детерминантами с целью принятия обоснованных управленческих решений по предупреждению возникновения и распространения ИСМП Подсистема управления Подсистема информационного обеспечения Подсистема эпидемиологической диагностики
 Подсистема информационного обеспечения Выявление, учет и регистрация случаев ГСИ среди пациентов Выявление, учет и регистрация случаев ГСИ среди медицинского персонала • Эпидемиологический мониторинг • Микробиологический мониторинг • Иммунологический мониторинг • Санитарно-гигиенический мониторинг
Подсистема информационного обеспечения Выявление, учет и регистрация случаев ГСИ среди пациентов Выявление, учет и регистрация случаев ГСИ среди медицинского персонала • Эпидемиологический мониторинг • Микробиологический мониторинг • Иммунологический мониторинг • Санитарно-гигиенический мониторинг
 МИКРОБИОЛОГИЧЕСКИЙ МОНИТОРИНГ это комплексное и динамическое наблюдение за патогенными и условно-патогенными микроорганизмами, выделенными от пациентов, персонала и объектов внешней среды стационара, их свойствами и особенностями циркуляции ЦЕЛЬ: характеристика микробного пейзажа стационара и тенденций его изменения для своевременной оценки эпидемиологической обстановки и проведения эффективных профилактических и противоэпидемических мероприятий
МИКРОБИОЛОГИЧЕСКИЙ МОНИТОРИНГ это комплексное и динамическое наблюдение за патогенными и условно-патогенными микроорганизмами, выделенными от пациентов, персонала и объектов внешней среды стационара, их свойствами и особенностями циркуляции ЦЕЛЬ: характеристика микробного пейзажа стационара и тенденций его изменения для своевременной оценки эпидемиологической обстановки и проведения эффективных профилактических и противоэпидемических мероприятий
 ЗАДАЧИ: § § этиологическая расшифровка случаев ГСИ; определение спектра микроорганизмов, выделяемых от пациентов, персонала, внешней среды в различных отделениях и в стационаре в целом; § определение ведущего возбудителя, «проблемных» возбудителей; § выявление госпитальных штаммов микроорганизмов; § оценка качества профилактической и очаговой дезинфекции, дезинфекции и стерилизации ИМН; § расшифровка групповых случаев и вспышек ВБИ; § установление путей и факторов передачи инфекции; § дифференцирование заносов инфекции и ВБИ; § корректировка дезинфекционных мероприятий § корректировка антимикробной терапии
ЗАДАЧИ: § § этиологическая расшифровка случаев ГСИ; определение спектра микроорганизмов, выделяемых от пациентов, персонала, внешней среды в различных отделениях и в стационаре в целом; § определение ведущего возбудителя, «проблемных» возбудителей; § выявление госпитальных штаммов микроорганизмов; § оценка качества профилактической и очаговой дезинфекции, дезинфекции и стерилизации ИМН; § расшифровка групповых случаев и вспышек ВБИ; § установление путей и факторов передачи инфекции; § дифференцирование заносов инфекции и ВБИ; § корректировка дезинфекционных мероприятий § корректировка антимикробной терапии
 Совершенствование лабораторной диагностики и мониторинга возбудителей ИСМП Оснащение лабораторий, участвующих в этиологической расшифровке и мониторинге возбудителей ИСМП, современным лабораторным оборудованием, диагностическими системами Совершенствование и унификация методов выделения и идентификации возбудителей ИСМП Оптимизация системы забора и доставки образцов биологического материала в лабораторию
Совершенствование лабораторной диагностики и мониторинга возбудителей ИСМП Оснащение лабораторий, участвующих в этиологической расшифровке и мониторинге возбудителей ИСМП, современным лабораторным оборудованием, диагностическими системами Совершенствование и унификация методов выделения и идентификации возбудителей ИСМП Оптимизация системы забора и доставки образцов биологического материала в лабораторию
 Совершенствование лабораторной диагностики и мониторинга возбудителей ИСМП Разработка и внедрение экспресс - методов микробиологической диагностики ИСМП Расшифровка генома актуальных возбудителей ИСМП, циркулирующих в учреждениях здравоохранения Разработка и внедрение унифицированного автоматизированного рабочего места врача - клинического микробиолога
Совершенствование лабораторной диагностики и мониторинга возбудителей ИСМП Разработка и внедрение экспресс - методов микробиологической диагностики ИСМП Расшифровка генома актуальных возбудителей ИСМП, циркулирующих в учреждениях здравоохранения Разработка и внедрение унифицированного автоматизированного рабочего места врача - клинического микробиолога
 Совершенствование лабораторной диагностики и мониторинга возбудителей ИСМП Обеспечение преемственности между этиологической расшифровкой ИСМП и клинической интерпретацией полученных результатов Оптимизация перечня показаний для микробиологического исследования клинического материала и объектов больничной среды Создание референслабораторий
Совершенствование лабораторной диагностики и мониторинга возбудителей ИСМП Обеспечение преемственности между этиологической расшифровкой ИСМП и клинической интерпретацией полученных результатов Оптимизация перечня показаний для микробиологического исследования клинического материала и объектов больничной среды Создание референслабораторий
 Разработка стандартов профилактики ИСМП ь ост и вн к кти акти е л фф фи Э ро п Стандартное определение случая ИСМП различных нозологических форм Стандартное определение госпитального штамма Стандарты эпидемиологического надзора Стандарты профилактических и противоэпидемических мероприятий
Разработка стандартов профилактики ИСМП ь ост и вн к кти акти е л фф фи Э ро п Стандартное определение случая ИСМП различных нозологических форм Стандартное определение госпитального штамма Стандарты эпидемиологического надзора Стандарты профилактических и противоэпидемических мероприятий
 Нормативно-технические документы, определяющие регламент микробиологического мониторинга • Сан. Пи. Н 2. 1. 3. 2576 -10 Гигиенические требования к размещению, устройству, оборудованию и эксплуатации больниц, родильных домов и других лечебных стационаров • Приказ МЗ РФ от 26. 11. 97 г. «О совершенствовании мероприятий по профилактике внутрибольничных инфекций в акушерских стационарах» . № 345. - 65 с. • МУ 4. 2. 2942 -11 Методы санитарно-бактериологических исследований объектов окружающей среды, воздуха и контроля стерильности в лечебных организациях (4. 2 МЕТОДЫ КОНТРОЛЯ. БИОЛОГИЧЕСКИЕ И МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ) • МУ № 287 -113 по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения от 1998 г. • МР Микробиологический мониторинг в системе эпидемиологического надзора за внутрибольничными гнойно-септическими инфекциями. – Пермь, 2006. – 23 с. • МР Совершенствование эпидемиологического надзора за внутрибольничными гнойно-септическими инфекциями на основе оптимизации микробиологического мониторинга. – Пермь, 20011 – 28 с.
Нормативно-технические документы, определяющие регламент микробиологического мониторинга • Сан. Пи. Н 2. 1. 3. 2576 -10 Гигиенические требования к размещению, устройству, оборудованию и эксплуатации больниц, родильных домов и других лечебных стационаров • Приказ МЗ РФ от 26. 11. 97 г. «О совершенствовании мероприятий по профилактике внутрибольничных инфекций в акушерских стационарах» . № 345. - 65 с. • МУ 4. 2. 2942 -11 Методы санитарно-бактериологических исследований объектов окружающей среды, воздуха и контроля стерильности в лечебных организациях (4. 2 МЕТОДЫ КОНТРОЛЯ. БИОЛОГИЧЕСКИЕ И МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ) • МУ № 287 -113 по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения от 1998 г. • МР Микробиологический мониторинг в системе эпидемиологического надзора за внутрибольничными гнойно-септическими инфекциями. – Пермь, 2006. – 23 с. • МР Совершенствование эпидемиологического надзора за внутрибольничными гнойно-септическими инфекциями на основе оптимизации микробиологического мониторинга. – Пермь, 20011 – 28 с.
 Организационные формы микробиологического мониторинга • Мониторинг, ориентированный на оценку санитарно-гигиенического режима учреждения • Мониторинг по непрерывному слежению за циркуляцией всех микроорганизмов в стационаре с полным изучением и сопоставлением их биологических свойств • Мониторинг, нацеленный на своевременное выявление внутрибольничных штаммов
Организационные формы микробиологического мониторинга • Мониторинг, ориентированный на оценку санитарно-гигиенического режима учреждения • Мониторинг по непрерывному слежению за циркуляцией всех микроорганизмов в стационаре с полным изучением и сопоставлением их биологических свойств • Мониторинг, нацеленный на своевременное выявление внутрибольничных штаммов
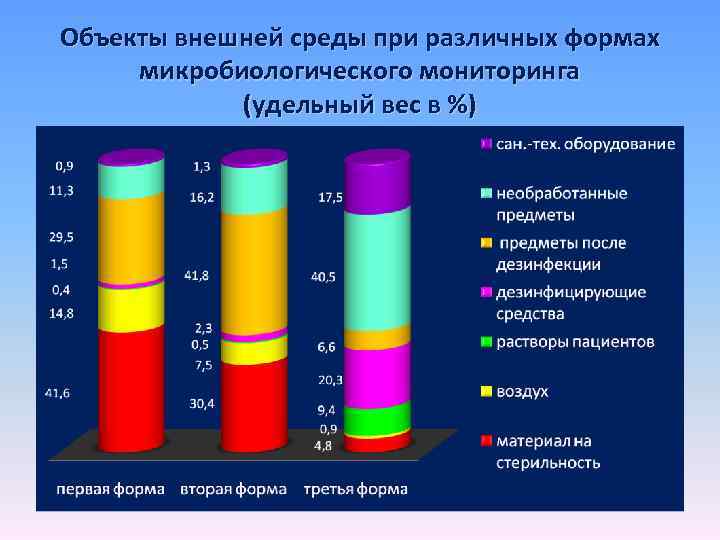 Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %)
Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %)
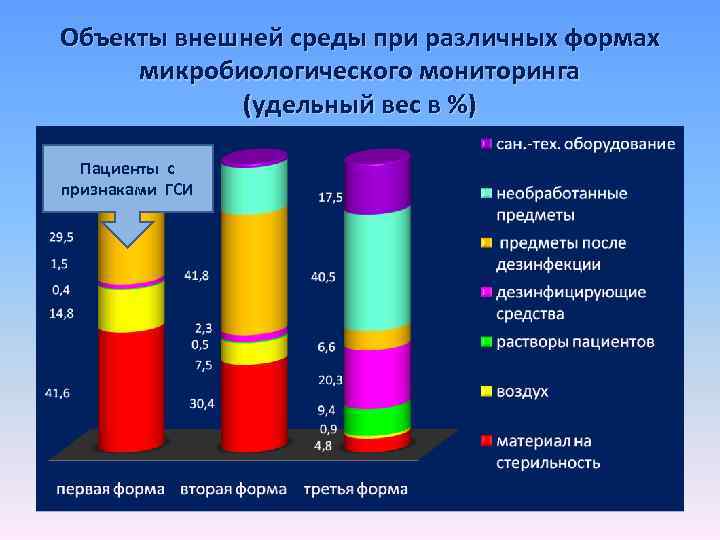 Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %) Пациенты с признаками ГСИ
Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %) Пациенты с признаками ГСИ
 Организационные формы микробиологического мониторинга • Мониторинг, ориентированный на оценку санитарно-гигиенического режима учреждения • Мониторинг по непрерывному слежению за циркуляцией всех микроорганизмов в стационаре с полным изучением и сопоставлением их биологических свойств • Мониторинг, нацеленный на своевременное выявление внутрибольничных штаммов
Организационные формы микробиологического мониторинга • Мониторинг, ориентированный на оценку санитарно-гигиенического режима учреждения • Мониторинг по непрерывному слежению за циркуляцией всех микроорганизмов в стационаре с полным изучением и сопоставлением их биологических свойств • Мониторинг, нацеленный на своевременное выявление внутрибольничных штаммов
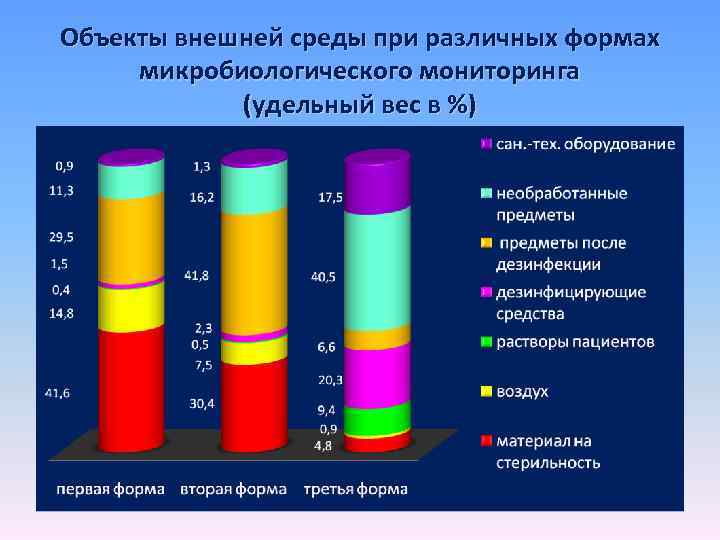 Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %)
Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %)
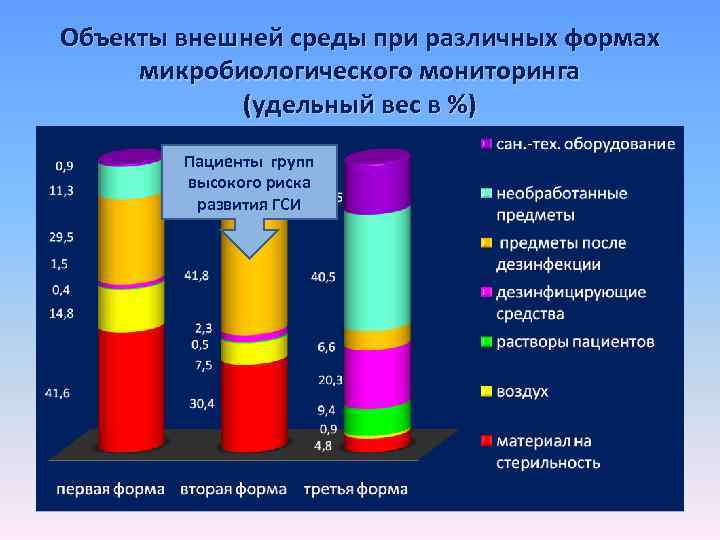 Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %) Пациенты групп высокого риска развития ГСИ
Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %) Пациенты групп высокого риска развития ГСИ
 Организационные формы микробиологического мониторинга • Мониторинг, ориентированный на оценку санитарно-гигиенического режима учреждения • Мониторинг по непрерывному слежению за циркуляцией всех микроорганизмов в стационаре с полным изучением и сопоставлением их биологических свойств • Мониторинг, нацеленный на своевременное выявление внутрибольничных штаммов
Организационные формы микробиологического мониторинга • Мониторинг, ориентированный на оценку санитарно-гигиенического режима учреждения • Мониторинг по непрерывному слежению за циркуляцией всех микроорганизмов в стационаре с полным изучением и сопоставлением их биологических свойств • Мониторинг, нацеленный на своевременное выявление внутрибольничных штаммов
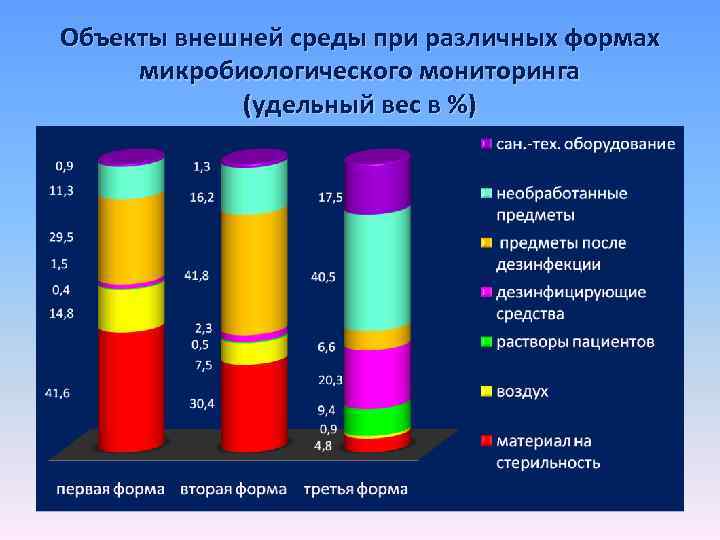 Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %)
Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %)
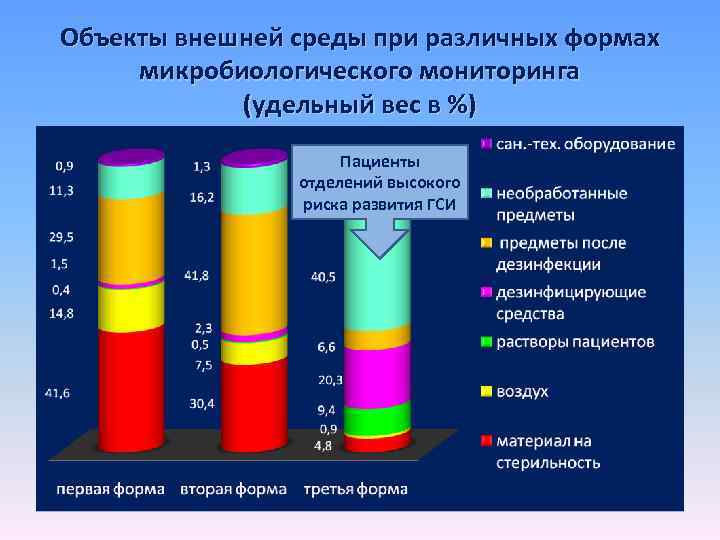 Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %) Пациенты отделений высокого риска развития ГСИ
Объекты внешней среды при различных формах микробиологического мониторинга (удельный вес в %) Пациенты отделений высокого риска развития ГСИ
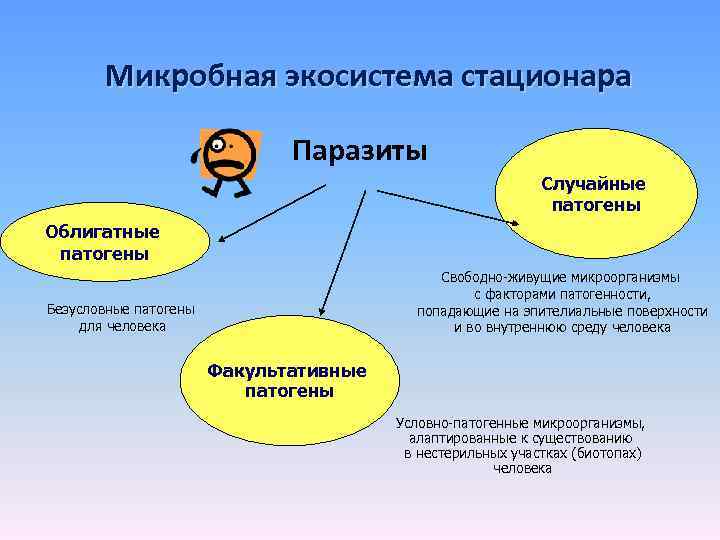 Микробная экосистема стационара Паразиты Случайные патогены Облигатные патогены Свободно-живущие микроорганизмы с факторами патогенности, попадающие на эпителиальные поверхности и во внутреннюю среду человека Безусловные патогены для человека Факультативные патогены Условно-патогенные микроорганизмы, алаптированные к существованию в нестерильных участках (биотопах) человека
Микробная экосистема стационара Паразиты Случайные патогены Облигатные патогены Свободно-живущие микроорганизмы с факторами патогенности, попадающие на эпителиальные поверхности и во внутреннюю среду человека Безусловные патогены для человека Факультативные патогены Условно-патогенные микроорганизмы, алаптированные к существованию в нестерильных участках (биотопах) человека
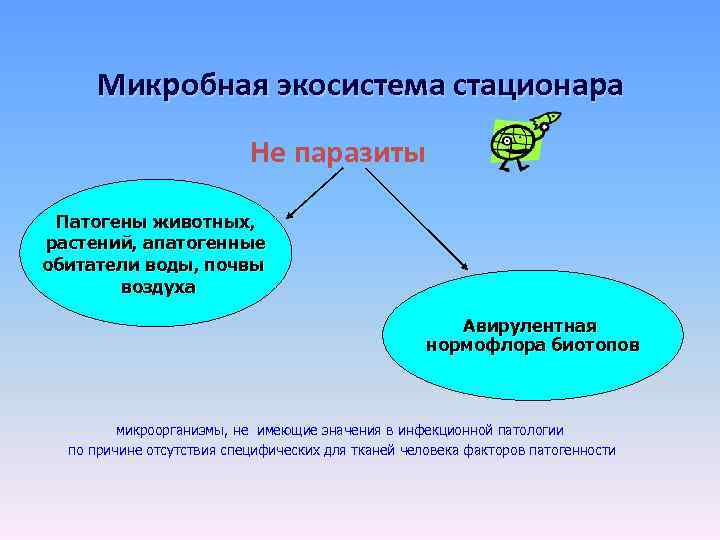 Микробная экосистема стационара Не паразиты Патогены животных, растений, апатогенные обитатели воды, почвы воздуха Авирулентная нормофлора биотопов микроорганизмы, не имеющие значения в инфекционной патологии по причине отсутствия специфических для тканей человека факторов патогенности
Микробная экосистема стационара Не паразиты Патогены животных, растений, апатогенные обитатели воды, почвы воздуха Авирулентная нормофлора биотопов микроорганизмы, не имеющие значения в инфекционной патологии по причине отсутствия специфических для тканей человека факторов патогенности
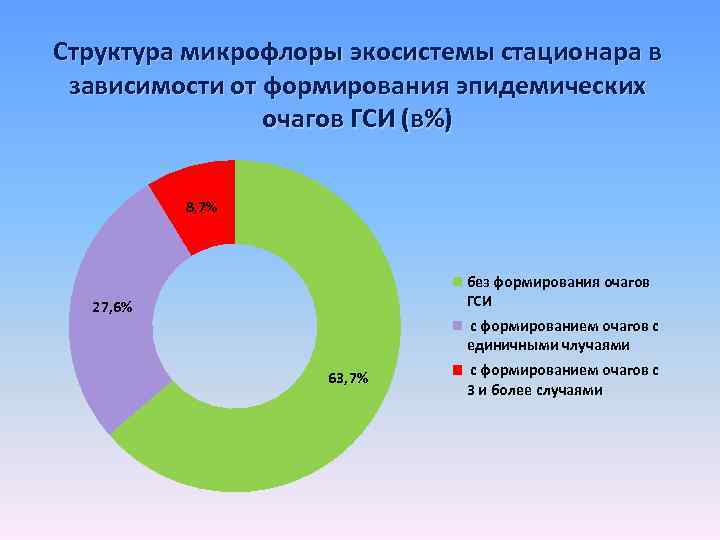 Структура микрофлоры экосистемы стационара в зависимости от формирования эпидемических очагов ГСИ (в%) 8, 7% без формирования очагов ГСИ 27, 6% с формированием очагов с единичными члучаями 63, 7% с формированием очагов с 3 и более случаями
Структура микрофлоры экосистемы стационара в зависимости от формирования эпидемических очагов ГСИ (в%) 8, 7% без формирования очагов ГСИ 27, 6% с формированием очагов с единичными члучаями 63, 7% с формированием очагов с 3 и более случаями
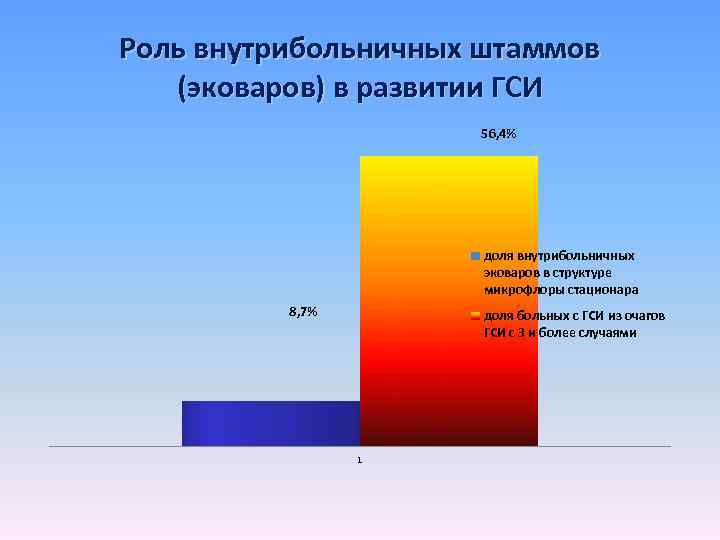 Роль внутрибольничных штаммов (эковаров) в развитии ГСИ 56, 4% доля внутрибольничных эковаров в структуре микрофлоры стационара 8, 7% доля больных с ГСИ из очагов ГСИ с 3 и более случаями 1
Роль внутрибольничных штаммов (эковаров) в развитии ГСИ 56, 4% доля внутрибольничных эковаров в структуре микрофлоры стационара 8, 7% доля больных с ГСИ из очагов ГСИ с 3 и более случаями 1
 Работа выполнена на клинических базах 6 ведущих многопрофильных ЛПУ Пермского края (2005 -2007 г. г. ) • • • Краевой хирургический центр Городской хирургический стационар Краевой родильный дом Межрайонный перинатальный центр Городская соматическая больница Межрайонная детская больница
Работа выполнена на клинических базах 6 ведущих многопрофильных ЛПУ Пермского края (2005 -2007 г. г. ) • • • Краевой хирургический центр Городской хирургический стационар Краевой родильный дом Межрайонный перинатальный центр Городская соматическая больница Межрайонная детская больница
 Структура изучаемых подразделений ЛПУ • • 6 ОРИТ 2 отделения гнойной хирургии 1 послеродовое отделение «мать-дитя» 1 отделение патологии беременных 1 отделение обсервации 1 отделение патологии новорожденных 1 отделение детской ортопедии и травматологии 1 педиатрическое отделение Всего: 14 отделений (эпидемические очаги с множественными случаями ГСИ)
Структура изучаемых подразделений ЛПУ • • 6 ОРИТ 2 отделения гнойной хирургии 1 послеродовое отделение «мать-дитя» 1 отделение патологии беременных 1 отделение обсервации 1 отделение патологии новорожденных 1 отделение детской ортопедии и травматологии 1 педиатрическое отделение Всего: 14 отделений (эпидемические очаги с множественными случаями ГСИ)
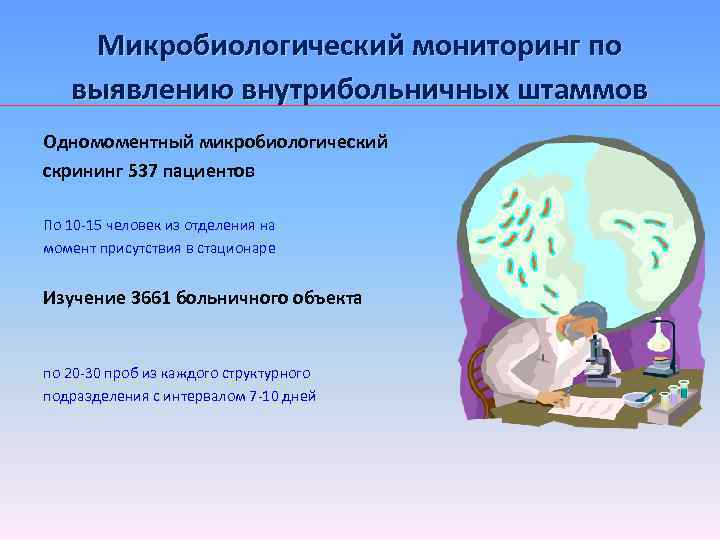 Микробиологический мониторинг по выявлению внутрибольничных штаммов Одномоментный микробиологический скрининг 537 пациентов По 10 -15 человек из отделения на момент присутствия в стационаре Изучение 3661 больничного объекта по 20 -30 проб из каждого структурного подразделения с интервалом 7 -10 дней
Микробиологический мониторинг по выявлению внутрибольничных штаммов Одномоментный микробиологический скрининг 537 пациентов По 10 -15 человек из отделения на момент присутствия в стационаре Изучение 3661 больничного объекта по 20 -30 проб из каждого структурного подразделения с интервалом 7 -10 дней
 Объекты внешней среды • • • 1131 материалов на стерильность 337 проб воздуха 1009 смывов с обработанных поверхностей 595 смывов с необработанных объектов 127 смывов с санитарно-технического оборудования 162 рабочих растворов дезинфектантов, используемых в отделениях Всего: 3361 проба
Объекты внешней среды • • • 1131 материалов на стерильность 337 проб воздуха 1009 смывов с обработанных поверхностей 595 смывов с необработанных объектов 127 смывов с санитарно-технического оборудования 162 рабочих растворов дезинфектантов, используемых в отделениях Всего: 3361 проба
 Биологические материалы от пациентов: • • • одномоментное исследование биоматериалов от 10 -15 человек Вагинальные мазки Содержимое пупочной ранки Раневые секреты Моча Трахеальные аспираты Мокрота Всего: 537 проб
Биологические материалы от пациентов: • • • одномоментное исследование биоматериалов от 10 -15 человек Вагинальные мазки Содержимое пупочной ранки Раневые секреты Моча Трахеальные аспираты Мокрота Всего: 537 проб
 Научная база исследований Централизованная микробиологическая лаборатория г. Соликамска
Научная база исследований Централизованная микробиологическая лаборатория г. Соликамска
 Изучение микроорганизмов с целью доказательства идентичности их свойств с определением: • Видовой принадлежности, согласно классическим и усовершенствованным методикам (патенты Рф № 2006123181/15(02154), № 2006123870/15(025900), 2006123869/15(025899), № 2006123148/20(025121) • Факторов патогенности (выявление у энтеробактерий и неферментирующих бактерий капсулы, адгезивной • Антибиотикочувствительности (диско-диффузионным методом – по диаметрам зон задержки роста и • Чувствительности к дезинфицирующим средствам (в микропланшетах, согласно МУ по • Продукции -лактамаз (двойных дисков, Е-теста, нитроцефинового теста), включая метод ПЦР диагностики (детекция генов TEM, SHV, CTX, OXA и MBL у 45 штаммов P. aeruginosa) • Чувствительности кпрепаратам бактериофагов (моновалентные и поливалентные активности, тиолзависимого и α-гемолитического гемолизина, слизеобразования. У стафилококков – лецитиназной активности, ДНК-азы, интерфероновой и антилизоцимной активности. У энтерококков и коринобактерий- гемолитической активности и т. д. ) методом серийных разведений – с определением МПК в плотной и жидкой среде Мюллера-Хинтона с помощью аппарата Densi -La-Meter II «Lachema» , диспенсера дисков Hi. Disc Dispenser Marc III «Hi. Media» с антибиотиками производства «Hi. Media» и НИЦФ, не менее, чем к 12 препаратов из профильных групп) ускоренному определению устойчивости бактерий к дезинфекционным средствам № 1100 -26 -0 -117 от 10. 01. 2000 г. ) бактериофаги производства НПО «Биомед» г. Пермь)
Изучение микроорганизмов с целью доказательства идентичности их свойств с определением: • Видовой принадлежности, согласно классическим и усовершенствованным методикам (патенты Рф № 2006123181/15(02154), № 2006123870/15(025900), 2006123869/15(025899), № 2006123148/20(025121) • Факторов патогенности (выявление у энтеробактерий и неферментирующих бактерий капсулы, адгезивной • Антибиотикочувствительности (диско-диффузионным методом – по диаметрам зон задержки роста и • Чувствительности к дезинфицирующим средствам (в микропланшетах, согласно МУ по • Продукции -лактамаз (двойных дисков, Е-теста, нитроцефинового теста), включая метод ПЦР диагностики (детекция генов TEM, SHV, CTX, OXA и MBL у 45 штаммов P. aeruginosa) • Чувствительности кпрепаратам бактериофагов (моновалентные и поливалентные активности, тиолзависимого и α-гемолитического гемолизина, слизеобразования. У стафилококков – лецитиназной активности, ДНК-азы, интерфероновой и антилизоцимной активности. У энтерококков и коринобактерий- гемолитической активности и т. д. ) методом серийных разведений – с определением МПК в плотной и жидкой среде Мюллера-Хинтона с помощью аппарата Densi -La-Meter II «Lachema» , диспенсера дисков Hi. Disc Dispenser Marc III «Hi. Media» с антибиотиками производства «Hi. Media» и НИЦФ, не менее, чем к 12 препаратов из профильных групп) ускоренному определению устойчивости бактерий к дезинфекционным средствам № 1100 -26 -0 -117 от 10. 01. 2000 г. ) бактериофаги производства НПО «Биомед» г. Пермь)

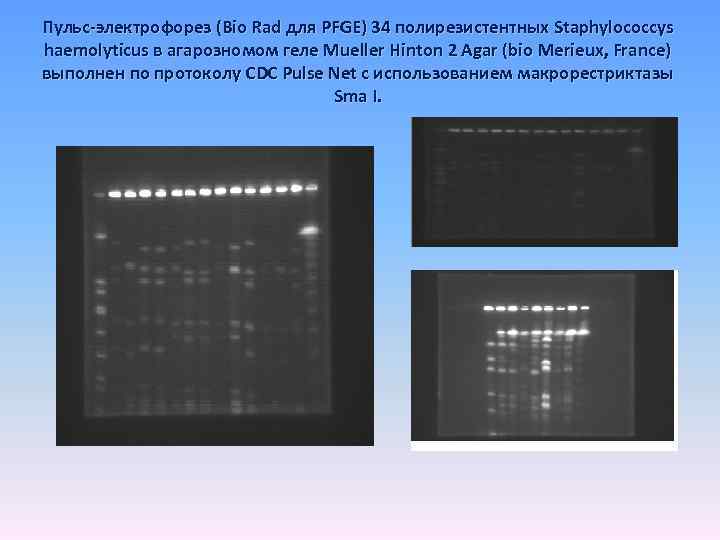 Пульс-электрофорез (Bio Rad для PFGE) 34 полирезистентных Staphylococcys haemolyticus в агарозномом геле Mueller Hinton 2 Agar (bio Merieux, France) выполнен по протоколу CDC Pulse Net с использованием макрорестриктазы Sma Ι.
Пульс-электрофорез (Bio Rad для PFGE) 34 полирезистентных Staphylococcys haemolyticus в агарозномом геле Mueller Hinton 2 Agar (bio Merieux, France) выполнен по протоколу CDC Pulse Net с использованием макрорестриктазы Sma Ι.
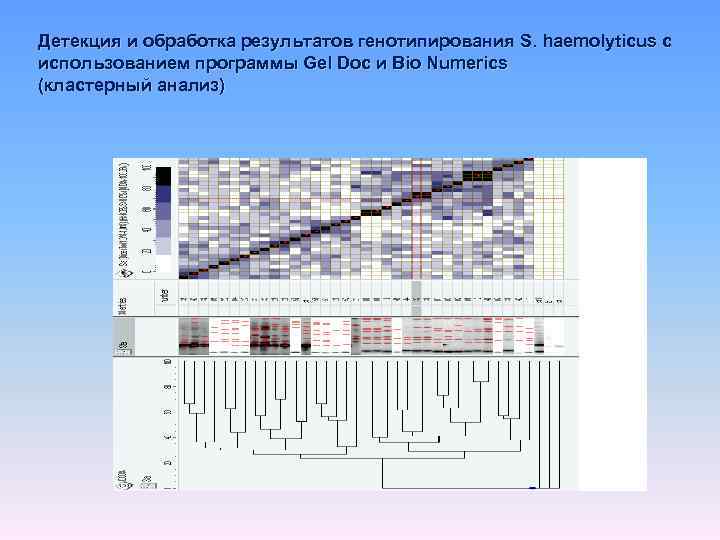 Детекция и обработка результатов генотипирования S. haemolyticus с использованием программы Gel Doc и Bio Numerics (кластерный анализ)
Детекция и обработка результатов генотипирования S. haemolyticus с использованием программы Gel Doc и Bio Numerics (кластерный анализ)
 Уровень микробной колонизации пациентов и контаминации объектов внешней среды стационаров Всего: 1452 штамма – представителей 355 биологических вариантов, из них 712 внутрибольничных эковара – 31 вариант
Уровень микробной колонизации пациентов и контаминации объектов внешней среды стационаров Всего: 1452 штамма – представителей 355 биологических вариантов, из них 712 внутрибольничных эковара – 31 вариант
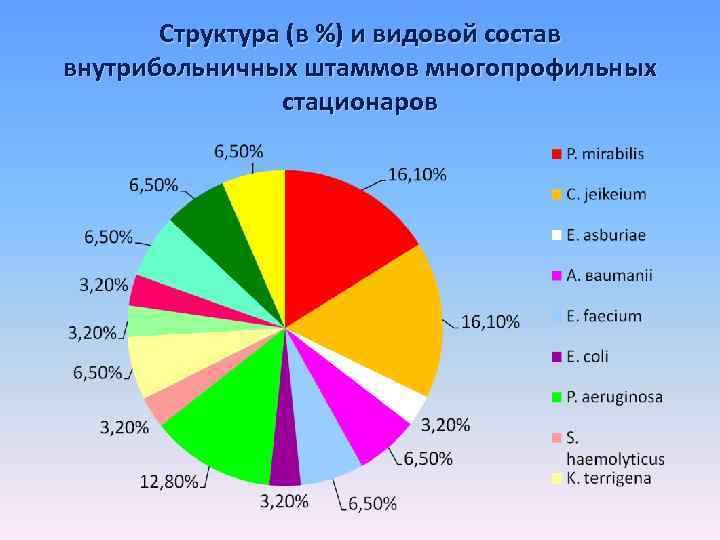 Структура (в %) и видовой состав внутрибольничных штаммов многопрофильных стационаров
Структура (в %) и видовой состав внутрибольничных штаммов многопрофильных стационаров
 ПЕРИНАТАЛЬНЫЙ ЦЕНТР 6 – E. asburiae (серый) ОТДЕЛЕНИЕ ПАТОЛОГИИ БЕРЕМЕННЫХ 5 – K. terrigena (голубой) 4 – S. aureus (красный) 3 - MRSE (желтый) 2 – E. faecalis (зеленый) 1 – E. coli (синий) Внешняя среда
ПЕРИНАТАЛЬНЫЙ ЦЕНТР 6 – E. asburiae (серый) ОТДЕЛЕНИЕ ПАТОЛОГИИ БЕРЕМЕННЫХ 5 – K. terrigena (голубой) 4 – S. aureus (красный) 3 - MRSE (желтый) 2 – E. faecalis (зеленый) 1 – E. coli (синий) Внешняя среда
 6 – E. asburiae (серый) ПЕРИНАТАЛЬНЫЙ ЦЕНТР 5 – K. terrigena (голубой) 4 – S. aureus (красный) ОТДЕЛЕНИЕ ФИЗИОЛОГИИ мать-дитя 3 - MRSE (желтый) 2 – E. faecalis (зеленый) 1 – E. coli (синий) Внешняя среда
6 – E. asburiae (серый) ПЕРИНАТАЛЬНЫЙ ЦЕНТР 5 – K. terrigena (голубой) 4 – S. aureus (красный) ОТДЕЛЕНИЕ ФИЗИОЛОГИИ мать-дитя 3 - MRSE (желтый) 2 – E. faecalis (зеленый) 1 – E. coli (синий) Внешняя среда
 ПЕРИНАТАЛЬНЫЙ ЦЕНТР 6 – E. asburiae (серый) ПАЛАТА ИНТЕНСИВНОЙ ТЕРАПИИ НОВОРОЖДЕННЫХ 5 – K. terrigena (голубой) 4 – S. aureus (красный) 3 - MRSE (желтый) 2 – P. aeruginosa (зеленый) 1 – E. coli (синий) Внешняя среда
ПЕРИНАТАЛЬНЫЙ ЦЕНТР 6 – E. asburiae (серый) ПАЛАТА ИНТЕНСИВНОЙ ТЕРАПИИ НОВОРОЖДЕННЫХ 5 – K. terrigena (голубой) 4 – S. aureus (красный) 3 - MRSE (желтый) 2 – P. aeruginosa (зеленый) 1 – E. coli (синий) Внешняя среда
 КАРЕВОЙ РОДИЛЬНЫЙ ДОМ ПАЛАТА ИНТЕНСИВНОЙ ТЕРАПИИ НОВОРОЖДЕННЫХ 5 – E. coli (зеленый) 4 – E. faecium (голубой) 3 – S. haemolyticus (сиреневый) 2 – C. jeikeium (черный) 1 – E. faecalis (оранжевый) Внешняя среда
КАРЕВОЙ РОДИЛЬНЫЙ ДОМ ПАЛАТА ИНТЕНСИВНОЙ ТЕРАПИИ НОВОРОЖДЕННЫХ 5 – E. coli (зеленый) 4 – E. faecium (голубой) 3 – S. haemolyticus (сиреневый) 2 – C. jeikeium (черный) 1 – E. faecalis (оранжевый) Внешняя среда
 КАРЕВОЙ РОДИЛЬНЫЙ ДОМ ОРИТ БЕРЕМЕННЫХ И РОДИЛЬНИЦ 5 – E. coli (зеленый) 4 – E. faecium (голубой) 3 – S. haemolyticus (сиреневый) 2 – C. jeikeium (черный) 1 – E. faecalis (оранжевый) Внешняя среда
КАРЕВОЙ РОДИЛЬНЫЙ ДОМ ОРИТ БЕРЕМЕННЫХ И РОДИЛЬНИЦ 5 – E. coli (зеленый) 4 – E. faecium (голубой) 3 – S. haemolyticus (сиреневый) 2 – C. jeikeium (черный) 1 – E. faecalis (оранжевый) Внешняя среда
 ДЕТСКАЯ БОЛЬНИЦА ОРИТ 3 – S. haemolyticus (розовый) 2 – P. aeruginosa (синий) 1 – E. faecium (зеленый) Внешняя среда
ДЕТСКАЯ БОЛЬНИЦА ОРИТ 3 – S. haemolyticus (розовый) 2 – P. aeruginosa (синий) 1 – E. faecium (зеленый) Внешняя среда
 СОМАТИЧЕСКАЯ ГОРОДСКАЯ БОЛЬНИЦА 2 – Р. mirabilis (желтый) 1 – A. baumanii (синий) ОРИТ Внешняя среда
СОМАТИЧЕСКАЯ ГОРОДСКАЯ БОЛЬНИЦА 2 – Р. mirabilis (желтый) 1 – A. baumanii (синий) ОРИТ Внешняя среда
 ГОРОДСКОЙ ХИРУРГИЧЕСКИЙ СТАЦИОНАР 3 – S. haemolyticus (сиреневый) ОРИТ 2 – A. baumanii (синий) 1 – S. maltophilia (голубой) Внешняя среда
ГОРОДСКОЙ ХИРУРГИЧЕСКИЙ СТАЦИОНАР 3 – S. haemolyticus (сиреневый) ОРИТ 2 – A. baumanii (синий) 1 – S. maltophilia (голубой) Внешняя среда
 ГОРОДСКОЙ ХИРУРГИЧЕСКИЙ СТАЦИОНАР 4– S. aureus (красный) 3 – E. faecium (зеленый) ОТДЕЛЕНИЕ ГНОЙНОЙ ХИРУРГИИ 2 – S. haemolyticus (сиреневый) 1 – P. aeruginosa (голубой) Внешняя среда
ГОРОДСКОЙ ХИРУРГИЧЕСКИЙ СТАЦИОНАР 4– S. aureus (красный) 3 – E. faecium (зеленый) ОТДЕЛЕНИЕ ГНОЙНОЙ ХИРУРГИИ 2 – S. haemolyticus (сиреневый) 1 – P. aeruginosa (голубой) Внешняя среда
 Уровень контаминации госпитальными штаммами объектов внешней среды стационаров 37, 4% 0, 5% 36, 5% 12, 3% 0, 6% 18, 1% 15, 4% 1, 6%
Уровень контаминации госпитальными штаммами объектов внешней среды стационаров 37, 4% 0, 5% 36, 5% 12, 3% 0, 6% 18, 1% 15, 4% 1, 6%
 Критерии формирования групп «случай» - «контроль» при разработке эпидемиологического стандартного определения внутрибольничного штамма «случай» Сопоставимые фенотипы, участвующие в формировании очагов ГСИ с множественными случаями (5 и более) – групповая заболеваемость (31 фенотип) «контроль» Сопоставимые фенотипы, участвующие в формировании очагов ГСИ с единичными случаями и выделенные из биологических материалов от пациентов при поступлении в стационар (98 фенотипов)
Критерии формирования групп «случай» - «контроль» при разработке эпидемиологического стандартного определения внутрибольничного штамма «случай» Сопоставимые фенотипы, участвующие в формировании очагов ГСИ с множественными случаями (5 и более) – групповая заболеваемость (31 фенотип) «контроль» Сопоставимые фенотипы, участвующие в формировании очагов ГСИ с единичными случаями и выделенные из биологических материалов от пациентов при поступлении в стационар (98 фенотипов)
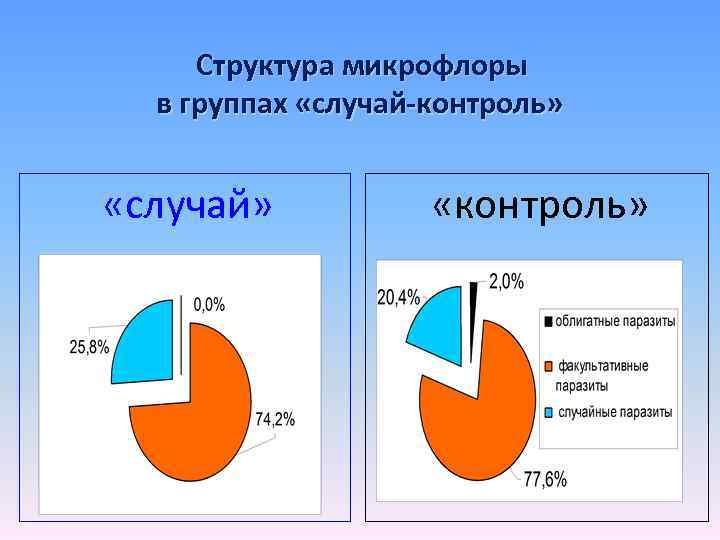 Структура микрофлоры в группах «случай-контроль» «случай» «контроль»
Структура микрофлоры в группах «случай-контроль» «случай» «контроль»
 Стандартное эпидемиологическое определение внутрибольничного штамма проведено с расчетом: 1. Чувствительности исследуемого теста 2. Специфичности исследуемого теста Согласно методике ВОЗ и данным Л. П. Зуевой (Эпидемиологическая диагностика / Л. П. Зуева, Р. Х. Яфаев, С. Р. Еремин. – СПб, 2003. – 265 с. )
Стандартное эпидемиологическое определение внутрибольничного штамма проведено с расчетом: 1. Чувствительности исследуемого теста 2. Специфичности исследуемого теста Согласно методике ВОЗ и данным Л. П. Зуевой (Эпидемиологическая диагностика / Л. П. Зуева, Р. Х. Яфаев, С. Р. Еремин. – СПб, 2003. – 265 с. )
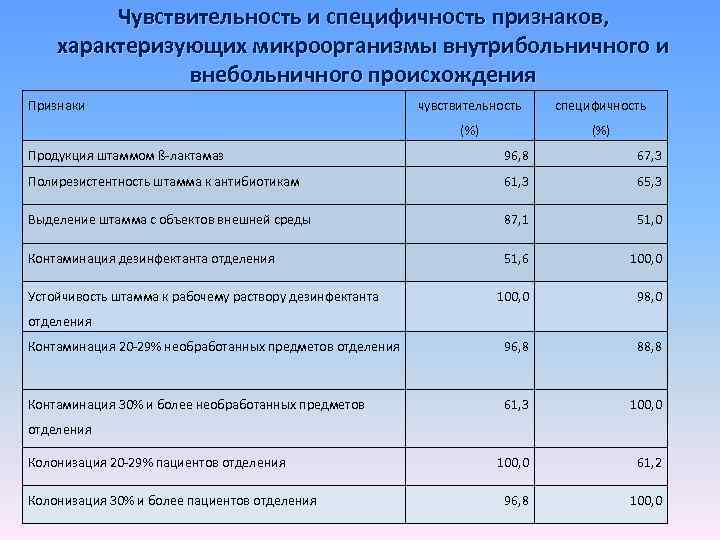 Чувствительность и специфичность признаков, характеризующих микроорганизмы внутрибольничного и внебольничного происхождения Признаки чувствительность специфичность (%) Продукция штаммом ß-лактамаз 96, 8 67, 3 Полирезистентность штамма к антибиотикам 61, 3 65, 3 Выделение штамма с объектов внешней среды 87, 1 51, 0 Контаминация дезинфектанта отделения 51, 6 100, 0 98, 0 Контаминация 20 -29% необработанных предметов отделения 96, 8 88, 8 Контаминация 30% и более необработанных предметов 61, 3 100, 0 61, 2 96, 8 100, 0 Устойчивость штамма к рабочему раствору дезинфектанта отделения Колонизация 20 -29% пациентов отделения Колонизация 30% и более пациентов отделения
Чувствительность и специфичность признаков, характеризующих микроорганизмы внутрибольничного и внебольничного происхождения Признаки чувствительность специфичность (%) Продукция штаммом ß-лактамаз 96, 8 67, 3 Полирезистентность штамма к антибиотикам 61, 3 65, 3 Выделение штамма с объектов внешней среды 87, 1 51, 0 Контаминация дезинфектанта отделения 51, 6 100, 0 98, 0 Контаминация 20 -29% необработанных предметов отделения 96, 8 88, 8 Контаминация 30% и более необработанных предметов 61, 3 100, 0 61, 2 96, 8 100, 0 Устойчивость штамма к рабочему раствору дезинфектанта отделения Колонизация 20 -29% пациентов отделения Колонизация 30% и более пациентов отделения
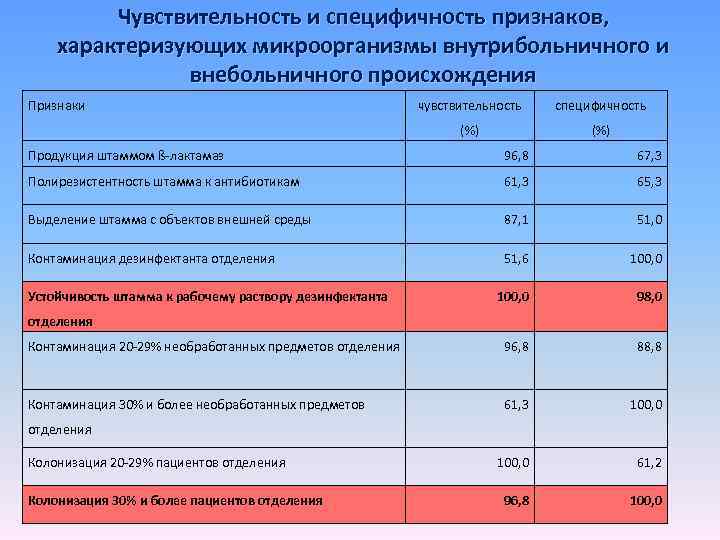 Чувствительность и специфичность признаков, характеризующих микроорганизмы внутрибольничного и внебольничного происхождения Признаки чувствительность специфичность (%) Продукция штаммом ß-лактамаз 96, 8 67, 3 Полирезистентность штамма к антибиотикам 61, 3 65, 3 Выделение штамма с объектов внешней среды 87, 1 51, 0 Контаминация дезинфектанта отделения 51, 6 100, 0 98, 0 Контаминация 20 -29% необработанных предметов отделения 96, 8 88, 8 Контаминация 30% и более необработанных предметов 61, 3 100, 0 61, 2 96, 8 100, 0 Устойчивость штамма к рабочему раствору дезинфектанта отделения Колонизация 20 -29% пациентов отделения Колонизация 30% и более пациентов отделения
Чувствительность и специфичность признаков, характеризующих микроорганизмы внутрибольничного и внебольничного происхождения Признаки чувствительность специфичность (%) Продукция штаммом ß-лактамаз 96, 8 67, 3 Полирезистентность штамма к антибиотикам 61, 3 65, 3 Выделение штамма с объектов внешней среды 87, 1 51, 0 Контаминация дезинфектанта отделения 51, 6 100, 0 98, 0 Контаминация 20 -29% необработанных предметов отделения 96, 8 88, 8 Контаминация 30% и более необработанных предметов 61, 3 100, 0 61, 2 96, 8 100, 0 Устойчивость штамма к рабочему раствору дезинфектанта отделения Колонизация 20 -29% пациентов отделения Колонизация 30% и более пациентов отделения
 Стандартное эпидемиологическое определение внутрибольничного штамма Внутрибольничный штамм структурного подразделения ЛПУ : • являлется представителем микрофлоры с выраженными природными или приобретенными патогенными (вирулентными) свойствами, определяющими развитие групповых инфекционных заболеваний среди пациентов (3 и более случая) • колонизирует 30% и более пациентов отделения • проявляет устойчивость к рабочему раствору дезинфицирующего средства, используемого в подразделении
Стандартное эпидемиологическое определение внутрибольничного штамма Внутрибольничный штамм структурного подразделения ЛПУ : • являлется представителем микрофлоры с выраженными природными или приобретенными патогенными (вирулентными) свойствами, определяющими развитие групповых инфекционных заболеваний среди пациентов (3 и более случая) • колонизирует 30% и более пациентов отделения • проявляет устойчивость к рабочему раствору дезинфицирующего средства, используемого в подразделении
 ОРГАНИЗАЦИЯ МИКРОБИОЛОГИЧЕСКОГО МОНИТОРИНГА В МЕДИЦИНСКОМ УЧРЕЖДЕНИИ НА ОСНОВЕ СТАНДАРТНОГО ЭПИДЕМИОЛОГИЧЕСКОГО ОПРЕДЕЛЕНИЯ ВНУТРИБОЛЬНИЧНОГО ШТАММА (ЭКОВАРА)
ОРГАНИЗАЦИЯ МИКРОБИОЛОГИЧЕСКОГО МОНИТОРИНГА В МЕДИЦИНСКОМ УЧРЕЖДЕНИИ НА ОСНОВЕ СТАНДАРТНОГО ЭПИДЕМИОЛОГИЧЕСКОГО ОПРЕДЕЛЕНИЯ ВНУТРИБОЛЬНИЧНОГО ШТАММА (ЭКОВАРА)
 Микробиологический мониторинг в плановом порядке Микробиологический мониторинг пациентов Плановый контроль объектов внешней среды осуществляется с целью выявления предвестников и предпосылок эпидемического неблагополучия Обязательному бактериологическому обследованию подлежат: • Больные с признаками гнойно-септических инфекций (по клиническим показаниям) Забор материала проводит медицинский персонал отделения стационара по направлениям лечащих врачей • Пациенты отделений (палат) реанимации и интенсивной терапии и пациенты отделений высокого риска развития ГСИ Забор материала производит персонал отделения независимо от клинических показаний спустя 48 часов после поступления пациента в отделение Учитывают только вирулентные штаммы микроорганизмов с природными или приобретенными факторами патогенности
Микробиологический мониторинг в плановом порядке Микробиологический мониторинг пациентов Плановый контроль объектов внешней среды осуществляется с целью выявления предвестников и предпосылок эпидемического неблагополучия Обязательному бактериологическому обследованию подлежат: • Больные с признаками гнойно-септических инфекций (по клиническим показаниям) Забор материала проводит медицинский персонал отделения стационара по направлениям лечащих врачей • Пациенты отделений (палат) реанимации и интенсивной терапии и пациенты отделений высокого риска развития ГСИ Забор материала производит персонал отделения независимо от клинических показаний спустя 48 часов после поступления пациента в отделение Учитывают только вирулентные штаммы микроорганизмов с природными или приобретенными факторами патогенности
 Микробиологический мониторинг в плановом порядке Микробиологический мониторинг внешней среды Плановый контроль объектов внешней среды осуществляется с целью выявления предвестников и предпосылок эпидемического неблагополучия Перечень объектов внешней среды: • • Изделия общего и специального медицинского назначения (инструменты, функциональные системы) Руки персонала Принадлежности персонала (перчатки, полотенца, фартуки, халаты, маски и т. д. ) Предметы, тесно контактирующие с больными (судна, мочеприемники, клеенки, кушетки, манипуляционные столы, кювезы, кровати, постельное белье, полотенца, перевязочный материал, расходные материалы, предметы гигиены, посуда, медицинские отходы и т. д. ) Растворы для питья и обработки пациентов Санитарно-техническое оборудование и уборочный инвентарь Дезинфицирующие средства (рабочие растворы, места и емкости для их приготовления и хранения, замоченный в растворах дезинфицируемый инвентарь) Забор материала производит персонал микробиологических лабораторий под контролем госпитального эпидемиолога или старшей медицинской сестры в обычном режиме работы подразделения Учету подлежат вирулентные штаммы микроорганизмов с природными или приобретенными факторами патогенности
Микробиологический мониторинг в плановом порядке Микробиологический мониторинг внешней среды Плановый контроль объектов внешней среды осуществляется с целью выявления предвестников и предпосылок эпидемического неблагополучия Перечень объектов внешней среды: • • Изделия общего и специального медицинского назначения (инструменты, функциональные системы) Руки персонала Принадлежности персонала (перчатки, полотенца, фартуки, халаты, маски и т. д. ) Предметы, тесно контактирующие с больными (судна, мочеприемники, клеенки, кушетки, манипуляционные столы, кювезы, кровати, постельное белье, полотенца, перевязочный материал, расходные материалы, предметы гигиены, посуда, медицинские отходы и т. д. ) Растворы для питья и обработки пациентов Санитарно-техническое оборудование и уборочный инвентарь Дезинфицирующие средства (рабочие растворы, места и емкости для их приготовления и хранения, замоченный в растворах дезинфицируемый инвентарь) Забор материала производит персонал микробиологических лабораторий под контролем госпитального эпидемиолога или старшей медицинской сестры в обычном режиме работы подразделения Учету подлежат вирулентные штаммы микроорганизмов с природными или приобретенными факторами патогенности
 Структура больничных объектов контаминированных госпитальными штаммами
Структура больничных объектов контаминированных госпитальными штаммами
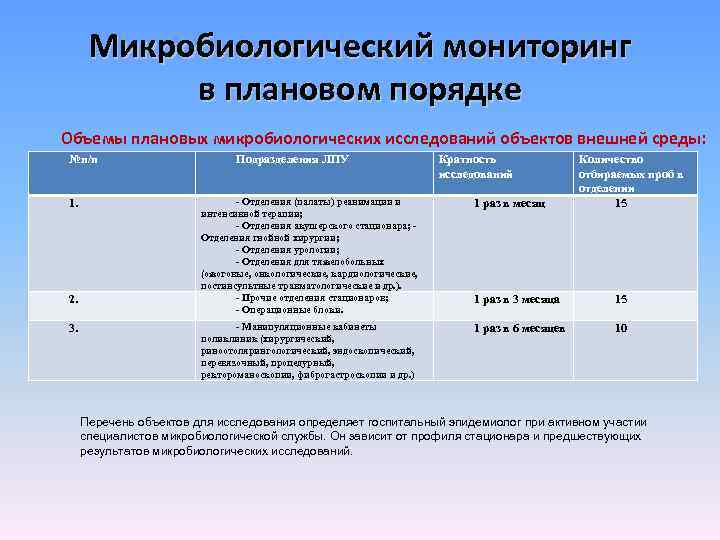 Микробиологический мониторинг в плановом порядке Объемы плановых микробиологических исследований объектов внешней среды: №п/п 1. 2. 3. Подразделения ЛПУ Кратность исследований Количество отбираемых проб в отделении 15 - Отделения (палаты) реанимации и интенсивной терапии; - Отделения акушерского стационара; Отделения гнойной хирургии; - Отделения урологии; - Отделения для тяжелобольных (ожоговые, онкологические, кардиологические, постинсультные травматологические и др. ). - Прочие отделения стационаров; - Операционные блоки. 1 раз в месяц 1 раз в 3 месяца 15 - Манипуляционные кабинеты поликлиник (хирургический, риноотолярингологический, эндоскопический, перевязочный, процедурный, ректороманоскопии, фиброгастроскопии и др. ) 1 раз в 6 месяцев 10 Перечень объектов для исследования определяет госпитальный эпидемиолог при активном участии специалистов микробиологической службы. Он зависит от профиля стационара и предшествующих результатов микробиологических исследований.
Микробиологический мониторинг в плановом порядке Объемы плановых микробиологических исследований объектов внешней среды: №п/п 1. 2. 3. Подразделения ЛПУ Кратность исследований Количество отбираемых проб в отделении 15 - Отделения (палаты) реанимации и интенсивной терапии; - Отделения акушерского стационара; Отделения гнойной хирургии; - Отделения урологии; - Отделения для тяжелобольных (ожоговые, онкологические, кардиологические, постинсультные травматологические и др. ). - Прочие отделения стационаров; - Операционные блоки. 1 раз в месяц 1 раз в 3 месяца 15 - Манипуляционные кабинеты поликлиник (хирургический, риноотолярингологический, эндоскопический, перевязочный, процедурный, ректороманоскопии, фиброгастроскопии и др. ) 1 раз в 6 месяцев 10 Перечень объектов для исследования определяет госпитальный эпидемиолог при активном участии специалистов микробиологической службы. Он зависит от профиля стационара и предшествующих результатов микробиологических исследований.
 Микробиологический мониторинг в плановом порядке Объемы плановых микробиологических исследований воздушной среды Объектами, подлежащими исследованию являются особо чистые помещения класса А: • • • Операционные блоки Родильные залы Асептические боксы (для ожоговых, гематологических больных и пр. ) Палаты для недоношенных детей Стерилизационная (чистая половина) Боксы бактериологических лабораорий Проводится 1 раз в 3 месяца. Учет результатов осуществляется согласно санитарным нормам и правилам «Гигиенические требования к размещению, устройству, оборудованию и эксплуатации больниц, родильных домов и других лечебных стационаров» Сан. Пин № 2. 1. 3. 1375 -03.
Микробиологический мониторинг в плановом порядке Объемы плановых микробиологических исследований воздушной среды Объектами, подлежащими исследованию являются особо чистые помещения класса А: • • • Операционные блоки Родильные залы Асептические боксы (для ожоговых, гематологических больных и пр. ) Палаты для недоношенных детей Стерилизационная (чистая половина) Боксы бактериологических лабораорий Проводится 1 раз в 3 месяца. Учет результатов осуществляется согласно санитарным нормам и правилам «Гигиенические требования к размещению, устройству, оборудованию и эксплуатации больниц, родильных домов и других лечебных стационаров» Сан. Пин № 2. 1. 3. 1375 -03.
 Микробиологический мониторинг в плановом порядке Контроль стерилизации Объектами, подлежащими исследованию являются : • • Оборудование для паровой и суховоздушной стерилизации; Контроль стерилизации осуществляют с использованием бактериологических тестов (биотесты со спорами B. stearothermophilus – для паровых стерилизаторов, со спорами B. licheniformis – для сушильно-стерилизационных шкафов), согласно Методическим указаниям по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения МУ № 287 -113 МЗ РФ от 30. 12. 1998 г. [10], ГОСТ Стерилизаторы паровые большие. Общие технические требования и методы испытания. ГОСТ Р 51935 -202 (ЕН 285 -96). Лечебно-диагностическое оборудование, аппараты и комплектующие к ним после стерилизации другими методами; Контроль стерилизации осуществляют в соответствие с Методическими указаниями «Очистка, дезинфекция и стерилизация эндоскопов и инструментов к ним» МУ № 3. 5. 13704 от 3. 03. 2004 г. , Санитарными правилами «Профилактика инфекционных заболеваний при эндоскопических манипуляциях» СП 3. 1. 1275 -03 от 2. 04. 2003 г. , ГОСТ «Стерилизация медицинской продукции. Биологические индикаторы» ГОСТ ИСО 11138 -1 -2000.
Микробиологический мониторинг в плановом порядке Контроль стерилизации Объектами, подлежащими исследованию являются : • • Оборудование для паровой и суховоздушной стерилизации; Контроль стерилизации осуществляют с использованием бактериологических тестов (биотесты со спорами B. stearothermophilus – для паровых стерилизаторов, со спорами B. licheniformis – для сушильно-стерилизационных шкафов), согласно Методическим указаниям по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения МУ № 287 -113 МЗ РФ от 30. 12. 1998 г. [10], ГОСТ Стерилизаторы паровые большие. Общие технические требования и методы испытания. ГОСТ Р 51935 -202 (ЕН 285 -96). Лечебно-диагностическое оборудование, аппараты и комплектующие к ним после стерилизации другими методами; Контроль стерилизации осуществляют в соответствие с Методическими указаниями «Очистка, дезинфекция и стерилизация эндоскопов и инструментов к ним» МУ № 3. 5. 13704 от 3. 03. 2004 г. , Санитарными правилами «Профилактика инфекционных заболеваний при эндоскопических манипуляциях» СП 3. 1. 1275 -03 от 2. 04. 2003 г. , ГОСТ «Стерилизация медицинской продукции. Биологические индикаторы» ГОСТ ИСО 11138 -1 -2000.
 МЕТОДИКА МИКРОБИОЛОГИЧЕСКОГО ИССЛЕДОВАНИЯ БИОЛОГИЧЕСКИХ МАТЕРИАЛОВ ОТ ПАЦИЕНТОВ • Первичный посев и идентификация микроорганизмов проводится в соответствие с регламентирующими документами. Учету подлежат вирулентные штаммы микроорганизмов: ü Условно-патогенные виды с выраженными природными патогенными свойствами ü Условно-патогенные микроорганизмы с приобретенными факторами вирулентности (типичные представители нормофлоры человека, свободноживущие виды)
МЕТОДИКА МИКРОБИОЛОГИЧЕСКОГО ИССЛЕДОВАНИЯ БИОЛОГИЧЕСКИХ МАТЕРИАЛОВ ОТ ПАЦИЕНТОВ • Первичный посев и идентификация микроорганизмов проводится в соответствие с регламентирующими документами. Учету подлежат вирулентные штаммы микроорганизмов: ü Условно-патогенные виды с выраженными природными патогенными свойствами ü Условно-патогенные микроорганизмы с приобретенными факторами вирулентности (типичные представители нормофлоры человека, свободноживущие виды)
 Методика исследования микробной обсемененности объектов внешней среды Предусматривает выявление вирулентных видов микроорганизмов, представителей аэробной и факультативноанаэробной микрофлоры: 1 день исследования: • Забор материала методом смывов производят стерильными тампонами в пробирки с глюкозным бульоном (5 -10 мл) • Жидкие пробы отбирают в стерильную лабораторную посуду или одноразовые шприцы 2 день исследования: • Высев материалов из жидких сред на питательные среды для первичного выделения (5% кровяной агар, ЖСА, Эндо)
Методика исследования микробной обсемененности объектов внешней среды Предусматривает выявление вирулентных видов микроорганизмов, представителей аэробной и факультативноанаэробной микрофлоры: 1 день исследования: • Забор материала методом смывов производят стерильными тампонами в пробирки с глюкозным бульоном (5 -10 мл) • Жидкие пробы отбирают в стерильную лабораторную посуду или одноразовые шприцы 2 день исследования: • Высев материалов из жидких сред на питательные среды для первичного выделения (5% кровяной агар, ЖСА, Эндо)
 Методика исследования микробной обсемененности объектов внешней среды Предусматривает выявление вирулентных видов микроорганизмов, представителей аэробной и факультативноанаэробной микрофлоры: 3 день исследования: • Просмотр чашек с высевами, фиксация в журнале характера роста выросших колоний, оценка тинкториальных и морфологических свойств штаммов, постановка ориентировочных тестов по определению родовой принадлежности микроорганизмов, вирулентных свойств и продукции влактамаз
Методика исследования микробной обсемененности объектов внешней среды Предусматривает выявление вирулентных видов микроорганизмов, представителей аэробной и факультативноанаэробной микрофлоры: 3 день исследования: • Просмотр чашек с высевами, фиксация в журнале характера роста выросших колоний, оценка тинкториальных и морфологических свойств штаммов, постановка ориентировочных тестов по определению родовой принадлежности микроорганизмов, вирулентных свойств и продукции влактамаз
 Коагулазоотрицательные стафилококки: • Наличие лецитиназы • Пигментообразование • Продукция и гиперпродукция в-лактамаз ü оксациллинрезистентность ü полирезистентность
Коагулазоотрицательные стафилококки: • Наличие лецитиназы • Пигментообразование • Продукция и гиперпродукция в-лактамаз ü оксациллинрезистентность ü полирезистентность
 Энтерококки: • Гемолитическая активность • Продукция и гиперпродукция в-лактамаз ü сниженная чувствительность к ампициллину ü устойчивость к ванкомицину ü полирезистентность
Энтерококки: • Гемолитическая активность • Продукция и гиперпродукция в-лактамаз ü сниженная чувствительность к ампициллину ü устойчивость к ванкомицину ü полирезистентность
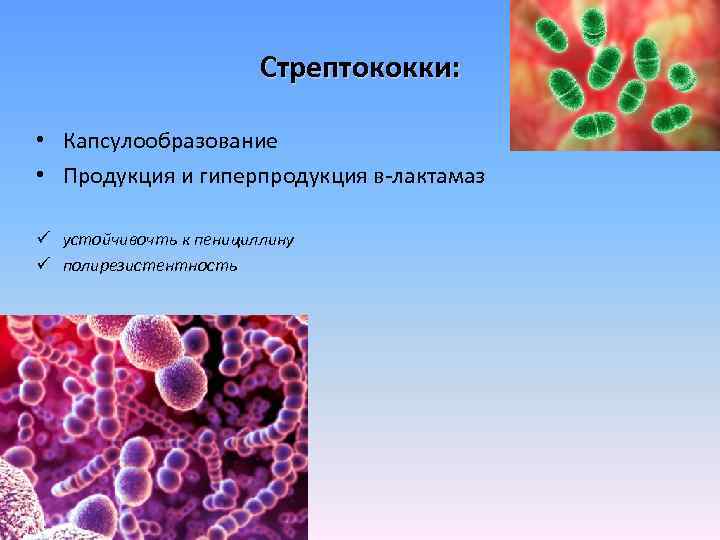 Стрептококки: • Капсулообразование • Продукция и гиперпродукция в-лактамаз ü устойчивочть к пенициллину ü полирезистентность
Стрептококки: • Капсулообразование • Продукция и гиперпродукция в-лактамаз ü устойчивочть к пенициллину ü полирезистентность
 Энтеробактерии: • • • Гемолитическая активность Капсулообразование Слизеобразование Отсутствие подвижности у подвижных видов Отсутствие лактозообразования у образующих Продукция и гиперпродукция в-лактамаз ü ü широкого спектра (устойчивочть к ампициллину) расширенного спектра (устойчивость к цефалоспоринам 3 поколения) полирезистентность (устойчивость к 5 и более профильным препаратам) панрезистентность (устойчивость ко всем тестируемым препаратам)
Энтеробактерии: • • • Гемолитическая активность Капсулообразование Слизеобразование Отсутствие подвижности у подвижных видов Отсутствие лактозообразования у образующих Продукция и гиперпродукция в-лактамаз ü ü широкого спектра (устойчивочть к ампициллину) расширенного спектра (устойчивость к цефалоспоринам 3 поколения) полирезистентность (устойчивость к 5 и более профильным препаратам) панрезистентность (устойчивость ко всем тестируемым препаратам)
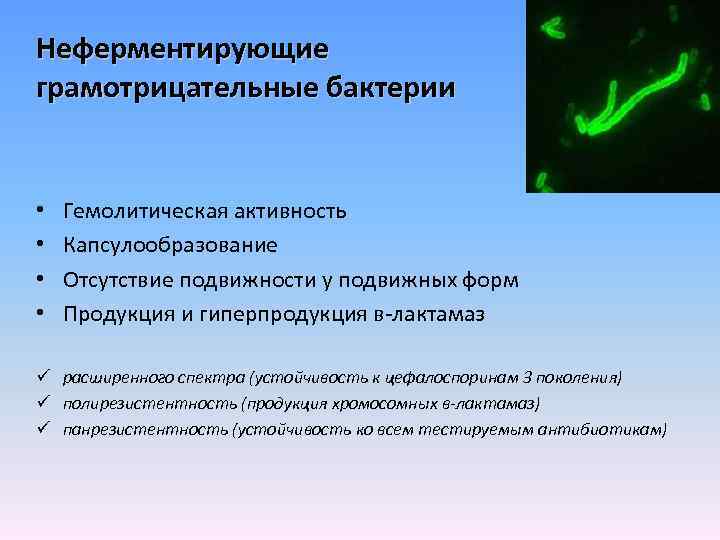 Неферментирующие грамотрицательные бактерии • • Гемолитическая активность Капсулообразование Отсутствие подвижности у подвижных форм Продукция и гиперпродукция в-лактамаз ü расширенного спектра (устойчивость к цефалоспоринам 3 поколения) ü полирезистентность (продукция хромосомных в-лактамаз) ü панрезистентность (устойчивость ко всем тестируемым антибиотикам)
Неферментирующие грамотрицательные бактерии • • Гемолитическая активность Капсулообразование Отсутствие подвижности у подвижных форм Продукция и гиперпродукция в-лактамаз ü расширенного спектра (устойчивость к цефалоспоринам 3 поколения) ü полирезистентность (продукция хромосомных в-лактамаз) ü панрезистентность (устойчивость ко всем тестируемым антибиотикам)
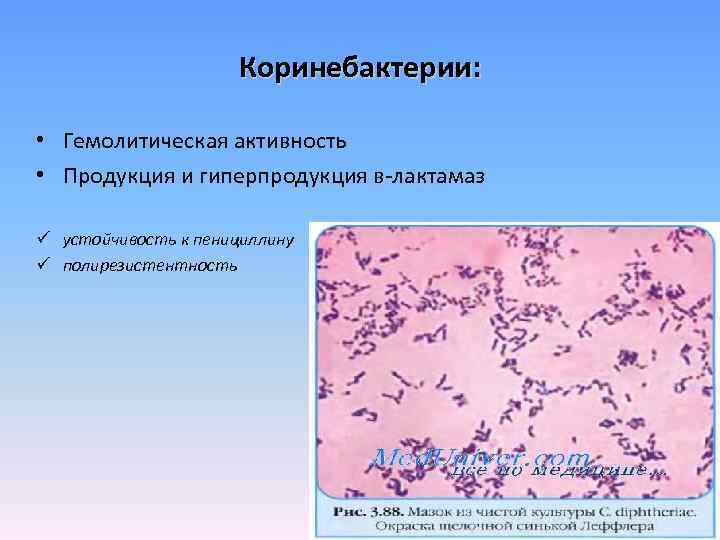 Коринебактерии: • Гемолитическая активность • Продукция и гиперпродукция в-лактамаз ü устойчивость к пенициллину ü полирезистентность
Коринебактерии: • Гемолитическая активность • Продукция и гиперпродукция в-лактамаз ü устойчивость к пенициллину ü полирезистентность
 Бациллы: • Гемолитическая активность • Наличие лецитиназы • Продукция и гиперпродукция в-лактамаз ü устойчивость к пенициллину ü полирезистентность
Бациллы: • Гемолитическая активность • Наличие лецитиназы • Продукция и гиперпродукция в-лактамаз ü устойчивость к пенициллину ü полирезистентность
 Грибы рода Candida: • • Гемолитическая активность Продукция фосфолипазы Устойчивость к нистатину Полирезистентность
Грибы рода Candida: • • Гемолитическая активность Продукция фосфолипазы Устойчивость к нистатину Полирезистентность
 Прочие микроорганизмы: Продукция в-лактамаз и других факторов патогенности (вирулентности)
Прочие микроорганизмы: Продукция в-лактамаз и других факторов патогенности (вирулентности)
 Методика исследования микробной обсемененности объектов внешней среды Предусматривает выявление ведущих биологических свойств у патогенных (вирулентных) видов микроорганизмов, представителей аэробной и факультативно-анаэробной микрофлоры: 4 -6 день исследования: • • • Постановка тестов по видовой идентификации микроорганизмов, антибиотикограммы фагограммы чувствительности к дезинфицирующим средствам внутривидовое типирование выписка результата
Методика исследования микробной обсемененности объектов внешней среды Предусматривает выявление ведущих биологических свойств у патогенных (вирулентных) видов микроорганизмов, представителей аэробной и факультативно-анаэробной микрофлоры: 4 -6 день исследования: • • • Постановка тестов по видовой идентификации микроорганизмов, антибиотикограммы фагограммы чувствительности к дезинфицирующим средствам внутривидовое типирование выписка результата
 Определение чувствительности внутрибольничных штаммов к дезинфицирующим средствам • Инструкция по определению бактерицидных свойств новых дезинфицирующих средств. - М: МЗ СССР, 1968 № 739 -68 • Методы испытаний дезинфекционных средств для оценки их безопасности и эффективности. – М: МЗ РФ, 1998. – 41 с. • Методика определения и показатели чувствительности (устойчивости) бактерий к дезинфектантам (Е. И. Гудков, А. П. Красильников, Кафедра микробиологии, вирусологии Минского медицинского института, Минск) 2003 г. • Методические рекомендации по ускоренному определению устойчивости бактерий к дезинфекционным средствам (№ 1100 -26 -0 -117, Лабораторный центр Московского городского центра дезинфекции, Москва) 2000 г. – 6 с.
Определение чувствительности внутрибольничных штаммов к дезинфицирующим средствам • Инструкция по определению бактерицидных свойств новых дезинфицирующих средств. - М: МЗ СССР, 1968 № 739 -68 • Методы испытаний дезинфекционных средств для оценки их безопасности и эффективности. – М: МЗ РФ, 1998. – 41 с. • Методика определения и показатели чувствительности (устойчивости) бактерий к дезинфектантам (Е. И. Гудков, А. П. Красильников, Кафедра микробиологии, вирусологии Минского медицинского института, Минск) 2003 г. • Методические рекомендации по ускоренному определению устойчивости бактерий к дезинфекционным средствам (№ 1100 -26 -0 -117, Лабораторный центр Московского городского центра дезинфекции, Москва) 2000 г. – 6 с.
 Методика определения устойчивости бактерий к дезинфектантам • Испытуемый штамм разводится по стандарту мутности 0, 5 ЕД Mc. Forland, согласно «Методическим указаниям по определению чувствительности микроорганизмов к антибактериальным препаратам. МУК 4 -2 -1890 -04» и засевается на питательную среду, соответствующую виду возбудителя (согласно МУК 4 -2 -1890 -04). После подсыхания чашки с культурой производится закапывание рабочего раствора дезинфектанта (с указанием концентрации) на поверхность агара калибровочной петлей диаметром 5 мм (обязательно обвести диаметр нанесения раствора маркером с обратной стороны чашки Петри). Дождаться полного высыхания и убрать чашку в термостат на 35 градусов 18 -24 часа (стандартный режим инкубации). На чашку наносим не более 4 рабочих растворов дезинфицирующих средств (обычно этого как раз хватает на одно отделение стационара).
Методика определения устойчивости бактерий к дезинфектантам • Испытуемый штамм разводится по стандарту мутности 0, 5 ЕД Mc. Forland, согласно «Методическим указаниям по определению чувствительности микроорганизмов к антибактериальным препаратам. МУК 4 -2 -1890 -04» и засевается на питательную среду, соответствующую виду возбудителя (согласно МУК 4 -2 -1890 -04). После подсыхания чашки с культурой производится закапывание рабочего раствора дезинфектанта (с указанием концентрации) на поверхность агара калибровочной петлей диаметром 5 мм (обязательно обвести диаметр нанесения раствора маркером с обратной стороны чашки Петри). Дождаться полного высыхания и убрать чашку в термостат на 35 градусов 18 -24 часа (стандартный режим инкубации). На чашку наносим не более 4 рабочих растворов дезинфицирующих средств (обычно этого как раз хватает на одно отделение стационара).
 Методика определения устойчивости бактерий к дезинфектантам • Оценка результата осуществляется по 4 кретной системе: • - отсутствие зоны просветления в месте нанесения раствора дезинфектанта на чашку; • + - зона просветления небольшая (просматривается большое количество выросших колоний внутри бляшки) • ++ - зона просветления значительная, может доходить до края нанесения бляшки, но не распространяться дальше; • +++ - полная зона просветления в месте нанесения бляшки, отсутствие роста наблюдается за пределами линии нанесения дезраствора; • ++++ - зона полного лизиса культуры, выходящая за пределы нанесения дезраствора, превосходящая диаметр бляшки в несколько раз. (очень активно так работает перекись водорода).
Методика определения устойчивости бактерий к дезинфектантам • Оценка результата осуществляется по 4 кретной системе: • - отсутствие зоны просветления в месте нанесения раствора дезинфектанта на чашку; • + - зона просветления небольшая (просматривается большое количество выросших колоний внутри бляшки) • ++ - зона просветления значительная, может доходить до края нанесения бляшки, но не распространяться дальше; • +++ - полная зона просветления в месте нанесения бляшки, отсутствие роста наблюдается за пределами линии нанесения дезраствора; • ++++ - зона полного лизиса культуры, выходящая за пределы нанесения дезраствора, превосходящая диаметр бляшки в несколько раз. (очень активно так работает перекись водорода).
 Оценка результатов микробиологического мониторинга Признаками благополучной эпидемической обстановки в подразделении являются : • Отсутствие циркуляции среди пациентов высоковирулентных штаммов условно-патогенных микроорганизмов, сопоставимых по виду и антибиотикограмме; Примечание. Сопоставимыми по виду являются штаммы, однотипные по тинкториальным, культуральным и биохимическим свойствам. Сопоставимыми по антибиотикограмме считаются штаммы, различающиеся не более чем на 2 -3 антибиотика (при одновременной постановке чувствительности к 10 препаратам), согласно критериям определения NССLS - «чувствительный» , «умеренно-устойчивый» , «чувствительный» . • Отсутствие во внешней среде высоковирулентных штаммов, сопоставимых по виду и профилю антибиотикочувствительности; • Отсутствие или снижение роста (относительно результатов предыдущего микробиологического мониторинга) циркуляции среди пациентов и во внешней среде штаммов условно-патогенных микроорганизмов - активных продуцентов ß-лактамаз; • Отсутствие контаминации высоковирулентным штаммом дезинфицирующего средства, применяемого в работе; • Удовлетворительные результаты контроля работы стерилизационного оборудования; • Отвечающая нормативным критериям бактериальная обсемененность воздушной среды особо чистых помещений класса А.
Оценка результатов микробиологического мониторинга Признаками благополучной эпидемической обстановки в подразделении являются : • Отсутствие циркуляции среди пациентов высоковирулентных штаммов условно-патогенных микроорганизмов, сопоставимых по виду и антибиотикограмме; Примечание. Сопоставимыми по виду являются штаммы, однотипные по тинкториальным, культуральным и биохимическим свойствам. Сопоставимыми по антибиотикограмме считаются штаммы, различающиеся не более чем на 2 -3 антибиотика (при одновременной постановке чувствительности к 10 препаратам), согласно критериям определения NССLS - «чувствительный» , «умеренно-устойчивый» , «чувствительный» . • Отсутствие во внешней среде высоковирулентных штаммов, сопоставимых по виду и профилю антибиотикочувствительности; • Отсутствие или снижение роста (относительно результатов предыдущего микробиологического мониторинга) циркуляции среди пациентов и во внешней среде штаммов условно-патогенных микроорганизмов - активных продуцентов ß-лактамаз; • Отсутствие контаминации высоковирулентным штаммом дезинфицирующего средства, применяемого в работе; • Удовлетворительные результаты контроля работы стерилизационного оборудования; • Отвечающая нормативным критериям бактериальная обсемененность воздушной среды особо чистых помещений класса А.
 Микробиологический мониторинг по эпидпоказаниям Показания для проведения выборочных одномоментных исследований пациентов и больничных объектов (признаки неблагополучной эпидемической обстановки): • • • • Увеличение среди пациентов числа случаев гнойно-септических инфекций; Преобладание в структуре заболеваемости ГСИ одной из клинических форм; Появление в структуре заболеваемости ГСИ случаев с множественной локализацией, тяжелых (генерализованных) клинических форм; Возникновение двух или более случаев заболеваний, эпидемиологически связанных между собой; Увеличение количества новорожденных с диагнозом «внутриутробное инфицирование» ; Увеличение сроков пребывания пациентов в стационаре; Увеличение расхода антибактериальных, противовоспалительных препаратов и перевязочного материала относительно среднемесячных норм; Рост числа малых оперативных вмешательств (вскрытие абсцессов, флегмон, повторная санация и дренирование операционных ран); Рост числа температурящих больных; Рост заболеваемости ГСИ среди медицинского персонала; Рост циркуляции среди пациентов штаммов микроорганизмов - активных продуцентов ß-лактамаз; Обнаружение среди пациентов с гнойно-септическими осложнениями высоковирулентных штаммов, сопоставимых по виду и антибиотикограмме; Контаминация сопоставимыми высоковирулентными штаммами предметов больничной среды; Контаминация высоковирулентным штаммом рабочего раствора дезинфицирующего средства; Несоответствие проб воздушной среды основных помещений класса А микробиологическим нормативам; Неудовлетворительные результаты микробиологического контроля стерилизационного оборудования.
Микробиологический мониторинг по эпидпоказаниям Показания для проведения выборочных одномоментных исследований пациентов и больничных объектов (признаки неблагополучной эпидемической обстановки): • • • • Увеличение среди пациентов числа случаев гнойно-септических инфекций; Преобладание в структуре заболеваемости ГСИ одной из клинических форм; Появление в структуре заболеваемости ГСИ случаев с множественной локализацией, тяжелых (генерализованных) клинических форм; Возникновение двух или более случаев заболеваний, эпидемиологически связанных между собой; Увеличение количества новорожденных с диагнозом «внутриутробное инфицирование» ; Увеличение сроков пребывания пациентов в стационаре; Увеличение расхода антибактериальных, противовоспалительных препаратов и перевязочного материала относительно среднемесячных норм; Рост числа малых оперативных вмешательств (вскрытие абсцессов, флегмон, повторная санация и дренирование операционных ран); Рост числа температурящих больных; Рост заболеваемости ГСИ среди медицинского персонала; Рост циркуляции среди пациентов штаммов микроорганизмов - активных продуцентов ß-лактамаз; Обнаружение среди пациентов с гнойно-септическими осложнениями высоковирулентных штаммов, сопоставимых по виду и антибиотикограмме; Контаминация сопоставимыми высоковирулентными штаммами предметов больничной среды; Контаминация высоковирулентным штаммом рабочего раствора дезинфицирующего средства; Несоответствие проб воздушной среды основных помещений класса А микробиологическим нормативам; Неудовлетворительные результаты микробиологического контроля стерилизационного оборудования.
 Микробиологический мониторинг по эпидпоказаниям Микробиологический мониторинг пациентов Обязательному бактериологическому обследованию подлежат: • Пациенты структурных подразделений, где были выявлены признаки эпидемического неблагополучия Забор образцов биологического материала (наиболее колонизируемого внутрибольничными эковарами) проводит медицинский персонал отделения стационара под контролем сотрудника микробиологической лаборатории на момент присутствия пациентов в отделении (не менее 10 -15 человек) не зависимо от наличия у них клинических показаний Учету подлежат вирулентные штаммы микроорганизмов (с природными или приобретенными факторами патогенности)
Микробиологический мониторинг по эпидпоказаниям Микробиологический мониторинг пациентов Обязательному бактериологическому обследованию подлежат: • Пациенты структурных подразделений, где были выявлены признаки эпидемического неблагополучия Забор образцов биологического материала (наиболее колонизируемого внутрибольничными эковарами) проводит медицинский персонал отделения стационара под контролем сотрудника микробиологической лаборатории на момент присутствия пациентов в отделении (не менее 10 -15 человек) не зависимо от наличия у них клинических показаний Учету подлежат вирулентные штаммы микроорганизмов (с природными или приобретенными факторами патогенности)
 Микробиологический мониторинг по эпидпоказаниям Микробиологический мониторинг больничной среды • • Внеплановый микробиологический контроль объектов внешней среды функционального подразделения осуществляется одновременно с микробиологическим мониторингом пациентов медицинским персоналом микробиологических лабораторий под контролем заведующего отделением, госпитального эпидемиолога и старшей медицинской сестры. Перечень отбираемых объектов и характер изучаемой микрофлоры определяется проявлениями эпидемического процесса и характеристикой его биологического фактора. Исследованию подлежат пробы в количестве 20 -25 предметов. В обязательном порядке отбирают рабочие растворы дезинфицирующих средств (для изучения их контаминации и для оценки чувствительности к ним выделенных высоковирулентных штаммов микроорганизмов). На основании критериев стандартного эпидемиологического определения внутрибольничного штамма делается заключение о наличии или отсутствии этих штаммов в структурном подразделении
Микробиологический мониторинг по эпидпоказаниям Микробиологический мониторинг больничной среды • • Внеплановый микробиологический контроль объектов внешней среды функционального подразделения осуществляется одновременно с микробиологическим мониторингом пациентов медицинским персоналом микробиологических лабораторий под контролем заведующего отделением, госпитального эпидемиолога и старшей медицинской сестры. Перечень отбираемых объектов и характер изучаемой микрофлоры определяется проявлениями эпидемического процесса и характеристикой его биологического фактора. Исследованию подлежат пробы в количестве 20 -25 предметов. В обязательном порядке отбирают рабочие растворы дезинфицирующих средств (для изучения их контаминации и для оценки чувствительности к ним выделенных высоковирулентных штаммов микроорганизмов). На основании критериев стандартного эпидемиологического определения внутрибольничного штамма делается заключение о наличии или отсутствии этих штаммов в структурном подразделении
 ЭФФЕКТИВНОСТЬ ТРЕХ ФОРМ МИКРОБИОЛОГИЧЕСКОГО МОНИТОРИНГА В МЕДИЦИНСКИХ УЧРЕЖДЕНИЯХ
ЭФФЕКТИВНОСТЬ ТРЕХ ФОРМ МИКРОБИОЛОГИЧЕСКОГО МОНИТОРИНГА В МЕДИЦИНСКИХ УЧРЕЖДЕНИЯХ
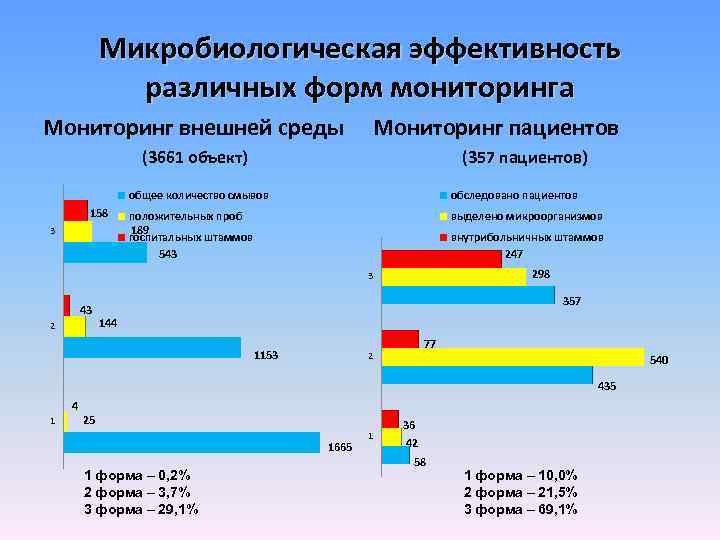 Микробиологическая эффективность различных форм мониторинга Мониторинг внешней среды Мониторинг пациентов (3661 объект) (357 пациентов) общее количество смывов 158 3 обследовано пациентов положительных проб 189 госпитальных штаммов 543 выделено микроорганизмов внутрибольничных штаммов 247 298 3 43 2 357 144 1153 77 2 540 435 4 1 25 1665 1 форма – 0, 2% 2 форма – 3, 7% 3 форма – 29, 1% 1 36 42 58 1 форма – 10, 0% 2 форма – 21, 5% 3 форма – 69, 1%
Микробиологическая эффективность различных форм мониторинга Мониторинг внешней среды Мониторинг пациентов (3661 объект) (357 пациентов) общее количество смывов 158 3 обследовано пациентов положительных проб 189 госпитальных штаммов 543 выделено микроорганизмов внутрибольничных штаммов 247 298 3 43 2 357 144 1153 77 2 540 435 4 1 25 1665 1 форма – 0, 2% 2 форма – 3, 7% 3 форма – 29, 1% 1 36 42 58 1 форма – 10, 0% 2 форма – 21, 5% 3 форма – 69, 1%
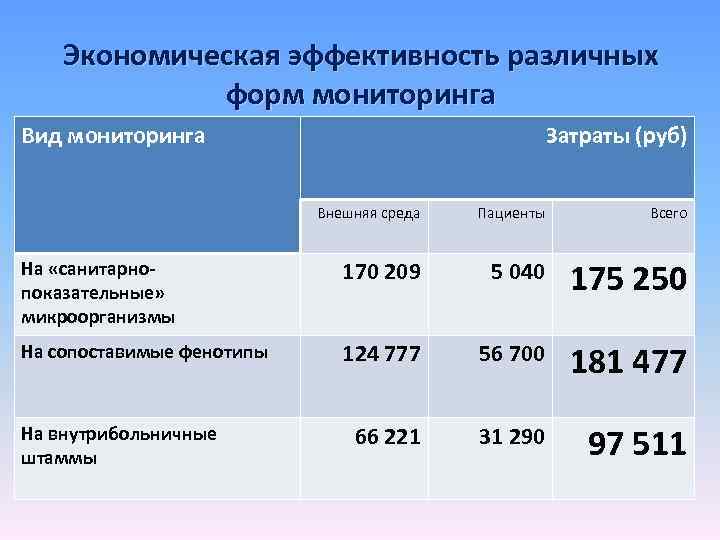 Экономическая эффективность различных форм мониторинга Вид мониторинга Затраты (руб) Внешняя среда Пациенты Всего На «санитарнопоказательные» микроорганизмы 170 209 5 040 175 250 На сопоставимые фенотипы 124 777 56 700 181 477 66 221 31 290 97 511 На внутрибольничные штаммы
Экономическая эффективность различных форм мониторинга Вид мониторинга Затраты (руб) Внешняя среда Пациенты Всего На «санитарнопоказательные» микроорганизмы 170 209 5 040 175 250 На сопоставимые фенотипы 124 777 56 700 181 477 66 221 31 290 97 511 На внутрибольничные штаммы
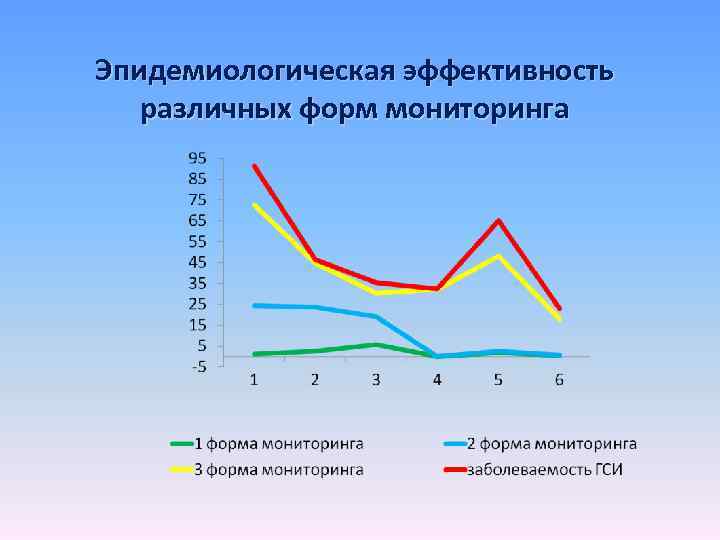 Эпидемиологическая эффективность различных форм мониторинга
Эпидемиологическая эффективность различных форм мониторинга
 Задачи предэпидемической диагностики ГСИ в акушерском стационаре • Прогнозирование послеродовых ГСИ • Предотвращение инфицирования в активный инфекционный процесс • Профилактика инфицирования
Задачи предэпидемической диагностики ГСИ в акушерском стационаре • Прогнозирование послеродовых ГСИ • Предотвращение инфицирования в активный инфекционный процесс • Профилактика инфицирования
 Биологические материалы пациентов акушерского стационара в системе мониторинга по профилю подразделения Отделение Биологический материал Женская консультация Вагинальный секрет, моча Гинекологическое Вагинальный секрет, операционная рана Патологии беременных Вагинальный секрет Физиологии, патологии новорожденных Пупочная ранка, кал Физиологии, патологии родильниц Вагинальный секрет ОРИТ По локализации инвазивного вмешательства Родовой блок Послед
Биологические материалы пациентов акушерского стационара в системе мониторинга по профилю подразделения Отделение Биологический материал Женская консультация Вагинальный секрет, моча Гинекологическое Вагинальный секрет, операционная рана Патологии беременных Вагинальный секрет Физиологии, патологии новорожденных Пупочная ранка, кал Физиологии, патологии родильниц Вагинальный секрет ОРИТ По локализации инвазивного вмешательства Родовой блок Послед
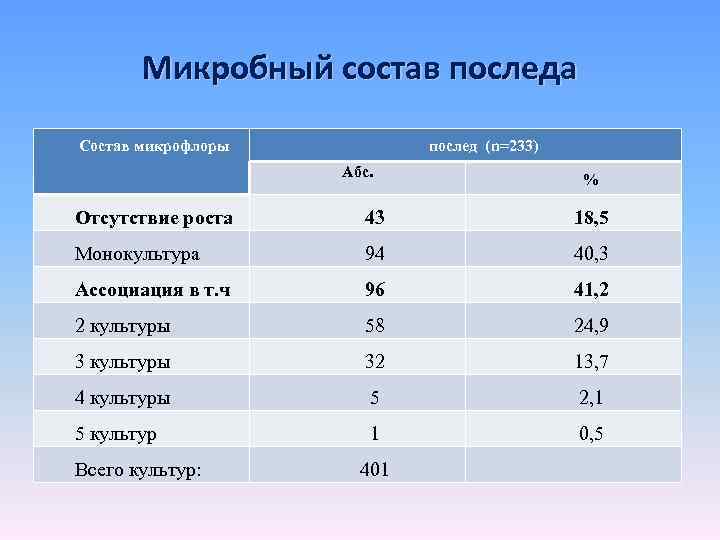 Микробный состав последа Состав микрофлоры послед (n=233) Абс. % Отсутствие роста 43 18, 5 Монокультура 94 40, 3 Ассоциация в т. ч 96 41, 2 2 культуры 58 24, 9 3 культуры 32 13, 7 4 культуры 5 2, 1 5 культур 1 0, 5 Всего культур: 401
Микробный состав последа Состав микрофлоры послед (n=233) Абс. % Отсутствие роста 43 18, 5 Монокультура 94 40, 3 Ассоциация в т. ч 96 41, 2 2 культуры 58 24, 9 3 культуры 32 13, 7 4 культуры 5 2, 1 5 культур 1 0, 5 Всего культур: 401
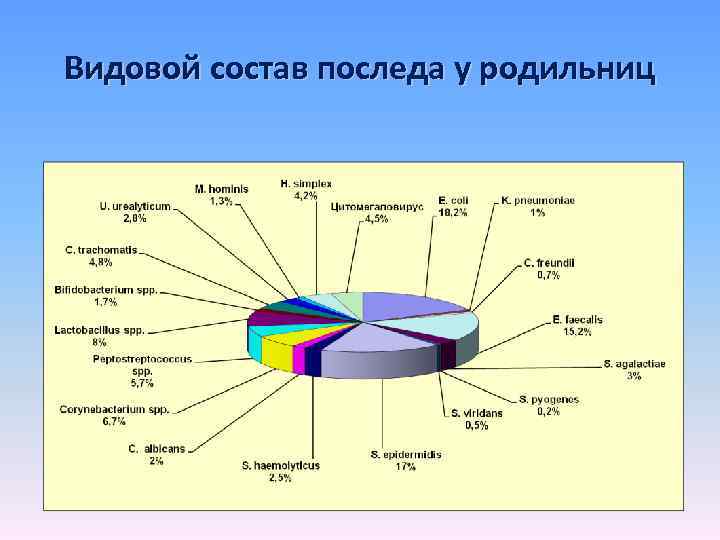 Видовой состав последа у родильниц
Видовой состав последа у родильниц
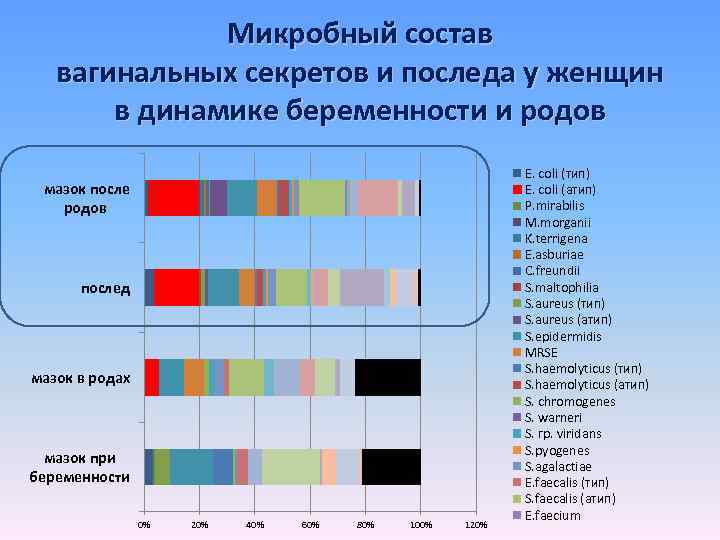 Микробный состав вагинальных секретов и последа у женщин в динамике беременности и родов мазок после родов послед мазок в родах мазок при беременности 0% 20% 40% 60% 80% 100% 120% E. coli (тип) E. coli (атип) P. mirabilis M. morganii K. terrigena E. asburiae C. freundii S. maltophilia S. aureus (тип) S. aureus (атип) S. epidermidis MRSE S. haemolyticus (тип) S. haemolyticus (атип) S. chromogenes S. warneri S. гр. viridans S. pyogenes S. agalactiae E. faecalis (тип) S. faecalis (атип) E. faecium
Микробный состав вагинальных секретов и последа у женщин в динамике беременности и родов мазок после родов послед мазок в родах мазок при беременности 0% 20% 40% 60% 80% 100% 120% E. coli (тип) E. coli (атип) P. mirabilis M. morganii K. terrigena E. asburiae C. freundii S. maltophilia S. aureus (тип) S. aureus (атип) S. epidermidis MRSE S. haemolyticus (тип) S. haemolyticus (атип) S. chromogenes S. warneri S. гр. viridans S. pyogenes S. agalactiae E. faecalis (тип) S. faecalis (атип) E. faecium
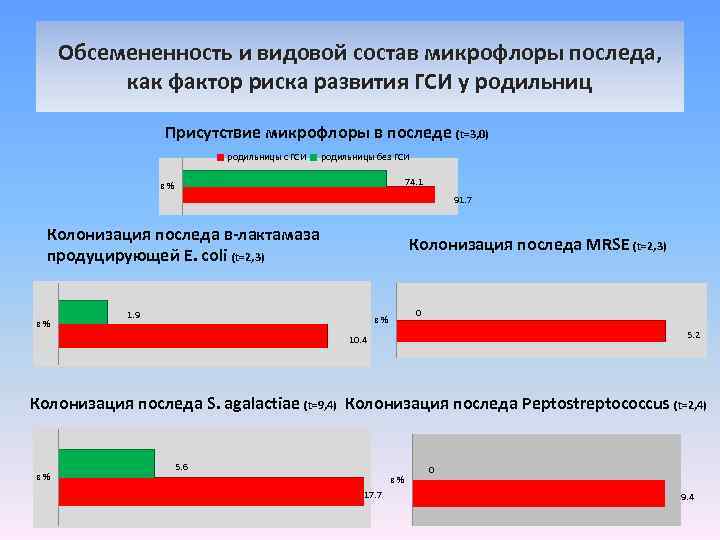 Обсемененность и видовой состав микрофлоры последа, как фактор риска развития ГСИ у родильниц Присутствие микрофлоры в последе (t=3, 0) родильницы с ГСИ родильницы без ГСИ 74. 1 в% 91. 7 Колонизация последа в-лактамаза продуцирующей E. coli (t=2, 3) в% Колонизация последа MRSE (t=2, 3) 1. 9 0 в% 5. 2 10. 4 Колонизация последа S. agalactiae (t=9, 4) Колонизация последа Peptostreptococcus (t=2, 4) в% 5. 6 в% 17. 7 0 9. 4
Обсемененность и видовой состав микрофлоры последа, как фактор риска развития ГСИ у родильниц Присутствие микрофлоры в последе (t=3, 0) родильницы с ГСИ родильницы без ГСИ 74. 1 в% 91. 7 Колонизация последа в-лактамаза продуцирующей E. coli (t=2, 3) в% Колонизация последа MRSE (t=2, 3) 1. 9 0 в% 5. 2 10. 4 Колонизация последа S. agalactiae (t=9, 4) Колонизация последа Peptostreptococcus (t=2, 4) в% 5. 6 в% 17. 7 0 9. 4
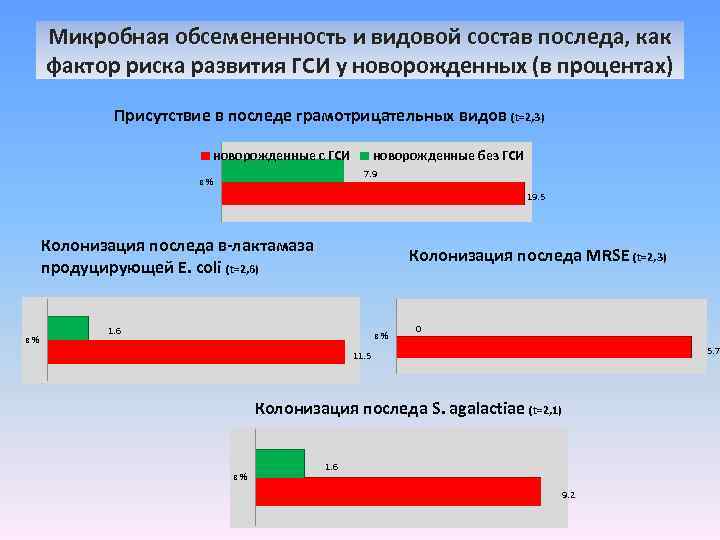 Микробная обсемененность и видовой состав последа, как фактор риска развития ГСИ у новорожденных (в процентах) Присутствие в последе грамотрицательных видов (t=2, 3) новорожденные с ГСИ новорожденные без ГСИ 7. 9 в% 19. 5 Колонизация последа в-лактамаза продуцирующей E. coli (t=2, 6) в% Колонизация последа MRSE (t=2, 3) 1. 6 в% 0 5. 7 11. 5 Колонизация последа S. agalactiae (t=2, 1) в% 1. 6 9. 2
Микробная обсемененность и видовой состав последа, как фактор риска развития ГСИ у новорожденных (в процентах) Присутствие в последе грамотрицательных видов (t=2, 3) новорожденные с ГСИ новорожденные без ГСИ 7. 9 в% 19. 5 Колонизация последа в-лактамаза продуцирующей E. coli (t=2, 6) в% Колонизация последа MRSE (t=2, 3) 1. 6 в% 0 5. 7 11. 5 Колонизация последа S. agalactiae (t=2, 1) в% 1. 6 9. 2
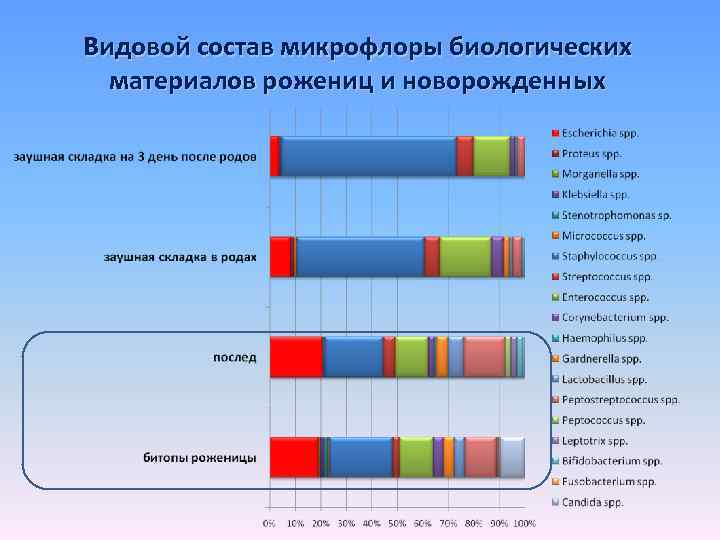 Видовой состав микрофлоры биологических материалов рожениц и новорожденных
Видовой состав микрофлоры биологических материалов рожениц и новорожденных
 Эпидемиологическое обоснование исследования последа в системе микробиологического мониторинга в акушерских стационарах Показания к микробиологическому исследованию последа у родильниц • • • наличие в анамнезе хронических форм ИМВП или перенесенная инфекция мочевых путей при беременности Показания к микробиологическому исследованию последа у новорожденных масса тела при рождении ниже 2800 гр. • госпитализация из родового блока в ОРИТ • патология плаценты, выявленная акушером-гинекологом • дородовая госпитализация матери в ОРИТ • отсутствие антибиотикопрофилактики при длительном безводном периоде (более 12 часов) и оперативном родоразрешении • перенесенная матерью ИМВП при беременности дородовая госпитализация в ОРИТ Исследование последа в системе микробиологического мониторинга позволяет своевременно выявить условно-патогенные штаммы, определяющие уровень гнойно-септической заболеваемости среди родильниц и новорожденных и прогнозировать у них развитие ГСИ в ранний послеродовой период
Эпидемиологическое обоснование исследования последа в системе микробиологического мониторинга в акушерских стационарах Показания к микробиологическому исследованию последа у родильниц • • • наличие в анамнезе хронических форм ИМВП или перенесенная инфекция мочевых путей при беременности Показания к микробиологическому исследованию последа у новорожденных масса тела при рождении ниже 2800 гр. • госпитализация из родового блока в ОРИТ • патология плаценты, выявленная акушером-гинекологом • дородовая госпитализация матери в ОРИТ • отсутствие антибиотикопрофилактики при длительном безводном периоде (более 12 часов) и оперативном родоразрешении • перенесенная матерью ИМВП при беременности дородовая госпитализация в ОРИТ Исследование последа в системе микробиологического мониторинга позволяет своевременно выявить условно-патогенные штаммы, определяющие уровень гнойно-септической заболеваемости среди родильниц и новорожденных и прогнозировать у них развитие ГСИ в ранний послеродовой период
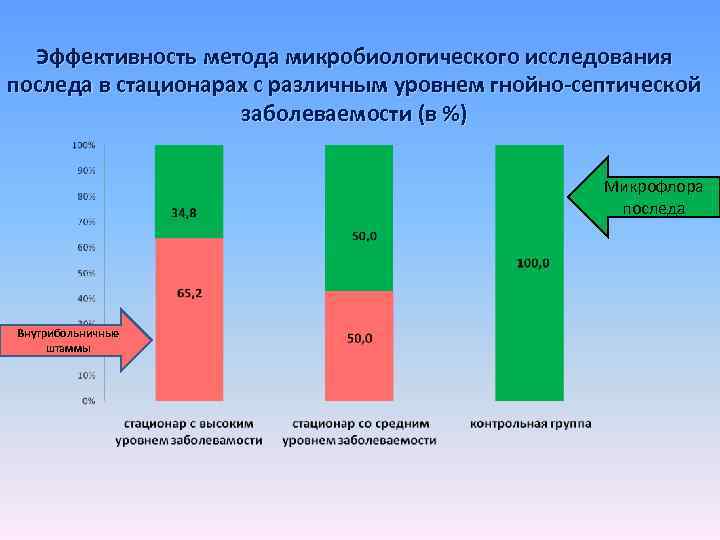 Эффективность метода микробиологического исследования последа в стационарах с различным уровнем гнойно-септической заболеваемости (в %) Микрофлора последа Внутрибольничные штаммы
Эффективность метода микробиологического исследования последа в стационарах с различным уровнем гнойно-септической заболеваемости (в %) Микрофлора последа Внутрибольничные штаммы


