livshitz 2.2.ppt
- Количество слайдов: 28

Состав и структура белков
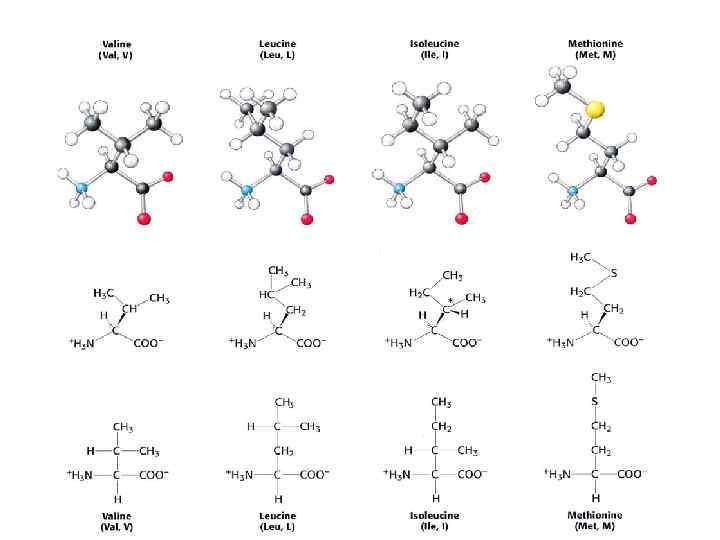
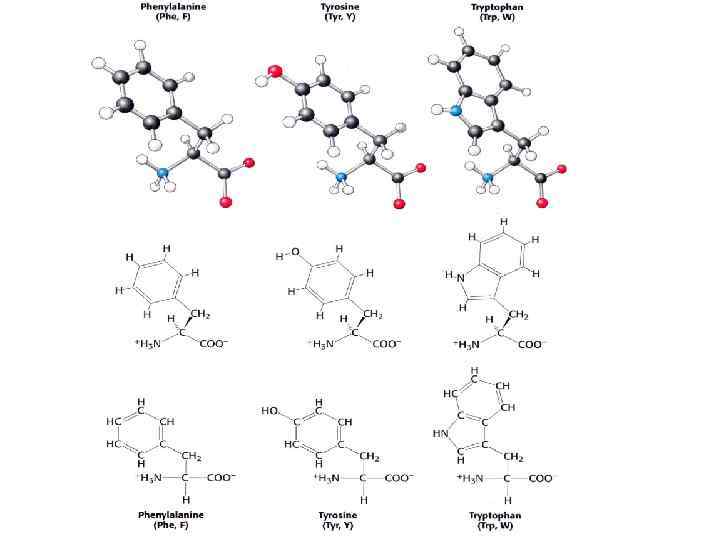
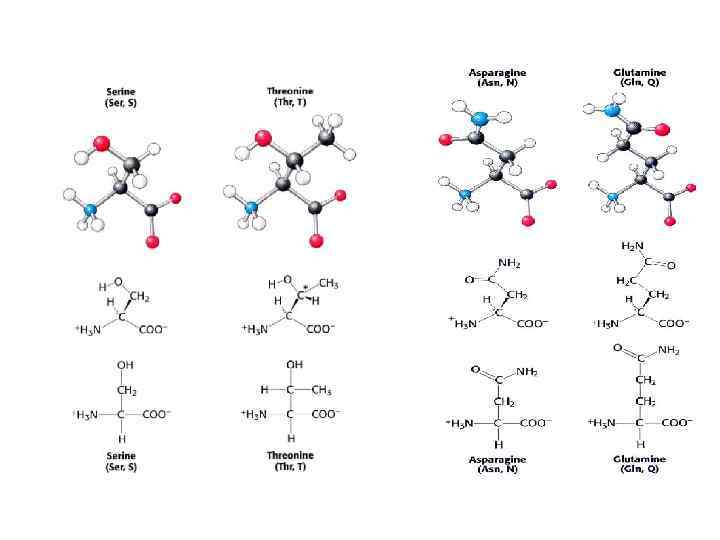
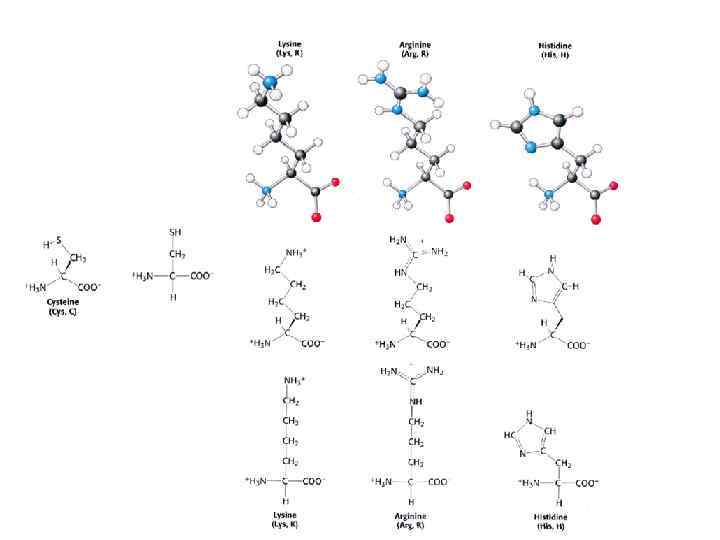
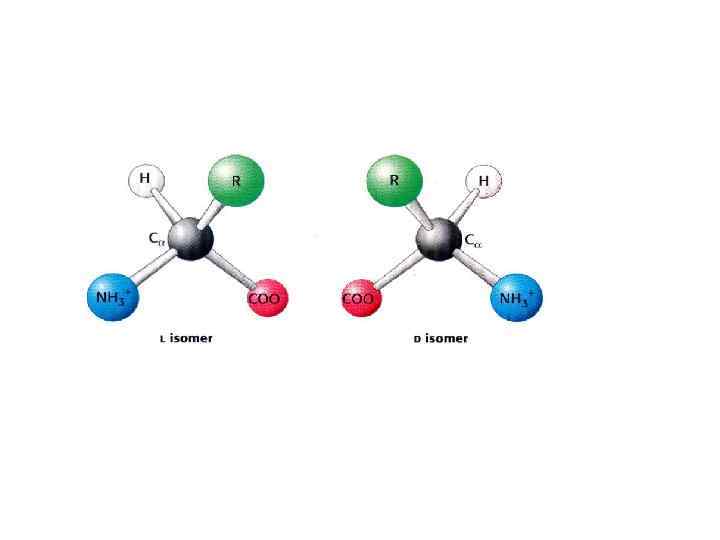
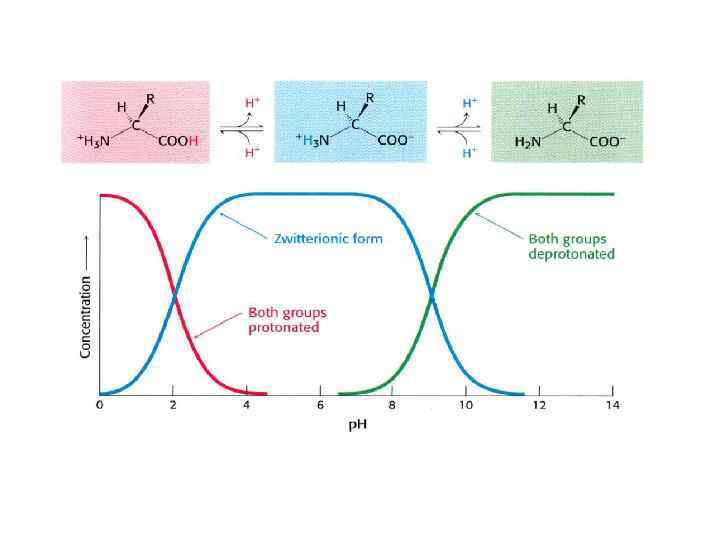
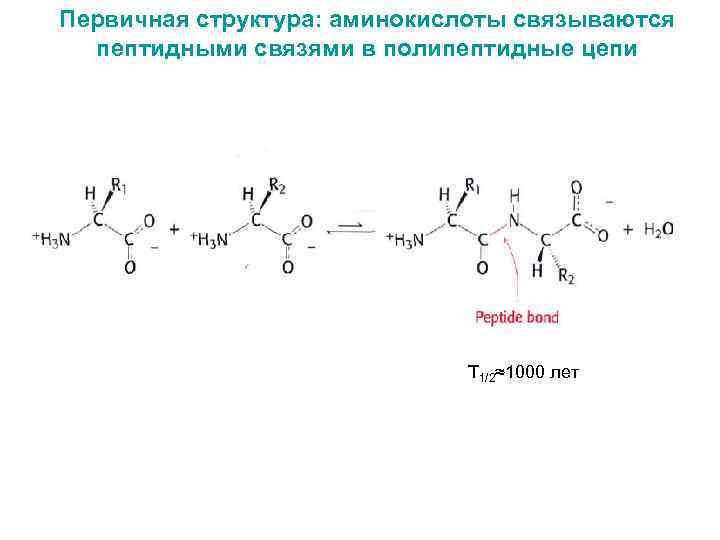
Первичная структура: аминокислоты связываются пептидными связями в полипептидные цепи Τ 1/2≈1000 лет
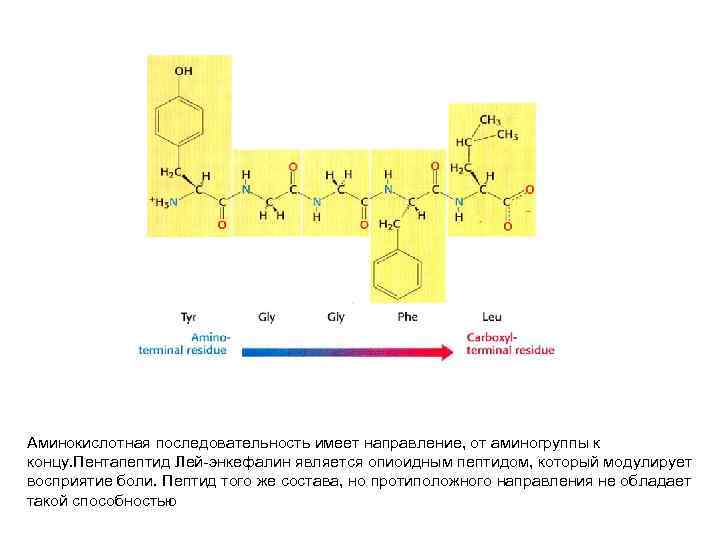
Аминокислотная последовательность имеет направление, от аминогруппы к концу. Пентапептид Лей-энкефалин является опиоидным пептидом, который модулирует восприятие боли. Пептид того же состава, но протиположного направления не обладает такой способностью
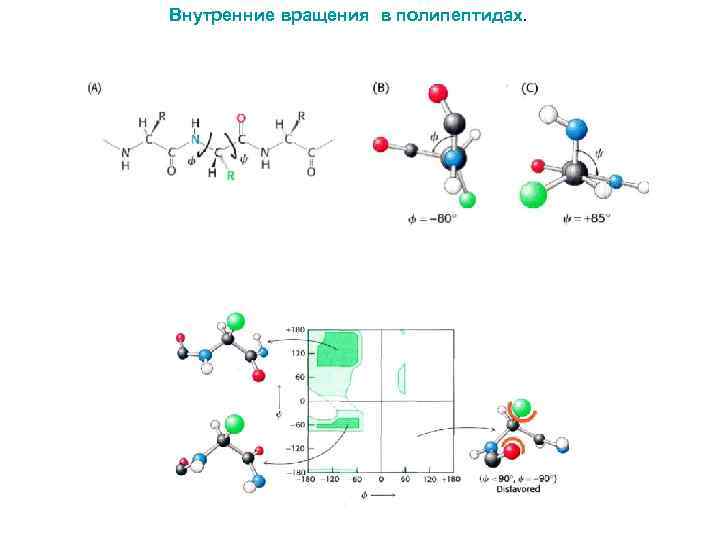
Внутренние вращения в полипептидах.
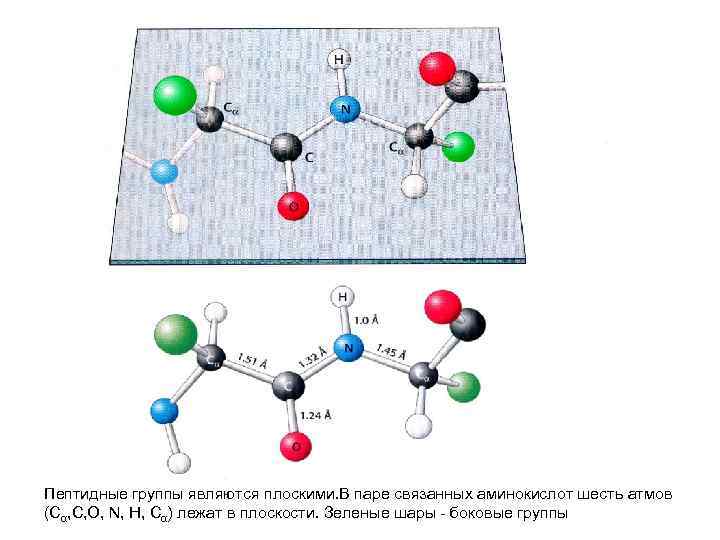
Пептидные группы являются плоскими. В паре связанных аминокислот шесть атмов (Сα, C, O, N, H, Cα) лежат в плоскости. Зеленые шары - боковые группы
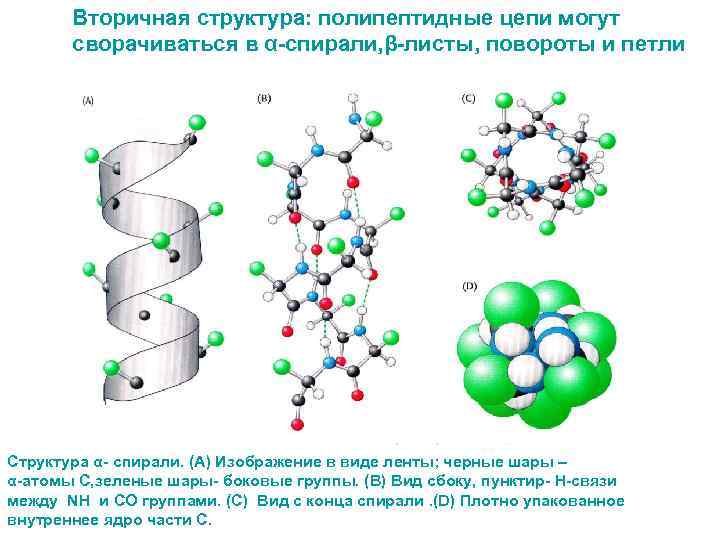
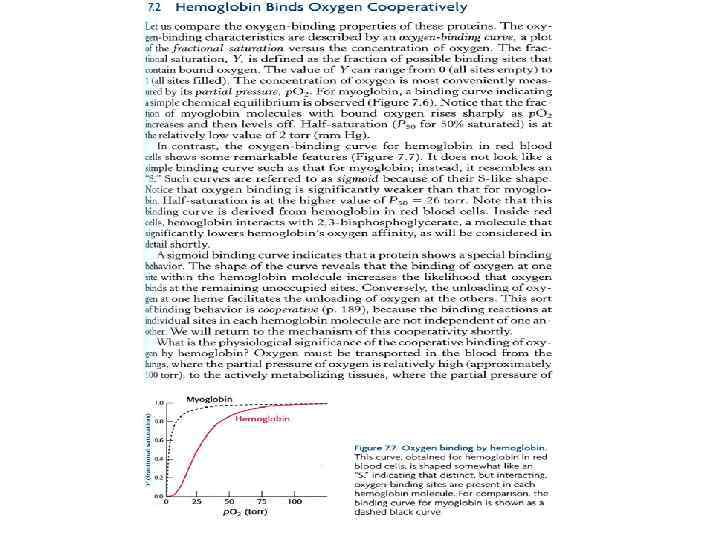
Вторичная структура: полипептидные цепи могут сворачиваться в α-спирали, β-листы, повороты и петли Структура α- спирали. (А) Изображение в виде ленты; черные шары – α-атомы С, зеленые шары- боковые группы. (В) Вид сбоку, пунктир- Н-связи между NH и CO группами. (С) Вид с конца спирали. (D) Плотно упакованное внутреннее ядро части С.
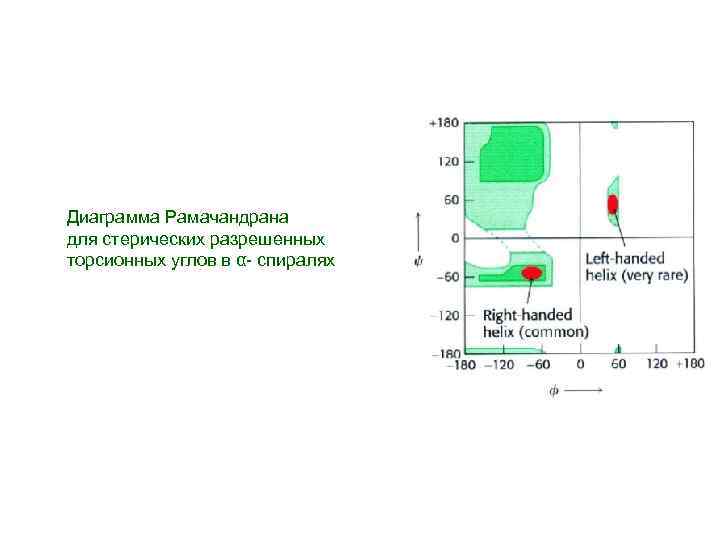
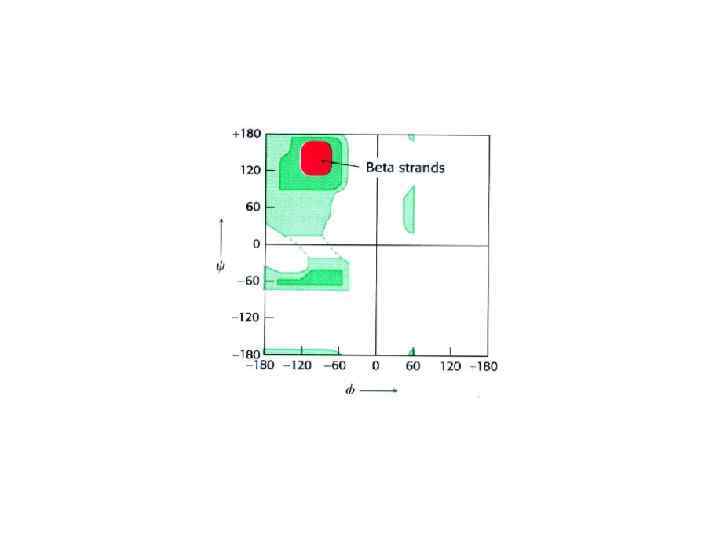
Диаграмма Рамачандрана для стерических разрешенных торсионных углов в α- спиралях
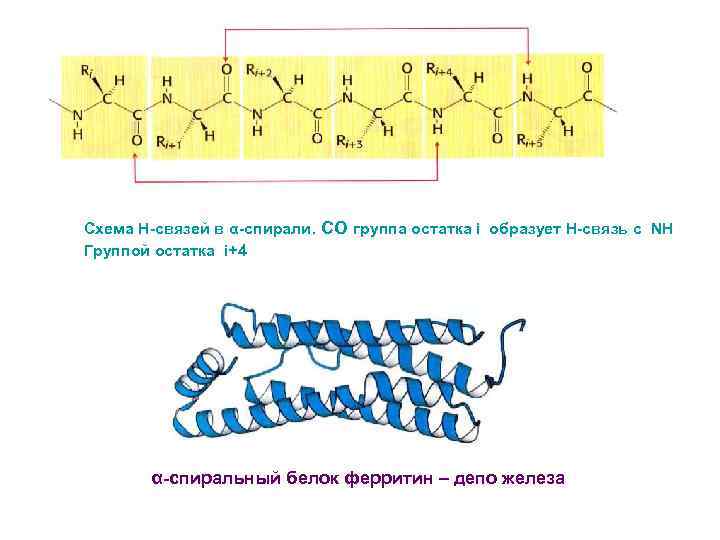
Схема Н-связей в α-спирали. СО группа остатка i образует Н-связь с NH Группой остатка i+4 α-спиральный белок ферритин – депо железа
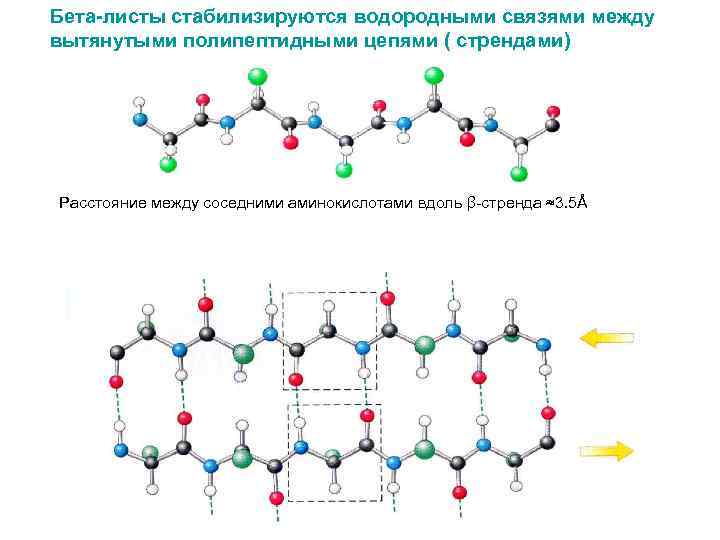
Бета-листы стабилизируются водородными связями между вытянутыми полипептидными цепями ( стрендами) Расстояние между соседними аминокислотами вдоль β-стренда ≈3. 5Å
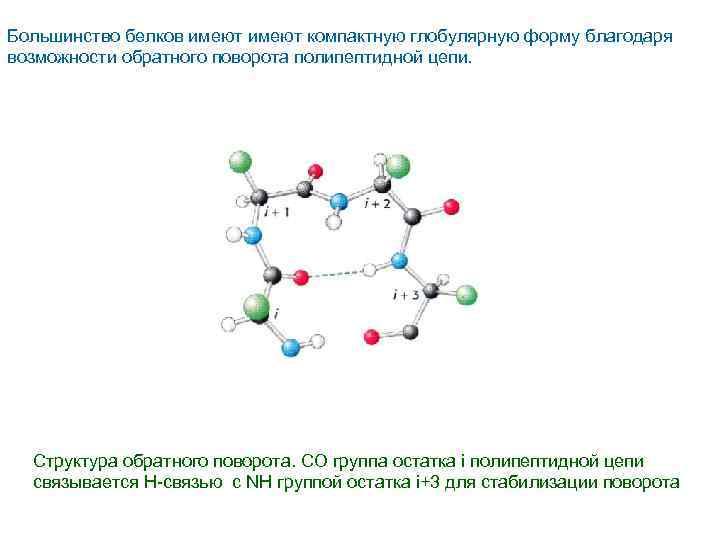
Большинство белков имеют компактную глобулярную форму благодаря возможности обратного поворота полипептидной цепи. Структура обратного поворота. СО группа остатка i полипептидной цепи связывается Н-связью с NH группой остатка i+3 для стабилизации поворота
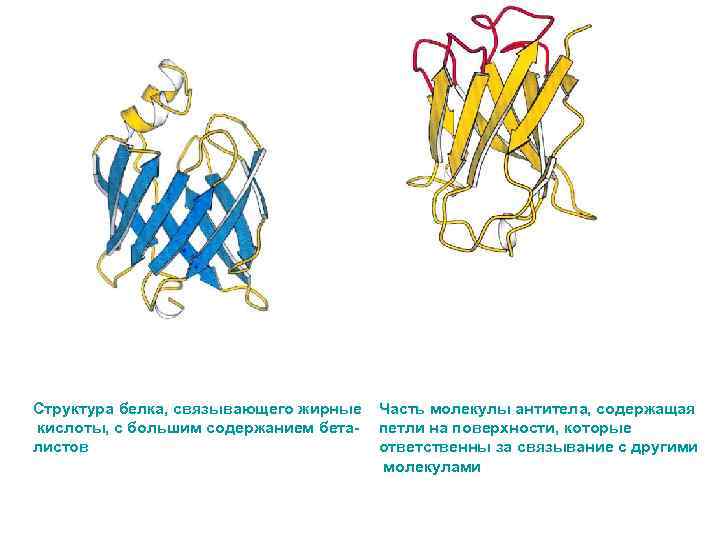
Структура белка, связывающего жирные кислоты, с большим содержанием беталистов Часть молекулы антитела, содержащая петли на поверхности, которые ответственны за связывание с другими молекулами

Фибриллярные белки обеспечивают поддержание структуры и формы клеток и тканей α- суперспираль ( Такие структуры найдены во многих белках, включая кератин в волосах, рогах и когтях.

Структура коллагена. Каждый стренд связан Н-связями с двумя другими стрендами.
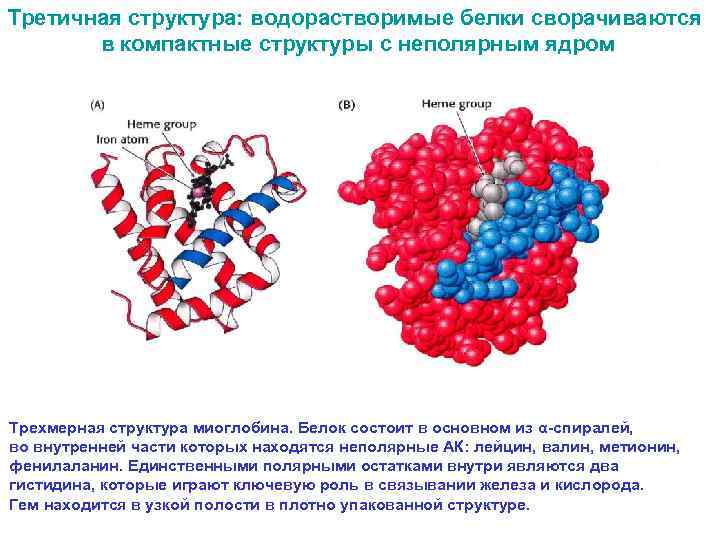
Третичная структура: водорастворимые белки сворачиваются в компактные структуры с неполярным ядром Трехмерная структура миоглобина. Белок состоит в основном из α-спиралей, во внутренней части которых находятся неполярные АК: лейцин, валин, метионин, фенилаланин. Единственными полярными остатками внутри являются два гистидина, которые играют ключевую роль в связывании железа и кислорода. Гем находится в узкой полости в плотно упакованной структуре.
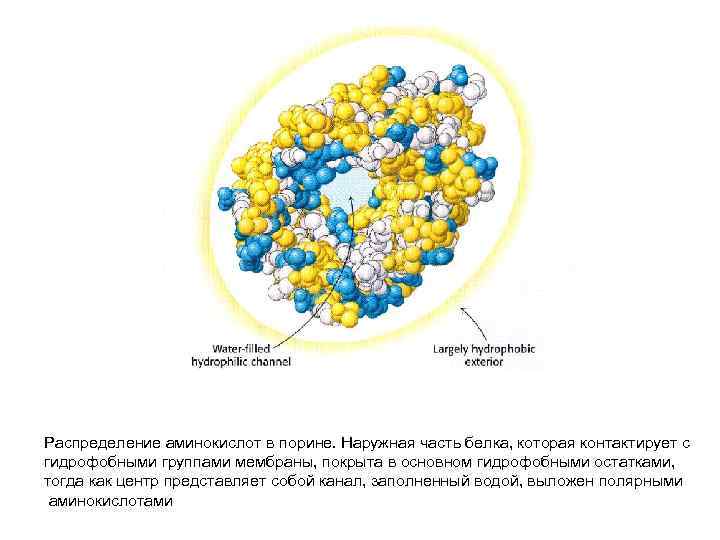
Распределение аминокислот в порине. Наружная часть белка, которая контактирует с гидрофобными группами мембраны, покрыта в основном гидрофобными остатками, тогда как центр представляет собой канал, заполненный водой, выложен полярными аминокислотами
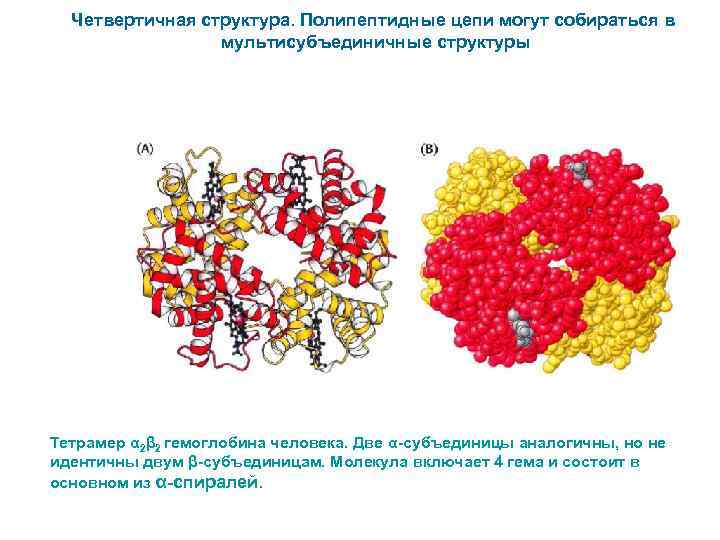
Четвертичная структура. Полипептидные цепи могут собираться в мультисубъединичные структуры Тетрамер α 2β 2 гемоглобина человека. Две α-субъединицы аналогичны, но не идентичны двум β-субъединицам. Молекула включает 4 гема и состоит в основном из α-спиралей.
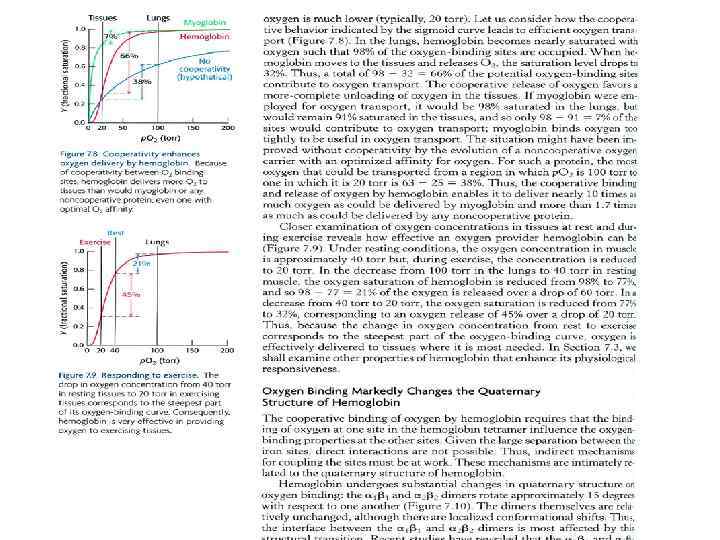
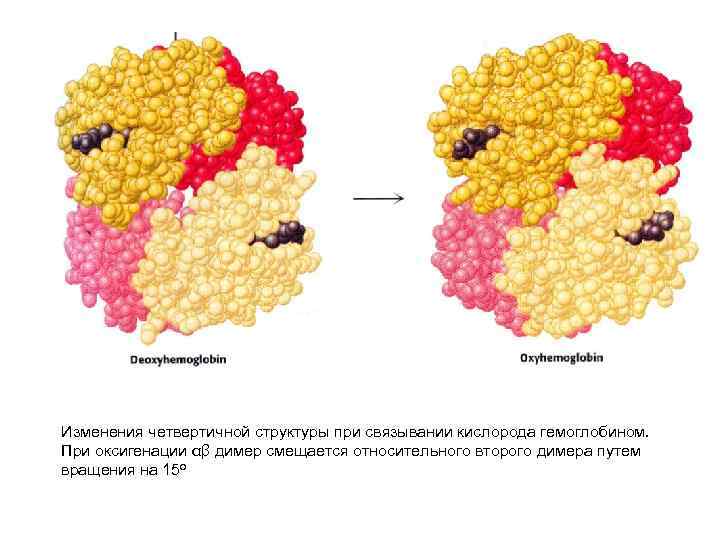
Изменения четвертичной структуры при связывании кислорода гемоглобином. При оксигенации αβ димер смещается относительного второго димера путем вращения на 15 о
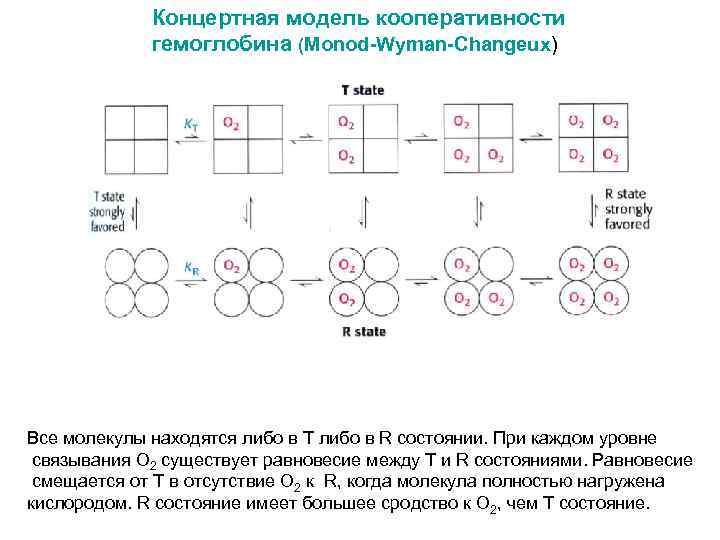
Концертная модель кооперативности гемоглобина (Monod-Wyman-Changeux) Все молекулы находятся либо в T либо в R состоянии. При каждом уровне связывания О 2 существует равновесие между T и R состояниями. Равновесие смещается от T в отсутствие О 2 к R, когда молекула полностью нагружена кислородом. R состояние имеет большее сродство к О 2, чем T состояние.
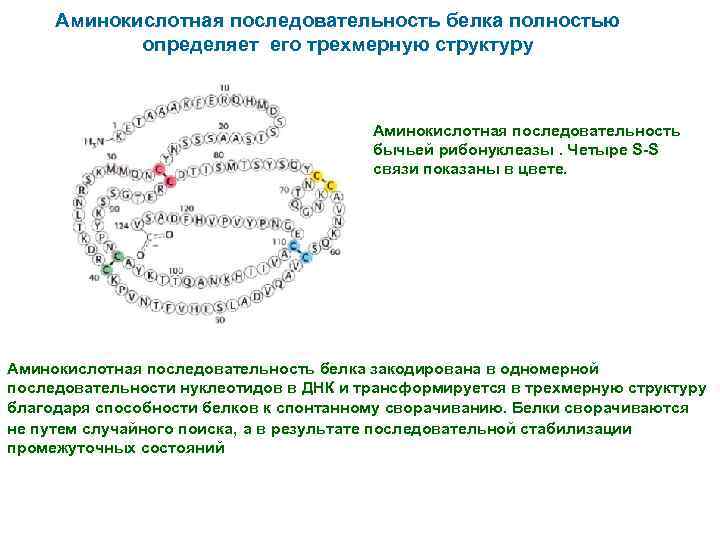
Аминокислотная последовательность белка полностью определяет его трехмерную структуру Аминокислотная последовательность бычьей рибонуклеазы. Четыре S-S связи показаны в цвете. Аминокислотная последовательность белка закодирована в одномерной последовательности нуклеотидов в ДНК и трансформируется в трехмерную структуру благодаря способности белков к спонтанному сворачиванию. Белки сворачиваются не путем случайного поиска, а в результате последовательной стабилизации промежуточных состояний
livshitz 2.2.ppt