08_Lecture_Proteins_Import_2010.ppt
- Количество слайдов: 22
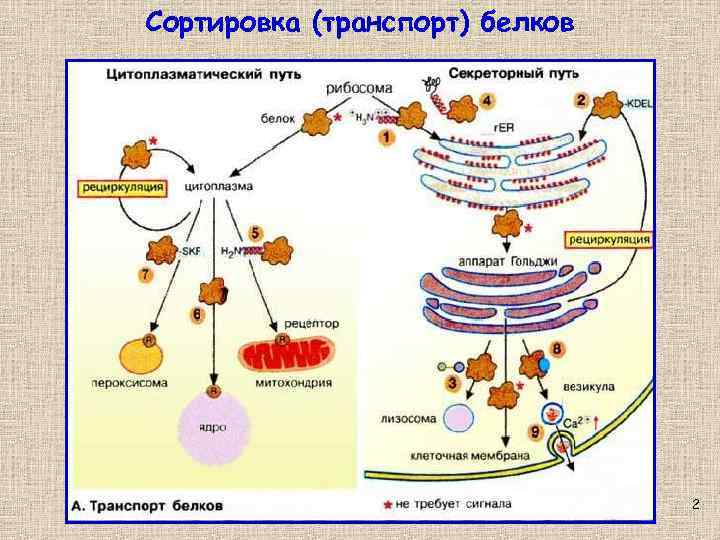
Сортировка (транспорт) белков 2

"Признаки адреса" для идентификации органеллы • В 1980 Гюнтер Блобель сформулировал основные принципы индентификации и нацеливания белков на специфические отделы клетки. Каждый белок несет в своей структуре информацию, необходимую, чтобы определить его местоположение в структуре клетки. • Уникальные аминокислотные последовательности (топогенные коды) определяют, пройдет ли белок через мембрану к специфической органелле, будет ли встроен в мембрану, или будет экспортирован из клетки. 1999 • Эти последовательности, фактически, образуют цепь различных аминокислот, представляющих либо короткий "хвост" на одном из концов белка, либо фрагмент, расположенный внутри цепи молекулы белка. 3
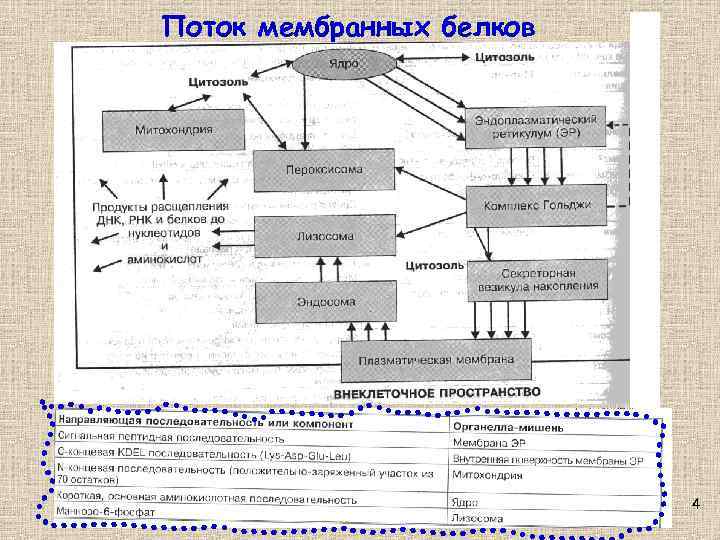
Поток мембранных белков 4
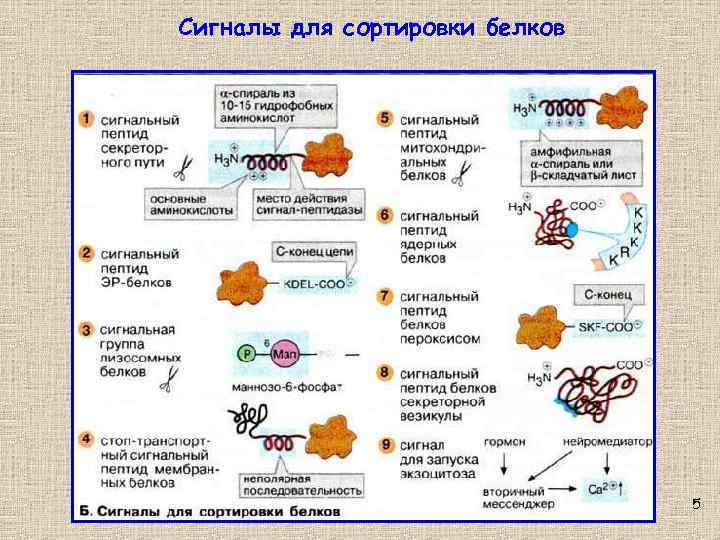
Сигналы для сортировки белков 5
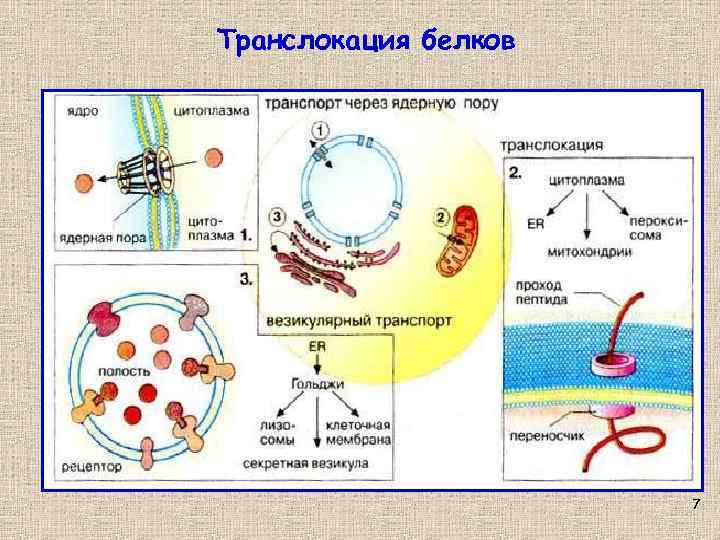
Транслокация белков 7
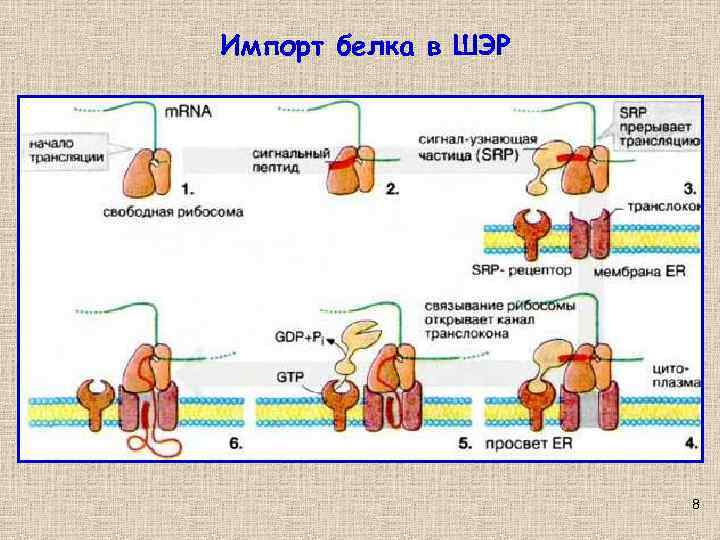
Импорт белка в ШЭР 8
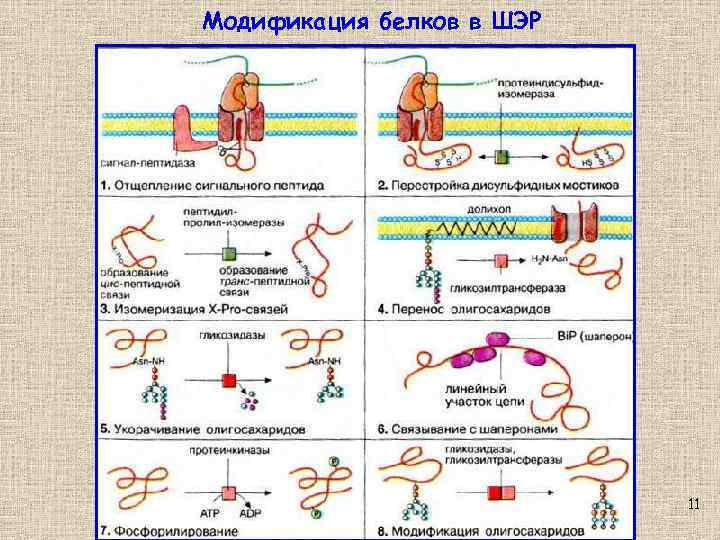
Модификация белков в ШЭР 11
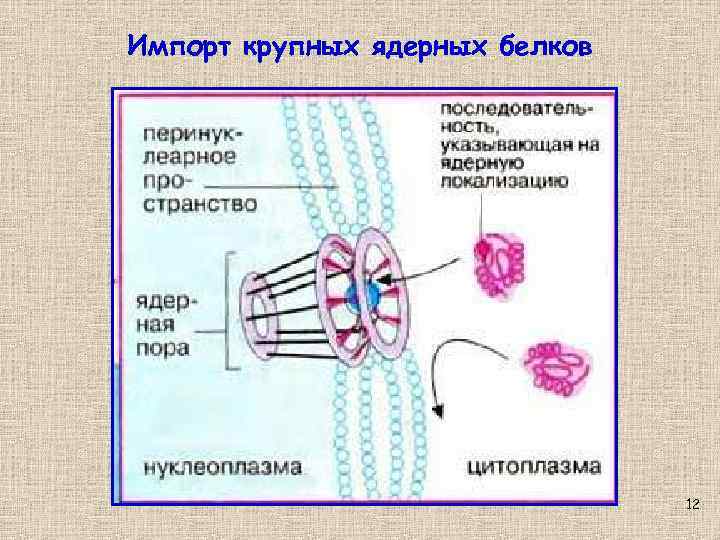
Импорт крупных ядерных белков 12
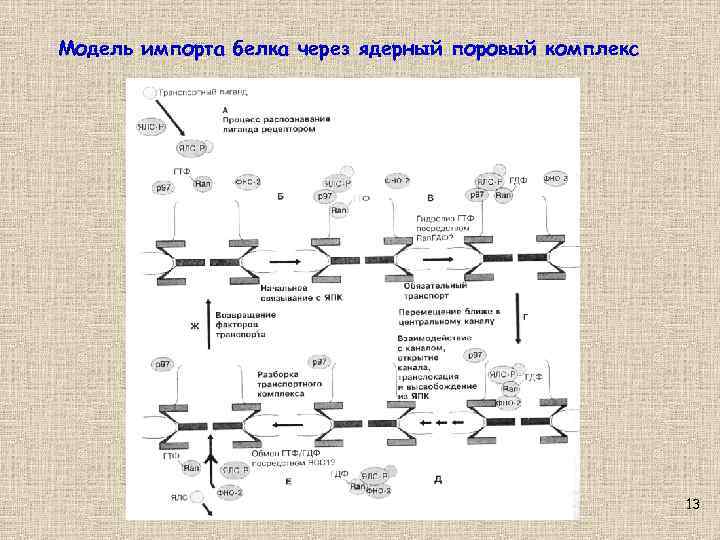
Модель импорта белка через ядерный поровый комплекс 13
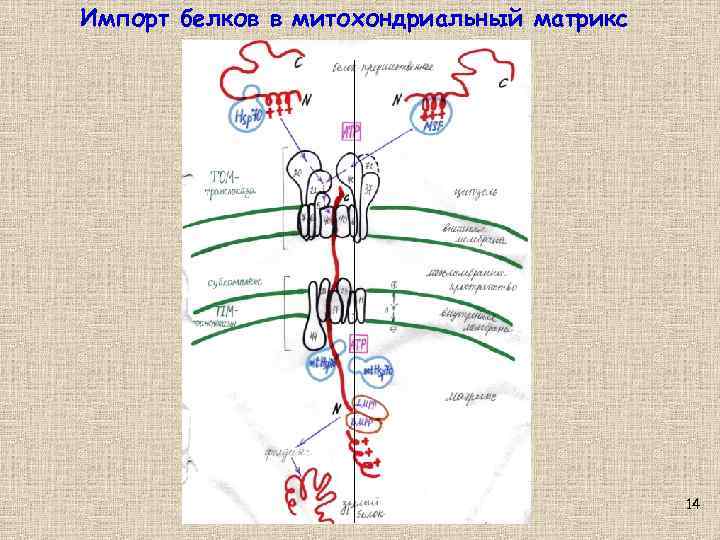
Импорт белков в митохондриальный матрикс 14
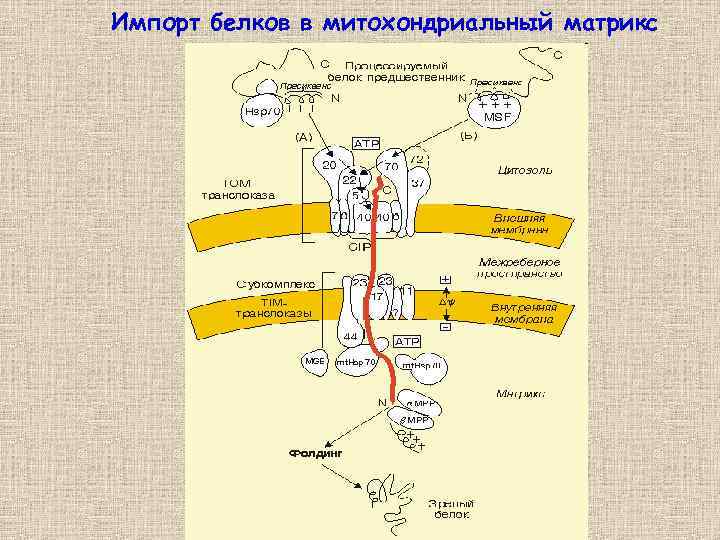
Импорт белков в митохондриальный матрикс
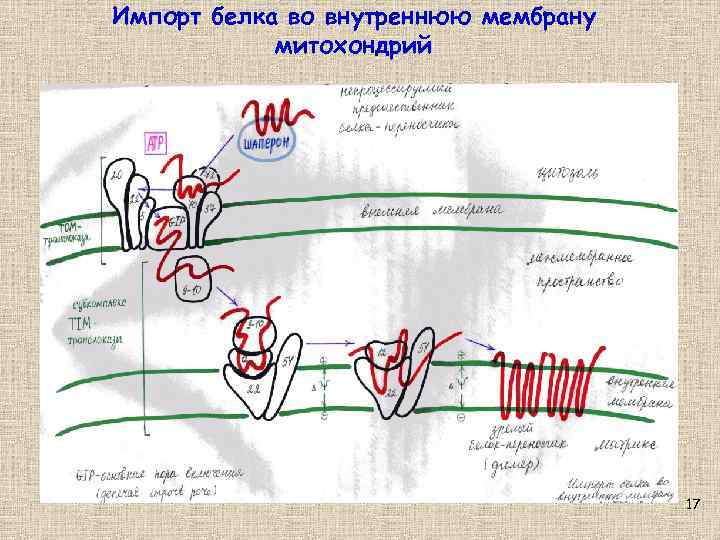
Импорт белка во внутреннюю мембрану митохондрий 17
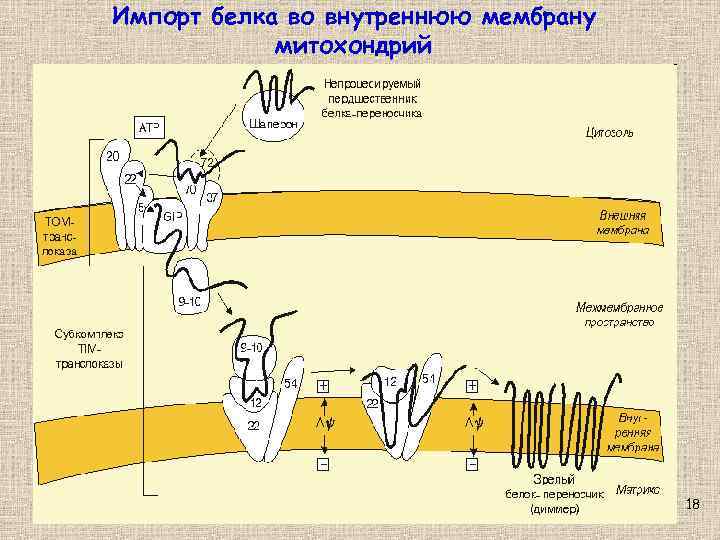
Импорт белка во внутреннюю мембрану митохондрий 18

Встраивание белков в мембрану Белок, имеющий один трансмембранный участок. Имеется один старт-пептид и один стоп-пептид, перенос белка прекращается, когда стоп-пептид достигнет вертикального участка петли. Синтез белка с цитозольной стороны продолжается. Старт-сигнал отрезается. Зрелый белок остается в мембране и пронизывает липидный бислой один раз. 19

Сигнальная гипотеза • • • Конкретные белки, ответственные за транслокацию, разные для разных органелл, но принцип один тот же: распознавание сигнального пептида, связывание с мембраной органеллы, связывание с трансмембранным каналом, проталкивание растущей пептидной цепи, отщепление сигнального пептида. 20
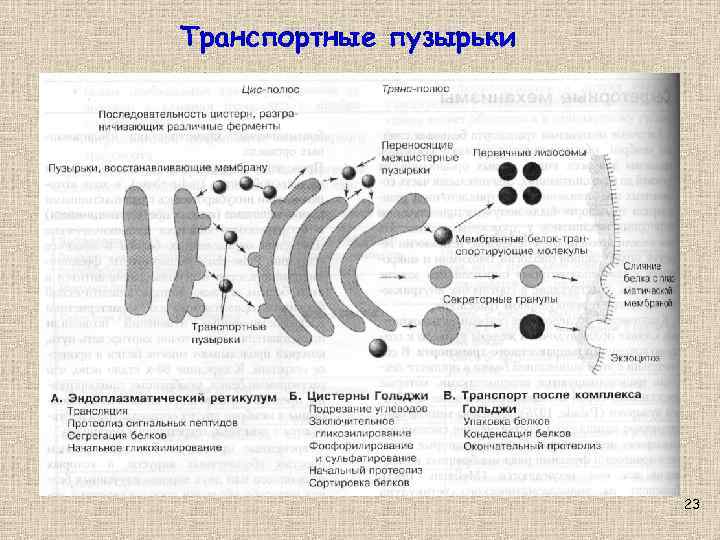
Транспортные пузырьки 23
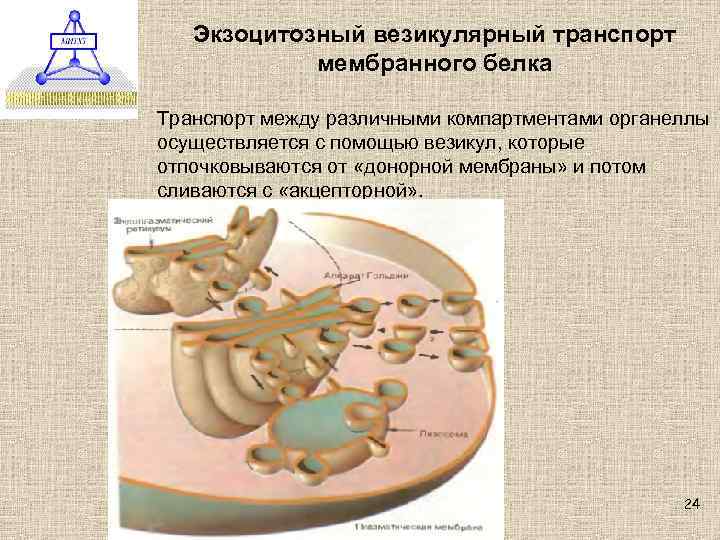
Экзоцитозный везикулярный транспорт мембранного белка Транспорт между различными компартментами органеллы осуществляется с помощью везикул, которые отпочковываются от «донорной мембраны» и потом сливаются с «акцепторной» . 24
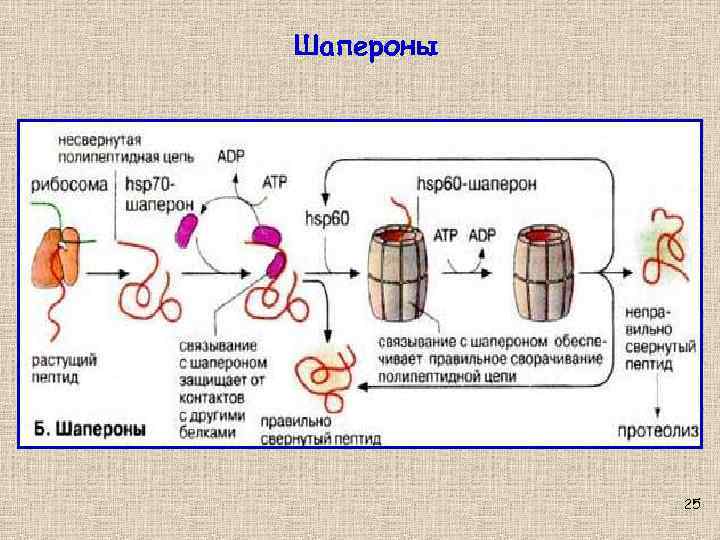
Шапероны 25

"В последние десятилетия биохимия прошла длинный путь в деле объяснения процессов образования различных белков в клетке. Но не так много ученых интересовались распадом белков. . . Лауреаты пошли наперекор этой тенденции и в начале 1980 -х открыли один из самых важных циклических клеточных процессов - регулируемый распад белков". Нобелевская премия по химии за 2004 год «за открытие убиквитин-опосредованного разложения белка» Аарон Цихановер, Аврам Гершко, Ирвин Роуз 26
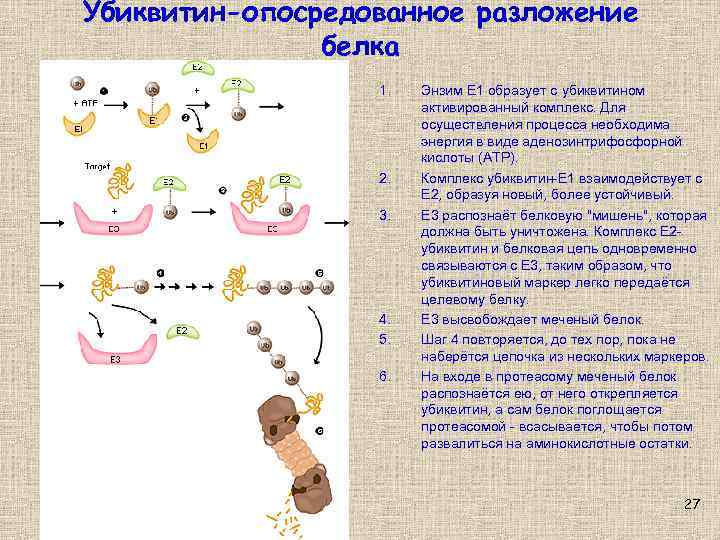
Убиквитин-опосредованное разложение белка 1. 2. 3. 4. 5. 6. Энзим E 1 образует с убиквитином активированный комплекс. Для осуществления процесса необходима энергия в виде аденозинтрифосфорной кислоты (ATP). Комплекс убиквитин-Е 1 взаимодействует с E 2, образуя новый, более устойчивый. E 3 распознаёт белковую "мишень", которая должна быть уничтожена. Комплекс E 2 убиквитин и белковая цепь одновременно связываются с Е 3, таким образом, что убиквитиновый маркер легко передаётся целевому белку. E 3 высвобождает меченый белок. Шаг 4 повторяется, до тех пор, пока не наберётся цепочка из нескольких маркеров. На входе в протеасому меченый белок распознаётся ею, от него открепляется убиквитин, а сам белок поглощается протеасомой - всасывается, чтобы потом развалиться на аминокислотные остатки. 27
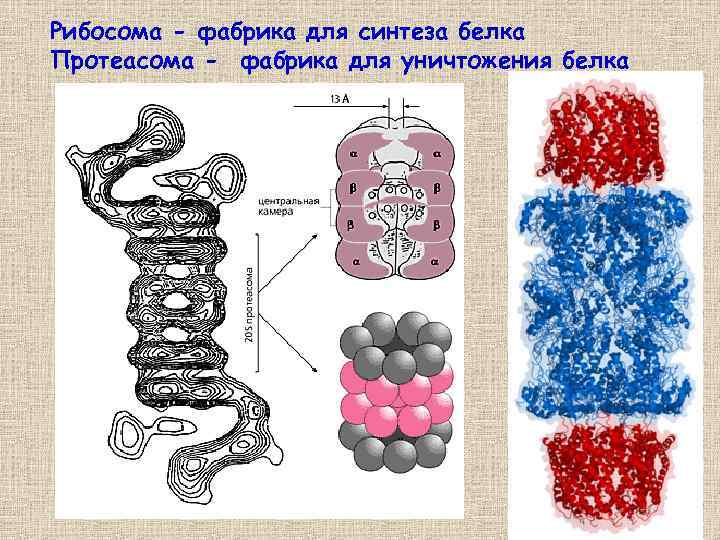
Рибосома - фабрика для синтеза белка Протеасома - фабрика для уничтожения белка 28
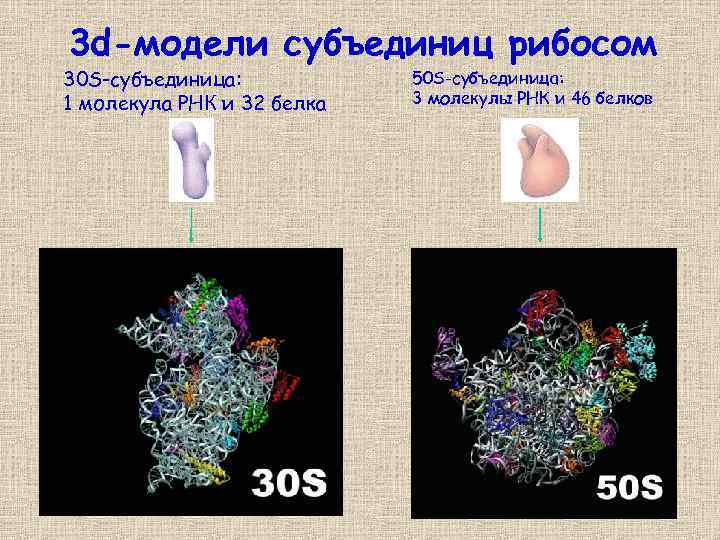
3 d-модели субъединиц рибосом 30 S-субъединица: 1 молекула РНК и 32 белка 50 S-субъединица: 3 молекулы РНК и 46 белков
08_Lecture_Proteins_Import_2010.ppt