сопряжение и ароматичность.ppt
- Количество слайдов: 27
 Сопряжение и ароматич ность. Взаимное влияние атомов в молекулах органических соединений и способы его передачи
Сопряжение и ароматич ность. Взаимное влияние атомов в молекулах органических соединений и способы его передачи
 План 1. Введение 2. Классификация органических соединений 3. Взаимное влияние атомов, индуктивный эффект 4. Сопряженные системы, сопряжение, ароматичность 5. Мезомерный эффект
План 1. Введение 2. Классификация органических соединений 3. Взаимное влияние атомов, индуктивный эффект 4. Сопряженные системы, сопряжение, ароматичность 5. Мезомерный эффект
 Введение Биоорганическая химия изучает строение и реакционную способность органических соединений, участвующих в процессах жизнедеятельности. Основные объекты: Биополимеры – ВМС, составляющие структурную основу организма (липиды, белки, полисахариды, нуклеиновые кислоты). Биорегуляторы – соединения, химически регулирующие обмен веществ (гормоны, витамины, лек. вещества).
Введение Биоорганическая химия изучает строение и реакционную способность органических соединений, участвующих в процессах жизнедеятельности. Основные объекты: Биополимеры – ВМС, составляющие структурную основу организма (липиды, белки, полисахариды, нуклеиновые кислоты). Биорегуляторы – соединения, химически регулирующие обмен веществ (гормоны, витамины, лек. вещества).
 Классификация органических соединений с. 17, 19.
Классификация органических соединений с. 17, 19.
 Взаимное влияние атомов, индуктивный эффект Реакционная способность соединений зависит от: - природы связываемых атомов - типа химической связи атомов - взаимного влияния атомов Свойства ковалентной связи: энергия, длина, насыщаемость, направленность, поляризуемость, направленность.
Взаимное влияние атомов, индуктивный эффект Реакционная способность соединений зависит от: - природы связываемых атомов - типа химической связи атомов - взаимного влияния атомов Свойства ковалентной связи: энергия, длина, насыщаемость, направленность, поляризуемость, направленность.
 Поляризуемость – способность электронов связи смещаться под действием внешнего электрического поля или другой реагирующей частицы. Полярность связи обусловлена неравномерным распределением электронной плотности вследствие разных значений электроотрицательностей (Э. О. ) связываемых атомов. Э. О. – способность атома в молекуле удерживать валентные электроны
Поляризуемость – способность электронов связи смещаться под действием внешнего электрического поля или другой реагирующей частицы. Полярность связи обусловлена неравномерным распределением электронной плотности вследствие разных значений электроотрицательностей (Э. О. ) связываемых атомов. Э. О. – способность атома в молекуле удерживать валентные электроны
 Шкала Полинга Э. О. зависит от: - заряда ядра - вида гибридизации атомных орбиталей - влияния заместителей
Шкала Полинга Э. О. зависит от: - заряда ядра - вида гибридизации атомных орбиталей - влияния заместителей
 Индуктивный эффект – передача электронного влияния заместителей по цепи σ-связей (Смещение электронной плотности по цепи σ-связей под влиянием заместителей) Обозначение : I (+I, ‑I )
Индуктивный эффект – передача электронного влияния заместителей по цепи σ-связей (Смещение электронной плотности по цепи σ-связей под влиянием заместителей) Обозначение : I (+I, ‑I )
 Заместители, по сравнению с атомом Н, смещающие сильнее электронную плотность σ-связи в сторону цепи (от себя), увеличивают электронную плотность в цепи, проявляют +I, электронодонорные свойства (Э. Д. ): радикалы, анионы, металлы.
Заместители, по сравнению с атомом Н, смещающие сильнее электронную плотность σ-связи в сторону цепи (от себя), увеличивают электронную плотность в цепи, проявляют +I, электронодонорные свойства (Э. Д. ): радикалы, анионы, металлы.
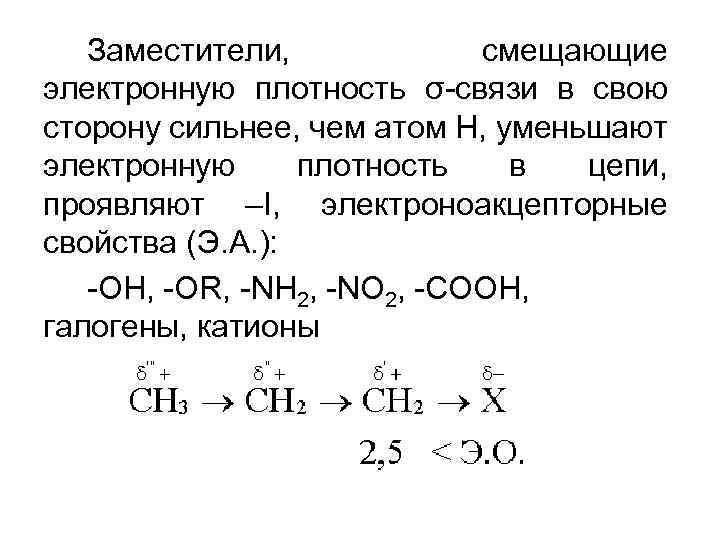 Заместители, смещающие электронную плотность σ-связи в свою сторону сильнее, чем атом Н, уменьшают электронную плотность в цепи, проявляют –I, электроноакцепторные свойства (Э. А. ): -ОН, -ОR, -NН 2, -NО 2, -СООН, галогены, катионы
Заместители, смещающие электронную плотность σ-связи в свою сторону сильнее, чем атом Н, уменьшают электронную плотность в цепи, проявляют –I, электроноакцепторные свойства (Э. А. ): -ОН, -ОR, -NН 2, -NО 2, -СООН, галогены, катионы

 Свойство индуктивного эффекта Эффект быстро затухает через 3 -4 связи из-за малой подвижности электронов σ-связи
Свойство индуктивного эффекта Эффект быстро затухает через 3 -4 связи из-за малой подвижности электронов σ-связи
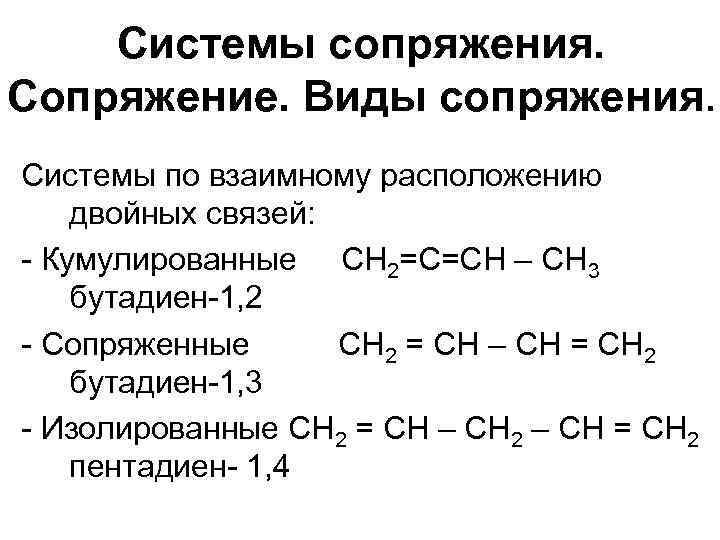 Системы сопряжения. Сопряжение. Виды сопряжения. Системы по взаимному расположению двойных связей: - Кумулированные СН 2=С=СН – СН 3 бутадиен-1, 2 - Сопряженные СН 2 = СН – СН = СН 2 бутадиен-1, 3 - Изолированные СН 2 = СН – СН 2 – СН = СН 2 пентадиен- 1, 4
Системы сопряжения. Сопряжение. Виды сопряжения. Системы по взаимному расположению двойных связей: - Кумулированные СН 2=С=СН – СН 3 бутадиен-1, 2 - Сопряженные СН 2 = СН – СН = СН 2 бутадиен-1, 3 - Изолированные СН 2 = СН – СН 2 – СН = СН 2 пентадиен- 1, 4
 Сопряженные системы с открытой цепью сопряжения
Сопряженные системы с открытой цепью сопряжения
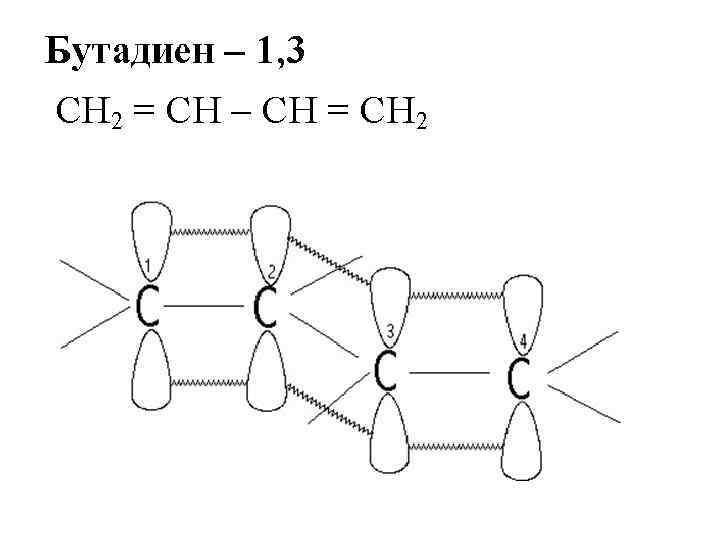
 Сопряжение – перераспределение, выравнивание электронной плотности в сопряженных системах, приводящее к образованию единого π -электронного облака, частичному выравниванию длин связей, выделению энергии (Е сопряжения). Чем ↑ длина цепи, тем ↑ Е сопряжения, тем ↑ устойчивость соединения. Е сопряжения бутадиена -1, 3 равна 15 кдж/моль.
Сопряжение – перераспределение, выравнивание электронной плотности в сопряженных системах, приводящее к образованию единого π -электронного облака, частичному выравниванию длин связей, выделению энергии (Е сопряжения). Чем ↑ длина цепи, тем ↑ Е сопряжения, тем ↑ устойчивость соединения. Е сопряжения бутадиена -1, 3 равна 15 кдж/моль.
 Виды сопряжения
Виды сопряжения
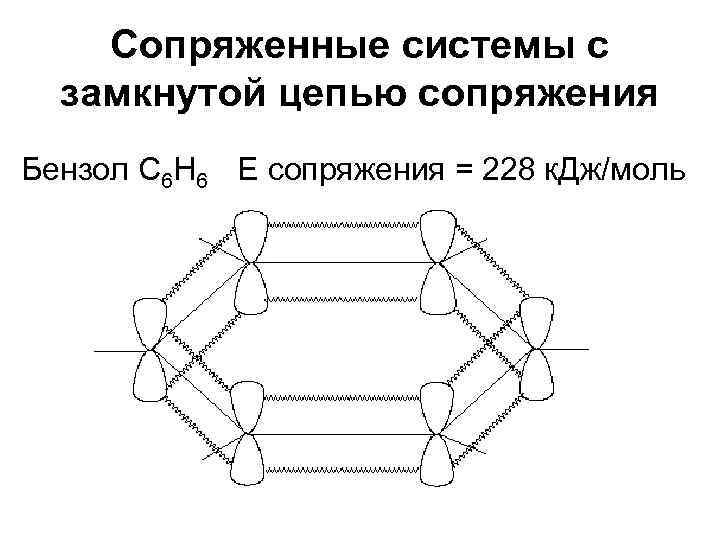 Сопряженные системы с замкнутой цепью сопряжения Бензол С 6 Н 6 E сопряжения = 228 к. Дж/моль
Сопряженные системы с замкнутой цепью сопряжения Бензол С 6 Н 6 E сопряжения = 228 к. Дж/моль
 Ароматичность – высокая т/д устойчивость к действию t 0 и окислителей Критерии ароматичности 1 Плоский замкнутый цикл 2 Сопряженная π- электронная система, охватывающая все атомы цикла 3 Соблюдается правило Хюккеля: cистема содержит (4 n + 2) π-электронов, где n = 1, 2, 3 - натуральные числа (число циклов)
Ароматичность – высокая т/д устойчивость к действию t 0 и окислителей Критерии ароматичности 1 Плоский замкнутый цикл 2 Сопряженная π- электронная система, охватывающая все атомы цикла 3 Соблюдается правило Хюккеля: cистема содержит (4 n + 2) π-электронов, где n = 1, 2, 3 - натуральные числа (число циклов)
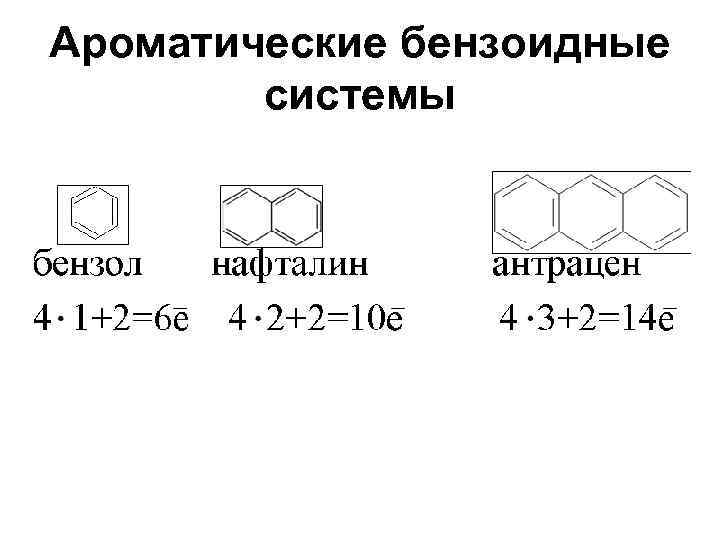 Ароматические бензоидные системы
Ароматические бензоидные системы
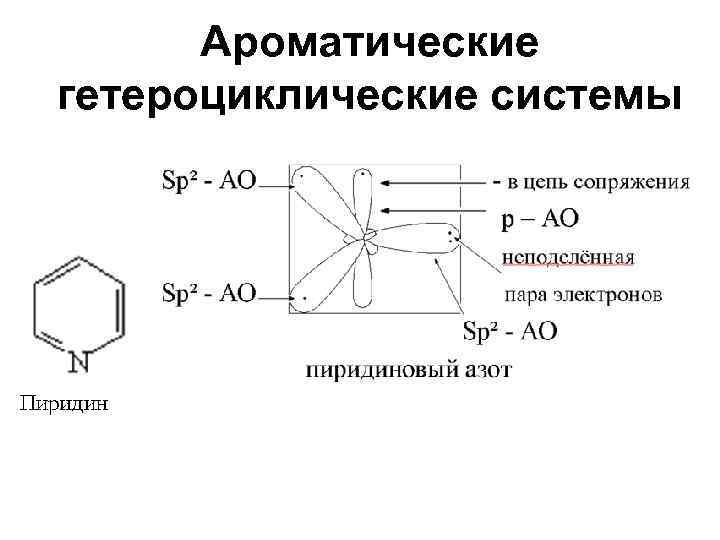 Ароматические гетероциклические системы
Ароматические гетероциклические системы
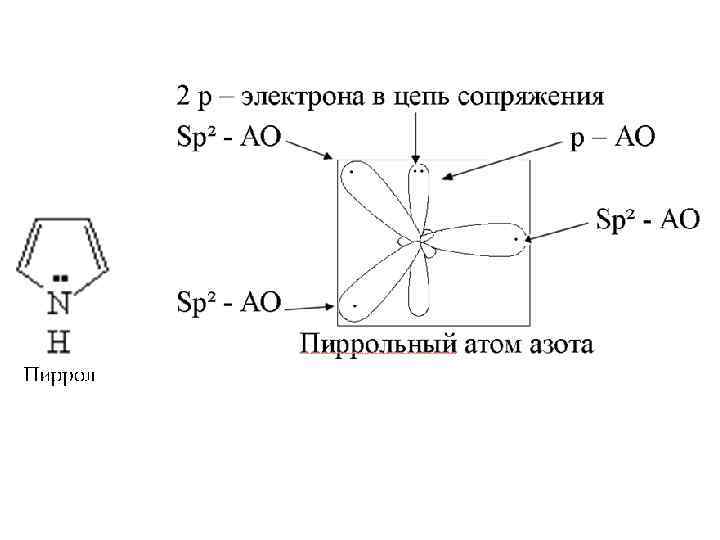
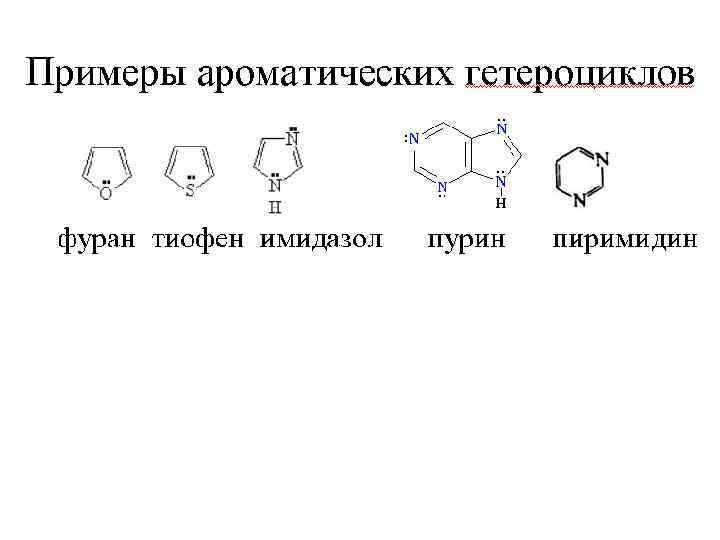
 Мезомерный эффект – передача электронного влияния заместителя по сопряженной системе (смещение электронной плотности по π-связи сопряженной системы под влиянием заместителя) Обозначение: М ( +М, –М)
Мезомерный эффект – передача электронного влияния заместителя по сопряженной системе (смещение электронной плотности по π-связи сопряженной системы под влиянием заместителя) Обозначение: М ( +М, –М)
 Заместители, смещающие электронную плотность в сторону цепи, повышают электронную плотность в системе, проявляют +М, Э. Д. свойства: - NH 2, -ОН, -ОR, - Сl
Заместители, смещающие электронную плотность в сторону цепи, повышают электронную плотность в системе, проявляют +М, Э. Д. свойства: - NH 2, -ОН, -ОR, - Сl
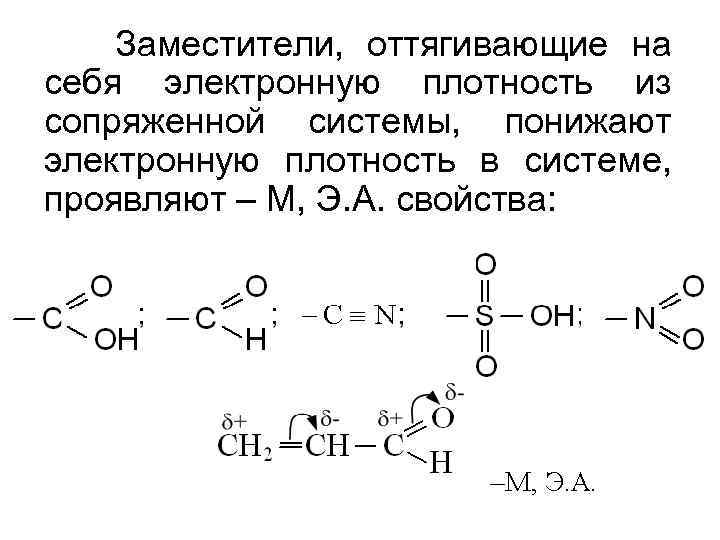 Заместители, оттягивающие на себя электронную плотность из сопряженной системы, понижают электронную плотность в системе, проявляют – М, Э. А. свойства:
Заместители, оттягивающие на себя электронную плотность из сопряженной системы, понижают электронную плотность в системе, проявляют – М, Э. А. свойства:
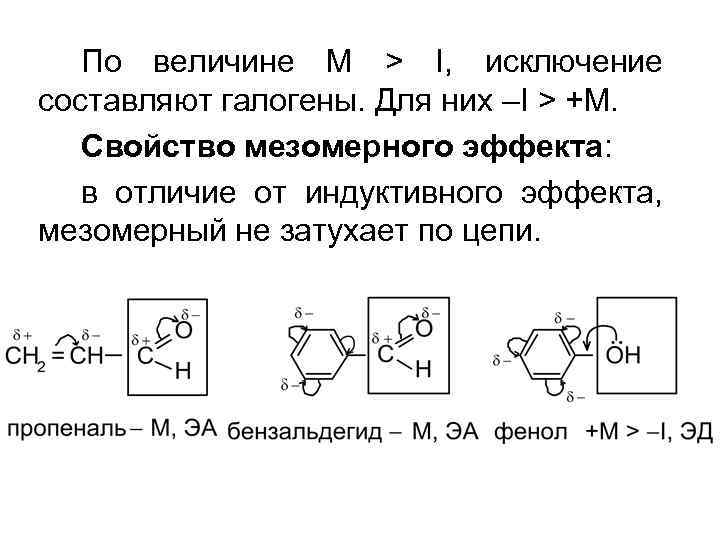 По величине M > I, исключение составляют галогены. Для них –I > +M. Свойство мезомерного эффекта: в отличие от индуктивного эффекта, мезомерный не затухает по цепи.
По величине M > I, исключение составляют галогены. Для них –I > +M. Свойство мезомерного эффекта: в отличие от индуктивного эффекта, мезомерный не затухает по цепи.


